浙江省苍南县勤奋高级中学2014-2015学年高二下学期期末考试化学试题
2014-2015学年第一学期高一期末化学试题(附答案)

高一化学试题可能用到的相对原子质量:H:1 N:14O:16S:32 Cl:35.5 Cu:64Ba:137第Ⅰ卷(选择题)一.选择题(每小题只有一个选项符合题意。
)1. 空气是人类生存所必需的重要资源。
为改善空气质量而启动的“蓝天工程”得到了全民的支持。
下列措施中,不利于“蓝天工程”建设的是A. 推广使用燃煤脱硫技术,防治SO2污染B. 实施绿化工程,防治扬尘污染C. 研制开发燃料电池汽车,消除机动车尾气污染D. 加大石油、煤炭的开采速度,增加化石燃料的使用量2. 银耳本身为淡黄色,某地生产的一种“雪耳”,颜色洁白如雪。
制作如下:将银耳堆放在密闭状态良好的塑料棚内,棚的一端支口小锅,锅内放有硫磺,加热使硫磺熔化并燃烧,两天左右,“雪耳”就制成了。
“雪耳”炖而不烂,对人体有害。
制作“雪耳”利用的是A. 硫的还原性B. 硫的漂白性C. 二氧化硫的还原性D. 二氧化硫的漂白性3. 在水泥、冶金工厂常用高压电对气溶胶作用,除去大量粉尘,以减少其对空气的污染,这种做法运用的原理是A. 丁达尔效应B. 电泳C. 渗析D. 聚沉4. 下列物质属于纯净物的是A. 盐酸B. 液氯C. 碘酒D. 漂白粉5. 下列变化需加氧化剂才能实现的是A. NH3NH4+B. N2NH3C. NH3NOD. Cl2Cl-6. 下列变化不属于氮的固定的是A. 根瘤菌把氮气转化为氨B. 氮气和氢气在适宜条件下合成氨C. 氮气和氧气在放电条件下合成NOD. 工业上用氨和二氧化碳合成尿素7. 下列物质均有漂白作用,其漂白原理相同的是①过氧化钠②次氯酸③双氧水④活性炭⑤臭氧A. ①②③⑤B.只有①③⑤C. ②③④D. 只有①②⑤8. 实验室不需用棕色试剂瓶保存的试剂是A. 浓硝酸B. 硝酸银C. 氯水D. 浓硫酸9. 自来水常用Cl2消毒,某学生用这种自来水去配制下列物质的溶液,不会产生明显的药品变质问题的是A. AgNO3B. Ca(OH)2C. Na2SO3D.AlCl310. 下列有关反应的离子方程式错误的是A. KOH 溶液与过量的SO 2反应: OH -+SO 2=HSO 3-B. Na 2SO 3溶液与稀硫酸反应: SO 32- +2H +=SO 2↑+H 2OC. NaBr 溶液中通入氯气: 2Br -+Cl 2=Br 2+2Cl -D. 石灰石与盐酸反应: CO 32-+2H +=H 2O+CO 2↑11. 下列叙述正确的为A. 石墨转化为金刚石属于化学变化B. 金刚石和石墨具有相似的物理性质C. C 60是碳元素的一种单质,其摩尔质量为720D. 由碳元素单质组成的物质一定是纯净物12. 下列化合物中不能由单质直接化合而制成的是A.FeSB.Cu 2SC.SO 3D.FeCl 313. 下列离子在溶液中可大量共存的一组是A. K +、Na +、OH -、SO 42- B. Ba 2+、Fe 2+、NO 3-、H + C. H +、Na +、CO 32-、SO 42- D. Fe 3+、Ba 2+、NO 3-、OH -14. 下列叙述正确的是A. 将钠放入硫酸铜溶液中可置换出铜B. 铜丝在氯气中燃烧,产生蓝色的烟C. 向氯化铁溶液中滴入KOH 溶液,可产生红褐色胶体D. 氢气在氯气中燃烧,火焰呈苍白色15. 甲、乙、丙三种溶液各含有一种X -(X -为Cl -、Br -、I -)离子。
2014-2015学年上杭一中高二期末考成绩
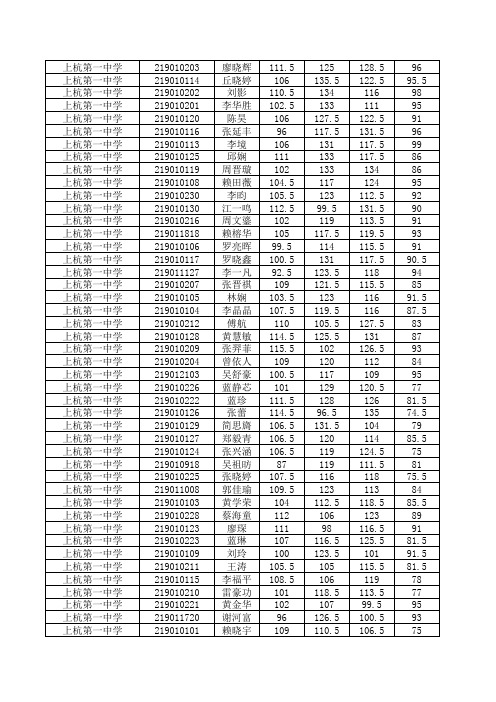
128.5 122.5 116 111 122.5 131.5 117.5 117.5 134 124 112.5 131.5 113.5 119.5 115.5 117.5 118 115.5 116 116 127.5 131 126.5 112 109 120.5 126 135 104 114 124.5 111.5 118 113 118.5 123 116.5 125.5 101 115.5 119 113.5 99.5 100.5 106.5
Hale Waihona Puke 刘珍华 张丽萍 林远冰 王玉峰 林琳 周昌海 游新硕 邱国良 陈芳 蓝晓燕 李舜华 丘凤珍 黄苏晴 蓝诗淇 谢贤旺 黄新英 刘丽珍 周煜华 廖逸飞 刘伏龙 蔡晨 许园丰 郑国庆 邓文军 钟友辉 邱红 黄秀芳 陈剑锋 温舒尚 周健豪 陈晓富 李淑婷 张晓璐 林智楠 李毓敏 雷贵龙 孔令相 赖晋 张轲容 刘林英 郭晟葳 丁湲珺 黄欣晨 林永源 陈欣
上杭第一中学 上杭第一中学 上杭第一中学 上杭第一中学 上杭第一中学 上杭第一中学 上杭第一中学 上杭第一中学 上杭第一中学 上杭第一中学 上杭第一中学 上杭第一中学 上杭第一中学 上杭第一中学 上杭第一中学 上杭第一中学 上杭第一中学 上杭第一中学 上杭第一中学 上杭第一中学 上杭第一中学 上杭第一中学 上杭第一中学 上杭第一中学 上杭第一中学 上杭第一中学 上杭第一中学 上杭第一中学 上杭第一中学 上杭第一中学 上杭第一中学 上杭第一中学 上杭第一中学 上杭第一中学 上杭第一中学 上杭第一中学 上杭第一中学 上杭第一中学 上杭第一中学 上杭第一中学 上杭第一中学 上杭第一中学 上杭第一中学 上杭第一中学 上杭第一中学
129.5 119.5 114 117.5 100.5 98.5 107.5 117.5 113.5 111 101 115.5 105.5 114.5 113.5 98.5 112.5 110.5 121.5 115.5 105.5 105.5 104 104 97.5 117.5 107 104 123.5 113 97 92.5 117.5 110.5 124 103.5 117.5 111 105 93 106.5 111.5 100.5 113 99.5
浙江省杭州求是高级中学2014-2015学年高二上学期期中考试化学试题

浙江省杭州求是高级中学2014-2015学年高二上学期期中考试化学试题可能使用的原子量:C:12 O:16 H:1 Cl:35.5一、选择题(本大题共30小题,每小题2分,共计60分。
在每题列出的四个选项中,只有一项是符合题目要求的)。
1、已知常温下0.01 mol/L CH3COOH溶液中c(H+)=4.32×10-4 mol/L,则该CH3COOH溶液中水的离子积常数为A、<1×10-14B、>1×10-14C、=1×10-14D、无法确定2、下列说法中正确的是A、需要加热才能发生的反应一定是吸热反应B、反应物能量大于生成物能量的是放热反应C、反应物能量大于生成物能量的是吸热反应D、化学反应中也存在着反应物能量与生成物能量相等的反应情况3、某pH=1的ZnCl2和HCl的混合溶液中含有FeCl3杂质,通过水解除去杂质,需将溶液调至pH=4,在调节溶液pH时,应选用的试剂是A、NaOHB、ZnOC、Na2CO3D、Fe2O34、沼气是一种能,它的主要成分是CH4。
0.5 mol CH4完全燃烧生成CO2和液态水时放出445KJ的热量,则下列热化学方程式中正确的是A、2CH4(g)+4O2(g)==2CO2(g)+4H2O(1);△H=+890kJ/molB、CH4(g)+2O2(g)==CO2(g)+2 H2O(l);△H=+890kJ/molC、CH4(g)+2O2(g)==CO2(g)+2H2O(1);△H=—890kJ/molD、1/2 CH4(g)+2O2(g)== 1/2CO2(g)+H2O(1);△H=—890kJ/mol5、已知在298K时下述反应的有关数据:C(s)+1/2 O2(g)=CO(g) △H1 = -110.5 kJ·mol-1C(s)+O2(g)=CO2(g) △H2= -393.5 kJ·mol-1则C(s)+CO2(g)=2CO(g) 的△H为A、+ 283.5 kJ· mol-1B、-504 kJ· mol-1C、-172.5 kJ· mol-1D、+ 172.5 kJ· mol-16、下列固体物质溶于水,再将其溶液加热、蒸发结晶、再灼烧,能得到化学组成与原固体物质相同的是①胆矾②氯化铝③硫酸铝④Na2CO3⑤NaHCO3⑥高锰酸钾A、③④B、①③④C、①②③④⑤D、全部7、200C时,测得反应物A的反应速率为0.1 mol/(L·s),已知温度每升高100C,化学反应速率增大到原的2倍,那么当现在改变温度后反应速率变成了1.6 mol/(L·s)时,求改温度变成了多少0CA、600CB、500CC、700CD、400C8、在水溶液中,因为发生水解反应而不能大量共存的一组微粒是A、CO2-3、OH-、Na+、H+B、Al3+、Na+、Cl-、AlO-2C、Ba2+、HCO-3、K+、SO2-4D、S2-、H+、SO2-4、Cu2+9、在2A + B = 3C + 4D的反应中,下列表示该反应速率最大的是A、V A =0.5mol / (L.min)B、V B =0.3mol / (L.min)C、V C =0.9mol / (L.min)D、V D = 0.08mol / (L.S)10、对于一个非可逆反应一定都能使反应速率加快的方法是。
2014-2015学年七年级下学期期末数学试题及答案

2014——2015学年第二学期期末考试参考答案七年级数学一、(每小题3分,共24分)1-----5 DABDD 6-----8 DBA二、(每小题3分,共21分)9.、2、3 12. 113. 89° 14. -5,-5 15. 26三、(本大题共8个小题,满分75分)16.(8分)(1)-122(2)-6-17.(7分) a=-3, b=-218. (8分) -1<x ≤314,画图略. 19. (10分)(1)S △ABC =12×≈6-1.5×1.414≈3.9(2)画图略.A’ (-5,2)、B’(2)、C’(0,5).20. (10分)解:设甲每天完成的零件数为x 个,乙每天完成的零件数为y 个,列方程组为:⎩⎨⎧=++-=++43032362430222y y x y x x 解得:⎩⎨⎧==4470y x 答:甲每天完成的零件数为70个,乙每天完成的零件数为44个.21. (10分)(1)∵∠1=∠4=1:2 ∠1=36° ∴∠4=72°又∵A B ∥CD ∴∠1+∠2+∠4=180°∴∠2=180°-36°-72°=72°又∵∠2+∠3=180° ∴∠3=180°-72°=108°(2) ∵AB ∥CD ∴∠ABE=∠4=72°∵∠2=72° ∴AB 平分∠EBG22. (10分)(1)500 (2)按先后顺序依次为A 80 C 160 D60 (3)4400023. (12分)(1)设购进A 型号的电脑x 台,那么购进B 型号的电脑(25-x )台,根据题意得:4000x+2500(25-x)≤80000 解得:x≤1123∵A型号的电脑购进不能低于8台,∴8≤x≤112 3∴电脑城有4种购进电脑的方案:①A型号购进8台时B型号购进17台②A型号购进9台时B型号购进16台③A型号购进10台时B型号购进15台④A型号购进11台时B型号购进14台.(2)∵A型号电脑的利润低,∴A型号电脑进的越少,B型号电脑进的越多时利润就越大,∴按方案①进货利润最大.最大利润为:8×800+17×1000=23400(元)。
浙江省桐乡市高级中学2014-2015学年高一上学期期中考试化学试题

浙江省桐乡市高级中学2014-2015学年高一上学期期中考试化学试题可能用到的原子量:H 1 He 4 C 12 N 14 O 16 Na 23 S 32一、选择题(1-10题每题2分,11-20题每题3分,共50分)1.化学知识广泛应用于生产生活中,下列叙述正确的是()A.空气中的臭氧对人体健康有益无害B.液氯罐泄漏时,可将其移入水塘中并加入生石灰C.工业用食盐水制取氯气过程中,不涉及氧化还原反应D.日常生活中物体能够热胀冷缩是因为构成物质的微粒能够热胀冷缩2.下列有关说法正确的是()A.道尔顿提出了原子学说 B.波尔提出了“葡萄干面包式”的原子结构模型C.卢瑟福提出核外电子在一系列稳定的轨道上运动时,既不放出能量,也不吸收能量D.汤姆生提出了带核的原子结构模型3.据最新科技报告,科学家发现了新的氢微粒,它由3个氢原子核(质子)和2个电子构成,关于这种微粒的下列说法中正确的是()A.一个该微粒含3个中子 B.它是氢的一种新的同位素C.其组成可用H3+表示D.它比一个普通氢分子多一个氢原子4. 下列四幅图中,小白球代表的是氢原子,大灰球代表的是氦原子。
最适合...表示同温同压下,等质量的氢气与氦气的混合气体的图示是()5.关于胶体的下列说法中错误的是()A.胶体中分散质的颗粒大小在10—9~ 10—7m之间B.胶体的外观是不均匀的C.将一束激光照射到胶体中会发现一条光亮的通路D.胶体可能有不同的颜色6.下列物质属于纯净物的是()A.漂白粉B.盐酸C.氯水D.液氯7.下列说法中正确的是()O所含的分子数和原子数都相等A.在任何状况下,1 mol CO2和1 mol H2B.只有在标准状况下,1 mol气体所占的体积才是22.4 LC.某物质含有阿伏加德罗常数个微粒,该物质在标准状况下体积为22.4 LD. 22.4 L CO所含的分子数为6.02×1023个8.标准状况下,有①6.72L甲烷,②3.01×1023个HCl分子,③34 gH2S气,④0.2 mol氨气,则下列四种气体关系表示正确的是()A.体积④<①<②<③B.密度①<③<④<②C.质量④<①<③<②D.氢原子数②<④<③<①9. 下列说法正确的是()A.固体溶解后,将溶液转移到容量瓶中,然后向容量瓶中直接加水稀释到刻度线B.分液操作时,分液漏斗中下层液体从下口放出,上层液体也从下口放出C.蒸馏时,温度计水银球靠近蒸馏烧瓶的支管口处, 且冷却水从冷凝管的下口通入上口流出D.将5.85gNaCl固体溶于1 L水中可配成0.1 mol·L-1的NaCl溶液10. 决定气体体积的因素是()①气体分子的直径②气体的物质的量多少③气体分子间的平均距离④气体分子的相对分子质量A.①② B.①③ C.②③ D.②④11.下列变化必须加入氧化剂才能完成的是()A.MnO4-→MnO2B. Cl2 →HClOC. Fe2+→Fe3+D.HCO3-→CO32-12.如果你家里的食用花生油不小心混入了大量的水,利用你所学的知识,最简便的分离方法是()13.对于某些离子的检验及结论正确的是()A.加入盐酸,产生能使澄清石灰水变浑浊的无色气体,则原溶液中一定有CO32ˉB.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,则一定有SO42ˉC.加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,则一定有NH4+D.某物质灼烧时,焰色反应呈黄色,则该物质中一定有Na+14.N A为阿伏伽德罗常数的值,下列叙述正确的是()A.常温常压下,2g 氢气所含原子数目为2N A B.36g H2O中含有的质子数为10N AC.标准状况下,11.2L水中含有的分子数是0.5N AD.1mol 氯气与足量水反应,转移的电子数是2N A15. 氧化还原反应中水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既非氧化剂又非还原剂等。
2014-2015学年度上学期期末考试高一化学试卷(含答案)

2014-2015学年度上学期期末考试高一化学试卷(含答案)可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 Al 27 S 32 Cl 35.5K 39 Ca 40 Zn 65 Fe 56 Cu 64注意事项:1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。
满分100分。
考试时间100分钟;2.第Ⅰ卷第Ⅱ卷答案用钢笔或签字笔写在答卷正确位置上;第I卷选择题一、选择题(本题包括20小题,每小题2分,共40分。
每小题只有一个选项符合题意。
)1.“化学,让生活更美好”,下列叙述不能直接体现这一主旨的是:A.风力发电,让能源更清洁B.合成光纤,让通讯更快捷C.合成药物,让人类更健康D.环保涂料,让环境更宜居2.下列化学用语正确的是:A.Cl-的结构示意图:B.光导纤维主要成分的化学式:SiIC.质子数为53,中子数为78的碘原子:13153D.H216O、D216O、H218O、D218O互为同位素34.下列操作中,不会发生明显颜色变化的是A.FeSO4溶液中滴入NaOH溶液B.硫酸铁溶液中滴加硫氰化钾溶液C.碳酸氢钠溶液中滴加稀盐酸D.氯化铁溶液中加入还原性铁粉5. 现有三种常见治疗胃病药品的标签:①②③药品中所含的物质均能中和胃里过量的盐酸,下列关于三种药片中和胃酸的能力比较,正确的是()A.③>②>①B.①>②>③C.①=②=③D.②>③>①6.关于NaHCO3与Na2CO3说法正确的是:① NaHCO3固体可以做干粉灭火剂,金属钠起火可以用它来灭火② NaHCO 3粉末中混有Na 2CO 3,可配置成溶液通入过量的CO 2,再低温结晶得到提纯 ③ Ca(HCO 3)2溶解度都比其正盐的溶解度大,因此NaHCO 3的溶解度也比Na 2CO 3大 ④Na 2CO 3固体中混有NaHCO 3,高温灼烧即可⑤区别NaHCO 3与Na 2CO 3溶液,Ca(OH)2溶液和CaCl 2溶液均可用 A .①③ B . ③⑤ C .②④ D . ②⑤ 7.下列关于Na 及其化合物的叙述正确的是:A .将钠投入FeSO 4溶液中,可以得到单质铁B .足量Cl 2、S 分别和二份等质量的Na 反应,前者得到电子多C .Na 2O 与Na 2O 2中阴阳离子的个数比均为1:2D .在2Na 2O 2+2H 2O=4NaOH+O 2反应中,每生成1molO 2,消耗2mol 氧化剂 8. 下列常见金属单质的工业冶炼方法正确的是:A .冶炼钠:电解氯化钠水溶液,同时得到副产品Cl 2、H 2B .冶炼镁:电解熔融MgCl 2.6H 2O ,同时得到副产品Cl 2,H 2OC .冶炼铝:电解熔融冰晶石(Na 3AlF 6),同时得到副产品Al 2O 3D .冶炼铁:高炉中生成CO ,CO 在高温下还原铁矿石,同时得到副产品CaSiO 3 9.设N A 代表阿伏伽德罗常数,下列说法正确的是 A .1mol MgCl 2中含有的离子数为2N AB .标准状况下,11.2L H 2O 中含有的原子数为1.5N AC .标准状况下,22.4L 氦气与22.4L 氯气所含原子数均为2N AD .常温下,2.7g 铝与足量的盐酸反应,失去的电子数为0.3 N A 10. 下列物质中,既能跟稀硫酸反应,又能跟NaOH 溶液反应的是①Al 2O 3;②Mg(OH)2;③Al(OH)3;④(NH 4)2CO 3;⑤NaHCO 3;⑥AlCl 3 A .①③⑤⑥ B .只有①③ C .只有②③ D .①③④⑤ 11.等质量的两根镁条,第一根在足量氧气中加热燃烧,第二根在足量CO 2气体中加热燃烧,则下列说法正确的是:①两根镁条失去电子一样多 ②第一镁根条失去电子多 ③第二根镁失去电子多 ④两根镁的产物质量一样大 ⑤第一根镁的产物质量大 ⑥第二根镁的产物质量大A .①④B . ①⑥C .③⑥D .②⑤12. Fe 和Fe 2O 3 、Fe 3O 4的混合物,加入200mL 5mol·L -1的盐酸,恰好完全溶解,再向其中加入KSCN 溶液,未见血红色,则所得溶液中Fe 2+的物质的量浓度为(假设反应后溶液体积仍为200mL) A 、2.5mol·L -1 B 、lmol·L -1 C 、2mol·L -1 D 、5mol·L -1 13.下列选用的相关仪器符合实验要求的是A .存放液溴B .量取9.50 mL 水C .称量8.55g 氯化钠固体D .配制240 mL0.1mol/L的NaCl溶液14.下列除去杂质(括号内的物质为杂质)的方法中错误..的是A.FeSO4 (CuSO4):加足量铁粉后,过滤B.CO (CO2):用NaOH溶液洗气后干燥C.MnO2 (KCl):加水溶解后,过滤、洗涤、烘干D.CO2 (HCl):用NaOH溶液洗气后干燥15.下列化学反应所对应的离子方程式正确的是:A.氧化铝和过量的氢氧化钠溶液反应:2OH-+Al2O3=2AlO2-+H2B.AlCl3溶液中加过量的氨水:Al3+ + 3NH3·H2O = Al(OH)3↓ + 3NH4+C.明矾溶液中加入过量的Ba(OH)2:Al3+ + SO42— + Ba2+ + 4OH—=BaSO4↓+AlO2—+H2OD.向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-16.已知KMnO4与浓HCl在常温下反应就能产生Cl2。
2014-2015学年度上学期期末考试高二化学试卷 (含答案解析)

2014-2015学年度上学期期末考试高二化学试卷(含答案解析)可能用到的相对原子质量:H:1 C:12 O:16 Na:23 Mg:24 Al:27Fe:56 Cu:64 Zn:65一、单选题(本题包括18小题,1-10每题2分,11-18每题3分,共44分。
每小题只有一...个.选项符合题意)1.关于吸热反应的说法,正确的是()A.凡需加热的反应一定是吸热反应B.只有分解反应才是吸热反应C.使用催化剂的反应是吸热反应D.酸碱中和反应的逆反应是吸热反应2.下列物质属于非电解质的是()A.NH3B.(NH4)2SO4 C.Cl2D.CH3COOH3.下列热化学方程式中△H的值能表示可燃物的燃烧热的是()A.H2(g)+Cl2(g)= 2HCl(g)△H=-184.6kJ/molB.CH4(g)+2O2(g)= CO2(g)+2H2O(g)△H=-802.3k J/molC.2H2(g)+O2(g)= 2H2O(l)△H=-571.6kJ/molD.CO(g)+1/2O2(g)= CO2(g)△H=-283kJ/mol4.下列物质中既属于芳香化合物又属于醇的是()5.下列有机物的命名正确的是()A. 3,3-二甲基丁烷B.3-甲基-2-丁烯C. 2-乙基丁烷D.CH3CH3名称为1,4-二甲苯6. 已知:①H2O(g)===H2O(l)ΔH=-Q1 kJ/mol ②C2H5OH(g)===C2H5OH(l)ΔH=-Q2 kJ/mol ③C2H5OH(g)+3O2(g)===2CO2(g)+3H2O(g)ΔH=-Q3 kJ/mol,若使23 g酒精液体完全燃烧,最后恢复到室温,则放出的热量为() (kJ)A.Q1+Q2+Q3B.0.5(Q1+Q2+Q3)C.0.5Q1-1.5Q2+0.5Q3D.1.5Q1-0.5Q2+0.5Q37. 反应4NH3(g)+5O2(g) =4NO(g)+6H2O(g) 在2 L的密闭容器中进行,1分钟后,NH3减少了0.12 mol,则平均每秒钟各物质浓度变化正确的是A、NO:0.001 mol·L-1B、H2O:0.002 mol·L-1C、NH3:0.002 mol·L-1D、O2:0.001 mol·L-18.下列实验事实不能..证明醋酸是弱酸的是()A.常温下,测得醋酸钠溶液的pH >7B.常温下,测得0.1 mol/L 醋酸溶液的pH =4C.常温下,将pH =1的醋酸溶液稀释1000倍,测得pH <4D.常温下,将物质的量相同的醋酸溶液与的氢氧化钠溶液等体积混合后恰好中和9.对于可逆反应 A(g)+B(g)C(g) (正反应为放热反应)来说,下列图象正确的是( )A BC D10.等物质的量的X(g)与Y(g)在密闭容器中进行可逆反应:X(g)+Y(g)2Z(g)+W(s),该反应的ΔH <0,下列叙述正确的是( )A .平衡常数K 值越大,X 的转化率越大B .达到平衡时,反应速率v 正(X)=2v 逆(Z)C .达到平衡后,降低温度,正向反应速率减小的倍数大于逆向反应速率减小的倍数D .达到平衡后,升高温度或增大压强都有利于该反应平衡向逆反应方向移动11.常温下,盐酸与氨水混合,所得溶液pH =7,则此溶液中( )A .c (NH 4+)<c (Cl -)B .c (NH 4+)=c (Cl -)C .c (NH 4+)>c (Cl -)D .无法确定c (NH 4+)与c (Cl -)的关系12. 水是最宝贵的资源之一,下列表述正确的是 ( )A.4 ℃时,纯水的pH =7B.温度升高,纯水中的c (H +)增大,c (OH -)减小C.水的电离程度很小,纯水中主要存在形态是水分子D.向水中加入酸或碱,都可抑制水的电离,使水的离子积减小13.在0.1mol·L -1CH 3COOH 溶液中存在如下电离平衡:CH 3COOH CH 3COO -+H +,对于该平衡,下列叙述正确的是( )A.加入水时,平衡向逆反应方向移动B.加入少量NaOH 固体,平衡向正反应方向移动C.加入少量0.1mol·L -1HCl 溶液,溶液中c(H +)减小D.加入少量CH 3COONa 固体,平衡向正反应方向移动14.一定条件下,将3molA 和1molB 两种气体混合于固定容积为2L 的密闭容器中,发生如下反应:3A(g)+B(g) xC(g)+2D(s)。
浙江省杭州市西湖高级中学2014-2015学年高二10月月考化学试题

浙江省杭州市西湖高级中学2014-2015学年高二10月月考化学试题可能用到的数据:Ag-108 Ca-40O-16 Mg-24 Al-27 S-32 Fe-56 Cu-64 Zn-65 Mn-55,Na-23 K-39一、选择题(每小题只有一个正确答案,每题2分,共48分)1.下列关于能量的变化及反应热的说法中正确的是 ( )。
A.任何化学反应都有反应热B.有些化学键断裂时吸收能量,有些化学键断裂时放出能量C.新化学键的形成不一定放出能量D.有热量变化的反应一定有化学键的断裂与形成2.已知化学反应A2(g)+B2(g)===2AB(g)的能量变化如图所示,判断下列叙述中正确的是( )。
A.每生成2分子AB吸收b kJ热量B.该反应热ΔH=+(a-b)kJ·mol-1C.该反应中反应物的总能量高于生成物的总能量D.断裂1 mol A—A和1 mol B—B键,放出a kJ能量3.向足量H2SO4溶液中加入100 mL 0.4 mol·L-1 Ba(OH)2溶液,放出的热量是5.12 kJ。
如果向足量Ba(OH)2溶液中加入100 mL 0.4 mol·L-1盐酸时,放出的热量为2.2 kJ。
则Na2SO4溶液与BaCl2溶液反应的热化学方程式为 ( )。
A.Ba2+(aq)+SO2-4(aq)===BaSO4(s) ΔH=-2.92 kJ·mol-1B.Ba2+(aq)+SO2-4(aq)===BaSO4(s) ΔH=-18 kJ·mol-1C.Ba2+ (aq)+SO2-4(aq)===BaSO4(s) ΔH=-73 kJ·mol-1D.Ba2+(aq)+SO2-4(aq)===BaSO4(s) ΔH=-0.72 kJ·mol-14.为探究NaHCO3、Na2CO3和盐酸(以下盐酸浓度均为1 mol·L-1)反应过程中的热效应,实验测得如下数据:A .Na 2CO 3溶液与盐酸的反应是吸热反应B .NaHCO 3溶液与盐酸的反应是放热反应C .20.0 ℃时,含3.2 g Na 2CO 3的饱和溶液和35 mL 盐酸混合后的温度将低于25.1 ℃D .20.0 ℃时,含2.5 g NaHCO 3的饱和溶液和35 mL 盐酸混合后的温度将低于16.2 ℃5.将TiO 2转化为TiCl 4是工业冶炼金属钛的主要反应之一。
2014~2015学年度第一学期期末考试九年级数学试卷答案
2014——2015学年度第一学期期末测试九 年 级 数 学参考答案一、选择题:本大题共10小题,每小题3分,共30分.在每小题给出的四个选项中,恰有一项是符合题目要求的,请将正确选项的代号填入题后括号内.1.D 2.B 3.C 4.A 5.B 6.C 7.D 8.A 9.B 10.C二、填空题:本大题共8小题,每小题3分,共24分.请把最后结果填在题中横线上. 11.0。
6 12.25 13.24 14.52 15.277 16.(9,0) 17.-1<x <3 18.②④三、解答题:本大题共10小题,共96分.解答时应写出文字说明、证明过程或演算步骤. 19.(本小题满分8分)每图4分解:由表可以看出,随机地摸取一个小球然后放回, 再随机地摸出一个小球,可能出现的结果有16个,它们出现的可能性相等.…………4分 (1)满足两次取的小球的标号相同的结果有4个,所以P (1)=164=41.……6分 (2)满足两次取的小球的标号的和等于4的结果有3个,所以P (2)=163.…8分21.(本小题满分9分)(1)8π (3分) (2)(3分)(3)③(3分)22.(本小题满分8分)证明:连接OC .………………………………………………1分∵OA =OC ,∴∠OAC =∠OCA .………………………2分∵CD 切⊙O 于点C ,∴OC ⊥CD .……………………3分∵AD ⊥CD ,∴∠ADC =∠OCD =90°,即∠ADC +∠OCD =180°,∴AD ∥OC ,……………………………………………5分∴∠DAC =∠OCA =∠OAC ,……………………………7分∴AC 平分∠DAB .……………………………………8分一 二1 2 3 4 1 (1,1) (2,1) (3,1) (4,1) 2 (1,2) (2,2) (3,2) (4,2) 3 (1,3) (2,3) (3,3) (4,3)4 (1,4) (2,4) (3,4) (4,4) A B C D O . (第22题图).O A B C解:设所围成圆锥的底面半径和高分别为r 和h .∵扇形半径为3㎝,圆心角为120°, ∴12032180r ππ⋅⋅=,……………………………………………………………………4分 ∴r =1,……………………………………………………………………………………6分∴h ==8分24.(本小题满分10分)解:(1)令y =0,得2230x x --=,………………………………………………………1分解得x 1=3,x 2=-1,………………………………………………………………3分 ∴抛物线与x 轴交点坐标为(3,0)和(-1,0).……………………………4分(2)令x =0,得y =-3,∴抛物线与y 轴交点坐标为(0,-3),…………………………………………5分 ∴将此抛物线向上平移3个单位后可以经过原点.……………………………7分 平移后抛物线解析式为22y x x =-.………………………………………10分25.(本小题满分9分)(1)证明:∵DE ∥BC ,EF ∥AB ,∴∠AED =∠ECF ,∠A =∠FEC ,……………2分∴△ADE ∽△EFC .………………………………………………………………4分(2)解:∵△ADE ∽△EFC , ∴AD DE EF FC=.…………………………5分 ∵AD =4,DE =5,EF =2, ∴FC =52.……………………………………6分 ∵DE ∥BC ,EF ∥AB ,∴四边形DEFB 是平行四边形,∴BF =DE =5,……8分∴BC =BF + FC =5+52=152.………………………………………………………9分26.(本小题满分10分)(1)证明:∵四边形ABCD 是正方形,∴∠A =∠B =90°,∴∠DEA +∠ADE =90°.…1分∵EF ⊥DE ,∴∠DEF =90°,∴∠DEA +∠FEB =90°,……………………………2分 ∴∠ADE =∠FEB ,……………………………………………………………………4分 ∴△ADE ∽△BEF .……………………………………………………………………5分(2)解:∵正方形的边长为4,AE =x ,∴BE =4-x .∵△ADE ∽△BEF , ∴DA AE EB BF =,……………………………………………7分 ∴44x x y =-, ∴2(4)144x x y x x -==-+,…………………………………10分解:(1)由题意得1060x y -=.…………………………………………………………3分 (2)由题意得1200040101)200)(1060()200(2++-=+-=+=x x x x x y z .6分 (3)由题意得)1060(201200040101202x x x y z w --++-=-= 10800421012++-=x x .…………………………………………9分 当每个房间的定价2102=-=a b x (元)时,w 有最大值,最大值是15210.………12分28.(本小题满分14分)解:(1)∵点A 坐标为(0,3),∴OA =3.∵矩形ABCO 面积为12,∴AB =4,……2分∴抛物线的对称轴为直线x =2.…………………………………………………4分(2)∵∠ADM =∠DOM ,∠AMD =∠DMO ,∴△ADM ∽△DOM , ∴MOMD MD AM =,∴MO AM MD ⋅=2.设MO=x ,则MA= x -3. ∴)3(4-=x x ,∴41=x ,12-=x ,∴MO=4,∴D 点坐标为(2,4).…6分 设抛物线的解析式为4)2(2+-=x a y . 将点A (0,3)代入得443+=a ,∴41-=a , ∴抛物线的解析式为4)2(412+--=x y .……………………………8分 (3)∵⊙P 在y 轴上截得线段长为2,OA =3, ∴P 点纵坐标为2或4.……9分在4)2(412+--=x y 中,令y=2或4得 4)2(4122+--=x 或4)2(4142+--=x ,………………………………11分 解得2221+=x ,2222-=x ,23=x ,∴P 点坐标为(222+,2)、(222-,2)或(2,4).………………14分。
2014—2015学年度第二学期期末考试安排

余干县海尔希望学校2014—2015学年度第二学期期末考试工作安排一、组织机构设置主考:占华平副主考:朱绍永考办:李保胜王国福刘佳莹曹笑艳卢清波熊玉荣楼层负责人:第1、2教学楼一楼:郑军福第1、2教学楼二楼:张海云第1、2教学楼三楼:张梁燕初中部:彭日彰、张元元第2教学楼后楼梯口:张森福负责人主要负责考试纪律和楼道安全。
司钟:雷春娇宿管:张森福二、考务守则1、参加监考的老师必须在第一场开考前20分钟进入自己的考场,摆好桌凳,按考号编排好学生的座位(从门口开始,“s”形编排)。
预备铃响铃之后,考办人员必须将试卷分别送到各考场监考老师手中。
2、监考老师必须在开考铃响之前将试卷分发到考生手中,当考生接过试卷后监考员须反复提醒考生按要求填写班级、姓名、考号等内容。
特别是一年级学生,应指导其填写,开考铃响前学生不准答卷。
3、各年级语文考试开始后,监考老师须提醒各考生先仔细阅读听力题目要求,2分钟后开始念听力材料(以正常朗读速度用普通话念两遍)。
每念完题后停顿3——5分钟让学生答题。
两遍念完后不可再念。
4、考试时,考生如发现试卷不够清晰,应先举手再提问,监考老师就考生提出的疑问,须面向全体学生给予答复。
5、监考老师要关心,爱护每位学生,反复叮嘱考生审清题意,认真作答,细心检查,不得要求或暗示学生提前交卷。
同时要提醒学生坐姿端正、讲究卫生。
6、为保证考试公平、公正,严禁监考老师或工作人员借故进入其他考场干预考试。
未经主考许可,任何老师或学生不得私自调换考场。
监考人员不得串场、接打电话,或聚集一起谈笑,不做与监考无关的事情,以免影响学生考试。
7、收卷时,监考老师一定要按考号顺序(小号在上,大号在下)整理好试卷,点清份数后交考办工作人员检查验收。
考办人员必须当面点清试卷确认没有遗失试卷后再进行装订,试卷不得漏装、倒装、错装。
8、各班主任和各考场监考人员必须教育好本班学生(或本考场学生)爱护考场桌椅、门窗等公共财物。
浙江省浙南名校2023-2024学年高二下学期6月期末考试化学试题含答案

2023学年第二学期浙南名校联盟期末联考高二化学学科试题(答案在最后)考生须知:1.本试题卷共8页,满分100分,考试时间90分钟。
2.答题前,在答题卷指定区域填写班级、姓名、考场号、座位号及准考证号。
3.所有答案必须写在答题卷上,写在试卷上无效。
4.考试结束后,只需上交答题卷。
5.可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Al-27 P-31 S-32 Cl-355 Ca-40 Ti-48.选择题部分一、选择题(本大题共16小题,每小题3分,共48分。
每小题列出的四个备选项中只有一个是符合题目要求的,不选、多选、错选均不得分。
)1.下列物质属于纯净物的是A.漂粉精B.聚丙烯酸钠C.明矾D.活性炭【答案】C【解析】【详解】A .漂粉精的主要成分是氯化钙和次氯酸钙是混合物,A 不符合题意;B .聚丙烯酸钠是高分子化合物,高分子化合物都是混合物,B 不符合题意;C .明矾是有固定的组成纯净物,C 符合题意;D .活性炭是混合物,不是纯净物,D 不符合题意;答案选C 。
2.高铁酸钠(24Na FeO )是一种新型绿色消毒剂,主要用于饮用水处理。
下列说法不正确的是A.高铁酸钠属于离子晶体B.可由次氯酸钠在强碱性的条件下氧化3+Fe 来制备高铁酸钠C.用高铁酸钠对饮用水处理过程中可能涉及胶体的性质D.高铁酸钠中铁元素位于元素周期表的ds 区【答案】D【解析】【详解】A .高铁酸钠是由阴阳离子构成的,属于离子晶体,A 正确;B .次氯酸钠在强碱性的条件下氧化3+Fe 来制备高铁酸钠,- 3+-2-423ClO +2Fe +10OH = 2FeO +3Cl +5H O ,B 正确;C .高铁酸钾转化为()3Fe OH 胶体,胶体表面积大,吸附水中杂质,C 正确;D .铁元素是第26号元素,位于元素周期表的d 区,D 错误;故选D 。
3.下列表示正确的是A.氯化钠的晶胞:B.HCl 的电子式:C.基态3+Fe 的价层电子轨道表示式:D.的名称:乙二酸乙二酯【答案】C【解析】【详解】A .氯化钠离子晶体中,阴、阳离子配位数均为6,晶胞结构如图:,A 错误;B .HCl 为共价化合物,电子式:,B 错误;C .Fe 原子序数26,基态3+Fe 价层电子排布:53d ,轨道表示式:,C 正确;D .的名称:乙二酸二乙酯,D 错误;答案选C 。
2014-2015学年上学期高中期末考试卷(高二理科生物)(含答案)

2014-2015学年上学期期末考试高二生物(理科)试卷说明:本试卷分第I卷(选择题)和第II卷(非选择题)两部分。
考试结束后,将答题卡交回。
满分100分,考试时间120分钟。
第一卷(选择题,共60分)一、选择题(本题包括40小题,每题1.5分,共60分。
每小题只有一个....选项符合题意)1.下列有关组成生物体化学元素和化合物的叙述,正确的是 ( )A.磷是脂肪、ATP、DNA等不可缺少的成分 B.酶和核酸都是含有氮的生物大分子C.肌肉细胞中含量最多的化合物是蛋白质 D.纤维素是植物细胞的主要储能物质2.下面关于蛋白质的叙述中,正确的是()A.蛋白质是酶,其基本组成单位是氨基酸B.每种蛋白质都是由20种氨基酸组成的C.蛋白质是肽链以一定方式形成具有复杂空间结构的高分子化合物D.各种蛋白质都含有C、H、O、N、P等元素3.右图是细胞亚显微结构模式图。
下列相关叙述,正确的是()A.②是内质网,是细胞内蛋白质合成和加工以及脂质合成的“车间”B.③是中心体,细胞分裂间期中心体发出纺锤丝,形成纺锤体C.④是核糖体,无生物膜结构,其合成与核仁有关。
D.⑤是核孔,是DNA进出细胞核的通道4.将三种洋葱鳞片叶表皮放在相同浓度的蔗糖溶液中,一段时间后制成临时装片放在显微镜下观察到下图所示的不同状态的细胞图像。
这3个细胞原来细胞液浓度的高低关系是()A.甲>乙>丙 B.甲<乙<丙C.乙>甲>丙 D.甲=乙=丙5对于下列各结构在生物中的叙述,不正确的是()①叶绿体②染色体③核膜④核糖体⑤细胞壁⑥拟核A.①~⑤在绿藻体内都存在 B.大肠杆菌和蓝藻共有的是④⑤⑥C.除①②③外其他都在乳酸菌的体内存在D.菠菜和发菜体内都含有①③④⑤6.如图所示:甲图中①②表示目镜,③④表示物镜,⑤⑥表示物镜与载玻片之间的距离,乙和丙分别表示不同物镜下观察到的图像。
下面描述正确的是 ( )A.①比②的放大倍数大,③比④的放大倍数小B.把视野里的标本从图中的乙转为丙时,应选用③,同时提升镜筒C.从图中的乙转为丙,正确调节顺序:转动转换器→调节光圈→移动标本→转动细准焦螺旋D.若使物像放大倍数最大,甲图中的组合一般是②③⑤7.下列关于人体细胞结构和功能的叙述,错误的是()A、唾液腺细胞和胰腺细胞中高尔基体数量较多B、在mRNA合成的同时就会有多个核糖体结合到mRNA上C、核孔是生物大分子可以选择性地进出的通道D、吸收和转运营养物质时,小肠绒毛上皮细胞内线粒体集中分布在细胞两端8.下列关于细胞膜的流动性和选择透过性的叙述,不正确的是( )A.流动性的基础是组成细胞膜的磷脂分子和蛋白质分子大多是可以运动的B.选择透过性的基础是细胞膜上的载体蛋白和磷脂分子具有特异性C.细胞的胞吞和胞吐体现了细胞膜的流动性D.钾离子通过主动运输的形式进入细胞,体现了细胞膜的选择透过性9.如图所示为细胞膜的亚显微结构,其中a和b为物质的两种运输方式,下列对细胞膜结构和功能的叙述不正确的是 ( )A.如果图中所示为肝细胞膜,则尿素的运输方向是Ⅱ→ⅠB.细胞间的识别、免疫、细胞的癌变与②有密切的关系C.大多数②可以运动D.b过程不需要能量,a过程能体现膜的选择透过性这一生理特性10. 对光合作用过程中物质转变途径的叙述,错误的是()A.碳原子:CO2→C3化合物→(CH2O) B.氧原子:H2O→O2C.氢原子:H2O→ATP→(CH2O) D.氧原子:CO2→C3化合物→(CH2O)11. 下图为不同条件下酶促反应的速率变化曲线,相关叙述错误的是()A.在c点增加酶的浓度,反应速率将加快B.Ⅱ比Ⅰ反应速率慢的原因是温度低使酶活性降低C.bc段影响反应速率的主要限制因子是底物浓度D.在a点增加底物浓度,反应速率将加快12.下图表示比较过氧化氢在不同条件下的分解实验。
XXX2014-2015学年高二上学期期末考试 化学试题

XXX2014-2015学年高二上学期期末考试化学试题XXX2014-2015学年高二上学期期末考试化学试题说明:1.测试时间:90分钟总分:100分2.选择题涂在答题纸上,非选择题答在答题纸的相应位置上可能用到的相对原子质量:H:1 C:12 O:16 Fe:56 Cu:64第Ⅰ卷(客观题,共50分)一、选择题(每小题只有1个选项符合题意,每小题2分,共20分)1.1,3-丁二烯和2-丁炔分别与氢气反应的热化学方程式如下:CH2=CH-CH=CH2(g)+2H2(g)→CH3CH2CH2CH3(g) ΔH=-236.6kJ/molCH3-C≡C-CH3(g)+2H2(g)→CH3CH2CH2CH3(g) ΔH=-272.7kJ/mol。
由此不能判断()A。
1,3-丁二烯和2-丁炔稳定性的相对大小B。
1,3-丁二烯和2-丁炔分子储存能量的相对高低C。
1,3-丁二烯和2-丁炔相互转化的热效应D。
一个碳碳三键的键能与两个碳碳双键的键能之和的大小2.下列有关说法错误的是()A。
NH3(g)+HCl(g)=NH4Cl(s)低温下能自发进行,说明该反应的ΔH<0B。
为保护海轮的船壳,常在船壳上镶入锌块C。
纯碱溶于热水中,去污效果增强,说明纯碱的水解是吸热反应D。
反应N2(g)+3H2(g)⇌2NH3(g)(ΔH<0)达平衡后,降低温度,正反应速率增大、逆反应速率减小,平衡向正反应方向移动3.运用有关概念判断下列叙述正确的是()A。
1 mol H2燃烧放出的热量为H2的燃烧热B。
活化分子之间的碰撞不一定都是有效碰撞反应C。
有0.1mol/L和-1互为同系物D。
BaSO4的水溶液不易导电,故BaSO4是弱电解质4.有三种溶液:①CH3COOH、②NaOH、③CH3COONa,下列说法正确的是()A。
溶液①中,c(CH3COO)=c(H+)B。
溶液①、②等体积混合,混合液中c(CH3COO)等于溶液③中的c(CH3COO)C。
2014-2015学年第2学期期末考试

姓名____________ 学号________________ 班级或选课课号______________________________ 座号_______任课教师______________
密 封 线 内 不 要 答 题 ―――――――――――――――――――密――――――――――――――――-封――――――――――――――――线――――――――――――――――――――
2014-2015学年第2学期期末考试
《课程名称全称(以人才培养方案为准)》答卷A(或B)
(供 院(系) 专业 班使用)
题 号 一 二 三 四 (请根据实际情况增减列数) 总 分
得 分 (请根据实际情况增减列数)
流水评卷人 签名
非流水评卷 签名
总分合计人(签名)________________ 评卷复核人(签名)________________
一、试题类型(共 题,每小题 分 ,共 分)
1. 2.
得分
密 封 线 内 不 要 答 题
――――――――――――――――――密――――――――――――――――-封―――――――――――――――――线――――――――――――――――――――――
二、试题类型(共 题,每小题 分 ,共 分)
1.
2.
三、试题类型(共题,每小题分,共分)
密 封 线 内 不 要 答 题
――――――――――――――――――密――――――――――――――――-封―――――――――――――――――线――――――――――――――――――――――
四、试题类型(共 题,每小题 分 ,共 分)
1.
2.。
2014-2015学年度高二上学期期末试卷

2014-2015学年度高二上学期期末试卷高二化学注意事项:1.答题前填写好自己的姓名、班级、考号等信息2.请将答案正确填写在答题卡上第I 卷(选择题)请点击修改第I 卷的文字说明一、选择题(题型注释)1.2010年上海世博会主题“城市.让生活更美好”;2011年“国际化学年”的主题是“化学,我们的生活,我们的未来”;2013年1月全国大部分地区出现雾霾天气,北京PM2.5浓度达993,系中国有该监测数据以来最高的一次。
“拯救人类的最后机会”只有节能减排,下列属最有希望的新能源是 ( )①天然气 ②煤 ③石油 ④水能 ⑤太阳能 ⑥地热能 ⑦风能 ⑧氢能A.①②③④B.⑤⑥⑦⑧C.③④⑤⑥D.除①②外2.分子式为C 2H 6O 的有机物,有两种同分异构体,乙醇(CH 3CH 2OH)、甲醚(CH 3OCH 3),则通过下列方法,不可能将二者区别开来的是 ( )A .红外光谱B .1H 核磁共振谱C .质谱法D .与钠反应3.下列有机物不是同一种物质的是( )A .C ClCl H H 和C Cl Cl H H B .CH 2=CH —CH=CH 2和 CH CH CH 2CH 2C.C(CH3)3C(CH3)3和CH3(CH2)3C(CH3)3 D.CH CHCH3CH3CH3CH3和CHCHCH3CH3CH3CH34.化学家们合成了如图所示的一系列的星烷,如三星烷、四星烷、五星烷等。
下列说法不正确的是 ( )A.它们之间互为同系物 B.三星烷的化学式为C9H12C.三星烷与丙苯互为同分异构体 D.它们的一氯代物均只有两种5.A、B两种有机物组成的混合物,当其质量相等时,无论A、B以何种比例混合,完全燃烧时产生H2O的量均相等,符合这一条件的组合是 ( )①同分异构体②同系物③最简式相同④含氢质量分数相同⑤分子中氢原子数相同⑥分子中氢、氧原子数分别相同A.①③④ B.①②③ C.①⑤⑥ D.②④⑥6.某有机物链状分子中含a个甲基,n个亚甲基(—CH2—),m个次甲基(),其余为氯原子。
2014—2015学年度第一学期期末考试

2014— 2015学年度第一学期期末考试八年级语文试卷(满分:100分;考试时间:120分钟)友情提示: 2.3.1. 根据拼音写汉字,(1)全桥结构y u n chan ()(),和四周景色配合得十分和谐。
()失措。
),或者是几座小山配合着 (5) 这些石刻狮子,有的母子相抱,有的交头接耳,有的像倾听水声,千态万状,惟妙惟肖( )。
(6) 日落的景象和日出同样壮观、绮 ()丽,而且神秘迷人。
2.结合句意,判断下列句子中加点词换成括号里的词恰当的一项是() ・ ・(2分)A. 他们杀孩子、老师、还有牧师,他们全是纯朴 勤劳的普通市民。
(淳朴)・ ・B. 今天,帝国居然还天真 地以为自己就是真正的物主。
(率真)・ ・C. 他们小声议论着,似乎怕惊扰那肃穆.的空气。
(严肃)D. 这些日子,家中光景很是惨淡.,一半为了丧事,一半为了父亲赋闲。
(冷 1.本试卷6页。
考生将自己的姓名、准考证号及所有答案均填写在答题卡上。
答题要求见答题卡上的“注意事项”。
一、语基(22分)或给加点字注音。
(4分)(2) 鬼子们拍打着水追过去,老头子张 hu d ng(3) 或者是重 lu d n ( )叠zh rng ( 竹子花木,全在乎设计者和匠师们生平多阅历。
(4) 因桥下多半是急流,人们到此总要 zh u ( )足欣赏飞瀑流泉。
淡)① 到处呈现一片衰草连天的景象,准备迎接风雪载途的寒冬②北雁南飞,活跃在田 间草际的昆虫销声匿迹③到了秋天,果实成熟,植物的叶子渐渐变黄,在秋风中簌簌地落了下来④在地球上温带和亚热带区域里,年年如是,周而复始。
①4.名著阅读。
(6分)(1)《钢铁是怎样炼成的》最大的成功之处在于塑造了______ 这个无 产阶级英雄形象,他在 ____________ 的影响下逐步走上革命道路。
在他的身上凝聚着那个时代最美好的精神品质,请写出两种: _______________ (4 分)(2) “两句一行,大约读了二三十行罢,他说:“给我读熟。
2014-2015学年度第一学期期末考试

2014-2015学年度第一学期期末考试九年级化学试卷考生注意:1、本卷共三大题,满分60分。
考试时间为45分钟。
14 P—31一、选择题(本大题共10小题,每题只有一个正确答案,每小题2分,共20分)请将选出的选项序号填入下面的答题表内。
1、自来水的生产过程主要包括以下流程,其中发生化学变化的是()2、我国新修订的《环境空气质量标准》增加了PM2.5监测指标。
PM2.5是指2.5微米以下的细微颗粒物,它对人体健康和环境质量的影响很大。
下列措施对PM2.5的治理起不到积极作用的是()A、城市道路定时洒水B、大力发展火力发电C、大力植树造林D、加强建筑工地扬尘控制3、下列微粒的结构示意图中,表示阴离子的是()4、从分子和原子的角度分析并解释下列事实,其中不正确的是()A、品红在水中扩散——分子在不断运动B、物体的热胀冷缩——分子的大小发生变化C、氧化汞分解成汞和氧气——分子可以再分D、一滴水中大约有1.67×1021个水分子——分子很小5、硒(Se)是一种非金属元素,如果缺硒可能会引起表皮角质化和癌症,含适量硒的矿泉水有益于人体健康。
在硒酸H2SeO4中,Se元素的化合价是()A、+2B、+3C、+4D、+66、下列图示实验操作中,正确的是( )7、如图为铝在元素周期表中的信息和原子结构示意图,从图中不能得到的信息是( )A 、铝是地壳中含量最多的金属元素B 、铝原子的质子数、核外电子数均为13C 、铝元素的相对原子质量为26.98D 、铝原子在化学反应中容易失去3个电子8、蚊虫叮咬时分泌的蚁酸(CH 2O 2)会使人体皮肤肿痛。
下列有关蚁酸的说法正确的是( )A 、蚁酸是氧化物B 、蚁酸是由碳、氢、氧三种原子构成的C 、蚁酸中碳、氧元素的质量比为1:2D 、蚁酸中氢元素的质量分数最小9、图中“●”和“○”分别表示两种元素的原子,能用该图表示的化学反应是( )A 、2CO+O 2 2CO 2B 、C+CO 2 2COC 、H 2+Cl 2 2HClD 、2H 2+O 2 2H 2O10、对比是学习化学的重要方法。
浙江省鄞州高级中学2014-2015学年高二上学期期中考试化学试题 Word版含答案

鄞州高级中学2014学年第一学期期中考试高二化学试题命制:化学命题小组审核:化学命题小组说明:1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷两部分。
满分100分,考试时间90分钟。
2.可能用到的相对原子质量:H-1,C-12,N-14, O-16,Na-23,Mg-24Al-27 S-32, Cl-35.5, Fe-56, Cu-64, Zn-65, Ag-108第Ⅰ卷(共58分)一、选择题:(本题包括14小题,每小题2分,共28分,每小题只有1个正确答案)1、某城市人口密度大,汽车等交通工具向大气的对流层中大量排放碳氢化合物、氮氧化物等有害物质,则下列现象最有可能发生的是A.酸雨B.臭氧空洞 C.光化学烟雾 D.温室效应2、下列反应属于放热反应的是A.焦炭和二氧化碳共热 B.NaOH溶于水C.KClO3受热分解D.CaO溶于水3、下列与化学反应能量变化相关的叙述正确的是A.生成物能量一定低于反应物总能量B.放热反应不必加热就一定能发生C.应用盖斯定律,可计算某些难以直接测量的反应的焓变D.同温同压下,H2(g)+Cl2(g)===2HCl(g)在光照和点燃条件的ΔH不同4、下列反应没有涉及原电池的是A.生铁投入稀盐酸中 B.铜片与银片用导线连接后,同时插入FeCl3溶液中C.纯锌投入硫酸铜溶液中 D.含铜的铝片投入浓硫酸中5、电解CuCl2和NaCl的混合溶液,阴极和阳极上分别析出的物质是A.H2和Cl2B.Cu和Cl2 C.H2和O2D.Cu和O26、反应2SO 2+O22SO3经一段时间后,SO3的浓度增加了0.4 mol·L-1,在这段时间内用O2表示的反应速率为0.04 mol·L-1·s-1,则这段时间为A.0.1 s B.2.5 s C.5 s D.10 s7、相同温度下,100 mL 0.01 mol·L-1的醋酸溶液与10 mL 0.1 mol·L-1的醋酸溶液相比较,下列数值前者大于后者的是A.中和时所需NaOH的量 B.c(H+) C.c(OH-) D.c(CH3COOH)8、反应CO+H 2O(g)CO2+H2在1000 K达到平衡时,分别改变下列条件,平衡常数K值发生变化的是A.将压强减小至原来的一半 B.将反应温度升高至1200 KC.添加催化剂 D.增大水蒸气的浓度9、不能用化学平衡移动原理说明的事实是A.合成氨在高压下进行是有利的 B.温度过高对合成氨不利C.使用催化剂能使合成氨速度加快 D.及时分离从合成塔中出来的混合气,有利于合成氨10、可确认发生化学平衡移动的是A.平衡常数发生了改变 B.有气态物质参加的可逆反应达到平衡后,改变了压强C.化学反应速率发生了改变 D.可逆反应达到平衡后,使用催化剂11、将相同质量的铜片分别和过量浓硝酸、稀硝酸反应,下列叙述正确的是A.反应速率:两者相同B.消耗硝酸的物质的量:前者多,后者少C.反应生成气体的颜色:前者浅,后者深D.反应中转移的电子总数:前者多,后者少12、在容积不变的密闭容器中存在如下反应:2A(g)+B(g)3C(g);ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是A.图Ⅰ表示的是t1时刻增大反应物的浓度对反应速率的影响B.图Ⅱ表示的一定是t1时刻加入催化剂后对反应速率的影响C.图Ⅲ表示的是温度对化学平衡的影响,且乙的温度较高D.图Ⅲ表示的是催化剂对平衡的影响,且甲的催化效率比乙高13、下列叙述不正确...的是A.钢铁腐蚀的正极反应:Fe-3e-=Fe3+B.铁船底镶嵌锌块,锌作负极,以防船体被腐蚀C.原电池是将化学能转化为电能的装置D.工业上电解饱和食盐水的阳极反应:2Cl--2e-=Cl2↑14、某小组为研究电化学原理,设计右图装置,下列叙述不.正确的是A.a和b不连接时,铁片上会有金属铜析出B.a和b用导线连接时,铜片上发生的反应为:Cu2++2e-===CuC.无论a和b是否连接,铁片均会溶解,溶液均从蓝色逐渐变成浅绿色D.a和b分别连接直流电源正、负极,电压足够大时,Cu2+向铜电极移动二、选择题:(本题包括10小题,每小题3分,共30分,每小题只有1个正确答案)15、用浓氯化铵溶液处理过的舞台幕布不易着火,其原因是①幕布的着火点升高②幕布的质量增加③氯化铵分解吸收热量,降低了温度④氯化铵分解产生的气体隔绝了空气A.①② B.③④ C.①③ D.②④16、下列说法错误的是A. NH4NO3溶于水虽然吸热,但其溶于水是自发过程B. 加热液体(温度高于沸点)会自发转变成气体,可用焓变解释C. 对于同一物质来讲,熵值的大小与其状态有关,固态物质的熵值通常最小D. 要正确判断化学反应能否自发进行,要综合考虑反应的ΔH 和ΔS 。
【精品解析纯word版】化学卷·2015届浙江省效实中学高二下学期期末考试

浙江效实中学2013—2014学年度下学期期末考试高二化学试题可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 Al 27 S 32 Cl 35.5 K 39 Ca 40 Zn 65 Mn 55 Fe 56 Cu 64 Br 80 Ag 108 I 127注意:(1)本试卷分Ⅰ卷(选择题)和Ⅱ卷(非选择题);(2)满分100分;考试时间100分钟;(3)本场考试不得使用计算器。
【试卷综析】本试卷在注重考查学科核心知识的同时,突出考查考纲要求的基本能力,重视学生科学素养的考查,知识考查涉及综合性较强的问题、注重主干知识,兼顾覆盖面。
以基础知识和基本技能为载体,以能力测试为主导。
化学计量的有关计算、有机物的基本反应类型、化学与环境、溶液中的离子反应、阿伏伽德罗定律、元素化合物知识、化学实验题、常见的有机物及其应用等主干知识,考查了较多的知识点。
注重常见化学方法,应用化学思想,体现学科基本要求。
第I卷选择题(共40分)一、选择题(每小题2分,共40分。
每小题只有一个选项符合题意。
)1. 化学与生产、生活密切相关。
下列叙述正确的是A.碘的升华、溴水中萃取溴、石油的分馏、煤的干馏均是物理变化B.BaSO4难溶于水是弱电解质,在医学上用作钡餐C.14C可用于文物年代的鉴定,14C与12C互为同位素D.明矾和氯气均用于水的消毒、杀菌【知识点】本题考查化学与生产、生活相关知识【答案解析】C 解析:A煤的干馏是化学变化,B.BaSO4难溶于水但是强电解质,D.明矾不能用于水的消毒、杀菌,明矾净水是吸附悬浮固体颗粒物。
C正确,所以选C【思路点拨】本题考查化学与生产、生活相关知识,属于简单题。
2.在80 g密度为d g·cm-3的硫酸铁溶液中,含有2.8 g Fe3+,则此溶液中SO2-4的物质的量浓度为(单位为mol·L-1)A.15d/16 B.5d/16 C.3d/8 D.5d/8知识点】本题考查溶液中浓度计算知识【答案解析】A解析:V(溶液)=80g/dg·cm-3,n Fe3+=2.8 g/56g·mol-1=0.05mol,则n SO2-4=0.075mol,所以C( SO2-4)= n SO2-4/V=15d/16 mol·L-1【思路点拨】本题考查溶液中浓度计算,注意单位换算及公式间的转换。
浙江省浙南名校2023-2024学年高二下学期4月期中考试化学试题(含答案)

2023学年第二学期浙南名校联盟期中联考高二年级化学学科试题考生须知:1.本卷共8页,满分100分,考试时间90分钟。
2.答题前,在答题卷指定区域填写班级、姓名、考场号、座位号及准考证号并填涂相应数字。
3.所有答案必须写在答题纸上,写在试卷上无效。
4.考试结束后,只需上交答题纸。
5.可能用到的相对原子质量:H-1 C-12 N-14 O-16 Fe-56选择题部分一、选择题(每小题只有一个选项符合题意,每小题3分,共48分)1. 下列属于离子晶体并含有共价键的是A. CH 3OHB. Mg 3N 2C. NH 4ClD. SiO 22. 下列表示错误的是A. Ca 2+的结构示意图:B. HClO 的电子式:C. 的名称是:2,2—二甲基—4—乙基己烷D. SO 2VSEPR 模型:3. 物质的性质决定用途,下列两者对应关系不正确的是A. 金刚砂(SiC)有类似金刚石结构,具有优异的耐高温性能,可用作高温结构材料B. 乙二醇易溶于水,黏度高,可用作汽车防冻液C. 液态氯乙烷气化时吸热,具有冷冻麻醉作用,可用于肌肉拉伤、关节扭伤等的镇痛D. 碳酸氢钠可中和酸并受热分解,可用于制作食品膨松剂4. 火箭推进发生反应的化学方程式为(C 2H 8N 2中C 、N 元素的的28224222C H N 2N O 2CO 4H O 3N =+↑++↑的化合价相等)。
N A 为阿伏加德罗常数的值,下列说法不正确的是A. C 2H 8N 2是还原剂B. N 2O 4被还原C. 氧化产物与还原产物物质的量之比为2:3D. 1molN 2O 4完全反应,有8N A 个电子转移5. 在溶液中能大量共存的离子组是A. 、K +、、Br - B. Ag +、Na +、、C. 、Fe 3+、Al 3+、SCN- D. Ca 2+、Mg 2+、F -、6. 下列有关说法不正确的是A. 配制一定物质的量浓度的氯化钾溶液步骤为:计算、称量、溶解、洗涤转移、定容、摇匀、装瓶B. 乙酸乙酯制备实验中,用NaOH 溶液除去粗酯中的杂质且可降低酯的溶解度,更利于分离C. 通过乙酸晶体的X 射线衍射实验,既能测晶胞中含有的乙酸分子数,也能推乙酸分子的空间结构D. 用一定量的浓溴水可以鉴别出溴乙烷、乙醛溶液和苯酚溶液7. 下列化学反应与离子方程式相符的是A. 用饱和Na 2CO 3溶液处理水垢中的CaSO 4:B. Al 溶于足量的NaOH 溶液:C. 向AgNO 3溶液中加入过量氨水:D. 氯乙酸乙酯在足量NaOH 溶液中加热:8. 下列有关实验操作或分析正确的是A. 装置甲用于验证浓硫酸的脱水性B. 装置乙用于证明乙炔能使溴水褪色C. 装置丙用于制备Fe(OH)2,且能长时间观察到白色沉淀D. 装置丁用于标准Na 2C 2O 4溶液测定未知KMnO 4溶液的浓度9. 石墨与F 2在450℃反应,石墨层间插入F 得到层状结构化合物(CF)x,该物质仍具润滑性,其单层局部4NH +3HCO -3NO -2S -4MnO -23SiO -2233CO CaCaCO -+↓+=()224Al 4OH 4H O Al OH H --⎡⎤↑⎣⎦++=+()32324Ag 4NH H O Ag NH 4H O ++⎡⎤⎦+⎣+⋅=225225ClCH COOC H 2OH HOCH COO C H OH Cl ∆---+−−→++结构如图所示,下列关于该化合物的说法错误的是A. 与石墨相比,(CF)x 导电性减弱B. 与石墨相比,(CF)x 抗氧化性增强C. 1mol(CF)x 中含有2.5xmol 共价单键D. (CF)x 中C-C 的键长比C-F 短10. 抗生素克拉维酸的结构简式如图所示,下列关于克拉维酸的说法错误的是A. 分子中含有手性碳原子B. 分子中含有6种官能团,分子式为C 8H 9NO 5C. 可形成分子间氢键D. 1mol 该物质最多可与2molNaOH 反应11. X 、Y 、Z 、M 、Q 五种短周期元素,原子序数依次增大。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
勤奋学校2014年学年度第二学期期末考试
高二化学
一、选择题
(每题4分,共60 分)
1、二甲醚和乙醇是同分异构体,其鉴别可采用化学方法或物理方法,下列鉴别方法中不能对二者进行鉴别的是( )
A.利用金属钠或者金属钾 B.利用质谱法
C.利用红外光谱法 D.利用核磁共振氢谱
2、下列各组有机物只用一种试剂无法鉴别的
是()
A.乙醇、甲苯、硝基苯 B.四氯化碳、己烷、己烯
C.苯、甲苯、环己烷 D.苯、乙醇、乙酸
3、将等体积的苯、汽油和水在试管中充分混合后静置。
下列图示现象正确的是:()
4、下列关于乙醇的说法不正确的是( )
A.可用纤维素的水解产物制取
B.可由乙烯通过加成反应制取
C.与乙醛互为同分异构体
D.通过取代反应可制取乙酸乙酯
5、山梨酸是一种常见的食物添加剂,它是一种无色针状晶体或白色粉末,它的结构简
式为。
下列关于山梨酸的叙述不正确的是
A.山梨酸易溶于乙醇
B.山梨酸能与氢气发生加成反应
C.山梨酸能和乙醇反应生成酯
D.1mol山梨酸能和金属钠反应生成1mol氢气
6、下列有机物命名正确的
是
A.3,3二甲基丁烷B.3甲基2乙基戊烷
C.4,5二甲基己烷D.2,3二甲基丁烷
7、CO2的的资源化利用是解决温室效应的重要途径。
以下是在一定条件下用NH3捕获CO2生成重要化工产品三
聚氰胺的反应:
下列有关三聚氰胺的说法正确的是
A、分子式为C3H6N3O3
B、分子中既含极性键,又含非极性键
C、属于共价化合物
D、生成该物质的上述反应为中和反应
8、如图是立方烷的球棍模型,下列有关说法不正确的是
( )
A.其一氯代物只有一种
B.其二氯代物有三种
C.在光照下,其能与氯水发生取代反应
D.它与苯乙烯(C6H5—CH===CH2)互为同分异构体
9、下列化学用语正确的是()
A
.聚丙烯的结构简式为:
B
.丙烷分子的比例模型为:
C
.四氯化碳分子的电子式为:D.2-乙基-1,3-
丁二烯的键线式:
10、下列营养物质中,属于高分子化合物的是
A.淀粉 B.蔗糖 C.油脂 D.葡萄糖
11、可以在有机反应中引入羟基的反应类型有①取代;②加成;③消去;④酯化;⑤氧化;⑥还原。
下列组合中正确的是:
A. ①②③ B ①②⑥ C ①④⑤⑥ D ①②③⑥
12、下列有机物属于烃的是
A.C2H5OH B.CCl4C.C2H6D.CH3COOH
13、第一次用无机物制备有机物尿素,开辟人工合成有机物先河的科学家是()
A.瑞典的贝采利乌斯B.德国的凯库勒
C.德国的李比希 D.德国的维勒
14、室内空气污染的主要来源之一是现代人的生活中使用的化工产品。
如泡沫绝缘材料的办公用品、化纤地毯及书报、油漆等不同程度释放出的气体。
该气体可能是 ( )
A.甲醛 B.甲烷 C.一氧化碳D.二氧化碳
15、下列物质中属于有机物的是()
①氰化钠(NaCN)②丙酮③丁炔④碳化硅(SiC)⑤碳酸⑥CO ⑦KSCN
A.①②③④⑦B.①②③ C.②
③D.全部都是
二、填空题
(每空2分,共40 分)
16、化学式为C6H12的某烯烃的所有碳原子都在同一平面上,则该烯烃的结构简式为___________________,其名称为______________;在核磁共振氢谱图上应该出现_____个峰。
17、如图是某种只含有C、H、O、N的有机物简易球棍模型。
请回答下列各题。
(1)该分子属氨基酸,其分子式为________。
(2)在一定条件下,该分子可以通过聚合反应生成________(填“糖类”“油脂”或“蛋白质”)。
(3)在一定条件下,该分子可以与乙醇发生反应,请写出该反应的化学方程式_________。
18、已知某有机物的结构简式为:
(1)该有机物中所含官能团的名称
是▲、▲。
(2)该有机物发生加成聚合反应后,所得产物的结构简式为▲。
(3)写出该有机物发生消去反应的化学方程式(注明反应条件):
▲
19、实验室制备少量硫酸亚铁晶体的实验步骤如下:取过量洁净的铁屑,加入20%~30%的稀硫酸溶液,在50℃~80℃水浴中加热至不再产生气泡.将溶液趁热过滤,滤液移至试管中,用橡胶塞塞紧试管口、静置、冷却一段时间后有浅绿色晶体析出,收集产品.
(1)写出该实验制备硫酸亚铁的化学方程式:▲;
(2)采用水浴加热的原因是▲;
(3)反应时铁屑过量的目的是(用离子方程式表示)▲;
(4)溶液趁热过滤的原因是▲;
(5)塞紧试管口的目的是▲。
20、均衡的膳食结构可以保障身体健康。
⑴如果人体缺少易患夜盲症的维生素是。
⑵碳酸镁可治疗胃酸过多的原理是_____ ____(用离子方程表示)。
⑶油脂在人体内通过水解生成和甘油,再氧化分解,为人体提供能量。
⑷发育出现障碍,患营养缺乏症,这主要是由于摄取_________(填“蛋白质”、“脂肪”或“糖类”)不足引起的。
下列食物中富含该物质的是(填字母)。
A.菠菜B.花生油 C.瘦肉 D.西瓜
参考答案
一、选择题
1、B
2、C
3、A
4、C
5、D
6、D
7、略
8、C
9、D
10、A
11、B
12、C
13、D
14、A
15、C
二、填空题
16、,2,3-二甲基-2-丁烯, 1。
(各2分)
17、(1) __ C3H7O3N ______。
(2) ___蛋白质_____。
(3) __略_。
18、(1)碳碳双键、(醇)羟基;
(2)
(3)
19、(1)Fe+H2SO4=FeSO4+H2↑(2)容易控制温度(3)Fe+2Fe3+═3Fe2+
(4)减小FeSO4的损失(5)防止空气进入试管将Fe2+氧化为Fe3+
20、【答案】
(1)维生素A (2)MgCO3+2H+==Mg2++H2O+CO2↑
(3)高级脂肪酸⑷蛋白质 C
【解析】
⑴人体缺少维生素A易患夜盲症。
(2)MgCO3+2H+==Mg2++H2O+CO2↑
⑶油脂在人体内通过水解生成高级脂肪酸和甘油。
⑷发育出现障碍,患营养缺乏症,这主要是由于摄取蛋白质不足引起的。
瘦肉中富含蛋白质。
