食品化学知识点
食品化学主要知识点

第一章水1、水结冰时体积增大;0℃下冰的导热值约为同温度下水的4倍;冰的热扩散速率是水的9倍;温差相等时,生物组织的冷冻速率比解冻速率更快。
(P11)2、分子的缔合:水分子在三维空间形成多重氢键键合,每个水分子具有相等数目的氢键给体和受体,能够在三维空间形成氢键网络结构。
(P13)3、水分子缔合的原因:①H-O键间电荷的非对称分布使H-O键具有极性,这种极性使分子之间产生引力;②由于每个水分子具有数目相等的氢键供体和受体,因此可以在三维空间形成多重氢键;③静电效应。
(P13)4、持水容量:通常用来描述基质分子(一般指大分子化合物)截留大量水的能力。
(P20)5、食品中水的存在形式:体相水(自由水、截留水)和结合水(化合水、邻近水、多分子层水)(P19)6、水与离子和离子基团的相互作用:①由于水中添加可解离的溶质,使纯水考氢键键合形成的四面体排列的正常结构遭到破坏②由于既不具有氢键受体又没有给体的简单无机离子,它们与水相互作用时仅仅是离子-偶极的极性结合③在稀水溶液中一些离子具有净结构破坏效应,这些离子大多为负离子和大的正离子,如:K+,Rb+,NH4+,Cl-,Br-,I-,NO3-,BrO3-,IO3-,ClO4-等④另外一些离子具有净结构形成效应,这些离子大多是电场强度大,离子半径小的离子。
如:Li+,Na+,Ca2+,Ba2+,Mg2+,Al3+,F-,OH-等(P23)7、水具有氢键键合能力的中性基团的相互作用:①水与溶质之间的氢键键合比水与离子之间的相互作用弱②氢键作用的强度与水分子之间的氢键相近③水能与某些基团,例如羟基、氨基、羰基、酰氨基和亚氨基等极性基团,发生氢键键合。
④结晶大分子的亲水基团间的距离是与纯水中最邻近两个氧原子间的距离相等⑤如果在水合大分子中这种间隔占优势,这将会促进第一层水和第二层水之间相互形成氢键⑥在生物大分子的两个部位或两个大分子之间可形成由几个水分子所构成的“水桥”8、水与非极性物质的相互作用:①水中加入疏水性物质,疏水基团与水分子产生斥力,从而使疏水基团附近的水分子之间的氢键键合增强,结构更为有序②疏水基团之间相互聚集,从而使它们与水的接触面积减小,结果导致自由水分子增多③非极性物质具有两种特殊的性质,蛋白质分子产生的疏水相互作用,极性物质能和水形成笼形水合物9、疏水水合:向水中添加疏水物质时,由于它们与水分子产生斥力,从而使疏水基团附近的水分子之间的氢键键合增强,使得熵减小,此过程成为疏水水合。
食品化学的知识点总结

食品化学的知识点总结一、食品成分食品的化学成分是指食品中含有的各种化学物质。
食品成分主要包括水分、蛋白质、脂肪、碳水化合物、维生素和矿物质等。
这些成分对于食品的营养价值和风味都有很大的影响。
1. 水分水是食品中最主要的成分之一,对于食品的质地、口感和营养价值都有着重要的影响。
食品中的水分含量是影响食品贮存以及微生物、酶、氧化、酶解等变质的主要因素之一。
2. 蛋白质蛋白质是食品中的主要营养成分,它是由氨基酸组成的,对于维持人体正常的生理功能和机体的发育都有重要的意义。
蛋白质在食品中的作用主要有增加食品的营养价值、影响食品的质地和口感等。
3. 脂肪脂肪是食品中的主要能量来源,也是体内沉积物和传导器,对于维持人的正常生理功能有重要的作用。
食品中的脂肪含量会影响食品的口感、香味和营养价值。
4. 碳水化合物碳水化合物是人体的主要能量来源,是构成膳食纤维的主要成分,对于维持人体生命活动和保持体能都有着重要的意义。
食品中的碳水化合物含量会影响食品的甜度、质地和口感。
5. 维生素维生素是对人体的新陈代谢活动和细胞分裂具有重要作用的微量营养素。
食品中的维生素种类繁多,对于维持人体的正常生理功能和增强人体的抵抗力都有着重要的作用。
6. 矿物质矿物质是人体必需的微量元素,对于人体的生理功能具有重要的作用。
食品中的矿物质种类繁多,对于人体的正常生长和发育都有着重要的意义。
二、食品的味道和香味的形成食品的味道和香味的形成是由于食品中的各种化学成分对人的感官器官产生的感觉。
食品的味道主要来自于咸、甜、酸、苦、鲜等味道,食品的香味主要来自于食品中的挥发性物质。
1. 咸味很多食品中都含有盐分,食品中的盐分会使食品呈现出咸味。
人的舌头上具有咸味感受器,当含有盐分的食品进入口腔时,就会产生咸味的感觉。
2. 甜味食品中含有碳水化合物会使食品呈现出甜味,当含有碳水化合物的食品进入口腔时,就会产生甜味的感觉。
3. 酸味食品中含有有机酸或无机酸会使食品呈现出酸味,当含有酸性物质的食品进入口腔时,就会产生酸味的感觉。
大一食品化学必背知识点

大一食品化学必背知识点食品化学作为食品科学与工程专业的一门重要课程,是探讨食品组成、结构、性质以及与食品相关的化学变化的学科。
在大一学习食品化学过程中,以下是一些必背的知识点,旨在帮助你更好地理解和掌握这门课程。
1. 食物营养成分分类:食物的主要营养成分包括碳水化合物、脂类、蛋白质、维生素和矿物质等。
其中,碳水化合物是食物的主要能源来源,脂类则提供能量和维护细胞结构,蛋白质是构成体细胞的重要成分,维生素和矿物质则在人体的代谢过程中起到调节和辅助作用。
2. 食物的化学成分:食物的化学成分是指食物中所含有的化学物质,主要包括水、有机物和无机物。
水是组成食物体积的主要成分,有机物包括碳水化合物、脂类和蛋白质等,无机物则包括无机盐和矿物质等。
3. 食物的理化性质:食物的理化性质是指食物在物理和化学方面所表现出的性质。
包括颜色、气味、味道、质地、pH值、溶解性以及吸湿性等。
这些性质直接影响到食物的品质和口感。
4. 食品中常见的食品添加剂:食品添加剂是指用于提高食品风味、保存食品、改善食品质地和色泽等目的而添加到食品中的物质。
常见的食品添加剂包括防腐剂、抗氧化剂、增稠剂、酸度调节剂、甜味剂等。
5. 食物加工过程中的化学反应:在食物加工过程中,会发生一系列的化学反应,如蛋白质的糖化反应、脂类的氧化反应、碳水化合物的糖热反应等。
了解这些反应有助于我们了解和掌握食物加工过程中需要注意的问题,以及如何优化食品的品质和口感。
6. 食品中的毒素与防治方法:食品中可能存在的毒素包括化学毒素和生物毒素。
化学毒素主要包括重金属、农药残留、致癌物质等,而生物毒素则包括细菌产生的毒素、霉菌毒素等。
了解这些毒素的来源、危害以及防治方法是食品安全的重要内容之一。
7. 食品中的保健成分:食品中的保健成分是指那些具有促进健康、预防疾病和延缓衰老等作用的物质。
常见的保健成分包括膳食纤维、多酚类化合物、维生素、矿物质等。
了解这些保健成分的作用和来源,有助于我们合理选择食品,保持健康生活方式。
食品化学中考知识点总结

食品化学中考知识点总结一、常见食品的化学成分及特性1. 碳水化合物碳水化合物是食品中的主要成分之一,包括单糖、双糖和多糖。
单糖主要是葡萄糖、果糖和半乳糖,双糖主要是蔗糖、麦芽糖和乳糖,多糖包括淀粉和纤维素。
碳水化合物在食品中主要作为能量的来源,同时也对食品的口感和外观有一定的影响。
2. 脂肪食品中的脂肪主要是甘油三酯,主要的饱和脂肪酸有硬脂酸、棕榈酸、豆酸、动物脂肪中的优酸等,而不饱和脂肪酸主要是亚油酸、亚麻酸、棕榈酸、还有芥麦油酸等。
食品中的脂肪可以提供热量和脂溶性维生素,同时对食品的口感和味道起到重要的作用。
3. 蛋白质食品中的蛋白质主要是由氨基酸构成的,常见的氨基酸有赖氨酸、异亮氨酸、苯丙氨酸和甲硫氨酸等。
蛋白质在食品中的作用主要是提供人体所需的氨基酸,同时也参与了食品的味道和口感。
4. 维生素食品中的维生素有水溶性维生素和脂溶性维生素两大类。
水溶性维生素主要有维生素C、维生素B1、维生素B2等,而脂溶性维生素主要有维生素A、维生素D、维生素E和维生素K等。
维生素对人体的生长发育和新陈代谢有重要的作用。
5. 矿物质食品中的矿物质主要包括钙、铁、锌、硒等,这些矿物质对人体骨骼的形成和维持、血液的凝血和免疫功能等都起到了重要的作用。
6. 食品添加剂食品添加剂是指用于改善食品品质、延长食品保质期、方便食品加工制作等目的而向食品中添加的各种化学物质。
主要包括色素、香精、甜味剂、防腐剂、抗氧化剂等。
二、常见食品的化学检测方法1. 蛋白质的检测蛋白质的检测方法主要包括比色法、滴定法和光学检测法等。
其中比色法是最常用的方法,基于蛋白质与某些物质发生颜色反应,通过测定反应产生的颜色的深浅来确定蛋白质的含量。
2. 脂肪的检测脂肪的检测方法主要有溶剂提取法、酶解法和氧值法等。
溶剂提取法是通过将食品中的脂肪提取出来,再用称量法或比色法来测定脂肪的含量。
3. 酸度值的检测食品中的酸度值是指其酸度的大小,通常以pH值来表示。
食品化学复习知识点

食品化学复习知识点一、名词解释1、食品化学:是从化学角度和分子水平上研究食品的化学组成、结构、理化性质、营养和安全性质以及它们在生产、加工、储存和运销过程中的变化及其对食品品质和安全性影响的科学。
2、构型:一个分子各原子在空间的相对分布或排列,即各原子特有的固定的空间排列,使该分子所具有的特定的立体结构形式。
3、变旋现象:当单糖溶解在水中的时候,由于开链结构和环状结构直接的相互转化,出现的一种现象。
4、间苯二酚反应:5、膨润现象:淀粉颗粒因吸水,体积膨胀到数十倍,生淀粉的胶束结构即行消失的现象。
6、糊化:生淀粉在水中加热至胶束结构全部崩溃,淀粉分子形成单分子,并为水所包围而成凝胶状态,由于淀粉分子是链状或分支状,彼此牵扯,结果形成具有粘性的糊状黏稠体系的现象。
7、淀粉老化:经过糊化后的淀粉在室温或低于室温的条件下放置后,溶液变得不透明甚至凝结而沉淀的现象。
8、多糖(淀粉)的改性:指在一定条件下通过物理或化学的方法使多糖的形态或结构发生变化,从而改变多糖的理化性能的过程。
(如胶原淀粉)9、同质多晶现象:同一种物质具有不同固体形态的现象。
10、油脂塑性:指在一定压力下表现固体脂肪具有的抗应变能力。
11、油脂的精炼:采用不同的物理或化学方法,将粗油(直接由油料中经压榨、有机溶剂提取到的油脂)中影响产品外观(如色素等)、气味、品质、的杂质去除,提高油脂品质,延长储藏期的过程。
(碱炼:NaOH去除游离脂肪酸)12、氨基酸的等电点:当氨基酸在某一pH值时,氨基酸所带正电荷和负电荷相等,即净电荷为零,此时的pH值成为氨基酸的等电点。
13、蛋白石四级结构:由多条各自具有三级结构的肽链通过非共价键连接起来的结构形式。
14、蛋白质的变性:把蛋白质二级及其以上的高级结构在一定条件下(如加热、酸、碱、有机溶剂、重金属离子等)遭到破坏而一级结构并未发生变化的过程。
15、水合性质:由于蛋白质与水的相互作用,使蛋白质内一部分水的物理化学性质不同于正常水。
食品化学知识点范文

食品化学知识点范文食品化学是研究食品组分、结构、性质、变化和相互作用的科学,涉及食品的营养和安全方面的知识。
下面是一些常见的食品化学知识点。
一、碳水化合物2.碳水化合物包括单糖、双糖和多糖,如葡萄糖、果糖、麦芽糖、蔗糖、淀粉和纤维素等。
3.碳水化合物分解为葡萄糖后进入血液循环,供给机体能量,并通过胰岛素调节血糖水平。
二、脂肪1.脂肪是由甘油和脂肪酸组成的化合物。
3.脂肪分为饱和脂肪、不饱和脂肪和转化脂肪酸等。
三、蛋白质1.蛋白质是由氨基酸组成的高聚合物,是构成生物体的重要组成部分。
2.蛋白质可以分为动物蛋白质和植物蛋白质,如肉、鱼、奶、豆类等。
3.蛋白质的主要功能包括供给机体能量、维持组织结构和功能、抗体产生和酶的催化等。
四、维生素1.维生素是一类对机体正常生长、发育、生理功能具有重要作用的有机物质。
2.维生素可以分为水溶性维生素和脂溶性维生素。
3.维生素不可被机体合成,需从食物中摄取。
五、矿物质1.矿物质是食物中的无机物质,包括钙、铁、锌、镁、钠、钾等。
2.矿物质对于机体的正常生理功能具有重要作用,如构成骨骼、维持神经传导、维持水平衡等。
六、食物添加剂1.食物添加剂是指用于改善食品品质和特性、提高加工性能和延长食品保质期的物质。
2.食物添加剂包括色素、甜味剂、防腐剂、抗氧化剂、增稠剂、着色剂等。
七、食品储藏和加工1.食品储藏是指将食品保存在适宜的条件下,防止食品变质和营养丢失的过程。
2.食品加工是指改变食品原有的物理、化学和生物学特性,提高食品的质量和风味的过程。
3.食品加工和储藏可以通过控制温度、湿度、氧气和光照等条件来保证食品的品质和安全。
八、食品变质和毒素1.食品变质是指食品由于微生物、酶和化学反应等原因而发生质量下降的过程。
2.食品变质可以表现为腐败、发酵、霉变等。
3.食品中的毒素包括微生物毒素、化学污染物和放射性物质等。
以上只是食品化学的一部分知识点,食品化学的研究范围广泛且深入。
对于食品的营养和安全,掌握食物化学的基本知识是非常重要的。
食品化学复习知识点

水1.冰:是水分子通过氢键有序排列成巨大且长的晶体。
2.冷冻食品中常见的4种冰晶体结构:六方形、不规则树枝状、粗糙的球形和易消失的球晶。
3.冰的特性——过冷(1)过冷是由于无晶核存在,当液体水冷却到冰点(0℃)以下仍不析出固体的现象(常常先被冷却成过冷状态,只有当温度降低到开始出现稳定性晶核时,或在震动促进下才会立即向冰晶体转化并促使温度回升到0℃,开始出现稳定性晶核的温度叫过冷温度)(2)若向冷水中投入一粒冰晶或摩擦器壁产生冰晶,过冷现象立即消失(3)过冷溶液中加入晶核,晶核逐渐形成长大的结晶,这种现象称之为异相成核(4)冰晶体的大小和结晶速度受溶质、温度、温度降低速度、溶质的种类和数量等因素影响4.水在食品中的存在状态:自由水、结合水(1)结合水特点:呈现低的流动性,在-40℃不会结冰,不能作为所加入溶质的溶剂,在质子核磁共振实验中使氢的谱线变宽(2)结合水分类:化合水——单层水——多层水——(自由水)(3)游离水分类:滞化水、毛细管水、自由流动水5.水与溶质的相互作用(1)水与离子或离子基团的相互作用:水合作用(2)水与极性基团的相互作用:各种有机分子与水之间的作用以氢键为主要方式(3)水与非极性基团的相互作用:主要为疏水水合作用疏水水合:含有非极性基团的烃类、脂肪酸、氨基酸以及蛋白质加入水中,由于极性的差异使疏水基尽可能聚集在一起以减少它们与水的接触,此过程称为疏水水合6.水分活度(Aw):在一定温度下,食品中水的蒸气压和该温度下纯水的饱和蒸气压的比值Aw与温度的关系:温度升高时,Aw随之升高,这对密封在袋中或罐内食品的稳定性有很大影响7.水的吸湿等温线:在一定温度条件下,用来联系食品的含水量(用每单位干物质中的水含量表示)与其水活度的关系图(MSI)【结合食品的吸湿等温线,解释各区间水的存在形式】区间Ⅰ:化合水,水与溶质结合最紧密区间Ⅰ与区间Ⅱ之间:化合水+单层水区间Ⅱ:化合水+单层水+多层水区间Ⅱ与区间Ⅲ之间:出现游离水区间Ⅲ:游离水,既可以作为溶剂,又有利于微生物生长8.滞后现象:食品的脱附曲线与吸湿曲线理论上应该一致,但实际不能重叠的现象【简述Aw与食品保存性的关系】1.Aw与微生物生命活动的关系:不同类群微生物生长繁殖的最低Aw范围是:大多数细菌为0.94-0.99,大多数霉菌为0.8.-0.94,大多数耐盐细菌为0.75,耐干燥霉菌和耐高渗透压酵母为0.60-0.65,、在Aw低于0.60时,绝大多数微生物就无法生长。
食品化学知识点
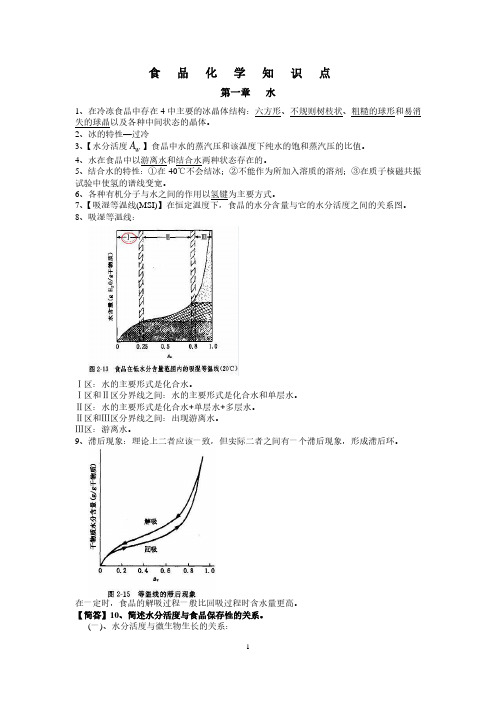
食品化学知识点第一章水1、在冷冻食品中存在4中主要的冰晶体结构:六方形、不规则树枝状、粗糙的球形和易消失的球晶以及各种中间状态的晶体。
2、冰的特性—过冷A】食品中水的蒸汽压和该温度下纯水的饱和蒸汽压的比值。
3、【水分活度W4、水在食品中以游离水和结合水两种状态存在的。
5、结合水的特性:①在-40℃不会结冰;②不能作为所加入溶质的溶剂;③在质子核磁共振试验中使氢的谱线变宽。
6、各种有机分子与水之间的作用以氢键为主要方式。
7、【吸湿等温线(MSI)】在恒定温度下,食品的水分含量与它的水分活度之间的关系图。
8、吸湿等温线:Ⅰ区:水的主要形式是化合水。
Ⅰ区和Ⅱ区分界线之间:水的主要形式是化合水和单层水。
Ⅱ区:水的主要形式是化合水+单层水+多层水。
Ⅱ区和Ⅲ区分界线之间:出现游离水。
Ⅲ区:游离水。
9、滞后现象:理论上二者应该一致,但实际二者之间有一个滞后现象,形成滞后环。
在一定时,食品的解吸过程一般比回吸过程时含水量更高。
【简答】10、简述水分活度与食品保存性的关系。
(一)、水分活度与微生物生长的关系:不同类群微生物生长繁殖的W A 最低范围是:大多数细菌为0.94~0.99,大多数霉菌为0.80~0.94,大多数耐盐细菌为0.75,耐干燥霉菌和耐高渗透压酵母为0.60~0.65。
在低于0.60时。
绝大多数微生物就无法生长。
细菌形成芽孢时的W A 阈值比繁殖生长时要高。
(二)、水分活度与酶水解的关系:当降低到0.25~0.30的范围,就能有效地减慢或阻止酶促褐变的进行。
(三)、水分活度与化学反应的关系:① 大多数化学反应都必须在水溶液中才能进行。
降低水分活度,食品中许多化学反应受到抑制,反应速率下降。
② 发生离子化学反应的条件是反应物首先必须进行离子的水合作用,所以要有足够的游离水。
③ 化学反应和生物反应都必须有水分子参与。
降低水分活度,减少了参加反应的水的有效数量,反应速率下降。
④ 当W A <0.8时,大多数酶活力受抑制;当W A 在0.25~0.30之间时,淀粉酶、多酚氧化酶和过氧化物酶就会丧失活力或受到强烈的抑制。
食品化学知识点

食品化学知识点一、食品组成及相关知识食品是指提供营养和能量,并满足人体生理和心理需求的物质。
食品大致可分为五大类:谷类、肉类、蔬菜类、水果类和奶类。
1.1 营养素营养素是指人体必须吸收的物质,包括碳水化合物、脂肪、蛋白质、维生素和矿物质等。
碳水化合物是人体能量的主要来源,包括单糖、双糖和多糖。
单糖包括葡萄糖、果糖和半乳糖等;双糖包括蔗糖、乳糖和麦芽糖等;多糖包括淀粉和纤维素等。
脂肪是人体必须吸收的营养素,包括不饱和脂肪酸和饱和脂肪酸等。
不饱和脂肪酸包括单不饱和脂肪酸和多不饱和脂肪酸等,可降低胆固醇水平,预防心血管疾病。
蛋白质是组成人体组织的重要成分,包括必需氨基酸和非必需氨基酸等。
维生素是维持人体生理功能的重要物质,包括水溶性维生素(如维生素B1、维生素B2、维生素B6、维生素C等)和脂溶性维生素(如维生素A、维生素D、维生素E、维生素K 等)等。
矿物质是人体必须吸收的元素,包括铁、钙、钾、镁、锌等。
1.2 食品添加剂食品添加剂是指在食品加工中添加的具有特定功能的物质,可分为色素、防腐剂、甜味剂、增味剂、膨松剂、酸味剂、稳定剂和乳化剂等。
色素可增加食品的色泽,使其更具吸引力;防腐剂可延长食品的保质期,防止细菌滋生;甜味剂可增加食品的甜度;增味剂可增强食品的香味和口感;膨松剂可增加食品的松软度;酸味剂可增加食品的酸味;稳定剂可提高食品的稳定性;乳化剂可使油水混合物更加均匀。
1.3 食品中的化学成分食品中含有多种化学成分,包括糖类、蛋白质、脂肪、矿物质、维生素、酸碱度等。
其中,糖类是食品中含量最高的成分之一,可分为单糖、双糖和多糖。
同时,食品中还含有不同种类的酸,如有机酸和脂肪酸等。
二、食品加工及相关知识2.1 食品生产加工食品生产加工包括原材料处理、加工制备、成品包装和贮存等环节。
其中,原材料处理包括采集、分级、分选、清洗、翻晒等步骤;加工制备包括切割、研磨、混合、腌制、烘干等步骤;成品包装包括采购包装材料、包装机械调试、包装等步骤;贮存包括成品的仓储、保管、配送、销售等步骤。
食品化学知识点总结

食品化学知识点总结work Information Technology Company.2020YEAR食品化学知识点总结1、食品剖析的目的包含两方面。
一方面是确切了解营养成分,如维生素,蛋白质,氨基酸和糖类;另一方面是对食品中有害成分进行监测,如黄曲霉毒素,农药残余,多核芳烃及各类添加剂等。
2、食品化学是研究食品的组成、性质以及食品在加工、储藏过程中发生的化学变化的一门科学。
3、食品分析与检测的任务:研究食品组成、性质以及食品在贮藏、加工、包装及运销过程中可能发生的化学和物理变化,科学认识食品中各种成分及其变化对人类膳食营养、食品安全性及食品其他质量属性的影响。
4、生物体六大营养物质:蛋白质、脂类、碳水化合物、无机盐、维生素、水5、蛋白质:催化作用,调节胜利技能,氧的运输,肌肉收缩,支架作用,免疫作用,遗传物质,调节体液和维持酸碱平衡. 蛋白质种类:动物蛋白和植物蛋白。
6、脂肪:提供高浓度的热能和必不的热能储备. 脂类分为两大类,即油脂和类脂油脂:即甘油三脂或称之为脂酰甘油,是油和脂肪的统称。
一般把常温下是液体的称作油,而把常温下是固体的称作脂肪类脂:包括磷脂,糖脂和胆固醇三大类。
7、碳水化合物在体内消化吸收较其他产能营养素迅速且解酵。
糖也被称为碳水化合物糖类可以分为四大类:单糖(葡萄糖等),低聚糖(蔗糖、乳糖、麦芽糖等等),多糖(淀粉、纤维素等)以及糖化合物(糖蛋白等等)。
8、矿物质又称无机盐.是集体的重要组成部分.维持细胞渗透压与集体的酸碱平衡,保持神经和肌肉的兴奋性,具有特殊生理功能和营养价值.9、维生素维持人体正常分理功能所必须的有机营养素.人体需要量少但是也不可缺少 .10、维生素A:防止夜盲症和视力减退,有抗呼吸系统感染作用;有助于免疫系统功能正常;促进发育,强壮骨骼,维护皮肤、头发、牙齿、牙床的健康;有助于对肺气肿、甲状腺机能亢进症的治疗。
11、维生素B1:促进成长;帮助消化。
食品化学(知识点)

10、引起滞后现象的原因 1、解吸过程中一些吸水与非水溶液成分作用而无法释放。 2、样品中不规则形状产生的毛细管现象的部位,欲填满或抽空水分需要不同的蒸汽压
(要抽出需要 P 内>P 外,要填满即吸着时需 P 外>P 内)。 3、解吸时,因组织改变,无法紧密结合水分,因此回吸相同水分含量时其水分活度较
从水的正常结构来看,所有离子对水的结构都起到破坏作用,因为它们都能阻止水在 0℃
下
结冰。
对全部高中资料试卷电气设备,在安装过程中以及安装结束后进行高中资料试卷调整试验;通电检查所有设备高中资料电试力卷保相护互装作置用调与试相技互术关,系电,通力根1保过据护管生高线产中敷工资设艺料技高试术中卷0资不配料仅置试可技卷以术要解是求决指,吊机对顶组电层在气配进设置行备不继进规电行范保空高护载中高与资中带料资负试料荷卷试下问卷高题总中2体2资,配料而置试且时卷可,调保需控障要试各在验类最;管大对路限设习度备题内进到来行位确调。保整在机使管组其路高在敷中正设资常过料工程试况1卷中下安,与全要过,加度并强工且看作尽护下可1都关能可于地以管缩正路小常高故工中障作资高;料中对试资于卷料继连试电接卷保管破护口坏进处范行理围整高,核中或对资者定料对值试某,卷些审弯异核扁常与度高校固中对定资图盒料纸位试,置卷编.工保写况护复进层杂行防设自腐备动跨与处接装理地置,线高尤弯中其曲资要半料避径试免标卷错高调误等试高,方中要案资求,料技编试术写5、卷交重电保底要气护。设设装管备备置线4高、调动敷中电试作设资气高,技料课中并3术试、件资且中卷管中料拒包试路调试绝含验敷试卷动线方设技作槽案技术,、以术来管及避架系免等统不多启必项动要方高式案中,;资为对料解整试决套卷高启突中动然语过停文程机电中。气高因课中此件资,中料电管试力壁卷高薄电中、气资接设料口备试不进卷严行保等调护问试装题工置,作调合并试理且技利进术用行,管过要线关求敷运电设行力技高保术中护。资装线料置缆试做敷卷到设技准原术确则指灵:导活在。。分对对线于于盒调差处试动,过保当程护不中装同高置电中高压资中回料资路试料交卷试叉技卷时术调,问试应题技采,术用作是金为指属调发隔试电板人机进员一行,变隔需压开要器处在组理事在;前发同掌生一握内线图部槽 纸故内资障,料时强、,电设需回备要路制进须造行同厂外时家部切出电断具源习高高题中中电资资源料料,试试线卷卷缆试切敷验除设报从完告而毕与采,相用要关高进技中行术资检资料查料试和,卷检并主测且要处了保理解护。现装场置设。备高中资料试卷布置情况与有关高中资料试卷电气系统接线等情况,然后根据规范与规程规定,制定设备调试高中资料试卷方案。
化学食品知识点总结

化学食品知识点总结一、化学食品的概念化学食品是指在生产、加工、处理过程中添加了化学成分的食品。
这些化学成分可能是防腐剂、色素、增味剂、增稠剂、抗氧化剂等。
其中一些化学成分可能对人体健康造成危害,因此化学食品备受关注。
二、常见的化学食品添加剂1. 防腐剂防腐剂是为了延长食品的保质期而添加的化学物质。
常见的防腐剂有亚硝酸盐、硫酸盐等。
亚硝酸盐可以防止细菌滋生,但长期食用会增加致癌风险;硫酸盐可以防止食品腐败,但过量摄入会对人体造成伤害。
2. 色素色素是为了使食品的颜色更加鲜艳而添加的化学物质。
一些常见的食品色素,如苏丹红、甲基橙,由于含有致癌物质而被禁用。
3. 增味剂增味剂是为了增加食品的味道而添加的化学物质。
例如,味精是一种常用的增味剂,但长期食用过量会对身体造成伤害。
4. 抗氧化剂抗氧化剂是为了延长食品的保质期而添加的化学物质。
常见的抗氧化剂有BHT、BHA等,但过量摄入会对身体造成危害。
5. 酸度调节剂酸度调节剂是为了调节食品的酸碱度而加入的化学物质。
常见的酸度调节剂有柠檬酸、乳酸等,但过量摄入会对人体造成不良影响。
三、化学食品对人体的危害1. 致癌一些化学食品添加剂含有致癌物质,长期摄入会增加罹患癌症的风险。
2. 增加慢性病的风险长期食用化学食品可能导致肥胖、糖尿病、高血压等慢性病的发生。
3. 损害器官功能某些化学食品添加剂会损害肝脏、肾脏等重要器官的功能,对人体健康造成威胁。
四、如何避免化学食品危害1. 多吃新鲜食材新鲜水果、蔬菜、肉类等食材不含化学添加剂,是最健康的食品选择。
2. 少食加工食品加工食品通常含有大量的化学添加剂,因此需要尽量减少食用。
3. 相关法规的了解了解食品安全相关法规,避免购买和食用含有禁用食品添加剂的食品。
五、结语化学食品对人体健康造成的危害备受关注,因此人们应该尽量避免食用化学食品,并选择新鲜食材做为食物来源。
同时,政府和相关部门也应该加强对食品添加剂的监管,确保食品安全。
食品化学知识点总结

食品化学知识点总结食品化学知识点总结食品化学是一门涉及食品中物质组成、变化过程以及相关理论的学科,是食品科学的一个重要分支。
在食品化学的研究中涉及了很多知识点,今天就来总结一下常用的食品化学知识点。
1. 食品中的物质组成:食品中的物质组成主要有水、蛋白质、碳水化合物、脂肪、矿物质、维生素、酶、香精、防腐剂等。
每种物质都有不同的作用,如碳水化合物主要提供能量,维生素和矿物质是构成人体细胞的必要元素,而酶则能促进食物的变化和消化。
2. 食品的加工方法:食品加工是指通过物理、化学、生物等手段对原料进行加工,使之成为食品。
常见的食品加工方法有烹饪、冷冻、烘干、研磨、熏制、蒸煮、烤制、腌渍、榨汁、凝固、混合等。
3. 口感特性:口感特性是指食物的质地、口味、气味、色泽等特征,它是影响食品受欢迎程度的重要因素。
口感特性主要由食品的物理性质和化学特性决定,如质地主要由结构性成分控制,口感主要由溶性物质控制,气味主要由挥发性物质控制,色泽主要由色素控制。
4. 食品安全:食品安全是指食品质量达到一定标准,确保不会对人体造成伤害,也就是不含有有害物质。
有害物质常见有有毒物质、有毒重金属、细菌、放射性物质等。
食品安全的管理措施有:遵守食品安全法律法规;实施食品安全管理体系;加强质量检测;落实危害溯源制度;采取防控措施等。
5. 食品添加剂:食品添加剂是指用于改变或增强食品的性质、口感、质量、安全性等的各种物质。
常见的食品添加剂有增稠剂、防腐剂、香精、着色剂、酸度调节剂、增味剂、抗氧化剂等。
食品添加剂在食品加工中起到了重要作用,但也要注意控制使用量,以免影响食品安全。
以上就是常见的食品化学知识点总结,这些知识点对于深入了解食品化学有重要作用,学习者可以把它们掌握好,以便将来更好地应用到食品科学的研究中去。
食品化学必备知识点[参考]
![食品化学必备知识点[参考]](https://img.taocdn.com/s3/m/8f318f020166f5335a8102d276a20029bc646347.png)
食品化学必备知识点[参考]食品化学是利用其食品组成部分、水解物质及食用物质等,及其形成机理及合成反应,研究食品的可食用物质及物理化学性质,以及它们之间的关系的学科。
一、食物组成1.蛋白质:是植物及动物体中重要的组成部分,具有复杂的结构及各种功能,是构成食物的主要成分,其中包括氨基酸、多肽、免疫球蛋白、淀粉蛋白及微量元素等。
2.脂肪:是食物的主要成份之一,其组成以脂肪酸为主,也含有一定数量的维生素及色素。
3.碳水化合物:也就是普通意义上的糖(含有果糖、蔗糖等),也有维生素、钙、铁等含量较高的碳水化合物,来源主要有谷物、饼干、面包等等。
4.矿物质:也称作微量元素,是食物中的重要成份,如钠、钙、钾、铁等,它们对人体的健康很重要。
5.水:占人体总重的 60-70%,是最重要的成份之一,有一定的温度、酸度和胃口等特性,另外,水里还含有某些水溶性维生素,对于食品加工和食物质量都至关重要。
二、食物水解食物水解就是把食物中的碳水化合物、脂肪、蛋白质等,通过酶及其他物质将其分解后形成更小分子物质,比如乳糖、氨基酸、脂肪酸等,这些物质可以被身体吸收利用,是人体能量及养分的主要来源。
食物合成是指食物原料中的化学物质,通过合成反应形成新的物质,从而获得食物的新特性或功能,比如改变口感、保质期等,也可以增加剂量、迅速上市等特殊功能。
四、口感化学口感化学是一门以研究人的口感体验及各种味道为核心的学科,它研究食物中的口感特性,如质地、口感、香味等,及其调整食物口感的方法,还可以通过技术评估食品及原料味道及口感品质,从而确定食品及原料的品质及满意度。
五、膳食纤维膳食纤维又称作非消化性纤维,它不会被人体的酶分解,它们能传导饱足感以及维持肠道蠕动,由食物中植物性组成部分所构成,如蔬菜、水果等,其作用通常是当食物经过肠道时,膳食纤维会被水解发生反应,增加大肠中有益细菌的生长,同时也会降低吸收的油类、脂肪,有缓解血脂升高,降低患病风险。
食品化学必备知识点[参考]
![食品化学必备知识点[参考]](https://img.taocdn.com/s3/m/fb2ac536a7c30c22590102020740be1e650ecc3c.png)
食品化学必备知识点[参考]
1.营养学基础知识:包括碳水化合物、脂肪、蛋白质、维生素、矿物质、水的作用、摄入量等基础营养学知识。
2. 食品成分分析:包括食品成分分析的方法和相关技术,如气相色谱、液相色谱、质谱等分析方法。
3. 蛋白质的结构和功能:包括蛋白质的结构、种类、功能和在食品加工中的应用。
4. 脂质的结构和功能:包括脂质的结构、种类、功能和在食品加工中的应用。
5. 食品添加剂:包括食品添加剂的种类、作用、应用范围、安全性等方面的知识。
6. 食品营养强化:包括食品营养强化的原理、方法和在食品生产中的应用。
7. 食品储藏和保质期:包括食品在储藏和运输过程中的易变质因素、储藏方式、保质期等方面的知识。
8. 食品加工过程中的化学反应:包括掌握食品加工过程中在不同条件下发生的化学反应及其机理。
9. 食品安全:包括食品卫生、食品灾害和突发事件应对等方面的知识。
10. 食品质量控制:包括食品质量标准、抽样检测、质量改进等方面的知识。
食品化学知识点总结

引言概述:食品化学是研究食品的组成成分、结构、性质以及其在加工、贮藏、烹饪等过程中的变化规律的科学。
它不仅与我们的日常饮食密切相关,还关系到食品的质量、安全和营养价值。
本文将就食品化学的主要知识点进行总结,以丰富读者对食品化学的了解。
正文内容:一、食品的主要成分1. 碳水化合物:食品中最主要的能量供给来源,包括单糖、双糖和多糖。
2. 蛋白质:由氨基酸组成的高聚物,是身体建筑材料和许多生化反应的催化剂。
3. 脂肪:主要作为能量储存和细胞膜成分,分为饱和脂肪酸、不饱和脂肪酸和转化脂肪酸。
4. 维生素:对身体的正常生理和代谢具有重要作用,分为脂溶性和水溶性维生素。
5. 矿物质:在体内起着构成骨骼、维持神经传导等重要作用,如钙、铁、锌等。
二、食品加工与化学反应1. 热处理:包括烹调、炖煮、烘焙等,通过破坏细胞膜结构和酶的活性,改变食品的口感和风味。
2. 调味品的作用:含有多种化学物质,如氨基酸、核苷酸、酸味物质等,可以增强食品的风味和口感。
3. 食品防腐:使用化学物质(如抗菌剂、抗氧化剂)阻止食品腐败和变质,延长食品的保质期。
4. 食品着色剂:用于提高食品的色泽,如天然色素和合成色素等。
5. 食品营养强化:通过添加维生素、矿物质等物质,提高食品的营养价值。
三、食品贮藏和变质1. 微生物的作用:细菌、霉菌和酵母菌会导致食品的变质和腐败,引起食品中毒等食品安全问题。
2. 酸碱平衡:食品的pH值对细菌生长和食品稳定性有影响,过高或过低的pH值会导致食品变质。
3. 氧化反应:氧气引起食品中脂肪的氧化,导致食品发生质量变化,出现异味和变色。
4. 食品贮藏方式:低温贮藏可以延缓食品变质,真空包装和气调包装可以减少氧化反应。
四、食品加工中的化学反应1. 糖的糊化和焦化:在烘焙、炒菜过程中,糖类可以发生糊化和焦化反应,产生香味和颜色。
2. 蛋白质的应用:在食品加工中,蛋白质可以发生凝胶化、变性和交联等反应,改变食品的质地和稳定性。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
可结冰,可作溶剂,有利于化学反应的进行和微生物的生长
9、滞后现象
向干燥样品中添加水,所得到的吸附等温线与将水从样品中移出所得到的解吸等温线并不相互重叠,这种不重叠性称为滞后现象(hysteresis)。滞后作用的大小、滞后曲线的形状、滞后曲线的起始点和终止点取决于食品的性质、食品除去或添加水分时所发生的物理变化,以及温度、解吸速度和解吸时的脱水程度等多种因素。在Aw一定时食品的解吸过程一般比吸附过程水分含量更高。
低聚糖:碳原子数目:二糖(蔗糖,麦芽糖)
单糖分子是否相同:均低聚糖(麦芽糖,环糊精)、
杂低聚糖(蔗糖、棉籽糖)
功能性质:普通低聚糖(蔗糖、麦芽糖、环糊精。供热)
功能性低聚糖(低聚果糖,低聚木糖。促进肠道有益菌的生长,改善消化道菌群结构)
多糖:1.同聚多糖(淀粉、纤维素、糖原),杂聚多糖(半纤维素、卡拉胶、茶叶多糖)
图:马铃薯淀粉的水分活度和温度的克劳修斯-克拉贝龙关系
7、食品在冰点上下水分活度的比较:
①在冰点以上,食品的水分活度是食品组成和温度的函数,并且主要与食品的组成有关;而在冰点以下,水分活度仅与食品的温度有关。
②就食品而言,冰点以上和冰点以下的水分活度的意义不一样。如在-15℃、水分活度为0.80时微生物不会生长且化学反应缓慢,然而在20℃、水分活度为0.80时,化学反应快速进行且微生物能较快地生长。
2、食品化学的研究范畴
第二章水
3、在温差相等的情况下,为什么生物组织的冷冻速率比解冻速率更快?
4、净结构破坏效应:一些离子具有净结构破坏效应(net structure-breaking effect),如:K+、Rb+、Cs+、NH4+、Cl-、I-、Br-、NO3-、BrO3-、IO3-、ClO4-等。这些大的正离子和负离子能阻碍水形成网状结构,这类盐溶液的流动性比纯水更大。
21、黏度多糖(亲水胶体或胶)具有增稠和胶凝的功能,此外还能控制流体食品与饮料的流动性质、质构以及改变半固体食品的变形性等。在食品中,一般使用0.25%~0.5%浓度的胶即能产生极大的黏度甚至形成凝胶。
对于带一种电荷的直链多糖(一般是带负电荷,它由羧基、硫酸半酯基或磷酸基电离而得),由于同种电荷产生静电斥力,引起链伸展,使链长增加,高聚物体积增大,因而溶液的黏度大大增加。
③不能用食品在冰点以下的水分活度来预测食品在冰点以上的水分活度,同样也不能用食品冰点以上的水分活度来预测食品冰点以下的水分活度。
8、水分吸附等温线
在恒定温度下,用来联系食品中的水分含量(以每单位干物质中的含水量表示)与其水分活度的图,称为水分吸附等温线曲线(moisture sorption isotherm,MSI)。
高度支链的多糖分子比具有相同相对分子质量的直链多糖分子占有的体积小得多,多糖在食品中主要是产生黏稠性、结构或胶凝等作用,所以线性多糖一般是最实用的
22、凝胶在许多食品中,一些高聚物分子(如多糖或蛋白质),能形成海绵状的三维网状凝胶结构,典型的三维网状凝胶结构见图3-24。凝胶具有二重性,既具固体性质,也具液体性质。
RVP= p/p0=ERH/100
注意:1)RVP是样品的内在性质,而ERH是当样品中的水蒸气平衡时的大气性质;
2)仅当样品与环境达到平衡时,方程的关系才成立。
6、水分活度与温度的关系:
水分活度与温度的函数可用克劳修斯-克拉贝龙方程来表示:
dlnaw/d(1/T)=-ΔH/R
lnaw=-ΔH/RT+C
第三章碳水化合物
12、定义:碳水化合物从结构上定义为多羟基醛或多羟基酮及其聚合物及衍生物的总称。
13、食品中碳水化合物的分类及代表性物质
依据单糖组成数量,可分为:单糖(monosaccharide)、低聚糖(oligasaccharide)和多糖(polysaccharide)
单糖:碳原子数目:戊糖、己糖;官能团:葡萄糖、果糖
9、MSI图形形态
大多数食品的水分吸附等温线呈S型,而水果、糖制品、含有大量糖的其他可溶性小分子的咖啡提取物以及多聚物含量不高的食品的等温线为J型。
图:低水分含量范围食品的水分吸附等温线
Ⅰ区:Aw=0~0.25约0~0.07g水/g干物质
作用力:H2O—离子,H2O—偶极,配位键
属单分子层水(含水合离子内层水)
意义:
(1)测定什么样的水分含量能够抑制微生物的生长;
(2)预测食品的化学和物理稳定性与水分含量的关系;
(3)了解浓缩和干燥过程中样品脱水的难易程度与相对蒸气压(RVP)的关系;
(4)配制混合食品必须避免水分在配料之间的转移;
(5)对于要求脱水的产品的干燥过程、工艺、货架期和包装要求都有很重要的作用。
2、(植物、动物、微生物)多糖
3、(结构性,储藏性,功能性)多糖
14、旋光性:旋光性(optical activity)是指一种物质使平面偏振光的振动平面发生旋转的特性。所谓比旋光度是指浓度为1g/mL的糖溶液在其透光层为1dm时使偏振光旋转的角度。
15、甜度:甜味的强弱通常以蔗糖作为基准物,采用感官比较法进行评价,因此所得数据为一个相对值。一般规定10%的蔗糖水溶液在20℃的甜度为1.0,其他糖在相同条件下与之比较得出相应的甜度(又称比甜度)。
(2)淀粉糊化的三个阶段:
①可逆吸水阶段,水分进入淀粉颗粒的非晶质部分,体积略有膨胀,此时冷却干燥,可以复原,双折射现象不变;
②不可逆吸水阶段,随着温度的升高,水分进入淀粉微晶间隙,不可逆大量吸水,结晶“溶解”;
③无定形状形成阶段,淀粉糊化后继续加热则会使膨胀的淀粉粒继续分离支解,淀粉颗粒成为无定形的袋状,淀粉分子全部进入溶液,溶液的黏度继续增高。将新鲜的糊化淀粉浆脱水干燥可得易分散于凉水的无定形粉末,即“可溶性α-淀粉”。
图:支链淀粉分子的链状结构图:支链淀粉的结构
23、糊化
(1)定义
淀粉的糊化,指未受损的淀粉颗粒不溶于冷水,但可逆地吸着水并产生溶胀,淀粉颗粒的直径明显地增加,经过搅拌后淀粉-水体系再进行加热处理,随着温度的升高淀粉分子运动加剧,使淀粉分子间的氢键开始断裂,所裂解的氢键位置就可以同水分子产生氢键,淀粉颗粒的体积增大,失去晶态。由于水分子的穿透,以及更多、更长的淀粉分子分散而呈糊状,体系的黏度增加,双折射现象消失,最后得到半透明的黏稠体系。
此外,功能性低聚糖还是一种低甜度、低热量的糖类物质,能够降低血脂,防止龋齿,食用后不会升高血糖等功能,常见的功能性低聚糖有低聚果糖、低聚半乳糖、低聚木糖和低聚异麦芽糖等。
20、低聚木糖低聚木糖(xylo-oligosaccharide)是由2~7个木糖以β-(1→4)糖苷键连接而成的,是木糖的直链低聚糖,其中以二糖(图3-20)和三糖为主。低聚木糖不仅具有优良的稳定性,能在较宽的pH和温度范围内保持稳定,而且与其他低聚糖相比,低聚木糖最难消化吸收,对双歧杆菌的增殖效果最好,有抗龋齿性,是一种优良的功能性食品原料,广泛应用于各类食品中。
表3-5各种果葡糖浆的组成和比甜度
成分
F-42
F-55
F-90
果糖
42%
55%
90%
葡萄糖
52%
40%
9%
多糖
6%
4%
1%
比甜度
1
1.1~1.4
1.5~1.6
19、功能性低聚糖功能性低聚糖(functional oligosaccharide)是指对人体有显著生理功能,能够促进人体健康的低聚糖。与普通低聚糖相比,功能性低聚糖由2~7个单糖组成,在机体胃肠道内不被消化吸收而直接进入大肠优先被双歧杆菌所利用,是双歧杆菌的增殖因子。
21、直链淀粉
直链淀粉由D-葡萄糖以α-(1→4)糖苷键缩合而成,在水中并不是直线型分子,而是由分子内的氢键作用使链卷曲成螺旋状,每个回转含有6个葡萄糖残基,相对分子质量为105~106 Da。
图:直链淀粉的结构
22、支链淀粉
支链淀粉是高度分支的淀粉,葡萄糖残基通过α-(1→4)糖苷键连接构成主链,支链通过α-(1→6)糖苷键与主链相连,分支点的α-(1→6)糖苷键占总糖苷键的4%~5%。
17、低聚糖的结构(麦芽糖,蔗糖,乳糖)
18、果葡糖聚果葡糖浆又称高果糖浆(high fructose corn syrup),素有天然蜂蜜之称,以酶法糖化淀粉所得糖化液经葡萄糖异构酶作用,将部分葡萄糖异构成果糖,由葡萄糖和果糖组成的一种混合糖浆,因此又叫异构糖浆。根据混合糖浆中所含果糖的多少分为F-42、F-55、F-90三代产品,其质量与果糖含量成正比。、
图12:核桃仁的水分吸附等温线的滞后现象(25℃)
10、引起滞后现象的原因
1、解吸过程中一些吸水与非水溶液成分作用而无法释放。
2、样品中不规则形状产生的毛细管现象的部位,欲填满或抽空水分需要不同的蒸汽压(要抽出需要P内>P外,要填满即吸着时需P外>P内)。
3、解吸时,因组织改变,无法紧密结合水分,因此回吸相同水分含量时其水分活度较高
(3)影响淀粉糊化的因素
①淀粉晶体结构,淀粉分子间的结合程度、分子排列紧密程度、淀粉分子形成微晶区的大小等,影响淀粉分子的糊化难易程度。
净结构形成效应:另外一些离子具有净结构形成效应(net structure-forming effect),这些离子大多是电场强度大、离子半径小的离子或多价离子。它们有助于形成网状结构,因此这类离子的水溶液的流动性比纯水的小,如:Li+、Na+、Ca2+、Ba2+、Mg2+、Al3+、F-、OH-等。
表3-2一些常见单糖的比甜度
单糖
比甜度
单糖
比甜度
蔗糖
1.0
