如何快速准确书写共价化合物电子式
电子式的书写方法

一、原子:依据元素得原子最外层电子个数得多少,先用小黑点“•”(或“*”)等符号在元素符号上、下、左、右各表示出1个电子,多余得电子配对。
例如:二、简单离子:1、简单阳离子:简单阳离子由于在形成过程中已失去最外层电子,所以其电子式就就是其离子符号本身。
例如:Na+ K+ Mg2+ Ca2+ Ba2+ Al3+2、简单阴离子得电子式一般非金属原子在形成阴离子时,得到电子,使最外层达到稳定结构,这些电子都应画出,并将符号用“[]”括上,右上角标出所带得电荷数,电荷得表示方法同于离子符号。
例如,[:]H-、[:..:]..F-、[:..:]..S2-。
三、共价型单质分子:必须正确地表示出共用电子对数,并满足每个原子得稳定结构。
例如:四、共价化合物:共价化合物电子式得书写,基本与共价型单质分子相同,一般为正价者在前。
对于不同价态得元素得原子,一般将化合价绝对值大得写在中间,绝对值小得写在周边。
例如:五.复杂离子(例如NH4+、H3O+等、) 除应标出共用电子对、非共用电子对等外,还应加中括号,并在括号得右上方标出离子所带得电荷。
复杂得阴离子,都应标出电子对等,还应加中括号,并在括号得右上方标出离子所带得电荷。
例如:六、离子化合物:离子化合物电子式得书写,就是将阴阳离子(阳离子在前,阴离子在后、)拼在一起。
对于不同价态得离子,也按其绝对值,遵照“大值在中间、小值在周边”得原则书写。
例如:七、用电子式表示化合物得形成过程:1、共价化合物得形成过程示例:2、离子化合物得形成过程示例:练习1、原子得电子式:H Ne NaAl C O2、离子得电子式:Na+ Mg+ Fe2+F- S2-NH4+ OH-3、共价化合物得电子式H2 Cl2 N2H2O NH3 CH4H2O2 HClO CO2N2H4 PCl34、离子化合物得电子式NaCl MgCl2 Na2SNaOH Na2O2NH4Cl Mg3N2。
书写电子式方法大全

精心整理如何正确书写电子式对于电子式的书写和判断正误是高考试题中常涉及到的一个知识点,现将不同粒子的电子式的书写方法总结如下:1.原子的电子式①书写方法:首先写出其元素符号,再在元素符号周围用“·”或“×”标出它的最外层电子 ②例子:钠原子;镁原子;氟原子 2.离子的电子式 (1)简单阳离子的电子式(2) (3②例子:硫离子;氟离子(4)复杂的阴离子的电子式 (过氧根离子电子式)3②例子:氢气分子;氧气分子③技巧:可以根据非金属单质中各原子最外层都要达到8电子稳定结构(He 除外),来确定非金属单质中的共用电子对数。
4.化合物的电子式(1)离子化合物的电子式①书写方法:离子化合物的电子式由阴、阳离子的电子式组合而成,但相同的离子不能合并②例子:NaCl 的电子式为; K 2S 的电子式为,(不能写成) (2)共价化合物的电子式FF S ClNa + NaMg H O K + S 2– K + K 2+ S2– N H H H精心整理①书写方法:共价化合物的电子式由对应原子的电子式组成,并要表示出 两原子之间的共用电子对情况。
②例子:HCl 的电子式为;CO 2的电子式: ③技巧:一般共价化合物中各元素的化合价的绝对值就是该元素原子形成的 共用电子对数5.基团的电子式—CH 3——OH —CHO子式表示物质的形成过程(1)共价化合物的形成过程示例:(2)离子化合物的形成过程示例:原子离子【练习】书写下列粒子的电子式Na +H +Cl -S 2-OH N a HH C N 2N O 2 N a M C l g O (NH 4)2H l 4 C F C H4 ClH C O O。
人教版高三化学一轮复习快速准确书写共价化合物电子式

CO2
胡乱添加电子
HClO H Cl O 原子排布顺序错误
H2O2 H O
OH
氧原子间的共用 电子对数目错误
以HClO和H2O2为例,介绍快速准确 书写共价化合物电子式的方法。
第一步:排序
遵循两条原则:
①原子需要的共用电子对=8—最外层电子数(H除外)
②需要共用电子对多的原子排在中间或中心 需要共用电子对少的原子排在两端或四周 H/Cl/Br 仅需要一个共用电子,只能排周边
H O Cl
H O OH
以HClO和H2O2为例,介绍快速准确 书写共价化合物电子式的方法。
第二步:标共用电子对
利用结构式,用短线准确画出原子间的 共用电子对,先满足缺电子对少的原子, 再满足缺电子对多的原子。
H —O — Cl
H—O—O—H
以HClO和H2O2为例,介绍快速准确 书写共价化合物电子式的方法。
HNNH
HH
00
HH
谢谢观看!
第三步:标写未成键的电子数目
为防止漏写或多写未成键的电子,可在各原子的旁 边写出其数目。如未成键电子数为0,则表示该原子 最外层电子全部提供出来用于共用,无余下电子。
H —O — Cl
04 6
H—O—O—H
044 0
以HClO和H2O2为例,介绍快速准确 书写共价化合物电子式的方法。
第四步:写出正确电子式
需要共用电子对多的原子排在中间或中心需要共用电子对少的原子排在两端或四周hclbr仅需要一个共用电子只能排周边hoclhooh以hclo和h2o2为例介绍快速准确书写共价化合物电子式的方法
人教版 · 高三化学 · 一轮复习
快速准确书写共价化合物电子式
执教人:
如何正确书写电子式

如何正确书写电子式电子式:在元素符号周围,用“· ”或“×”表示原子最外层电子的图示。
书写原则:表示电子的“· ”或“×”尽量对称分占元素符号四周,一般为上下左右四方;单质或化合物中,未成键电子尽量成对对称存在,共用电子或得失电子,谁提供的,书写时应靠向谁。
1.原子的电子式①书写方法:首先写出其元素符号,再在元素符号周围用“· ”或“×”标出它的最外层电子②例子:钠原子 ;镁原子 ;氟原子 2.离子的电子式(1)简单阳离子的电子式①书写方法:用该阳离子的离子符号表示②例子:钠离子 Na + ;镁离子 Mg 2+ ;钡离子 Ba 2+(2)简单阴离子的电子式①书写方法:不但要标出最外层电子数,而且要用“[ ]”括起来,并在右上角标明离子所带的电荷②例子:硫离子;氟离子(3)原子团的电子式①书写方法:不仅要标出最外层电子数,而且要用“[ ]”括起来,并在右上角标明离子所带的电荷②例子:铵根离子 ;氢氧根离子3.单质分子的电子式①书写方法:对于以共价键作用结合成的非金属单质分子,他们的电子式由对应原子的电子式组合而成,但同时要表示出共用电子对数;而对其他(金属单质、稀有气体单质等)则一律用FN H H H H F S 2– Na Mg O – H原子的电子式表示②例子:氢气分子 ;氧气分子③技巧:可以根据非金属单质中各原子最外层都要达到8电子稳定结构(He 除外),来确定非金属单质中的共用电子对数4.化合物的电子式(1)离子化合物的电子式①书写方法:离子化合物的电子式由阴、阳离子的电子式组合而成,但相同的离子不能合并②例子:NaCl 的电子式为 ;K 2S 的电子式为 ,(不能写成) (2)共价化合物的电子式①书写方法:共价化合物的电子式由对应原子的电子式组成,并要表示出两原子之间的共用电子对情况 ②例子:HCl 的电子式为 ;CO 2的电子式: ③技巧:一般共价化合物中各元素的化合价的绝对值就是该元素原子形成的共用电子对数 5.用电子式表示物质的形成过程如:H 2的形成过程 +NaCl 的形成过程 +Cl Na + H H O O K + S 2– K + Cl H C O OK 2+ S2– H H H H Na Cl Cl Na + K S S2– K+ K +K2S的形成过程 2 +注意:①用“→”表示形成过程,不用“=”;②“→”左边是形成该物质的所有原子的电子式,相同的原子可以合并,“→”右边是该物质的电子式;③用电子式表示离子化合物的形成过程时,可以在原子之间用箭头表示电子得失的关系,也可以不表示。
电子式书写之诀窍

电子式书写之诀窍电子式是一种重要的化学用语,能清楚地表示出原子、离子、离子化合物和共价化合物的结构,是中学化学教学的重点,也是高考考纲中要求学生必须掌握的重要内容之一,已成为各类考试的热点。
电子式在表达形式上有严格的要求,学习时一定要掌握其书写诀窍。
一、明确物质类别,分类记忆书写规则1.原子的电子式直接在原子符号周围用小黑点“·”或“×”来表示原子的最外层电子。
如:2.离子的电子式⑴简单阳离子:离子符号即为电子式。
如:Na +、Mg 2+、Al 3+⑵复杂阳离子和阴离子:在原子符号周围用小黑点“·”或“×”来表示原子的最外层电子,并用方括号括起来,在方括号的右上角标明所带的电荷数。
如:3.化合物的电子式⑴共价化合物共价化合物是原子间通过共用电子对结合而形成的,书写时将共用电子对画在两原子之间。
每个原子的未成对电子和孤对电子也应画出,使每个原子周围的电子都达到稳定结构。
如:⑵离子化合物离子化合物是阴、阳离子通过离子键结合而形成的,书写时先根据离子电子式的书写方法,分别画出阳离子和阴离子的电子式,然后让阴、阳离子间隔排列,注意相同离子不能并合。
如:二、善于归纳总结,熟练掌握规律技巧1.同一个式子中同一元素原子的电子要用同一符号,都用“·”或“×”。
2.要注意共价化合物与离子化合物电子式的区别。
前者不加括号,不写表示电荷的符号,后者阴离子(复杂阳离子)加方括号,括号外写表示电荷的符号。
3.离子化合物中阴阳离子个数比不是1∶1时,要注意每一个离子都与带相反电荷的离子O N ClH直接相邻的事实。
如:4.不同元素的原子形成分子时,共用电子对的数目不同,一般原子的共用电子对数目=8—最外层电子数。
三、有备无患,储存记忆常见物质电子式1.离子化合物2.共价化合物(单质分子)3.特殊微粒CaC 2NH 4ClNH 3 CH 4 HClO CCl 4 OH —(氢氧根离子) —OH (羟基)。
高中化学考试注意事项及电子式书写技巧

高中化学考试注意事项及电子式书写技巧1 、排列顺序时,分清是“由大到小”还是“由小到大”,类似的:“由强到弱”、“由高到低”等等。
2 、书写化学方程式时,分清是“=”还是“⇌”,如一种盐水解方程式一定用“⇌”不能用“=”,其产物也不能标“↓”或“↑”,弱酸、弱碱的电离一定要用“⇌”不能用“=”。
多元弱酸电离、多元弱酸根离子水解:不能一步写成和或漏写可逆符号;3 、别忽视题干中“混合物”、“化合物”、“单质”等限制条件。
4 、有单位的要写单位,没有单位的就不要写了。
如“溶解度”单位是“ g ”,却不写出,“相对分子质量”、“相对原子质量”无单位,却加上“g ”或“g ·mol -1”。
摩尔质量有单位(g ·mol -1) 却不写单位,阿伏加德罗常数单位是“ mol -1”而未写,失分。
5 、要求写“名称”却写分子式或其他化学式,要求写分子式或结构式却写名称。
电子式、原子或离子结构示意图、结构简式、结构式不看清,张冠李戴。
要求写离子方程式而错写成化学方程式。
书写电子式时,共价化合物忘了未成对电子,离子化合物中的阴离子与原子团离子忘了加中括号;元素符号和元素名称、结构简式和分子式、化学方程式和结构简式不要混淆。
6 、所有的稀有气体都是单原子分子而误认为双原子分子。
7 、273 ℃与273K 不注意区分,是“标况”还是“非标况”,是“气态”还是“液态”“固态”不分清楚。
22.4L.mol-1的适用条件。
注意三氧化硫、乙烷、己烷、水等物质的状态。
区分液态氯化氢和盐酸,液氨和氨水,液氯和氯水。
8 、计算题中往往出现“将样品分为两等份” ( 或“从 1000mL 溶液中取出50mL ”) ,最后求的是“原样品中的有关的量”,你却只求了每份中的有关量。
9 、请注意选择题“正确的是”,“错误的是”两种不同要求。
请注意,做的正确,填卡时却完全填反了,要十分警惕这种情况发生。
10 、求“物质的质量”与“物质的物质的量”、求气体的“体积分数”与“质量分数”不看清楚,失分。
电子式的书写规则口诀

电子式的书写规则口诀
1.无论何种微粒,其电子式都是由原子为基本单位组成的,不能出现角码甚至系数。
2.组成各种微粒的各个原子的电子式,必须力求均匀、对称。
稳定的8电子结构通常表示为四对电子(一般为元素符号的上、下、左、右各一对电子)。
3.电子式只能用示表示由主族元素形成的物质,不能表示由过渡元素形成的物质。
电子式
在化学反应中,一般是原子的外层电子发生变化。
为了简便起见,化学中常在元素符号周围用黑点“.”和叉“×”来表示元素原子的最外层电子。
这种表示的物质的式子叫做电子式。
但是,中学所学习的经典的八隅体的电子式属于过时的理论,只能用于表示很少一部分由主族元素形成的物质,不能表示由过渡元素形成的物质,亦不能正确表示多种常见物质的结构。
高三化学 电子式的书写规则口诀

电子式的书写规则口诀定义:在化学反应中,一般是原子的最外层电子数目发生变化。
为了简便起见,化学中常在元素符号周围用小黑点“·”或小叉“×”来表示元素原子的最外层电子,相应的式子叫做电子式。
(1)原子的电子式:H·、Na·、(2)阳离子的电子式:不画出离子最外层电子数,元素右上角标出“n+”电荷字样:Na+、Al3+、Mg2+(3)阴离子的电子式:要画出最外层电子数,用“[ ]”括起来,右上角标出“n-”:、、(4)离子化合物的电子式:由阴、阳离子的电子式组成,相同离子不能合并:、(5)共价化合物的电子式:画出离子最外层电子数:、(6)用电子式表示物质形成的过程:氯化氢的形成过程:氯化镁的形成过程:结构式:共价键中的每一对共用电子用一根短线表示,未成键电子不写出,物质的电子式就变成了结构式。
例如:书写电子式的常见错误:漏写未参与成键的电子,如:化合物类型不清,漏写或多写“[]”及错写电荷数,如:书写不规范,错写共用电子对如:N2的电子式为:,不能写成:,更不能写成:或。
不考虑原子间的结合顺序如:HClO的电子式为,而非。
因氧原子需形成2对共用电子才能达到稳定结构,而H、Cl各需形成1对共用电子就能达到稳定结构。
不考虑原子最外层有几个电子均写成8电子结构如:的电子式为,而非,因中碳原子最外层应有6个电子(包括共用电子),而非8个电子。
不清楚A如型离子化合物中两个B是分开写还是写一块如:中均为-l 价,Br-、H-已达到稳定结构,应分开写;C原子得一个电子,最外层有5个电子,需形成三对共用电子才能达到稳定结构,不能分开写;氧原子得一个电子,最外层有7个电子,需形成一对共用电子才能达到稳定结构,也不能分开写。
它们的电子式分别为:。
共价型化合物电子式书写--苏榕凤

专题1 第三单元
电子式的书写
泉州培元中学 苏榕凤
分类
1、原子
阳离子
2、离子
阴离子
3、共价型分子
4、带电原子团
5、离子化合物
3、共价型分子电子式的书写:
物质 构成原子
H2
Cl2
H
Cl
原子最外层电子数
1
7
达稳定结构所需电子数 2
8
共用电子对数 电子式
1
1
··
H H :C····l:·C···l:
1、原子达稳定结构缺电子个数 = 所成共用电子对数
2、补齐8电子(H为2电子)
你学会了吗?
N2
5 3
N ······N
··N ······N··
CCl4
47 41
··C····l······CC·C······ll····团:
OH-
O22-
6 7
NH4+
‥‥ ‥‥ ‥
‥
[ ‥O H]-
‥‥
[ ‥O ‥O ]2-
H+
[H··HN······H]+ H
4、带电原子团:
原则:(1)用“[ ]”括起来,右上角标明离子所带的电荷 (2)计算共用电子对数,标出最外层电子数
5、离子化合物 阴、阳离子组成
书写原则:阴、阳离子的电子式组成,但相同离子不能合并
Na+ NaCl
Cl-
2Na+ Na2S
S2-
Na+
Na+
Na+
练习: 请书写下列物质的电子式。
H2S
(NH4)2S
共价化合物
离子化合物
电子式书写方法一览

电子式书写方法一览电子式是表示微粒最外层电子结构的化学式。
通常是在元素符号的周围,用小黑点·(或×)等符号表示元素的原子或离子的最外层电子个数。
用电子式可以表示原子、离子、单质分子,也可表示共价化合物、离子化合物及其形成过程。
书写电子式应该注意:1. 无论何种微粒,其电子式都是由原子为基本单位组成的,不能出现角码甚至系数。
2. 组成各种微粒的各个原子的电子式,必须力求均匀、对称。
稳定的8电子结构通常表示为四对电子(一般为元素符号的上、下、左、右各一对电子.)。
3. 电子式只能用来表示由主族元素形成的物质,不能表示由过渡元素形成的物质。
一. 原子:依据元素的原子最外层电子个数的多少,先用小黑点“•”(或“*”)等符号在元素符号上、下、左、右各表示出1个电子,多余的电子配对。
例如:二. 离子:1. 阳离子:简单阳离子由于在形成过程中已失去最外层电子,所以其电子式就是其离子符号本身。
例如:Na+K+Mg2+Ca2+Ba2+Al3+复杂的阳离子(例如NH4+、H3O+等.) 除应标出共用电子对、非共用电子对等外,还应加中括号,并在括号的右上方标出离子所带的电荷。
2. 阴离子:无论是简单阴离子,还是复杂的阴离子,都应标出电子对等,还应加中括号,并在括号的右上方标出离子所带的电荷。
例如:三. 共价型单质分子:必须正确地表示出共用电子对数,并满足每个原子的稳定结构。
例如:四. 共价化合物:共价化合物电子式的书写,基本与共价型单质分子相同,一般为正价者在前。
对于不同价态的元素的原子,一般将化合价绝对值大的写在中间,绝对值小的写在周边。
例如:五. 离子化合物:离子化合物电子式的书写,是将阴阳离子(阳离子在前,阴离子在后.)拼在一起。
对于不同价态的离子,也按其绝对值,遵照“大值在中间、小值在周边”的原则书写。
例如:六. 用电子式表示化合物的形成过程:1. 共价化合物的形成过程示例:2. 离子化合物的形成过程示例:电子式书写中的常见错误一、漏写没有参加成键的电子对Cl ClCl C Cl (正确)Cl C Cl (错误)N N (正确)NN(错误)Cl Cl二、漏写或多加[]及错写电荷数Na+(正确)[Na ]+(错误)H F (正确)H [ F ]-(错误)HNa+[ Cl ]-(正确)Na+Cl (错误)[ H N H ]+[ Cl ]-(正确)NH4+[ Cl ]-(错误)H三、漏标离子所带的电荷数或与化合价混淆[ Cl ]-Ca2+[ Cl ]-(正确)[ Cl ]Ca2+[ Cl ](错误)[ Cl ]-1Ca2+[ Cl ]-1(错误)Na+[ S ]2-Na+(正确)Na+[ S ]Na+(错误)Na+1[ S ]-2Na+1(错误)四、将相同离子错误合并[ Cl ]-Mg2+[ Cl ]-(正确)Mg2+[ Cl ]2-(错误)Na+[ S ]2-Na (正确)Na2+[ S ]2-(错误)五、电子式中微粒排列错误H O Cl (正确)H Cl O (错误)[ H O ]-Ca2+[ O H ]-(正确)[ O H ]Ca2+[ O H ](错误)Mg2+[ N ]3-Mg2+[ N ]3-Mg2+(正确)Mg2+Mg2+Mg2+[ N ]3-[ N ]3-(错误)六、电子(电子对)排列错误N N (正确)N N (错误)N N (错误)O C O (正确)O C O (错误)七、用电子式表示形成过程时错误化学方程式中的反应物与生成物之间用“=”连接,而不用“→”连接。
高考化学中常见的电子式大全
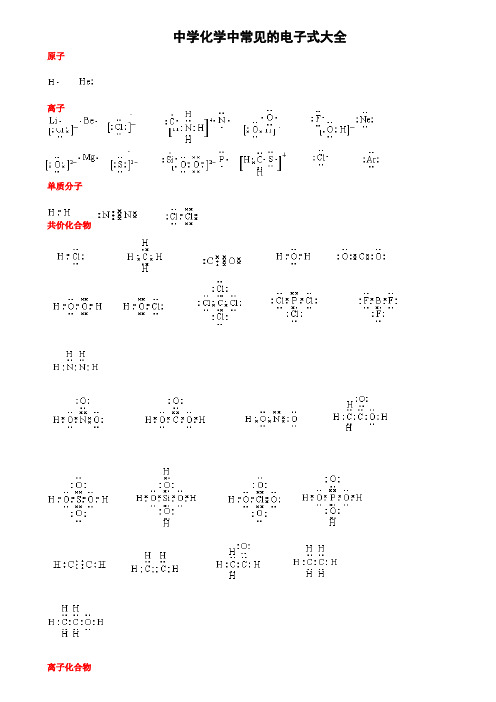
6.“基”中至少有一个原子是不符合8电子稳定结构,“基”是不显电性的,例如:-CH3、-OH。
三、注意微粒间的排列方式。
7.离子化合物多离子微粒阴阳离子交替排列。
8.共价化合物(有机物除外)多原子微粒正负价原子交替排列。
(4) 盐:氯化钠、氯化钙、硫化钠、氯化铵、硫化铵、甲酸钠、乙酸钠、次氯酸钠、次氯酸钙。
Na+[]-[]-Ca2+[]-Na+[]2-Na+
H H H
[]+[]-[]+[]2-[]+
H H H
H
[]-Na+[]-Na+
H
Na+[]-[]-Ca2+[]-
(5)类盐:电石、二氮化三镁。
Ca2+[]2-Mg2+[]3-Mg2+[]3-Mg2+
7.用电子式表示物质的形成过程
①离子化合物的形成过程
形成用“→”表示,形成之前为原子的电子式并用弯箭头表示电子得失,形成之后为离子化合物的电子式。例如,NaCl的形成过程为:
N2()CO()、
NO+()、
CN-()、
C22-()
CO2(电子式见前)NO2+、N3-、CNS-
SO
PO43-
掌握了微粒电子式的写法,就可以快速书写该微粒的结构式,也可以用电子式来表示微粒的形成过程。对于简单短周期元素的原子形成的微粒还可以依据其电子式推导其空间结构,
如BF3()中B原子上无孤对电子,此分子应为平
一般非金属原子在形成阴离子时,得到电子,使最外层达到稳定结构,这些电子都应画出,并将符号用“[]”括上,右上角标出所带的电荷数,电荷的表示方法同于离子符号。例如, 、 、 。
电子式的书写方法

知识就堤力量一. 原子:依据元素的原子最外层电子个数的多少,先用小黑点“ 下、左、右各表示出 1个电子,多余的电子配对。
例如: Na ** Mg *-Si *: P -- S - s Cl *: Ar s■n■■a a.二. 简单离子:1. 简单阳离子:简单阳离子由于在形成过程中已失去最外层电子,所以其电子式就是其离 子符号本身。
例如:Na + K + Mg 2+ Ca 2+ Ba 2+ Al 3+2.简单阴离子的电子式一般非金属原子在形成阴离子时,得到电子,使最外层达到稳定结构,这些 电子都应画出,并将符号用“ □”括上,右上角标出所带的电荷数,电荷的表示 方法同于离子符号。
例如,[H:]、[: F:]、[: S:]2。
三. 共价型单质分子:必须正确地表示出共用电子对数,并满足每个原子的稳定结构。
例如: =He=H = H: Cl : Cl =0::6:N :=N :■・ ■■ ・・・・ ・■四•共价化合物:共价化合物电子式的书写,基本与共价型单质分子相同,一般为正价者在前。
对于不同价 态的元素的原子,一般将化合价绝对值大的写在中间,绝对值小的写在周边。
例如:五. 复杂离子(例如NH4、H0等.)除应标出共用电子对、非共用电子对等外,还应加中括H[H-N=H J + [ H-O'II 广号,并在括号的右上方标出离子所带的电荷。
- -复杂的阴离子,都应标出电子对等,还应加中括号,并在括号的右上方标出离子所带的电 荷。
例如:[lOijir [ifi-oi]*- [ifiifi-fii]*'I IVH ■■■ ■■0*六. 离子化合物:离子化合物电子式的书写,是将阴阳离子(阳离子在前,阴离子在后.)拼在一起。
对于不同价态的离子,也按其绝对值,遵照“大值在中间、小值在周边”的原则书写。
例如:(或“ * ”)等符号在元素符号上、H■■"g:H HC="H印:H Ii=“H■・HHO:" 0=喰■ ■■■H9c»o»: :O-Na*[: CL:]'Ha +[:O:O :p-Ma 4知识就堤力量H・・"P「・・1H:K:H :€1:HCa2+[:O; O?]2- Ca1*■[: O:O :]3_Nlf-Na+Na+七.用电子式表示化合物的形成过程:1. 共价化合物的形成过程示例:H- + *C1:------------ H =C1 =■十--------------- ・3::c ::62H* 十-0 * -------------- * H = 5 = H2. 离子化合物的形成过程示例:Na^^-Cl^ --------------- -Na4" [ »Cl = ] ~z ca ci =——[f 】y尹[D丁» “ ■■ ・・K s K ——-K* [ ’ S =]Z_K*1、原子的电子式:H Ne NaAl C O2、离子的电子式:[Na4■[: N:]3-Na+Na+F- S2-Na+Mg +Fe2+知识就堤力量NH4+OH-3、共价化合物的电子式H2CI2N2出0NH3CH4 H2O2HClO CO2 N2H4PCI34、离子化合物的电子式NaCl MgCD Na2S NaOH Na?O2NH4CI Mg3N2Love is not a maybe thing. You know whe n you love some one.F- S2-。
(完整版)书写电子式方法大全

如何正确书写电子式对于电子式的书写和判断正误是高考试题中常涉及到的一个知识点,现将不同粒子的电子式的书写方法总结如下:1.原子的电子式①书写方法:首先写出其元素符号,再在元素符号周围用“· ”或“×”标出它的最外层电子②例子:钠原子;镁原子 ;氟原子 2.离子的电子式(1)简单阳离子的电子式 ①书写方法:用该阳离子的离子符号表示②例子:钠离子 Na + ;镁离子 Mg 2+ ;钡离子 Ba 2+(2)复杂的阳离子的电子式 ①书写方法:不仅要标出最外层电子数,而且要用“[ ]”括起来,并在右上角标明离子所带的电荷 ②例子:铵根离子电子式如下图(铵根离子电子式)(3)简单阴离子的电子式①书写方法:不但要标出最外层电子数,而且要用“[ ]”括起来,并在右上角标明离子所带的电荷②例子:硫离子 ;氟离子(4)复杂的阴离子的电子式 ①书写方法:不仅要标出最外层电子数,而且要用“[ ]”括起来,并在右上角标明离子所带的电荷 ②例子:过氧根离子和氢氧根离子的电子式分别如下图(过氧根离子电子式)(氢氧根离子电子式)3.单质分子的电子式①书写方法:对于以共价键作用结合成的非金属单质分子,他们的电子式由对应原子的电子式组合而成,但同时要表示出共用电子对数;而对其他(金属单质、稀有气体单质等)则一律用原子的电子式表示②例子:氢气分子 ;氧气分子③技巧:可以根据非金属单质中各原子最外层都要达到8电子稳定结构(He 除外),来确定非金属单质中的共用电子对数。
4.化合物的电子式(1)离子化合物的电子式FFS 2–Na Mg H H OON H H H H①书写方法:离子化合物的电子式由阴、阳离子的电子式组合而成,但相同的离子不能合并②例子:NaCl 的电子式为;K 2S的电子式为 ,(不能写成)(2)共价化合物的电子式①书写方法:共价化合物的电子式由对应原子的电子式组成,并要表示出两原子之间的共用电子对情况。
电子式的书写方法

一. 原子:依据元素的原子最外层电子个数的多少,先用小黑点“?”(或“*”)等符号在元素符号上、下、左、右各表示出1个电子,多余的电子配对。
例如: 二. 简单离子:1. 简单阳离子:简单阳离子由于在形成过程中已失去最外层电子,所以其电子式就是其离子符号本身。
例如: Na + K + Mg 2+ Ca 2+ Ba 2+ Al3+ 2.简单阴离子的电子式一般非金属原子在形成阴离子时,得到电子,使最外层达到稳定结构,这些电子都应画出,并将符号用“[]”括上,右上角标出所带的电荷数,电荷的表示方法同于离子符号。
例如,[:]H -、[:..:]..F -、[:..:]..S 2-。
三. 共价型单质分子:必须正确地表示出共用电子对数,并满足每个原子的稳定结构。
例如: 四. 共价化合物:共价化合物电子式的书写,基本与共价型单质分子相同,一般为正价者在前。
对于不同价态的元素的原子,一般将化合价绝对值大的写在中间,绝对值小的写在周边。
例如:五.复杂离子(例如NH 4+、H 3O +等.) 除应标出共用电子对、非共用电子对等外,还应加中括号,并在括号的右上方标出离子所带的电荷。
复杂的阴离子,都应标出电子对等,还应加中括号,并在括号的右上方标出离子所带的电荷。
例如:六. 离子化合物:离子化合物电子式的书写,是将阴阳离子(阳离子在前,阴离子在后.)拼在一起。
对于不同价态的离子,也按其绝对值,遵照“大值在中间、小值在周边”的原则书写。
例如: 七. 用电子式表示化合物的形成过程: 1. 共价化合物的形成过程示例: 2. 离子化合物的形成过程示例:练 习1、原子的电子式:H Ne Na Al C O2、离子的电子式:Na + Mg + Fe 2+ F - S 2- NH 4+ OH - 3、共价化合物的电子式H 2 Cl 2 N 2 H 2O NH 3 CH 4 H 2O 2 HClO CO 2 N 2H 4 PCl 3 4、离子化合物的电子式NaCl MgCl 2 Na 2SNaOH Na 2O 2 NH 4Cl Mg 3N 2。
(完整版)书写电子式方法大全

如何正确书写电子式对于电子式的书写和判断正误是高考试题中常涉及到的一个知识点,现将不同粒子的电子式的书写方法总结如下: 1.原子的电子式①书写方法:首先写出其元素符号,再在元素符号周围用“· ”或“×”标出它的最外层电子②例子:钠原子 ;镁原子 ;氟原子2.离子的电子式(1)简单阳离子的电子式①书写方法:用该阳离子的离子符号表示②例子:钠离子 Na + ;镁离子 Mg 2+ ;钡离子 Ba 2+(2)复杂的阳离子的电子式①书写方法:不仅要标出最外层电子数,而且要用“[ ]”括起来,并在右上角标明离子所带的电荷②例子:铵根离子电子式如下图 (铵根离子电子式)(3)简单阴离子的电子式①书写方法:不但要标出最外层电子数,而且要用“[ ]”括起来,并在右上角标明离子所带的电荷②例子:硫离子 ;氟离子 (4)复杂的阴离子的电子式①书写方法:不仅要标出最外层电子数,而且要用“[ ]”括起来,并在右上角标明离子所带的电荷②例子:过氧根离子和氢氧根离子的电子式分别如下图(过氧根离子电子式)(氢氧根离子电子式)3.单质分子的电子式①书写方法:对于以共价键作用结合成的非金属单质分子,他们的电子式由对应原子的电子式组合而成,但同时要表示出共用电子对数;而对其他(金属单质、稀有气体单质等)则一律用原子的电子式表示②例子:氢气分子 ;氧气分子③技巧:可以根据非金属单质中各原子最外层都要达到8电子稳定结构(He 除外),来确定非金属单质中的共用电子对数。
4.化合物的电子式F FS 2–Na Mg H H O ON H H H H(1)离子化合物的电子式①书写方法:离子化合物的电子式由阴、阳离子的电子式组合而成,但相同的离子不能合并②例子:NaCl 的电子式为;K 2S 的电子式为 ,(不能写成 )(2)共价化合物的电子式 ①书写方法:共价化合物的电子式由对应原子的电子式组成,并要表示出两原子之间的共用电子对情况。
高考化学中常见的电子式大全

5.用电子式表示物质的形成过程
如:H2的形成过程+
NaCl的形成过程+
K2S的形成过程2 +
注意:①用“→”表示形成过程,不用“=”;
②“→”左边是形成该物质的所有原子的电子式,相同的原子可以合并,“→”
右边是该物质的电子式;
2.金属阳离子的电子式
金属原子在形成阳离子时,最外层电子已经失去,但电子式仅画出最外层电子,所以在画阳离子的电子式时,就不再画出原最外层电子,但离子所带的电荷数应在元素符号右上角标出。所以金属阳离子的电子式即为离子符号。如钠离子的电子式为 ;镁离子的电子式为 ,氢离子也与它们类似,表示为 。
3.非金属阴离子的电子式
三、“等电子体”带动“家族”亮起来。
在2004年江苏省高考试题化学卷中给出了“等电子体”的概念并有以下引申(第二卷第22题):由短周期元素组成的微粒,只要其原子数相同,各原子最外层电子数之和相同,可互称为等电子体,它们也具有相似的结构特征。根据此定义我们可以从一种微粒的电子式推导出上述概念范围内的等电子体的电子式。如:
这条规律几乎适用于所有的离子化合物,运用时要求大家首先能正确判断化学式含有的微粒种类和它们所带的电荷的正负。如MgCl2由Mg2+和Cl-以1:2的比例构成,Na2O2由Na+和O22-以2:1的比例构成。而对于共价微粒、只有少数氧化性(电负性)相差很小的非金属原子形成的共价体有例外,例如HCN(其中C为+4价、N为-3价,电子式为)。高中阶段涉及的常见共价微粒(由短周期元素原子形成的共价微粒)的电子式基本都可以采用该规律来解决。
(2)氧化物:Na2O、Na2O2、MgO、Al2O3。
高中化学中电子式的书写方法

电子式的书写方法在元素符号周围用“·”和“×”来表示原子的最外层电子(价电子),这种式子叫做电子式。
1. 原子的电子式由于中性原子既没有得电子,也没有失电子,所以书写电子式时应把原子的最外层电子全部排列在元素符号周围。
排列方式为在元素符号上、下、左、右四个方向,每个方向不能超过2个电子。
2. 金属阳离子的电子式金属原子在形成阳离子时,最外层电子已经失去,但电子式仅画出最外层电子,所以在画阳离子的电子式时,就不再画出原最外层电子,但离子所带的电荷数应在元素符号右上角标出。
所以金属阳离子的电子式即为离子符号。
3. 非金属阴离子的电子式一般非金属原子在形成阴离子时,得到电子,使最外层达到稳定结构,这些电子都应画出,并将符号用“[]”括上,右上角标出所带的电荷数,电荷的表示方法同于离子符号。
4. 共价化合物的电子式共价化合物是原子间通过共用电子对结合而成的。
书写时将共用电子对画在两原子之间,每个原子的未成对电子和孤对电子也应画出。
因不同元素原子吸引电子能力不同,则共用电子对偏向吸引电子能力强的原子,而偏离吸引电子能力弱的原子。
5. 根离子的电子式根离子中,若不同原子间以共价键结合,画法同共价化合物,因根离子带有电荷,所以应把符号用“[]”括起来,右上角标出电荷数。
6. 离子化合物的电子式先根据离子电子式的书写方法,分别画出阴、阳离子的电子式,然后让阴、阳离子间隔排列,注意相同离子不能合并。
①离子化合物的形成过程形成用“→”表示,形成之前为原子的电子式并用弯箭头表示电子得失,形成之后为离子化合物的电子式。
②共价化合物或非金属单质的形成过程表示方法基本同离子化合物相同,不同的是因没有电子得失,所以不要再画弯箭头,并且“→”之后为共价化合物或非金属单质的电子式。
电子式书写中应该注意的几个问题

电子式书写中应该注意的几个问题电子式是重要的化学用语,能清楚地表示出原子、离子、离子化合物和共价化合物的结构和形成,要能正确地掌握和应用,书写时必须注意以下问题。
1. 用电子式表示离子化合物的形成的注意点(1)左边写出形成离子化合物中各原子的电子式,右边写出生成的离子化合物的电子式,中间用“→”连接,而不是“=”。
(2)用电子式表示离子化合物的结构时,对于阳离子来说,一般用阳离子符号表示,如等;而阴离子则不同,应在元素符号的周围用小黑点(·)或小叉(×)表示最外层电子数,外面加上中括号([ ]),并在中括号的右上角标上离子所带的负电荷数,如。
(3)构成离子化合物的每一个离子都要单独书写,不可合并,书写原子的电子式时,若有几个相同的原子,可合并书写。
如:2. 用电子式表示共价化合物的形成的注意点(1)左边书写出形成共价化合物的原子的电子式,相同可以合并,右边写出生成的共价化合物的电子式,相同原子不可合并,中间用“”连接。
(2)不同元素的原子形成分子时,共用电子对的数目不同,原子最外层电子数目离稳定结构差几个电子,一般要共用几对电子。
(3)共价化合物的电子式中,要注意使每个原子周围的电子数均达到稳定结构。
(4)由于共价化合物中没有阴、阳离子,所以用电子式表示共价化合物的结构时,不使用中括号,也不标电荷数。
如:3. 电子式书写中的常见错误(1)漏写未参加成键的电子对。
如:(2)离子错误合并。
如:(3)错写分子中原子间的结合方式。
如:中是O与H和Cl成键,应写为。
(4)离子化合物、共价化合物不分,乱用或丢掉中括号。
如:(5)不遵循成键规律,胡乱添加电子。
如:4. 例题解析例1. 下列化合物的电子式书写正确的是()A. 氨气:B. 四氯化碳:C. 甲烷:D. 二氧化碳:解析:A项中N的最外层电子没有全部标出;B项中Cl的最外层电子也没有全部标出;D项中C、O共用电子对数目标错。
故选C项。
快速电子式书写的技巧

快速书写电子式的技巧陕西省陇县中学721200 魏芳年电子式是在元素符号周围用“×”或“.”来表示原子的最外层电子(价电子)的式子。
它能真实的反映出原子得失电子的能力,体现出元素的金属性和元素的非金属性,单质的氧化性和还原性等。
这一部分既是教学的重点也是学生学习的难点。
对此,现将教学中的尝试归纳如下:一:原子电子书的书写对主族元素而言,一般规律为族序数为几标几。
如:×M g×二:离子电子式的书写1:阳离子电子式的书写(1)简单阳离子电子式的书写:其实为其离子符号,也可以理解为:族序数为几标几正。
如:Mg2+(2)复杂阳离子电子式书写:一般是由非金属间组成的,逢氢原子补齐2,其余补齐8,用中括号括起来,并在其右上角标几正(失去的电子数)。
如:2:阴离子电子式的书写(1)简单阴离子电子式的书写:一般规律为族序数距8缺几补几标几负。
如:(2)复杂阴离子电子式的书写:一般是由非金属间组成的,逢氢原子补齐2,其余补齐8,用中括号括起来,并在其右上角标几负(得到或共用的电子数)。
如:三:物质电子式的书写1:离子化合物电子式的书写:一般可以看作是阴阳离子电子式的简单组合(注意相同离子不能合并写,一般写在对称位置上)。
如:2:含共价键的物质电子式的书写:一般是由非金属间组成的,逢氢原子补齐2,其余补齐8(1)共价单质电子式的书写:一般是由非金属间组成的,逢氢原子补齐2,其余补齐8,如:(2)共价化合物电子式的书写:应注意符号其空间构型a:氢化物电子式的书写:第四主族元素的氢化物:空间构型:正四面体,电子式为:第五主族元素的氢化物:空间构型:三角锥型,电子式为:第六主族元素的氢化物:空间构型:v字型,电子式为:第七主族元素的氢化物:空间构型:直线型,电子式为:b:氧化物或硫化物电子式的书写:二氧化碳二硫化碳过氧化氢C:次卤酸的电子式:次氯酸:四:物质形成过程的电子式的书写左边为原子的电子式(相同原子的电子式可以合并写),右边为物质的电子式,用单箭斗相连。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
如何快速准确书写
共价化合物电子式
共价化合物中各成键原子间通过共用电子对相结合。
根据共
价键的“饱和性”和电子式的书写规则,按照“一摆”、“二画”、
“三补齐”的方法,可以快速准确地书写共价化合物的电子式。
一摆:就是摆正共价化合物中各成键原子的相对位置。
根据
共价键的饱和性,以共价键结合的原子,缺几个电子达到稳定结
构,就可以和其它原子形成几对共用电子对。
为此,在书写共价
化合物电子式时,把达到稳定结构缺电子多的原子摆在“中间”,
缺电子少的原子摆在“两边”或周围。
例如在确定HClO分子中各原子摆放位置时,根据共价键“饱
和性”, H、Cl各缺一个电子达到稳定结构,可与其它原子形成一
对共用电子对;O缺两个电子达到稳定结构,它可与其它原子形成
两对共用电子对,故HClO分子电子式中三种原子位置为H O
Cl 。
二画:画成键原子间共用电子对。
首先从成键时缺电子少的
原子画起,然后再考虑成键时缺电子多的原子。
例如:H2O2分子根据“一摆” H O O H 根据“二画”H :O O :H
H :O :O :H
三补齐:把成键各原子最外层未参与形成共用电子对的电子
补出来。
O O
::
例如:CH2O分子根据“一摆”H C H 根据“二画” H :C:H
:0:
::
根据“三补齐” H :C :H
按照“一摆”、“二画”、“三补齐”的方法,能够思路清晰地
书写共价化合物的电子式,不仅快速,而且准确,同学们不妨一
试。
河南省偃师六高魏振超。
