常见的电子式书写
电子式的书写方法

一、原子:依据元素得原子最外层电子个数得多少,先用小黑点“•”(或“*”)等符号在元素符号上、下、左、右各表示出1个电子,多余得电子配对。
例如:二、简单离子:1、简单阳离子:简单阳离子由于在形成过程中已失去最外层电子,所以其电子式就就是其离子符号本身。
例如:Na+ K+ Mg2+ Ca2+ Ba2+ Al3+2、简单阴离子得电子式一般非金属原子在形成阴离子时,得到电子,使最外层达到稳定结构,这些电子都应画出,并将符号用“[]”括上,右上角标出所带得电荷数,电荷得表示方法同于离子符号。
例如,[:]H-、[:..:]..F-、[:..:]..S2-。
三、共价型单质分子:必须正确地表示出共用电子对数,并满足每个原子得稳定结构。
例如:四、共价化合物:共价化合物电子式得书写,基本与共价型单质分子相同,一般为正价者在前。
对于不同价态得元素得原子,一般将化合价绝对值大得写在中间,绝对值小得写在周边。
例如:五.复杂离子(例如NH4+、H3O+等、) 除应标出共用电子对、非共用电子对等外,还应加中括号,并在括号得右上方标出离子所带得电荷。
复杂得阴离子,都应标出电子对等,还应加中括号,并在括号得右上方标出离子所带得电荷。
例如:六、离子化合物:离子化合物电子式得书写,就是将阴阳离子(阳离子在前,阴离子在后、)拼在一起。
对于不同价态得离子,也按其绝对值,遵照“大值在中间、小值在周边”得原则书写。
例如:七、用电子式表示化合物得形成过程:1、共价化合物得形成过程示例:2、离子化合物得形成过程示例:练习1、原子得电子式:H Ne NaAl C O2、离子得电子式:Na+ Mg+ Fe2+F- S2-NH4+ OH-3、共价化合物得电子式H2 Cl2 N2H2O NH3 CH4H2O2 HClO CO2N2H4 PCl34、离子化合物得电子式NaCl MgCl2 Na2SNaOH Na2O2NH4Cl Mg3N2。
书写电子式方法大全

精心整理如何正确书写电子式对于电子式的书写和判断正误是高考试题中常涉及到的一个知识点,现将不同粒子的电子式的书写方法总结如下:1.原子的电子式①书写方法:首先写出其元素符号,再在元素符号周围用“·”或“×”标出它的最外层电子 ②例子:钠原子;镁原子;氟原子 2.离子的电子式 (1)简单阳离子的电子式(2) (3②例子:硫离子;氟离子(4)复杂的阴离子的电子式 (过氧根离子电子式)3②例子:氢气分子;氧气分子③技巧:可以根据非金属单质中各原子最外层都要达到8电子稳定结构(He 除外),来确定非金属单质中的共用电子对数。
4.化合物的电子式(1)离子化合物的电子式①书写方法:离子化合物的电子式由阴、阳离子的电子式组合而成,但相同的离子不能合并②例子:NaCl 的电子式为; K 2S 的电子式为,(不能写成) (2)共价化合物的电子式FF S ClNa + NaMg H O K + S 2– K + K 2+ S2– N H H H精心整理①书写方法:共价化合物的电子式由对应原子的电子式组成,并要表示出 两原子之间的共用电子对情况。
②例子:HCl 的电子式为;CO 2的电子式: ③技巧:一般共价化合物中各元素的化合价的绝对值就是该元素原子形成的 共用电子对数5.基团的电子式—CH 3——OH —CHO子式表示物质的形成过程(1)共价化合物的形成过程示例:(2)离子化合物的形成过程示例:原子离子【练习】书写下列粒子的电子式Na +H +Cl -S 2-OH N a HH C N 2N O 2 N a M C l g O (NH 4)2H l 4 C F C H4 ClH C O O。
电子式的书写

3、电子式
概念:在元素符号周围用“”或“”来表示原子最外层电子的式子。
(1)原子电子式的书写:一般将原子的最外层电子写在元素符号的上、下、左、右四个位置上,先单后双。
氢原子
钠原子钙原子氧原子
(2)简单阳离子的电子式即为离子符号。
钠离子镁离子钙离子
(3)复杂阳离子的电子式要在元素符号周围标出电子,用括上,括号外标明电性及电量。
铵根离子
(4)阴离子的电子式要在元素符号周围标出电子,用括上,括号外标明电性及电量。
氯离子氧离子
氢氧根离子过氧根离子
(5)离子化合物电子式的书写:由阳离子和阴离子电子式组成,同性不相邻,相同离子不能合并。
氯化钠氯化钙
氯化铵氧化钠
(6)用电子式表示离子化合物的形成过程:电子转移方向用弧形箭头表示,变化过程用“”,箭头左边是原子,相同原子能合并。
氯化钠的形成
氯化镁的形成。
如何正确书写电子式

如何正确书写电子式电子式:在元素符号周围,用“· ”或“×”表示原子最外层电子的图示。
书写原则:表示电子的“· ”或“×”尽量对称分占元素符号四周,一般为上下左右四方;单质或化合物中,未成键电子尽量成对对称存在,共用电子或得失电子,谁提供的,书写时应靠向谁。
1.原子的电子式①书写方法:首先写出其元素符号,再在元素符号周围用“· ”或“×”标出它的最外层电子②例子:钠原子 ;镁原子 ;氟原子 2.离子的电子式(1)简单阳离子的电子式①书写方法:用该阳离子的离子符号表示②例子:钠离子 Na + ;镁离子 Mg 2+ ;钡离子 Ba 2+(2)简单阴离子的电子式①书写方法:不但要标出最外层电子数,而且要用“[ ]”括起来,并在右上角标明离子所带的电荷②例子:硫离子;氟离子(3)原子团的电子式①书写方法:不仅要标出最外层电子数,而且要用“[ ]”括起来,并在右上角标明离子所带的电荷②例子:铵根离子 ;氢氧根离子3.单质分子的电子式①书写方法:对于以共价键作用结合成的非金属单质分子,他们的电子式由对应原子的电子式组合而成,但同时要表示出共用电子对数;而对其他(金属单质、稀有气体单质等)则一律用FN H H H H F S 2– Na Mg O – H原子的电子式表示②例子:氢气分子 ;氧气分子③技巧:可以根据非金属单质中各原子最外层都要达到8电子稳定结构(He 除外),来确定非金属单质中的共用电子对数4.化合物的电子式(1)离子化合物的电子式①书写方法:离子化合物的电子式由阴、阳离子的电子式组合而成,但相同的离子不能合并②例子:NaCl 的电子式为 ;K 2S 的电子式为 ,(不能写成) (2)共价化合物的电子式①书写方法:共价化合物的电子式由对应原子的电子式组成,并要表示出两原子之间的共用电子对情况 ②例子:HCl 的电子式为 ;CO 2的电子式: ③技巧:一般共价化合物中各元素的化合价的绝对值就是该元素原子形成的共用电子对数 5.用电子式表示物质的形成过程如:H 2的形成过程 +NaCl 的形成过程 +Cl Na + H H O O K + S 2– K + Cl H C O OK 2+ S2– H H H H Na Cl Cl Na + K S S2– K+ K +K2S的形成过程 2 +注意:①用“→”表示形成过程,不用“=”;②“→”左边是形成该物质的所有原子的电子式,相同的原子可以合并,“→”右边是该物质的电子式;③用电子式表示离子化合物的形成过程时,可以在原子之间用箭头表示电子得失的关系,也可以不表示。
电子式书写

构成原子的电子式→物质的电子式
H2 I2
H ·+ ·H → · · · · :I · + · I: → · · · ·
H H · · · · : I :I : · ·· ·
· ·
单质
共价化合物
HF
H
×
+
F
→
H F
×O × H
×
H2O
H ×+ O + ×H → H
离子化合物
Na2O: ?
MgCl2: ?
用电子式书写时的注意事项:
(1)要弄清该物质是通过离子键形成离子化合物,还
是用共价键形成共价化合物或单质,然后 才能按照各自的方法来书写电子式。
(2)书写离子化合物时要注意二标:标
正负电荷;阴离子标[ ]。 标正负电荷时,还要特别注意正负电荷总数相等。 ▲共价化合物书写时不标[ ]及电荷。
三、用电子式表示简单物质形成过程
试写出氧气,氮气的电子式
· ·
3、化合物电子式的书写:
(1)离子化合物:
由阴、阳离子的电子式组成,但相同离 子不能合并。 AB型
A2B型 AB2型
如:H2S为 H ﹕S ﹕H H NH3为 H ﹕N ﹕ H
﹕ ﹕
试写出氢氧化钠、过氧化钠、氯化铵、过氧 化氢的电子式
﹕ ﹕
(2)共价化合物。 根据原子最外层电子数判断共用电子对数, 画好共用电子后再补充所有原子的最外层 电子
小结
电子式
一、定义: 二、书写: 原子、离子电子式的书写; 单质、离子化合物、共价化合物电子式 的的书写。 三、用电子式表示简单物质的形成过程
· · · ·
· ·
★氢分子的形成:
H﹣Cl(结构式)
中学化学中常见的电子式大全

中学化学中常见的电子式大全原子离子单质分子共价化合物离子化合物形成过程常见的20种电子式N 2N N O 2 O O Cl 2 Cl Cl H 2O H O H H 2O 2H O O HCO 2 O C O HclO H O Cl NH 3H N H H PCl 3 Cl P Cl Cl CH 4H H C H H CCl 4 Cl C Cl Cl Cl NaOH O H 〔 〕-Na + Na 2O 2 O O Na + 2-Na + MgCl 2 -Mg 2+ -NH 4Cl+ - CaC 2 Ca 2+ 2- ClCl H H N H H Cl C C-CH 3 —OH如何正确书写电子式(李运强 湖北省大悟县第一中学高一化学组 432800)对于电子式的书写和判断正误是高考试题中常涉及到的一个知识点,现将不同粒子的电子式的书写方法总结如下:1.原子的电子式①书写方法:首先写出其元素符号,再在元素符号周围用“· ”或“×”标出它的最外层电子②例子:钠原子 ;镁原子 ;氟原子2.离子的电子式(1)简单阳离子的电子式①书写方法:用该阳离子的离子符号表示②例子:钠离子 Na + ;镁离子 Mg 2+ ;钡离子 Ba 2+(2)简单阴离子的电子式①书写方法:不但要标出最外层电子数,而且要用“[ ]”括起来,并在右上角标明离子所带的电荷 ②例子:硫离子 ;氟离子 (3)原子团的电子式 ①书写方法:不仅要标出最外层电子数,而且要用“[ ]”括起来,并在右上角标明离子所带的电荷②例子:铵根离子 ;氢氧根离子 3.单质分子的电子式①书写方法:对于以共价键作用结合成的非金属单质分子,他们的电子式由对应原子的电子式组合而成,但同时要表示出共用电子对数;而对其他(金属单质、稀有气体单质等)则一律用原子的电子式表示②例子:氢气分子 ;氧气分子③技巧:可以根据非金属单质中各原子最外层都要达到8电子稳定结构(He 除外),来确定非金属单质中的共用电子对数4.化合物的电子式(1)离子化合物的电子式①书写方法:离子化合物的电子式由阴、阳离子的电子式组合而成,但相同的离子不能合并②例子:NaCl 的电子式为 ;K 2S 的电子式为 ,(不能写成 ) (2)共价化合物的电子式①书写方法:共价化合物的电子式由对应原子的电子式组成,并要表示出两原子之间的共用电子对情况②例子:HCl 的电子式为;CO 2的电子式: ③技巧:一般共价化合物中各元素的化合价的绝对值就是该元素原子形成的共用电子对数5.用电子式表示物质的形成过程如:H 2的形成过程 +NaCl 的形成过程 + HH C H HO F N H HH H F S2– Cl Na + Na Mg H H O OK + S 2– K + Cl H C O O K 2+ S2– O – H H HH H Na Cl Cl Na +K 2S 的形成过程 2 +注意:①用“ → ”表示形成过程,不用“=”;②“ → ”左边是形成该物质的所有原子的电子式,相同的原子可以合并,“ → ”右边是该物质的电子式;③用电子式表示离子化合物的形成过程时,可以在原子之间用箭头表示电子得失的关系,也可以不表示。
(完整版)中学化学中常见的电子式大全(1)
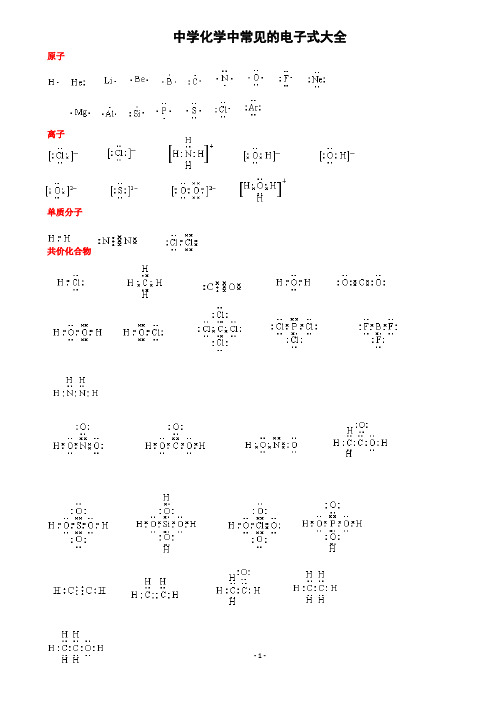
中学化学中常见的电子式大全原子离子单质分子共价化合物离子化合物形成过程常见的20种电子式N 2N NO 2 O O Cl 2 Cl Cl H 2O H O H H 2O 2H O O H CO 2 O C O HclO H O ClNH 3 H N H H PCl 3 Cl P Cl Cl CH 4H H C H H CCl 4 Cl C Cl Cl ClNaOH O H 〔 〕-Na + Na 2O 2 O O Na + 2-Na + MgCl 2 -Mg 2+ -Cl H N HHNH 4Cl+ - CaC 2 Ca 2+ 2- -CH 3 —OH如何正确书写电子式(李运强 湖北省大悟县第一中学高一化学组 432800)对于电子式的书写和判断正误是高考试题中常涉及到的一个知识点,现将不同粒子的电子式的书写方法总结如下:1.原子的电子式①书写方法:首先写出其元素符号,再在元素符号周围用“· ”或“×”标出它的最外层电子②例子:钠原子 ;镁原子 ;氟原子2.离子的电子式(1)简单阳离子的电子式①书写方法:用该阳离子的离子符号表示②例子:钠离子 Na + ;镁离子 Mg 2+ ;钡离子 Ba 2+(2)简单阴离子的电子式①书写方法:不但要标出最外层电子数,而且要用“[ ]”括起来,并在右上角标明离子所带的电荷 ②例子:硫离子 ;氟离子 (3)原子团的电子式①书写方法:不仅要标出最外层电子数,而且要用“[ ]”括起来,并在右上角标明离子所带的电荷②例子:铵根离子 ;氢氧根离子 3.单质分子的电子式①书写方法:对于以共价键作用结合成的非金属单质分子,他们的电子式由对应原子的电子式组合而成,但同时要表示出共用电子对数;而对其他(金属单质、稀有气体单质等)则一律用原子的电子式表示②例子:氢气分子 ;氧气分子③技巧:可以根据非金属单质中各原子最外层都要达到8电子稳定结构(He 除外),来确定非金属单质中的共用电子对数4.化合物的电子式(1)离子化合物的电子式①书写方法:离子化合物的电子式由阴、阳离子的电子式组合而成,但相同的离子不能合并②例子:NaCl 的电子式为 ;K 2S 的电子式为 ,(不能写成 )(2)共价化合物的电子式①书写方法:共价化合物的电子式由对应原子的电子式组成,并要表示出两原子之间的共用电子对情况ClCl C C HH C H HO F N H H H H FS 2– Cl Na + Na Mg H H O OK + S 2– K + K 2+ S 2– O – H②例子:HCl 的电子式为 ;CO 2的电子式: ③技巧:一般共价化合物中各元素的化合价的绝对值就是该元素原子形成的共用电子对数5.用电子式表示物质的形成过程如:H 2的形成过程 + NaCl 的形成过程 + K 2S 的形成过程 2 +注意:①用“ → ”表示形成过程,不用“=”;②“ → ”左边是形成该物质的所有原子的电子式,相同的原子可以合并,“ → ”右边是该物质的电子式;③用电子式表示离子化合物的形成过程时,可以在原子之间用箭头表示电子得失的关系,也可以不表示。
电子式的书写方法

知识就堤力量一. 原子:依据元素的原子最外层电子个数的多少,先用小黑点“ 下、左、右各表示出 1个电子,多余的电子配对。
例如: Na ** Mg *-Si *: P -- S - s Cl *: Ar s■n■■a a.二. 简单离子:1. 简单阳离子:简单阳离子由于在形成过程中已失去最外层电子,所以其电子式就是其离 子符号本身。
例如:Na + K + Mg 2+ Ca 2+ Ba 2+ Al 3+2.简单阴离子的电子式一般非金属原子在形成阴离子时,得到电子,使最外层达到稳定结构,这些 电子都应画出,并将符号用“ □”括上,右上角标出所带的电荷数,电荷的表示 方法同于离子符号。
例如,[H:]、[: F:]、[: S:]2。
三. 共价型单质分子:必须正确地表示出共用电子对数,并满足每个原子的稳定结构。
例如: =He=H = H: Cl : Cl =0::6:N :=N :■・ ■■ ・・・・ ・■四•共价化合物:共价化合物电子式的书写,基本与共价型单质分子相同,一般为正价者在前。
对于不同价 态的元素的原子,一般将化合价绝对值大的写在中间,绝对值小的写在周边。
例如:五. 复杂离子(例如NH4、H0等.)除应标出共用电子对、非共用电子对等外,还应加中括H[H-N=H J + [ H-O'II 广号,并在括号的右上方标出离子所带的电荷。
- -复杂的阴离子,都应标出电子对等,还应加中括号,并在括号的右上方标出离子所带的电 荷。
例如:[lOijir [ifi-oi]*- [ifiifi-fii]*'I IVH ■■■ ■■0*六. 离子化合物:离子化合物电子式的书写,是将阴阳离子(阳离子在前,阴离子在后.)拼在一起。
对于不同价态的离子,也按其绝对值,遵照“大值在中间、小值在周边”的原则书写。
例如:(或“ * ”)等符号在元素符号上、H■■"g:H HC="H印:H Ii=“H■・HHO:" 0=喰■ ■■■H9c»o»: :O-Na*[: CL:]'Ha +[:O:O :p-Ma 4知识就堤力量H・・"P「・・1H:K:H :€1:HCa2+[:O; O?]2- Ca1*■[: O:O :]3_Nlf-Na+Na+七.用电子式表示化合物的形成过程:1. 共价化合物的形成过程示例:H- + *C1:------------ H =C1 =■十--------------- ・3::c ::62H* 十-0 * -------------- * H = 5 = H2. 离子化合物的形成过程示例:Na^^-Cl^ --------------- -Na4" [ »Cl = ] ~z ca ci =——[f 】y尹[D丁» “ ■■ ・・K s K ——-K* [ ’ S =]Z_K*1、原子的电子式:H Ne NaAl C O2、离子的电子式:[Na4■[: N:]3-Na+Na+F- S2-Na+Mg +Fe2+知识就堤力量NH4+OH-3、共价化合物的电子式H2CI2N2出0NH3CH4 H2O2HClO CO2 N2H4PCI34、离子化合物的电子式NaCl MgCD Na2S NaOH Na?O2NH4CI Mg3N2Love is not a maybe thing. You know whe n you love some one.F- S2-。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
电子式书写规则
在元素符号周围用“·”和“×”来表示原子的最外层电子(价电子),这种式子叫做电子式。
1. 原子的电子式
由于中性原子既没有得电子,也没有失电子,所以书写电子式时应把原子的最外层电子全部排列在元素符号周围。
排列方式为在元素符号上、下、左、右四个方
向,每个方向不能超过2个电子。
例如,、、、。
2. 金属阳离子的电子式
金属原子在形成阳离子时,最外层电子已经失去,但电子式仅画出最外层电子,所以在画阳离子的电子式时,就不再画出原最外层电子,但离子所带的电荷数应在元素符号右上角标出。
所以金属阳离子的电子式即为离子符号。
如钠离子的电
子式为;镁离子的电子式为,氢离子也与它们类似,表示为。
3. 非金属阴离子的电子式
一般非金属原子在形成阴离子时,得到电子,使最外层达到稳定结构,这些电子都应画出,并将符号用“[]”括上,右上角标出所带的电荷数,电荷的表示方
法同于离子符号。
例如,、、。
4. 共价化合物的电子式
共价化合物是原子间通过共用电子对结合而成的。
书写时将共用电子对画在两原子之间,每个原子的未成对电子和孤对电子也应画出。
因不同元素原子吸引电子能力不同,则共用电子对偏向吸引电子能力强的原子,而偏离吸引电子能力弱的
原子。
例如,、。
5. 根离子的电子式
根离子中,若不同原子间以共价键结合,画法同共价化合物,因根离子带有电荷,所以应把符号用“[]”括起来,右上角标出电荷数。
例如,铵根阳离子:;
氢氧根离子:。
6. 离子化合物的电子式
先根据离子电子式的书写方法,分别画出阴、阳离子的电子式,然后让阴、阳离
子间隔排列,注意相同离子不能合并。
例如,NaCl、MgCl
2、Na
2
O的电子式分别为
、、。
7. 用电子式表示物质的形成过程
①离子化合物的形成过程
形成用“→”表示,形成之前为原子的电子式并用弯箭头表示电子得失,形成之后为离子化合物的电子式。
例如,NaCl的形成过程为:
MgCl
2
的形成过程为:
②共价化合物或非金属单质的形成过程
表示方法基本同离子化合物相同,不同的是因没有电子得失,所以不要再画弯箭头,并且“→”之后为共价化合物或非金属单质的电子式。
HCl:
Cl
2
:
电子式书写中的常见错误
一、漏写没有参加成键的电子对
Cl Cl
Cl C Cl (正确)Cl C Cl (错误)N N (正确)N N(错误)
Cl Cl
二、漏写或多加[]及错写电荷数
Na+(正确)[Na ]+(错误)H F (正确)H [ F ]-(错误)
H
Na+[ Cl ]-(正确)Na+Cl (错误)[ H N H ]+[ Cl ]-(正确)NH 4+[ Cl ]-(错误)
H
三、漏标离子所带的电荷数或与化合价混淆
[ Cl ]-Ca2+[ Cl ]-(正确)[ Cl ]Ca2+[ Cl ](错误)[ Cl ]-1Ca2+[ Cl ]-1(错误)
Na+[ S ]2-Na+(正确)Na+[ S ]Na+(错误)Na+1[ S ]-2Na+1(错误)
四、将相同离子错误合并
[ Cl ]-Mg2+[ Cl ]-(正确)Mg2+[ Cl ]2-(错误)Na+[ S ]2-Na (正确)Na2+[ S ]2-(错误)
五、电子式中微粒排列错误
H O Cl (正确)H Cl O (错误)[ H O ]-Ca2+[ O H ]-(正确)[ O H ]Ca2+[ O H ](错误)Mg2+[ N ]3-Mg2+[ N ]3-Mg2+(正确)Mg2+Mg2+Mg2+[ N ]3-[ N ]3-(错误)
六、电子(电子对)排列错误
N N (正确)N N (错误)N N (错误)O C O (正确)O C O (错误)
七、用电子式表示形成过程时错误
化学方程式中的反应物与生成物之间应该用“→”连接,而不用“=”连接。
H + Cl →H Cl (正确)H + Cl = H Cl (错误)
离子化合物或离子共价化合物
(I)NaOH _____________(1)H2O_____________
(2)Na2O2_____________ (2)H2O2_____________
(3)NH4Cl_____________(3)NH3_____________
(4)CaH2_____________ (4)CO2_____________
(5)CaC2_____________ (5)C2H2_____________
(6)Na2O_____________ (6)}HClO_____________
(7)Na3N_____________ (7) BF3_____________
(8)OH-_____________。
