ISO 15189实验室认可性能验证方案
ISO-15189实验室认可性能验证方案

医学实验室ISO 15189认可性能验证实验方案为了满足目前医学实验室认可的需求保证实验室检测结果的准确性,特制定本方案。
适用于强生VITROS产品的试验项目的性能验证,包括V250/V350/V950/FS5.1//V3600/V5600上所能开展的所有定性检测项目。
本方案从准确度、精密度、参考范围、线性范围以及方法学比对5个方面对各个试验项目进行评价。
一、精密度(Precision):精密度是指在规定条件下所获得的检测结果的接近程度,表示测定结果中随机误差大小程度的指标。
精密度通常用不精密度表示。
可以分别评价连续精密度(批内精密度)、重复性不精密度(中间精密度,包括批间、日间精密度等)和再现性精密度。
本方案采用批内和天间两种方法对各个试验项目的精密度进行评价。
全部实验过程使用同批号试剂和质控品,并且保证检测当日质控在控。
1、批内精密度(连续精密度):方法:在检测患者标本过程中,连续运行高低水平质控品各20次,记录检测结果。
计算批内精密度的CV值和SD值。
结果评价(1)厂家评价标准:计算精密度指数=验证SD/厂商SD,精密度指数要求小于等于1,或者实测CV小于等于厂家要求的CV,两者符合其一即可。
具体见《精密度评价》表格。
(2)按照国际推荐标准:批内精密度应在CLIA88允许误差的1/4以内,见美国CLIA’88能力比对检验的分析质量要求。
2、天间精密度(中间精密度):方法:同样使用两个水平的质控品,若需复溶冻干质控品做实验,要注意选择产品的稳定性和瓶间差。
要严格控制每次复溶冻干品时的操作手法。
连续测试20天,每天检测1次。
在次过程中不能更换试剂批号及质控品批号,是否需要重新定标则取决于实验室。
测试完成后记录检测结果。
结果评价(1)厂家评价标准: 计算天间的SD及CV值,并计算精密度指数=验证SD/厂商SD。
精密度指数要求小于等于1,或者实测CV小于等于厂家要求的CV,两者符合其一即可。
具体见《精密度评价》表格。
微生物检验15189认可

ISO15189实验室认可中临床微生物检验要点举例分析首都医科大学附属北京友谊医院临床检验中心苏建荣主要内容Guidance in the Field of Clinical Microbiology痰涂片:质量(回答问题),既是人员也是检验前在生物安全柜中(现场检查),也是安全Hodge试验(霍奇试验)常规?M ulti-D rug R esistanceMDR什么是MDR/PDR?摘自天津胡志东稿什么是MDR/PDR?MDR(多重耐药)指细菌对包括头孢菌素类、青霉素类、喹诺酮类、氨基糖甙类、碳青霉烯类等在内的抗生素中的至少2-3类耐药。
PDR(泛耐药)指细菌除对粘菌素、舒巴坦可能敏感外,对临床上常见的抗生素全部耐药,PDR是MDR中的特殊类型。
PDR产KPC酶(A类碳青霉烯酶)细菌的检测◆对一种或多种头孢菌素碳青霉烯类(续)对由这些分离菌引起的感染患者,应通知临床经治医师和感染控制人员,考虑选用其他抗菌药物。
初筛试验--2009、2010初筛试验--2011天津医科大学总医院⏹执行Modified Hodge Test (MHT)试验时机?⏹初筛试验阳性和对III亚类头孢菌素(如头孢哌酮、头孢噻肟、头孢他啶、头孢唑肟和头孢曲松)中一种或多种药物耐药改良Hodge试验耐药基因检测PCRTaq基因检测结果M 1 2 31500900700500400200100920bp注:M 为DNA marker, 1.KPC 阳性对照菌;2.临床分离肺炎克雷伯菌;3.阴性对照ATCC25922图2肺炎克雷伯菌bla KPC-2基因PCR 扩增产物电泳图小结:纸片初筛阳性5.2 设施环境5.2.1.1 实验室设施符合等级要求要有评估评估程序及依据生物安全(运送与交接)5.2.1.2 空间足够(领导)分子生物学要有独立设置三区5.2.2 闭门器洗眼设施有消毒及放水日期5.2 设施环境5.2.4 照明及电源(UPS)5.2.5 温湿度(记录)(校准的修正因子)5.2.10 病原存放遵守安全条例专人、专地、专记录设备5.3.1 设备配置(*关键技术要求评审原则) 无菌体液的直接显微镜检查应具备细胞离心机。
ISO15189实验室认可质量手册之检验程序的质量保证

ISO15189实验室认可质量手册之检验程序的质量保证检验程序的质量保证1 总则实验室必须建立完善的质量保证体系,加强对实验室检验质量的控制,通过质控、比对等手段对实验室检验质量随时进行监测,提高工作人员的质量意识,确保为服务对象提供准确、可靠的检测数据。
2 质量保证程序2.1 通过合同评审的方式对医生开具检验申请单进行规范,并在工作中对不合格的检验申请单进行控制和记录,与临床加强沟通,消除检验申请过程中对检验质量造成的影响。
2.2 实验室应加强对临床医护人员和医院护工的培训、监督,确保原始样品的采集、留取、运送符合质量体系要求,并向其提供相关的咨询服务。
2.3 实验室应对工作人员进行专业培训,并制定有效的管理程序,避免工作人员在样品处理、检验和报告等过程中差错的发生。
2.4 实验室应建立有效的室内质控程序,保证检验程序持续有效性。
a)凡是能够获得有证质控品项目,均应开展室内质控,每次试验随样品一起操作,保持相应的记录,并制定质控规则,对每日质控数据进行分析判断,及时纠正违反规则的项目,并分析失控原因,做好相关记录,保证检测系统的稳定性;b)对室内质控定期进行总结汇总,并进行趋势性分析,以提前发现潜在不符合项。
c)无法获得有证质控品的项目或一些特殊项目,可采取自制质控品、留样复查或其它方法进行室内质控,并将质控的操作规程形成文件。
2.5 实验室在适用且可能时候,应对所开展项目检验结果的不确定度进行确定。
分析不确定度的来源时应包括:采样、样品制备、样品部分的选择、校准品、参考物质、加入量、所用的设备、环境条件、样品的状态及操作人员的变更等。
2.6 实验室应建立检验结果量值溯源管理程序,使测量结果能够通过一条具有规定不确定度的连续溯源链,将结果溯源至SI单位,或可参比至自然常数或其他规定的参考值,从而使检测结果与国际标准或者其他参考标准具有可比性,在技术上保证检验结果的准确可靠性。
实验室应根据自身实际情况选择合适的溯源方式,目前实现量值溯源可采用下列方法之一:a)对测量系统定期进行校准和正确度验证;b)参加适当的实验室间比对计划;c)使用有证书说明其材料特性的适当参考物质;d)比率或倒易型测量;e)使用己明确建立的、经规定的、性能己确定的、被各方承认的协议标准或方法;f)若由供应商或制造商提供溯源性,应有关于试剂、程序或检验系统溯源性的声明文件。
ISO15189性能验证个人经验分享 ZT

的均值及CV,以CV≤20%时的最大稀释管浓度作为可报告范围的低限;高值样 本按照一定比例稀释后的系列样本都重复测定3次,计算回收率R=测定均值/理 论值,回收率R在80%-120%之间的最大稀释倍数即为该方法的最大可稀释倍数, 可报告范围上限 = 最大可稀释倍数×线性范围上限。
7、参考文献
1、 CNAS-CL02-A003:2018《医学实验室质量和能力认可准则在临床化学检 验领域的应用说明》
注1:通常较高值样本的不精密度较小,较低值样本的不精密度偏大。对低值有临床意 义的检测项目,宜评估有判断价值的低水平样本的不精密度。 注2:如检测结果没有明确的医学决定水平,可在参考区间上限左右选一个浓度,再根 据检验项目的特点在测量区间内选择另一个浓度。 注3:如与厂商或文献报导的不精密度比较,所选样本水平宜与被比较的样本水平接近。
4、线性区间ቤተ መጻሕፍቲ ባይዱ
1.2、验证方法及结果判断 方法:每个浓度水平的样本重复测定3~4次。所有样本应在一次运行中
或几次间隔很短的运行中随机测定,最好在1天之内完成。 判断:免疫法:相关系数r2≥0.95,a在0.95-1.05范围内,截距b与0无显著
差异;酶法: r2≥0.99 , a在0.97-1.03范围内,截距b与0无显著差异。或者按照 WS/T 408-2012文件要求做线性回归分析和线性检验。
可报告范围高限验证(最大可稀释倍数):使用混合血清或5%牛血清白 蛋白生理盐水溶液或测定方法要求的稀释液对高值待测样本(必要时可添加被 分析物,并计算出理论值)进行一系列稀释,并记录稀释倍数。
6、临床可报告范围
1.2、验证方法及结果判断 在一次运行中将每个低值样本重复测定5~10次,分别计算每个低值样本
4、线性区间
iso15189实验室认可准则

测定浓度 基本样本 分析样本1 分析样本2
加入浓度
回收浓度
回收率
基础样
基础样本
基础样本+高值
本
+C.fas
质控
项目 第一次 第二次 第三次 均值 第一次 第二次 第三次 均值 第一次 第二次 第三次 均值
TP
68 70 68 68.67 73 73 73 73.00 73 72 75 73.33
ALB
iso15189实验室认可 准则
5. 技术要求
5.1 人员 5.2 设施和环境条件 5.3 实验室的设备 5.4 检验前程序 5.5 检验程序 5.6 检验程序的质量保证 5.7 检验后程序 5.8 结果报告
2
5.5检验程序-- 5.5.1
实验室应当制定符合实验室工作要求和检验要求的 检验程序,包括选择和分取样品程序。
在应用于医学检验之前,选择的检验方法和程序应 当经过验证并得到满意的验证结果。实验室主任或 其指定人员应当对检验程序进行最初的和定期的审 核。审核通常每年进行一次。审核应当记录。
4
理解要点:检验程序的确认, 临床验证, 定期评审
5.5检验程序-- 5.5.3
所有程序应当采用实验室人员能够普遍理解的语种文件 化且置放在工作区域以方便相关人员使用。
16
清mL
实例分析-1
方法:参考EP6-A文件要求,选取高浓度和低浓度人血清标本,通过倍比稀释的方式得 到6份梯度浓度待测样本,每样本重复测定4次,进行该项目的线性范围评估
项目 总胆固醇 TC
日期 2010/8/7
仪器 Roche 7600
试剂批号
标准液批号
操作者 付红伟
审核者 王倩
医学实验室ISO15189认可性能验证实验方案

医学实验室ISO15189认可性能验证实验方案
1.引言
引言部分应该简要介绍实验室的背景和目的。
解释为什么需要进行性能验证实验,并描述该实验对实验室的重要性。
2.目标
明确性能验证实验的目标。
例如,验证分析方法的准确性、精确性、灵敏度和特异性,以及实验室是否能够在正常操作条件下提供可靠和一致的结果。
3.实验原则
描述性能验证实验的基本原则。
例如,实验应在真实且代表性的样本中进行,应根据适当的统计方法进行数据分析,结果应与已建立的参考标准进行比较,等等。
4.实验设计
详细描述实验设计。
实验设计应包括实验样本的选择和样本数量的确定。
样本应具有广泛的范围和不同的特征,以便能够提供对实验方法的全面评估。
5.实验步骤
详细描述性能验证实验的实施步骤。
每个步骤应包括所需的试剂、设备和仪器,以及步骤的详细说明。
这些步骤可能包括样本的准备、分析方法的执行、数据记录和分析等。
6.数据分析
描述实验数据的分析方法。
分析应包括对数据的描述性统计分析、准确性和精确性的计算、结果的比较和解释等。
7.结果和讨论
描述性能验证实验的结果和讨论。
结果应与已建立的参考标准进行比较,以评估实验方法的准确性和可靠性。
讨论应分析实验结果并解释其意义,讨论实验过程中可能出现的问题,并提出改进措施。
8.结论
总结性能验证实验的结果和结论。
结论应明确实验方法的准确性和可靠性,并提出改进实验方法或流程的建议。
15189认证仪器项目性能参数验证简要方案
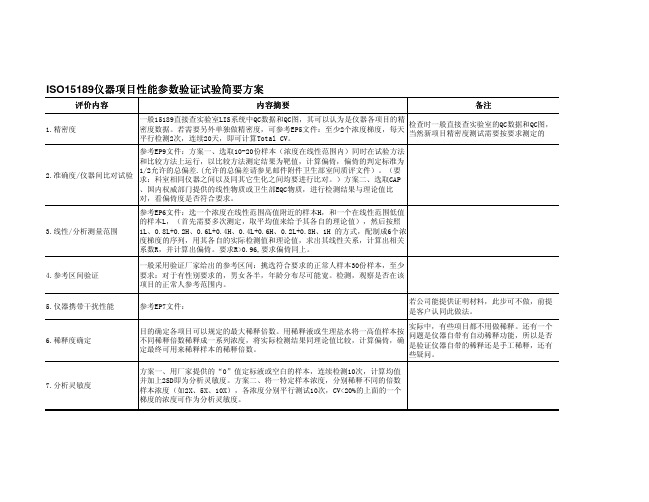
评价内容
1.精密度
内容摘要
备注
一般15189直接查实验室LIS系统中QC数据和QC图,其可以认为是仪器各项目的精 检查时一般直接查实验室的QC数据和QC图, 密度数据。若需要另外单独做精密度,可参考EP5文件:至少2个浓度梯度,每天 当然新项目精密度测试需要按要求测定的 平行检测2次,连续20天,即可计算Total CV。
参考EP9文件:方案一、选取10-20份样本(浓度在线性范围内)同时在试验方法 和比较方法上运行,以比较方法测定结果为靶值,计算偏倚,偏倚的判定标准为 1/2允许的总偏差.(允许的总偏差请参见邮件附件卫生部室间质评文件)。(要 2.准确度/仪器间比对试验 求:科室相同仪器之间以及同其它生化之间均要进行比对。)方案二、选取CAP 、国内权威部门提供的线性物质或卫生部EQC物质,进行检测结果与理论值比 对,看偏倚度是否符合要求。 参考EP6文件:选一个浓度在线性范围高值附近的样本H,和一个在线性范围低值 的样本L,(首先需要多次测定,取平均值来给予其各自的理论值),然后按照 1L、0.8L+0.2H、0.6L+0.4H、0.4L+0.6H、0.2L+0.8H、1H 的方式,配制成6个浓 度梯度的序列,用其各自的实际检测值和理论值,求出其线性关系,计算出相关 系数R,并计算出偏倚。要求R>0.96,要求偏倚同上。 一般采用验证厂家给出的参考区间:挑选符合要求的正常人样本30份样本,至少 要求:对于有性别要求的,男女各半,年龄分布尽可能宽。检测,观察是否在该 项目的正常人参考范围内。 参考EP7文件: 若公司能提供证明材料,此步可不做,前提 是客户认同此做法。
7.分析灵敏度
3.线性/分析测量范围
4.参考区间验证
ISO15189实验室认可性能验证方案报告

医学实验室ISO 15189认可性能验证实验方案为了满足目前医学实验室认可的需求保证实验室检测结果的准确性,特制定本方案。
适用于强生VITROS产品的试验项目的性能验证,包括V250/V350/V950/FS5.1//V3600/V5600上所能开展的所有定性检测项目。
本方案从准确度、精密度、参考围、线性围以及方法学比对5个方面对各个试验项目进行评价。
一、精密度(Precision):精密度是指在规定条件下所获得的检测结果的接近程度,表示测定结果中随机误差大小程度的指标。
精密度通常用不精密度表示。
可以分别评价连续精密度(批精密度)、重复性不精密度(中间精密度,包括批间、日间精密度等)和再现性精密度。
本方案采用批和天间两种方法对各个试验项目的精密度进行评价。
全部实验过程使用同批号试剂和质控品,并且保证检测当日质控在控。
1、批精密度(连续精密度):方法:在检测患者标本过程中,连续运行高低水平质控品各20次,记录检测结果。
计算批精密度的CV值和SD值。
结果评价(1)厂家评价标准:计算精密度指数=验证SD/厂商SD,精密度指数要求小于等于1,或者实测CV小于等于厂家要求的CV,两者符合其一即可。
具体见《精密度评价》表格。
(2)按照国际推荐标准:批精密度应在CLIA88允许误差的1/4以,见美国CLIA’88能力比对检验的分析质量要求。
2、天间精密度(中间精密度):方法:同样使用两个水平的质控品,若需复溶冻干质控品做实验,要注意选择产品的稳定性和瓶间差。
要严格控制每次复溶冻干品时的操作手法。
连续测试20天,每天检测1次。
在次过程中不能更换试剂批号及质控品批号,是否需要重新定标则取决于实验室。
测试完成后记录检测结果。
结果评价(1)厂家评价标准: 计算天间的SD及CV值,并计算精密度指数=验证SD/厂商SD。
精密度指数要求小于等于1,或者实测CV小于等于厂家要求的CV,两者符合其一即可。
具体见《精密度评价》表格。
15189实验室认可程序文件之检验方法选择和评审程序

检验方法选择和评审程序1 目的规范检验方法的选择和评审程序,采用权威或者已被同行公认的方法对实验室使用的检验方法进行评价、确认、核实,并根据评审结果对检验方法不断改进,保证所选用的检验方法和检验程序能满足实验室服务对象的需要,确认其符合相应的用途。
2 适用范围实验室使用的检验方法。
3 职责3.1 技术负责人和各专业组组长共同负责检验方法评审和选择。
3.2 各专业组组长负责组织本组工作人员对所选方法的验证确认。
4 定义和术语4.1 标准检测方法简称标准方法,是指卫生标准、技术标准或检测工作规范中明确规定必须采用的检测方法,并具有检测方法名称和标准文号。
4.2 非标准检测方法指卫生标准、技术标准和检测工作规范中未明确规定而可以由检测机构自行选择的检测方法。
非标准方法可以是权威机构发布的方法,或有关科技文献、杂志、教科书上发表的方法。
4.3 自编(建)方法实验室根据工作需要自行设计开发的检测方法。
4.4 评价实验室自行研究或开发了一个新的检测系统或方法,或自行改变或组合检测系统(如在“开放”仪器上或原检测系统上,实验室自行换用试剂和/或校准品、任意修改操作程序等),为了使方法的检验结果符合临床要求,必须对方法的不精密度、不准确度、病人结果线性范围、分析灵敏度、分析特异性(干扰)、参考区间等6大基本性能逐一进行实验评估,以实验资料说明检测系统的可靠性。
4.5 确认通过提供客观证据对特定的预期用途或应用要求已得到满足的认定。
4.6 核实实验室准备采用的检测系统,己被许多实验室广泛应用,实验室期望核实该系统能不能被认可,进行的评估为核实实验。
通过实验至少应说明检测系统可以得到厂商报告一致的不精密度和不准确度,也能和检测系统其他用户的性能一致。
4.7 检出限:给定分析程序具有适当的确定检出的分析物的最小浓度或量。
4.8 分析灵敏度:为校准曲线的斜率及对于规定量的变化分析程序产生信号的变化。
4.9 功能灵敏度:以天间重复CV为20%时对应检测限样品具有的平均浓度,确定为检测系统或方法可定量报告分析物的最低浓度或其他量值的限值。
15189实验室认可程序文件之检验方法选择和评审程序

15189实验室认可程序文件之检验方法选择和评审程序检验方法选择和评审程序1 目的规范检验方法的选择和评审程序,采用权威或者已被同行公认的方法对实验室使用的检验方法进行评价、确认、核实,并根据评审结果对检验方法不断改进,保证所选用的检验方法和检验程序能满足实验室服务对象的需要,确认其符合相应的用途。
2 适用范围实验室使用的检验方法。
3 职责3.1 技术负责人和各专业组组长共同负责检验方法评审和选择。
3.2 各专业组组长负责组织本组工作人员对所选方法的验证确认。
4 定义和术语4.1 标准检测方法简称标准方法,是指卫生标准、技术标准或检测工作规范中明确规定必须采用的检测方法,并具有检测方法名称和标准文号。
4.2 非标准检测方法指卫生标准、技术标准和检测工作规范中未明确规定而可以由检测机构自行选择的检测方法。
非标准方法可以是权威机构发布的方法,或有关科技文献、杂志、教科书上发表的方法。
4.3 自编(建)方法实验室根据工作需要自行设计开发的检测方法。
4.4 评价实验室自行研究或开发了一个新的检测系统或方法,或自行改变或组合检测系统(如在“开放”仪器上或原检测系统上,实验室自行换用试剂和/或校准品、任意修改操作程序等),为了使方法的检验结果符合临床要求,必须对方法的不精密度、不准确度、病人结果线性范围、分析灵敏度、分析特异性(干扰)、参考区间等6大基本性能逐一进行实验评估,以实验资料说明检测系统的可靠性。
4.5 确认通过提供客观证据对特定的预期用途或应用要求已得到满足的认定。
4.6 核实实验室准备采用的检测系统,己被许多实验室广泛应用,实验室期望核实该系统能不能被认可,进行的评估为核实实验。
通过实验至少应说明检测系统可以得到厂商报告一致的不精密度和不准确度,也能和检测系统其他用户的性能一致。
4.7 检出限:给定分析程序具有适当的确定检出的分析物的最小浓度或量。
4.8 分析灵敏度:为校准曲线的斜率及对于规定量的变化分析程序产生信号的变化。
ISO15189:2012与临床实验室定量检测程序分析性能评价

•短篇论著•IS015189 =2012与临床实验室定量检测程序分析性能评价任亚萍,胡敏八(中南大学湘雅二医院检验科,长沙410011)摘要:目的根据国际标准化组织(ISO)15189:2012要求,建立适用于临床实验室定量检测程序分析性 能评价的实验方案,对Beckman Coulter IM M A G E 800检测系统进行性能评价。
方法参照美国临床和实验室标准化委员会(CLSI)的有关文件及相关文献,结合工作实际,设计验证方案,对Beckman Coulter IM M A G E 800检测系统6个常规检测项目的正确度、精密度、分析测量范围(A M R)、临床可报告范围(CRR)和生物参考 区间5个性能指标进行评价,并与厂家提供的分析性能或公认的质量指标进行比较。
结果 IM M A G E 800特定蛋白分析仪各项目的相对偏倚在0. 88%〜3. 25%,均小于规定的允许偏倚;各项目批内精密度在1.07%〜■4.00%范围内,均小于原卫生部临检中心能力验证(P T)/室间质量评价(E Q A)的l/4T E a质量要求,各项目批 间精密度在1.39%〜6. 17%范围内均小于P T/E Q A的l/3T E a质量要求;各项目的回归方程斜率均在0.97〜1.03范围内,r2>0. 995,线性良好;各项目临床可报告范围能够满足临床检测需求;各项目引用的参考区间合 适。
结论 Beckman Coulter IM M A G E 800特定蛋白分析仪在正确度、精密度、分析测量范围、临床可报告范 围和生物参考区间5个方面验证合格,能满足实验室需求。
该研究验证方案和实验方法简便易行,对规范实验 室建设和实验室认可具有重要意义。
关键词:特定蛋白分析仪;性能评价;I SO 15189:2012D O I:10. 3969/j.issn. 1673-4130. 2018. 02. 027 中图法分类号:R446文章编号d673-4130(2018)02-0209-05 文献标识码:B国际标准化组织(IS0)1518 9:2 012[1](以下简称 新版准则)是目前国际最权威、全球通行的医学实验 室认可规范。
ISO15189性能验证

PAB方法学评估
CLIA88 https:///clia.htm 生物学变异数据库 https:///biodatabase1.htm#1
依据检测系统不同评价的范围不同 自建检测系统 :六大性能外(不精密度,不准确度,病人结果可 报告范围,分析灵敏度,分析特异性和参考区间等),还必须确 定检测系统校准和控制方法。 封闭检测系统 :必须做三个性能(不精密度,不准确度,病人结 果可报告范围)。对于低值在临床上特别有用的项目,还须加做 分析灵敏度。 外用检测系统 :核实的性能为不精密度和不准确度
方法学评价-检测系统一览表
方法学评估的相关指南及文件
方法学评估的相关指南及文件
按照实验室操作规范和制造商的推荐收集和处理患者标本。
应在有临床意义的范围内,即医学决定水平范围内评价待评方法。
参比方法的范围应至少与待评方法的范围相同,以便在分析测定范 围内可以比较。
至少需分析40个样本
双份测定
欧洲标准 https:///europe.htm
质量目标
方法学评价-检测系统一览表
7.2评价数据的产生:连续测定5d,每天一个分析批,每批两个浓度水平,每一个 浓度水平同一样本重复测定3次;如果因为质量控制程序或操作问题判断一批为失
控,应剔除数据,并增加执行一个分析批;如果厂家指出其声明的不精密度数据是 在多个校准周期下产生的,则操作者在实验期间应选择重新校准。
质量管理之系列5
方法学评估
分子生物室 张正君
目录
• 相关法律法规及规范性文件 • 方法学评估概述 • 方法学评估的相关指南及文件 • 程序性文件展示 • Q-expert软件在方法学评估中的应用
ISO15189实验室认可及评审流程介绍

• 3.14 质量管理体系 quality management system
• 3.15 委托实验室 referral laboratory
• 3.16 样品 sample
• 3.17 溯源性 traceability
• 3.18 测量正确度 trueness of measurement
证 • 5.7检验后程序 • 5.8结果报告
三、实验室认可评审流程
实验室认可主要流程
• 意向申请 • 实验室准备 • 正式申请阶段 • 现场评审阶段
认可条件
• 具有明确的法律地位。 • 符合中国合格评定国家认可委员会(CNAS)
认可准则。 • 遵守CNAS认可规则、认可政策的有关规定,
履行相关义务。
IS09000认证活动的对象主要是制造型企业和服务 型企业
两者的主要区别
对象不同:认可对象是检测实验室或(和)校准实验室; 认证对象是产品、过程或服务。
负责机构不同:认可由权威机构进行(不少国家是由政 府机构进行的,可确保权威性);认证则由第三方进行。
性质不同:认可是权威机构正式承认,说明经批准 可从事某项活动,其结果常得到国家的承认;认证 是书面保证,通过由第三方认证机构颁发的认证证 书,使其它方面确信经认证的产品、过程和服务满 足质量体系的要求。
认可:正式表明合格评定机构具备实施 特定合格评定工作的能力的第三方证明
认可:
• 是“权威机构对某一组织或个人有能力完 成特定任务做出正式承认的程序”。
-ISO/IEC导则2:1996
• 实验室认可常常是由经过授权的认可机构 对实验室的管理能力和技术能力按照约定 的标准进行评价,并将评价结果向社会公 告以正式承认其能力的活动。
ISO 15189实验室认可性能验证方案

医学实验室ISO 15189认可性能验证实验方案为了满足目前医学实验室认可的需求保证实验室检测结果的准确性,特制定本方案。
适用于强生VITROS产品的试验项目的性能验证,包括V250/V350/V950/FS5.1//V3600/V5600上所能开展的所有定性检测项目。
本方案从准确度、精密度、参考范围、线性范围以及方法学比对5个方面对各个试验项目进行评价。
一、精密度(Precision):精密度是指在规定条件下所获得的检测结果的接近程度,表示测定结果中随机误差大小程度的指标。
精密度通常用不精密度表示。
可以分别评价连续精密度(批内精密度)、重复性不精密度(中间精密度,包括批间、日间精密度等)和再现性精密度。
本方案采用批内和天间两种方法对各个试验项目的精密度进行评价。
全部实验过程使用同批号试剂和质控品,并且保证检测当日质控在控。
1、批内精密度(连续精密度):方法:在检测患者标本过程中,连续运行高低水平质控品各20次,记录检测结果。
计算批内精密度的CV值和SD值。
结果评价(1)厂家评价标准:计算精密度指数=验证SD/厂商SD,精密度指数要求小于等于1,或者实测CV小于等于厂家要求的CV,两者符合其一即可。
具体见《精密度评价》表格。
(2)按照国际推荐标准:批内精密度应在CLIA88允许误差的1/4以内,见美国CLIA’88能力比对检验的分析质量要求。
2、天间精密度(中间精密度):方法:同样使用两个水平的质控品,若需复溶冻干质控品做实验,要注意选择产品的稳定性和瓶间差。
要严格控制每次复溶冻干品时的操作手法。
连续测试20天,每天检测1次。
在次过程中不能更换试剂批号及质控品批号,是否需要重新定标则取决于实验室。
测试完成后记录检测结果。
结果评价(1)厂家评价标准: 计算天间的SD及CV值,并计算精密度指数=验证SD/厂商SD。
精密度指数要求小于等于1,或者实测CV小于等于厂家要求的CV,两者符合其一即可。
具体见《精密度评价》表格。
血站酶免实验室15189认可性能验证方案

酶免一、精密度:(购买HIV-Ag 及HCV 0.05NCU/ml的质控各50支)1,批内精密度:用康彻思坦的血筛四项标准物质以及HCV-Ab标准物质、HIV-Ag标准物质,分别在对应项目同一酶免板内重复加样20次检测,记录结果,计算S/CO值的X和SD,计算CV值,评价HBsAg、HCV-Ab、HIV-Ab、HIV-Ag/Ab以及TP-Ab ELISA试剂的重复性精密度,CV值<15%。
2,中间精密度:用康彻思坦的血筛四项标准物质以及HCV-Ab标准物质、HIV-Ag标准物质,在对应项目酶标板内每天检测一次,连续检测20天,记录结果,计算S/CO值的X和SD,计算出CV值,评价HBsAg、HCV-Ab、HIV-Ab、HIV-Ag/Ab以及TP-Ab ELISA检测试剂的中间精密度, CV值<20%。
二、符合率:采用商品化血清盘对HBsAg、HCV-Ab、HIV-Ab、HIV-Ag/Ab以及TP-Ab ELISA进行FAME检测,结果与血清盘结果比较,分别计算阳性符合率和阴性符合率。
阴性符合率(%)=被测试剂盒测定真阴性数/血清盘阴性数×100%,阳性符合率(%)=被测试剂盒测定真阳性数/血清盘阳性数×100%。
评价标准:阴性符合率≥90%,阳性符合率≥90%。
(购买四个项目的血清盘,20阴20阳,HCV4代及HIV-Ag 再单独一份血清盘)三、最低检出限用北京康彻思坦的血筛四项标准物质以及HCV标准物质(0.05NCU/ml)、HIV P24标准物质作为定值样本,用阴性血清做一系列稀释,依次对稀释样本做检测,选取OD值与试剂说明书上的Cut-off参考值最接近(但≥Cut-off参考值)的稀释度,再将该稀释度样本作20次重复测试,如果95%以上OD测量值≥Cut-off参考值,则该稀释度对应样本的浓度即为检出低限,反之则需要重新稀释验证。
四、cutoff值验证(南京的方案?)选择60份健康人新鲜血浆(来自无锡红十字血液中心,编号为S1-S60)和60份目标标志物阴性而有其他免疫标志物阳性的患者新鲜血清(来自无锡二院,编号为1-60),共120份,分三批进行检测,计算所有标本检测结果OD值的均值(X)和标准差(SD),计算X+3SD并与试剂盒说明书计算出的Cut-off值进行比较。
医学实验室ISO15189认可性能验证实验方案

医学实验室ISO15189认可性能验证实验方案德信诚咨询为了满足目前医学实验室认可的需求保证实验室检测结果的准确性,特制定本方案。
本方案从准确度、精密度、参考范围、线性范围以及方法学比对5个方面对各个试验项目进行评价。
一、精密度(Precision):精密度是指在规定条件下所获得的检测结果的接近程度,表示测定结果中随机误差大小程度的指标。
精密度通常用不精密度表示。
可以分别评价连续精密度(批内精密度)、重复性不精密度(中间精密度,包括批间、日间精密度等)和再现性精密度。
本方案采用批内和天间两种方法对各个试验项目的精密度进行评价。
全部实验过程使用同批号试剂和质控品,并且保证检测当日质控在控。
1、批内精密度(连续精密度):方法:在检测患者标本过程中,连续运行高低水平质控品各20次,记录检测结果。
计算批内精密度的CV值和SD值。
结果评价(1)厂家评价标准:计算精密度指数=验证SD/厂商SD,精密度指数要求小于等于1,或者实测CV小于等于厂家要求的CV,两者符合其一即可。
具体见《精密度评价》表格。
(2)按照国际推荐标准:批内精密度应在CLIA88允许误差的1/4以内,见美国CLIA’88能力比对检验的分析质量要求。
2、天间精密度(中间精密度):方法:同样使用两个水平的质控品,若需复溶冻干质控品做实验,要注意选择产品的稳定性和瓶间差。
要严格控制每次复溶冻干品时的操作手法。
连续测试20天,每天检测1次。
在次过程中不能更换试剂批号及质控品批号,是否需要重新定标则取决于实验室。
测试完成后记录检测结果。
结果评价(1)厂家评价标准: 计算天间的SD及CV值,并计算精密度指数=验证SD/厂商SD。
精密度指数要求小于等于1,或者实测CV小于等于厂家要求的CV,两者符合其一即可。
具体见《精密度评价》表格。
(2)按照国际推荐标准:批内精密度应在CLIA88允许误差的1/3以内,见美国CLIA’88能力比对检验的分析质量要求。
ISO15189认可关于IQ200全自动尿沉渣分析仪性能验证方案

ISO15189认可关于IQ200全自动尿沉渣分析仪性能验证方案赵曙光;李晶;白雪;王毅【期刊名称】《医学检验与临床》【年(卷),期】2017(028)007【摘要】目的:提供一套满足ISO15189认可的评价IQ200全自动尿沉渣分析仪的性能验证方案.方法:通过精密度、正确度、携带污染率、可报告范围、生物参考区间验证五个方面对仪器进行性能验证.结果:IQ200的性能验证各项指标均合格.批内精密度变异系数(CV)分别为RBC 4.3%和WBC 4.3%;RBC和WBC批间精密度的CV分别为18.7%、18.5%.正确度验证方案以室间比对方式替代,各参数符合率均≥80%.RBC和WBC的携带污染率分别为-0.14%、0.00%.RBC的可报告范围为0~15342个/μL,WBC的可报告范围为0~5745个/μL.生物参考区间验证各参数R值均≥0.9.结论:IQ200全自动尿沉渣分析仪的性能验证各项均合格且满足ISO15189认可要求.【总页数】4页(P27-29,35)【作者】赵曙光;李晶;白雪;王毅【作者单位】天津市天津医院检验科,天津 300211;天津市天津医院检验科,天津300211;天津市天津医院检验科,天津 300211;天津市天津医院检验科,天津300211【正文语种】中文【相关文献】1.ISO15189认可中IQ-200全自动尿液显微镜系统性能验证 [J], 王芳;冯长超;吴迪;马宁;刘匀;郝殿晋;王术艺2.ISO15189认可关于CYP2C19基因多态性检测性能验证评价 [J], 师志云;贾伟;梁小燕;张玉英;赵玥;赵倩颖;郭雅琪;何学虎;董洁;赵志军3.ISO15189认可与血液筛查实验室酶联免疫吸附试验法试剂质量性能验证 [J], 杨忠思;李伟;许雷4.实验室核酸检测性能验证中ISO15189认可准则应用研究 [J], 陈士团;陈勤波5.实验室核酸检测性能验证中ISO15189认可准则应用研究 [J], 陈士团;陈勤波因版权原因,仅展示原文概要,查看原文内容请购买。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
医学实验室ISO 15189认可性能验证实验方案为了满足目前医学实验室认可的需求保证实验室检测结果的准确性,特制定本方案。
适用于强生VITROS产品的试验项目的性能验证,包括V250/V350/V950/FS5.1//V3600/V5600上所能开展的所有定性检测项目。
本方案从准确度、精密度、参考范围、线性范围以及方法学比对5个方面对各个试验项目进行评价。
一、精密度(Precision):精密度是指在规定条件下所获得的检测结果的接近程度,表示测定结果中随机误差大小程度的指标。
精密度通常用不精密度表示。
可以分别评价连续精密度(批内精密度)、重复性不精密度(中间精密度,包括批间、日间精密度等)和再现性精密度。
本方案采用批内和天间两种方法对各个试验项目的精密度进行评价。
全部实验过程使用同批号试剂和质控品,并且保证检测当日质控在控。
1、批内精密度(连续精密度):方法:在检测患者标本过程中,连续运行高低水平质控品各20次,记录检测结果。
计算批内精密度的CV值和SD值。
结果评价(1)厂家评价标准:计算精密度指数=验证SD/厂商SD,精密度指数要求小于等于1,或者实测CV小于等于厂家要求的CV,两者符合其一即可。
具体见《精密度评价》表格。
(2)按照国际推荐标准:批内精密度应在CLIA88允许误差的1/4以内,见美国CLIA’88能力比对检验的分析质量要求。
2、天间精密度(中间精密度):方法:同样使用两个水平的质控品,若需复溶冻干质控品做实验,要注意选择产品的稳定性和瓶间差。
要严格控制每次复溶冻干品时的操作手法。
连续测试20天,每天检测1次。
在次过程中不能更换试剂批号及质控品批号,是否需要重新定标则取决于实验室。
测试完成后记录检测结果。
结果评价(1)厂家评价标准: 计算天间的SD及CV值,并计算精密度指数=验证SD/厂商SD。
精密度指数要求小于等于1,或者实测CV小于等于厂家要求的CV,两者符合其一即可。
具体见《精密度评价》表格。
(2)按照国际推荐标准:批内精密度应在CLIA88允许误差的1/3以内,见美国CLIA’88能力比对检验的分析质量要求。
二、准确度准确度(accuracy)指检测结果与被测量物真值之间的接近程度。
是分析测量范围、分析灵敏度以及生物参考区间评价的基础。
准确度的评价方法很多,比如检测定值参考物质,同参考方法进行比对,同有溯源性的检测系统进行方法学比对,卫生部临检中心质评的汇报结果均可以作为评价准确性的方法之一。
本方案采用测定定值标准物质的方法来评价各个检测项目的准确度。
定值标准物质采用厂家定值标准品。
方法:(1)试验期间保证机器状态正常,保证试验当日室内质控在控。
(2)按厂家要求准备各个项目的新批号定标品(要与定标时使用的定标品批号不同)各一套,按照标准复溶。
(3)记录该新批号定标品的定值。
(4)在设备上检测各个定标品(多水平)的相关项目,每个水平重复2次,记录检测结果,将检测结果录入《准确度评价》表格。
结果评价:(1)厂家标准:按照各定标品各水平的定值和不确定度(厂家提供),来确定准确度的偏倚范围。
计算实测均值的各项目各水平定标品的偏倚,与偏倚范围相比较,来判断偏倚是否可以接受。
详见《准确度评价》表,实测的均值如果落在该限度内,则为其准确度认为可被接受。
(2)按照国际推荐标准:准确度偏倚应该在CLIA88允许误差的1/2以内,见美国CLIA’88能力比对检验的分析质量要求。
三、参考范围验证参考 NCCLSC28一A2文件,本方案仅对厂家提供的或者实验室正在使用的各个项目的参考范围进行验证。
方法:(1)选择20个能够代表实验室的健康总体的标本。
(2)保证试验系统运行正常,依照标准操作程序检测标本。
(3)运行该20份标本,记录结果,将结果填入《参考区间验证》表格。
结果评价如果20个参考个体中不超过2例的检测值在验证的参考限之外,厂商或提供参考区间的实验室报告的95%参考区间可以接受。
如果3例以上超出界限,再选择20个参考个体进行验证,若少于或等于2个观测值超过原始参考值,则可接受,若还有3个超出参考限,需要重新检查各种条件,决定是否建立自己的参考区间。
四、线性范围分析测量范围即定量检测项目的线性范围,是整个检测系统(包括仪器、试剂、校准品、质控品、操作程序、检验人员等)对应于系列分析浓度的仪器最终输出的信号间是否呈恒定比例的性能,是一个很重要的仪器性能分析指标。
本实验通过测定不同配比比例的高低值新鲜患者标本,以验证实测值和理论值的线性关系,来评估每个检测项目的线性范围。
方法:(1)实验室人员必须十分熟悉仪器的操作、质量控制和定标方法,以及正确的收集样本。
试验期间保证仪器状态良好下,质控在控。
(2)全部实验数据尽可能在较短的时间内收集,如可能,单个分析试验最好在一天内做完。
(3)用于验证线性范围的标本类型应与临床测试所用的标本类型相同或相类似,所有标本应不含厂家所标定的干扰因素(如溶血、黄疸、脂血等)。
如果上述条件不可避免,则应在最后的报告中注明在评价实验中所用的标本处理方法或基质类型。
注意:收集的高浓度标本应尽可能的接近线性范围高限。
(4)按照《线性评价》表格要求配比标本。
将H 和L 样品按: 5L 、4L+IH 、3L+2H 、2L十3H 、lL十4H 、5H 关系各自配制棍合,形成系列评价样品。
(5)难以收集到低限样品,可收集高值样品,用相应稀释液作系列不同程度稀释,形成系列评价样品。
(6)在《线性评价》表格记录检测结果。
结果评价:将数据填入《线性评价》表格,以X表示各样品的预期值,以Y表示各样品的实测值,得出散点图。
若所有实验点呈明显直线趋势,用直线回归对数据进行统计,得直线回归Y=bX+a,若r2>0.95,斜率b在1.00±0.03范围内,可直接判断测定方法在实验所涉及的浓度范围内成线性。
五、用患者标本进行方法比对及偏倚评估实验室准备用一个新的检测系统或测定方法(或新的试剂盒、新仪器进行病人标本测定前,应与原有的检测系统或者公认的参考方法-起检测一批病人标本,从测定结果间的差异了解新检测系统或方法引人后的偏倚。
如果偏倚不大,或者偏倚量在允许误差范围内,说明两检测系统或方法对病人标本测定结果基本相符,新检测系统或方法替代原有检测系统或方法不会对临床引人明显偏倚,这样的实验称为方法学比较实验。
在方法学比较中,常将新方法称为实验方法,与之比较的方法称为比较方法。
试验方法:(1)各种仪器处于良好的工作状态,严格按SOP操作。
(2)检验人员有足够的时间熟悉检测系统的各个环节,熟悉评价方案。
(3)在整个实验中,保持实验方法和比较方法都处于完整的质量控制之下,始终对实验结果有校准措施。
(4)实验时间至少做5天,时间长一些更好,可以客观反映实际情况。
(5)至少做40份病人标本,多一点更好。
(6)尽可能使50%的实验标本分析物的含量不在参考区间内,各个标本分析物含量越宽越好。
(7)不要使用对任一方法有干扰的标本。
(8)每份标本应有足够的量,以便使实验方法和比较方法都能做双份测定。
例如,第l次序号为1 、2..3..4 、5..6 、7 、8 ,第2次序号为8 、7 、6 、5 ,, 4 、3 、2...1 。
两方法都按此实验。
(9)应在2个小时内两种方法对同批标本分别开始实验,最好使用当天采集的标本。
(10)实验结束后,记录数据。
保留原始数据。
结果评价:(1)不采用已明确有人为误差的结果。
(2)将所有无明显误差的实验结果记录下来。
但是,若两种方法结果的各自差值大于任一方法的批内不精密度,应查对标本,并重新实验。
若找不出原因,应保留数据备考。
(3)整个实验一定要有内部质量控制,失控时结果必须重做。
(4)对实验数据的初步筛查:①设比较方法测定结果为X 值,实验方法测定结果为Y 值。
在《方法学比对》表格上录入检测数据,若有40个标本,则有 80个 X 和Y 的结果。
②检查每一方法内现份测定值有无离群表现,先计算每一标本每一方法成对结果的差值和差值的均值。
以4 倍的各方法差值的均值为判断限,各方法内标本的成对差值都应在限值内,说明双份测定结果符合要求。
③若原数据仅40 例病人标本的结果,剔除的数据应另做实验补上。
若有1 例以上需剔除,应检查原因是标本原因,其他数据仍可使用。
无法找出原因,则保留使用所有数据。
若最大差异超过临床允许误差,应从仪器、试剂、方法上寻找原因,停止继续实验。
(5)在《方法学比对》表格上,以X均值、Y 均值和(Y-X)、X作图,通过这两种图了解线性关系,即有无明显离群点,是否呈恒定变异等情况。
如果实验结果具良好线性关系,继续处理数据。
(6)X 、Y 关系实验点有无离群表现先看图在无明显离群点。
若无,可作以后的统计;若有,应对X 、Y 配对值作离群值计算。
将每一个标本两个方法的前后两个测定值一一对应,求出第1 个X 与第1 个Y 的差值和第2 个X 与第2 个Y 的差值,并计算出所有标本总的平均差值,以4 倍的平均差值为判断限值。
所有差值都不应超出限值。
若有,为离群点,仅一点离群点,剔除。
有一点以上离群点,需查原因,判断是否保留数据。
若原因不清,不能随意剔除,全部保留作统计分析,或者用一批新标本重做评价。
凡有剔除的,应另用标本补做。
(7)标本内分析物含量分布是否适当的检验。
相关系数r 常用来表示两个变量间互相关系密切的程度。
在直线回归统计时,除所有实验点和回归线间的离散度会影响r 值的大小外,实验点对应的分析物含量分布宽度也会明显影响r 值的大小。
若实验点过于密集,尽管离散度不大,但r 值偏小。
因此,可用r 检验X 取值范围是否适当。
一般要求r 大于或等于0.975 (或r2大于或等于0. 95) ,认为X 范围是适合的。
若r 小于0.975时,应再多做实验,扩大数据范围。
(8)线性回归统计可用直线回归分析来估计斜率和截距。
数据以回归式Y=bX十a,表示这些数据的直线趋.这是以X 方法为准,Y 方法与之配合的关系式。
式中b 为斜率,a为截距。
两方法理想状态的回归式应为Y=X,即b =1 ,a=0。
根据临床使用要求,可在各个临床医学决定水平浓度 Xc 处,了解Y 方法引人后相对于X方法的系统误差(SE) , SE == | (b -1)Xc + a |。
(9)以美国CLIA’88能力比对检验的分析质量要求允许误差的1/2为判断依据,由方法学比较评估的系统误差(SE)不大于允许误差,认为系统误差在可接受水平内。
备注:1、各个实验室应该根据自己的实际情况,建立性能验证的方法和标准。
该方法适用于科室内所有生化设备的验证。
2、上述试验方案可用于强生 Vitros 系列产品,仅供实验室参考。
参考文献:1、临床检验质量管理技术,冯仁丰,上海科学技术文献出版社2、临床检验方法学评价,杨有业张秀明,人民卫生出版社3、NCCLS, Method Comparison and Bias Estimation UsingPatient Samples; Approved Guideline—Second Edition4、NCCLS,Evaluation of the Linearity of QuantitativeMeasurement Procedures: A Statistical Approach;Approved Guideline5、NCCLS,Evaluation of Precision Performance ofQuantitative Measurement Methods; ApprovedGuideline—Second Edition。
