第十章 醛酮
有机化学第10章醛、酮及亲核加成反应

醛、酮的分子中都含有羰基(>C=O)
O R
H
醛
-CHO 醛基
O
R
R'
酮
>C=O 酮基
分子中的烃基(R)可以相同也可以不相同。醛、酮分子 中的烃基可以是直链的或是环状的,脂肪的或芳香的。
一、羰基的结构
CO
CO
碳原子SP2杂化轨道与另外三个原子以键结合的,所以这 三个键都处于同一个平面上,键角约为120°。
C6H5CHO
NaHSO3 H2O
C6H5CHSO3Na OH
NaCN H2O
C6H5CHCN OH
三、与氢氰酸的加成
醛及多种活泼的酮(脂肪族甲基酮及少于8个碳原子的脂环 酮)与氰基负离子的碳原子发生加成反应,生成-羟基腈.
R CO
(R')H
+ H+ CN-
R OH C
(R')H CN
反应速度受CN-进攻羰基的影响,加入碱,增 加了CN-的解离,促进反应进行.
H3C O
H3C
Ph3P CH2
O
C CH3
Ph3P CH2CH3
H3C H3C
CH2
CH2CH3 C CH3
第三节 α氢的反应
一、 酸性及互变异构 醛、酮的-亚甲基上的氢受到邻位羰基的活化而 呈一定的酸性,可以通过烯醇式表现出来。
HO
CH3 C C
H+
CH3 1
CH3
(酮式)
O
CH3 C C
CH3
O C H CH2
+ H2O
O
O
C
CH
+ H2O
H CH2 CH3
有机化学 第十章 酮和醛 名词解释

第十章酮和醛1.醛:羰基分别与一个烃基和一个氢相连的化合物。
2.酮:羰基与两个烃基直接相连的化合物。
3.酰基:4.单箭头表示均裂,双箭头表示异裂。
5.脂肪族醛、酮亲核加成反应活性次序:6.增长碳链的反应:酮和醛:与氢氰酸加成、与格式试剂反应、与炔金属化合物反应。
7.羟醛缩合:两分子含有α-氢的醛在酸或碱的催化下(最常用的是稀碱),相互结合形成β-羟基醛的反应。
(反应可逆)8.克莱森-施密特反应:芳香醛与含有α-氢的脂肪醛/酮进行交叉羟醛缩合反应生成α,β-不饱和醛/酮的反应。
9.卤代反应:醛/酮在酸或碱催化下,与卤素反应α-氢被卤代(溶剂:四氯化碳、水、醋酸、酸酐、醇)。
10.制备少一个碳的羧酸:卤仿反应。
11.曼尼希反应:含有α-活泼氢的酮与甲醛及胺反应,可以在酮的α为引入一个氨甲基,这个反应也称为氨甲基化反应。
12.制备α、β-不饱和酮:曼尼希反应、克莱森-施密特反应、羟醛缩合。
13.过氧酸氧化反应:酮在酸催化下与过氧酸作用生成酯的反应。
(过氧酸:过氧乙酸、过氧三氟乙酸、过氧苯甲酸、过氧间氯苯甲酸等)14.康尼扎罗反应:无α-H的醛在浓碱作用下可在两分子间发生反应,一分子醛被还原成醇,另一分子醛被氧化成酸。
(也称歧化反应)15.维悌希反应:醛、酮与磷叶立德反应生成烯烃。
(磷叶立德试剂也称为维悌希试剂)。
16.安息香缩合反应:芳醛在氰基负离子催化下,生成α-羟基酮的反应。
(最简单的芳香α-羟基酮称为安息香)。
17.盖特曼-可赫反应:在催化剂(无水三氯化铝和氯化亚铜)存在下,芳烃与氯化氢和一氧化碳混合气体作用,生成芳醛的反应。
18.在乙醛分子的羰基与甲基这几间插入一个或者多个乙烯基,原来的甲基和醛基间的相互影响依旧存在。
19.迈克尔加成:α,β-不饱和醛/酮和碳负离子发生1,4-共轭加成反应。
20.狄尔斯-阿尔德反应:共轭双烯与含有烯键或炔键的化合物反应生成六元环状化合物的反应。
21.制备乙酰乙酸乙酯:烯酮与乙醇反应。
有机化学第二版第十章醛和酮

第十章 醛酮含有羰基的化合物:O H O CH3CCH3 O C CH3醛和酮:CH 3C羧酸 羧酸:CH3CO OHCOOH COOH COOHOH CH3CHCOOHO羧酸衍生物:CH3COCl (CH3CO) ( )2OCOOC 2H 5NHOβ-二羰基化合物:CH3CCH2COOC 2H5CH2COOC2H5 COOC2H5210 醛和酮教学大纲(醛和酮)醛和酮的结构与物理性质 醛和酮的结构与物理性质; 醛和酮的化学性质:1.与氢氰酸加成; 2.与亚硫酸氢钠加成; 3.与醇亲核加成; 4.与氨的衍生物反应; 5.与Grignard试剂加成; 试剂加成 6.醇醛缩合反应; 7 卤化和卤仿反应; 7. 卤化和卤仿反应 还 原 反 应 —— 催 化 加 氢 、 金 属 氢 化 物 还 原 、 Clemmenson 还 原 、 WolffKishner黄鸣龙还原、Cannizzaro反应;氧化反应)。
羰基 carbonylOR C H R O C R'醛(aldehyde)O R C O R C R' Ar H Ar O C O C R H酮(Ketone K t )Oβ αC H(R)CC脂肪族醛、酮芳香族醛、酮α,β-不饱和醛、酮4命名:O CH3CCH2CH2CHOO O CH3CCHCCH3 CH2CH=CH24-氧代戊醛3-烯丙基-2,4-戊二酮OO CHO环己酮CHO2'-氧代环己基甲醛CHO OH O CHO苯甲醛2-羟基苯甲醛 (水杨醛)呋喃甲醛 (糠醛)5z醛和酮的结构2spCσOδ C+δO键角接近 120 °1 C=O双键是由一个σ键和一个π键组成的。
2 羰基碳原子为 sp2杂化轨道与氧原子的 p 轨道和其它两个原子 形成三个 形成 个σ键 键,一个 个 p轨 轨道与氧原子的 与氧 子 p轨 轨道侧面交盖成 侧面交 成π键 键, 氧原子上另有两对孤对电子处于氧的s轨道和p轨道中。
有机化学第10章醛酮

HCN + OH NC
+
CN + H2O C O
慢
质子转移反应
C CN
O
决速步
C CN
O
+
H CN
快
C CN
OH
+
OH
质子转移反应
2.与格氏试剂的加成
• 在格氏试剂的分子中,由于Mg的电正性, 使与其相连的碳原子带部分负电荷,极 易与羰基化合物起亲核加成反应。
H3O
C R
O
C R
OMgX
C R
OH
• 酸催化的卤化反应是通过烯醇式进行的:
O R C H CHR' OH R C C HR' X
+
OH X X _ R O R C CHR' X C CHR' X H
+
X
• 碱催化的卤化反应是通过烯醇负离子进行的:
O R C CHR'
+
O X X R C C HR' X
+
X
• 因此,醛酮在酸碱催化下的卤化实际是卤素对碳碳双 键的亲电加成反应
C O δ C δ O
• 羰基的结构可用共振式表示为:
C O C O
二、醛、酮的分类
• 按分子中烃基的不同分为:
脂肪族醛酮和芳香族醛酮;
• 按分子中烃基的饱和程度:
饱和醛酮和不饱和醛酮;
• 分子中羰基的数目:
一元醛酮,二元醛酮和多元醛酮。
1.普通命名法
• 醛的普通命名法和伯醇类似。
CH3CH2CH2CHO (CH3)2CHCHO C6H5CHO
•
•
• 醛 > 甲基酮>脂肪酮 > 芳香酮 • 环酮 > 脂肪酮
有机化学-第十章

10.2 醛酮的化学性质
如果利用NaHSO3与羰基化合物加成的可逆性,将 NaCN 与 α-羟基磺酸钠作用,使生成的 HCN 与分解出的羰基化合 物加成生成α-羟基腈,这样也可避免 HCN 的直接使用。 例如:
10.2 醛酮的化学性质
醛、酮与碳负离子的加成
Grignard 试剂,炔钠,Wittig试剂等,都含有碳负离子, 它们与羰基化合物的反应活性很高,有机合成上有广泛的 应用。
10.2 醛酮的化学性质
一、与氨、伯胺的反应
脂肪族醛、酮与氨、伯胺的反应可生成亚胺,也称为席夫 碱(Schiff base):
10.2 醛酮的化学性质
脂肪族醛、酮生成的亚胺中含的C=N双键在反应条件下不 是很稳定的,它易于发生进一步的聚合反应。芳香族的醛、 酮与伯胺反应生成的亚胺则比较稳定。
10.1 醛酮的结构及分类
在醛、酮分子中,羰基碳原子是以sp2 杂化状态与其它三 个原子构成键的,羰基碳原子的P轨道与氧原子上的P轨道 以相互平行的方式侧面重叠形成π键,即羰基是一个平面 构型的; 与羰基碳原子直接相连的其它三个原子处于同一平面内, 相互间的键角约为120度,而π键是垂直于这个平面的。
> > >
>
>
>
>
10.2 醛酮的化学性质
一、与水的加成
甲醛、乙醛、丙酮等小分子羰基化合物在水中的溶解性非 常好,这不仅是它们与水分子之间可以形成氢键,还在于 它们可以与水分子发生加成反应,生成了水合物; 这种水合物只有在水溶液中在一定浓度范围、一定的温度 下才是比较稳定的,游离的羰基水合物(同碳二元醇)是 极不稳定的,它将迅速脱水成为羰基化合物。
第十章_醛和酮

O (CH3)2CHCCH(CH3)2 + (CH3)2CHLi [(CH3)2CH]3C-OLi
H2 O
= = =
加成产物
0%
[(CH3)2CH]3C-OH
*2 醛、酮的极限构象式
O S L R
SR
M
O M L
O M
L
S R
(1)交叉式
H2O
OH Ar-C-OH R
-H2O
O ArC-R
ArCOOH + R’MgX
ArCOOMgX
+ R’ H
3 由酰胺和腈制备
NMgBr ArCC10H7- n
-C10H7MgBr
NH
O
H2O
ArCC10H7- n
H+ H2O
ArCC10H7- n
ArCN
HCl
Cl ArC=NH
-H2O
SnCl2
主 2.5 > 4 5 49
: : : :
次 1 1 1 1
Ph H HO R C2H5 H H H
Ph C2H5 OH R
主 499 : 5.6 :
次 1 1
主要产物
次要产物
(2)与HCN的加成
*1 反应式
-OH溶液
(CH3)2C=O + HCN
CH3 CH3
CN H2O CH3 C CH3 O-
亲核加成 氢化还原
O C H
-活泼H的反应 (1)烯醇化 (2) -卤代(卤仿反应) (3)醇醛缩合反应 醛的氧化 (1)碳碳双键的亲电加成
C
H
C=C–C=O
有机化学第10章 醛和酮

Witting反应是在醛酮基碳所在处形成碳碳双键的一个重要方法,产物中 没有双键位置不同的异构体。反应条件温和,产率也较好,但产物双键 的构型较难控制。 Witting也因该工作而与Brown H C共享了1979年的诺 贝尔化学奖。 另一种类型的磷叶立德试剂是霍纳(Horner L)提出的:用亚磷酸 酯为原料来代替三苯基膦与溴代乙酸酯得到的试剂磷酸酯,后者在强碱 作用下形成Horner试剂。
另一种类型的磷叶立德试剂是霍纳(Horner L)提出的:用亚磷酸 酯为原料来代替三苯基膦与溴代乙酸酯得到的试剂磷酸酯,后者在强碱 作用下形成Horner试剂。
补充: 醛、酮与炔化钠的加成
R-CC-Na+ NaNH2 (-NH3) R-CCH +
C=O
NH3(液) 或乙醚
C C ONa CR H O 2
• 醛和脂肪族甲基酮(或七元环以下的环酮)与之反应,生成
• -羟基磺酸钠
白色
过量
在酸碱下可逆反应,分离提纯
-羟基磺酸钠与等摩尔的NaCN作用,则磺酸基可被氰基取代, 生成 -羟基腈,避免用有毒的氰化氢,产率也比较高。
3、与醇的加成
*1 反应情况介绍 ① 与醛反应 CH3CH=O + CH3CH2OH
(hydrazine)
C 6H 5 H C O + H2NNH O2 N NO2
(hydrazone)
C 6H 5 H C NNH O 2N NO2 + H 2O
2,4–二硝基苯肼
O O + H2NNHCNH2
2,4–二硝基苯腙
O NNHCNH2 + H2O
氨基脲
(semicarbazine)
缩氨基脲 (半卡巴腙)
第十章醛和酮

OH 的亲核性比H2O强。 酸催化:
(2)醇
C O ROH, H+ C OH OR ROH, H+ C OR OR
H3C H3C
C
OH
机理:
C O H+
半缩醛、酮 不稳定
C OH ROH C
缩醛、酮
1
(2)脂环族醛酮 羰基在环内称“环某酮” ;羰基在环外,环当作取代基。
O CH2COCH2CH3 CH2CH2CHO
2-甲基环戊酮 1-环己基-2-丁酮 2-methylcyclopentanone 1-cyclohexyl-2-butanone
3-(3,3-二甲基环己基)丙醛 3-(3,3-dimethylcyclohexyl) propanal
σ-p 超共轭 sp →sp ,位阻。
2 3
水合物稳定性:HCH(OH)2 > CH3CH(OH)2 > (CH3)2C(OH)2
苯环的 p-π共轭和体阻分别使醛酮稳定、水合物不稳定。 2°酸碱催化
O CH3CCH3 + H2 O
18 18
OH CH3CCH3 OH
O
18
CH3CCH3
+
H2O
pH = 7,交换很慢;微量OH 或H+,很快达到平衡。
CH2CH3 CH3CH2CHCHCHO CH3 CH3CH=CHCHCOCH3 CH3 (H3C)2HC
CH2CH3
H3C
O H
3-甲基-2-乙基戊醛 2-ethyl-3-methylpentanal
3-甲基-4-己烯-2-酮 3-methyl-4-hexen-2-one
十章节醛和酮

主要内容:
醛酮旳化学性质(II) ▪ 醛酮与醇旳加成——缩醛(酮)旳生成 ▪ 醛酮与胺类化合物旳加成——生成亚胺和烯胺 ▪ Beckmann重排
一. 醛酮旳性质(II)
复习:醛酮与负离子型亲核试剂旳加成
OH
R C CCR
OH RC R
H(R)
(R)H
1. M C C R
OH
1. RMgX 2. H2O
2. H2O
RC H
1. LiAlH4
H(R)
O
or NaBH4
C
R
H(R)
2. H2O
ONa R C SO3H
H(R)
NaHSO3
HCN / NaOH OH
R C CN H(R)
1. 醛酮羰基上旳亲核加成反应(2)
分析:分子型亲核试剂旳特点及与醛酮旳加成
•特点分析
H Nu
H2O
or RMgX
经过烯胺还原制备胺类化合物
NHR CR
2o or 3o 胺
O
C CH2R
HNR'2 H+
R'
R'
N
C CHR
H2 Pd / C
烯胺
R'
R'
N
CH
CH2R
3o 胺
肟类化合物旳Beckmann重排
R
H
C NOH
R'
O
O
R' C NH R or R C NH R'
Beckmann重排
水、醇、胺
H OH H OR H NHR H NR2
✓有活泼 H ✓亲核性不强
•预测:直接与羰基加成
有机化学:第十章 醛 酮(1)
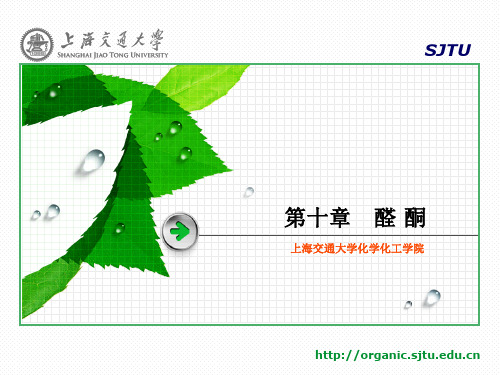
(2) O
O
C OC2H5
H+
O
HOCH2CH2OH
O
O C OC2H5
LiAlH4 (C2H5)2O
O
O
CH2OH H+, H2O
O
CH2OH + HOCH2CH2OH
上海交通大学化学化工学院
(3) 维尼纶:聚乙烯醇含有多个亲水基团,为了提高其耐水性能,可用 甲醛使其部分缩醛化,得到性能优良的合成纤维——维尼纶。
(Ph)3P
- R1 C
R2
上海交通大学化学化工学院
G.Wittg于1953年开始系统研究了它与醛酮的反应,并应用在合 成上。建立了独特的结构和合成方法。
R1 C O + Ph3P C
R2
Ph3P + C
O- C
(Ph)3PO +
R1 CC
R2
缩醛对氧化剂、还原剂、碱稳定,对酸不稳定。
上海交通大学化学化工学院
应用:保护羰基。
(1) CH2 CHCHO
CH2 CH CHO OH OH
2C2H5OH
CH2 CHCH
OC2H5
[O]
OC2H5 H2O
H+, H2O
CH2 CH OH OH
OC2H5 OC2H5
SJTU
第十章 醛 酮
上海交通大学化学化工学院
(一)结构和命名:
1. 结构:
通式:CnH2nO ,醛、酮互为同分异构体。
官能团:
O
O
C H 醛基
C
羰基
碳原子采用sp2 杂化,三个σ键共 平面,羰基碳原子和氧原子上的p轨道 在侧面重叠生成π键 ,氧原子上还有 两对未共用电子。
有机化学第十章醛酮PPT课件

在醇氧化制备醛的过程中,应控制反应条件,如温度、浓度、催化剂 等,以避免过度氧化或其它副反应的发生。
通过醇的氧化制备酮
总结词
醇氧化是制备酮的一种常用方法,常用的氧化剂有高锰酸 钾、硝酸、铬酸等。
详细描述
醇氧化制备酮的反应机理是醇分子中的羟基被氧化成羰基, 同时生成氢离子,常用的氧化剂可以将醇氧化成相应的酮, 同时生成水或其它相应的产物。
醛酮还可以用于合成生物活性分子,如激素、维生素等,对生命过程具有重要影响。
05 醛酮的制备方法
通过醇的氧化制备醛
总结词
醇氧化是制备醛的一种常用方法,常用的氧化剂有高锰酸钾、硝酸、 铬酸等。
详细描述
醇氧化制备醛的反应机理是醇分子中的羟基被氧化成羰基,常用的 氧化剂可以将醇氧化成相应的醛,同时生成水或其它相应的产物。
亲核加成反应
与氢氰酸加成
酮在氢氰酸的作用下,可以发生亲核加成反应, 生成相应的羟基腈。
与水加成
酮在水的作用下,可以发生亲核加成反应,生成 相应的醇。
与醇加成
酮在醇的作用下,可以发生亲核加成反应,生成 相应的酯。
亲电加成反应
与溴加成
01
酮在溴的作用下,可以发生亲电加成反应,生成相应的溴代酮。
与硫酸加成
02 醛的化学性质
还原反应
还原成醇
还原成醇和烃的混合物
在催化剂存在下,醛基可被还原成醇, 如用氢化铝锂(LiAlH4)作为还原剂。
在某些条件下,醛基可被还原成醇和 烃的混合物,如用氢气作为还原剂。
还原成烃
在酸性条件下,醛基可被还原成烃, 如用硫酸铜和亚硫酸氢钠作为还原剂。
氧化反应
氧化成酸
在强氧化剂存在下,醛基可被氧化成羧基,如用高锰酸钾 (KMnO4)作为氧化剂。
第十章醛和酮

第十章 醛和酮学习要求1.掌握羰基(碳氧双键)和碳碳双键的结构差异及其在加成上的不同。
2.掌握醛酮的主要制法。
3.熟练掌握醛酮的化学性质,理解亲核加成反应历程。
4.掌握醛与酮在化学性质上的差异,如氧化反应、歧化反应等。
醛和酮都是分子中含有羰基(碳氧双键)的化合物,羰基与一个烃基相连的化合物称为醛,与两个烃基相连的称为酮。
§11.1 醛、酮的分类,同分异构和命名 11.1.1 分类醛 酮RC R'OR C R'OR C HO ( RCHO )( )醛酮CH 3CH 2CH 2CHOCH 3CH 2-C-CH 3OCHO O CHO3OCH 3CH=CHCHO CH 3CH=CH-C-CH 3OCH 2CHO CH 2CHOOCH 3-C-CH 2-C-CH 3OO脂肪醛脂肪酮脂环醛脂环酮芳香醛芳香酮不饱和醛不饱和酮二元醛二元酮11.1.2 同分异构现象醛酮的异构现象有碳连异构和羰基的位置异构。
11.1.3 醛酮的命名选择含有羰基的最长碳链为主链,从靠近羰基的一端开始编号。
例如:碳原子的位置也可用希腊字母表示。
例如:§11.2 醛、酮的结构、物理性质和光谱性质 11.2.1 醛、酮的结构醛酮的官能团是羰基,所以要了解醛酮必须先了解羰基的结构。
CH3-CH-CH 2CHOC 6H 5-CH-CHOCH 3CH 3CH3-C=CHCH 2CH 2-CH-CH 2CHOCH 2CH 3CH 3CH 2-C-CH 2CH 3CH 3-C-CH 2-C-CH 3OOOH 3CO甲基丁醛苯基丙醛二甲基 辛醛戊酮戊二酮甲基环戊酮32,433,7623C-CH 2CH 3C-CH 3COCH 2CH 2CH 3OO环己烯酮环己基丙酮苯基 乙酮萘丁酮α111112C C C COHCH 3CH=CHCH 2CHOβ丁烯醛O116.5。
杂化键键近平面三角形结构πσC=O = σ+π 与 相似 C=O 双键中氧原子的电负性比碳原子大,所以π电子云的分布偏向氧原子,故羰基是极化的,氧原子上带部分负电荷,碳原子上带部分正电荷。
有机化学课件第十章 醛酮.ppt

英文名称: 醛将相应简单酸中基本词尾“ic acid”去掉, 然后加aldehyde;酮用ketone做母体表示;酮与苯相连时, 称为酰基苯,将羧酸词尾“ic acid”去掉,后加上 “ophenone”:
CH3COCH2CH3
教学重点和难点 1. 醛酮的命名 2 醛酮的亲核加成反应
3. 醛酮常见的基本反应
教学内容
一. 醛酮的结构和分类 二. 醛酮的物理性质 三. 醛酮的化学性质
1. 羰基的亲核加成反应 2. 不饱和醛酮的的加成反应 3. 羰基还原反应 4. 活泼氢的反应 5. Favorshi重排 6. 二苯乙醇酸的重排 7. 叶立德的反应 8. 氧化反应
甲(基)乙(基)(甲)酮 ethyl methyl ketone
CH2=CHCHO
丙烯醛 acrylaldehyde
BrCH2CH2CH2CHO
-溴丁醛 - bromobutyraldehyde
O C CH3
乙酰苯(习惯称苯乙酮) acetophenone
Cl CH3CHCOCH2CH2Cl
-氯乙基 -氯乙基酮 - chloroethyl - chloroethyl ketone
第十章 醛 酮
Aldehydes and Ketones
黑龙江大学化学化工与材料学院 School of Chemistry and Materials, Heilongjiang University
教学目的和要求
1. 掌握醛酮的结构特点和命名 2. 掌握醛酮的化学性质。 3. 掌握醛酮的基本反应与鉴别方法。 4. 了解醛酮的主要制备方法和重要用途。
上述不发生正常加成反应原因,是酮主要发生“烯醇化”和“还原” 两个副反应。
《有机化学》第十章 醛酮的结构与性质

第十章醛酮的结构与性质引言醛酮分之中都会含有羰基( ),羰基中碳原子是sp2杂化的,三个杂化轨道形成三个δ键,其中一个是和氯形成的δ键。
这三个键在同一平面上,彼此间理论键角为120°,但由于三个键所连基团不同,相互作用有差别,因此键角和理论值略有出入。
碳原子和剩下的一个轨道和氧原子的轨道重叠形成Л键,因此羰基是由一个δ键和一个Л键所组成的碳氧双键,如图:图10.1羰基的结构及其电子云示意图羰基中碳氧双键与烯烃中碳碳双键不同,是极性的双键(由于氯原子的电负性比碳大),成键电子云密度在氧原子处较高,氧原子带部分负电荷(δ-),而碳原子处电子云分布较低,因而带部分正电荷(δ+)。
极性碳氧双键易受到带负电荷或孤对电子的试剂(即亲核试剂)的进攻,发生亲核加成反应,这是羰酮经典的反应之一。
羰基是极性基团具有较强的吸电子诱导反应,因而羰基的α-H具有一定的“酸性”,在碱性条件下离去后形成碳负离子,作为亲核试剂与另一分子的醛(或酮)发生醇醛缩合(或醇酮缩合)反应。
另外醇酮的羰基易发生氧化还原反应。
10.1 亲核加成反应醛酮的亲核加成反应是其经典的反应之一,可用下列通式表示:在反应过程中,首先是试剂的亲核部分(Nu-)向羰基碳进攻,形成负氧离子,再与带正电荷的亲电部分(A+)结合。
影响亲核加成速度主要是电子效应和空间效应。
羰基碳原子的正电性的高低决定反应速度的快慢,吸电子取代基加快反应进程,供电子取代基减慢反应进程。
由于在决定反应速度的步骤中碳原子由于sp2杂化转变为sp3杂化,键角变小,基团的排斥作用增强,因此羰基所连的基团的大小也对反应速度产生影响。
基团越大,空间位阻越大,反应速度越慢。
下列醛酮的亲核加成反应活性由强到弱的顺序为:(1)(2)10.1.1含氧亲核试剂的加成反应1.与水的加成反应水和醇都是含氧的亲核试剂。
在一定的条件下水可与醛酮的羰基加成形成水合物,但是水合物极不稳定,很易失水:(平衡主要偏向反应物方向)只有活性较强的醛的水合物较稳定,如甲醛在水溶液中几乎全部以水合物形式存在,但不能分裂,而三氯乙醛的水合物其吸收光谱图表明不含羰基:水合氯醛2.与醇的加成反应:在干燥的HCl作用下,醛与等摩尔的醇亲核加成生成半缩醛,半缩醛可与另一摩尔的醇发生反应,生成缩醛:半缩醛缩醛缩醛对碱和氧化剂都很稳定,在有机合成中常用此反应来保护醛酮。
第十章 醛、酮、醌-1(1~30〕

有的反应不必加酸催化,如:甲醛与氨的反应;甚至有的反 应可加强碱,如:NH2-OH与酮加成时,可用KOH催化:
-OH NH2OH
-H2O
NH2-O-
NH-OH
NH-OH 负离子更有利于对羰基的进攻。所以,这类反应根据 反应物对方的性质,可决定反应介质的酸碱度。
(a) 与 NH3 的反应
胺 胺与与胺甲甲醛与氨醛反甲反与应醛应甲,反,生醛应生成,反成一生应一个成个结 ,能一结 构个生很构结成特很构殊特 一很的殊个特笼的殊结状笼的晶构状笼体很晶状化体 特合晶化物殊体合 :化的物合笼:物状:晶体化合物:
电荷的碳稳定,在发生反应时,反应是分两步 进行的。首先,带负电荷的原子或原子团加成到带正电荷的羰 基碳上,然后带正电荷的原子或原子团加成到羰基氧原子上。 我们称富有电子的试剂为亲核试剂,而由亲核试剂进攻引起的 加成反应叫做亲核加成反应。
醛、酮的典型反应是亲核加成反应。
1、 与 HCN 的反应 HCN 对醛、酮的羰基发生加成反应,生成α-羟基腈:
SO3Na
稀HCI
R CH3 H C=O + NaCl+ SO2 + H2O
所以,此反应是纯制醛或酮的方法之一。
另外,α-羟基乙磺酸钠与 NaCN 作用,能够生成羟基腈,以 避免使用 HCN (挥发性大,毒性大),是合成羟基腈的好方法。
例:
dl-苦杏仁酸
4、 与醇的加成
在少量干燥HCl气体作用下,等摩尔的醇与醛进行加成 反应,生成半缩醛,而大多数半缩醛是不稳定的化合物,容 易失醇发生逆反应;但半缩醛也可与醇继续反应生成缩醛。 缩醛比较稳定,可以分离出来:
OO HCCH
乙二醛
O
O
1,3-环己二酮
有机化学 key note ch10 第十章 醛 酮

O R C Cl + R'MgCl
OMgCl
乙醚 低温
O
H2O
R
C R'
Cl
R
C
R'
格氏试剂与二氯化镉作用,生成有机镉化合物,当烃基是芳基或一级烷基时,就可以将 酰氯还原得到高产量的酮:
RMgCl +CdCl2
RCdCl
+
RCdCl
苯 温热
+
MgCl2
R'COCl
R'COR + CdCl2
二烃基铜锂与酰氯反应也可制备铜,在低温条件下与酮反应很慢,与酯、腈、卤代烷不 反应,如:
ArCHO + HCHO
3. 醛、酮的制备 (1)醇的氧化和脱氢
△
ArCH2OH + HOONa
RCH2OH
C5H5NH CrO3Cl (PCC) CH2Cl2
RCHO
O
OH
Na2Cr2O7 H2SO4
(2)用芳烃氧化
C6H5CH3
MnO2
C6H5CHO
(3)由羧酸衍生物还原 三特丁醇铝锂[LiAlH(Ot-Bu)3]和二异丁基铝锂[i-Bu2AlH 或 DIBAL-H]也是现代实验室 常用的还原剂,它们的还原活性小于 LiAlH4,可以把酰氯、酯、腈还原为醛:
O RCH2C H
+
RCH H
CHO
10%NaOH 5 0C
RCH OH
CHCHO R
RCH
CCHO R
CH3 PhCHO
+
CH3CHO
OH
PhCH OH
CH2CHO
OH100C
PhCH
中药学课件第第十章 醛和酮
反应可逆,缩醛或缩酮是在酸(无水)催化下形成的,
若有水(稀酸)存在又可分解成原来的醛、酮。但缩醛、
缩酮对碱和氧化剂是稳定的。因此,在有机合成上常利用
这一性质来保护羰基、羟基。
22
应用举例:
例一 将 CH2 CH CHO 转化成 CH2CHCHO OH OH
2 C2H5OH
OC2H5
CH2 CH CHO
空间位阻影响(反应1h):
丙酮
丁酮
3-戊酮
产率: 56.2 % 36.4 % 2 %
苯基影响也较大,与芳香酮几乎不反映,如:苯乙酮1%
*** 加成产物a-羟基磺酸钠与氰化钠作用生成a-羟腈。 这样可避免直接使用剧毒的HCN。
O CH3CCH3 + NaHSO3
OH
OH
CH3 C CH3 NaCN CH3 C CH3
核试剂亲核性的强弱,羰基碳原子亲电性的强弱,羰基
碳上取代基的大小。
12
空阻大(立体因素)、给电子基团(电性因素),降低羰 基碳的正电性,使反应活性降低。
O HCH
O RCH
O RCR'
O RCAr
O
O
O
O
CH
CH
C CH3
C
反应性下降
不同结构的醛、酮的亲核加成反应的活性顺序为:
O
O
O
O
O
H C H > CH3 C H > CH3 C CH3 > CH3 C R > R C R
第十章 醛和酮
分子中含有羰基(carbonyl)(羰基化合物)
饱和醛、酮的通式:CnH2nO。
HCHO O RCHO O
HCH
有机化学第十章 醛酮

• 在稀碱的作用下,两分子的醛(酮)相互作用,
生成β-羟基醛(酮)的反应称为羟醛缩合。
含α-氢的醛或简单酮 ✓ 可两分子缩合(亲核加成) ✓ 得到β-羟基醛或α,β-不饱和醛
O
OH
CH3CH
O
O CH3CH CH2CH
O CH3C
H
O CH2CH
H2O
OH
O
CH3CHCH2CH
O CH3CH CHCH
亲核加成 R
O-Na+
C
H
SO2OH
硫比氧有更强的亲核性
III)用 途
i) 鉴别醛酮:
例1:
O C-CH3
x
饱和NaHSO3
CH2CHO
白
所有的醛、脂肪族甲基酮、八个碳以下的环酮
(丙) 与醇加成
R
干HCl
CO
H
R'OH
R OR' 干HCl C
H OH R'OH
半缩醛
R OR' C
H OR'
缩醛
R C O + HO CH2 干HCl
C-NH-Y -H2O OH
C=N-Y
失水(消去)
(1). 与胺作用生成希夫碱(Schiff base)
(Ar)R C
H2N
O
R''
(Ar)R OH C
H2O (Ar)R C NR''
(R')H
(R')H NHR''
(R')H
只有伯胺可发生此反应
希夫碱
(2). 与羟胺(H2N-OH)作用生成肟
R C O H2N OH (R')H
自行整理第十章醛酮重要知识点总结

与水加成
可用有机锂代替,其亲核性比格利雅试剂强,锂原子体积小,几乎无副产物产 生
酸碱催化的区别:酸催化是通过生成qiang盐以强化羰基碳原子的缺电子性;碱催化 (如OH-)则是使醇转化为烷氧负离子以增强其亲核能力。 半缩醛是不稳定的化合物,在酸催化下与醇发生反应生成同碳二元醚即缩醛。 缩醛只能在酸催化条件生成。 由于缩醛或缩酮是稳定的醚型结构,反应是可逆的,所以在有机合成中可以用于 保护羰基。
在生成的三卤基酮中,由于三卤甲基-I效应使羰基碳原子缺电子加剧,与OH-迅速 发生亲核加成,而后离去CH3-,生成卤仿和少一个碳原子的羧酸。 如果所用的卤素为碘,则生成碘仿(黄色沉淀),称为碘仿反应,反应现象十 分明显,可用于甲基酮的鉴别。
含有α-H的脂肪醛在碱的作用下可以形成它的烯醇式负离 子,它对另一醛的羰基进行亲核加成,生成β-羟基醛,这 就是羟醛缩合反应。 β-羟基醛含有α-H容易脱水,如不含有,不发生脱水。 应用:制备碳链增长的羟基醛、不饱和醛。
不羟氨的反应亏的生成及贝克曼重排芳香族酮亏用浓硫酸或pcl5处理収生分子内重排结果是氮原子上的羟基不处于双键碳原子异侧的基团互换位置生成一个烯醇型中间物然后转化为酰胺这种酮亏的反应重排称为贝克曼重排
第十章醛酮重要知识点总结
本章重点掌握以下几点
① ② ③ 醛酮的结构 反应类型 亲核加成 α-H的反应 氧化还原反应 反应机理 插烯规律
与亚硫酸氢钠的加成 条件:醛、脂肪族甲基酮以及少于8个碳的环酮可以与亚硫酸氢钠的 饱和溶液发生亲核加成,反应是可逆的,生成的产物是α-羟基磺酸钠, 它不溶于反应体系析出,这个反应是生成磺酸化合物的一种方法。 注意:环脂酮与NaHSO4加成的反应活性顺序。P356
与氢氰酸加成 条件同上 由于氢氰酸有剧毒,且易于挥发,在实际操作中是用KCN或NaCN的溶 液与醛或酮混合,然后逐步加入无机强酸,如硫酸,生成的HCN立即 与羰基加成,得到产物。 加入微量的碱能使反应迅速完成,加入酸则反应相当缓慢;这是因为 氢氰酸是一个弱酸,它在水中的解离常数很小,加入碱,生成CN-, 从而促进了加成反应。 应用:这个反应在有机合成中可用于制备增加一个碳原子的α-羟基腈, α-羟基腈可进一步转化为α-羟基酸、α,β-不饱和酸以及胺化合物。 可用于制备甲基丙烯酸甲酯(有机玻璃的单体)。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
OR' R-CH-OR' H2O/H+
缩醛 对碱和氧化剂稳定
O R-C-H + 2R'OH
所以,制备缩醛时必须用干燥的HCl气体,体系中不能含水。
反应机理
R H
CO R'
R
R"OH H OR"
C OH
R C OH
R'
R'
H
OR"
H
OR"
R C OH
R C OH2
R'
R'
H2O
OR" R"OH
OR"
羟醛缩合反应在合成中的应用:
合成碳链增长的化合物
例如: 由不多于三个碳的原料合成
CH2OH
CHO
CHO
(C2以下的有机原料任选)
CHO
CH3CHO
H2 Ni
CHO
2分
O H+
O
H2O
1分
OH
O
OH
H+
O
1分
CHO
1分
(丙) 卤化反应和卤仿反应
✓在酸或碱的催化下,醛和酮的α-H可以被卤代 ✓酸催化下只发生一取代 ✓碱催化下可发生多取代,直至发生卤仿反应
II) 反应范围:
所有的醛、脂肪族甲基酮、八个碳以下的环酮。
下列化合物中,哪个不能与饱和 NaHSO3水溶液发生加成反应?
O
O
(A) CH3COCH3
(B) CH3COCH2CH3
(C)
(D)
反应机理
R C=O +
H
HO O-Na+ S
O
分子内的
酸碱反应 R
OH
C
H
SO3Na
亲核加成 R
O-Na+
强碱
或C6H5Li
醛或酮
磷叶立德
烯烃 氧化三苯基膦
醛、酮与磷叶立德反应,是制备烯烃的重要方法之一: 例:
• 1)产物中亚甲基碳所占的位置就是羰基氧的位置;
反
没有双键位置不同的异构体。
应 特 点
• 2)反应条件温和,产率较高;可以合成一些用其 它方法难以合成的烯烃。
• 3)维蒂希试剂对水和空气都不稳定,制得到后无 需分离即可以直接用于下一步的反应。
NH2OH NH2NH2
羟胺
肼
O2N
NHNH2
NO2
2,4-二硝基苯肼
NHNH2
苯肼
O NH2NHCNH2
氨基脲
反应通式
C=O + H2N-Y
亲核加成
C-N+H2-Y O-
C-NH-Y -H2O OH
C=N-Y
失水(消去)
(1). 与胺作用生成希夫碱(Schiff base)
(Ar)R C
H2N
O
OH
CH3CH
O
O CH3CH CH2CH
O CH3C
H
O CH2CH
H2O
OH
O
CH3CHCH2CH
O CH3CH CHCH
OH
2 CH3CH2CH2CHO
OH O CH3CH2CH2CHCHCH
CH2CH3
CH3CH2CH2CH
O CHCH CH2CH3
下列化合物能发生羟醛缩合反应的是
O A
O
O
CH3 C CH2 C CH3
OH
O
CH3 C CH C CH3
可与FeCl3发生颜色反应
(乙) 羟醛缩合反应
R
O C
[ H
B-
CHR'
R
O 碳负离子
] _
C CHR'
亲核试剂
OH R C CHR'
• 在稀碱的作用下,两分子的醛(酮)相互作用,
生成β-羟基醛(酮)的反应称为羟醛缩合。
含α-氢的醛或简单酮 ✓ 可两分子缩合(亲核加成) ✓ 得到β-羟基醛或α,β-不饱和醛
缩氨脲
反应特点:
a. 反应在酸催化下进行(pH≈4)
b.加成缩合产物都为结晶,通常用来鉴别醛和酮 c.在稀酸条件下能够水解为原来的醛和酮 可以分离和提纯醛和酮
R CO
(R')H
H2N NH
R C N NH
(R')H
苯腙
稀HCl
R
C (R')H
O
+
H2N NH
(戊) 与金属有机试剂加成
I)加RMgX
① 醛的活性大于酮;脂肪族醛、酮大于芳香族醛、酮。
HCHO>CH3CHO>ArCHO>RCOR>ArCOAr
空间效应
② 对于芳香族的醛酮而言,对位吸电子基团使羰基C的 电正性增加,有利于亲核试剂的进攻。
O2N
CHO >
CHO > CH3
电子效应
CHO
比较下列化合物羰基上亲核加成的活性大小
(A) CH3CHO
-OH (CH3)2C=O + HCN 溶液
CH3 CH3
C
CN H2O CH3
O-
CH3
C
CN OH
-羟腈(或-氰醇)
H+ H2O
CH3 C COOH
CH3
OH
-羟基酸
-H2O
CH2=C-COOH CH3
,-不饱和酸
有机玻璃制品
相框
纸巾盒
课堂习题
1.
b
2. 下列化合物和HCN亲核加成反应速度顺序( )。
H2O/H+
C(CH3) 2 OH
OH
CH3CHCH3
KMnO4
O
CH3CCH3
OH
PBr3
Br
Mg 醚
O CH3CCH3
醚
H3+O
产物
II). 加有机锂
有机锂的亲核性和碱性均比格氏试剂强。 例如下列反应格氏试剂不能发生:
(CH3)3CLi + (CH3)3C-C-C(CH3)3 O
乙醚
-60。C
C=O
RO R'
m=2.8D
m=1.3D
溶解度:
与醇相似。低级醛、酮可溶于水;高级 醛、酮不溶于水。
因为醇、醛、酮都可与水形成氢键:
10.4 醛和酮的化学性质
➢亲核加成,还原。
O
C C H(R)
氧化
H
✓活泼α-H的反应
1 羰基的亲核加成
(甲) 与氢氰酸加成 (乙) 与亚硫酸氢钠加成 (丙) 与醇加成 (丁) 与金属有机试剂加成 (戊) 与氨的衍生物加成缩 (己) 与Wittig试剂加成
C=O + R-Mg X 干醚 R-C-OMgX H2O/H+
烷氧基卤化镁
R-C-OH
CH2O
RMgX
H2O
R CH2 OH
1o 醇
R'CHO
O
C
R'
R''
RMgX RMgX
H2O
H2O
水解
OH R' CH R
OH R' C R
R''
2o 醇 3o 醇
例:由环己醇和丙烯为原料合成
CH3CH=CH2
O
O
O
a.
C H;
b. H3C C
; c. H3C C
解答:a>b>c。此题主要考虑亲核加成速度 与羰基活性的关系(电子效应,位阻效应)
(乙) 与亚硫酸氢钠加成
R C=O + NaHSO3
H
R OH
H
H
C
H
SO3Na
α-羟基磺 酸钠
C=O or OH
R
I) 反应活性: 似与HCN的加成。(醛>酮、脂肪族>芳香族)
合成用NaOCl, 氧化性强,且价格低廉。
5
4
3
21
CH3CH2CH2CHCHO
CH3
(2-甲基戊醛α-甲基戊醛)
说
明
醛基总是处在链端,命名时不需要标出它的位子。 酮的羰基是在碳链的中间,命名时必须标出羰基的位子
10.3 醛和酮的物理性质
沸 点:与分子量相近的醇、醚、烃相比, b.p:醇>醛、酮>醚>烃。为什么?
原因:a. 醇分子间可形成氢键,而醛、酮分子间不能; b. 醛、酮的偶极矩大于醚、烃的偶极矩:
CHO B
C (CH3)3CCHO
D
CHO
O
(1) 交叉羟醛缩合
若两分子都含α-H的不同醛发生羟醛缩合,产物为混合物 无合成意义
若一分子含α-H,另一分子不含α-H的醛相互缩合 可得到合成产物
CHO
NaOH
CH3CHO
CH CHCHO
肉桂醛
历程:
O HH O
H2O
O OH-
O OH
H2O
O
OO O
(1) 卤化反应(酸催化):
O
H
CH3CH2CH
OH
H
CH3CH2CH
OH CH3CH CH
OH
Br2
Br
CH3CH CH
HBr
Br
O CH3CHCH
Br
O
CH3-C-CH2-H
(2) 卤仿反应 (碱催化下)
O
OH慢
CH3-C-CH2-
O-
CH3 C CH2 + H2O 活性更高!
X-X
O CH3-C-CH2-X
H2O
3)3C]3C-OH
体积大
三叔丁基甲醇
课堂习题
1、试分离2-戊酮、3-戊酮的混合物。
