生物化学重点_第八章 生物氧化和能量转换教学提纲
医学生物化学(第八章)生物氧化

* 铁硫蛋白为单电子传递体 ( Fe2+-e Fe3+)
+e
20
3. 泛醌(ubiquinone , Q) 又称辅酶Q (Coenzyme Q , CoQ)
21
**泛醌的特点 1)是双电子传递体 2)不与蛋白结合的游离存在的电子载体 3)是复合物Ⅰ、Ⅱ、Ⅲ之间的连接者,
是多种底物的电子进入呼吸链的中心点
53
四、 ATP与能量的释放、储存和利用
H2O+CO2 ATP
有机物氧化 产能
生物大分子 主动
合成
运输
肌肉 收缩
遗传信 息传递
O2 ADP+Pi
54
一、 ATP分子中的高能磷酸基的来源 (一) 氧化磷酸化: 主要来源 (二) 底物水平磷酸化 概念: 在反应过程中,由于分子内部能 量重新分配,形成高能磷酸化合物,进一 步将高能磷酸基转移给ADP,形成ATP
67
AH2
2H+
2Cu2+
O2-
H2O
A 2Cu+
1/2O2
属氧化酶主要有:细胞色素氧化酶、 酚氧化酶、 抗坏血酸氧化酶等
68
(二)需氧脱氢酶 (aerobic dehydrogenase)
特点: 使作用物氢活化, 受氢体:除氧以外还有其他试剂 产物之一是H2O2
69
AH
FMN(FAD)
H2O2
氧化磷酸化
4
糖
脂肪
葡萄糖 脂肪酸 + 甘油
乙 酰CoA
蛋白质
氨基酸
TCA cycle
CO2
H++e (进 入 呼 吸 链 )
生成H2O 及释 放 出 能 量
5
生物化学课件(生物氧化和能量转换)

NAD+ + 2H NADP+ + 2H
NADH + H+ NADPH + H+
NAD(P)+的结构
2. 黄素蛋白:是指几种以黄素核 苷酸(FMN或FAD)为辅基的酶
代谢物
FMN/FAD
已氧化代谢物
FMNH2/FADH2
3. 铁硫蛋白:无机硫原子和/或蛋白质Cys残基的硫原子 相连。铁-硫中心(Fe-S)最简单的是单铁原子与4个Cys 的-SH相连,更复杂的是有2个或4个铁原子
and in a cell!
线粒体的跨膜转运系统:线粒体外胞液中NADH跨 膜转运
1. 苹果酸-天 冬氨酸穿梭: 主要存在于 哺乳动物的 肝脏、肾和
心肌中
2. 磷酸甘油穿 梭:昆虫的飞 翔肌中大量存 在。哺乳动物 中主要存在于 肌肉和脑组织
中
电子传递链的主要组分
1. 烟酰胺腺嘌呤核苷酸NAD+和NADP+:是许多脱氢酶的 辅酶
型,半醌型和还原型。
CoQ不仅接受NADH脱氢酶的H,还
接受线粒体其他脱氢酶的H,如琥
珀酸脱氢酶,脂酰CoA脱氢酶及其
他黄素脱氢酶脱下的H,在电子传
递链中处于中心地位。
氢醌
氧化型泛醌 半醌自由基
5. 细胞色素:是一类含铁卟啉(血红素)辅基的蛋白 质。根据其吸收光谱的不同,可分为a,b,c三类。
Fe3+ + e
电子走向:琥珀酸→FADH2→ Fe-S →Cyt b560 →CoQ
3. 复合物Ⅲ:CoQ-细胞色素C氧化还原酶 含有:1)细胞色素b、c1 2)铁硫蛋白: 含有铁硫簇Fe-S
电子走向:CoQ →Cytb→ Fe-S →Cytc1 →Cytc
生物化学 生 物 氧 化和能量转换课件

解偶联动画
主菜单
㈠ 抑制剂 3.氧化磷酸化抑制剂
三.影响氧化磷酸化的因素
既抑制氧的利用又抑制ATP的形成,但不 直接抑制电子传递链上载体的作用。
返回
主菜单
三.影响氧化磷酸化的因素
㈡ ADP的调节作用
[ ADP]增高,氧化磷酸化加快。
㈢ 甲状腺激素(T3) T3 诱导Na+,K+-ATP酶生成→ADP↑→氧化磷酸化↑ T3 →使解偶联蛋白基因表达增加→耗氧及产热↑
图
返回
主菜单
㈡ 氧化磷酸化偶联机制 2.ATP合成酶 (ATP Synthase)
ATP合成系统中成功的重组实验证明膜囊泡 上电子传递链的酶系,而且含有将电子传递 链与氧化磷酸化连接起来的偶联因子的酶。 ATP合成酶又称复合体Ⅴ(complex V),有 合成ATP的功能。
㈠ ATP合酶的结构 ㈡ ATP合酶工作机制
二、过氧化物酶体中的氧化酶类
㈠ 过氧化氢酶(触酶) 过氧化氢酶
2H2O2
2H2O + O2
㈡ 过氧化物酶
过氧化物酶
R + H2O2
RO + H2O
过氧化物酶
RH2 + H2O2
R + 2H2O
主菜单
三、超氧化物歧化酶 43; 2H+
H2O2 + O2
H2O2 或ROOH
E°'低的化合物失电子能力强, 处于呼吸链前端;
E°'高的化合物得电子能力强, 处于呼吸链后端。
而分子氧E°’数值最大, 处于末端。
主菜单
(2H)
NADH
NADH
FADH
(Fe-S-Pr)
(2H)
生物化学 第8章 生物氧化

天冬 氨酸
①苹果酸脱氢酶
②天冬氨酸氨基转移酶
存在部位:肝脏、心肌组织
两种穿梭系统的比较
α-磷酸甘油穿梭 穿梭 物质 进入线粒 体后转变 成的物质 进入 呼吸链 α-磷酸甘油 磷酸二羟丙酮 苹果酸-天冬氨酸穿梭 苹果酸、 谷氨酸 天冬aa、α-酮戊二酸
FADH2
琥珀酸 氧化呼吸链
NADH+ H+
NADH 氧化呼吸链
琥珀酸由琥珀酸脱氢酶催化脱下的2H经复合 体Ⅱ(FAD,Fe—S)使COQ形成COQH2, 再往下传递与NADH氧化呼吸链相同。(见 上图)
NADH氧化呼吸链和琥珀酸氧化呼 吸链总图
FADH2
NADH
FMN
CoQ
Cyt-b c1
c
aa3
O2 H2O
3、分别进入两条呼吸链的底物
苹果酸 异柠檬酸 β -羟丁酸 谷氨酸 NAD+ FMN 琥珀酸 FAD(Fe-S) CoQ b c1 c aa3 O2
10
血红素b、c1 Fe-S 血红素c 血红素a 血红素a3 Cu2+ O2
Q
Cytc
13
1
Cytc Cyta
Ⅳ
细胞色素C氧化酶
13
(一)尼克酰胺核苷酸类(NAD+)
NAD+ 和NADP+的结构
NAD+:R=H NADP+:R=PO32-
尼克酰胺核苷酸的作用原理
H
H H CONH 2
C CONH2 N R
AH2 2H(2H++2e)
吸 链
1 2 O2
H2O
氧化
A
ADP+Pi
能量 ATP 磷酸化
第八章 生物氧化和能量转换

(biological oxidation)
• 生物氧化概述
• 线粒体及其内部氧化体系
• 氧化磷酸化作用
• 其他末端氧化系统
第一节 生物氧化概述
一、生物氧化的基本概念
• 生物氧化(biological oxidation):细胞内的糖、脂肪和 蛋白质进行氧化分解而生成 CO2 和 H2O ,并释放能量的过 程。 • 又称为细胞氧化或细胞呼吸、组织呼吸。
3. 铁硫蛋白(铁硫中心)
是一类金属蛋白质,在生物氧化中起传递电子的作用。分 子中含有非血红素铁和对酸不稳定的硫。根据所含铁原子 的数目不同,可将铁硫蛋白分为2Fe-2S、4Fe-4S。利用铁 的化合价的改变来传递电子。
4. 泛醌
泛醌(辅酶Q,CoQ,Q)是游离存在于线粒体内膜中的 脂溶性有机化合物,由多个异戊二烯连接形成较长的疏水 侧链,氧化还原反应时可在醌型与氢醌型之间相互转变, 因此是递氢体。
• CO2 如何形成? 直接脱羧、氧化脱羧 • H2O 如何形成? 脱氢酶、氧化酶、传递体 • 能量如何形成?
生物氧化的一般过程
糖原 甘油三酯 蛋白质
葡萄糖
脂肪酸+甘油
氨基酸
乙酰CoA
TCA
CO2
ADP+Pi
ATP
2H
呼吸链
H2O
二、生物氧化的特点
(与体外燃烧相比)
(1)生物氧化是在细胞内进行的;
生物氧化过程中水的生成
五、自由能和氧化还原电位
自由能:一个化合物分子结构中所固有的能量,是指能用于 做功的能量。 1878年,Josiah Willard Gibbs提出关于自由能的公式。 △G为在恒压和恒温下发生变化的体系的自由能的变化。反 应的自由能变化(△G)是反应能否自发进行的重要标准。
生物化学三大代谢重点总结

第八章生物氧化1. 生物氧化:物质在生物体内进行氧化称生物氧化,主要指糖、脂肪、蛋白质等在体内彻底分解时逐步释放能量,最终生成C02和H2O的过程。
2. 生物氧化中的主要氧化方式:加氧、脱氢、失电子3. CO2的生成方式:体内有机酸脱羧4. 呼吸链:代谢物脱下的成对氢原子通过位于线粒体内膜上的多种酶和辅酶所催化的连锁反应逐步传递,最终与氧结合生成水,这一系列酶和辅酶称为呼吸链,又称电子传递链。
组成(1) N ADH 氧化呼吸链:苹果酸-天冬氨酸穿梭NADH —复合物I —CoQ —复合物III —Cyt c —复合物IV f O 产2.5个ATP(2) 琥珀酸氧化呼吸链:3-磷酸甘油穿梭琥珀酸—复合物II —CoQ —复合物III —Cyt c —复合物IV —O 产1.5个ATP含血红素的辅基:血红蛋白、肌红蛋白、细胞色素、过氧化物酶、过氧化氢酶5. 细胞质NADH 的氧化:胞液中NADH必须经一定转运机制进入线粒体,再经呼吸链进行氧化磷酸化。
转运机制(1 ) 3-磷酸甘油穿梭:主要存在于脑和骨骼肌的快肌,产生 1.5个ATP(2 )苹果酸-天冬氨酸穿梭:主要存在于肝、心和肾细胞;产生2.5个ATP6. ATP的合成方式:(1 )氧化磷酸化:是指在呼吸链电子传递过程中偶联ADP磷酸化,生成ATP,又称为偶联磷酸化。
偶联部位:复合体I、III、IV(2 )底物磷酸化:是底物分子内部能量重新分布,通过高能基团转移合成ATP。
磷/氧比:氧化磷酸化过程中每消耗1摩尔氧原子(0.5摩尔氧分子)所消耗磷酸的摩尔数或合成ATP的摩尔数。
7. 磷酸肌酸作为肌肉中能量的一种贮存形式第九章糖代谢寸一、糖的生理功能:(1 )氧化供能(2 )提供合成体内其它物质的原料(3 )作为机体组织细胞的组成成分吸收速率最快的为-半乳糖二、血糖1. 血糖:指血液中的葡萄糖正常空腹血糖浓度:3.9~6.1mmol/L2. 血糖的来源:(1)食物糖消化吸收(2)肝糖原分解(3)糖异生去路:(1 )氧化分解供能(2)合成糖原(3)转化成其它糖类或非糖物质3. 血糖调节:肝脏调节、肾脏调节(肾糖阈)、神经调节、激素调节体内主要升血糖激素:胰高血糖素、糖皮质激素、肾上腺素、生长激素、甲状腺素三、糖代谢1. 无氧酵解(无氧或缺氧;生成乳酸;释放少量能量)关键酶:己糖激酶、6- 磷酸果糖激酶1、丙酮酸激酶反应部位:胞液产能方式:底物磷酸化净生成2ATP⑴ 葡萄糖磷酸化为6- 磷酸葡萄糖-1ATP⑵ 6- 磷酸葡萄糖转变为6- 磷酸果糖⑶ 6- 磷酸果糖转变为1,6- 二磷酸果糖-1ATP⑷ 1,6- 二磷酸果糖裂解⑸ 磷酸丙糖的同分异构化⑹ 3- 磷酸甘油醛氧化为1,3- 二磷酸甘油酸【脱氢反应】⑺ 1,3- 二磷酸甘油酸转变成3- 磷酸甘油酸【底物磷酸化】+1*2ATP⑻ 3- 磷酸甘油酸转变为2- 磷酸甘油酸⑼ 2- 磷酸甘油酸转变为磷酸烯醇式丙酮酸⑽ 磷酸烯醇式丙酮酸转变成丙酮酸,并通过底物水平磷酸化+1*2ATP(11)丙酮酸加氢转变为乳酸生理意义:(1)是机体在缺氧情况下获取能量的有效方式。
生物化学 第八章 生物氧化

第二节 线粒体氧化体系
一、呼吸链(respiratory chain) 二、呼吸链的组成成分和作用 三、呼吸链的蛋白质复合体 四、呼吸链中各组分的排列顺序
Go on~
一、呼吸链(respiratory chain)
• 呼吸链是代谢物上的氢原子被脱氢酶激活 脱落后,经过一系列的传递体,最后传递 给被激活的氧原子,而生成水的全部体系。 • 在真核生物细胞内,它位于线粒体内膜上, 原核生物中,它位于细胞膜上。
功能:将底物上的氢激活
并脱下。
辅酶:NAD+或NADP+
NAD+ 和NADP+的结构
OR
NAD+:R=H NADP+:R=PO32-
尼克酰胺核苷酸的作用原理:
H
H H CONH 2
C CONH2 N R
+
+ H + e + H+
N R
+ H+
H
2H
H
e
H+
NAD(P)+
+2H
-2H
NAD(P)H+H+
Cys Cys
S S
Fe3+
S S
Fe3+S S来自Cys Cys+e-
Cys Cys
S S Fe3+
S S Fe2+
S S
Cys Cys
(4)泛醌(CoQ)
一种脂溶性的醌类化合物,其分子中的苯醌 结构能进行可逆的加氢反应,是氢传递体。
CoQ + 2H
CoQH2
(5)细胞色素(cytochrome,Cyt)
生物化学第八章 生物氧化

1 O2 2
H2O
实测得FADH2呼吸链: P/O~ 2
FADH2
线粒体是真核细胞的一种细胞器,是生物氧化和能 量转换的主要场所。是组织细胞的“发电厂”。 线粒体内,外膜的化学组成有显著的区别; 外膜:磷脂,胆固醇含量高,蛋白质含量低 内外膜间隙:腺苷酸激酶,核苷酸激酶等 内膜:有些脱氢酶,氧化呼吸链有关的酶, ATP 合成酶 基质: 催化糖有氧分解,脂肪酸氧化,氨基酸分 解和蛋白质生物合成的酶
3
二、生物氧化的一般过程
主要解决三个问题:
1.代谢物中C如何在酶催化下生成CO2;
2.细胞如何利用O2将代谢物中的H氧化成H2O;
3.氧化产生的自由能怎样被收集、转换和储存。
4
生物氧化的三个阶段
脂肪 多糖 蛋白质
大分子降解 成基本结构 单位
脂肪酸、甘油
葡萄糖、 其它单糖
氨基酸
乙酰CoA
小分子化合物 分解成共同的 中间产物(如 丙酮酸、乙酰 CoA等)
31
2. 高能化合物
生化反应中,在水解时或基团转移反应中可释
放出大量自由能( >20 千焦 / 摩尔)的化合物称为 高能化合物。
32
高 能 化 合 物 类 型
33
3. ATP的特点
在 pH=7 环 境 中 , ATP 分子中的三个磷 酸基团完全解离成带 4个负电荷的离子形 式 ( ATP4-), 具 有 较大势能,加之水解 产物稳定,因而水解 自由能很大( ΔG°′= -30.5千焦/摩尔)。
34
4.ATP的特殊作用
在机体的能量代谢中, ATP 就好像能量通币, 高能化合物虽有多种,只有 ATP 可为一切生 理机能与生物合成反应提供能量; ATP是细胞内磷酸基团转移的中间载体
生物化学课件(生物氧化和能量转换)

尽了(
生物氧化概述
кин羔 ,4roller the
scrnof a融洽羔饽饽饽``
生物氧化概述
03
\
01
,
02
``
生物氧化概述
down on ones饽
`` \ tear. has.
生物氧化概述
1
2
3
草坪.
蠕
on⒊ rot侪
生物氧化概述
01
拇指1羔 P U菖chuille on庄园 onve(`` on
开发新型抗氧化剂
随着人们对健康需求的提高,开发新型抗氧化剂成为研究热点,以预防和治疗与氧化应激相关的疾病。
探索生物氧化的调控机制
未来将进一步探索生物氧化的调控机制,以实现对其过程的精准调控,为农业生产、医学治疗和工业生产等领域提供新的思路和方法。
生物氧化的发展趋势
谢谢
THANKS
生物化学课件(生物氧化和能量转换)
目录
CONTENTS
生物氧化概述 生物氧化中的能量转换 生物氧化中的酶 生物氧化中的呼吸链 生物氧化中的ATP合成 生物氧化中的其他问题
01
生物氧化概述
CHAPTER
(
on this ,壳
ier C on board * the i about the chip in this about
热力学第二定律
03
在自然过程中,一个封闭系统的总熵(代表无序程度)只可能增加,不可能减少。这意味着能量转换总是向着熵增加的方向进行,即向着更加无序、混乱的状态发展。
能量转换的原理
植物通过光合作用将太阳能转换为化学能,并存储在有机物中。
光合作用
呼吸作用
ATP合成
生物化学重点知识归纳

生物化学重点知识归纳第一章绪论1.生物化学的发展过程大致分为三阶段:叙述生物化学、动态生物化学和机能生物化学。
2.生物化学研究的内容大体分为三部分:①生物体的物质组成及生物分子的结构与功能②代谢及其调节③基因表达及其调控第二章糖类化学1.糖类通常根据能否水解以及水解产物情况分为单糖、寡糖和多糖。
2.单糖的分类:①按所含C原子的数目分为:丙糖、丁糖......②按所含羰基的特点分为:醛糖和酮糖。
3.葡萄糖既是生物体内最丰富的单糖,又是许多寡糖和多糖的组成成分。
4.甘油醛是最简单的单糖。
5.两种环式结构的葡萄糖:6.核糖和脱氧核糖的环式结构:(见下图)7.单糖的重要反应有成苷反应、成酯反应、氧化反应、还原反应和异构反应。
8.蔗糖是自然界分布最广的二糖。
9.多糖根据成分为:同多糖和杂多糖。
同多糖又称均多糖,重要的同多糖有淀粉、糖原、纤维素等;杂多糖以糖胺聚糖最为重要。
10.淀粉包括直链淀粉和支链淀粉。
糖原分为肝糖原和肌糖原。
11.糖胺聚糖包括透明质酸、硫酸软骨素和肝素。
第三章脂类化学1. 亚油酸、α亚麻酸和花生四烯酸是维持人和动物正常生命活动所必必需的脂肪酸,是必需脂肪酸。
2. 类花生酸是花生四烯酸的衍生物,包括前列腺素、血栓素和白三烯。
3. 脂肪又称甘油三酯。
下图是甘油三酯、甘油和脂肪酸的结构式:1. 皂化值:水解1克脂肪所消耗KOH的毫克数。
皂化值越大,表示脂肪中脂肪酸的平均分子量越小。
6.磷脂根据所含醇的不同分为甘油磷脂和鞘磷脂。
7.糖脂包括甘油糖脂和鞘糖脂。
8.类固醇是胆固醇及其衍生物,包括胆固醇、胆固醇脂、维生素D、胆汁酸和类固醇激素等。
9.胆汁酸有游离胆汁酸和结合胆汁酸两种形式。
10.类固醇激素包括肾上腺皮质激素(如醛固酮、皮质酮和皮质醇)和性激素(雄激素、雌激素和孕激素)。
11.肾上腺皮质激素具有升高血糖浓度和促进肾脏保钠排钾的作用。
其中皮质醇对血糖的调节作用较强,而对肾脏保钠排钾的作用很弱,所以称为糖皮质激素;醛固酮对水盐平衡的调节作用较强,所以称为盐皮质激素。
《生物化学基础》教学大纲

《生物化学基础》(104010007)(供国家基础药学理科基地班使用)一、说明1、该课程的目的和任务生物化学是研究生命的化学,亦即研究生命现象本质的一门科学。
是当代生物科学领域中发展最为迅速的学科之一。
它从分子水平来研究和阐述生物体(包括人类、动物、植物和微生物)内基本物质的化学组成和生命活动中所进行的化学变化(即代谢反应)的规律及其与生理机能关系的一门科学。
组成生物体的重要物质有蛋白质、核酸、糖类、脂类、无机盐和水分等,此外还有多种含量较少而对生命活动极为重要的维生素、激素和微量元素。
生物化学的任务之一就是研究这些基本物质的化学组成、结构、理化性质、生物功能以及结构与功能的关系,这些内容也被称为静态生物化学。
生物体内的各种基本物质在生命活动过程中不断地进行着互相联系,互相制约,互相对立而又统一的,多种多样,复杂而又有规律的化学变化。
这一系列化学变化就是生物体与外界环境进行的物质交换,称为新陈代谢。
它是生命的基本特征之一,是揭示生命现象本质的重要环节,代谢一停止,生命也就随之停止,所以生物化学的另一任务就是研究代谢的规律。
这些内容又被称为动态生物化学。
总之,生物化学的任务就是研究组成生物体基本物质的性质、结构与功能,以及这些物质在生命活动过程中所进行的化学变化的规律及其与生理机能的关系,从而阐明生命现象的本质,并把这些知识应用到社会实践中去,以达到征服自然和改造自然的目的。
2、课程的基本要求本大纲要求通过讲授及实验,使学生达到:(1)熟悉生物化学的含义和任务以及本课程在药学者的地位和重要性(2)掌握组成生物体基本物质的性质、结构、功能以及结构与功能的关系和验证这些性质的方法。
(3)掌握生物体内各种基本物质在生命活动中进行这的各种合成、分解代谢以及各种物质在代谢过程中互相联系,互相转换的规律。
以及研究这些内容的实验方法和技能。
3、学时安排51学时。
4、教材选用情况《生物化学》,姚文兵主编,人民卫生出版社,2011年,第7版二、教学内容和要求绪论【3课时】[基本内容]1、生物化学的定义、内容、研究目的及任务2、生物化学与医药卫生及工农业生产的相互关系,本学科与其他学科的关系及其在医药工业中的地位和重要性3、生物化学的发展概况、成就及其发展前景[基本要求]1、重点掌握生物化学的概念、内容和研究任务。
生物化学第八章 新陈代谢总论与生物氧化知识点归纳

CH4+NADH + O2
CH3OH+ H2O +NAD+
氧化酶
催化以氧分子为电子受体的氧化反应
细胞色素c氧化酶
2细胞色素c (Fe2+) + 1/2O2 +2H+
2细胞色素c (Fe3+)+H2O
3. 脱羧氧化
(1)直接脱羧作用
CH3COCOOH
CH3CHO + CO2
丙酮酸
丙酮酸脱羧酶 乙醛
CO2来源于氧化 代谢中间产物羧
生物氧化
有氧氧化 无氧氧化
一、生物氧化概述
1、有氧氧化: 需氧生物和兼性好氧生物有氧条件下,以分子氧作为最终电
子受体,将能源物质完全氧化分解成CO2和H2O,同时释放能量 用于ATP的合成 (底物燃烧完全,产能多。)
2、无氧氧化: 在无氧条件下,最终的电子受体是氧化型物质,或某些外源性电子 受体,将能源物质不完全氧化分解。(底物燃烧不完全,产能少)。
酵解途径中1,6-二磷酸果糖裂解生成了2分子三碳糖。
4.突变体研究法
1、基因突变
大肠杆菌 基因突变
酶缺失
β-半乳糖 苷酶缺失
该酶作用的底物 积累,产物缺失
乳糖堆积
2. 营养缺陷型微生物或人类遗传性代谢病的研究 糖尿病例研究蛋白质与糖、脂代谢的关系 生糖氨基酸和生酮氨基酸的确定
5.测定特征性酶
△G0′= -nF△E0′=-nF (E0' 受体-E0' 供体)
△G0´:氧化还原反应的标准自由能变化,单位为kJ/mol; n:转移的电子数目; F:法拉第常数,其值为96.485kJ/(V∙mol) △E0´:为两个氧还对之间标准氧化还原电势差值;
生物化学复习提纲

生物化学复习提纲1.生物氧化a)呼吸链:代谢物上的氢原子被脱氢酶激活脱落后,经过一系列的传递体,最后传递给被激活的氧分子,并与之结合生成水的全部体系称呼吸链。
b)P/O比值:物质氧化时,每消耗1摩尔氧原子所消耗无机磷的摩尔数,即一对电子经电子传递链转移至1摩尔氧原子时生成ATP的摩尔数。
c)生物氧化:有机物在生物体内氧的作用下,生成CO2和水并释放能量的过程称为生物氧化。
d)高能化合物:含自由能高的磷酸化合物称为高能化合物。
e)氧化磷酸化:伴随放能的氧化作用而进行的磷酸化作用称为氧化磷酸化。
f)底物水平磷酸化:底物水平磷酸化是在被氧化的底物上发生磷酸化作用,即在底物被氧化的过程中,形成了某些高能的磷酸化合物,这些高能磷酸化合物通过酶的作用使ADP生成ATP。
g)电子水平磷酸化:电子由NADH或FADH2经呼吸链传递给氧,最终形成水的过程中伴有ADP磷酸化为ATP,这一过程称为电子水平磷酸化。
h)磷酸-甘油穿梭系统:在脑和骨骼肌,胞液中产生的还原当量转运进入线粒体氧化的方式。
以磷酸甘油为载体,进入线粒体FADH2氧化呼吸链氧化,生成1.5分钟ATP。
i)苹果酸-天冬氨酸穿梭系统:在心肌和肝,胞液中产生的还原当量转运进入线粒体氧化的方式。
以苹果酸为载体,进入线粒体NADH氧化呼吸链氧化,生成2.5分钟ATP。
各种生物的新陈代谢过程虽然复杂,但却有共同特点:反应条件温和,由酶所催化,对内外环境条件有高度的适应性和灵敏的自动调节机制。
有机物在生物体内氧的作用下,生成CO2和H2O并释放能量的过程称为生物氧化。
生物体内氧化反应有脱氢、脱电子、加氧等类型。
常见的高能化合物:磷酸烯醇丙酮酸、乙酰磷酸、腺苷三磷酸、磷酸肌酸、乙酰辅酶A典型的呼吸链有NADH呼吸链与FADH2呼吸链。
呼吸链由线粒体内膜上NADH脱氢酶复合物(复合物I),细胞色素b、c1复合物(复合物III)和细胞色素氧化酶(复合物IV)3个蛋白质复合物组成。
巫-第八章生物氧化和能量转化
n:转移电子数; F:法拉第常数[96.5 KJ/(V.mol)]
六、高能磷酸化合物
生物体内有许多磷酸化合物,当其磷酰基 水解时,释放大量的能量,这些化合物称为 高能磷酸化合物。如 ATP。 一般将水解时能够释放21 kJ /mol (5千卡 / mol )以上自由能(G’ < -21 kJ / mol)的 化合物称为高能化合物。 根据生物体内高能化合物键的特性可以把 他们分成以下几种类型。
• 一、线粒体
• 成熟的成纤维细胞中线粒体(mitochondria)是含 量最丰富的细胞器.
• 每个细胞中约有1000个线粒体,占整个细胞体积 的25%。
• 线粒体功能: • 能量转换 • 合成ATP • 物质运输 • 信息传递 等
线粒体--细胞的能量转换器
• 两层单位膜构成 • 封闭囊状结构
FMN → FMNH2
Fe2+
Fe3++e
10
1
通过异咯嗪环第1位和第10位上的两个氮 原子反复进行加氢和脱氢反应。
铁硫蛋白(铁硫中心):它主要以 (2Fe-2S) 或
(4Fe-4S) 形式存在。(2Fe-2S)含有两个活泼的 无机硫和两个铁原子。 铁硫蛋白通过Fe3+ Fe2+ 变化起传递电子的 作用。
氧化型
H2O
一个或多个传递体
M
还原型
1/2O2
脱氢酶
氧化酶
五、自由能和氧化还原电位
1. 自由能 自由能是指一个化合物分子结构中所固有
的能量,是一种能在恒温、恒压条件下作功 的能量。
如果 A
B , 则△G =GB – GA
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第八章生物氧化和能量转换
一、生物氧化的概念和特点:
生物氧化(biological oxidation)是指细胞内的糖、蛋白质和脂肪进行氧化分解而生成CO2和H2O,并释放能量的过程。
生物氧化在细胞内进行的;在常温、常压、近于中性及有水环境中进行的;反应逐步释放出能量,相当一部分能量以高能磷酸酯键的形式储存起来。
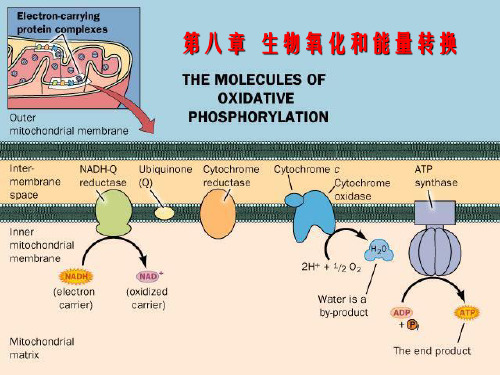
二、线粒体氧化呼吸链:
生物氧化过程中,从代谢物上脱下的氢由一系列传递体依次传递,最后与氧形成水的整个体系称为呼吸链。
这些递氢体或递电子体往往以复合体的形式存在于线粒体内膜上。
主要的复合体有:
1.复合体Ⅰ(NADH-泛醌还原酶):其作用是将(NADH+H+)传递给CoQ。
2.复合体Ⅱ(琥珀酸-泛醌还原酶):其作用是将FADH2传递给CoQ。
3.复合体Ⅲ(泛醌-细胞色素c还原酶):其作用是将电子由泛醌传递给Cytc。
4.复合体Ⅳ(细胞色素c氧化酶):其作用是将电子由Cytc传递给氧。
三、呼吸链成分的排列顺序:
由上述递氢体或递电子体组成了NADH氧化呼吸链和琥珀酸氧化呼吸链两条呼吸链。
1.NADH氧化呼吸链:其递氢体或递电子体的排列顺序为:NA DH→ FMN→CoQ→b→ c1 → c →aa3 →1/2O2 。
丙酮酸、α-酮戊二酸、异柠檬酸、苹果酸、β-羟丁酸、β-羟脂酰CoA脱氢后经此呼吸链递氢。
2.琥珀酸氧化呼吸链:其递氢体或递电子体的排列顺序为:FAD→CoQ→b→ c1 → c →aa3 →1/2O2 。
琥珀酸和脂酰CoA脱氢后经此呼吸链递氢。
四、生物体内能量生成的方式:
1.氧化磷酸化:在线粒体中,底物分子脱下的氢原子经递氢体系传递给氧,在此过程中释放能量使ADP磷酸化生成ATP,这种能量的生成方式就称为氧化磷酸化。
2.底物水平磷酸化:直接将底物分子中的高能键转变为ATP分子中的末端高能磷酸键的过程称为底物水平磷酸化。
五、P/O比:
是指一对电子通过呼吸链传递到氧时所产生的ATP分子数称为P/O比值。
当底物脱氢以NAD+为受氢体时,P/O比值约为2.5;而当底物脱氢以FAD为受氢体时,P/O比值约为1.5。
六、氧化磷酸化的偶联机制:
目前公认的机制是1961年由Mitchell提出的化学渗透学说。
这一学说认为氧化呼吸链存在于线粒体内膜上,当氧化反应进行时,H+通过氢泵作用(氧化还原袢)被排斥到线粒体内膜外侧(膜间腔),从而形成跨膜pH梯度和跨膜电位差。
这种形式的能量,可以被存在于线粒体内膜上的ATP合酶利用,生成高能磷酸基团,并与ADP结合而合成ATP。
ATP合酶分为F0和F1两部分。
七、呼吸链的抑制剂与解偶联剂:
鱼藤酮抑制NADH→CoQ;抗霉素A抑制b→ c1;CO、H2S和CN- 等抑制aa3 →O2。
解偶联剂(uncoupler)作用是使电子传递和ATP生成的两个过程分离。
它只抑制ATP的形成,而不抑制电子传递过程。
如:2,4-二硝基苯酚(DNP)
八、高能磷酸键的类型:
生物化学中常将水解时释放的能量>20kJ/mol的磷酸键称为高能磷酸键,主要有以下几种类型:
1. 磷氧键型(-O~P):1,3-二磷酸甘油酸、ATP等。
2.磷氮键型(-N~P):磷酸肌酸。
磷酸肌酸是肌肉和脑组织中能量的贮存形式。
3.硫碳键型(-C~S):琥珀酰辅酶A。
九、线粒体外NADH的穿梭:
胞液中的3-磷酸甘油醛脱氢均可产生NADH。
这些NADH可经穿梭系统而进入线粒体氧化磷酸化,产生H2O和ATP。
1.磷酸甘油穿梭系统:NADH通过此穿梭系统带一对氢原子进入线粒体,则只得到1.5分子ATP。
2.苹果酸穿梭系统:经此穿梭系统带入一对氢原子可生成2.5分子ATP。
