化学方程式的计算专题——表格题
(完整)初中化学图表型计算题+答案

图形类计算题1、用“侯氏联合制碱法”制得的纯碱常含有少量的氯化钠。
为测定某纯碱样品中碳酸钠的含量,小明称取该纯碱样品3.3g,充分溶解于水中,再滴加氯化钙溶液,产生沉淀的质量与加入氯化钙溶液的质量关系如图所示。
求:(1)该纯碱样品中碳酸钠的质量分数。
(精确到0.1%)(2)所加入氯化钙溶液的溶质质量分数。
2、已知Na2cO3的水溶液呈碱性,在一烧杯中盛有20.4gNa2cO3和NaCl组成的固体混合物。
向其中逐渐滴加溶质质分数为10%的稀盐酸。
放出气体的总质量与所滴入稀盐酸的质量关系曲线如下图所示,请根据题意回答问题:(1)当滴加稀盐酸至图中B点时,烧杯中溶液的pH7(填>、=、<)。
(2)当滴加稀盐酸至图中A点时,烧杯中为不饱和溶液(常温),通过计算求出其中溶质的质量分数。
(计算结果保留一位小数)第2题3、将29.1g由NaCl和BaCl2组成的固体混合物溶解于94.2mL水中(=1g/cm3),向所得溶液中滴加质量分数为14.2%的Na2sO4溶液,至恰好完全反应。
下图是所加Na2sO4溶液质量与生成沉淀质量的关系图,计算:(1)生成沉淀的质量是多少?(2)所得溶液中溶质的质量分数为多少?第3题4、刘明用石灰石(杂质不与酸反应,也不溶于水)和稀盐酸反应制取二氧化碳,在准备将反应后的废液倒进废液缸时,发现实验桌上有一瓶未知质量分数的Na2cO3溶液,他决定利用该废液,测定Na2cO3溶液中溶质的质量分数。
他将废液过滤,然后向废液中慢慢滴加Na2c03溶液,加入Na2cO3溶液的质量与生成沉淀质量的关系如图所示。
2323(1)在加入Na2cO3溶液的过程中,开始时没有发现沉淀生成,说明滤液中的溶质除含有%@在2外,还含有;(2)计算NacO溶液中溶质的质量分数。
(计算结果精确到0.1%)23第4题5、在化学实验技能考试做完“二氧化碳的制取和性质”实验后,废液桶中有大量的盐酸与氯化钙的混合溶液(不考虑其他杂质)。
九年级上册化学计算专题——表格型计算(无答案)

化学表格计算题归纳1、某科学兴趣小组在综合实践活动中,从石灰厂带来一块石灰石样品,技术员告诉他们此样品中含有的杂质是二氧化硅,二氧化硅难溶于水且不与盐酸反应。
为了测定该石灰石的纯度,兴趣小组的同学取用4g这种石灰石样品,用实验室现有的未知溶液质量分数的稀盐酸40g分4次加入,充分反应后,经过滤、干燥等操作后称量,得到如下数据:(1)表示m的值为_________g。
(2)该石灰石样品的纯度。
(3)所用的稀盐酸中溶质的质量分数。
2、某同学去风景区游玩,带回了几小块石灰石样品。
为了检测样品中碳酸钙的含量,他称取10.0g样品,将60.0g稀盐酸分四次加入,测量的有关数据见下表(已知样品中的杂质不溶于水,且不与稀酸盐反应)。
求:⑴样品中碳酸钙的质量分数;⑵所用稀盐酸的溶质质量分数。
⑶10.0g该样品与足量稀盐酸反应后可产生二氧化碳多少克?(结果精确到小数点后两位)3、某化学兴趣小组为了测定某石灰石样品中碳酸钙的质量分数,取用2.0 g石灰石样品,把25.0g质量分数为10%的稀盐酸分五次加入样品中(样品中的杂质既不与盐酸反应,也不溶解于水),每次充分反应后都经过滤、干燥、称量,得实验数据如下:请计算:(1)2.0g石灰石样品中碳酸钙的质量为,石灰石中碳酸钙的质量分数为。
(2)请你继续计算反应生成溶液中氯化钙的质量分数(计算过程和结果均保留一位小数)。
4、有一种含碳酸钙的“石头纸”:为测定其中碳酸钙的含量,课外活动小组的同学称取50g碎纸样品。
分别在5只烧杯中进行了实验,实验数据见下表(假设纸张其他成分既不溶于水,也不与水反应):(1)10g样品与足量稀盐酸反应最多生成 g气体;(2)求样品中碳酸钙的质量分数;(3)烧杯④中物质充分反应后所得溶液的质量。
5、某课外小组为了测定铜铁合金中铁的质量分数,现取铜铁合金样品20.0g,将80.0g稀硫酸平均分成4份,分4次逐渐加入到样品中,每次充分反映后测得剩余固体质量见下表:试求:(1)20.0g铜铁合金中,铜的质量为_______g。
6化学方程式计算表格型

本考点贯穿整个试卷,出题形式多样,比较灵活,注重考查书写化学方程式的基本能力,考查的命题点有:判断化学方程式的书写正误(以选择题形式呈现)、根据所给信息书写化学方程式等。
1、答题模板以“求6.8 gH 2O 2分解可以得到氧气的质量”为例:2、计算公式(1)有关不纯物质的计算 = =100% = 100%+ =1⨯⨯⨯纯净物的质量混合物的质量纯度纯净物的质量纯净物的质量纯度混合物的质量纯净物的质量杂质的质量纯-杂质的度质量分数(2)有关溶质质量分数的计算=100%=100%+ = =+ = ⨯⨯⨯⨯溶质质量溶质质量溶质的质量分数溶液质量溶质质量溶剂质量溶质质量溶液质量 溶质质量分数(溶质质量溶剂质量-生成沉淀的质量-生成气体的 质)量溶质质量分数溶液质量-反应物中不参与化学反应前各物质反应的固体杂的质量总和质的质量抓住四查:一查化学式,即是否符合客观事实;二、查配平,即是否符合质量守恒定律;三查反应条件。
四查箭头,即检测气体符号或沉淀符合的使用是否规范。
1、实验室有一瓶标签已毁损的稀盐酸,为了重新标定其浓度,化学兴趣小组的同学做了以下实验:①用电子天平称量200.00g 该稀盐酸并转移至锥形瓶中;①向该锥形瓶中逐次加入等质量同质量分数的Na 2CO 3溶液,并测出每次完全反应后溶液的总质量。
实验数据记录如下表。
第一次第二次第三次第四次第五次加入Na 2CO 3溶液的质量/g20.00 20.00 20.00 20.00 20.00反应后溶液的总质量/g218.90 237.80 R 275.60 295.60(1)表格中R 的数值应为 ; (2)计算恰好完全反应时消耗Na 2CO 3的质量; (3)计算该稀盐酸中HCl 的质量分数。
【答案】(1)256.70(2)第五次加入20gNa 2CO 3溶液,共产生CO 2的质量为:200g+20g×5295. 6g=4. 4g ,故可知第四次加入Na 2CO 3和HCl 恰好完全反应。
化学图表计算类型专项训练

化学专题训练-------图表计算可能用到原子量:H-1、O-16、Zn-65、S-32、K-39、Cl-35.5、Ag-108、N-14 Ca--40、Na--23、Cu--64、Cl--35.51.化学实验室现有98%的浓硫酸,但在实验中常用到较稀的硫酸。
要把50g 质量分数98%的浓硫酸,稀释为质量分数20%的硫酸。
(1)稀释后硫酸溶液中溶质的质量是多少? (2)稀释时所需水的质量是多少? 2.现有一瓶未开启的浓硫酸,试剂瓶标签上的部分内容如右图所示, 请仔细阅读后计算:(写出计算过程)(1)该瓶浓硫酸中硫元素的质量分数是多少?(计算结果保留一位小数,下同。
)(2)欲配制200 g 溶质质量分数为20%的稀硫酸,需用这种浓硫酸的体积是多少?需加水的质量是多少?3.向10g 氢氧化钠和硫酸钠的混合物中加入100g 溶质的质量分数为9.8%的硫酸溶液,恰好完全反应。
计算:(1)原混合物中氢氧化钠的质量分数;(2)反应后所得溶液中溶质的质量分数。
4.镁条在空气中易被氧化。
有一根在空气中放置一段时间的镁条样品,其质量为2.56g ,将该样品与44g 足量的稀硫酸充分混合,反应过程中测得数据如下:请计算 (写出计算过程) :(1)2.56g 样品中含金属镁的质量是多少? (2)氧化前镁条的质量是多少?5.实验室有一瓶久置的氢氧化钠固体,某同学想了解其变质情况,设计了实验,实验过程如下:实验一:取少量样品于试管中,滴加适量稀盐酸,观察到有气泡产生,说明氢氧化钠已变质,变质的原因是_________________ ______ ____(用化学方程式表示)。
实验二:通过实验二,能进一步推算出氢氧化钠变质的程度。
(1)请计算实验二中参加反应的碳酸钠质量。
(化学方程式:Na 2CO 3+ CaC12=CaCO 3↓+2NaCl )(2)通过实验一的分析和(1)的计算结果,可以进一步计算出样品中已变质的氢氧化钠。
化学方程式的表格计算
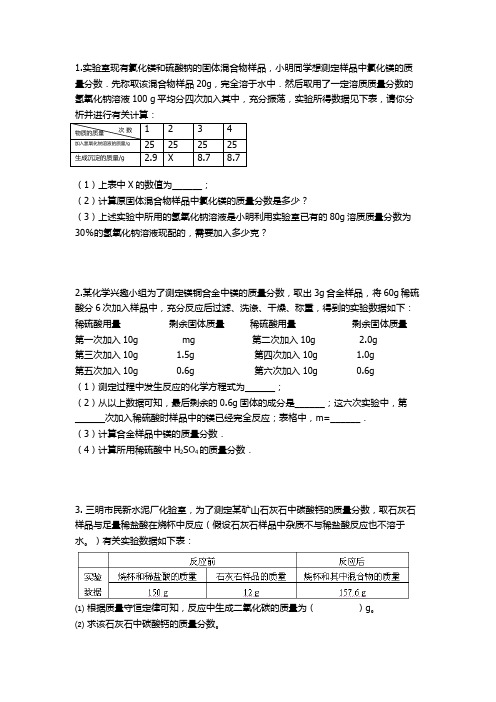
1.实验室现有氯化镁和硫酸钠的固体混合物样品,小明同学想测定样品中氯化镁的质量分数.先称取该混合物样品20g,完全溶于水中.然后取用了一定溶质质量分数的氢氧化钠溶液100 g平均分四次加入其中,充分振荡,实验所得数据见下表,请你分1 2 3 4物质的质量次数加入氢氧化钠溶液的质量/g 25 25 25 25生成沉淀的质量/g 2.9 X 8.7 8.7(1)上表中X的数值为______;(2)计算原固体混合物样品中氯化镁的质量分数是多少?(3)上述实验中所用的氢氧化钠溶液是小明利用实验室已有的80g溶质质量分数为30%的氢氧化钠溶液现配的,需要加入多少克?2.某化学兴趣小组为了测定镁铜合金中镁的质量分数,取出3g合金样品,将60g稀硫酸分6次加入样品中,充分反应后过滤、洗涤、干燥、称重,得到的实验数据如下:稀硫酸用量剩余固体质量稀硫酸用量剩余固体质量第一次加入10g mg 第二次加入10g 2.0g 第三次加入10g 1.5g 第四次加入10g 1.0g第五次加入10g 0.6g 第六次加入10g 0.6g(1)测定过程中发生反应的化学方程式为______;(2)从以上数据可知,最后剩余的0.6g固体的成分是______;这六次实验中,第______次加入稀硫酸时样品中的镁已经完全反应;表格中,m=______.(3)计算合金样品中镁的质量分数.(4)计算所用稀硫酸中H2SO4的质量分数.3. 三明市民新水泥厂化验室,为了测定某矿山石灰石中碳酸钙的质量分数,取石灰石样品与足量稀盐酸在烧杯中反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水。
)有关实验数据如下表:⑴根据质量守恒定律可知,反应中生成二氧化碳的质量为()g。
⑵求该石灰石中碳酸钙的质量分数。
4. 某同学为了测定黄铜屑(由锌和铜形成的合金)样品组成,取四份样品分别加入稀硫酸反应,其实验数据记录如下表。
样品第1份第2份第3份第4份取样品质量(g) 50.0 50.0 50.0 50.0取稀硫酸质量(g)40.0 80.0 120.0 160.0产生气体质量(g)0.4 0.8 1.0 m(1)上表中m的数值是();(2)在四份样品所做实验中,稀硫酸有剩余的是();(3)假黄金外观与黄金相似,社会上一些不法分子用黄铜(Cu-Zn合金)假冒黄金进行诈骗活动。
3化学方程式计算(表格型)(原卷版)
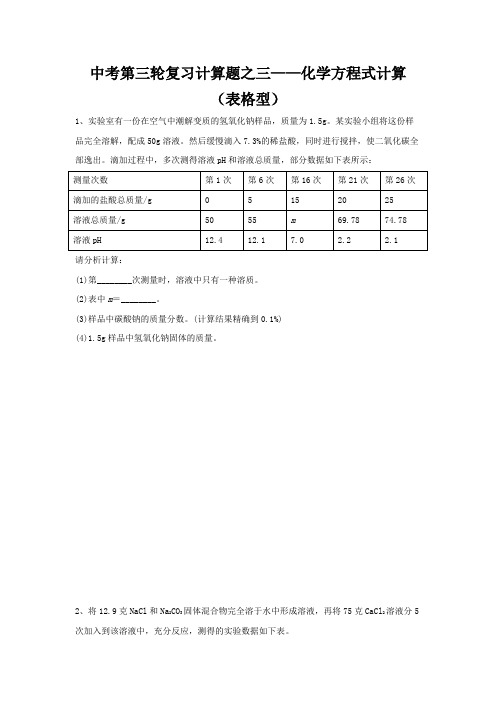
中考第三轮复习计算题之三——化学方程式计算(表格型)1、实验室有一份在空气中潮解变质的氢氧化钠样品,质量为1.5g。
某实验小组将这份样品完全溶解,配成50g溶液。
然后缓慢滴入7.3%的稀盐酸,同时进行搅拌,使二氧化碳全部逸出。
滴加过程中,多次测得溶液pH和溶液总质量,部分数据如下表所示:请分析计算:(1)第________次测量时,溶液中只有一种溶质。
(2)表中m=________。
(3)样品中碳酸钠的质量分数。
(计算结果精确到0.1%)(4)1.5g样品中氢氧化钠固体的质量。
2、将12.9克NaCl和Na2CO3固体混合物完全溶于水中形成溶液,再将75克CaCl2溶液分5次加入到该溶液中,充分反应,测得的实验数据如下表。
求:(1)表格中m的数值是________。
(2)溶液中Na2CO3完全反应是在第________次实验。
(3)固体混合物Na2CO3的质量分数。
(精确到0.1%)(4)请画出上述过程中溶液中NaCl质量的变化图。
3、为测定CuCl2和FeCl2组成的混合溶液中FeCl2的质量分数,进行如下实验:①取200g混合溶液加入足量的AgNO3溶液,经过滤、洗涤、干燥、称量得到143.5gAgCl 固体;②另取原混合溶液各200g与含有杂质的废铁屑反应(杂质不溶于水,也不参与反应),共做了五组实验,其实验数据如下表。
请分析计算:(1)表中第三组实验的m值为________。
(2)第________组实验恰好完全反应。
(3)铁屑中铁的质量分数为多少?(计算结果精确到0.1%)(4)原混合溶液中FeCl2的质量分数为多少?(计算结果精确到0.1%)4、钙是人体中的常量元素,缺钙时可通过食用保健药剂来增加摄入量。
某补钙药剂说明书的部分信息如图1所示。
现将100g盐酸分成5等份,逐次加到用40片该药剂制成的粉末中(其他成分不与盐酸反应),得到部分数据与图像如图2所示。
请根据有关信息回答问题。
第4次图1 图2(1)人体缺钙易出现的疾病是_______________,这时除在医生指导下服用保健药剂外,日常生活中要多摄入________________________________等食物。
【化学】化学方程式的计算专题(含答案)

【解析】
【分析】
根据恰好完全反应时溶液的总质量求算盐酸溶液的质量,进而结合对应的化学方程式求算该氢氧化钾溶液的溶质质量分数。
【详解】
设该氢氧化钾溶液的溶质质量分数为x
反应的稀盐酸溶液的质量为40g-20g=20g
x=11.2%
答:该氢氧化钾溶液的溶质质量分数为11.2%。
【点睛】
根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整。
2.生铁和钢都是由铁和碳组成的合金,生铁中碳的含量为2%~4.3%,钢中碳的含量为0.03%~2%,为测定某种铁合金中碳的含量,小王同学取一定质量的合金样品盛放在烧杯中,并向其中逐滴加入稀盐酸至恰好完全反应,实验数据如下表所示:
烧杯质量
样品的质量
稀盐酸的质量
烧杯+剩余物的总质量
50g
5.8g
94.6g
KCl的质量分数= 。
答:固体混合物中KCl的质量分数最大,其数值为67.73%。
(2)取一定量该生铁样品,加入一定溶质质量分数的稀硫酸充分反应,加入稀硫酸的质量与产生氢气的质量之间的关系如图所示。
计算所用稀硫酸的溶质的质量分数______。
【答案】1750 t9.8%
【解析】
【分析】
【详解】
解:(1)设:至少需要用含氧化铁80%的赤铁矿的质量为x。
x=1750t
至少需要用含氧化铁80%的赤铁矿的质量1750t。
(1)b~c段产生氧气的速度明显比O~b段加快,其原因是______。
(2)反应结束后所得固体混合物中质量分数最大的物质的质量分数是多少?___(写出计算过程,精确到小数点后一位)
【答案】高锰酸钾分解产生的二氧化锰作为催化剂,加速了氯酸钾的分解67.73%(详见解析)
化学方程式计算专题

化学方程式计算专题work Information Technology Company.2020YEAR化学方程式计算(一)——常见题型1、计算步骤:(一设 二写 三排 四列 五解 六答)2、计算要领:①步骤要完整 ②格式要规范 ③得数要准确3、计算关键:①准确书写化学方程式 ②化学方程式要配平 ③准确计算相对分子质量④代入计算的必须是纯物质质量4、常见题型:①文字叙述题、②表格题、③图像题24、专题练习可能用到的相对原子质量:C-12 H-1 O-16 N-14 S-32 Cl-35.5 K-39 Mn-55 Ca-40 Zn-65 Fe-56 Cu-641.利用右图装置能制取氢气并测定所收集气体的体积。
聪聪同学在锥形瓶中装入0.65g 锌粒,往长颈漏斗中加入100g 稀硫酸,两者恰好完全反应。
(1)求生成氢气的质量。
例1、文字叙述题实验室常用一定质量分数的过氧化氢溶液制取氧气.某同学取2g 二氧化锰于锥形瓶中,然后慢慢滴入34g过氧化氢溶液,完全反应后,称得锥形瓶内剩余物质的总质量是34.4g.求:(1)生成氧气的质量解:2g+34g-34.4g.=1.6g(2)参加反应的.过氧化氢的质量是多少?解:设过氧化氢的质量为x2H 2O 2 MnO 2H 2O+ O 2 ↑ 6832x 16g68/x=32/1.6gx=3.4g答:参加反应的.过氧化氢的质量是3.4g例2、表格题为测定某石灰石中碳酸钙的质量分数,把石灰石样品与稀盐酸反应,反应数据如下:(单位:克)实验 第一次第二次 第三次样品 质量 10 10 15 盐酸 质量 250 200 200 生成 气体3.33.33.3求:(1)哪一次恰好完全反应? 解:第二次反应是恰好完全反应。
(2)该样品中碳酸钙的质量分数? 解:该样品的碳酸钙的质量为x CaCO 3 + 2HCl === CaCl 2 + H 2O + CO 2↑ 100 44 x 3.3g100/x=44/3.3gx=7.5g7.5g/10g ×100%=75%答:该样品中碳酸钙的质量分数为75%例3、图像题取某铜锌合金10g 与100g 稀硫酸反应,记录不同时刻剩余固体的质量,并绘制成如下图像:求:(1)生成氢气的质量?解:10g+100g -109.8g=0.2g(2) 合金中锌的质量分数? 解:设参加反应的锌的质量为x Zn +H 2SO 4= ZnSO4 + H 2↑ 65 2 x 0.2g65/x=2/0.2g x=6.5g6.5g/10g ×100%=65%/g t 109.8 0110.0(2)右图装置采用的是法收集氢气;若要收集本题中所求的氢气(0.0899g/L),应选用 mL(填“10”或“100”或“500”)量筒2、某同学为了测定黄铜屑(由锌和铜形成的合金)样品组成。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
九年级化学中考计算专题复习――表格类计算
教学目标:
1、通过计算分析,使学生进一步理解化学方程式有关量的意义。
2、让学生在计算过程中,养成正确的审题习惯、规范完整的书写习惯,提高分析、归纳、解决问题的能力。
3、通过习题训练,提高学生对图表的分析、数据的选择能力,体会出质量守恒定律是进行化学方程式计算的基本依据。
4、培养学生严肃认真、不畏困难的科学态度。
教学过程:
一、河北理综36题(5分宝典--3要2关2注意)
3个要领:步骤完整,格式规范,得数准确。
2个关键:准确书写化学方程式,准确计算相对分子质量。
2个注意事项:计算时单位要统一,代入量要纯且完全反应。
二、近9年河北计算题考情
归纳总结:
文字叙述类-3次;实物流程图类-2次;表格类-3次;
坐标曲线类-1次;标签类-0次。
对于表格类的计算题,存在表格数据分析不清,导致代入量找不准,本节课重点突破表格类的计算题。
三、例题精练
例1:将生理盐水与足量硝酸银溶液混合,计算生理盐水的溶质质量分数。
(各找2名学生前板书写并讲解分析解题过程,教师点评)
例2:计算石灰石中碳酸钙的质量分数;所用稀盐酸的溶质质量分数。
归纳总结:
1、学生总结表格题的突破口
表格体现出反应前后质量关系的,找差量(质量守恒定律)
表格为分次加入反应物的,找到一组恰好完全反应的量。
2、老师总结
此类试题重在考察学生对实验数据的分析、归纳能力。
因此解题的关键是通过比较图表数据所表达的物质质量的变化规律,从中选取关键的数据(一般是恰好完全反应的数据或完全反应的物质),再利用其质量来进行解答。
(注意:解设!!!)
练习巩固:
10g Cu-Zn合金于烧杯中,取60g稀硫酸分6次加入,充分反应。
1、计算黄铜中锌的质量分数;
2、所用稀硫酸质量分数。
(找1名学生分析表格)
课后作业:将其改编为实物流程图类。
(为下节课做铺垫)
四、表格类计算题小结
分析表格:反应前后质量关系的,找差量(质量守恒定律);分次加入反应物的,找到恰好完全反应的一组量(注意:解设!!)。
