第九篇第4讲醛羧酸酯
高三复习27:烃的衍生物——醛-羧酸-酯

专题27烃的衍生物——醛 羧酸 酯年 级:高三辅导科目:化学课时数:3 课题高三复习:烃的衍生物——醛 羧酸 酯教学目的1、 了解醛、羧酸、酯的典型代表物的组成和结构特点以与它们的相互联系2、 了解有机反应的主要类型:取代反应、加成反应等3、 结合实际了解某些有机化合物对环境和健康可能产生影响,了解有机化合物的安全使用教学内容一、课前检测1、有机物的化学式为C 5H 10O,它能发生银镜反应和加成反应.若将它与H 2加成,所得产物的结构简式可能是 A .〔CH 3〕3CCH 2OH B .〔CH 3CH 2〕2CHOH C .CH 3〔CH 2〕3CH 2OH D .CH 3CH 2C 〔CH 3〕2OH [答案]C2、某中性有机物2168O H C 在稀硫酸作用下加热得到M 和N 两种物质,N 经氧化最终可得M,则该中性有机物的结构可能有A. 1种B. 2种C. 3种D. 4种 [答案]B3.下列五种有机化合物中,能够发生酯化、加成和氧化三种反应的是< >①CH 2===CHCOOH ②CH 2===CHCOOCH 3③CH 2===CHCH 2OH ④CH 3CH 2CH 2OHA .①③④B .②④⑤C .①③⑤D .①②⑤解析:题中出现的官能团中能发生酯化反应的官能团有醇羟基和羧基,能发生加成反应的官能团有醛基和碳碳不饱和键,能发生氧化反应的官能团有醛基和碳碳不饱和键.[答案]C4、有机物广泛存在于水果中,尤以苹果、葡萄、西瓜、山楂内为多.<1>有机物中含有的官能团名称是________;在一定条件下有机物X 可发生化学反应的类型有<填序号>________. A .水解反应B .取代反应C .加成反应D .消去反应E .加聚反应F .中和反应 <2>写出X 与金属钠发生反应的化学方程式________________________________________________________________________. <3>与X 互为同分异构体的是<填序号>________.<4>写出X与O2在铜作催化剂加热的条件下发生反应所得到的有机物产物的结构简式______________.答案:<1>羟基、羧基B、D、F二、知识点梳理〔一〕、醛和酮1、醛、酮的结构醛基的结构简式是_________________,饱和一元脂肪醛和饱和一元脂肪酮的分子通式是__________,具有相同分子组成的这两类物质的关系是_____________.通常情况下,甲醛是___________________________________,______于水.组成最简单的芳香醛是_____________.含醛基的物质有_____________________________________________〔至少写出四种不同类物质〕2、醛和酮的化学性质O〔1〕加成反应:CH3CHO+H2__________________ CH3—C—CH3+H2________________〔2〕氧化反应①银镜反应:简述配制银氨溶液的方法__________________________________________________________________________________________________________________________________________写出发生的反应的离子方程式______________________________________________________乙醛与银氨溶液反应的离子方程式是_________________________________________________②与新制Cu<OH>2悬浊液反应乙醛与新制Cu<OH>2悬浊液反应的化学方程式是______________________________________③乙醛催化氧化反应的的化学方程式是_____________________________________________〔一〕1、—CHO C n H2n O 同分异构体有强烈刺激性气味的无色气体易溶苯甲醛〔-CHO〕乙醛、甲酸、甲酸钠、甲酸甲酯、葡萄糖2、〔1〕CH3CH2OH,CH3CH2 CH3〔2〕①在一支洁净的试管中,加入一定量2%的AgNO3溶液,边振荡边滴加2%的稀氨水,直至最初产生的沉淀恰好消失Ag++NH3.H2O=AgOH↓+NH4+AgOH+2NH3.H2O=[Ag<NH3>2]++OH—+2H2O2[Ag<NH3>2]++2OH—+CH3CHO △CH3COO—+NH4++2Ag↓+3NH3+H2O②CH3CHO+2Cu<OH>2△CH3COOH+Cu2O↓+2H2O③2CH3CHO+O2催化剂△2CH3COOH〔二〕、羧酸1、羧酸的结构写出下列羧酸的结构简式或名称:甲酸______________、乙酸______________、草酸______________、苯甲酸______________、COOHCOOH______________2、羧酸的化学性质根据乙酸的分子结构,判断发生反应时断键的部位,并完成反应的方程式:CH3〔1〕酸性:断开键①乙酸溶液和碳酸钠粉末反应的离子方程式②乙酸和氨反应的化学方程式〔2〕取代反应:断开______键COO—H乙酸和C2H518OH发生酯化反应,〔3〕还原反应:LiAl H4CH3CH2COOH[实验]:乙酸和乙醇发生酯化反应实验中,加入试剂的操作是_______________________________________________________________________________________________________浓硫酸的作用是___________________;碎瓷片的作用是_____________ ;饱和碳酸钠溶液的作用是_________________________________________________________________ ;右边竖直玻璃长导管的作用是______________________,导管末端不能插入液面以下,其原因是________________ ,小火加热的原因是___________________________________,该实验所得产物的物理性质是_____________________.COOH对苯二甲酸〔二〕1、—COOH 〔2〕HCOOH CH3COOH HOOC—COOHCOOH2、〔1〕O—H①2CH3COOH+CO32—→2CH3COO—+CO2↑+H2O②CH3COOH+NH3→CH3COONH4〔2〕C—OCH3COOH+C2H518OH CH3CO18OC2H5+H2O〔3〕CH3CH2CH2OH[实验]先向试管中加入一定量的乙醇和乙酸的混合物,然后一边摇动试管一边加入浓硫酸.〔或者先向试管中加入一定量的乙醇和,然后一边摇动试管一边加入浓硫酸,最后加入乙酸〕,催化剂、吸水剂防止液体爆沸吸收乙酸,溶解乙醇,降低乙酸乙酯在水中的溶解度导气冷凝防止倒吸减少乙酸和乙醇的挥发,提高酯的产率和纯度. 无色有香味的油状液体,密度比水小,难溶于水〔三〕、酯1、酯的结构〔1〕酯的官能团是酯基,结构简式是_____________〔2〕写出下列酯的结构简式:甲酸甲酯______________苯甲酸苯甲酯______________乙酸乙二酯_____________乙二酸二乙酯_______________2、酯的物性:酯的密度一般比水______,______溶于水,易溶于乙醇和乙醚等有机溶剂;低级酯是有_______味的液体,许多水果和花草的气味就是由其含有的酯产生的.3、酯的化学性质:〔1〕水解反应:以CH 3CO 18OCH 2CH 3为例写出方程式:酸性水解____________ __________ 碱性水解_____________<三>、酯1、〔1〕 〔2〕HCOOCH 32、小 难 芳香气3、〔1〕CH 3CO 18OC 2H 5+H 2O CH 3COOH+C 2H 518OHCH 3CO 18OC 2H 5+NaOHCH 3COONa+C 2H518OH<四>、烃的衍生物的比较类别官能团分子结构特点分 类主要化学性质卤代烃卤原子<-X>碳-卤键<C-X>有极性,易断裂 ①氟烃、氯烃、溴烃;②一卤烃和多卤烃;③饱和卤烃、不炮和卤烃和芳香卤烃①取代反应<水解反应>:R -X+H 2O R -OH + HX②消去反应: R -CH 2-CH 2X + NaOH RCH =H 2 + NaX + H 2O醇均为羟基 <-OH>-OH 在非苯环碳原子上①脂肪醇<包括饱和醇、不饱和醇>; ②脂环醇<如环己醇>③芳香醇<如苯甲醇>,④一元醇与多元醇<如乙二醇、丙三醇>①取代反应:a .与Na 等活泼金属反应;b .与HX 反应,c .分子间脱水;d .酯化反应 ②氧化反应:2R -CH 2OH + O 2 2R -CHO+2H 2O③消去反应,CH 3CH 2OHCH 2=H 2↑+ H 2OC OO —R 稀硫酸 △酚-OH直接连在苯环碳原上.酚类中均含苯的结构一元酚、二元酚、三元酚等①易被空气氧化而变质;②具有弱酸性③取代反应④显色反应醛醛基<-CHO>分子中含有醛基的有机物①脂肪醛<饱和醛和不饱和醛>;②芳香醛;③一元醛与多元醛①加成反应<与H2加成又叫做还原反应>:R-CHO+H2R-CH2OH②氧化反应:a.银镜反应;b.红色沉淀反应:c.在一定条件下,被空气氧化羧酸羧基<-COOH>分子中含有羧基的有机物①脂肪酸与芳香酸;②一元酸与多元酸;③饱和羧酸与不饱和羧酸;④低级脂肪酸与高级脂肪酸①具有酸的通性;②酯化反应羧酸酯酯基<R为烃基或H原子,R′只能为烃基>①饱和一元酯:CnH2n+lCOOCmH2m+1②高级脂肪酸甘油酯③聚酯④环酯水解反应:RCOOR′+ H2ORCOOH + R'OHRCOOR′+ NaOHRCOONa + R'OH<酯在碱性条件下水解较完全>〔五〕、有机反应的主要类型反应类型定义举例<反应的化学方程式>消去反应有机物在一定条件下,从一个分子中脱去一个小分子<如H2O、HBr等>而生成不饱和<含双键或叁键>化合物的反应C2H5OH CH2=H2↑+ H2O苯酚的显色反应苯酚与含Fe3+的溶液作用,使溶液呈现紫色的反应还原反应有机物分子得到氢原子或失去氧原子的反应CH≡CH + H2CH2=H2 CH2=H2 + H2CH3CH3 R—CHO + H2R-CH2OH氧化反应燃烧或被空气中的O2氧化有机物分子得到氧原子或失去氢原子的反应2CH3CH2OH + O22CH3CHO + 2H2O2CH3CHO + O22CH3COOH 银镜反应CH3CHO + 2Ag<NH3>2OHCH3COONH4+2Ag↓+ 3NH3↑+ H2O红色沉淀反应CH3CHO + 2Cu<OH>2CH3COOH +Cu2O↓+ 2H2O取代反应卤代烃的水解反应在NaOH水溶液的条件下,卤代烃与水作用,生成醇和卤化氢的反应R-CH2X + H2O RCH2OH + HX 酯化反应酸<无机含氧酸或羧酸>与醇作用,生成酯和水的反应RCOOH + R'CH2OHRCOOCH2R′+ H2O酯的水解反应在酸或碱存在的条件下,酯与水作用生成醇与酸的反应RCOOR′+ H2O RCOOH + R'OHRCOOR′+ NaOH →RCOONa + R'OH〔六〕、烃与其重要衍生物之间的相互转化关系三、重难点突破考点一、烃的含氧衍生物的结构与性质[典例1]某有机物A的结构简式为,若取等质量的A分别与足量的Na、NaOH、新制的Cu<OH>2充分反应,理论上消耗这三种物质的物质的量之比为<>A.3∶2∶1B.3∶2∶2C.6∶4∶5D.3∶2∶3[解析]:能与Na反应的有醇羟基、酚羟基和羧基;能与NaOH反应的有酚羟基和羧基;能与新制Cu<OH>2反应的有醛基和羧基.为便于比较,可设A为1mol,则反应需消耗Na 3mol,需消耗NaOH 2mol;当A与新制Cu<OH>2反应时,1mol —CHO与2mol Cu<OH>2完全反应生成1mol —COOH,而原有机物含有1mol —COOH,这2mol —COOH需消耗1mol Cu<OH>2,故共需消耗3mol Cu<OH>2,即物质的量之比为3 ∶2 ∶3.[答案]D[变式1]分子式为C5H10O3的有机物,在一定条件下能发生如下反应:①在浓硫酸存在下,能分别与CH3CH2OH或CH3COOH反应;②在特定温度与浓硫酸存在下,能生成一种能使溴水褪色的物质;③在特定温度与浓硫酸存在下,还能生成一种分子式为C5H8O2的五元环状化合物.则C5H10O3的结构简式为<>A.HOCH2CH2COOCH2CH3B.HOCH2CH2CH2CH2COOHC.CH3CH2CH<OH>CH2COOHD.CH3CH<OH>CH2CH2COOH解析:C5H10O3"①在浓硫酸存在下,能分别与CH3CH2OH或CH3COOH反应〞说明该物质中有一个羟基和一个羧基;"②在特定温度与浓硫酸存在下,能生成一种能使溴水褪色的物质〞说明该物质能够发生消去反应生成不饱和物质;"③在特定温度与浓硫酸存在下,还能生成一种分子式为C5H8O2的五元环状化合物〞说明该物质中羟基和羧基之间有3个碳原子.答案:D[变式2]某课外活动小组对甲酸进行了如下的实验,以验证其含有醛基,并考查其化学性质,首先做了银镜反应.<1>在甲酸进行银镜反应前,必须在其中加入一定量的________,因为____________________________.<2>写出甲酸进行银镜反应的化学方程式________________________________________________________________________.<3>某同学很成功的做了银镜反应,他肯定没有进行的操作________<写字母>:A.用洁净的试管;B.在浓度为2%的NH3·H2O中滴入稍过量的浓度为2%的硝酸银;C.用前几天配制好的银氨溶液;D.在银氨溶液里加入稍过量的甲酸;E.用小火对试管直接加热;F.反应过程中,振荡试管使之充分反应.然后,同学们对甲酸与甲醇进行了酯化反应的研究:<4>写出甲酸和甲醇进行酯化反应的化学方程式________________________________________________________________________________________________.<5>选择甲装置还是乙装置好?________,原因是______________________________________________.<6>实验过程中选用的药品与试剂有:浓H2SO4、甲醇、甲酸还有________、________两种必备用品.<7>一同学用装有饱和氢氧化钠的三颈瓶接收甲酸甲酯,几乎没有收集到产物,请给予合理的解释__________________________________________________________.答案:<1>NaOH溶液银镜反应必须在碱性条件下进行<2>HCOOH+2Ag<NH3>2OH错误!CO2+2Ag↓+4NH3+2H2O<3>B、C、D、E、F<4>HCOOH+CH3OH错误!HCOOCH3+H2O<5>乙甲醇有毒,需密封操作<6>沸石饱和Na2CO3溶液<7>甲酸甲酯在NaOH溶液中发生水解考点二、同系物与同分异构体[典例2]〔2011·##高考·17节编〕写出同时满足下列条件的C〔OCHCOOHCH3〕的一种同分异构体的结构简式:.①能与金属钠反应放出H2;②是萘〔〕的衍生物,且取代基都在同一个苯环上;③可发生水解反应,其中一种水解产物能发生银镜反应,另一种水解产物分子中有5种不同化学环境的氧.[解析]条件③说明C的同分异构体中含有1个酯基〔C中仅含有3个氧原子〕,"其中一种水解产物能发生银镜反应〞说明C的同分异构体中的酯基由甲酸形成,C的同分异构体中仅含有3个氧原子,结合①可知C的同分异构体中含有1个羟基,联系C的同分异构体的另一种水解产物有5种处于不同化学环境下的氢原子和萘环结构,推断、书写C的同分异构体的结构简式;[答案][变式1]某分子式为C10H20O2的酯,在一定条件下可发生如下图的转化过程:则符合上述条件的酯的结构可能有<>A.2种B.4种C.6种D.8种解析:由转化图可知,B、C两物质分子的碳原子数相等,均含5个碳原子.C是醇、E是羧酸,由于C能经两步氧化生成E,所以C必是伯醇,可表示为C4H9—CH2OH,E可表示为C4H9—COOH,且C和E中—C4H9的结构相同.依据丁基<—C4H9>有4种可判断符合题意的酯有4种.答案:B考点三有机物分子式和结构式的确定[典例3]某研究人员发现一个破裂的小瓶中渗漏出一未知有机物A,有催泪作用.经分析A的相对分子质量为161,该化合物中除含有C、H元素外还含有一种卤族元素,且分子中只含有一个甲基.化合物A—F的转化关系如图所示,其中1 mol C与足量的新制Cu<OH>2溶液反应可生成1 mol D和1 mol Cu2O,B1和B2均为较稳定的化合物且互为同分异构体.已知〔1〕〔2〕一个碳原子上连有两个碳碳双键的结构〔—C=C=C—〕不稳定.请完成下列问题:〔1〕化合物A含有的官能团是___________.B1的相对分子质量是___________.〔2〕①、②、③的反应类型分别是___________、___________、___________.〔3〕写出A、F的结构简式:A. ______________________;F. _________________________.〔4〕写出C→D反应的化学方程式:____________________________________________.[解析]本题利用已知信息可知:据F的化学式可知卤原子为溴;A能与NaOH的醇溶液反应生成稳定的B1、B2,两者互为同分异构体,说明溴原子发生消去反应后有两种可能,同时又能被O 3氧化,所以一定含有碳碳双键,分子中只含有一个CH 3-,C 中只含有一个-CHO,说明甲基连在含碳碳双键的碳原子上,推知D 为羧酸,E 为含醇-OH 的羧酸,F 为酯类,所以反应①为消去反应,②为加成反应,③为酯化反应;根据F 的化学式C 6H 9BrO 2,计算不饱和度为2,可知F 中除含有碳氧双键外,还形成了一〔因为E 中不可能有碳碳双键〕,且分子中有一个甲基,其结构为,则E 的结构为,D 结构为,A 结构为.A 发生消去反应后脱去HBr,B 1、B 2的化学式为C 6H 8.其相对分子质量是80. [答案]:〔1〕碳碳双键、溴原子〔-Br 〕;80〔2〕消去反应;加成反应〔或还原反应〕;酯化反应〔或取代反应〕〔3〕〔4〕[变式1]A 是一种含碳、氢、氧三种元素的有机化合物.已知:A 中碳的质量分数为44.1%,氢的质量分数为8.82%;A 只含有一种官能团,且每个碳原子上最多只连一个官能团,A 能与乙酸发生酯化反应,但不能在两个相邻碳原子上发生消去反应.请填空: 〔1〕A 的分子式是;其结构简式是. 〔2〕写出A 与乙酸反应的化学方程式:.[解析]由于A 中碳的质量分数为44.1%,氢的质量分数为8.82%,故A 中氧的质量分数为1-44.1%-8.82%=47.08%.由此可算出C :H :O=5:12:4,分子式为C 5H 12O 4,A 只含有一种官能团,又能与乙酸发生酯化反应,该官能团必为羟基.但该羟基不能在两个相邻碳原子上发生消去反应,故邻位碳原子上应无氢原子.该分子中各原子已达到饱和,4个氧必为4个羟基.综上所述其结构为C 〔CH 2OH 〕4.[答案]:〔1〕C 5H 12O 4,C<CH 2OH>4 〔2〕C<CH 2OH>4 + 4CH 3COOH ∆−−−→浓硫酸C<CH 2OOCCH 3>4 +4H 2O四、课堂练习1.下列说法正确的是< >A .酸和醇发生的反应一定是酯化反应B .酯化反应中一般是羧酸脱去羧基中的羟基,醇脱去羟基上的氢原子C .浓H 2SO 4在酯化反应中只起催化剂的作用D.欲使酯化反应生成的酯分离并提纯,可以将弯导管伸入饱和Na2CO3溶液的液面下,再用分液漏斗分离答案:B2.某物质中可能有甲酸、乙酸、甲醇和甲酸乙酯4种物质中的1种或几种,在鉴定时有下列现象:<1>有银镜反应;<2>加入新制Cu<OH>2悬浊液沉淀不溶解;<3>与含酚酞的NaOH溶液共热发现溶液中红色逐渐消失以至无色,下列叙述正确的是<>A.几种物质都有B.有甲酸乙酯、甲酸C.有甲酸乙酯和甲醇D.有甲酸乙酯,可能有甲醇答案:D3.阿司匹林是一种解热、镇痛药,用于治疗伤风、感冒、头疼、发烧、神经痛、关节痛与风湿病等,近年来其治疗X围又进一步扩大到预防血栓形成,治疗心血管疾病等.阿司匹林的结构简式为:把阿司匹林放在足量的NaOH溶液中煮沸,能发生断裂的化学键是<>A.①④B.①③C.②③D.②④答案:A4.有机物甲能发生银镜反应,甲催化加氢还原成有机物乙,1mol乙跟足量的金属钠反应放出标准状况下的氢气22.4L.据此推断乙一定不是<>解析:由1mol乙<醇类物质>与钠反应生成1mol H2可推知乙分子中含有2个醇羟基.答案:D5.食品香精菠萝酯的生产路线<反应条件略去>如下:下列叙述错误的是<>A.苯酚和菠萝酯均可与酸性KMnO4溶液发生反应B.Cl—CH2COOH既能发生中和反应、取代反应,又能发生消去反应C.菠萝酯不能与NaOH溶液发生反应D.步骤<1>产物中残留的苯酚可用FeCl3溶液检验答案:BC6.A、B、C、D都是含碳、氢、氧的单官能团化合物,A水解得B和C,B氧化可以得到C或D,D氧化也得到C.若M<X>表示X的摩尔质量,则下式中正确的是<>A.M<A>=M<B>+M<C> B.2M<D>=M<B>+M<C>C.M<B><M<D><M<C> D.M<D><M<B><M<C>解析:本题转化关系可表示为:,可推知A为酯,B为醇,D为醛,C为羧酸,且B、C、D分子中所含碳原子数相同,A分子中所含碳原子数为B或C或D的2倍.从而可知,M<B>+M<C>>M<A>,M<D><M<B><M<C>,M<B>+M<C>>2M<D>.答案:D7.某有机物A是农药生产中的一种中间体,其结构简式如下.下列叙述中正确的是<>A.有机物A属于芳香烃B.有机物A可以与Br2的CCl4溶液发生加成反应C.有机物A与浓硫酸混合加热,可以发生消去反应D.1molA与足量的N aOH溶液反应,最多可以消耗3molNaOH答案:D8.在同温同压下,某有机物和过量Na反应得到V1L氢气,另一份等量的有机物和足量的Na HCO3反应得V2L二氧化碳,若V1=V2≠0,则有机物可能是<>解析:Na既能与羧基反应,又能与羟基反应,NaHCO3只能与羧基反应.能生成CO2与H2的量相等的只有A.答案:A9.咖啡酸<A>具有止血、镇咳、祛痰等疗效,它是芳香烃的衍生物,其分子结构模型如下左图所示<图中球与球之间的线代表化学键,如单键、双键等>.它具有如下右图转化关系:<1>写出A中除酚羟基外的含氧官能团名称________,A的结构简式________.<2>写出下列化学方程式或反应类型:①A―→B反应类型是______________________________________________________;②A―→D化学方程式为____________________________________________________.<3>1molA和Na2CO3溶液反应,最多消耗Na2CO3________mol.<4>E是1molA与1molH2加成后的产物,同时符合下列三个要求的E的同分异构体共有________种.①苯环上有三个取代基,其中两个为酚羟基'②属于酯类且能发生银镜反应'③苯环上的一氯代物只有两种[来源:Z##K]<5>现有咖啡酸和甲苯<C7H8>的混合物,它们的物质的量之和为n mol.该混合物在足量的氧气中完全燃烧,并将生成的产物通过盛有足量的无水硫酸铜的装置,则该装置增重________g.解析:<1>A的结构简式为:,所以A中含有的含氧官能团为酚羟基和羧基;<2>A―→B 是A分子中的碳碳双键与Br2发生加成反应,A―→D是A与CH3CH2OH发生酯化反应;<3>在有酚羟基存在的情况下,酚羟基、羧基与Na2CO3反应的产物均为NaHCO3,故1molA最多和3molNa2CO3反应;<4>E的分子式为C9H10O4,符合条件的同分异构体有:;<5>咖啡酸的分子式可改写为C7H8·<CO2>2,所以咖啡酸与甲苯以任意比混合,只要混合物的物质的量一定,燃烧后生成的水的量均为该混合物物质的量的4倍,即为72n g.答案:<1>羧基<3>3<4>4<5>72n10.有饱和一元脂肪酸和饱和一元脂肪醇形成的酯A.已知:①燃烧2.2gA可生成4.4gCO2和1.8g水;②1.76gA 和50mL0.5mol·L-1的氢氧化钠溶液共热后,为中和剩余的碱液,耗去0.2mol·L-1的盐酸25mL;③取A水解后所得的醇0.64g,跟足量钠反应时,放出224mLH2<标况>.求:<1>A的相对分子质量、分子式、结构简式.<2>写出下列反应的化学方程式:①A+NaOH错误!②A水解生成的醇+Na③A+O2错误!解析:<1>n<NaOH>=0.05L×0.5mol·L-1=0.025mol,n<HCl>=0.025L×0.2mol·L-1=0.005mol,所以n<A>=n<NaOH>-n<HCl>=0.02mol,则M<A>=错误!=88g·mol-1,2.2gA的物质的量为错误!=0.025mol.2.2gA燃烧后生成CO2和水的物质的量分别为:n<CO2>=4.4g/44g·mol-1=0.1mol,n<H2O>=1.8g/18g·mol-1=0.1mol,所以一个A分子中含C原子个数为4个,含氢原子个数为8个.[来源:Z##K]则A的分子式为C4H8O2.A水解后所得醇0.64g与钠反应产生的H2的物质的量n<H2>=错误!=0.01mol.所以M<醇>=错误!=32g·mol-1,为甲醇.所以酯A的结构简式为CH3CH2COOCH3.答案:<1>A的相对分子质量为88,分子式为C4H8O2,结构简式为CH3CH2COOCH3<2>①CH3CH2COOCH3+NaOH错误!CH3CH2COONa+CH3OH②2CH3OH+2Na―→2CH3ONa+H2↑③CH3CH2COOCH3+5O2错误!4CO2+4H2O[感悟高考真题]1.〔2010•##卷〕核黄素又称为维生素B2,可促进发育和细胞再生,有利于增进视力,减轻眼睛疲劳.核黄素分子的结构为:已知:有关核黄素的下列说法中,不正确的是:A.该化合物的分子式为C17H22N4O6B.酸性条件下加热水解,有CO2生成C.酸性条件下加热水解,所得溶液加碱后有NH3生成D.能发生酯化反应试题分析:本题是有机化学综合题,包含分子式、官能团性质、反应类型等内容.A、分子式的书写可以采用数数或分析不饱和度的方法.先检查C\N\O的个数,正确.再看氢的个数:20.故A错.B、酸性水解是N-CO-N部分左右还原羟基得到碳酸,分解为CO2.C、同样加碱后有NH3生成.D、因其有很多羟基,可以发生酯化反应.本题答案:A2.〔2011##高考11〕β—紫罗兰酮是存在于玫瑰花、番茄等中的一种天然香料,它经多步反应可合成维生素A1.下列说法正确的是A.β—紫罗兰酮可使酸性KMnO4溶液褪色B.1mol中间体X最多能与2molH2发生加成反应C.维生素A1易溶于NaOH溶液D.β—紫罗兰酮与中间体X互为同分异构体解析:该题以"β—紫罗兰酮是存在于玫瑰花、番茄等中的一种天然香料,它经多步反应可合成维生素A1〞为载体,考查学生对有机化合物的分子结构、官能团的性质、同分异构体等基础有机化学知识的理解和掌握程度.A.β—紫罗兰酮中含有还原性基团碳碳双键,可使酸性KMnO4溶液褪色.B.1mol中间体X含2mol碳碳双键和1mol醛基,最多能与3molH2发生加成反应C.维生素A1以烃基为主体,水溶性羟基所占的比例比较小,所以难于溶解于水或水溶性的溶液如NaOH溶液.D.β—紫罗兰酮比中间体X少一个碳原子,两者不可能互为同分异构体.答案:A3.〔2011##〕NM-3和D-58是正处于临床试验阶段的小分子抗癌药物,结构如下:关于NM-3和D-58的叙述,错误..的是A.都能与NaOH溶液反应,原因不完全相同B.都能与溴水反应,原因不完全相同C.都不能发生消去反应,原因相同D.遇FeCl3溶液都显色,原因相同解析:本题考察有机物的结构、官能团的判断和性质.由结构简式可以看出NM-3中含有酯基、酚羟基、羧基、碳碳双键和醚键,而D-58含有酚羟基、羰基、醇羟基和醚键.酯基、酚羟基和羧基均与NaOH溶液反应,但前者属于水解反应,后两者属于中和反应,A正确;酚羟基和碳碳双键均与溴水反应,前者属于取代反应,后者属于加成反应,B正确;NM-3中没有醇羟基不能发生消去反应,D-58中含有醇羟基,但醇羟基的邻位碳上没有氢原子,故不能发生消去反应,属于选项C不正确;二者都含有酚羟基遇FeCl3溶液都显紫色,D正确.答案:C4.<2011全国II卷7>下列叙述错误的是A.用金属钠可区分乙醇和乙醚B.用高锰酸钾酸性溶液可区分乙烷和3-乙烯C.用水可区分苯和溴苯D.用新制的银氨溶液可区分甲酸甲酯和乙醛解析:乙醇可与金属钠反应生成氢气,而乙醚不可以;3-乙烯属于烯烃可以使高锰酸钾酸性溶液褪色;苯和溴苯F :OCH 3CH 3OCH 3O.〔1〕熟悉键线式. 〔2〕判断反应类型.〔3〕了解有机化学研究方法,特别是H-NMR 的分析. 〔4〕酯化反应注意细节,如和H 2O 不能漏掉.〔5〕分析推断合成流程,正确书写结构简式.〔6〕较简单的同分异构体问题,主要分析官能团类别和位置异构. 答案:〔1〕C 14H 12O 3. 〔2〕取代反应;消去反应. 〔3〕4; 1︰1︰2︰6.〔4〕COOH CH 3OCH 3O浓硫酸△++H 2O CH 3O H COOCH 3CH 3OCH 3O〔5〕CH 2Br CH 3OCH 3O;CH 2CH 3OCH 3OCHOH OCH 3.〔6〕CH 2O H CHO ;O H CH 2CHO ;CH 3O CH O .6.〔2011##高考30,16分〕直接生成碳-碳键的反应是实现高效、绿色有机合成的重要途径.交叉脱氢偶联反应是近年备受关注的一类直接生成碳-碳键的新反应.例如:化合物Ⅰ可由以下合成路线获得:〔1〕化合物Ⅰ的分子式为____________,其完全水解的化学方程式为_____________〔注明条件〕. 〔2〕化合物Ⅱ与足量浓氢溴酸反应的化学方程式为_____________〔注明条件〕.〔3〕化合物Ⅲ没有酸性,其结构简式为____________;Ⅲ的一种同分异构体Ⅴ能与饱和NaHCO 3溶液反应放出CO 2,化合物Ⅴ的结构简式为___________________.〔4〕反应①中1个脱氢剂Ⅵ〔结构简式如下〕分子获得2个氢原子后,转变成1个芳香族化合物分子,该芳香族化合物分子的结构简式为_________________.〔5〕1分子与1分子在一定条件下可发生类似反应①的反应,其产物分子的结构简式为____________;1mol该产物最多可与______molH2发生加成反应.解析:本题考察有机物的合成、有机物的结构和性质、有机反应的判断和书写以与同分异构体的判断和书写.〔1〕依据碳原子的四价理论和化合物Ⅰ的结构简式可写出其分子式为C5H8O4;该分子中含有2个酯基,可以发生水解反应,要想完全水解,只有在解析条件下才实现,所以其方程式为H3COOCCH2COOCH3+2NaOH △2CH3OH+NaOOCCH2COONa.〔2〕由化合物Ⅰ的合成路线可知,Ⅳ是丙二酸,结构简式是HOOCCH2COOH,因此Ⅲ是丙二醛,其结构简式是HOCCH2CHO,所以化合物Ⅱ的结构简式是HOCH2CH2CH2OH.与浓氢溴酸反应方程式是HOCH2CH2CH2OH+2HBr △CH2BrCH2CH2Br+2H2O.〔3〕Ⅴ能与饱和NaHCO3溶液反应放出CO2,说明分子中含有羧基,根据Ⅲ的结构简式HOCCH2CHO可知化合物Ⅴ的结构简式为CH2=CHCOOH.〔4〕芳香族化合物必需含有苯环,由脱氢剂Ⅵ的结构简式可以写出该化合物的结构简式是〔5〕反应①的特点是2分子有机物各脱去一个氢原子形成一条新的C-C键,因此1分子与1分子在一定条件下发生脱氢反应的产物是.该化合物中含有2个苯环、1个碳碳三键,所以1mol该产物最多可与8molH2发生加成反应.答案:〔1〕C5H8O4;H3COOCCH2COOCH3+2NaOH △2CH3OH+NaOOCCH2COONa.〔2〕HOCH2CH2CH2OH+2HBr △CH2BrCH2CH2Br+2H2O.。
高考化学一轮复习 有机化学 第4讲 醛 羧酸 酯课件

第4讲
解析 欲使银镜反应实验成功,必须用 NaOH 溶液煮沸试管 以除去油污,以免析出的银难以附着在试管上。配制银氨溶 液时,一定注意不要把 AgNO3 溶液滴加到氨水中,应把氨水 滴加到 AgNO3 溶液中,且氨水不要过量,否则容易生成易爆 炸的 Ag3N。 答案 1NaOH 2AgNO3 稀氨水 最初产生的沉淀恰好溶解 3水浴
第4讲
(4)实验步骤:在一支试管里先加入 3 mL 乙醇,然后一边摇 动,一边慢慢地加入 2 mL 浓 H2SO4 和 2 mL 冰醋酸,按上图 所示连接好装置。用酒精灯小心均匀地加热试管 3~5 min, 产生的蒸气经导管通入到饱和 Na2CO3 溶液的液面上,此时 可以观察到有透明的油状液体浮在液面上。取下盛有饱和 Na2CO3 溶液的试管,并停止加热,振荡盛有饱和 Na2CO3 溶 液的试管后静置,待溶液分层后,可观察到上层的透明油状 液体——乙酸乙酯,并可闻到果香气味。
1为产生光亮的银镜,试管应先用
溶液煮沸,
倒掉煮沸液后再用清水将试管洗干净。
2配制银氨溶液时向盛有
溶液的试管中逐滴滴
加
溶液,边滴加边振荡直到
为止。
3加热时应用
加热,产生银镜的化学方程式是
__________________________________________________ ______________________。 解题指导 银氨溶液的配制:取 1 mL 2%的 AgNO3 溶液于洁 净的试管中,然后边振荡试管边逐滴滴入 2%的稀氨水,至最 初产生的沉淀恰好溶解为止,制得银氨溶液。
第4讲
解析 这是一组“形似而神不似”的问题。在(1)中,断键与 成键不受限制,加入的 H128O 与 CO 反应,使 CO2 中含 18O, 又通过 CO2 与 H2 的反应使 CO 中也含 18O,所以含氧的物质 中均含有 18O;对于(2)看其断键与成键规律:
醛、羧酸、酯

()
A.①②
B.②③
C.③④
D.①④
3.(2011·永州模拟)某有机化合物结构简式如图所示,关于
该化合物的下列说法中不正确的是
()
.
A.该化合物能发生消去反应 B.1 mol该化合物与NaOH溶液完全反应,最多可消耗
6 mol NaOH C.该化合物能和溴的CCl4溶液发生加成反应 D.该化合物在稀硫酸存在下水解所得产物之一可发生
消去反应
二、考察相关实验
1、醛基的检验
与新制 Ag(NH3)2OH 溶液 与新制 Cu(OH)2 悬浊液反
反应
应
反应 原理
RCHO+2Ag(NH3)2OH ―△ ―→RCOONH4+3NH3
RCHO+2Cu(OH)2―△ ―→
RCOOH+Cu2O↓+2H2O
+2Ag↓+H2O
反应 现象
产生光亮的银镜
羟基
止。
(3)从理论上讲,凡含有
的有机物,都可以发生
银镜反应[也可还原新制 Cu(OH)2 悬浊液]。主要有醛类、甲酸、 甲酸盐、甲酸酯、葡萄糖、麦芽糖等。醛类一般能发生银镜反应,
但能发生银镜反应的物质不一定是醛类。
1.某学生做乙醛还原性的实验,取1 mol·L-1的硫酸铜溶
液2 mL和0.4 mol·L-1的氢氧化钠溶液4 mL,在一个试
管里混合后加入0.5 mL 40%的乙醛溶液加热至沸腾,
无砖红色沉淀,实验失败的原因是
()
A.氢氧化钠的量不够
B.硫酸铜的量不够
C.乙醛溶液太少
D.加热时间不够
解析:据题意知CuSO4与NaOH溶液反应,由于NaOH不
足量,因此Cu2+不能完全沉淀,而此反应要求NaOH是过
醛 羧酸 酯

考纲要求
• 以甲醛、乙醛、乙酸、乙酸乙酯、脂肪酸、甘油酯为例,了解
官能团在化合物中的作用。掌握各主要官能团的性质和主要化 学反应。
• 了解在生活和生产中常见有机物的性质和用途。
醛类
醛(RCHO):烃分子中的H被-CHO取代后所生成的烃的衍生物
O 官能团:醛基-CHO或 -C-H
饱和一元醛通式:CnH2nO
• 醛基的数目:一元醛、多元醛
• 烃基饱和程度:饱和醛、不饱和醛 • 烃基种类:脂肪醛、芳香醛 O 酮:分子中含有C=O(羰基)的有机物,R-C-R(R不代表H) 饱和一元酮和饱和一元醛的通式相同,等碳原子时互为同 分异构体。 含醛基的有机物:醛、甲酸、甲酸酯、葡萄糖(多羟基醛)、麦 芽糖等 空间构型:羰基以及与羰基直接相连的原子处于同一平面上。
• 官能团:-COOH 通式: R-COOH • 饱和一元酸:CnH2nO2
羧酸的物理性质
• 甲酸、乙酸、丙酸有强烈的刺激性气味的无色液体,含有4—9
个碳原子的饱和一元羧酸是具有腐败气味的油状液体,饱和高 级脂肪酸,常温下呈固体。不饱和高级脂肪酸,常温下呈液态。
二元羧酸和芳香酸都是结晶固体。
• 低级羧酸可与水混溶,随着相对分子质量的增大,溶解度逐渐 减小. • 羧酸的溶沸点随着分子质量的增加而升高。
△
(NH4)2CO3 +6NH3+4Ag↓+2H2O 2Cu2O↓+CO2↑+5H2O O O C C
△
ONH4
OHC-CHO+4Cu(OH)2
△
2Cu2O↓ +HOOC-COOH+4H2O
醛基的检验
• 能发生银镜反应
• 与新制的Cu(OH)2共热煮沸有砖红色沉淀生成 CH3 -C= CH-CH2-CH2-C=CH-CHO CH3 CH3 先加足量的银氨溶液(或新制的Cu(OH)2)使醛基氧化。然 后再用酸性KMnO4溶液(或溴水)检验碳碳双键,碳碳双键能 使酸性KMnO4溶液(或溴水)褪色 例:柠檬醛的检验:
有机化学考点二醛、羧酸、酯

【要点解读】1.醛(1)醛:由烃基或氢原子与醛基相连而构成的化合物,可表示为RCHO。
甲醛是最简单的醛。
饱和一元醛分子的通式为C n H2n O (n≥1)。
(2)甲醛、乙醛的比较物质颜色气味状态密度水溶性甲醛无色刺激性气味气体—易溶于水乙醛无色刺激性气味液体比水小与水互溶(3)醛类物质既有氧化性又有还原性,其氧化、还原关系为醇错误!醛错误!羧酸,以乙醛为例完成下列反应的化学方程式:特别提醒(1)醛基只能写成—CHO 或,不能写成-COH。
(2)醛与新制的Cu(OH)2悬浊液反应时碱必须过量且应加热煮沸.(3)银镜反应口诀:银镜反应很简单,生成羧酸铵,还有一水二银三个氨。
2.羧酸(1)羧酸:由烃基或氢原子与羧基相连构成的有机化合物.官能团为—COOH。
饱和一元羧酸分子的通式为C n H2n O2(n≥1)。
(2)甲酸和乙酸的分子组成和结构物质分子式结构简式官能团甲酸CH2O2HCOOH—COOH和—CHO乙酸C2H4O2CH3COOH—COOH(3)羧酸的化学性质羧酸的性质取决于羧基,反应时的主要断键位置如图:①酸的通性(以乙酸为例)乙酸是一种弱酸,其酸性比碳酸强,在水溶液里的电离方程式为CH3COOH CH3COO-+H+.②酯化反应CH3COOH和CH3CH错误!OH发生酯化反应的化学方程式为CH3COOH+C2H518OH错误!CH3CO18OC2H5+H2O。
3.酯(1)概念①酯:羧酸分子羧基中的—OH被-OR′取代后的产物,简写为RCOOR′,官能团为COO(R′)。
②酯的物理性质错误!错误!③酯的化学性质特别提醒酯的水解反应为取代反应;在酸性条件下为可逆反应;在碱性条件下,能中和产生的羧酸,反应能完全进行.④酯在生产、生活中的应用a.日常生活中的饮料、糖果和糕点等常使用酯类香料.b.酯还是重要的化工原料。
【重难点指数】★★★【重难点考向一】醛、羧酸、酯的结构与性质【典型例题1】某有机化合物的结构简式为,下列有关该物质的叙述正确的是()A.1 mol该物质最多可以消耗3 mol NaB.1 mol该物质最多可以消耗7 mol NaOHC.不能与Na2CO3溶液反应D.易溶于水,可以发生加成反应和取代反应【答案】B【名师点睛】(1)多官能团有机物性质的确定步骤第一步,找出有机物所含的官能团,如碳碳双键、碳碳三键、醇羟基、酚羟基、醛基等;第二步,联想每种官能团的典型性质;第三步,结合选项分析对有机物性质描述的正误(注意:有些官能团性质会交叉。
化学知识点-醛、羧酸、酯

醛知识点(主要以甲醛、乙醛为例说明):醛:烃基与醛基相连的化合物。
饱和一元醛的通式:C n H 2n O 。
1、物理性质:甲醛:最简单的醛,又称“蚁醛”,无色具有刺激性气味气体,对人眼、鼻子有刺激性作用,可用来制作农药、消毒剂、树脂。
易溶于水和乙醇(任意比例互溶),35%-40%的甲醛水溶液称为福尔马林,通常用来防腐、消毒和漂白。
----------在烃的含氧衍生物中,只有甲醛在标准状况下是气体。
乙醛:无色、有刺激性气味液体,密度比水小,易挥发,能与水和乙醇任意比互溶。
乙醛对呼吸道和眼睛有刺激性作用。
2、化学性质:醛的官能团:醛基-CHO(但有醛基的物质不一定是醛,如甲酸、甲酸某酯等)1)氧化性:特征实验一:在洁净的试管里加入1ml 2%的硝酸银溶液,然后,一边摇动试管,一边逐滴滴加2%的稀氨水,直到最初产生的沉淀恰好溶解为止,制得银氨溶液。
再滴入3滴乙醛溶液,振荡后把试管放在水浴里加热。
现象:在试管壁上产生光亮的银镜。
结论:银氨溶液被还原成了银,乙醛被氧化成乙酸。
银氨溶液的形成过程:AgNO 3+NH 3·H 2O→AgOH↓+NH 4NO 3AgOH 常温下极不稳定分解:2AgOH→Ag 2O (暗红色)+H 2O 继续滴加氨水:Ag 2O+4NH 3·H 2O →2Ag(NH 3)2++2OH -+3H 2O 总离子方程式:Ag ++2NH 3·H 2O →Ag(NH 3)2++2H 2O 乙醛与银氨溶液反应方程式:CH 3CHO+2Ag(NH 3)2OH →CH 3COOH+2Ag ↓+4NH 3+H 2O甲酸会与氨继续反应:HCOOH+NH 3→HCOONH 4银镜反应是检验有机物中是否含有醛基的重要方法。
注意事项:(1)银氨溶液必须随用随配,不能久置,否则可能会产生爆炸性物质。
(2)应将稀氨水滴入硝酸银中,至产生的沉淀刚好溶解为之,需严格控制氨水的量,若氨水过量会产生爆炸性物质。
高三有机化学复习 第4讲醛 羧酸 酯

现象)。则Z的结构简式为
。
基础回归
1.结构
羧酸酯的官能团“
”,通式
饱和一元羧酸与饱和一元醇所生成酯的通式为 CnH2nO2(n≥2) 。
2.性质 (1)物理性质:一般酯的密度比水 小,难溶于水,
易溶于乙醇、乙醚等有机溶剂,低级酯是具有果香
气味的液体。
(2)化学性质 水解反应:
要点精讲
要点一 醛基的检验 1.检验醛基主要有以下两种方法 (1)银镜反应
醛具有较强的还原性,能和银氨溶液发生反应被氧 化为羧酸,同时得到单质银,若控制好反应条件, 可以得到光亮的银镜,实验时应注意以下几点: ①试管内壁必须洁净; ②必须水浴加热,不可用酒精灯直接加热; ③加热时不可振荡和摇动试管; ④须用新配制的银氨溶液; ⑤乙醛用量不宜太多。 实验后,银镜可用硝酸浸泡,再用水洗而除去。
2.醛的性质 (1)物理性质
乙醛是无色有刺激性气味、 易 挥发的液体,能与 水、乙醇、氯仿等 互 溶;甲醛是无色有刺激性气味 的气体,易溶于水,35%~40%的甲醛水溶液叫 福尔 马林 。
(2)化学性质
①加成反应:醛基中的羰基(
HCN等加成,但不与Br2加成。
RCHO+H2 ②氧化反应
RCH2OH
a.燃烧: 2 CH3CHO+ 5 O2
b.催化氧化: 2 RCHO+O2
c.被弱氧化剂氧化:
RCHO+ 2 Ag(NH3)2OH +2Ag↓+H2O (银镜反应)。
)可与H2、
4CO2+4H2O 。 2RCOOH 。
RCOONH4+3NH3
RCHO+ 2Cu(OH)2 (生成红色沉淀)。
高考化学一轮总复习课件醛羧酸酯

THANKS
感谢观看
还原反应
某些羧酸在还原剂的作用下可以被还原成相应的醛或醇。 这一反应在有机合成中具有一定的应用价值。
03
酯类化合物
酯类化合物的定义与性质
定义
物理性质
酯是一类由羧酸与醇通过酯化反 应生成的有机化合物,通式为 RCOOR'。
酯类化合物多为无色或淡黄色液 体,具有芳香气味,密度一般比 水小,难溶于水,易溶于有机溶 剂。
常见醛类化合物的结构与性质
甲醛
最简单的醛类化合物,无色气体,具有强烈的刺激性和还原性。能 与蛋白质结合生成不溶性的蛋白质盐,使蛋白质变性而凝固。
乙醛
无色液体,具有刺激性气味。能与氢气、氨等发生加成反应;也能 被氧化成乙酸。
苯甲醛
无色液体,具有苦杏仁味。能与氢气、氨等发生加成反应;也能被氧 化成苯甲酸。
水解反应
生物柴油制 备
许多香料都是酯类化合物或其衍生物,通过合成不同 结构的酯类化合物可以制备出各种香型的香料,满足
人们的不同需求。
香料合成
利用动植物油脂通过酯交换反应制备生物柴油,是一 种可再生、环保的能源替代品。生物柴油具有燃烧性 能好、污染少等优点。
04
醛、羧酸、酯之间的关系与转化
醛、羧酸、酯之间的转化关系
酸碱中和滴定等方法测定生成的羧酸和醇的含量。
醛、羧酸、酯在有机合成中的应用
醛作为合成中间体
醛可以通过还原、氧化、缩合等反应转化为其他有机化合物,如醇、羧酸、酯等。因此,在有机合成中,醛常被用作 合成中间体。
羧酸的衍生化反应
羧酸可以通过酯化、酰卤化、酰胺化等反应转化为相应的衍生物,这些衍生物在有机合成中具有广泛的应用。
融合多学科知识,拓宽知识视野
高中化学——醛 羧酸与酯
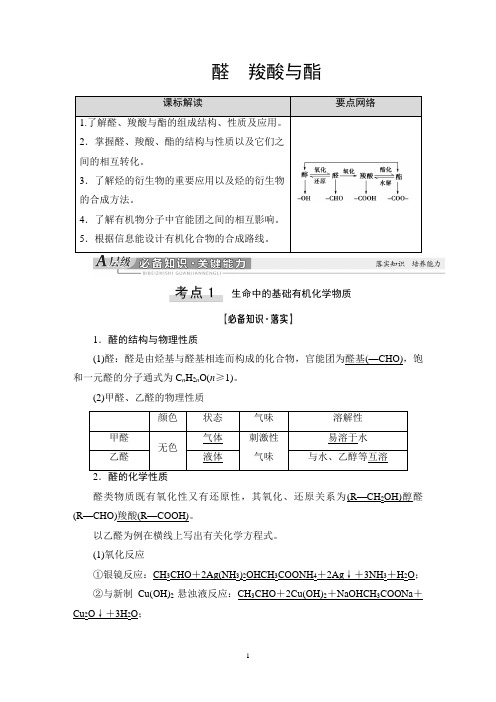
醛羧酸与酯课标解读要点网络1.了解醛、羧酸与酯的组成结构、性质及应用。
2.掌握醛、羧酸、酯的结构与性质以及它们之间的相互转化。
3.了解烃的衍生物的重要应用以及烃的衍生物的合成方法。
4.了解有机物分子中官能团之间的相互影响。
5.根据信息能设计有机化合物的合成路线。
生命中的基础有机化学物质1.醛的结构与物理性质(1)醛:醛是由烃基与醛基相连而构成的化合物,官能团为醛基(—CHO),饱和一元醛的分子通式为C n H2n O(n≥1)。
(2)甲醛、乙醛的物理性质颜色状态气味溶解性甲醛无色气体刺激性气味易溶于水乙醛液体与水、乙醇等互溶醛类物质既有氧化性又有还原性,其氧化、还原关系为(R—CH2OH)醇醛(R—CHO)羧酸(R—COOH)。
以乙醛为例在横线上写出有关化学方程式。
(1)氧化反应①银镜反应:CH3CHO+2Ag(NH3)2OHCH3COONH4+2Ag↓+3NH3+H2O;②与新制Cu(OH)2悬浊液反应:CH3CHO+2Cu(OH)2+NaOHCH3COONa+Cu2O↓+3H2O;③催化氧化反应:2CH 3CHO +O 2――→催化剂△2CH 3COOH ; ④乙醛可被酸性KMnO 4溶液氧化生成乙酸。
(2)还原反应:与氢气的加成反应CH 3CHO +H 2――→催化剂△CH 3CH 2OH 。
注意:①醛基只能写成—CHO 或,不能写成—COH 。
②醛与新制的Cu(OH)2悬浊液反应时碱必须过量且应加热煮沸。
③醛类使酸性KMnO 4溶液或溴水退色,二者均为氧化反应。
(3)醛的应用和对环境、健康产生的影响①醛是重要的化工原料,广泛应用于合成纤维、医药、染料等行业。
②35%~40%的甲醛水溶液俗称福尔马林;具有杀菌(用于种子杀菌)和防腐性能(用于浸制生物标本)。
③劣质的装饰材料中挥发出的甲醛是室内主要污染物之一。
④甲醛与苯酚发生缩聚反应生成酚醛树脂。
3.醛与酮()可以为异类异构体,如CH 3CH 2CHO 与互为同分异构体。
高中化学【 醛 羧酸 酯]
![高中化学【 醛 羧酸 酯]](https://img.taocdn.com/s3/m/a9113bbc7e21af45b207a82f.png)
6.醛和酮的区别与联系 官能团
官能团位置
形式
醛 区别
碳链末端(最简 单的醛是甲醛)
酮
碳链中间(最简
单的酮是丙酮)
联系
碳原子数相同的饱和一元醛和饱和一元酮互为同 分异构体
夯基础•小题
1.判断正误(正确的打“√”,错误的打“×”)。
(1)甲醛分子中的所有原子都在同一平面上
(√ )
(2)醛基的结构简式可以写成—CHO,也可以写成—COH
成反应制得,符合题意。
答案:D
知识点二 羧酸的结构 与性质
考必备•清单
1.羧酸的定义 由 __烃__基__与__羧__基__ 相 连 构 成 的 有 机 化 合 物 。 官 能 团 为 __—__C_O__O_H____ , 饱 和 一 元 羧 酸 分 子 的 通 式 为 _C__nH__2_nO__2_(n_≥__1_)_。
答案:BC
3.下列物质中不能发生银镜反应的是
()
解析:分子中有醛基的有机物可以发生银镜反应,若分子 中没有醛基,则不能发生银镜反应。丙酮分子中只有羰基, 没有醛基,所以本题选 D。 答案:D
4.不能由醛或酮加氢还原制得的醇是
()Leabharlann A.CH3CH2OHB.CH3CH2CH(OH)CH3
C.(CH3)3CCH2OH
(1)酸的通性(以乙酸为例) 乙酸是一种弱酸,其酸性比碳酸_强__,在水溶液中的电离方 程式为_C__H_3_C__O_O__H____C__H_3_C_O__O_-_+__H__+___。 乙酸分别与 Na2CO3 和 NaHCO3 反应的化学方程式: _N_a_2_C_O__3_+__2_C_H__3C__O_O__H_―__→__2_C__H_3_C_O__O_N__a_+__H_2_O__+__C_O__2↑_, _N__a_H_C__O_3_+__C_H__3_C_O__O_H__―__→__C_H__3C__O_O__N_a_+__H__2_O_+__C__O_2_↑_。
2015届高考一轮课件第九章醛 羧酸 酯(图片版)

三、酯 1.酯 (1)组成和结构 官能团:—COO—(酯基) ,饱和一元羧酸和饱和一元醇形成的酯分子通式为 CnH2nO2或RCOOR′。 (2)物理性质密度比水小,难溶于水,易溶于有机溶剂
(3)化学性质——水解反应。
RCOOH+R′OH
RCOONa+R′OH
【总结5】乙酸乙酯的制备实验1.反应原料:乙酸、 乙醇、浓硫酸、饱和 Na2CO3 溶液。 2.实验原理
密度/g· cm-3 0.79 1.05 0.90 1.84
学生在实验室制取乙酸乙酯的主要步骤如下:
①在 30 mL 的大试管 A 中按体积比 1∶4∶4 的比例配 制浓硫酸、乙醇和乙酸的混合溶液;②按图 连接好装 置(装置气密性良好),用小火均匀地加热装有混合溶液
的大试管 5~10min;③待试管 B 收集到一定量的产物 后停止加热,撤去试管 B并用力振荡,然后静置等待 分层;④分离出乙酸乙酯层、洗涤、干燥。
很强,会使乙酸乙酯彻底水解。
(5)实验中小火加热保持微沸,这样有利于产物的生成 和蒸发,提高乙酸乙酯的产率。(6)饱和 Na2CO3 溶液 溶解乙醇。
的作用是:减小酯在水中溶解度(利于分层);中和乙酸;
(7)酯化反应中可用 18O 作示踪原子,证明在酯化反应 其余部分结合成酯。(8)酯化反应是一个可逆反应
应后的澄清溶液中再加入溴水或酸性 KMnO4 溶液检验
碳碳双键(或碳碳三键)。
【例 2】有机物 A 是合成二氢荆芥内酯的重
要原料,其结构简式为正确的是 A.先加酸性高锰酸钾溶液,后加银氨溶液,微热 B.先加溴水,后加酸性高锰酸钾溶液 C.先加银氨溶液,微热,再加入溴水 D.先加入新制氢氧化铜,加热煮沸,酸化后再加溴水
(2)实验现象:产生红色沉淀。(3)量的关系:RCHO~ 2Cu(OH)2~Cu2O,HCHO~4Cu(OH)2~2Cu2O。 (4)注意事项:①新制 Cu(OH)2 悬浊液要随用随配,不
2020年高考化学(鲁科版)总复习 第9章 第4节 醛 羧酸与酯

后
否含有碳碳双键。]
限
时
集
训
返 首 页
课
堂
反
2.(2015·山东高考)分枝酸可用于生化研究,其结构简
馈
真
式如图所示。下列关于分枝酸的叙述正确的是( )
题
体
考
A.分子中含有 2 种官能团
验
点
B.可与乙醇、乙酸反应,且反应类型相同
课
后
C.1 mol 分枝酸最多可与 3 mol NaOH 发生中和反应
限
真
(4)醛的化学性质
题 体
验
考 点
醛类物质既有氧化性又有还原性,其氧化、还原关系为(_R_—__C__H_2_O_H__)醇__―还―原→
醛(R—CHO)―氧―化→_羧__酸__(_R_—__C_O__O_H__) 。
课 后 限
时
集
训
返 首 页
以乙醛为例在横线上写出有关化学方程式。
课 堂
反
①氧化反应:
返 首 页
课 堂 反 馈
D [水杨酸与甲醇发生酯化反应可生成冬青油,酯化反应属于取代反应,A 真
题
项正确;阿司匹林的分子式为
C9H8O4,阿司匹林在酸性条件下水解可得水杨酸,
体 验
考
点 B 项正确;冬青油苯环上有 4 种不同化学环境的氢原子,故其苯环上的一氯取代
物有 4 种,C 项正确;冬青油中含有的酚羟基和酯基都能与 NaOH 溶液反应,
课 后
限
故不能用 NaOH 溶液除去冬青油中少量的水杨酸,D 项错误。]
时 集
训
返 首 页
课
堂
反
5.(2019·洛阳模拟)有机物 A、B 均为合成某种抗支气管哮喘药物的中间体, 馈
高考化学一轮复习专题 醛 羧酸 酯讲

复习目标:1、 了解醛、羧酸、酯的典型代表物的组成和结构特点。
2、 了解醛、羧酸、酯的主要化学性质。
3、 了解醛、羧酸、醇和酯等烃的衍生物之间的相互转化关系。
4、 结合生产和生活实际,了解常见的醛、羧酸和酯的重要应用,了解某些有机化合物对环境和健康可能产生的影响,关注有机物的安全使用问题。
基础知识回顾:一、醛 1、概念醛是由烃基与醛基相连而构成的化合物。
2、分子结构分子式 结构简式 官能团甲醛 CH 2O HCHO—CHO乙醛C 2H 4OCH 3CHO3、物理性质颜色 状态 气味 溶解性 甲醛 无色 气态 刺激性气味 易溶于水 乙醛无色液态刺激性气味与水、乙醇互溶4、化学性质(以CH 3CHO 为例) (1)加成反应醛基中的羰基( )可与H 2、HCN 等加成,但不与Br 2加成。
RCHO+H 2 错误! RCH 2OH—C —O(2)氧化反应A.燃烧:2CH3CHO+ 5O2错误!4H2O+4CO2B.催化氧化:2RCHO+O2错误!2RCOOHC.被弱氧化剂氧化:RCHO+ 2Ag(NH3)2OH 错误!RCOONH4+3NH3+2Ag↓+H2O(银镜反应)。
RCHO+2Cu(OH)2错误!RCOOH+Cu2O↓+2H2O (生成红色沉淀)。
【注意】1、凡是含有醛基的化合物均具有氧化性、还原性,1mol的醛基(—CHO)可与1mol的H2发生加成反应,与2mol的Cu(OH)2或2mol的[Ag(NH3)2]+发生氧化反应。
2、醇(R—CH2OH)错误!R—CHO 错误!R—COOH分子组成关系:C n H2n+1CH2OH 错误!C n H2n+1CHO 错误!C n H2n+1COOH相对分子质量:M M—2M+143、可在一定条件下与H2加成的有:苯环、醛、酮、—N=N—等,但酯基不行。
【典型例题1】橙花醛是一种香料,结构简式为:(CH3)2C===CHCH2CH2C(CH3)===CHCHO 下列说法正确的是()A.橙花醛不可以与溴发生加成反应B.橙花醛可以发生银镜反应C.1mol橙花醛最多可以与2mol H2发生加成反应D.橙花醛是乙烯的同系物【迁移训练1】有机物A是合成二氢荆芥内酯的重要原料,其结构简式为,下列检验A中官能团的试剂和顺序正确的是()A.先加酸性高锰酸钾溶液,后加银氨溶液,微热B.先加溴水,后加酸性高锰酸钾溶液C.先加银氨溶液,微热,再加入溴水D.先加入新制氢氧化铜,微热,酸化后再加溴水二、羧酸1、羧酸概述:由羧基与烃基相连构成的有机物。
知识点梳理:醛、羧酸、酯知识点归纳

知识点梳理:醛、羧酸、酯知识点归纳一、醛醛是一类有机化合物,其官能团是醛基(CHO)。
醛的通式可以表示为 RCHO,其中 R 代表烃基。
(一)醛的物理性质醛在常温下,甲醛是气体,其他常见的醛如乙醛、丙醛等是液体。
醛的沸点比相对分子质量相近的醇低,这是因为醛分子间不能形成氢键。
醛的溶解性与醇相似,低级醛能与水混溶,随着碳原子数的增加,醛在水中的溶解度逐渐减小。
(二)醛的化学性质1、加成反应醛基中的碳氧双键可以发生加成反应。
例如,在催化剂的作用下,醛可以与氢气发生加成反应生成醇。
以乙醛为例:CH₃CHO + H₂ → CH₃CH₂OH2、氧化反应(1)醛能被氧气氧化为羧酸。
例如:2CH₃CHO + O₂ →2CH₃COOH(2)醛能被弱氧化剂氧化,常见的弱氧化剂有银氨溶液和新制的氢氧化铜悬浊液。
银镜反应:醛与银氨溶液反应生成银镜。
例如,乙醛与银氨溶液反应的化学方程式为:CH₃CHO + 2Ag(NH₃)₂OH → CH₃COONH₄+2Ag↓ + 3NH₃+ H₂O与新制氢氧化铜反应:醛与新制的氢氧化铜悬浊液反应生成砖红色沉淀。
例如,乙醛与新制氢氧化铜反应的化学方程式为:CH₃CHO +2Cu(OH)₂+NaOH → CH₃COONa + Cu₂O↓ + 3H₂O(三)重要的醛1、甲醛(HCHO)甲醛是最简单的醛,具有强烈的刺激性气味,有毒。
甲醛的水溶液俗称福尔马林,具有杀菌、防腐的作用,常用于制作生物标本。
2、乙醛(CH₃CHO)乙醛是一种有刺激性气味的液体,易挥发,能跟水、乙醇等互溶。
二、羧酸羧酸是一类有机化合物,其官能团是羧基(COOH)。
羧酸的通式可以表示为 RCOOH,其中 R 代表烃基。
(一)羧酸的物理性质羧酸的沸点比相对分子质量相近的醇高,这是因为羧酸分子间可以形成氢键。
低级羧酸能与水混溶,随着碳原子数的增加,羧酸在水中的溶解度逐渐减小。
(二)羧酸的化学性质1、酸性羧酸具有酸性,能使紫色石蕊试液变红。
第九章 有机化合物性质及其应用 第4讲 醛 羧酸 酯

M 与 A 均属于高分子聚合物,1 mol A 消耗 n mol 金属钠,放出 气体的物质的量为 n/2 mol,D 错误。
答案 D
考点一
知识梳理
递进题组
返回
递进题组 题组一
1 2 3
题组二
4
5
6
题组三
7
题组三
根据有机物的性质确定官能团或有机物的结构
7.有机物 A 是常用的食用油抗氧化剂,分子式为 C10H12O5,可发 生如下转化:
考点一
知识梳理
递进题组
返回
知识梳理
3.酯 (1)酯:羧酸分子羧基中的 —OH 产物。可简写为 RCOOR′ (2)酯的物理性质 被
—OR′
取代后的 。
,官能团为
难
易
考点一
知识梳理
递进题组
返回
知识梳理
(3)酯的化学性质 无机酸 + H2O △ H2 O + NaOH——→ △
。
。
特别提醒
酯的水解反应为取代反应; 在酸性条件下为可逆反应;
考点一
知识梳理
递进题组
返回
递进题组 题组一
1 2 3
题组二
4
5
6
题组三
7
考点一
知识梳理
递进题组
返回
递进题组 题组一 题组一
1 2 3
题组二
4
5
6
题组三
7
正确理解醛、羧酸、酯的结构特点
解析
1.下列物质不属于醛类的物质是 ( )
考点一
知识梳理
递进题组
返回
递进题组 题组一 题组一
1 2 3
题组二
4
5
考点一
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第4讲醛羧酸酯[考纲要求] 1.了解烃的含氧衍生物(醛、羧酸、酯)的组成、结构特点和性质。
2.认识不同类型化合物之间的转化关系。
3.了解常见的有机化学反应类型。
4.结合实际,了解某些有机化合物对环境和健康的影响,关注有机化合物的安全使用问题。
考点一醛、羧酸和酯的结构与性质1.醛(1)概念烃基与醛基相连而构成的化合物,可表示为RCHO。
甲醛是最简单的醛。
饱和一元醛的通式为C n H2n O。
(2)甲醛、乙醛物质颜色气味状态密度水溶性甲醛无色刺激性气味气体易溶于水乙醛无色刺激性气味液体比水小与水互溶(3)醇氧化还原醛――→氧化羧酸以乙醛为例完成下列反应的化学方程式:特别提醒(1)醛基只能写成—CHO或,不能写成—COH。
(2)醛与新制的Cu(OH)2悬浊液反应时碱必须过量且应加热煮沸。
(3)银镜反应口诀:银镜反应很简单,生成羧酸铵,还有一水二银三个氨。
2.羧酸(1)羧酸:由烃基或氢原子与羧基相连构成的有机化合物。
官能团为—COOH。
饱和一元羧酸分子的通式为C n H2n O2。
(2)甲酸和乙酸的分子组成和结构物质分子式结构简式官能团甲酸CH2O2HCOOH —COOH和—CHO乙酸C2H4O2CH3COOH —COOH(3)羧酸的化学性质羧酸的性质取决于羧基,反应时的主要断键位置如图:①酸的通性乙酸是一种弱酸,其酸性比碳酸强,在水溶液里的电离方程式为CH3COOH CH3COO-+H+。
②酯化反应CH3COOH和CH3CH182OH发生酯化反应的化学方程式为CH3COOH+C2H185 CH3CO18OC2H5+H2O。
OH浓H2SO4△3.酯(1)酯:羧酸分子羧基中的—OH被—OR′取代后的产物。
可简写为RCOOR′,官能团为。
(2)酯的物理性质(3)酯的化学性质特别提醒酯的水解反应为取代反应;在酸性条件下为可逆反应;在碱性条件下,能中和产生的羧酸,反应能完全进行。
(4)酯在生产、生活中的应用①日常生活中的饮料、糖果和糕点等常使用酯类香料。
②酯还是重要的化工原料。
深度思考1.你是怎样理解有机化学中的氧化反应和还原反应的?请完成下列表格:利用氧化反应或还原反应,可以实现有机物官能团的转变,实现醇、醛、羧酸等物质间的相互转化。
如:CH 4――→Cl 2光CH 3Cl ――→水解CH 3OH氧化还原HCHO ――→氧化HCOOH21733答案 是同系物,因为它们分子中都含有羧基和同类型的烃基,即分子结构相似,并且在组成上相差15个CH 2原子团,完全符合同系物的定义。
3.判断正误,正确的划“√”,错误的划“×”(1)乙醛分子中的所有原子都在同一平面上 (×) (2)凡是能发生银镜反应的有机物都是醛(×) (3)醛类既能被氧化为羧酸,又能被还原为醇(√) (4)完全燃烧等物质的量的乙醛和乙醇,消耗氧气的质量相等(×)(5)在水溶液里,乙酸分子中的—CH 3可以电离出H +(×)(2011·福建理综,8C)4.(选修5P 63-3)有机物A 的分子式为C 3H 6O 2,它与NaOH 溶液共热蒸馏,得到含B 的蒸馏物。
将B 与浓硫酸混合加热,控制温度可以得到一种能使溴的四氯化碳溶液褪色,并可作果实催熟剂的无色气体C 。
B 在一定温度和催化剂存在的条件下,能被空气氧化为D ,D 与新制的Cu(OH)2悬浊液加热煮沸,有砖红色沉淀和E 生成。
写出下述变化的反应方程式。
(1)A ―→B (2)B ―→C (3)B ―→D (4)D ―→E 答案 (1)HCOOC 2H 5+NaOH ――→△HCOONa +C 2H 5OH (2)CH 3CH 2OH ――→浓H 2SO 4170 ℃CH 2===CH 2↑+H 2O (3)2CH 3CH 2OH +O 2――→催化剂△2CH 3CHO +2H 2O (4)CH 3CHO +2Cu(OH)2+NaOH ――→△CH 3COONa +Cu 2O ↓+3H 2O题组一 正确理解醛、羧酸、酯的结构特点 1.下列物质不属于醛类的物质是( )答案 B解析 本题考查的是醛的概念。
根据醛的定义可以判断出OCH 3COH 不属于醛类,而是酯类。
2.由下列5种基团中的2个不同基团两两组合,形成的有机物能与NaOH 反应的有( )①—OH ②—CH 3 ③—COOH ④ ⑤—CHOA .2种B .3种C .4种D .5种特别注意 HO —与—COOH 相连时为H 2CO 3。
解题方法 ①⎩⎪⎨⎪⎧②③④⑤②⎩⎪⎨⎪⎧③④⑤③⎩⎪⎨⎪⎧④⑤ ④—⑤组合后看物质是否存在。
答案 D解析 两两组合形成的化合物有10种,其中—OH 与—COOH 组合形成的H 2CO 3为无机物,不合题意。
只有 (甲酸)、CH 3COOH 、、OHC —COOH 5种有机物能与NaOH 反应。
3.某中性有机物C 8H 16O 2在稀硫酸作用下加热得到M 和N 两种物质,N 经氧化最终可得到M ,则该中性有机物的结构可能有( )A .1种B .2种C .3种D .4种审题指导 中性有机物C 8H 16O 2能水解,则该物质为酯,由信息知N 能氧化为M ,则N 为醇,M 为酸,且碳架结构相同,N 只能为伯醇。
答案 B解析 中性有机物C 8H 16O 2在稀硫酸作用下可生成两种物质,可见该中性有机物为酯类。
由“N 经氧化最终可得到M ”,说明N 与M 中碳原子数相等,碳架结构相同,且N 应为羟基在碳链端位的醇,M 则为羧酸,从而推知该中性有机物的结构只有和两种。
题组二 多官能团的识别与有机物性质的预测4.科学家研制出多种新型杀虫剂代替DDT ,其中一种的结构如图。
下列关于该有机物的说法正确的是(双选)( )A.该有机物既能发生氧化反应,又能发生酯化反应B.与FeCl3溶液发生反应后溶液显紫色C.1 mol A最多可以与4 mol Cu(OH)2反应D.1 mol A最多与1 mol H2加成答案AC解析该有机物的醛基可发生氧化反应,醇羟基可发生酯化反应,A正确;该有机物中无苯环,没有酚羟基,B不正确;1 mol A中含2 mol —CHO、1 mol,则最多可与4 mol Cu(OH)2反应,C正确;可与3 mol H2发生加成反应,D不正确。
5.迷迭香酸是从蜂花属植物中提取得到的酸性物质,其结构简式如图所示。
下列叙述正确的是()A.迷迭香酸与溴单质只能发生取代反应B.1 mol迷迭香酸最多能和9 mol氢气发生加成反应C.迷迭香酸可以发生水解反应、取代反应和酯化反应D.1 mol迷迭香酸最多能和5 mol NaOH发生反应答案 C解析该有机物结构中含有酚羟基和碳碳双键,能与溴发生取代反应和加成反应,A项错;1分子迷迭香酸中含有2个苯环,1个碳碳双键,则1 mol迷迭香酸最多能和7 mol 氢气发生加成反应,B项错;1分子迷迭香酸中含有4个酚羟基、1个羧基、1个酯基,则1 mol迷迭香酸最多能和6 mol NaOH发生反应,D项错。
6.聚乙炔衍生物分子M的结构简式及M在稀硫酸作用下的水解反应如图所示。
下列有关说法不正确的是()MA.M与A均能使酸性高锰酸钾溶液和溴水褪色B.B中含有羧基和羟基两种官能团,能发生消去反应和酯化反应C.1 mol M与热的烧碱溶液反应,可消耗2n mol NaOHD.A、B、C各1 mol分别与金属钠反应,放出气体的物质的量之比为1∶2∶2答案 D解析由M的结构简式及A的分子式可知二者均含有碳碳双键,均能使酸性高锰酸钾溶液和溴水褪色,A正确;由M的结构简式可知其水解后产物B(C3H6O3)的分子结构中含有羧基和羟基两种官能团,能发生消去反应和酯化反应,B正确;1 mol M的单体可以消耗2 mol NaOH,则1 mol M可消耗2n mol NaOH,C正确;M与A均属于高分子聚合物,1 mol A消耗n mol金属钠,放出气体的物质的量为n/2 mol,D错误。
题组三根据有机物的性质确定官能团或有机物的结构7.有机物A是常用的食用油抗氧化剂,分子式为C10H12O5,可发生如下转化:已知B的相对分子质量为60,分子中只含一个甲基。
C的结构可表示为(其中:—X、—Y均为官能团)。
请回答下列问题:(1)根据系统命名法,B的名称为__________。
(2)官能团—X的名称为________,高聚物E的链节为________________________。
(3)A的结构简式为______________。
(4)反应⑤的化学方程式为______________________________________。
(5)C有多种同分异构体,写出其中2种符合下列要求的同分异构体的结构简式________。
Ⅰ.含有苯环Ⅱ.能发生银镜反应Ⅲ.不能发生水解反应(6)从分子结构上看,A具有抗氧化作用的主要原因是____(填序号)。
a.含有苯环b.含有羰基c.含有酚羟基答案(1)1-丙醇(2)羧基(写出上述3个结构简式中的任意2个即可)(6)c解析E为高分子化合物,则D有可能是烯烃,B是醇,结合B的相对分子质量为60可推知B为丙醇,只有一个甲基,则B为CH3CH2CH2OH,D为CH2===CH—CH3,E为。
C能与NaHCO3溶液反应产生气泡,则含有—COOH,与FeCl3发生显色反应,含有酚羟基,则C的结构简式只能是,则A的结构简式为。
(1)CH3CH2CH2OH的系统命名为1-丙醇。
(2)因为C只有7个碳原子,所以Y只能是—OH,X是—COOH。
(3)由反应条件可基本确定是酯的水解,A的结构简式为HOHOCOOCH2CH2CH3HO。
(4)该反应是—COOH与HCO-3的反应,产物为CO2和H2O。
(5)不发生水解反应则不含结构,能发生银镜反应则含有—CHO。
(6)酚羟基具有还原性,能被O2氧化,因此A可作为抗氧化剂使用。
1.多官能团有机物性质的确定步骤第一步,找出有机物所含的官能团,如碳碳双键、碳碳三键、醇羟基、酚羟基、醛基等;第二步,联想每种官能团的典型性质;第三步,结合选项分析对有机物性质描述的正误。
(注意:有些官能团性质会交叉。
例如,碳碳三键与醛基都能被溴水、酸性高锰酸钾溶液氧化,也能与氢气发生加成反应等)。
2.官能团与反应类型考点二烃的衍生物转化关系及应用深度思考写出以乙醇为原料制备的化学方程式(无机试剂任选)并注明反应类型。
答案 (1)CH 3CH 2OH ――→浓H 2SO 4170 ℃CH 2===CH 2↑+H 2O(消去反应)题组一有机物的推断1.由乙烯和其他无机原料合成环状酯E和高分子化合物H的示意图如下所示:请回答下列问题:(1)写出以下物质的结构简式:A________,F__________,C__________。
