病毒载量检测方法及其意义
浅谈昆明慢性丙型肝炎高病毒载量基因的分型及临床意义

1 资料 与方 法 11 一般资料 1 例 为慢 性丙型肝 炎高病毒 载量患者 , . l l HC —RNA>1 0 E 0 I ML。 V . 3 + 6U/ 男性6 例, 0 女性5 例 , l 年龄
l- 3 。 17 岁
12 . 方法
1 2. H CV . 1 RNA提 取 取 患者 血 清 l O lI u  ̄ 人 O 1 2 0 l NA提取液 , 合摇匀,ri后8 0 离 mi 去除 0uR t 昆 5 n 0 0X a g 62 n, 上清 液 。 O uRNA提取 液 , 合摇 匀 ,0 0 离 2 n, 加2 o l 混 8 0 g 6 mi 去 X 除上 清 液 。 7 %乙醇 ( F C 溶 解 )0u ?合 摇 匀 ,0 0X 加 5 D P 水 40 l N 8 0 g离 2mi 去 除上 清 液 , 复 一 次 。 开 管 盖 , 5℃ 干 燥 6 n, 重 打 6 1mi 盖 上 管 盖 备 用 或一7 ℃冻 存 备 用 。 0 n, O 1 22 RNA逆转录及扩增 在上述提取 的RNA管中分 . .
《 求医问药 半月刊 Se 下 ekMei l n s h Mein 2 1 年 第 9 d a A dA kT e dc e 0 1 c i 卷 第 9 期
3 3
℃)轻摇(0 5 X )避 光反应 imi, , 3— 0 g , 0 n 去除结合 液。 加入3ml 0 杂交液 (0 3 " , 2- 0 C)室温轻摇 , 重复洗涤3 , 次 每次5 n 去除杂 mi, 交液 。 加入 新 配 制 的 显 色 液 , 光 反 应 5 0 n 去 除显 色 液 。 避 —1mi , 加 入 3 ml 液 , 温 轻 摇 3 n, 去 溶 液 。 入 3ml 除 离子 0 溶 室 mi 弃 加 0 去 水, 室温轻摇3 n 取出杂交膜条 ; 吸水纸吸去膜条表 面水 mi , 用 分 。 用 扫 描 仪 扫 描 膜 条 得 出信 号 值 , 使 根据 信 号 值 采 用 专 业 分 析软件进行基 因型结果判断( 各基因型别位点c tf值根据统 u of 计学方法计算得 出 , 已预设在分析软件 中) 。
EBV+DNA定量检测在诊断儿童EB病毒感染中的临床意义

Methods:Fluorescence
quantitative polymerase chain reaction was used to detect EBV
load in peripheral blood of 205 children with fever.Atypical lymphocyte in peripheral blood shaped
to 6 years
0(2=1.0246.P=0.3 1 1 4).EBV
old were higher,there was
cases
DNA positive rate from l to 3 years and from 4
no
significant differences among different ages
lylnphocytes
rate was significantly higher than that EBV DNA—negative
children with
fever.and the difference was statistically
significant(X2:31.3551,P<0.O001).④The 42
Results:@The
42 out of 205
cases
with fever were positive for EBV DNA in peripheral
blood,the positive rate was 20.5%,and 23 males and 1 9 females,the difference Wash’t significant
Children
目
录
引言…………………………………………………………………………………….1
儿童外周血单个核细胞EB病毒DNA载量检测在病情评估中的临床意义

儿童外周血单个核细胞EB病毒DNA载量检测在病情评估中的临床意义蔡勉珊;方炳雄;黄丽旋;游丽莎;秦泽鸿;谢城【摘要】目的探讨儿童外周血单个核细胞EB病毒(EBV)DNA载量检测在病情评估中的临床意义.方法统计2016年1月~2017年12月本院儿科收治的1171例发热患儿EBV检测阳性率.将符合纳入标准的146例EBV阳性的患儿,分为高病毒载量组和低病毒载量组,分析两组患儿的临床资料和实验室指标.结果以发热为主诉的患儿,EBV阳性率为20.32%,其中7岁以内的儿童比大龄儿童EBV阳性检测率高(P<0.05);高病毒载量组患儿扁桃体炎发生率、淋巴结肿大发生率和外周血异常淋巴细胞比例、淋巴细胞计数、淋巴细胞比例,以及血清中TBA、LD、LDH和CK-MB水平,均比低病毒载量组高(P<0.05);高病毒载量组患儿热退时间和住院天数比低病毒载量组长(P<0.05).结论儿童外周血单个核细胞EB病毒DNA载量检测有助于病情评估,EBV载量可预测患儿的临床转归情况.【期刊名称】《中国医药科学》【年(卷),期】2018(008)014【总页数】5页(P7-11)【关键词】儿童;EBV病毒DNA;外周血单个核细胞;病情评估【作者】蔡勉珊;方炳雄;黄丽旋;游丽莎;秦泽鸿;谢城【作者单位】广东省普宁市人民医院儿科,广东普宁 515300;广东省普宁市人民医院检验科,广东普宁 515300;广东省普宁市人民医院检验科,广东普宁 515300;广东省普宁市人民医院检验科,广东普宁 515300;广东省普宁市人民医院检验科,广东普宁 515300;广东省普宁市人民医院儿科,广东普宁 515300【正文语种】中文【中图分类】R720.5EB 病毒(Epstein-barr virus, EBV)为双链DNA病毒,是一种嗜人B淋巴细胞病毒。
EBV感染是儿科比较常见的一类病毒性传染病,感染时,症状轻重不一,多以扁桃体炎、淋巴结肿大、肝脾肿大为主要临床特征[1-2]。
病毒载量检测对1型艾滋病病毒的诊断价值分析

Mod Diagn Treat现代诊断与治疗2021Jan32(1)艾滋病是由于感染人类免疫缺陷病毒(HIV)而引发的全身性疾病,该疾病可导致人体出现不同程度的免疫缺陷,且随着病程越长,免疫缺陷越严重,因此应早诊断早治疗,以降低疾病损伤[1]。
HIV分为HIV-1型和HIV-2型,以HIV-1为主。
目前临床多采用免疫印迹实验(WB)确诊艾滋患者,但诊断过程中,仍会出现部分不确定感染患者[2]。
根据技术要求,HIV抗体不确定的样本需要结合同时期流行病学资料,并于4周后进行随访检测,且在随访期间,带型患者有进展但是检测结果并不满足阳性标准的患者,仍需随访至第8周,再次检测,整体耗时2个月,时间较长,可能会增加病毒传播风险,同时可能延误患者早期治疗。
当人体被HIV-1感染后,病毒载量随之增加,且会对淋巴系统进行攻击,从而对机体免疫系统造成损伤,而有部分研究学者认为,病毒载量检测可提高HIV-1的检出率[3]。
基于此,本研究选取我院治疗的128例疑似艾滋病患者作为研究对象,旨在分析病毒载量检测对1型艾滋病病毒的诊断价值。
报道如下。
1资料与方法1.1一般资料选取2018年8月~2020年3月我院收治的128例疑似艾滋病患者,所有患者均进行酶联免疫吸附试验、WB检测,不确定患者进行病毒载量检测。
其中男82例、女46例;年龄26~39(32.31±5.80)岁。
1.2纳入与排除标准纳入标准:(1)近3个月内未服用免疫抑制剂等药物;(2)首次检查;(3)患者同意翻阅病历资料。
排除标准:(1)抗病毒药物治疗史;(2)依从性差、无法完全配合检查;(3)无其他免疫系统疾病。
1.3方法HIV抗体检测程序和方法根据《全国艾滋病检测技术规范(2015年修订版)》[4]进行。
1.3.1筛查阳性复试实验分别使用北京金豪公司HIV-1+2抗体和珠海丽珠公司HIV-1+2抗原抗体进行两种不同酶联免疫吸附试验。
操作严格按照试剂盒说明书进行。
艾滋病检测技术HIV-1核酸检测规范

艾滋病检测技术HIV-1核酸检测规范1 范围本章规定了HIV-1核酸定性和定量检测(病毒载量)的意义、实验室要求、检测方法、质量控制及结果判定标准,适用于HIV-1核酸的定性检测和定量的测定。
2 核酸检测的意义核酸检测可用于HIV感染诊断、血液筛查、病程评估及抗病毒治疗效果监测。
2.1 感染诊断2.1.1 作为补充试验:用于筛查试验有反应但抗体确证试验不确定或阴性样本的判定;对筛查试验有反应但抗体确证试验不确定或阴性的疑似艾滋病晚期患者需将核酸检测、临床病史和CD4+T淋巴细胞计数检测结果综合判断。
对于抗体筛查试验阴性但免疫功能低下者,也可进行核酸检测,结合临床综合判断。
2.1.2 急性期诊断:对近期有明确流行病学史的个体,包括患有性病或有性病史,有同性和异性性接触不安全性行为,有共用注射器吸毒史,有医源性暴露史,有职业暴露史,HIV/AIDS 患者的配偶或性伴侣,HIV/AIDS 母亲所生子女等,如抗体筛查试验无反应,可通过核酸检测判定是否为急性期感染。
核酸检测结果阴性或低于最低检测限不能排除HIV-1感染。
2.1.3 HIV-1暴露婴儿感染早期诊断HIV-1感染母亲所生小于18个月龄的婴儿,不同时间的两次HIV-1核酸检测均为阳性即可作出诊断。
18个月龄以上儿童诊断与成人相同。
2.2 血液筛查:对献血者及采供血机构的原料血浆进行核酸检测,可及时发现窗口期感染,降低输血的“残余危险度”,减少二代传播。
2.3 抗病毒治疗效果监测HIV感染者和艾滋病病人经抗病毒药物治疗后,定期进行HIV-1病毒载量检测,可判断抗病毒药物治疗的疗效。
病毒载量结果动态分析,对决定是否继续使用原定的治疗方案以及是否需要更改治疗方案起到重要作用。
一般启动抗病毒治疗6个月后应进行病毒载量检测,以监测治疗效果,每年应检测一次。
治疗前进行检测可了解病人的病毒载量基线,有助于评价治疗后效果。
如适时重复检测病毒载量,没有低于检测限,需要考虑治疗是否失败。
病毒载量检测方法及其意义

工效率
6.5小时48份标本
48小时192份标本
二、病毒载量检测的意义
早期诊断 婴儿的早期诊断:感染HIV的母亲所生婴儿小 于18个月时,不能按照常规检测程序进行抗体检测 来确证是否感染了HIV。这种情况下,采集婴儿不 同时间的样本进行HIV核酸检测。 也可使用集合法对采供血机构的原料血浆及 HIV抗体阴性的高危人群样品进行核酸检测,及时 发现窗口期感染者,降低“残余危险度”,预防传 播。
指导抗病毒治疗及疗效判定
通常在病毒载量达到一定水平后(如>3500050000拷贝/毫升)抗病毒治疗才显示良好的 治疗效果。治疗后通过病毒水平的检测能够 确定治疗是否有效。理想的结果是治疗24周 后,病毒水平会控制在检测线以下。
.耐药性监测
可用于HIV耐药性检测和监测。治疗后病毒载 量得不到有效控制时被认为治疗失败。引起 治疗失败的原因之一是病毒对治疗药物的敏 感性降低或不敏感,也就是产生了耐药。对 病毒载量>1000拷贝/毫升的样本进行耐药性 检测对临床医生修改治疗方案有一定的帮助。
Roche
Simens(Bayer)
RT-PCR bDNA 产物为DNA,易发生污染,不对目标进行扩增,只进 对实验室区域划分严格 行信号放大
检测
辣根过氧化物酶标记检测 探针,TMB底物显色 用样品OD值和定标物OD 值的比值计算结果,需要 稀释扩增产物,检测范围 小,并且受酶活性、底物 氧化显色的影响 每次检测12或24个标本 需要设一个阴性、一个弱 阳性和一个强阳性对照 48人份/盒 每次试验12人份分装 一旦打开试剂盒,需要在 1个月内使用完48人份, 否则试剂失效 8小时24份标本
标记的探针与该复合体杂交结合。与化学发光底物共同孵育,所产生的光强度与
东北制药HIV病毒载量检测试剂技术参数

东北制药HIV病毒载量检测试剂技术参数
包3-病毒载量试剂(东北制药)
东北制药HIV病毒载量检测试剂技术参数
1.原理和方法:采用磁珠法提取血清或血浆样本中病毒RNA,采用Taqman探针法进行HIV-1的实时荧光定量RT-PCR检测。
2.定量方法:外部标准品定量
3.检测项目:HIV-1RNA定量检测
4.最低检出限:≤50IU/mL(约28copies/mL,置信度≥95%。
)
5.线性范围:2×102~1×109IU/mL
6.特异性:100%。
7.性能指标:Ct值的变异系数<10%,浓度变异系数<50%
8.样品类型:血清或血浆
9.样品体积和规格:可选0.2mL、0.4mL;48T/盒
10.样品处理能力:可以同时进行检测8~96个样品
11.检测效率:96个样品的检测时间约为4小时
12.检测亚型:HIV-1A,B,C,D,AE,F,G,AG-GH和O组,共9个亚型
13.抗污染方案:核酸提取及反应体系建立设备:Hamilton Microlab STAR,TECAN EVO全自动液体工作站;核酸扩增设备:ABI7500荧光定量PCR仪。
14.检测平台:核酸提取及反应体系建立设备:Hamilton Microlab STAR,TECAN EVO全自动液体工作站;核酸扩增设备:ABI7500荧光定量PCR仪。
15.注册资格:须提供国食药监械(准)字号注册证。
16.供货计划:按用户要求数量准时分批次供货,到货试剂有效期大于10个月。
艾滋病实验室检测【最新】

艾滋病实验室检测HIV/AIDS 的实验室检测主要包括HIV抗体检测、HIV核酸定性和定量检测、CD4+ T淋巴细胞计数、HIV耐药检测等。
HIV⁃1/2抗体检测是HIV感染诊断的金标准,HIV核酸检测(定性和定量)也用于HIV 感染诊断;HIV 核酸定量(病毒载量)和CD4+ T 淋巴细胞计数是判断疾病进展、临床用药、疗效和预后的两项重要指标;HIV 耐药检测可为HAART方案的选择和更换提供指导。
1.HIV⁃1/2 抗体检测:包括筛查试验和补充试验。
HIV⁃1/2抗体筛查方法包括酶联免疫吸附试验(ELISA)、化学发光或免疫荧光试验、快速试验(斑点ELISA和斑点免疫胶体金或胶体硒、免疫层析等)、简单试验(明胶颗粒凝集试验)等。
补充试验方法包括抗体确证试验(免疫印迹法,条带/线性免疫试验和快速试验)和核酸试验(定性和定量)。
筛查试验呈阴性反应可出具HIV⁃1/2抗体阴性报告, 见于未被HIV感染的个体,但窗口期感染者筛查试验也可呈阴性反应。
若呈阳性反应,用原有试剂双份(快速试验)/双孔(化学发光试验或ELISA)或两种试剂进行重复检测,如均呈阴性反应,则报告为HIV抗体阴性;如一阴一阳或均呈阳性反应,需进行补充试验。
补充试验:抗体确证试验无HIV特异性条带产生,报告HIV⁃1/2抗体阴性;出现条带但不满足诊断条件的报告不确定,可进行核酸试验或2~4周后随访,根据核酸试验或随访结果进行判断。
补充试验HIV⁃1/2 抗体阳性者,出具HIV⁃1/2抗体阳性确证报告。
核酸试验:核酸定性检测结果阳性报告HIV⁃1核酸阳性,结果阴性报告HIV⁃1核酸阴性。
病毒载量检测结果低于检测线报告低于检测线;>5 000拷贝/ml 报告检测值;检测线以上但≤5 000拷贝/ml建议重新采样检测,临床医生可结合流行病学史、CD4+、CD8+T淋巴细胞计数或HIV抗体随访检测结果等进行诊断或排除诊断。
2.CD4+T淋巴细胞检测CD4+T淋巴细胞是HIV感染最主要的靶细胞,HIV感染人体后,出现CD4+T淋巴细胞进行性减少,CD4+/CD8+T淋巴细胞比值倒置,细胞免疫功能受损。
新冠病毒的快速诊断试剂与检验方法

新冠病毒的快速诊断试剂与检验方法新冠病毒(COVID-19)自2019年底以来迅速传播,成为全球关注的焦点。
快速且准确的诊断方法对于控制疫情、及时隔离患者和阻断传播链至关重要。
在病毒检测的进程中,快速诊断试剂和检验方法起着关键的作用。
本文将介绍新冠病毒快速诊断试剂和检验方法的最新进展。
一、快速诊断试剂1. RT-PCR(逆转录聚合酶链反应)逆转录聚合酶链反应(RT-PCR)是目前最常用的新冠病毒检测方法。
它通过提取病毒RNA,利用逆转录酶将RNA转录成DNA,再进行聚合酶链反应,扩增病毒基因片段。
RT-PCR具有高灵敏度和特异性,能够检测患者体内非常低水平的病毒载量。
然而,RT-PCR需要在专门的实验室条件下进行,并且需要几个小时的测试时间,不适用于大规模筛查。
2. 抗原快速检测抗原快速检测是一种新兴的检测方法,采用抗原检测试剂盒。
这种试剂盒可以直接检测新冠病毒的抗原,通常使用鼻咽拭子或唾液样本进行检测。
抗原快速检测具有快速、便携和高效的优点,可以在30分钟内提供结果。
它适用于初步的新冠病毒筛查和群体检测,但其灵敏度相对较低,可能会出现假阴性结果。
3. 抗体检测抗体检测是通过检测人体内新冠病毒感染后产生的抗体来确定感染情况。
抗体检测可以通过血清、血浆或其他体液样本进行,可以分为IgM和IgG两种类型。
IgM抗体在感染初期阶段产生,随后逐渐转为IgG抗体,持续时间较长。
抗体检测具有快速、简便和成本低廉的优点,适用于流行病学调查和免疫学研究。
但是,抗体检测在早期感染时的敏感度较低,并且不能直接检测病毒,仅能确定是否感染过病毒。
二、检验方法1. 核酸序列分析核酸序列分析是一种基于新冠病毒基因组的检验方法。
通过分离和提取病毒RNA,对其进行测序和分析,以确定感染者的病毒株类型、变异情况和传播链。
核酸序列分析对于疫情追踪、回溯和监测变异病毒株具有重要意义。
它可以帮助科学家了解病毒传播动态和病毒的演化过程。
病毒载量每年查几次才够?

病毒载量多久测一次?病毒载量检测是HIV携带者定期需要进行的检测之一,一般情况下,治疗后的感染者,血液中病毒载量都处在一个很低甚至查不出的水平,“四免一关怀”政策下,大部分地区都有每年1次或2次的免费病毒载量检测。
什么是HIV病毒载量感染HIV以后,病毒在体内快速复制,血浆中可检测出病毒RNA(病毒载量),一般用血浆中每毫升HIVRNA的拷贝数或每毫升国际单位(IU/ml)来表示。
检测结果在“测不到”到一个具体的庞大数字不等,通常情况下若病毒量在100 copies/ml以下是“低病毒载量",100000copies/ml以上“高病毒载量”。
通常在抗病毒治疗开始后半年以内,病毒载量就可以达到查不出的水平,否则就应该咨询你的主治医师是否需要更换药物方案或是否可能存在耐药的情况。
随着抗逆转录病毒药物越来越高效,根据美国卫生和人类服务部(DHHS)在2014年5月1日发布了指导方针,病毒载量被单独用来确定治疗是否有效,不再强调使用CD4计数作为衡量治疗成功的标准。
病毒载量检测的意义CD4计数是直接反映免疫状态的以及间接反映治疗效果的指标,而病毒载量直接反映了血液中的病毒数量以及抗病毒治疗的效果。
HIV病毒载量是衡量治疗效果的金标准,可以借此预测疾病进程,指导治疗方案调整,评估治疗效果等。
也可作为HIV感染诊断的补充试验,用于急性期/窗口期诊断、晚期感染者诊断、HIV感染诊断和小于18个月龄的婴幼儿HIV感染诊断。
作为HIV确证的补充实验之一,在确证试验无法确证HIV,即无HIV特异性条带产生,或出现条带但不满足诊断条件,可进行病毒载量检测,也就是所谓的核酸试验,若出现连续2次核酸检测结果>5 000拷贝/ml,即可作为确证HIV感染的依据。
同时HIV病毒载量检测也是作为新生儿HIV感染的确证手段。
当然,对感染者来说,病毒载量肯定是越低越好!*U=U,病毒载量测不出,不会通过性行为传播HIV 当感染者达到了血液中病毒载量无法检出之时可以获得•更低的HIV感染的发病率和病死率;•更低的非艾滋病相关疾病的发病率和病死率;•重建或者改善免疫功能;•使感染者获得更长的期望寿命,提高生活质量;•减少异常的免疫激活,降低癌症风险,使得CD4/CD8比值趋于正常;•最大程度地抑制病毒复制,减少耐药株产生的可能;•减少HIV的传播、预防母婴传播,阻断由性传播HIV的可能。
病毒性感冒的分子生物学检测方法及意义

病毒性感冒的分子生物学检测方法及意义近年来,随着生物科技的快速发展,分子生物学检测方法已成为病毒性感冒诊断的重要手段。
病毒性感冒是由多种病毒引起的一种常见病,其中以流感病毒最为常见。
传统的病毒性感冒诊断主要依靠病原学检测,如病毒培养、免疫荧光、抗原检测等方法。
这些检测方法存在着敏感度低、特异性差等限制,而分子生物学检测方法则以其高度灵敏、特异、快速和准确等特点,成为病毒性感冒诊断的重要手段。
分子生物学检测方法主要包括PCR(聚合酶链式反应)、实时荧光PCR和核酸微阵列等。
其中PCR是应用最广泛的分子生物学技术,它能够在短时间内扩增某一段DNA序列。
对于病毒性感冒的检测,可以选择不同区域的基因进行扩增,如Hemagglutinin (HA)、Neuraminidase(NA)和Matrix(M)等基因。
通过PCR扩增后,可以采用凝胶电泳、荧光探针等方法进行检测。
实时荧光PCR是在PCR的基础上发展起来的一种新技术。
它可以实现PCR过程和检测结果的同时完成,具有高灵敏度、高准确性和高通量等优点。
实时荧光PCR检测原理是在PCR过程中不断检测荧光信号的变化,当PCR产物与特异性荧光探针结合时,荧光强度增加,反之则减少。
通过实时监测荧光信号的变化,可以确定扩增产物的数量和特异性,达到高灵敏度的检测结果。
核酸微阵列(Microarray)是另一种基于分子生物学技术的检测方法。
它可以同时检测多个基因的表达水平,并进行大规模筛查。
在病毒性感冒的检测中,可以选择多个高度特异的基因进行检测,提高检测的灵敏度和特异性。
核酸微阵列技术的核心是借助于DNA探针和标记技术进行检测,具有高通量、高度特异的优点。
病毒性感冒的分子生物学检测方法在诊断临床病例中发挥了重要的作用。
它可以检测出低病毒载量、不可培养的病毒和新型病毒等,有助于尽早发现、诊断、治疗和防控病毒性感冒。
特别是在流感疫情高发的时期,分子生物学检测方法可以快速检测出感染流感病毒的患者,有助于及时隔离和治疗,降低流感病毒传播的风险。
人乳头瘤病毒检测方法及其应用进展

人乳头瘤病毒检测方法及其应用进展1. 引言1.1 背景介绍人乳头瘤病毒(HPV)是一种常见的性传播病毒,可以引起多种疾病,包括宫颈癌、外阴癌、阴茎癌、肛门癌等。
据统计,HPV感染是导致宫颈癌的主要原因之一,全球每年约有50万人死于宫颈癌。
对HPV的检测和诊断至关重要。
随着科技的不断进步,人们对HPV的检测方法也在不断更新和完善。
目前,常见的HPV检测方法包括基因检测方法、蛋白检测方法和病毒载量检测方法。
这些方法不仅能够准确快速地检测出HPV感染,还可以帮助医生进行早期诊断和治疗。
本文旨在介绍人乳头瘤病毒的检测方法及其应用进展,希望通过系统的分析和总结,为进一步的研究和临床应用提供参考,从而更好地应对HPV感染所带来的健康问题。
1.2 研究目的人乳头瘤病毒(HPV)是一种常见的性传播病毒,已被证实与多种癌症,特别是宫颈癌的发生密切相关。
开发准确、灵敏的HPV检测方法对于早期诊断和预防HPV相关疾病具有重要意义。
本文旨在系统总结各种HPV检测方法的原理、优缺点以及应用进展,为进一步提高HPV检测的准确性和效率提供参考。
本研究旨在探讨基因检测、蛋白检测和病毒载量检测等方法在HPV相关疾病的临床应用前景,为临床医生提供更多的治疗选择和疾病预防策略。
通过本研究的深入探讨,有望为未来的HPV检测方法研究和临床应用提供宝贵的参考和指导。
2. 正文2.1 人乳头瘤病毒检测方法人乳头瘤病毒(HPV)是一种广泛存在于人类中的病毒,被认为是引起多种癌症的主要致癌因素之一。
及早检测HPV感染对于癌症的预防和治疗至关重要。
目前,人乳头瘤病毒的检测方法主要包括基因检测方法、蛋白检测方法和病毒载量检测方法。
基因检测方法通过检测HPV的DNA或RNA来确定感染情况。
这种方法的优势在于能够准确识别不同型号的HPV,对于研究HPV的感染机制和流行病学具有重要意义。
常用的基因检测方法包括PCR技术、原位杂交法和基因芯片技术。
蛋白检测方法则是通过检测HPV蛋白在体内的表达水平来判断感染情况。
HIV核酸检测技术及应用

常用的病毒载量检测方法
主要核酸扩增和信号放大扩增两种方法 Q (,生物梅里埃) (,罗氏) m2000(,雅培) 440 (西门子) 国内:凯杰(匹基),科华,达安、东北
制药、万泰 丽珠、科华等
血浆样本
病毒载量分析仪
扩增技术 ( ,核酸序列依赖性扩增法)
引物1 延伸
逆转录酶 H和 引物 2延伸 逆转录酶 T7 聚合酶
初筛+复检+
补充试验(核酸试验)
定性检测试剂盒
试剂:必须是经国家食品药品监督管理总局注册批 准、在有效期内的试剂。严格按说明书操作。全球 目前正式用于临床诊断1 急性期感染的核酸检测试 剂比较少 公司生产的 1 核酸定性试剂盒 公司生产的M2000 1 定性检测试剂盒 公司生产的® ® ® 1 2.0
核酸检测在新版规范主要内容
u 新增补充试验的概念,补充试验包括抗体确证试验和核 酸试验(定性和定量试验)
u 新增核酸检测流程,对复检结果有反应的情况,增加了 可以选择核酸诊断的策略;对于抗体确证结果不确定和 疑似急性期感染的样品建议采用1 核酸试验。
u 修改了艾滋病感染产妇所生儿童感染早期感染检测流程
感染的自然史
急性感染期 无症状期 艾滋病期
感染后标志物变化时间
Reactivity
HIV RNA
p24 Ag
IgM AntiHIV
IgG Anti-HIV
012345678
Weeks post-infection
核酸检测的意义
耐药性 艾滋的“元凶”
核酸
缩短窗口期
指导治疗
病程 自然史
核酸检测的意义
核酸检测技术及应用
目录
核酸简介 核酸检测意义 核酸检测技术现状与发展 核酸检测质量控制 核酸检测流程(新规范) 核酸检测实例应用
血液透析患者病毒感染相关指标检测及临床意义

03 病毒感染相关指标的临床意义
白细胞计数与感染的关系
白细胞计数是评估感染的重要指标之一。当血液透析患者出 现感染时,白细胞计数通常会升高,表明机体正在动员免疫 系统对抗感染。白细胞计数的动态变化可以反映感染的严重 程度和治疗效果。
白细胞分类计数:除了白细胞总数,医生还会关注白细胞分 类计数的变化。例如,中性粒细胞比例增加可能提示细菌感 染,而淋巴细胞比例增加可能提示病毒感染。
C反应蛋白与感染的关系
C反应蛋白是一种由肝脏合成的急性时相反应蛋白,在感染、炎症和组织损伤时 其水平会显著升高。检测C反应蛋白可以帮助诊断感染,并评估病情的严重程度 和治疗效果。
C反应蛋白水平越高,通常表示感染或炎症越严重。在血液透析患者中,C反应蛋 白的升高可能还与心血管疾病风险增加有关。
免疫球蛋白与感染的关系
血液透析患者病毒感 染相关指标检测及临
床意义
目录
• 血液透析患者病毒感染概述 • 病毒感染相关指标检测方法 • 病毒感染相关指标的临床意义 • 血液透析患者病毒感染的治疗与管
理 • 结论与展望
血液透析患者病毒感染概述
01
ห้องสมุดไป่ตู้
病毒感染对血液透析患者的影响
01
增加并发症风险
病毒感染可导致血液透析患者出现多种并发症,如心血 管疾病、肺部感染等,影响患者的生存质量和预后。
02
加重病情
病毒感染可加剧血液透析患者的病情,如肾功能恶化、 电解质紊乱等,增加治疗难度和风险。
03
增加死亡风险
病毒感染是血液透析患者死亡的独立危险因素之一,可 导致患者死亡风险的增加。
病毒感染的传播途径与预防措施
传播途径
HIV病毒载量的检测

HIV病毒载量检测1 实验室条件1.1 实验室功能分区1.1.1 实验室原则上应分为4个独立工作区试剂准备区、样品处理区、扩增区和扩增产物分析区,并设在不同房间。
前两区为扩增前区,后两区为扩增后区。
各区的功能是:1.1.1.1 试剂准备区:扩增试剂的配制、分装和保存。
1.1.1.2 样品处理区:样品登记、分装;核酸提取、保存和加样。
套式PCR的第二轮加样不能在此区。
1.1.1.3 扩增区:核酸扩增。
1.1.1.4 扩增产物分析区:扩增产物的电泳、杂交、成像、序列测定、结果分析、登记及报告。
1.1.2 扩增前区与扩增后区应严格分开,须使用不同的房间,两区之间最好有一定的间隔距离。
1.1.3 使用商品化试剂盒可在样品处理区进行少量试剂配制。
1.1.4 在满足下列操作和清洁处理要求的前提下,样品处理区和试剂准备区可设在同一房间内:1.1.4.1 在生物安全柜内操作。
1.1.4.2 每个实验人员、实验组分别使用各自的试剂及耗材。
1.1.4.3 盛放污染材料的器皿密封并一次性使用。
1.1.4.4 用有效的方法对操作区域和共享器具在实验前后进行清洁及消毒。
1.1.4.5 推荐的实验室处理程序是:(1)实验前将次氯酸钠溶液或70%乙醇涂布于操作台或器具表面,两分钟后用纸巾擦除。
(2)移入盛放污染材料的器皿、所需的试剂、耗材和样品,进行试验。
(3)一个实验区域在同一时间段只进行一种实验。
(4)实验结束后移出个人专用材料至个人专用区域;封好污染材料盛放器皿并移至污物袋;移出共享器具至专门区域保管;将次氯酸钠溶液或70%乙醇涂布于操作台或器具表面,两分钟后用纸巾擦除;打开紫外灯照射至少15min。
1.1.5 产物分析使用相对封闭的系统时,如特定的检测系统或全自动分析仪,扩增区和扩增产物分析区可设在同一房间内。
1.1.6 各区域的仪器、设备、器具和试剂为该区专用,不得交叉使用。
1.2 人员进行HIV核酸检测的人员须具有艾滋病检测实验室的上岗资格,并接受过省级以上艾滋病实验室生物安全及实验操作技术培训。
PCR项目及临床意义
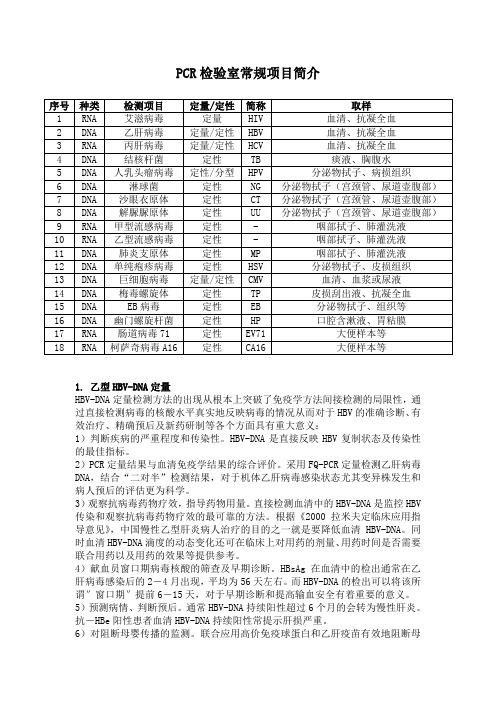
PCR检验室常规项目简介1. 乙型HBV-DNA定量HBV-DNA定量检测方法的出现从根本上突破了免疫学方法间接检测的局限性,通过直接检测病毒的核酸水平真实地反映病毒的情况从而对于HBV的准确诊断、有效治疗、精确预后及新药研制等各个方面具有重大意义:1)判断疾病的严重程度和传染性。
HBV-DNA是直接反映HBV复制状态及传染性的最佳指标。
2)PCR定量结果与血清免疫学结果的综合评价。
采用FQ-PCR定量检测乙肝病毒DNA,结合“二对半”检测结果,对于机体乙肝病毒感染状态尤其变异株发生和病人预后的评估更为科学。
3)观察抗病毒药物疗效,指导药物用量。
直接检测血清中的HBV-DNA是监控HBV 传染和观察抗病毒药物疗效的最可靠的方法。
根据《2000拉米夫定临床应用指导意见》,中国慢性乙型肝炎病人治疗的目的之一就是要降低血清HBV-DNA。
同时血清HBV-DNA滴度的动态变化还可在临床上对用药的剂量、用药时间是否需要联合用药以及用药的效果等提供参考。
4)献血员窗口期病毒核酸的筛查及早期诊断。
HBsAg在血清中的检出通常在乙肝病毒感染后的2-4月出现,平均为56天左右。
而HBV-DNA的检出可以将该所谓″窗口期″提前6-15天,对于早期诊断和提高输血安全有着重要的意义。
5)预测病情、判断预后。
通常HBV-DNA持续阳性超过6个月的会转为慢性肝炎。
抗-HBe阳性患者血清HBV-DNA持续阳性常提示肝损严重。
6)对阻断母婴传播的监测。
联合应用高价免疫球蛋白和乙肝疫苗有效地阻断母婴传播,但仍有5-10%婴儿对疫苗呈低反应,荧光定量PCR可对此进行监测。
7)器官移植中的作用。
肝脏器官移植是目前肝硬化晚期治疗的唯一方法,定量检测HBV-DNA为肝移植术后的跟踪观测具有较好的临床价值。
乙肝病毒定量相关检测还有:乙肝标志物定性,乙肝标志物定量,乙型HBV-DNA 定量,肝脏功能检测。
2. 乙型HBV-DNA定性HBV-DNA是乙肝病毒基因,其有无、多少是乙肝病毒存在及有无复制能力的直接标志。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
COBAS Amplicor HIV-1 Monitor 1.5
扩增:RT-PCR 检测:底物显色 先扩增再检测
普通方法:400-750,000 Copies/ml 超敏方法:50-75,000 Copies/ml 线性范围有限,高浓度 样本需稀释检测,超敏 方法需要用低温超速离 心机离心1个小时
? NucliSens EasyQ HIV-1实验 是使用NASBA技术的靶扩增试验。NASBA技术选 择性地直接扩增RNA而没有PCR步骤,用2个寡核苷酸引物、3个酶、三磷酸脱 氧核苷和合适的缓冲液进行一步夹心杂交。首先用异硫氰酸胍和氧化硅颗粒提取 高纯度RNA,RNA通过重复的合成和转录双链DNA中间体得到扩增。在AMVRT的作用下,HIV-1gag区的引物P1介导由标本RNA合成cDNA,RNA链被 RNAse降解。引物P2结合启动第二条DNA链合成,反义RNA通过T7多聚酶启动 双链DNA合成,这个循环不断重复,使得靶RNA在等温条件下大量扩增100万到 1000万倍,然后直接用化学发光法确定核酸量,通过HIV特异的gag和pol区的3 个内标同时扩增而达到定量目的。它具有高度敏感性和广阔的动态范围。 最近 NucliSens HIV-1定量实验有了较大改进,将NASBA核酸扩增技术与实时(realtime)检测技术结合起来,能够对检测进行实时监控。结果表达方式由每毫升标本 的拷贝数(cp/ml)改变为每毫升国际单位(IU/ml)。
AMPLICOR 分析仪根据HIV-1定量标准品的 数据计算每一个样本的HIV-1RNA 的含量。 可扩增HIV-1 M组的A-H基因亚型。
? 标准试验:能够定量400-750000拷贝/毫升的 HIV RNA,需要0.2毫升血浆。
? 超敏试验:能够定量50-75000拷贝/毫升的 HIV RNA,需要0.5毫升血浆。
Hale Waihona Puke 厂家 商品名 扩增和检测原理 线性范围
核酸提取
bioMerieux
Roche
Simens(Bayer)
Nuclisens Easy Q
扩增:NASBA 检测:Real Time. Molecular Beacon 实时扩增检测
50-3,000,000IU/ml(v1.1) 线性范围广,无需稀释标本重复检测, 报告国际单位,易于统一标准 25-10,000,000IU/ml(v2.0)
病毒载量检测方法及检测意义
新疆疾病预防控制中心 佐合拉.吐尔地 2012-05-16 伊宁市
? 病毒载量(viral load)代表的是病毒的负荷, 即体内复制的病毒的数量。实际上,体内复 制的病毒的数量是不能直接测量的,一般用 每毫升血浆中HIV RNA的拷贝数代表HIV的 病毒载量。
一、通常的病毒载量测定方法
可扩增HIV-1 M组的A-G亚型。
NucliSens 核酸分析系统利用三项技术: ?专利的BOOM核酸提纯技术:手 工 manual
半自动miniMAG 自 动 easyMAG ? “扩增RNA”的NASBA技术 ?使用荧光分子信标(molecular beacon)对扩 增产物的实时检测技术
三种病毒载量检测技术比较
COBAS AMPLICOR HIV-1 MONITOR实验包 括以下步骤: ? 样本制备 ? 靶RNA的逆转录产生cDNA ? 用HIV-1特异互补引物进行靶cDNA PCR扩增 ? 通过比色进行与探针结合的扩增产物的测定
? COBAS AMPLICOR HIV-1 MONITOR 试剂 对HIV-1病毒RNA的定量检测是采用HIV-1定 量标准品来完成的。HIV-1定量标准品是包括 作为HIV-1靶RNA引物结合部位和HIV-1扩增 子单一探针结合区的非感染性RNA转录物。 将已知拷贝数的HIV-1定量标准品加到每一个 样本中和HIV-1靶序列一起共同进行样本制备、 逆转录、PCR扩增、杂交和检测。COBAS
扩增HIV-1 M组的A-H亚型。
? 本实验系统检测的定量范围为50至500,000HIV-1 RNA拷贝 /ml。
? 检测结果以如下形式报告: ? 低于最低定量限的值报告为“<50” HIV-1 RNA拷贝/毫升。 ? 在最低定量限和最高定量限之间的值报告为实际检测值。 ? 高于最高定量限的值报告为“>500,000” HIV-1 RNA拷贝/
毫升。 ? 高于500,000HIV-1 RNA拷贝/毫升的样本位于检测的最高定
量限以上,必须适当稀释以获得确切的量值。在人血浆中稀 释高浓度样本,稀释用血浆需经VERSANT HIV-1 RNA3.0 Assay (bDNA) 检测鉴定不含HIV-1 RNA,按照实验流程重 新检测,得出的结果乘以稀释倍数以确定初始样本的病毒载 量。
bDNA方法(分枝DNA杂交试验) NASBA(核酸序列扩增试验) Cobas Amplicor HIV-1 Monitor(逆转录聚合酶链反应) 荧光定量PCR
? bDNA 是一种夹心式的核算杂交反应过程,用于直接定量检测血浆中HIV-1 RNA 的含量。首先,通过离心将血浆中的HIV-1 富集起来。HIV-1 病毒基因组RNA从 病毒颗粒中释放出来后,首先会被一组合成的寡核苷酸探针又称捕获探针所结合 并连接在微孔板上,然后通过另外一些靶定探针使病毒RNA与预放大探针结合。 捕获探针包括十七个可与基因组特异结合的捕获位,靶定探针包括81个可与基 因组特异结合的靶定区,分别靶定在病毒RNA pol 基因的不同区段。放大探针结 合到预防大探针上,从而形成支链DNA复合体。随后多拷贝的碱性磷酸酶(AP) 标记的探针与该复合体杂交结合。与化学发光底物共同孵育,所产生的光强度与 样品中HIV-1RNA的量成正比,以相对光强度单位(RLUs)表示的光度值被分 析系统记录下来,试剂盒中含有已知浓度的经β-丙内酯(BPL)处理的HIV18E5/LAV病毒液作为标准品,根据标准品的光吸收值绘制标准曲线,样品中 HIV-1 RNA的量可对照标准曲线求得。
