化学氧化还原反应的专项培优练习题(含答案)及答案
氧化还原反应练习及答案

氧化还原反应同步练习一、选择题:1.有关氧化还原反应的叙述正确的是( )A .氧化还原反应的实质是有氧元素的得失B .氧化还原反应的实质是元素化合价的升降C .氧化还原反应的实质是电子的转移(得失或偏移)D .物质所含元素化合价升高的反应是还原反应 2.下列化学反应基本类型中一定是氧化还原反就的是( )A .化合反应B .分解反应C .复分解反应D .置换反应3.下列哪一个反应表示二氧化硫被还原( )4.下列化学方程式中电子转移不正确的是( )5.某元素在化学反应中由化合态变为游离态,则该元素( )A .一定被氧化B .一定被还原C .既可能被氧化又可能被还原D .以上都不是6.下列反应盐酸作还原剂的是( )A.在被氧化B.是氧化剂C.被还原D.是还原剂8.下列变化需要加入还原剂才能实现的是( )A .Na 2SO 3−−→− SO 2B .HCl −−→− Cl 2C .H 2SO 4(浓) −−→− SO 2D .SO 2−−→− S9.下列反应属于氧化还原反应,但水既不作氧化剂也不作还原剂的是( ) OHA .KClO 3B .KClC .KCl+H 2OD .H 2O量比为( )A .1:1B .5:1C .1:5D .3:112.盐酸能发生下列反应:+H 2O 因此盐酸应当具有的性质是( )A .只有酸性B .只有氧化性C .只有还原性D .有酸性、有氧化性和还原性13.下面三个方法都可以用来制氯气:则三种氧化剂由强到弱的顺序是( )A .O 2 MnO 2 KMnO 4B .KMnO 4 MnO 2 O 2C .MnO 2 KMnO 4 O 2D .O 2 KMnO 4 MnO 2A .+2B .+3C .+4D .+6个数比是( )A .6:5B .5:6C .11:5D .11:6物,③H 2O 是氧化剂,④CaH 2中的H 元素被还原,⑤此反应中的氧化产物和还原产物的分子个数之比为1:1。
备战高考化学氧化还原反应(大题培优 易错 难题)附答案

备战高考化学氧化还原反应(大题培优 易错 难题)附答案一、高中化学氧化还原反应1.2ClO 是一种优良的消毒剂,浓度过高时易发生分解,为了运输和贮存便利常将其制成2NaClO 固体,模拟工业上用过氧化氢法制备2NaClO 固体的实验装置如图所示。
已知:2ClO 熔点-59℃、沸点11℃、22H O 沸点150℃A 中的化学方程式:32224222422NaClO H O H SO 2ClO O Na SO 2H O ++=↑+↑++(1)3NaClO 放入仪器A 中,仪器B 中的药品是__________(写化学式)。
如果仪器B 改成分液漏斗,实验过程中可能会出现的实验现象__________。
(2)C 装置有明显缺陷,请绘出合理的装置图(标明气流方向)__________。
(3)向A 装置中通入空气,其作用是赶出2ClO ,然后通过C 再到D 中反应。
通空气不能过快的原因是__________,通空气也不能过慢原因是__________。
(4)冰水浴冷却的目的是__________。
a.降低2NaClO 的溶解度b.减少22H O 的分解c.使2ClO 变为液态d.加快反应速率(5)写出D 中发生反应的化学方程式__________,22H O 在反应起到__________作用。
假设在反应中消耗掉22H O a g 则有__________mol 电子转移。
【答案】H 2O 2 液体无法顺利滴落 空气流速快时,2ClO 不能被充分吸收 空气流速过慢时,2ClO 不能及时被移走,浓度过高导致分解 abc2ClO 2+H 2O 2+2NaOH=2NaClO 2+O 2↑+2H 2O 还原剂 a/17【解析】【分析】氯酸钠(NaClO 3)在酸性条件下与过氧化氢生二氧化氯,ClO 2与氢氧化钠溶液和过氧化氢发生氧化还原反应生成NaClO 2,NaClO 2的溶解度随温度升高而增大,通过冷却结晶,过滤洗涤得到晶体NaClO 2•3H 2O 。
备战高考化学 氧化还原反应 培优练习(含答案)含答案解析

备战高考化学 氧化还原反应 培优练习(含答案)含答案解析一、高中化学氧化还原反应1.工业上处理含苯酚废水的过程如下。
回答下列问题:Ⅰ.测定废水中苯酚的含量。
测定原理:+3Br 2→↓+3HBr 测定步骤:步骤1:准确量取25.00mL 待测废水于250mL 锥形瓶中。
步骤2:将5.00mL 1amol L -⋅浓溴水(量)迅速加入到锥形瓶中,塞紧瓶塞,振荡。
步骤3:打开瓶塞,向锥形瓶中迅速加入bmL 10.10mol L -⋅KI 溶液(过量),塞紧瓶塞,振荡。
步骤4:滴入2~3滴指示剂,再用10.010mol L -⋅223Na S O 标准溶液滴定至终点,消耗223Na S O 溶液1V mL (反应原理:2223246I 2Na S O 2NaI Na S O +=+)。
待测废水换为蒸馏水,重复上述步骤(即进行空白实验),消耗223Na S O 溶液2V mL 。
(1)“步骤1”量取待测废水所用仪器是________。
(2)为了防止溴的挥发,上述步骤中采取的措施包括迅速加入试剂和________。
(3)“步骤4”滴定终点的现象为________。
(4)该废水中苯酚的含量为________1mg L -⋅(用含1V 、2V 的代数式表示)。
如果空白实验中“步骤2”忘记塞紧瓶塞,则测得的废水中苯酚的含量________(填“偏高”“偏低”或“无影响”,下同);如果空白实验中“步骤4”滴定至终点时俯视读数,则测得的废水中苯酚的含量________。
Ⅱ.处理废水。
采用Ti 基2PbO 为阳极,不锈钢为阴极,含苯酚的废水为电解液,通过电解,阳极上产生羟基(·OH ),阴极上产生22H O 。
通过交排列的阴阳两极的协同作用,在各自区域将苯酚深度氧化为2CO 和2H O 。
(5)写出阳极的电极反应式:________。
(6)写出苯酚在阴极附近被22H O 深度氧化的化学方程式:________。
化学氧化还原反应的专项培优练习题含详细答案

一、高中化学氧化还原反应练习题(含详细答案解析)1.亚氯酸钠(NaClO2)是二氧化氯(ClO2)泡腾片的主要成分。
实验室以氯酸钠(NaClO3)为原料先制得ClO2,再制备NaClO2粗产品,其流程如图:已知:①ClO2可被NaOH溶液吸收,反应为2ClO2+2NaOH=NaClO3+NaClO2+H2O。
②无水NaClO2性质稳定,有水存在时受热易分解。
(1)反应Ⅰ中若物质X为SO2,则该制备ClO2反应的离子方程式为___。
(2)实验在如图-1所示的装置中进行。
①若X为硫磺与浓硫酸,也可反应生成ClO2。
该反应较剧烈。
若该反应在装置A的三颈烧瓶中进行,则三种试剂(a.浓硫酸;b.硫黄;c.NaClO3溶液)添加入三颈烧瓶的顺序依次为___(填字母)。
②反应Ⅱ中双氧水的作用是___。
保持反应时间、反应物和溶剂的用量不变,实验中提高ClO2吸收率的操作有:装置A中分批加入硫黄、___(写出一种即可)。
(3)将装置B中溶液蒸发可析出NaClO2,蒸发过程中宜控制的条件为___(填“减压”、“常压”或“加压”)。
(4)反应Ⅰ所得废液中主要溶质为Na2SO4和NaHSO4,直接排放会污染环境且浪费资源。
为从中获得芒硝(Na2SO4·10H2O)和石膏(水合硫酸钙),请补充完整实验方案:___,将滤液进一步处理后排放(实验中须使用的试剂和设备有:CaO固体、酚酞、冰水和冰水浴)。
已知:CaSO4不溶于Na2SO4水溶液;Na2SO4的溶解度曲线如图−2所示。
【答案】2ClO3-+SO2═2ClO2+SO42- cab 作还原剂水浴加热时控制温度不能过高(或加一个多孔球泡等)减压向废液中分批加入适量CaO固体并搅拌,用冰水浴控制反应温度,对浊液取样并滴加酚酞,至溶液呈浅红色时停止加入CaO。
静置后过滤,用水洗涤沉淀2-3次得到石膏;滤液蒸发浓缩,冷却结晶至32.4℃以下,接近0℃,过滤,所得晶体用冰水洗涤2-3次,低温干燥得到芒硝【解析】【分析】用二氧化硫将NaClO3还原制得ClO2,ClO2和NaOH反应制得NaClO3和NaClO2,再用过氧化氢将NaClO3还原成NaClO2制得NaClO2粗品。
化学氧化还原反应的专项培优练习题(含答案)及答案.docx

一、高中化学氧化还原反应练习题(含详细答案解析)1.ClO2是一种优良的消毒剂,浓度过高时易发生分解,为了运输和贮存便利常将其制成NaClO2 固体,模拟工业上用过氧化氢法制备NaClO2固体的实验装置如图所示。
已知: ClO2熔点-59℃、沸点11℃、H2O2沸点150℃A 中的化学方程式:2NaClO 3H 2O 2H 2SO42ClO 2O 2Na 2SO42H 2O(1)NaClO 3放入仪器A中,仪器B中的药品是__________(写化学式)。
如果仪器B改成分液漏斗,实验过程中可能会出现的实验现象__________。
(2)C 装置有明显缺陷,请绘出合理的装置图(标明气流方向 )__________。
(3)向A装置中通入空气,其作用是赶出ClO2,然后通过 C 再到 D 中反应。
通空气不能过快的原因是__________ ,通空气也不能过慢原因是__________。
(4)冰水浴冷却的目的是__________ 。
a.降低NaClO2的溶解度b.减少H 2 O2的分解c.使ClO2变为液态d.加快反应速率(5)写出D中发生反应的化学方程式__________ ,H2O2在反应起到 __________作用。
假设在反应中消耗掉H 2O2a g 则有__________mol电子转移。
【答案】 H2O2液体无法顺利滴落空气流速快时,ClO2不能被充分吸收空气流速过慢时,ClO2不能及时被移走,浓度过高导致分解abc2ClO +H O +2NaOH=2NaClO +O ↑ +2H O 还原剂 a/17222222【解析】【分析】氯酸钠 (NaClO32)在酸性条件下与过氧化氢生二氧化氯,ClO 与氢氧化钠溶液和过氧化氢发生氧化还原反应生成 NaClO22的溶解度随温度升高而增大,通过冷却结晶,过滤洗涤, NaClO得到晶体NaClO2?3H2O。
【详解】(1)NaClO 3放入仪器A中,仪器B中的药品是H2O2,仪器B为滴液漏斗,其目的是平衡气压,使得溶液能够顺利滴入,如果仪器 B 改成分液漏斗,实验过程中可能会出现的实验现象是:分液漏斗中的液体无法顺利滴落,反应无法继续进行;(2)实验中 C 的作用是防止倒吸, C 装置中的右侧导管太短,不利于气体的流动,合理的装置图为:;(3)向A装置中通入空气,其作用是赶出ClO2,然后通过C再到D中反应。
2020-2021高考化学 氧化还原反应 培优 易错 难题练习(含答案)及详细答案
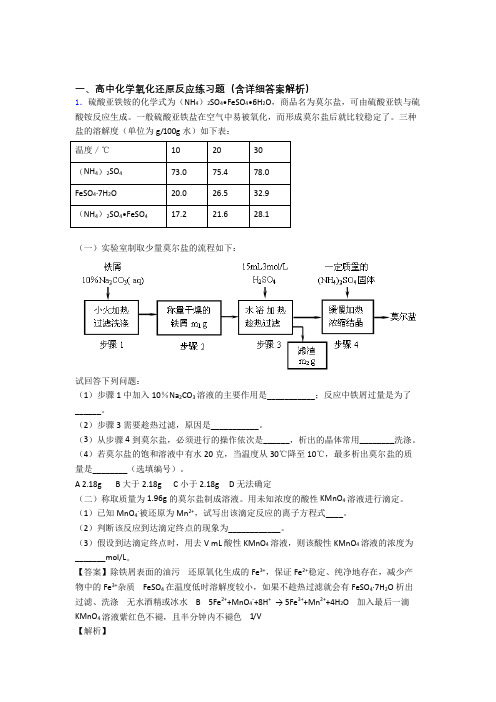
一、高中化学氧化还原反应练习题(含详细答案解析)1.硫酸亚铁铵的化学式为(NH4)2SO4•FeSO4•6H2O,商品名为莫尔盐,可由硫酸亚铁与硫酸铵反应生成。
一般硫酸亚铁盐在空气中易被氧化,而形成莫尔盐后就比较稳定了。
三种盐的溶解度(单位为g/100g水)如下表:温度/℃102030(NH4)2SO473.075.478.0FeSO4·7H2O20.026.532.9(NH4)2SO4•FeSO417.221.628.1(一)实验室制取少量莫尔盐的流程如下:试回答下列问题:(1)步骤1中加入10%Na2CO3溶液的主要作用是___________;反应中铁屑过量是为了______。
(2)步骤3需要趁热过滤,原因是___________。
(3)从步骤4到莫尔盐,必须进行的操作依次是______,析出的晶体常用________洗涤。
(4)若莫尔盐的饱和溶液中有水20克,当温度从30℃降至10℃,最多析出莫尔盐的质量是________(选填编号)。
A 2.18gB 大于2.18gC 小于 2.18gD 无法确定(二)称取质量为1.96g的莫尔盐制成溶液。
用未知浓度的酸性KMnO4溶液进行滴定。
(1)已知MnO4-被还原为Mn2+,试写出该滴定反应的离子方程式____。
(2)判断该反应到达滴定终点的现象为____________。
(3)假设到达滴定终点时,用去V mL 酸性KMnO4溶液,则该酸性KMnO4溶液的浓度为_______mol/L。
【答案】除铁屑表面的油污还原氧化生成的Fe3+,保证Fe2+稳定、纯净地存在,减少产物中的Fe3+杂质 FeSO4在温度低时溶解度较小,如果不趁热过滤就会有FeSO4·7H2O析出过滤、洗涤无水酒精或冰水 B 5Fe2++MnO4-+8H+→ 5Fe3++Mn2++4H2O 加入最后一滴KMnO4溶液紫红色不褪,且半分钟内不褪色 1/V【解析】【分析】(一)(1)碳酸钠水解显碱性;(2)FeSO4在温度低时溶解度较小;(3)浓缩结晶后需要过滤、洗涤;温度低时,硫酸亚铁铵的溶解度小;(4)(NH4)2SO4·FeSO4在30℃和10℃的溶解度分别为:28.1g和17.2g;(二)(1)MnO4-将二价铁离子氧化为三价铁离子,被还原为Mn2+;(2)高锰酸钾本身有颜色,滴定亚铁离子是不需要指示剂的;(3)根据亚铁离子和高锰酸根反应的实质,可以找到亚铁离子与高锰酸根之间的量的关系,根据原子守恒可以找到亚铁离子和酸亚铁铵之间量的关系,进而进行计算。
初一化学氧化还原反应练习题及答案20题

初一化学氧化还原反应练习题及答案20题1. 在下面的反应方程式中,标出氧化剂和还原剂:2H2 + O2 -> 2H2O答案:氧化剂: O2 还原剂: H22. 在下面的反应方程式中,标出氧化剂和还原剂:Cu + 2AgNO3 -> Cu(NO3)2 + 2Ag答案:氧化剂: Cu 还原剂: AgNO33. 在下面的反应方程式中,标出氧化剂和还原剂:2Na + Cl2 -> 2NaCl答案:氧化剂: Cl2 还原剂: Na4. 在下面的反应方程式中,标出氧化剂和还原剂:Zn + 2HCl -> ZnCl2 + H2答案:氧化剂: HCl 还原剂: Zn5. 在下面的反应方程式中,标出氧化剂和还原剂:Fe + CuSO4 -> FeSO4 + Cu答案:氧化剂: CuSO4 还原剂: Fe6. 下列哪个物质是被氧化的?a) Nab) Cac) H2d) Cl2答案:d) Cl27. 下列哪个物质是被还原的?a) KClb) Alc) H2Od) O2答案:b) Al8. 认识下面方程式中的还原剂和氧化剂:MnO2 + 4HCl -> MnCl2 + 2H2O + Cl2答案:还原剂: MnO2 氧化剂: HCl 9. 认识下面方程式中的还原剂和氧化剂:2KBr + Cl2 -> 2KCl + Br2答案:还原剂: Cl2 氧化剂: KBr10. 认识下面方程式中的还原剂和氧化剂:2Fe + 3Cl2 -> 2FeCl3答案:还原剂: Fe 氧化剂: Cl211. 在下列反应中,N2H4是()。
a) 还原剂b) 氧化剂答案:a) 还原剂12. 在下列反应中,H2O2是()。
a) 还原剂b) 氧化剂答案:b) 氧化剂13. 在下列反应中,Cl2是()。
a) 还原剂b) 氧化剂答案:b) 氧化剂14. 在下列反应中,O2是()。
a) 还原剂b) 氧化剂答案:a) 还原剂15. 判断下面方程式中的物质是被氧化还是被还原:C + O2 -> CO2答案:C被氧化。
2020-2021高考化学氧化还原反应(大题培优 易错 难题)含答案

一、高中化学氧化还原反应练习题(含详细答案解析)1.过硫酸钠(Na2S2O8)具有极强的氧化性,且不稳定,某化学兴趣小组探究过硫酸钠的相关性质,实验如下。
已知SO3是无色易挥发的固体,熔点16.8℃,沸点44.8℃。
(1)稳定性探究(装置如图):分解原理:2Na2S2O82Na2SO4+2SO3↑+O2↑。
此装置有明显错误之处,请改正:______________________,水槽冰水浴的目的是____________________;带火星的木条的现象_______________。
(2)过硫酸钠在酸性环境下,在Ag+的催化作用下可以把Mn2+氧化为紫红色的离子,所得溶液加入BaCl2可以产生白色沉淀,该反应的离子方程式为______________________,该反应的氧化剂是______________,氧化产物是________。
(3)向上述溶液中加入足量的BaCl2,过滤后对沉淀进行洗涤的操作是___________________________。
(4)可用H2C2O4溶液滴定产生的紫红色离子,取20mL待测液,消耗0.1mol·L-1的H2C2O4溶液30mL,则上述溶液中紫红色离子的浓度为______mol·L-1,若Na2S2O8有剩余,则测得的紫红色离子浓度将________(填“偏高”“偏低”或“不变”)。
【答案】试管口应该略向下倾斜冷却并收集SO3木条复燃 2Mn2++5S2O+8H2O2MnO+10SO+16H+ S2O MnO用玻璃棒引流,向漏斗中加蒸馏水至没过沉淀,使蒸馏水自然流下,重复操作2~3次(合理即可) 0.06 偏高【解析】【分析】(1)在试管中加热固体时,试管口应略微向下倾斜;根据SO3、氧气的性质进行分析;(2)X为MnO4-,向所得溶液中加入BaCl2溶液可以产生白色沉淀,则产物中有SO42-,据此写出离子方程式,并根据氧化还原反应规律判断氧化剂、氧化产物;(3)根据沉淀洗涤的方法进行回答;(4)根据得失电子守恒可得到关系式:5H2C2O4---2MnO4-,带入数值进行计算;Na2S2O8也具有氧化性,氧化H2C2O4。
化学氧化还原反应的专项培优练习题(含答案)附答案解析.docx

一、高中化学氧化还原反应练习题(含详细答案解析)1.碘酸钾(KIO3)是重要的微量元素碘添加剂。
实验室设计下列实验流程制取并测定产品中 KIO 3的纯度:其中制取碘酸(HIO 3)的实验装置见图,有关物质的性质列于表中物质性质3白色固体,能溶于水,难溶于CCl4HIOKIO①白色固体,能溶于水,难溶于乙醇-+ Cl-②碱性条件下易发生氧化反应:ClO-+IO3- =IO43回答下列问题(1)装置 A 中参加反应的盐酸所表现的化学性质为______________。
(2)装置 B 中反应的化学方程式为 ___________________ 。
B 中所加 CCl4的作用是_________从而加快反应速率。
(3)分离出 B 中制得的HIO 3水溶液的操作为____________;中和之前,需将HIO3溶液煮沸至接近于无色,其目的是____________,避免降低KIO 3的产率。
(4)为充分吸收尾气,保护环境,C 处应选用最合适的实验装置是____________(填序号)。
(5)为促使KIO3晶体析出,应往中和所得的KIO 3溶液中加入适量的___________。
(6)取 1.000g KIO3产品配成 200.00mL 溶液,每次精确量取20.00mL 溶液置于锥形瓶中,加入足量KI 溶液和稀盐酸,加入淀粉作指示剂,用0.1004mol/L Na 2S2 O3溶液滴定。
滴定至终点时蓝色消失(I 2 +2S2 O32- =2I - +S4O 62-),测得每次平均消耗Na 2S2O3溶液25.00mL。
则产品中KIO3的质量分数为 ___(结果保留三位有效数字)。
【答案】还原性、酸性5CI 2 +I 2 +6H 2O==2HIO 3 +10HCl充分溶解 I 2和 Cl 2,以增大反应物浓度分液除去 Cl 2(或ClO-),防止氧化KIO 3 C 乙醇(或酒精)89.5%。
【解析】【分析】装置 A 用于制取Cl2,发生的反应为:KClO3+6HCl(浓 )=KCl+3Cl2↑+3H2O,装置 B 中发生的是制取 HIO3的反应,装置 C 为尾气处理装置,既要吸收尾气中的HCl 和 Cl2,还要防止倒吸。
高中化学 氧化还原反应 练习题(含答案)
原创化学专题卷专题四氧化还原反应考点08氧化还原反应的概念与判断(1-6 题 8-10题)考点09 氧化性、还原性的强弱对比(11-19题)考点10 氧化还原反应方程式的配平( 7题 20-25题)(综合26-29)考试时间:90分钟满分:100分可能用到的相对原子质量: O-16 K-39 Cl-35.5 Fe-56第I卷(选择题)一、选择题(本题共25小题,每小题2分,共50分。
在每小题给出的四个选项中,只有一项是最符合题目要求的。
)1.下列叙述不涉及氧化还原反应的是( )A.谷物发酵酿造食醋B.小苏打用作食品膨松剂C.含氯消毒剂用于环境消毒D.大气中NO参与酸雨形成22.下列除杂试剂选用正确且除杂过程不涉及氧化还原反应的是( )A. AB. BC. CD. D3.下列叙述正确的是( )A.金属元素从化合态变为游离态时,该元素一定被还原B.氧化还原反应的实质是电子的得失C.氧化还原反应中一种元素化合价升高一定有另一种元素化合价降低D.有单质参加或有单质生成的反应一定是氧化还原反应4.锑(Sb)在自然界一般以硫化物的形式存在,我国锑的蕴藏量为世界第一,从硫化物中提取单质锑一般是先在高温下将硫化物转化为氧化物,再用碳还原: ①2322Sb S +3O +6Fe 高温 46Sb O +6FeS ②46Sb O +6C 高温 4Sb+6CO ↑,关于反应①、②的说法正确的是( )A. 反应①②中的氧化剂分别是2346Sb S Sb O 、B. 反应①中每生成3mol FeS 时,共转移6mol 电子C. 反应②说明C 的还原性比Sb 强D. 每生成4mol Sb 时,反应①与反应②中还原剂的物质的量之比为4:35.为了探究铁及其化合物的氧化性和还原性,某同学设计了如下实验方案,其中符合实验要求且完全正确的是( )A. 答案AB. 答案BC. 答案CD. 答案D6.硼在化合物中一般显正价.可用下述方法合成储氢材料氨硼烷:44332LiBH +NH Cl=NH BH +LiCl+H ↑.33NH BH 在催化剂存在时可以与水发生催化脱氢反应:A.33NH BH 中H 元素均为+1价B. 合成反应中每生成1 mol 33NH BH 会转移2 mol e -C. 两个反应中,H 2均既是氧化产物,又是还原产物D. 0.1 mol 33NH BH 发生上述催化脱氢反应,一定生成6.72 L H 27.二氧化氯()2ClO 常用于废水的处理。
备战高考化学氧化还原反应(大题培优 易错 难题)含详细答案

一、高中化学氧化还原反应练习题(含详细答案解析)1.叠氮化钠(NaN3)是一种白色剧毒晶体,是汽车安全气囊的主要成分。
NaN3易溶于水,微溶于乙醇,水溶液呈弱碱性,能与酸发生反应产生具有爆炸性的有毒气体叠氮化氢。
实验室可利用亚硝酸叔丁酯(t-BuNO2,以t-Bu表示叔丁基)与N2H4、氢氧化钠溶液混合反应制备叠氮化钠。
(1)制备亚硝酸叔丁酯取一定NaNO2溶液与50%硫酸混合,发生反应H2SO4+2NaNO2===2HNO2+Na2SO4。
可利用亚硝酸与叔丁醇(t-BuOH)在40℃左右制备亚硝酸叔丁酯,试写出该反应的化学方程式:____________。
(2)制备叠氮化钠(NaN3)按如图所示组装仪器(加热装置略)进行反应,反应的化学方程式为:t-BuNO2+NaOH+N2H4===NaN3+2H2O+t-BuOH。
①装置a的名称是______________;②该反应需控制温度在65℃,采用的实验措施是____________________;③反应后溶液在0℃下冷却至有大量晶体析出后过滤。
所得晶体使用无水乙醇洗涤。
试解释低温下过滤和使用无水乙醇洗涤晶体的原因是____________。
(3)产率计算①称取2.0g叠氮化钠试样,配成100mL溶液,并量取10.00mL溶液于锥形瓶中。
②用滴定管加入0.10mol·L-1六硝酸铈铵[(NH4)2Ce(NO3)6]溶液40.00mL(假设杂质均不参与反应)。
③充分反应后将溶液稀释并酸化,滴入2滴邻菲罗啉指示液,并用0.10mol·L-1硫酸亚铁铵[(NH4)2Fe(SO4)2]为标准液,滴定过量的Ce4+,终点时消耗标准溶液20.00mL(滴定原理:Ce4++Fe2+===Ce3++Fe3+)。
已知六硝酸铈铵[(NH4)2Ce(NO3)6]与叠氮化钠反应生成硝酸铵、硝酸钠、氮气以及Ce(NO3)3,试写出该反应的化学方程式____________________________;计算叠氮化钠的质量分数为________(保留2位有效数字)。
备战高考化学氧化还原反应(大题培优)及答案
备战高考化学氧化还原反应(大题培优)及答案一、高中化学氧化还原反应1.据报道,磷酸二氢钾(KH2PO4)大晶体已应用于我国研制的巨型激光器“神光二号”中。
利用氟磷灰石(化学式为Ca5P3FO12)制备磷酸二氢钾的工艺流程如下图所示(部分流程步骤已省略):已知萃取的主要反应原理:KCl+H 3PO4KH2PO4+HCl;其中,反应产生的HCl易溶于有机萃取剂。
请回答下列问题:(1)流程中将氟磷灰石粉碎的目的是__________________________________。
(2)不能使用二氧化硅陶瓷材质的沸腾槽的主要原因是____________(用化学方程式表示)。
(3)副产品N的化学式是____________;在得到KH2PO4晶体的一系列操作Ⅲ,其主要包括____________、过滤、洗涤、干燥等。
(4)若用1000kg质量分数为50.4%的氟磷灰石(化学式为Ca5P3FO12,摩尔质量为504g/mol)来制取磷酸二氢钾晶体,其产率为80%,则理论上可生产KH2PO4(摩尔质量为136g/mol)的质量为_______kg。
(5)电解法制备KH2PO4的装置如图所示.该电解装置中,a 区属于_______区(填“阳极”或“阴极”),阴极区的电极反应式是________________。
(6)工业上还可以用氟磷灰石与焦炭、石英砂混合,在电炉中加热到1500℃生成白磷,同时逸出SiF4和CO,该反应的化学方程式为________________________________________。
【答案】增大氟磷灰石与稀硫酸反应的接触面积,加快化学反应速率4HF+SiO2═SiF4↑+2H2O NH4Cl 蒸发浓缩、冷却结晶 326.4kg 阴极 2H++2e-=H2↑4Ca5P3FO12+21SiO2+30C20CaSiO3+3P4+SiF4↑+30CO↑【解析】【分析】氟磷灰石(化学式为Ca5P3FO12)粉碎后加入浓硫酸,反应生成氢氟酸、硫酸钙、磷酸等,加入氯化钾后用有机萃取剂,KCl+H 3PO4KH2PO4+HCl,反应产生的HCl易溶于有机萃取剂,有机相中含有氯化氢,加入氨水反应生成氯化铵,因此副产品主要为氯化铵,水相中含有KH2PO4,经过一系列操作得到KH2PO4晶体。
高中化学氧化还原反应题目训练卷

高中化学氧化还原反应题目训练卷一、选择题(每题 5 分,共 50 分)1、下列化学反应中,属于氧化还原反应的是()A Na₂CO₃+ 2HCl = 2NaCl + H₂O + CO₂↑B CaO + H₂O = Ca(OH)₂C 2KMnO₄=△= K₂MnO₄+ MnO₂+ O₂↑D Na₂O + SO₃= Na₂SO₄【答案】C【解析】判断一个反应是否为氧化还原反应,关键是看反应前后元素的化合价是否有变化。
A 选项中各元素的化合价均未发生变化,不属于氧化还原反应;B 选项中各元素的化合价也没有改变,不是氧化还原反应;C 选项中锰元素的化合价由+7 价变为+6 价和+4 价,氧元素的化合价由-2 价变为 0 价,属于氧化还原反应;D 选项中各元素的化合价均未发生变化,不属于氧化还原反应。
2、在反应 3Cl₂+ 6KOH = 5KCl + KClO₃+ 3H₂O 中,氧化剂与还原剂的质量之比为()A 5∶1B 1∶5C 2∶1D 1∶2【答案】A【解析】在该反应中,Cl₂既是氧化剂又是还原剂。
化合价降低生成 KCl 的 Cl₂是氧化剂,化合价升高生成 KClO₃的 Cl₂是还原剂。
由化学计量数可知,有 5 个 Cl 原子化合价降低,1 个 Cl 原子化合价升高,所以氧化剂与还原剂的质量之比为 5∶1,故选 A。
3、下列变化过程中,需要加入氧化剂才能实现的是()A H₂SO₄ → H₂B Fe²⁺ → Fe³⁺C CuO → CuD HNO₃ → NO【答案】B【解析】需要加入氧化剂才能实现的变化,说明物质本身是还原剂,在反应中元素的化合价升高。
A 选项中,H₂SO₄ → H₂,氢元素的化合价从+1 价降低到 0 价,需要加入还原剂;B 选项中,Fe²⁺ → Fe³⁺,铁元素的化合价从+2 价升高到+3 价,需要加入氧化剂;C 选项中,CuO → Cu,铜元素的化合价从+2 价降低到 0 价,需要加入还原剂;D 选项中,HNO₃ → NO,氮元素的化合价从+5 价降低到+2 价,需要加入还原剂。
氧化还原反应练习题(含答案)

高一化学氧化还原反应专题训练和答案1.以油类为溶剂的防锈漆称为油基防锈漆,由于环保方面的原因,目前要推广使用水基防锈漆,但水基漆较易溶解O2,在干燥之前易导致金属表面产生锈斑,为此要在水基漆中加入缓蚀剂,以下可作为缓蚀剂添加的是()A.KMnO4B.NaNO2C.FeCl3D.HNO32.下列物质转化需要加入还原剂才能实现的是()A.SO32-→SO2B.HCl→Cl2C.Na→Na+D.SO2→S3.下列反应所生成的气体中,含有被还原的元素是()A.炭粉和二氧化硅均匀混和后强热B.石英和纯碱均匀混和后强热C.铜片放入浓硫酸中加热D.铝粉放入氢氧化钾溶液中振荡4.已知:2Fe+3Br2=2FeBr32Fe3++2I—=2Fe2++I2,现将Fe(NO3)2溶液分别滴入到以下溶液中:①H2SO4②HNO3③溴水④碘水,其中能使Fe2+转变成Fe3+的是()A.只有②③B.①②③C.②③④D.全部5.下列反应中有一种物质既是氧化剂又是还原剂的是()A.2KI+Br2=2KBr+I2 B.2AgNO32Ag+2NO2↑+O2↑C.Cu2(OH)2CO32CuO+CO2↑+H2O D.2Na2O2+2H2O=4NaOH+O2↑6.下列反应中,水既不是氧化剂,也不是还原剂,但反应是氧化还原反应的是()A.2Na2O2+2H2O=4NaOH+O2↑B.C+H2O CO+H2C.Cl2+H2O=HCl+HClO D.2F2+2H2O=4HF+O27.有甲、乙、丙、丁四种金属,仅甲在自然界主要以游离态存在;丙盐的水溶液不能用丁制的容器盛放;丁与乙盐的水溶液不反应。
则这四种金属的活动性由强到弱的顺序可能是()A.甲乙丙丁B.丁乙丙甲C.丙乙丁甲D.乙丁丙甲8.在反应3BrF3+5H2O=HBrO3+Br2+9HF+O2中,若有5mol水发生氧化反应,则被还原的BrF3物质的量为()A.2mol B.5mol C.53mol D.103mol9.单质A能从盐溶液中置换出单质B,则下列说法不正确的是()A.A、B都是金属时,A一定比B的金属活动性强B.当A、B都是非金属时,A一定比B的非金属活动性强C.当A是金属时,B可能是金属,也可能是非金属D.当A是非金属时,B可能是非金属,也可能是金属10.下列叙述中正确的是()A.阳离子只有氧化性,阴离子只有还原性B.含氧酸可作氧化剂而无氧酸则不能C.失电子难的原子获得电子的能力就强D.氯气分子可作氧化剂,但也可被其他氧化剂所氧化11.下列说法中正确的是()A.强氧化剂和弱还原剂易发生氧化还原反应B.实验室制氯气的反应中,氯离子通过还原反应生成氯气C.由HgCl2生成Hg2Cl2时,汞元素被还原了D.I-、Br-、Cl-的还原性依次减弱,氧化性依次增强12.C1SO3H称为氯磺酸,是一种强酸。
氧化还原反应习题(有答案,有分析)

氧化还原反应习题(有分析)1.锌与很稀的硝酸反应生成硝酸锌、硝酸铵和水。
当生成 1 mol 硝酸锌时,被还原的硝酸的物质的量为( )A.2 mol B.1 molC.0.5mol D. 0.25 mol【解析】锌在反应时失去2 mole-,而 1 mol HNO 转化为+时得到 8 mole-,故被NH3 4还原的硝酸是 0.25 mol 。
解答该题时要注意参加反应的硝酸与被还原的硝酸二者间的区别。
【答案】 D2.三聚氰酸 [C 3N3(OH)3] 可用于消除汽车尾气中的NO2。
其反应原理为:△C3N3(OH)3=====3HNCO;△8HNCO+ 6NO2=====7N2+ 8CO2+4H2O下列说法正确的是( ) A.C3N3(OH) 3 与 HNCO为同一物质B.HNCO是一种很强的氧化剂C.1 mol NO 2 在反应中转移的电子为4 molD.反应中NO2是还原剂【解析】A项,二者是不同的物质:从方程式△8HNCO+ 6NO2=====7N2+8CO2+4H2O知,HNCO中 N 的化合价升高,是还原剂;NO2中N 的化合价降低,是氧化剂,B、 D 都错。
【答案】 C3.金属铜的提炼多从黄铜矿开始,黄铜矿在焙烧过程中主要反应之一的化学方程式为2CuFeS+ O2===Cu2S+2FeS+ SO2下列说法不正确的是( ) A.O2 只作氧化剂B.CuFeS2 既是氧化剂又是还原剂C.SO2 既是氧化产物又是还原产物D.若有1 molO2 参加反应,则反应中共有4mol电子转移【解析】氧元素的化合价只降低未升高,故A 正确。
CuFeS2 中铜元素的化合价降低,硫元素部分化合价升高,故CuFeS2 既是氧化剂又是还原剂。
在 D 中若有 1 mol O 2 参加反应,得到 4 mol 电子,同时 2 mol CuFeS 2 中的铜元素也得到2 mol 电子,即反应中共有 6 mol 电子转移。
【化学】化学氧化还原反应的专项培优练习题(含答案)附答案

【化学】化学氧化还原反应的专项培优练习题(含答案)附答案一、高中化学氧化还原反应1.硫代硫酸钠(Na2S2O3)是一种解毒药,用于氟化物、砷、汞、铅、锡、碘等中毒,临床常用于治疗荨麻疹,皮肤瘙痒等病症.硫代硫酸钠在中性或碱性环境中稳定,在酸性溶液中分解产生S和SO2实验I:Na2S2O3的制备。
工业上可用反应:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2制得,实验室模拟该工业过程的装置如图所示:(1)仪器a的名称是_______,仪器b的名称是_______。
b中利用质量分数为70%〜80%的H2SO4溶液与Na2SO3固体反应制备SO2反应的化学方程式为_______。
c中试剂为_______(2)实验中要控制SO2的生成速率,可以采取的措施有_______ (写出一条)(3)为了保证硫代硫酸钠的产量,实验中通入的SO2不能过量,原因是_______实验Ⅱ:探究Na2S2O3与金属阳离子的氧化还原反应。
资料:Fe3++3S2O32-⇌Fe(S2O3)33-(紫黑色)装置试剂X实验现象Fe2(SO4)3溶液混合后溶液先变成紫黑色,30s 后几乎变为无色(4)根据上述实验现象,初步判断最终Fe3+被S2O32-还原为Fe2+,通过_______(填操作、试剂和现象),进一步证实生成了Fe2+。
从化学反应速率和平衡的角度解释实验Ⅱ的现象:_______实验Ⅲ:标定Na2S2O3溶液的浓度(5)称取一定质量的产品配制成硫代硫酸钠溶液,并用间接碘量法标定该溶液的浓度:用分析天平准确称取基准物质K2Cr2O7(摩尔质量为294g∙mol-1)0.5880g。
平均分成3份,分别放入3个锥形瓶中,加水配成溶液,并加入过量的KI并酸化,发生下列反应:6I-+Cr2O72-+14H+ = 3I2+2Cr3++7H2O,再加入几滴淀粉溶液,立即用所配Na2S2O3溶液滴定,发生反应I2+2S2O32- = 2I- + S4O62-,三次消耗 Na2S2O3溶液的平均体积为25.00 mL,则所标定的硫代硫酸钠溶液的浓度为_______mol∙L-1【答案】分液漏斗 蒸馏烧瓶 24232422H SO Na SO Na SO H O =SO +++↑ 硫化钠和碳酸钠的混合液 调节酸的滴加速度 若 SO 2过量,溶液显酸性.产物会发生分解 加入铁氰化钾溶液.产生蓝色沉淀 开始生成 Fe(S 2O 3)33-的反应速率快,氧化还原反应速率慢,但Fe 3+与S 2O 32- 氧化还原反应的程度大,导致Fe 3++3S 2O 32-⇌Fe(S 2O 3)33-(紫黑色)平衡向逆反应方向移动,最终溶液几乎变为无色 0.1600【解析】【分析】【详解】(1)a 的名称即为分液漏斗,b 的名称即为蒸馏烧瓶;b 中是通过浓硫酸和Na 2SO 3反应生成SO 2,所以方程式为:24232422H SO Na SO Na SO H O =SO +++↑;c 中是制备硫代硫酸钠的反应,SO 2由装置b 提供,所以c 中试剂为硫化钠和碳酸钠的混合溶液;(2)从反应速率影响因素分析,控制SO 2生成速率可以调节酸的滴加速度或者调节酸的浓度,或者改变反应温度;(3)题干中指出,硫代硫酸钠在酸性溶液中会分解,如果通过量的SO 2,会使溶液酸性增强,对制备产物不利,所以原因是:SO 2过量,溶液显酸性,产物会发生分解;(4)检验Fe 2+常用试剂是铁氰化钾,所以加入铁氰化钾溶液,产生蓝色沉淀即证明有Fe 2+生成;解释原因时一定要注意题干要求,体现出反应速率和平衡两个角度,所以解释为:开始阶段,生成3233Fe(S O )-的反应速率快,氧化还原反应速率慢,所以有紫黑色出现,随着Fe 3+的量逐渐增加,氧化还原反应的程度变大,导致平衡逆向移动,紫黑色逐渐消失,最终溶液几乎变为无色;(5)间接碘量法滴定过程中涉及两个反应:①2327226I Cr O 14H =3I 2Cr7H O --++++++;②2222346=I 2S O 2I S O ---++;反应①I -被氧化成I 2,反应②中第一步所得的I 2又被还原成I -,所以①与②电子转移数相同,那么滴定过程中消耗的227Cr O -得电子总数就与消耗的223S O -失电子总数相同 ;在做计算时,不要忽略取的基准物质重铬酸钾分成了三份进行的滴定。
化学氧化还原反应的专项培优练习题(含答案)附详细答案

一、高中化学氧化还原反应练习题(含详细答案解析)1.阳极泥处理后的沉渣中含AgCl,工业上可用Na2SO3溶液作浸取剂浸出回收。
某小组在实验室模拟该过程。
已知:i.25o C时,部分物质的溶解度:AgCl 1.9×10–4 g;Ag2SO3 4.6×10–4 g;Ag2SO40.84 g。
ii.25o C时,亚硫酸钠溶液酸化过中含4S+微粒的物质的量分数随pH变化如图所示。
Ⅰ.浸出氯化银取AgCl固体,加入1 mol/L Na2SO3溶液作浸取剂,充分反应后过滤得到浸出液(pH=8),2SO- [Ag(SO3)2]3– + Cl–。
该过程中发生的反应为AgCl +23(1)用平衡移动原理解释AgCl溶解的原因是___。
Ⅱ. 酸化沉银(2)经检测,沉淀m为AgCl,则溶液m中含4S+微粒的主要存在形式是________。
(3)探究沉淀n的成分。
①甲同学认为沉淀n一定不含Ag2SO4,其依据是________。
②乙同学认为沉淀n可能含Ag2SO3,进行实验验证。
i. 本实验设计的依据是:Ag2SO3具有________性。
ii. 乙同学观察到________,得出结论“沉淀n不含Ag2SO3”。
③丙同学从溶液n的成分角度再次设计实验证明沉淀n不含Ag2SO3。
i. 本实验设计的依据是:若沉淀n含Ag2SO3,则溶液n中含1Ag+微粒的总物质的量___(填“>”、“=”或“<”)Cl–物质的量。
ii. 结合实验现象简述丙同学的推理过程:____。
Ⅲ.浸取剂再生(4)溶液m经处理后可再用于浸出AgCl,请简述该处理方法____。
【答案】AgCl(s)Ag+(aq)+ Cl-(aq) ,Ag+与SO 32- 结合生成[Ag(SO3)2]3–,促进AgCl的溶解平衡正向移动 HSO3- Ag2SO4的溶解度远大于AgCl或Ag2SO3,溶液中Ag+ 的浓度很小还原b.中清液的颜色与..,均为浅紫色溶液< e中无沉淀生成,说明清液中没有Cl-,则.......c.相同溶液n中加入稀硝酸使[Ag(SO3)2]3–全部转化为Ag+,Ag+将Cl–全部沉淀,由此可知溶液n中含Ag元素的微粒总物质的量不小于n(Cl–) 加NaOH溶液调节pH至9~10【解析】【分析】I、(1)利用平衡移动的知识答题即可;II、(2)生成沉淀m时,溶液m的pH为5,观察图像,可以得知HSO3-的物质的量分数占100%;(3)①溶液中Ag+的浓度很小,而Ag2SO4的溶解度较大,故不会形成Ag2SO4沉淀;②依据Ag2SO3的还原性答题;③e中无沉淀生成,说明清液中没有Cl-,则溶液n中加入稀硝酸使[Ag(SO3)2]3–全部转化为Ag+,Ag+将Cl–全部沉淀,由此可分析出溶液n中含Ag元素的微粒总物质的量不小于n(Cl–);III、(4)m溶液中的溶质为NaHSO3,浸取剂为Na2SO3溶液,需要加入NaOH溶液将NaHSO3转化为Na2SO3。
2020-2021培优氧化还原反应辅导专题训练含答案

2020-2021培优氧化还原反应辅导专题训练含答案一、高中化学氧化还原反应1.亚氯酸钠(NaClO2)是二氧化氯(ClO2)泡腾片的主要成分。
实验室以氯酸钠(NaClO3)为原料先制得ClO2,再制备NaClO2粗产品,其流程如图:已知:①ClO2可被NaOH溶液吸收,反应为2ClO2+2NaOH=NaClO3+NaClO2+H2O。
②无水NaClO2性质稳定,有水存在时受热易分解。
(1)反应Ⅰ中若物质X为SO2,则该制备ClO2反应的离子方程式为___。
(2)实验在如图-1所示的装置中进行。
①若X为硫磺与浓硫酸,也可反应生成ClO2。
该反应较剧烈。
若该反应在装置A的三颈烧瓶中进行,则三种试剂(a.浓硫酸;b.硫黄;c.NaClO3溶液)添加入三颈烧瓶的顺序依次为___(填字母)。
②反应Ⅱ中双氧水的作用是___。
保持反应时间、反应物和溶剂的用量不变,实验中提高ClO2吸收率的操作有:装置A中分批加入硫黄、___(写出一种即可)。
(3)将装置B中溶液蒸发可析出NaClO2,蒸发过程中宜控制的条件为___(填“减压”、“常压”或“加压”)。
(4)反应Ⅰ所得废液中主要溶质为Na2SO4和NaHSO4,直接排放会污染环境且浪费资源。
为从中获得芒硝(Na2SO4·10H2O)和石膏(水合硫酸钙),请补充完整实验方案:___,将滤液进一步处理后排放(实验中须使用的试剂和设备有:CaO固体、酚酞、冰水和冰水浴)。
已知:CaSO4不溶于Na2SO4水溶液;Na2SO4的溶解度曲线如图−2所示。
【答案】2ClO3-+SO2═2ClO2+SO42- cab 作还原剂水浴加热时控制温度不能过高(或加一个多孔球泡等)减压向废液中分批加入适量CaO固体并搅拌,用冰水浴控制反应温度,对浊液取样并滴加酚酞,至溶液呈浅红色时停止加入CaO。
静置后过滤,用水洗涤沉淀2-3次得到石膏;滤液蒸发浓缩,冷却结晶至32.4℃以下,接近0℃,过滤,所得晶体用冰水洗涤2-3次,低温干燥得到芒硝【解析】【分析】用二氧化硫将NaClO3还原制得ClO2,ClO2和NaOH反应制得NaClO3和NaClO2,再用过氧化氢将NaClO3还原成NaClO2制得NaClO2粗品。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
一、高中化学氧化还原反应练习题(含详细答案解析)1.2ClO 是一种优良的消毒剂,浓度过高时易发生分解,为了运输和贮存便利常将其制成2NaClO 固体,模拟工业上用过氧化氢法制备2NaClO 固体的实验装置如图所示。
已知:2ClO 熔点-59℃、沸点11℃、22H O 沸点150℃A 中的化学方程式:32224222422NaClO H O H SO 2ClO O Na SO 2H O ++=↑+↑++(1)3NaClO 放入仪器A 中,仪器B 中的药品是__________(写化学式)。
如果仪器B 改成分液漏斗,实验过程中可能会出现的实验现象__________。
(2)C 装置有明显缺陷,请绘出合理的装置图(标明气流方向)__________。
(3)向A 装置中通入空气,其作用是赶出2ClO ,然后通过C 再到D 中反应。
通空气不能过快的原因是__________,通空气也不能过慢原因是__________。
(4)冰水浴冷却的目的是__________。
a.降低2NaClO 的溶解度b.减少22H O 的分解c.使2ClO 变为液态d.加快反应速率(5)写出D 中发生反应的化学方程式__________,22H O 在反应起到__________作用。
假设在反应中消耗掉22H O a g 则有__________mol 电子转移。
【答案】H 2O 2 液体无法顺利滴落 空气流速快时,2ClO 不能被充分吸收 空气流速过慢时,2ClO 不能及时被移走,浓度过高导致分解 abc2ClO 2+H 2O 2+2NaOH=2NaClO 2+O 2↑+2H 2O 还原剂 a/17【解析】【分析】氯酸钠(NaClO 3)在酸性条件下与过氧化氢生二氧化氯,ClO 2与氢氧化钠溶液和过氧化氢发生氧化还原反应生成NaClO 2,NaClO 2的溶解度随温度升高而增大,通过冷却结晶,过滤洗涤得到晶体NaClO 2•3H 2O 。
【详解】(1)3NaClO 放入仪器A 中,仪器B 中的药品是H 2O 2,仪器B 为滴液漏斗,其目的是平衡气压,使得溶液能够顺利滴入,如果仪器B 改成分液漏斗,实验过程中可能会出现的实验现象是:分液漏斗中的液体无法顺利滴落,反应无法继续进行;(2)实验中C 的作用是防止倒吸,C 装置中的右侧导管太短,不利于气体的流动,合理的装置图为:;(3)向A 装置中通入空气,其作用是赶出2ClO ,然后通过C 再到D 中反应。
空气流速不能过快,因为空气流速快时,2ClO 不能被充分吸收;空气流速也不能过慢,空气流速过慢时,2ClO 不能及时被移走,浓度过高导致分解;(4) NaClO 2的溶解度随温度升高而增大,过氧化氢易分解,所以冰水浴冷却的目的是:降低2NaClO 的溶解度、减少22H O 的分解,由于2ClO 的沸点较低,所以还能使2ClO 变为液态,方便使用;(5)写出D 中发生反应的化学方程式为:2ClO 2+H 2O 2+2NaOH=2NaClO 2+O 2↑+2H 2O ,22H O 在反应中得电子,起到还原剂的作用。
反应中存在关系:22H O ~2e -,若在反应中消耗掉22H O a g ,则转移的电子的物质的量为:2×a g/(34g·mol -1)= a/17mol 。
2.高锰酸钾是一种用途广泛的强氧化剂,实验室制备高锰酸钾所涉及的化学方程式如下: MnO 2熔融氧化:3MnO 2+ KClO 3+ 6KOH 熔融3K 2MnO 4+ KCl+3H 2OK 2MnO 4歧化:3K 2MnO 4+2CO 2=2KMnO 4+MnO 2↓+2K 2CO 3将MnO 2熔融氧化所得产物的热浸取液装入三颈烧瓶,再通入CO 2气体,使K 2MnO 4歧化的过程在如图装置中进行,A 、B 、C 、D 、E 为旋塞,F 、G 为气囊,H 为带套管的玻璃棒。
回答下列问题:(1)仪器a 的名称是______。
(2)MnO 2熔融氧化应放在______中加热(填仪器编号)。
①烧杯 ②瓷坩埚 ③蒸发皿 ④铁坩埚(3)为了能充分利用CO 2,装置中使用了两个气囊。
当试管内依次加入块状碳酸钙和盐酸后,关闭旋塞B 、E ,微开旋塞A ,打开旋塞C 、D ,往热K 2MnO 4溶液中通入CO 2气体,未反应的CO 2被收集到气囊F 中。
待气囊F 收集到较多气体时,关闭旋塞______,打开旋塞______,轻轻挤压气囊F,使CO2气体缓缓地压入K2MnO4溶液中再次反应,未反应的CO2气体又被收集在气囊G中。
然后将气囊G中的气体挤压入气囊F中,如此反复,直至K2MnO4完全反应。
(4)除去K2MnO4歧化产物中MnO2的操作方法是______。
(5)将三颈烧瓶中所得产物经过一系列操作得到针状的高锰酸钾晶体,最后采用低温烘干的方法来干燥产品,原因是______。
【答案】长颈漏斗④ AC BDE 过滤高锰酸钾晶体受热易分解【解析】【分析】(1)由实验装置可知,仪器a为长颈漏斗;(2)熔融固体物质需要在坩埚内加热,加热熔融物含有碱性KOH应用铁坩埚;(3)该操作的目的是将气囊F中的二氧化碳排出,据此判断正确的操作方法;(4)高锰酸钾溶于水,二氧化锰不溶于水;(5)高锰酸钾晶体受热易分解。
【详解】(1)由实验装置可知,仪器a为长颈漏斗,故答案为:长颈漏斗;(2)熔融固体物质需要在坩埚内加热,加热熔融物中含有碱性KOH,瓷坩埚中含有二氧化硅,二氧化硅能够与氢氧化钾反应,所以应用铁坩埚,故答案为:④;(3)待气囊F收集到较多气体时,需要将气囊F中二氧化碳排出到热K2MnO4溶液中,所以需要关闭A、C,打开B、D、E,轻轻挤压气囊F,从而使CO2气体缓缓地压入K2MnO4溶液中再次反应,故答案为:AC;BDE;(4)高锰酸钾溶于水,二氧化锰不溶于水,固液分离应用过滤的方法,则除去高锰酸钾溶液中的二氧化锰应用过滤的方法,故答案为:过滤;(5)高锰酸钾晶体受热易分解,实验时应采用低温烘干的方法来干燥产品,避免高锰酸钾晶体受热发生分解,故答案为:高锰酸钾晶体受热易分解。
3.某工业废水中主要含有Cr3+,同时还含有少量的Fe3+、Fe2+、Al3+、Ca2+和Mg2+等,且酸性较强。
为回收利用,通常采用如下流程处理:注:部分阳离子常温下以氢氧化物形式完全沉淀时溶液的pH见下表。
氢氧化物Fe(OH)3Fe(OH)2Mg(OH)2Al(OH)3Cr(OH)3pH 3.79.611.189(>9溶解)(1)氧化过程中可代替H2O2加入的试剂是________(填序号)。
A.Na2O2 B.HNO3 C.FeCl3 D.KMnO4(2)加入NaOH溶液调整溶液pH=8时,除去的离子是________;已知钠离子交换树脂的原理:M n++nNaR→MR n+nNa+,此步操作被交换除去的杂质离子是__________。
A.Fe3+B.Al3+C.Ca2+D.Mg2+(3)还原过程中,每消耗0.8 mol Cr2O72-转移4.8 mol e-,该反应离子方程式为____________。
【答案】A AB CD 3S2O32— + 4Cr2O72— + 26H+ = 6SO42— + 8Cr3+ +13H2O【解析】【分析】某工业废水中主要含有Cr3+,同时还含有少量的Fe3+、Al3+、Ca2+和Mg2+等,加双氧水把亚铁离子氧化为铁离子,同时Cr3+被氧化为Cr2O72-,加氢氧化钠调节pH=8,则Fe3+、Al3+转化为氢氧化铁和氢氧化铝沉淀,过滤,滤液中主要含有Cr2O72-、Ca2+和Mg2+等,通过钠离子交换树脂,除去Ca2+和Mg2+,然后加Na2S2O3把Cr2O72-还原为Cr3+,再调节pH得到Cr(OH)(H2O)5SO4;(1)加氧化剂主要目的是把亚铁离子氧化为铁离子,注意不能引入新的杂质;(2)根据表中数据判断;通过钠离子交换树脂,除去Ca2+和Mg2+;(3)每消耗0.8mol Cr2O72-转移4.8mol e-,则1molCr2O72-转移6mol电子,所以生成Cr3+,S2O32-被氧化为SO42-,结合得失电子守恒和原子守恒写出离子方程式。
【详解】某工业废水中主要含有Cr3+,同时还含有少量的Fe3+、Al3+、Ca2+和Mg2+等,加双氧水把亚铁离子氧化为铁离子,同时Cr3+被氧化为Cr2O72-,加氢氧化钠调节pH=8,则Fe3+、Al3+转化为氢氧化铁和氢氧化铝沉淀,过滤,滤液中主要含有Cr2O72-、Ca2+和Mg2+等,通过钠离子交换树脂,除去Ca2+和Mg2+,然后加Na2S2O3把Cr2O72-还原为Cr3+,再调节pH得到Cr(OH)(H2O)5SO4;(1)加氧化剂主要目的是把亚铁离子氧化为铁离子,同时不能引入新的杂质,所以可以用Na2O2代替H2O2,故答案为:A;(2)根据表中数据可知,pH=8时,Fe3+、Al3+转化为氢氧化铁和氢氧化铝沉淀,则Fe3+、Al3+被除去;通过钠离子交换树脂,除去Ca2+和Mg2+;(3)每消耗0.8mol Cr2O72-转移4.8mol e-,则1molCr2O72-转移6mol电子,所以生成Cr3+,S2O32-被氧化为SO42-,则反应的离子方程式为:3S2O32— + 4Cr2O72— + 26H+ = 6SO42— + 8Cr3+ +13H2O。
4.二氧化氯(ClO2)具有强氧化性,在工业上常用作水处理剂、漂白剂。
ClO2是一种易溶于水的黄绿色气体,其体积分数超过10%时易引起爆炸。
某研究小组欲用以下三种方案制备ClO2,回答下列问题:(1)以黄铁矿(FeS2)、氯酸钠和硫酸溶液混合反应制备ClO2,黄铁矿中的硫元素在酸性条件下被ClO3-氧化成SO42-,写出制备ClO2的离子方程式__。
(2)用过氧化氢作还原剂,在硫酸介质中还原NaClO3制备ClO2,并将制得的ClO2用于处理含CN-废水。
实验室模拟该过程的实验装置(夹持装置略)如图所示。
①装置A的名称是__,装置C的作用是__。
②反应容器B应置于30℃左右的水浴中,目的是__。
③通入氮气的主要作用有3个,一是可以起到搅拌作用,二是有利于将ClO2排出,三是__。
④ClO2处理含CN-废水的离子方程式为__,装置E的作用是__。
(3)氯化钠电解法是一种可靠的工业生产ClO2的方法。
①用于电解的食盐水需先除去其中的Ca2+、Mg2+、SO42-等杂质。
某次除杂操作时,往粗盐水中先加入过量的__(填化学式),至沉淀不再产生后,再加入过量的Na2CO3和NaOH,充分反应后将沉淀一并滤去。
②用石墨做电极,在一定条件下电解饱和食盐水制取ClO2,工作原理如图所示,写出阳极产生ClO2的电极反应式__。
