沉降菌检查原始记录
微检室沉降菌检验原始记录
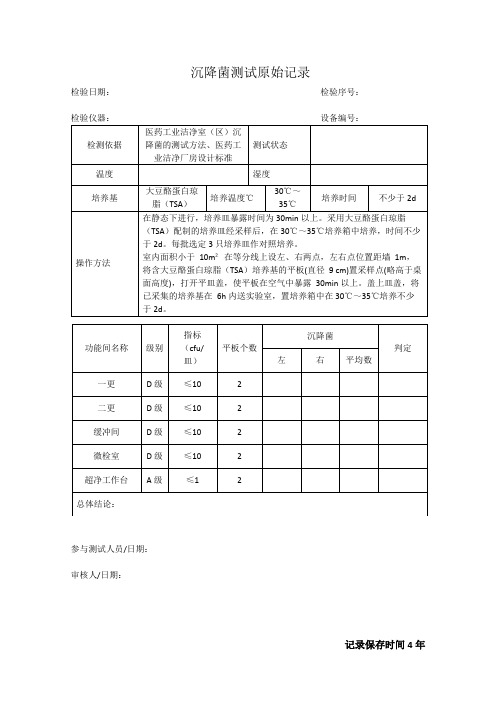
检验日期:检验序号:
检验仪器:设备编号:
检测依据
医药工业洁净室(区)沉降菌的测试方法、医药工业洁净厂房设计标准
测试状态
温度
湿度
培养基
大豆酪蛋白琼脂(TSA)
培养温度℃
30℃~35℃
培养时间
不少于2d
操作方法
在静态下进行,培养皿暴露时间为30min以上。采用大豆酪蛋白琼脂(TSA)配制的培养皿经采样后,在30℃~35℃培养箱中培养,时间不少于2d。每批选定3只培养皿作对照培养。
室内面积小于10m²在等分线上设左、右两点,左右点位置距墙1m,将含大豆酪蛋白琼脂(TSA)培养基的平板(直径9cm)置采样点(略高于桌面高度),打开平皿盖,使平板在空气中暴露30min以上。盖上皿盖,将已采集的培养基在6h内送实验室,置培养箱中在30℃~35℃培养不少于2d。
功能间名称
级别
指标
(cfu/皿)
平板个数
沉降菌
判定
左
右ቤተ መጻሕፍቲ ባይዱ
平均数
一更
D级
≤10
2
二更
D级
≤10
2
缓冲间
D级
≤10
2
微检室
D级
≤10
2
超净工作台
A级
≤1
2
总体结论:
参与测试人员/日期:
审核人/日期:
沉降菌监测记录

测试区域:测试状态:□静态□动态
测试依据:洁净室(区)环境监控管理规程
采样记录:
环境温度:℃、相对湿度:%
区域内采样时间:年月日时分至日时分静态测试每个皿采样时间30分钟。
动态测试每个培养皿采样时间4小时。
动态测试时,记录生产或检验开始和结束时间。
□生产时间:年月日时分至日时分
□检验时间:年月日时分至日时分采样人员数:人(静态测试洁净区内不得多于两人。
)
每个培养皿作好标示后,将每个房间的洁净级别、采样皿数填入下一页表中。
备注:
采样人员(签名):
培养记录
培养基名称:批号:有效期:
培养温度:℃设备编号:
培养时间:年月日时至日时;培养箱设定温度:℃培养温度:℃设备编号:
培养时间:年月日时至日时;培养箱设定温度:℃观察人(签名):
计数记录:
计数时间:年月日时
计数人将计数结果填入下表中,并计算平均菌落数。
计数人(签名):
判定标准:
每个房间或测点的沉降菌平均菌落数必须低于标准中的界限。
沉降菌监测记录。
洁净区沉降菌监SOP和检测记录

8、培养基表面暴露0.5小时后,收集培养皿,将培养皿倒置于恒温培养箱中,30-35℃培养48小时,每批培养基应有对照试验,每批可选定3只培养皿做对照培养,其中2只培养皿做阳性对照,1只培养皿做阴性对照。
9、达到规定的培养时间后,菌落数用肉眼直接计数、标记或在菌落计数器上点计,并用5-10倍放大镜检查,有否遗漏。
测试单位
测试依据
测试状态
环境温度
相对湿度
培养基
培养温度
检测日期
静压差
报告日期
平面
菌落数
区域
1
2
3
4
平均数
级别
备注
测定标准:
结论:
检验者:
复核者:
WM/QMS2-06-27
12、注意事项
(1)测试用具要作灭菌处理,以确保测试的可靠性、正确性。
(2)防止人为对样本的污染。
(3)采样时应仔细检查每个培养皿的质量,如发现变质、破损或污染的应剔除。
(4)一般采用透射光于培养皿背面或正面仔细观察,应注意培养皿边缘生长的菌落,并注意菌落与培养基沉Байду номын сангаас物的区别。
洁净室沉降菌检测记录
检验编号
责任者:质量部、车间相关人员。
程序:
1、质量保证室根据洁净区(室)的验证结果,建立洁净区(室)的日常监测计划,依计划和生产需要填写洁净区(室)环境监测通知(以下简称通知),经质量部负责人批准后,下发中心化验室和车间。
2、中心化验室接通知后,与车间讨论确定具体监测时间,安排好监测工作,确保监测工作如期完成,如不能按期完成监测,应由室主任填写“分析/评价延迟报告书”,经质量部负责人批准后,予以重新安排。
5、在监测前,对被监测洁净区(室)消毒。
沉降菌测试原始记录
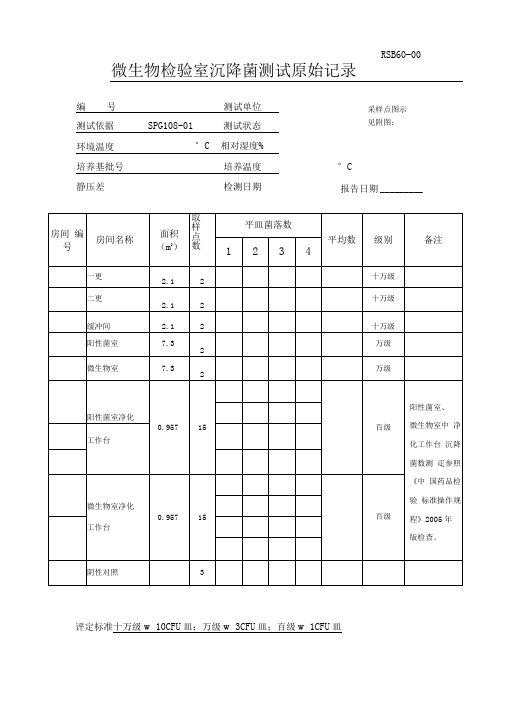
微生物检验室沉降菌测试原始记录评定标准十万级w 10CFU 皿;万级w 3CFU 皿;百级w 1CFU 皿RSB60-00°C采样点图示 见附图:报告日期 _________结 论 _______________________ 检验者 ____________ 复核者 ___________________RSB64-00固体制剂车间沉降菌测试原始记录(2)编 号______________________ 测试依据SPG108-01环境温度________________ °C培养基批号__________________ 测试单位 ______________ 测试状态 ______________ 相对湿度% _____________培养温度 ______________采样点图示 见附图:评定标准:十万级w 10CFU皿;万级w 3CFU皿;百级w 1CFU皿结论___________________检验者_________________ 复核者______________RSB63-00 固体制剂车间沉降菌测试原始记录(1 )评定标准: 十万级w 10CFU/皿; 万级w 3CFU/皿; 百级w 1CFU/皿 结 论 检验者 复核者 _____________________RSB61-00原料车间沉降菌测试原始记录编 号 ______________________ 测试单位 ________________ 测试依据SPG108-01 测试状态 _______________环境温度 _______________ ° C 相对湿度% ______________ 培养基批号 _________________ 培养温度 _________________ °C 静压差 ___________________ 检测日期 __________________ 报告采样点图示 见附图:日期评定标准:十万级w 10CFU/皿;万级w 3CFU/皿;百级w 1CFU/皿检验者复核者RSB62-00 原料车间沉降菌测试原始记录评定标准:十万级w 10CFU皿;万级w 3CFU皿;百级w 1CFU皿结论检验者复核者____________________RSB61-01 原料车间沉降菌测试原始记录编号测试单位测试依据SPG108-01 测试状态环境温度°C相对湿度% 培养基批号培养温度静压差检测日期采样点图示见附图:报告日期 _________评定标准:十万级w 10CFU/皿;万级w 3CFU/皿;百级w 1CFU/皿结论________________ 检验_______________ 复核者_______________。
沉降菌监测记录

沉降菌监测记录
集团企业公司编码:(LL3698-KKI1269-TM2483-LUI12689-ITT289-
沉降菌监测记录编码:SOR-QC-03
一、前期准备:
1、器皿灭菌:将已洗涤干净的培养皿(9cm),置于160℃干热灭菌4h备用。
2、培养基平皿的制备:
(1)平皿的制备:将制备好的培养基冷至约40℃,在无菌操作要求下将培养基注入培养皿每皿约15ml,同一方向旋转平皿,置净化工作台上待凝。
(2)将凝固后平皿倒置于培养箱中30℃-35℃恒温培养箱中培养48h,若培养基平皿上确无菌落生长,即可供采样用。
二、采集样品:
(1)将已制备好的培养皿,按洁净室沉降菌采样点布置图的要求放置,打开
培养皿盖,使培养基表面暴露30分钟,再将培养皿盖盖上后倒置。
(2)对照试验:每批培养基选定3个培养皿作对照培养,检验培养基本身是
否污染。
(3)培养:全部采样结束后,将平皿倒置于培养箱中按规定条件培养。
三、检测结果:
见附表:
附表1固体车间
附表2
液体车间
附表3
栓剂车间
附表4
提取理车间
附表5
质检中心
取样间。
沉降菌监测记录
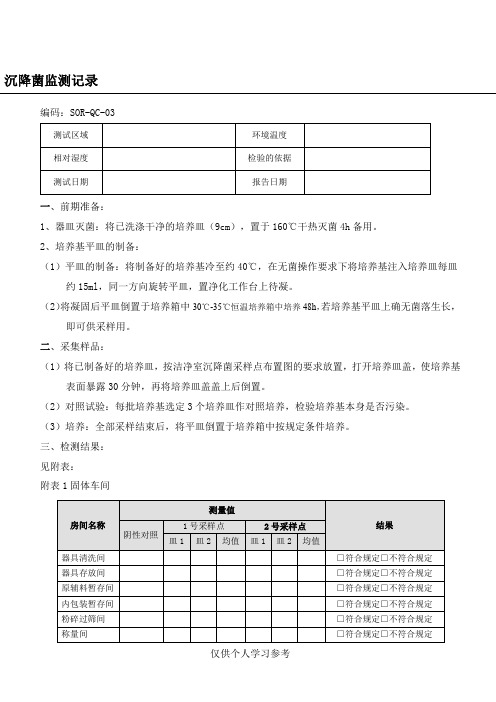
□符合规定□不符合规
器具存放间
□符合规定□不符合规
器具清洗间
□符合规定□不符合规
收膏间
□符合规定□不符合规
物料暂存间
□符合规定□不符合规
灭菌室
□符合规定□不符合规
总混室
□符合规定□不符合规
粉碎过筛间
□符合规定□不符合规
标准规定
≤10CFU/皿·0.5h
结论:□符合规定□不符合规
测试人
复核人
日期
结论:□符合规定□不符合规定
测试人
复核人
日期
□符合规定□不符合规
标准规定
≤3CFU/皿·0.5h
结论:□符合规定□不符合规定
测试人
复核人
日期
取样间
房间名称
测量值
结果
阴性对照
1号采样点
2号采样点
皿1
皿2
均值
皿1
皿2
均值
二更
□符合规定□不符合规
手消毒间
□符合规定□不符合规
走道
□符合规定□不符合规
取样间
□符合规定□不符合规
标准规定
≤10CFU/皿·0.5h
□符合规定□不符合规定
男二更
□符合规定□不符合规定
称量间
□符合规定□不符合规定
工衣清理间
□符合规定□不符合规定
女二更
□符合规定□不符合规定
原辅料存放间
□符合规定□不符合规定
器具清洗间
□符合规定□不符合规定
器具存放间
□符合规定□不符合规定
包材暂存间
□符合规定□不符合规定
灌装间2
□符合规定□不符合规定
灌装间3
(3)培养:全部采样结束后,将平皿倒置于培养箱中按规定条件培养。
检验室洁净区沉降菌测试记录表
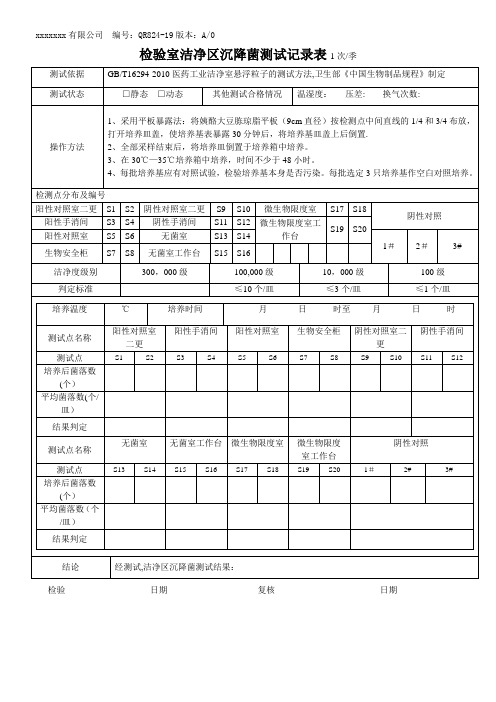
检验室洁净区沉降菌测试记录表1次/季
测试依据
GB/T16294-2010医药工业洁净室悬浮粒子的测试方法,卫生部《中国生物制品规程》制定
测试状态
□静态□动态
其他测试合格Βιβλιοθήκη 况温湿度:压差:换气次数:
操作方法
1、采用平板暴露法:将姨酪大豆胨琼脂平板(9cm直径)按检测点中间直线的1/4和3/4布放,打开培养皿盖,使培养基表暴露30分钟后,将培养基皿盖上后倒置.
2、全部采样结束后,将培养皿倒置于培养箱中培养。
3、在30℃—35℃培养箱中培养,时间不少于48小时。
4、每批培养基应有对照试验,检验培养基本身是否污染。每批选定3只培养基作空白对照培养。
检测点分布及编号
阳性对照室二更
S1
S2
阴性对照室二更
S9
S10
微生物限度室
S17
S18
阴性对照
阳性手消间
S3
S4
阴性手消间
S11
S12
微生物限度室工作台
S19
S20
阳性对照室
S5
S6
无菌室
S13
S14
1#
2#
3#
生物安全柜
S7
S8
无菌室工作台
S15
S16
洁净度级别
300,000级
100,000级
10,000级
100级
判定标准
-----
≤10个/皿
≤3个/皿
≤1个/皿
培养温度
℃
培养时间
月日时至月日时
测试点名称
阳性对照室二更
阳性手消间
洁净区沉降菌检测记录

洁净区沉降菌检测记录
编号:
房间名称
房间面积
洁净级别
测试状态
检测日期
报告日期
测试依据
培养基名称
胰酪大豆胨琼脂培养基
配制日期
培养温度
35℃
培养时间
天
采样点数目及编号
每点培养皿数
(个)
每点培养皿
菌落总数
平均菌落数
(个/皿)
评价标准
(个/皿)
数目
编号
结果评价
检测人
复核人
洁净区沉降菌检测记录
编号:
房间名称
房间面积
洁净级别
测试状态
检测日期
报告日期
测试依据
培养基名称
胰酪大豆胨琼脂培养基
配制日期
培养温度
35℃
培养时间
天
采样点数目及编号
每点培养皿数
(个)
每点培养皿
菌落总数
平均菌落数
(个/皿)Biblioteka 评价标准(个/皿)数目
编号
结果评价
检测人
复核人
洁净区(室)沉降菌测试记录

ABC制药有限公司
洁净区(室)沉降菌测试记录
文件编码:
测试依据:《医药工业洁净室(区)沉降菌的测试方法》GB/T16294-1996测试状态静态静压差Pa
相对湿度%培养基批号培养日时年月日时
环境温度℃培养温度℃ 被测单位记数日时年月日时
皿号
菌落数
ABC制药有限公司GMP文件
文件名称
洁净区(室)沉降菌测试记录
共 页
文件编码
文件类型
JL
颁发部门
GMP办公室
分发数量
起 草 人
日 期
审 核 人
日 期
批 准 人
日 期
执Байду номын сангаас日期
变更内容
修订号修订原因与内容执行日期
00
分发部门
总经 理 [ ] 副 总 经 理 [ ] 设备动力部 [ ]
生产 部 [ ] 质 保 部 [ ] 营 销 部 [ ]
房间名称
1
2
3
4
5
6
7
8
9
10
11
12
13
14
平均数
净化级别
评定标准
结论
检验人:复核人:
超净工作台沉降菌检测记录

嘉兴康谷医用材料有限公司 QMR-086-00
检测人
复核人
生效日期:2016年05月18日
KANGGU
无菌室
微生物限度室 1 2 3
无菌室
123
结果计 算:
平均菌落 数 M(个/ 皿) =
M1+ M2+. ..… Mn
n
456
456
M-平均 菌落 数
M11号 培养 皿菌 落数
M22号 培养 皿菌 落M数nnn号-培养
1 2 3 4 5 6 7 8 9 10 11 12 13 14
微生物限度室 1 2 3 4 5 6 7 8 9 10 11 12 13 14
无菌室
1 2 3 4 5 6 7 8 9 10 11 12 13 14
微生物限度室 1 2 3 4 5 6 7 8 9 10 11 12 13 14
无菌室
1 2 3 4 5 6 7 8 9 10 11 12 13 14
超净工作台沉降菌检测记录
7 8 9 10 11 12 13 14 7 8 9 10 11 12 13 14-086-00
生效日期:2016年05月18日
无菌室
1 2 3 4 5 6 7 8 9 10 11 12 13 14
微生物限度室 1 2 3 4 5 6 7 8 9 10 11 12 13 14
无菌室
1 2 3 4 5 6 7 8 9 10 11 12 13 14
微生物限度室 1 2 3 4 5 6 7 8 9 10 11 12 13 14
无菌室
KANGGU
超净工作台沉降菌检测记录
洁净度级
别:100
级测
试状态:
静态
检测依
洁净度微生物原始记录
18~26℃
45~65%
18~26℃
45~65%
18~26℃
45~65%
18~26℃
45~65%
18~26℃
45~65%
18~26℃
45~65%
18~26℃
45~65%
18~26℃
45~65%
18~26℃
45~65%
18~26℃
45~65%
广东省河源市药品检验所
洁净度检测记录
被检测单位
检测地点
广东省河源市药品检验所
洁净度检测记录
被检测单位
检测地点
功能间数
采样日期
检测状态
静态
检验依据
《药品生产质量管理规范》(1998年修订)
一、沉降菌落数
仪器及试剂:1、LS-B50L高压蒸汽灭菌器(器号:HX02U-265)上海华线医用核子仪器有限公司
2、DH5000A电热恒温培养箱(537)天津市泰斯特特仪器有限公司
3、营养琼脂培养基(批号070119)中国药品生物制品检定所
检测结果:
功能间名称
级别
温度(℃)
湿度(%)
沉降菌微生物数量
最大允许数(个/皿)
Байду номын сангаас检测
结论
标准
实测
标准
实测
标准
实测
18~26℃
45~65%
18~26℃
45~65%
18~26℃
45~65%
18~26℃
45~65%
18~26℃
45~65%
18~26℃
功能间数
采样日期
检测状态
静态
检验依据
《药品生产质量管理规范》(1998年修订)
微生物分析室洁净室沉降菌检测记录
嘉兴康谷医用材料有限公司
洁净度级 别:十万 级技、 术万 指级 标: ≤3个/皿
微生物分析室洁净室沉降菌检测记录
检测日期
检测地点
平皿编号及菌落数
平均值(个/皿)
空白对照长菌数 (个/皿)
1
2
阳性间一更(十万级)
1
2
阳性间二更(十万级)
阳性对照间(万级)
1
2
1
2
微限室一更(十万级)
1
2
微限室二更(十万级)
M1-1号
培养皿
n
菌落数
Mn-n号培养皿 菌落数
结论
QMR-067-00
检测人 复核人
n--培养皿 总数
生效日期:2016年05月18日
2
阳性间一更(十万级)
1
2
阳性间二更(十万级)
阳性对照间(万级)
1
2
1
2
微限室一更(十万级)
1
2
微限室二更(十万级)
1
2
微生物限度室(万级)
1
2
无菌室一更(十万级)
1
2
无菌室二更(十万级)
结果计 算:
1
无菌室(万级)
M1+M2+...…Mn
2
M--平均 菌落数
M2-2号培养皿 菌落数
平均菌落数 M(个/皿)
1
2
微生物限度室(万级)
1
2
无菌室一更(十万级)
1
2
无菌室二更(十万级)无菌室(万级)121
2
阳性间一更(十万级)
1
2
阳性间二更(十万级)
阳性对照间(万级)
