化合物的颜色
高中阶段化合物,离子,单质的颜色大全

蓝CuO、CuS 黑FeSCN2+血红Fe(OH)3红褐Mn2+水红Cu2O红Fe(CN)64- 黄Fe(OH)2白Cr3+绿Cu(NH3)42+ 深蓝Fe(CN)63- 红MnS粉红Cr2+蓝白CrO42-黄KMnO4紫Fe3+浅黄CuSO4.5H2O 蓝Cr2O72-橙K2MnO4绿Fe2+绿Cu(OH)2蓝Cr2O3绿Ag2CrO4砖红Co2+无色Cu2[Fe(CN)6] 红蓝MnO2黑褐Cu+无色Zn3[Fe(CN)6]2白Co(H2O)62+红AgCl白1、常见物质的颜色:多数气体为无色,多数固体化合物为白色,多数溶液为无色。
2、一些特殊物质的颜色:黑色:MnO2、CuO、Fe3O4、C、FeS(硫化亚铁)蓝色:CuSO4•5H2O、Cu(OH)2、CuCO3、含Cu2+ 溶液、液态固态O2(淡蓝色)红色:Cu(亮红色)、Fe2O3(红棕色)、红磷(暗红色)黄色:硫磺(单质S)、含Fe3+ 的溶液(棕黄色)绿色:FeSO4•7H2O、含Fe2+ 的溶液(浅绿色)、碱式碳酸铜[Cu2(OH)2CO3]无色气体:N2、CO2、CO、O2、H2、CH4有色气体:Cl2(黄绿色)、NO2(红棕色)有刺激性气味的气体:NH3(此气体可使湿润pH试纸变蓝色)、SO2有臭鸡蛋气味:H2S3、常见一些变化的判断:①白色沉淀且不溶于稀硝酸或酸的物质有:BaSO4、AgCl(就这两种物质)②蓝色沉淀:Cu(OH)2、CuCO3③红褐色沉淀:Fe(OH)3Fe(OH)2为白色絮状沉淀,但在空气中很快变成灰绿色沉淀,再变成Fe(OH)3红褐色沉淀④沉淀能溶于酸并且有气体(CO2)放出的:不溶的碳酸盐⑤沉淀能溶于酸但没气体放出的:不溶的碱另外有一个较系统的中学常见物质颜色说明:①元素基本上按周期表的族序数排列;②物质基本上按单质、氢化物、氧化物及其水化物、盐、有机物的顺序排列;③许多物质晶状为无色,粉末状为白色,晶型不同可能有不同颜色;④硫化物和过渡元素化合物颜色较丰富。
化学常见物质颜色

化学常见物质颜色:
1.银白色:铁,铝,锡,银等金属。
2.红色:铜,氧化铁,红磷,三氧化二铬等。
3.绿色:碱式碳酸铜,亚铁离子的盐类,除铜以外的铜合金。
4.蓝色:蓝色硫酸铜,氢氧化铜等。
5.黄色:硫,过氧化钠,溴化银等。
6.橙色:溴水,液态的氟碳银等。
7.紫色:高锰酸钾,碘的淀粉溶液,石蕊试液等。
8.黑色:多数过渡金属的化合物,还原剂的氧化物,低价铁的化
合物,多数非金属元素的单质(石墨)等。
9.灰色:多数主族金属的化合物,还原剂的氧化物,低价铜的化
合物,少数非金属元素的单质(灰锡)等。
10.白色:行无常性,下雪,霜,盐,白磷等。
附录2 常见离子和化合物的颜色

高中化学教研团队
2− Cr2 O 7 (橙色)、 CrO 2 4 (黄色)、 MnO 4 (紫色)、
阴离子
3− 4MnO 24 (绿色)、 [Fe(CN) 6 ] (黄绿色)、 [Fe(CN) 6 ] (黄棕色)
表 2 有特征颜色的常见无机化合物 红色 粉红色 黄色 绿色 蓝色 紫色 黑色 Fe2O3、Cu2O、HgO、Pb3O4 MnSO4·7H2O 等锰盐 PbO、AgI、铬酸盐(如 BaCrO4、K2CrO4) 镍盐、亚铁盐、铬盐、某些铜盐如 CuCl2·2H2O、碱式碳酸铜 CuSO4·5H2O、Cu(NO3)2·3H2O 高锰酸盐 CuO、FeO、Fe3O4、MnO2、FeS、CuS、Ag2S、PbS
附录 2 常见离子和化合物的颜色
表 1 常见离子的颜色 无 色
2+ 2+ 2+ 3+ 2+ 4+ Ag+、K+、Ca2+、Pb2+、Zn2+、Na+、 NH + 4 、Ba 、Hg 、Mg 、Al 、Sn 、Sn
阳离子 有 色 Mn2+(浅玫瑰色,稀溶液无色)、 [Fe ( H2 O )6 ]3+ (淡紫色,常见铁盐黄色或红棕色)、
阳离子 Fe2+(浅绿色,稀溶液无色)、Cr3+(绿色或紫色)、Co2+(玫瑰色)、Ni2+(绿色)、Cu2+(浅蓝色) 无 色
2322− SO 24 、 PO 4 、 F 、 SCN 、 C 2 O 4 、 SO3 、 Cl 、 NO 3 、 S 、
阴离子 有 色ຫໍສະໝຸດ 22− 、 CO 3 、 SiO3 、 I- 、 CH 3COO- 、 BrO3 Br - 、 NO-2 、 ClO3
常见化合物颜色

常见物质的颜色的状态1、白色固体:MgO、P2O5、CaO、NaOH、Ca(OH)2、KClO3、KCl、Na2CO3、NaCl、无水CuSO4;铁、镁为银白色(汞为银白色液态)2、黑色固体:石墨、炭粉、铁粉、CuO、MnO2、Fe3O4▲KMnO4为紫黑色3、红色固体:Cu、Fe2O3 、HgO、红磷▲硫:淡黄色▲ Cu2(OH)2CO3为绿色4、溶液的颜色:凡含Cu2+的溶液呈蓝色;凡含Fe2+的溶液呈浅绿色;凡含Fe3+的溶液呈棕黄色,其余溶液一般不无色。
(高锰酸钾溶液为紫红色)5、沉淀(即不溶于水的盐和碱):①盐:白色↓:CaCO3、BaCO3(溶于酸)AgCl、BaSO4(也不溶于稀HNO3) 等②碱:蓝色↓:Cu(OH)2 红褐色↓:Fe(OH)3白色↓:其余碱。
Cu CuO Cu2(OH)2CO3 CuSO4 Cu(OH)2 CuSO4溶液红色黑色绿色蓝色蓝色蓝色Fe Fe2O3 Fe3O4 Fe2+溶液Fe3+溶液Fe(OH)3银白色红色黑色浅绿色黄色红褐色在初三阶段,接触最多的沉淀可以总结为“六白”“一蓝”“一红褐”“六白”CaCO3 Ag2 CO3 BaCO3 BaSO4 AgCl Mg(OH)2“一蓝”Cu(OH)2“一红褐” Fe(OH)3一。
关键以下(1)Cu的:单质红色,CuO黑色,无水CuSO4白色,遇到水和其余二价铜蓝色(2)Fe的:单质银白色,实验得到的单质黑色,二价铁浅绿色,三价铁中氧化铁红色,溶液黄色,Fe(OH)3沉淀红褐色(3)白色的沉淀:BaCO3 CaCO3 BaSO4 AgCl ,其中前面两个虽不溶于水,但溶于酸且放出二氧化碳。
后面两个不溶于水,也不溶于酸。
一共14种物质,不用两小时可以记住。
记住这14种物质后,花两分钟再记住下列4种不常考到的二。
比较少考到的颜色:KMnO4紫黑色;MnO2和C粉黑色;KClO3白色一、初中阶段一共14种物质的颜色是关键:(1) Cu的:单质红色,CuO黑色,无水CuSO4白色,遇到水和其余二价铜都是蓝色(2)Fe的:单质银白色,实验得到的是单质黑色粉末状,二价铁浅绿色,三价铁中氧化铁红色,溶液黄色,Fe(OH)3沉淀红褐色(3)白色的沉淀:BaCO3 、CaCO3 ,虽不溶于水,但溶于酸且放出二氧化碳。
过渡金属化合物的颜色

常见过渡金属离子及化合物颜色:一.铜副族(IB):1.1铜化合物:焰色绿;CuF 红;CuCl 白↓;CuBr 黄↓;CuI 棕黄↓;Cu2SO4灰黑色(在水溶液中歧化)CuCN 白↓;Cu2O暗红;Cu2S 黑;CuF2 白;CuCl2 棕黄(浓溶液黄绿);CuBr2 棕;Cu(CN)2 棕黄;CuO 黑;CuS黑↓;CuSO4 无色;CuSO4·5H2O 蓝;Cu(OH)2 淡蓝↓;Cu(OH)2·CuCO3 墨绿;[Cu(H2O)4]2+蓝;[Cu(OH)4]2‐蓝紫;Cu(NH3)4]2+ 深蓝;[CuCl4]2‐黄;[Cu(en)2]2+ 深蓝紫;(CuCO3·Cu(OH) 2)亮红色(孔雀石)(Cu3 (CO3) 2 (OH) 2)蓝色(石青)K2[Cu(CO3)2](暗蓝色)、K2 [Cu(CO3)2]·2H2O(亮蓝色)K2[Cu(CO3)2]·4H2O(浅蓝绿色)炔铜红↓.1.2 银化合物:AgOH 白(常温分解);Ag2O 黑;新制AgOH 棕黄(混有Ag2O);蛋白银(AgNO3滴手上) 黑↓;AgF 白;AgCl 白↓;AgBr 淡黄↓;AgI 黄↓(胶体);Ag2S 黑↓;Ag4[Fe(CN)6]白↓;Ag3[Fe(CN)6] 白↓;Ag+,[Ag(NH3)2]+,[Ag(S2O3)2]3‐,[Ag(CN)2]‐无色.1.3 金化合物:HAuCl4·3H2O 亮黄晶体;KAuCl4·1.5H2O 无色片状晶体;Au2O3 黑;H[Au(NO3)4]·3H2O 黄色晶体;AuBr 灰黄↓;AuI 柠檬黄↓.二.锌副族(IIB):2.1 锌化合物:ZnO 白(锌白颜料)↓;ZnI2 无色;ZnS 白↓;ZnCl2 白色晶体(溶解度极大,水溶液酸性).2.2 镉化合物:CdO 棕灰↓;CdI2 黄;CdS 黄(镉黄颜料)↓;HgCl2(升汞) 白色;HgNH2Cl白↓;Hg2Cl2(甘汞) 白↓.2.3 汞化合物:HgO 红(大晶粒)或黄(小晶粒)↓;HgI2 红或黄(微溶);HgS 黑或红↓;Hg2NI·H2O 红↓;Hg2(NO3)2 无色晶体.三. 钪副族(IIIB):略四.钛副族(IVB):4.1 钛化合物:Ti3+ 紫红;[TiO(H2O2)2]2+ 橘黄;H2TiO3 白色↓;TiO2 白(钛白颜料)或桃红(金红石)↓;(NH4)2TiCl6 黄色晶体;[Ti(H2O)6]Cl3 紫色晶体;[Ti(H2O)5Cl]Cl2·H2O 绿色晶体;TiCl4 无色发烟液体.4.2 锆、铪:MO2,MCl4 白.五. 钒副族(VB):5.1 钒化合物:V2+ 紫;V3+ 绿;V4+ 蓝;V5+ 黄;VO 黑;V2O3 黑;VO2 黄;V2O5 黄或砖红;水合V2O5 棕红;饱和V2O5 溶液(微溶) 淡黄.VO4^3‐黄。
无机化合物颜色大全

无机化合物颜色大全

无机颜色表含部分元素化合物常温下物态、颜色、形态等物理化学性质卤族(英VIIA):Solid:I2 紫黑;ICl 暗红;IBr 暗灰;IF3 黄色;ICl3 橙;I2O5 白;I2O4 黄(离子晶体);I4O9 黄(离子晶体). Liquid:Br2 红棕;BrF3 浅黄绿;IBr3 棕;Cl2O6暗红;Cl2O7 无色油状;HClO4 无色粘稠状;(SCN)2 黄色油状.Gas:F2 浅黄;(CN)2无色;Cl2 黄绿;I2(g) 紫;BrF 红棕;BrCl 红;Cl2O 黄红;ClO2 黄色;Br2O 深棕;(SCN)n 砖红色固体.氧族(英VIA):Solid:S 淡黄;Se 灰,褐;Te 无色金属光泽;Na2S,(NH4)2S,K2S,BaS 白,可溶;ZnS 白↓;MnS 肉红↓;FeS 黑↓;PbS 黑↓;CdS 黄↓;Sb2S3 橘红↓;SnS 褐色↓;HgS 黑(沉淀),红(朱砂);Ag2S 黑↓;CuS 黑↓;Na2S2O3 白;Na2S2O4 白;SeO2 白,易挥发;SeBr2 红;SeBr4 黄;TeO2 白加热变黄;H2TeO3 白;TeBr2 棕;TeBr4 橙;TeI4 灰黑;PoO2 低温黄(面心立方),高温红(四方);SO3 无色;SeO3 无色易潮解;TeO3 橙色;H6TeO6 无色.Liquid:H2O 无色;纯H2O2 淡蓝色粘稠;CrO(O2)2(aq) 蓝;纯H2SO4 无色油状;SO32-(aq) 无色;SO42-(aq) 无色;SeO2(l) 橙;TeO2(l) 深红.Gas:O2 无色;O3 低浓度无色,高浓度淡蓝(鱼腥味);S2(g) 黄,上浅下深;H2S 无色;SO2 无色;H2Se 无色;H2Te 无色.卤化硫(未注明者均为无色):Liquid:SF6;S2F10;SCl4 淡黄;SCl2 红籗2Cl2 无色;S2Br2 红.Gas:SF4;SF2;S2F2.卤砜、卤化亚砜、卤磺酸:Liquid:SOCl2 白色透明;SO2Cl2 无色发烟.氮族(英VA):Solid:铵盐无色晶体;氮化金属白;N2O3 蓝色(低温);N2O5 白;P 白,红,黑;P2O3 白;P2O5 白;PBr3 黄;PI3 红;PCl5 无色;P4Sx 黄;P2S3 灰黄;P2S5 淡黄;H4P2O7 无色玻璃状;H3PO2 白;As 灰;As2O3 白;As2O5 白;AsI3 红;As4S4 红(雄黄);As4S6 黄(雌黄);As2S5 淡黄;Sb 银白;Sb(OH)3 白↓;Sb2O3 白(锑白,颜料);Sb2O5 淡黄;SbX3(XI) 白;SbI3 红;Sb2S3 橘红↓;Sb2S5 橙黄;Bi 银白略显红;Bi2O3 淡黄;Bi2O5 红棕;BiF3 灰白;BiCl3 白;BiBr3 黄;BiI3 黑↓;Bi2S3 棕黑.Liquid:N2H4 无色;HN3 无色;NH2OH 无色;发烟硝酸红棕;NO3^-(l)无色;王水浅黄,氯气味;硝基苯黄色油状;氨合电子(液氨溶液) 蓝;PX3 无色;纯H3PO4 无色粘稠状;AsX3(XI) 无色;.Gas:N2 无色;NH3 无色;N2O 无色甜味;NO 无色;NO2 红棕;PH3 无色;P2H6 无色;AsH3 无色;SbH3 无色;BiH3 无色.卤化氮(未注明者均为无色):Solid:NBr3•(NH3)6 紫,爆炸性;NI3•(NH3)6 黑,爆炸性;Liquid:NCl3;无色Gas:NF3;无色碳族(英IVA):Solid:C(金刚石) 无色透明;C(石墨) 黑色金属光泽;Si 灰黑色金属光泽;Ge 灰白;Sn 银白;Pb 暗灰;SiO2 无色透明;H2SiO3 无色透明胶状↓;Na2SiF6 白晶;GeO 黑;GeO2 白;SnO 黑;SnO2 白;Sn(OH)2 白↓;PbO黄或黄红;Pb2O3 橙;Pb3O4 红;PbO2 棕;CBr4 淡黄;CI4 淡红;GeI2 橙;GeBr2 黄;GeF4 白;GeBr4 灰白;GeI4 黄;SnF2 白;SnCl2 白;SnBr2 淡黄;SnI2 橙;SnF4 白;SnBr4 无色;SnI4 红;PbF2 无色↓;PbCl2 白↓;PbBr2 白;PbI2 金黄;PbF4 无色;GeS 红;GeS2 白;SnS 棕↓;SnS2 金黄(俗称“金粉”)↓;PbS 黑↓;PbS2 红褐;Pb(NO3)2 无色;Pb(Ac)2•3H2O 无色晶体;PbSO4 白↓;PbCO3 白↓;Pb(OH)2 白↓;Pb3(CO3)2(OH)2 铅白↓;PbCrO4 亮黄↓.Liquid:CCl4 无色;CS2 无色;GeCl4 无色;SnCl4 无色;PbCl4 无色.Gas:CO CO2 CH4 CF4 SiF4 SiH4 均为无色.硼族(英IIIA):Solid:B(无定型) 棕色粉末;B(晶体) 黑灰;Al 银白;Ga 银白(易液化);In 银灰;Tl 银灰;B2O3 玻璃状;H3BO3 无色片状;BN 白;Na2B4O7•10H2O 白色晶体;Cu(BO2)2 蓝↓;Ni(BO2)2 绿↓;NaBO2•Co(BO2)2 蓝↓;NaBO2•4H2O 无色晶体;无水NaBO2 黄晶;Al2O3 白晶;AlF3 无色;AlCl3 白;AlBr3 白;AlI3 棕;Al(OH)3 白↓;Ga2O3 白↓Ga(OH)3 白↓;GaBr3 白;GaI3 黄;In2O3 黄;InBr3 白;InI3 黄;TlOH 黄;Tl2O 黑;Tl2O3 棕黑;TlCl 白↓;TlBr 浅黄↓;TlI 黄↓(与银相似);TlBr3 黄;TlI3 黑.Liquid:BCl3 无色发烟.Gas:硼烷无色;BF3 无色(有窒息气味).碱土(英IIA):单质:银白焰色:Ca 砖红;Sr 洋红;Ba 绿.氧化物:均为白色固体.氢氧化物:白色固体Be(OH)2↓,Mg(OH)2↓.盐:多为无色或白色晶体;BeCl2 浅黄;BaCrO4 黄↓;CaF2 白↓.碱金属(英IA):单质:银白焰色:Li 红;Na 黄;K 紫;Rb 紫红;Cs 紫红.氧化物、过氧化物、超氧化物、臭氧化物:Li2O 白;Na2O 白;K2O 淡黄;Rb2O 亮黄;Cs2O 橙红;Na2O2 淡黄;KO2橙黄;RbO2深棕;CsO2 深黄;KO3 橘红.氢氧化物:白色,LiOH白↓.盐:多为无色或白色晶体且易溶于水.不溶盐↓(未注明者皆为白色晶体):LiF Li2CO3 Li3PO4 LiKFeIO6 Na[Sb(OH)6] NaZn(UO2)3(A c)9•6H2O 黄绿;M=K,Rb,Cs M3[Co(NO2)6] 亮黄;MBPh4 MClO4 M2PtCl6 淡黄;CsAuCl4.铜副族(英IB):单质:Cu 紫红或暗红;Ag 银白;Au 金黄.铜化合物:焰色绿;CuF 红;CuCl 白↓;CuBr黄↓;CuI 棕黄↓;CuCN 白↓;Cu2O 暗红;Cu2S 黑;CuF2 白;CuCl2 棕黄(溶液黄绿);CuBr2 棕;Cu(CN)2 棕黄;CuO 黑↓;CuS黑↓;CuSO4 无色;CuSO4•5H2O 蓝;Cu(OH)2 淡蓝↓;Cu(OH)2•CuCO3 墨绿;[Cu(H2O)4]2+ 蓝;[Cu(OH)4]2- 蓝紫;[Cu(NH3)4]2+ 深蓝;[CuCl4]2- 黄;[Cu(en)2]2+ 深蓝紫;Cu2[Fe(CN)6] 棕红;炔铜红↓.银化合物:AgOH 白(常温分解);Ag2O 黑;新制AgOH 棕黄(混有Ag2O);蛋白银(AgNO3滴手上) 黑↓;AgF 白;AgCl 白↓;AgBr 淡黄↓;AgI 黄↓(胶体);Ag2S 黑↓;Ag4[Fe(CN)6] 白↓;Ag3[Fe(CN)6] 白↓;Ag+,[Ag(NH3)2]+,[Ag(S2O3)2]3-,[Ag(CN)2]- 无色.金化合物:HAuCl4•3H2O 亮黄晶体;KAuCl4•1.5H2O 无色片状晶体;Au2O3 黑;H[Au(NO3)4]•3H2O 黄色晶体;AuBr 灰黄↓;AuI 柠檬黄↓.锌副族(I英IB):单质:均为银白,Hg在水溶液中的沉淀为黑色.锌化合物:ZnO 白(锌白颜料)↓;ZnI2 无色;ZnS 白↓;ZnCl2 白色晶体(溶解度极大,水溶液酸性);K3Zn3[Fe(CN)6] 白;Zn3[Fe(CN)6]2 黄褐.镉化合物:CdO 棕灰↓;CdI2 黄;CdS 黄(镉黄颜料)↓;HgCl2(升汞) 白色;HgNH2Cl 白↓;Hg2Cl2(甘汞) 白↓.汞化合物:HgO 红(大晶粒)或黄(小晶粒)↓;HgI2 红或黄(微溶);HgS 黑或红↓;Hg2NI•H2O 红↓;Hg2(NO3)2 无色晶体.ZnS荧光粉:Ag 蓝;Cu 黄绿;Mn 橙.钪副族(英IIIB):略.钛副族(英IVB):钛化合物:Ti3+ 紫红;[TiO(H2O2)2]2+ 橘黄;H2TiO3 白色↓;TiO2 白(钛白颜料)或桃红(金红石)↓;(NH4)2TiCl6 黄色晶体;[Ti(H2O)6]Cl3 紫色晶体;[Ti(H2O)5Cl]Cl2•H2O 绿色晶体;TiCl4 无色发烟液体. 锆、铪:MO2,MCl4 白.钒副族(英VB):钒化合物:V2+ 紫;V3+ 绿;VO2+ 蓝;V(OH)4^- 黄;VO4^3- 黄;VO 黑;V2O3 灰黑;V2S3 棕黑;VO2 蓝色固体;VF4 绿色固体;VCl4 暗棕色液体;VBr4 洋红色液体;V2O5 黄或砖红;水合V2O5 棕红;饱和V2O5溶液(微溶) 淡黄;[VO2(O2)2]3- 黄;[V(O2)3]3- 红棕.钒酸根缩聚:随着钒氧原子数之比的减少的,由浅黄~深红~淡黄.铌、钽:略.铬副族(英VIB):铬化合物:Cr2+ 蓝;Cr3+ 紫;Cr2O72- 橙红;CrO42- 黄;Cr(OH)4- 亮绿;Cr(OH)3灰蓝;Cr2O3 绿;CrO3 暗红色针状;[CrO(O2)2]OEt2 蓝;CrO2Cl2 深红色液体;Na2Cr2O7,K2CrO7 橙红;Ag2CrO4 砖红↓;BaCrO4 黄↓;PbCrO4 黄↓.紫红Cr2(SO4)3•18H2O——〉绿色Cr2(SO4)3•6H2O——〉桃红Cr2(SO4)3暗绿[Cr(H2O)4Cl2]Cl—冷却HCl—〉紫色[Cr(H2O)6]Cl3—乙醚HCl—〉淡绿[Cr(H2O)5Cl]Cl2[Cr(H2O)6]3+ 紫;[Cr(H2O)4(NH3)2]3+ 紫红;[Cr(H2O)3(NH3)3]3+ 浅红;[Cr(H2O)2(NH3)4]3+ 橙红;[Cr (NH3)5H2O]3+ 橙黄;[Cr(NH3)6]3+ 黄.钼、钨:MoO3 白;棕色MoCl3;绿色MoCl5;MoS3 棕色↓;(NH4)3[P(Mo12O40)]•6H2O 黄色晶状↓;WO3 深黄;H2WO4•xH2O 白色胶体.锰副族(英VIIB):锰化合物:Mn2+ 肉红;Mn3+ 紫红;MnO42- 绿;MnO4- 紫;MnO3+ 亮绿;Mn(OH)2 白↓;MnO(OH)2 棕↓;MnO2 黑↓;无水锰盐(MnSO4) 白色晶体;六水合锰盐(MnX2•6H2O, X=卤素,NO3,ClO4) 粉红;MnS•nH2O 肉红↓;无水MnS 深绿;MnCO3 白↓;Mn3(PO4)2 白↓;KMnO4 紫红;K2MnO4 绿;K2[MnF6] 金黄色晶体;Mn2O7 棕色油状液体.锝、铼:略.铁系(第四周期VIII族):铁化合物:Fe2+ 浅绿;[Fe(H2O)6]3+ 浅紫;[Fe(OH)(H2O)5]2+ 黄;FeO42- 紫红;FeO 黑;Fe2O3 暗红;Fe(OH)2 白↓;Fe(OH)3 棕红↓;FeCl3 棕红晶体;无水FeSO4 白;FeSO4•7H2O 绿;K4[Fe(CN)6](黄血盐) 黄色晶体;K3[Fe(CN)6](赤血盐) 红色晶体;Fe2[Fe(CN)6] 普鲁士蓝↓;Fe[Fe(CN)6] 黑↓;Fe(C5H5)2(二茂铁) 橙黄色晶体;M2Fe6(SO4)4(OH)12(黄铁矾,M=NH4,Na,K) 浅黄色晶体;Fe(CO)5 黄色液体.钴化合物:Co2+ 粉红;CoO 灰绿;Co3O4 黑;Co(OH)3 棕↓;Co(OH)2 粉红↓;Co(CN)2 红;K4[Co(CN)6] 紫色晶体;Co2(CO)8 黄色晶体;[Co(SCN)6]4- 紫;氯化钴脱水变色:粉红CoCl2•6H2O—325K—〉紫红CoCl2•2H2O—3l3K—〉蓝紫CoCl2•H2O—393K—〉蓝CoCl2.镍化合物:Ni2+ 亮绿;[Ni(NH3)6]2+ 紫;Ni(OH)2 绿↓;Ni(OH)3 黑↓;无水Ni(II)盐黄;Na2[Ni(CN)4] 黄;K2[Ni(CN)4] 橙;Ni(CO)4 无色液体.铂系元素(第五、六周期VIII族):Os 蓝灰色易挥发固体;Pd↓(aq) 黑;OsO4 无色有特殊气味气体;H2PtCl6 橙红色晶体;Na2PtCl6 橙黄色晶体;M2PtCl6(M=K,Rb,Cs,NH4) 黄色↓.镧系锕系元素:暂无.稀有气体元素:单质:He、Ne、Ar、Kr、Xe、Rn 无色,微溶于水;氪化合物:KrF2 无色,25℃分解;氙化合物:XeF2,XeF4,XeF6无色,熔沸点依次降低;XeOF4,XeO2F2,XeO2无色;XeO3 黄色,0℃爆炸;氙-金属配合物:XeF[RuF6],[Xe2F3][AsF6],XeF3[SbF6],XeF3[Sb2F11] 黄绿色固;XeF[Sb2F11]黄;XeF5[AsF6] 白固;XeF5[RuF6] 绿固。
Ⅷ族化合物的颜色

FeO42-紫红色
CoCl2·6H2O(粉红色) CoCl2·2H2O(紫红色) CoCl2·H2O(蓝紫色) CoCl2(蓝色)
NiSO4·6H2O绿色晶体
络合物/络合离子
[Fe(H2O)6]2+淡绿色
K4[Fe(CN)6]·3H2O黄色晶体
铂系元素
单质
Os蓝灰色金属
其余铂系金属银白色
络合物/络合离子
PtCl4红棕色
合成方法:H2PtCl6 PtCl4
PtCl3暗绿色
合成方法:PtCl4 PtCl3 + Cl2
[PtCl6]2-淡黄橙色(溶液中)
H2[PtCl6]·6H2O
橙红色晶体
Na2[PtCl6]橙红色晶体
M[PtCl6]难溶的黄色晶体
[Ni(Ⅱ)(NH3)6]Br2紫色
Na2[Ni(CN)4]·3H2O黄色
K2[Ni(CN)4]·H2O橙色
二丁二酮肟合镍
鲜红色沉淀
(图略) 是分析化学中检验Ni2+ 的特征反应
Ni(CO)4无色液体
Ni + CO 合成
Fe(CO)5淡黄色液体
Fe + CO 合成
Co2(CO)8橙黄色晶体
(图略)制备方法:CoCO3 + H2 +CO → Co2(CO)8 + CO2 + H2O
俗称黄血盐,脱水后为白色。可用于检验Fe3+,生成普鲁士蓝。
KFe[
Fe(Ⅱ)(C5H5)2橙黄色晶体
二茂铁,可作燃油添加剂,高温润滑剂,导弹、卫星涂料
K3[Fe(CN)6]深红色
无机化合物颜色大全(按颜色分类)

无机化合物颜色大全1.红色Fe(SCN)]2+(血红色);Cu2O(砖红色);Fe2O3(红棕色);红磷(红棕色);液溴(深红棕色);Fe(OH)3(红褐色);I2的CCl4溶液(紫红色);MnO4-(紫红色);Cu(紫红色);在空气中久置的苯酚(粉红色).2.橙色:溴水;K2Cr2O7溶液.3.黄色:AgI(黄色);AgBr(浅黄色);K2CrO4(黄色);Na2O2(淡黄色);S(黄色);FeS2(黄色);久置浓HNO3(溶有NO2);工业浓盐酸(含Fe3+);Fe3+水溶液(黄色);久置的KI溶液(被氧化成I2)4.绿色:Cu2(OH)CO3;Fe2+的水溶液;FeSO4.7H2O;Cl2(黄绿色);F2(淡黄绿色);Cr2O35.蓝色:Cu(OH)2;CuSO4.5H2O;Cu2+的水溶液;I2与淀粉的混合物.6.紫色:KMnO4(紫黑色);I2(紫黑色);石蕊(pH=8—10);Fe3+与苯酚的混合物.7.黑色:FeO,Fe3O4,FeS,CuS,Cu2S,Ag2S,PbS,CuO,MnO2,C粉.8.白色:Fe(OH)2,AgOH,无水CuSO4,Na2O,Na2CO3,NaHCO3,AgCl,BaSO4,CaCO3,CaSO3,Mg(OH)2,Al(OH)3,三溴苯酚,MgO,MgCO3,绝大部分金属等.说明:①元素基本上按周期表的族序数排列;②物质基本上按单质、氢化物、氧化物及其水化物、盐、有机物的顺序排列;③许多物质晶状为无色,粉末状为白色,晶型不同可能有不同颜色;④硫化物和过渡元素化合物颜色较丰富。
一、单质绝大多数单质:银白色。
主要例外:镧系锕系及下表物质 Cu 紫红 O2无 Au 黄 S 黄 B 黄或黑 F2淡黄绿 C(石墨黑 Cl2黄绿 C(金刚石)无 Br2红棕 Si 灰黑 I2紫黑 H2无稀有气体无 P 白、黄、红棕。
二、氢化物 LiH等金属氢化物:白NH3等非金属氢化物:无三、氧化物大多数非金属氧化物:无主要例外: NO2棕红 N2O5和P2O5白 N2O3暗蓝 ClO 2 黄 大多数主族金属的氧化物:白 主要例外: Na 2O 2 浅黄 PbO 黄 K 2O 黄 Pb 3O 4 红 K 2O 2 橙 Rb 2O 亮黄 Rb 2O 2 棕 Cs 2O 橙红 Cs 2O 2 黄 大多数过渡元素氧化物有颜色 MnO 绿 CuO 黑 MnO 2黑 Ag 2O 棕黑 FeO 黑 ZnO 白 Fe 3O 4 黑 Hg 2O 黑 Fe 2O 3 红棕 HgO 红或黄 Cu 2O 红 V 2O 5 橙四、氧化物的水化物 大多数:白色或无色 其中酸:无色为主 碱:白色为主 主要例外: CsOH 亮黄 Fe(OH)3红褐 HNO 2 溶液亮蓝 Cu(OH)2 蓝 Hg(OH)2 桔红五、盐 大多数白色或无色 主要例外: K 2S 棕黄 CuFeS 2 黄 KHS 黄 ZnS 白 Al 2S 3 黄 Ag 2S 黑 MnS 浅红 CdS 黄 FeS 黑棕 SnS 棕 FeS 2 黄 Sb 2S 3 黑或橙红 CoS 黑 HgS 红 NiS 黑 PbS 黑 CuS 、Cu 2S 黑 Bi 2S 3 黑 FeCl 3·6H 2O 棕黄 Na 3P 红 FeSO 4·9H 2O 蓝绿 NaBiO 3 黄 Fe 2(SO 4)3·9H 2O 棕黄 MnCl 2 粉红 Fe 3C 灰 MnSO 4 淡红 FeCO 3 灰 Ag 2CO 3 黄 Fe (SCN )3 暗红 Ag 3PO 4 黄 CuCl 2 棕黄 AgF 黄 CuCl 2·7H 2O 蓝绿 AgCl 白 CuSO 4 白 AgBr 浅黄 CuSO 4·5H 2O 蓝 AgI 黄 Cu 2(OH )2CO 3 暗绿 盐溶液中离子特色: NO 2- 浅黄 Cu 2+或[Cu (H 2O )4]2+ 蓝 MnO 4-紫红 [CuCl 4]2- 黄 MnO 42- 绿 [Cu (NH 3)4]2+ 深蓝 Cr 2O72- 橙红 Fe 2+ 浅绿 CrO 42- 黄Fe 3+ 棕黄 非金属互化物 PCl 3 无 XeF 2、XeF 4、XeF6 无 PCl5 浅黄 氯水 黄绿 CCl 4 无 溴水 黄—橙 CS 2 无 碘水 黄褐 SiC 无或黑 溴的有机溶液 橙红—红棕 SiF 4 无 I 2的有机溶液 紫红六.其它 甲基橙 橙 C X H Y (烃)、C X H Y O Z 无(有些固体白色) 石蕊试液 紫 大多数卤代烃 无(有些固体白色) 石蕊试纸 蓝或红 果糖 无 石蕊遇酸 变红 葡萄糖 白 石蕊遇碱 变蓝 蔗糖 无 酚酞 无 麦芽糖 白 酚酞遇碱 红 淀粉 白 蛋白质遇浓HNO 3变黄 纤维素 白 I 2遇淀粉 变蓝 TNT 淡黄 Fe 3+遇酚酞溶液 紫 焰色反应 Li 紫红 Ca 砖红 Na 黄 Sr 洋红 K 浅紫(通过蓝色钴玻璃) Ba 黄绿 Rb 紫 Cu 绿 稀有气体放电颜色 He 粉红 Ne 鲜红 Ar 紫。
配位化合物的颜色和配位理论

配位化合物的颜色和配位理论配位化合物是由一个中心金属离子和周围的配体离子或原子团组成的化合物。
这类化合物通常具有丰富多彩的颜色,这种颜色的差异主要由于配位体和中心金属离子之间的电子转移引起。
在这篇文章中,我们将探讨配位化合物的颜色以及配位理论的相关原理。
一、配位化合物的颜色配位化合物的颜色与其中的配体和中心金属离子的电子结构息息相关。
主要有以下几种情况:1. 配体的颜色:首先,配体本身的颜色会直接影响到整个化合物的颜色。
比如,水合铜离子的配位化合物通常呈现出蓝色,这是因为水配体吸收红光,而对蓝光具有较好的透明度。
2. 中心金属离子的d电子结构:在配位化合物中,中心金属离子的d电子能级分裂是产生颜色的重要原因。
根据分裂的大小,d电子能级吸收光的波长也会发生改变。
例如,在八配位的铜离子中,d电子能级的分裂较大,它们能够吸收红光,因此形成了蓝色的化合物。
二、配位理论配位理论是解释配位化合物形成和性质的基本原理。
其中最重要的理论是分子轨道理论和晶场理论。
1. 分子轨道理论:分子轨道理论认为,在形成配位化合物时,配体与中心金属离子之间的相互作用会形成分子轨道。
这些分子轨道由配体和中心金属离子的原子轨道合成而来。
电子在这些分子轨道中运动,从而导致电子结构的改变,进而影响化合物的颜色。
例如,在八配位的铜离子均匀分布在d轨道中,形成了大的d电子能级分裂,这就是为什么铜配合物通常呈现出蓝色的原因。
2. 晶场理论:晶场理论是另一种解释配位化合物颜色和结构的重要理论。
该理论认为,配位离子周围的配体形成了一个电场,根据电场的性质,分为强场和弱场。
在强场的作用下,d电子能级发生分裂,能量差较大,会吸收较短波长的光,呈现出相应的颜色。
而在弱场的作用下,能量差较小,吸收较长波长的光,形成不同的颜色。
这就是为什么不同的配体会导致不同颜色的化合物。
综上所述,配位化合物的颜色与其中的配体和中心金属离子的电子结构密切相关。
通过配位理论的解释,我们可以更好地理解和解释这些化合物的颜色变化。
化学颜色描述

化学颜色描述一、红色红色是一种非常鲜艳和明亮的颜色,常常与热情、活力和力量相关联。
在化学中,红色通常与具有氧化性质的物质相关。
例如,氧化铁(Fe2O3)是一种红色的化合物,常见于锈迹、红土和红矿石中。
红色还可以由一些含有色素的化合物产生,例如红色的罗丹明B (Rhodamine B)和偶氮染料。
二、橙色橙色是介于红色和黄色之间的一种颜色,常常与温暖、快乐和创造力相关联。
在化学中,橙色通常与富含有机化合物的物质相关。
例如,某些具有橙色色素的植物和水果,如胡萝卜和橙子,其橙色来自于富含的β-胡萝卜素。
此外,橙色还可以由一些含有橙色染料的化合物产生,如橙色的苏丹III(Sudan III)染料。
三、黄色黄色是一种明亮而愉悦的颜色,常常与快乐、希望和活力相关联。
在化学中,黄色通常与含有硫的化合物相关。
例如,硫化氢(H2S)是一种具有强烈硫黄气味的气体,常常被描述为“蛋臭味”,其颜色也呈现出淡黄色。
此外,某些含有黄色色素的化合物也可以产生黄色,如黄色的农药硫磺磷(Sulprofos)。
四、绿色绿色是一种令人感到平静和放松的颜色,常常与生命、自然和健康相关联。
在化学中,绿色通常与富含铜离子的化合物相关。
例如,铜(II)硫酸盐(CuSO4)是一种常见的绿色固体,常用于实验室中的化学试剂。
此外,叶绿素是一种天然的绿色色素,它在光合作用中起到捕捉太阳能并产生养分的关键作用。
五、蓝色蓝色是一种冷静和沉稳的颜色,常常与信任、智慧和深度相关联。
在化学中,蓝色通常与含有过渡金属离子的化合物相关。
例如,铜(II)硫氰化物(Cu(SCN)2)是一种具有蓝色晶体结构的化合物,常用于制备蓝色染料和颜料。
此外,蓝色还可以由一些含有蓝色色素的化合物产生,如蓝色的甲基蓝(Methylene Blue)和亚甲基蓝(Methylthioninium chloride)。
六、紫色紫色是一种神秘和优雅的颜色,常常与创造力、幻想和奢华相关联。
在化学中,紫色通常与含有芳香环的化合物相关。
配位化合物的颜色与配位数

配位化合物的颜色与配位数配位化合物是指由一个或多个金属离子与一或多个配体形成的化合物。
这些化合物在溶液中或固态中表现出丰富多彩的颜色,这与金属离子的配位数密切相关。
在本文中,我们将探讨配位化合物的颜色与配位数之间的关系。
1. 单配位单配位化合物指的是一个金属离子与一个配体形成的化合物。
这种化合物通常呈现为无色或淡黄色。
这是因为光线通过这种化合物时,金属离子与配体之间发生的电子转移和能级差异不大,无法吸收特定波长的光线。
因此,这些化合物对可见光的吸收很弱,呈现出无色或淡黄色。
2. 双配位双配位化合物由一个金属离子与两个配体形成。
这种化合物通常呈现出浅色,如淡黄色、浅绿色、浅蓝色等。
这是因为金属离子与配体之间的电子转移和能级差异增加,可以吸收较高能量的光,使得化合物呈现出浅色。
3. 四配位四配位化合物由一个金属离子与四个配体形成。
这类化合物通常呈现出浓烈的颜色,如深黄色、红色、紫色等。
这是因为四配位化合物中金属离子与配体之间的电子转移和能级差异更大,可以吸收更多能量的光线。
这导致化合物吸收可见光中的某些波长,呈现出鲜明的颜色。
4. 六配位六配位化合物由一个金属离子与六个配体形成。
这种类型的化合物通常呈现出浓烈的颜色,如鲜红色、深蓝色或黑色。
六配位化合物中金属离子与配体之间的电子转移和能级差异最大,可以吸收大量能量的光线,吸收特定波长的光线形成饱和颜色。
需要注意的是,以上颜色与配位数的关系并不是绝对的。
其他因素,如配体的选择、配体的立体结构以及反应条件等也会影响配位化合物的颜色。
此外,化合物的溶剂、光源及浓度等因素也会对颜色产生一定的影响。
总结起来,配位化合物的颜色与配位数之间存在着紧密的关系。
随着配位数的增加,化合物呈现的颜色将逐渐加深。
这种关系为我们理解配位化合物的光学性质提供了重要依据,也为合理设计和调控具有特定颜色的化合物提供了指导。
化学颜色大全对照表

化学颜色大全对照表在化学中,颜色常常被用来表示不同化合物或物质的特征。
通过观察物质的颜色,我们可以了解其成分、结构以及其他的性质。
以下是一份化学颜色大全对照表,希望能对您有所帮助。
1. 无色/透明:物质呈现无色或透明状态,不吸收可见光。
2. 白色:物质反射所有波长的可见光,使其呈现白色。
3. 黑色:物质吸收所有波长的可见光,使其呈现黑色。
4. 红色:物质吸收短波长的蓝绿光,反射长波长的红光。
5. 橙色:物质吸收短波长的蓝光和长波长的红光,反射中等波长的橙光。
6. 黄色:物质吸收短波长的蓝紫光和长波长的红光,反射中等波长的黄光。
7. 绿色:物质吸收短波长的红光和长波长的紫光,反射绿光。
8. 蓝色:物质吸收短波长的红光和绿光,反射蓝光。
9. 靛蓝色:物质吸收短波长的黄光和绿光,反射靛蓝光。
10. 紫色:物质吸收短波长的黄绿光和橙光,反射紫光。
11. 粉红色:物质吸收短波长的绿光和橙光,反射粉红光。
12. 棕色:物质吸收短波长和中波长的光,反射较长波长的棕色光。
13. 灰色:物质反射所有波长的可见光,但颜色较暗淡,呈现灰色。
14. 金色:物质反射金黄色光,呈现类似金属的光泽。
15. 银色:物质反射银白色光,呈现类似银质的光泽。
16. 纯色:物质呈现单一的颜色,没有其他颜色的杂质。
17. 彩色:物质不仅具有一种颜色,还包含其他颜色的特性。
18. 变色:物质在不同的条件下可呈现不同的颜色,具有颜色可变性。
19. 深色:物质具有较深的颜色,反射较少的光。
20. 浅色:物质具有较浅的颜色,反射较多的光。
请注意,该颜色大全对照表仅供参考,具体颜色的产生与物质的成分、结构以及光的吸收、反射有关。
在化学研究、实验或工业应用中,我们常常通过光谱分析等手段来准确测定物质的颜色。
希望这份化学颜色大全对照表能够对您有所帮助,如果您有任何需要补充或改进的地方,请随时提出。
感谢您的阅读!。
常见化合物的物理性质与化学性质

常见化合物的物理性质与化学性质化合物是由不同元素以一定比例结合而成的物质。
它们具有一系列独特的物理性质和化学性质,这些性质不仅有利于我们对化合物的分类和识别,也有助于我们了解它们的性质和用途。
本文将介绍一些常见化合物的物理性质和化学性质以及相关的实验方法。
一、常见化合物的物理性质1. 熔点和沸点:化合物的熔点是指在大气压下从固态转变为液态的温度,沸点则是在大气压下从液态转变为气态的温度。
不同的化合物由于其分子结构和相互作用力的不同,具有不同的熔点和沸点。
通过测定熔点和沸点可以对化合物进行初步的鉴别和纯度检验。
2. 密度:化合物的密度是指单位体积内所含质量的大小。
密度可以用来区分不同的物质,因为不同化合物的分子量和分子之间的相互作用力不同,从而影响了其密度。
常见的实验方法包括测量物质的质量和容积,然后计算密度。
3. 折射率:化合物的折射率是指光在其内部传播时的弯曲程度。
不同的化合物由于其分子结构的不同,对光的折射率也不同。
使用折射计测量样品的折射率可以用来确定其物质的成分和浓度。
4. 颜色:化合物的颜色是由其分子内部和外部电子的结构所确定的。
不同的化合物吸收和反射的光的波长不同,从而呈现出不同的颜色。
通过观察化合物的颜色可以初步了解其结构和性质。
二、常见化合物的化学性质1. 酸碱性:化合物的酸碱性是指其在水溶液中所呈现出的酸性或碱性的性质。
酸性化合物会产生氢离子,而碱性化合物会产生氢氧根离子。
酸碱性的测定可以通过PH试纸或PH计来实现,其中酸性溶液的PH值低于7,碱性溶液的PH值高于7。
2. 氧化还原性:化合物的氧化还原性是指其在化学反应中电子的转移能力。
氧化剂具有接受电子的能力,而还原剂具有释放电子的能力。
通过氧化还原反应可以完成电子的转移和化学物质的转化。
3. 水解性:一些化合物在水中能够与水发生反应,产生可溶性的产物。
这种化合物被称为具有水解性。
水解性的实验方法常常包括观察化合物的溶解度和产生的各种产物。
常见化合物颜色

CO(与血红蛋白结合),Cl2,Br2(气),F2(气),HF,氢氟酸等。
(2)毒性物质
NO(与血红蛋白结合),NO2,CH3OH,H2S。
苯酚、甲醛、二氧化硫、重铬酸盐、汞盐、可溶性钡盐、可溶性铅盐、可溶性铜盐等。
1常见物质的颜色:多数气体为无色,多数固体化合物为白色,多数溶液为无色。
2一些特殊物质的颜色:黑色:MnO2、CuO、Fe3O4、C、FeS(硫化亚铁)
蓝色:CuSO4?5H2O、Cu(OH)2、CuCO3、含Cu2+ 溶液、
液态固态O2(淡蓝色)
红色:Cu(亮红色)、Fe2O3(红棕色)、红磷(暗红色)
运用上述规律便于记忆溶液或结晶水合物的颜色。
(3)主族金属单质颜色的特殊性
ⅠA,ⅡA,ⅣA,ⅤA的金属大多数是银白色。
铯:带微黄色 钡:带微黄色
铅:带蓝白色 铋:带微红色
(4)其他金属单质的颜色
铜呈紫红色(或红),金为黄色,其他金属多为银白色,少数为灰白色(如锗)。
有臭鸡蛋气味:H2S
3常见一些变化的判断:
① 白色沉淀且不溶于稀硝酸或酸的物质有:BaSO4、AgCl(就这两种物质)
② 蓝色沉淀:Cu(OH)2、CuCO3
③ 红褐色沉淀:Fe(OH)3
Fe(OH)2为白色絮状沉淀,但在空气中很快变成灰绿色沉淀,再变成Fe(OH)3红褐色沉淀
③ 难溶于水的
如:液态烃、醚和卤代烃。
(3)固体的水溶性(无机物略)
有机物中羟基和羧基具有亲水性,烃基具有憎水性,烃基越大,则水溶性越差,反而易I溶于有机溶剂中。如:甲酸、乙酸与水互溶,但硬脂酸、油酸分子中因—COOH比例过少反而不溶于水而溶于CCl4,汽油等有机溶剂。苯酚、三溴苯酚、苯甲酸均溶于苯。
常见无机化合物颜色
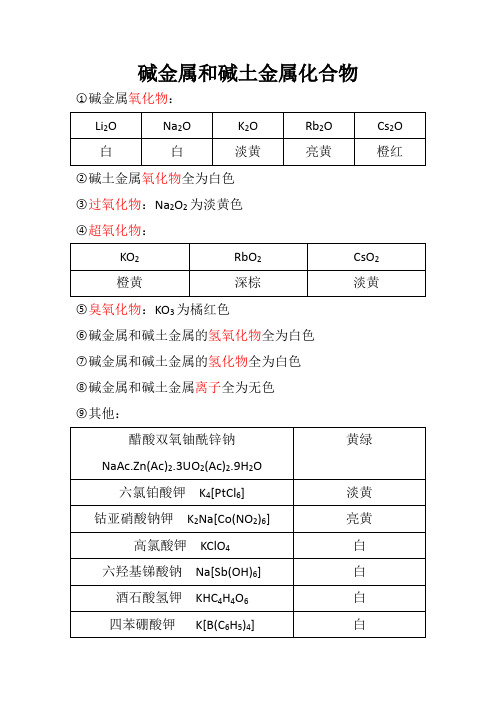
碱金属和碱土金属化合物○1碱金属氧化物:○2碱土金属氧化物全为白色○3过氧化物:Na2O2为淡黄色○4超氧化物:○5臭氧化物:KO3为橘红色○6碱金属和碱土金属的氢氧化物全为白色○7碱金属和碱土金属的氢化物全为白色○8碱金属和碱土金属离子全为无色○9其他:锗、锡、铅的化合物○1氧化物:○2氢氧化物:○3二卤化物:○4四卤化物:○5硫化物:○6铅的含氧酸盐:锑、铋的化合物○1氢化物都是无色的气体○2氧化物:○3三卤化物:○4五卤化物:○5硫化物:铜的化合物○1氧化物:○2氢氧化物:Cu(OH)2为蓝色○3硫化物:Cu2S为黑色○4卤化物:CuCl2在浓度很高时为黄绿色;浓时为绿色;稀时为蓝色;无水时为棕黄色○5配合物:○6其他:银和金的化合物○1银:○2金:锌族元素的化合物○1锌族M2+离子全为无色○2氧化物:○3硫化物:○4卤化物:○5配合物:钛的化合物钒的化合物○1氧化物:○2离子:铬的化合物○1Cr(Ⅲ):○2Cr(Ⅵ):锰的化合物○1Mn(Ⅱ):○2Mn(Ⅳ):○3Mn(Ⅵ)和Mn(Ⅶ):铁的化合物○1氧化物和氢氧化物:○2盐类:Fe(Ⅱ)一般为浅绿色;Fe(Ⅲ)一般为红棕色○3配合物:钴和镍的化合物○1氧化物:○2氢氧化物:○3盐类:○4配合物:铂系金属的化合物○1氧化物:○2卤化物:○3配合物:氯铂酸盐为黄色其他过渡金属化合物○1锆和铪的化合物:○2铌和钽的化合物:○3钼和钨的化合物:○4锝和铼的化合物:非金属元素的化合物。
常见离子和化合物的颜色

Mn2+浅玫瑰色,稀溶液无色;Fe(H2O)63+淡紫色,但平时所见Fe3+盐溶液黄色或红棕色;Fe2+浅绿色,稀溶液无色;Cr3+绿色或紫色;Co2+玫瑰色;Ni2+绿色;Cu2+浅蓝色。
3.以下阴离子均为无色
SO42-,PO43-,F-,SCN-,C2O42-,MoO42-,SO32-,BO2-,CI-,NO3-,S2-,WO42-,S2O32-,B4O72-,Br-,NO2-,CIO3-,VO3-,CO3-,SiO32-,I-,Ac-,BrO3-。
常见离子和化合物的颜色
一.常见离子的颜色
1.以下阳离子均无色
Ag+,Cd2+,K+,Ca2+,As3+(在溶液中主要以AsO33-存在),Pb2+,Zn2+,Na+,Sr2+,As5+(在溶液中几乎全部以AsO43-,存在),Hg22+,Bi3+,Ba2+,Sb3+或Sb5+(主要以SbCI63-或SbCI6-存在),Hg2+,Mg2+,AI3+,Sn2+,Sn4+。
4.以下阴离子均为有色
Cr2O72-橙色;CrO42-黄色;MnO4-紫色;Fe(CN)64-黄绿色;Байду номын сангаасe(CN)63-黄棕色。
二有特征颜色的常见无机化合物
黑色
CuO、NiO、FeO、Fe3O4、MnO2、FeS、CuS、Ag2S,NiS、CoS,PbS
蓝色
CuSO4·5H2O、Cu(NO3)2·6H2O、许多水合铜盐、无水CoCI2
绿色
各种化合物的颜色

卤族(英VIIA):固体:I2 紫黑;ICl 暗红;IBr 暗灰;IF3 黄色;ICl3 橙;I2O5 白;I2O4黄(离子晶体);I4O9 黄(离子晶体).液体:Br2 红棕;BrF3 浅黄绿;IBr3 棕;Cl2O6暗红;Cl2O7 无色油状;HClO4 无色粘稠状;(SCN)2 黄色油状.气体:F2 浅黄;(CN)2无色;Cl2 黄绿;I2(g) 紫;BrF 红棕;BrCl 红;Cl2O 黄红;ClO2 黄色;Br2O 深棕;(SCN)n 砖红色固体.氧族(英VIA):固体:S 淡黄;Se 灰,褐;Te 无色金属光泽;Na2S,(NH4)2S,K2S,BaS 白,可溶;ZnS 白↓;MnS 肉红↓;FeS 黑↓;PbS 黑↓;CdS 黄↓;Ag2S 黑↓;CuS 黑↓;Na2S2O3 白;Na2S2O4 白;SeO2 白,易挥发;SeBr2 红;SeBr4 黄;TeO2 白(加热变黄);H2TeO3 白;TeBr2 棕;TeBr4 橙;TeI4 灰黑;PoO2 低温黄(面心立方),高温红(四方);SO3 无色;SeO3 无色易潮解;TeO3 橙色;H6TeO6 无色.液体:H2O 无色;纯H2O2 淡蓝色粘稠;CrO(O2)2(aq) 蓝;纯H2SO4 无色油状;SO32-(aq) 无色;SO42-(aq) 无色;SeO2(l) 橙;TeO2(l) 深红.气体:O2 无色;O3 低浓度无色,高浓度淡蓝(鱼腥味);S2(g) 黄,上浅下深;H2S 无色;SO2 无色;H2Se 无色;H2Te 无色.卤化硫(未注明者均为无色):液体:SF6,S2F10,SCl4 淡黄;SCl2 红;S2Cl2 无色;S2Br2 红.气体:SF4 ;SF2 ;S2F2 .液体:SOCl2 白色透明;SO2Cl2 无色发烟. 氮族(英V A):固体:铵盐无色晶体;氮化金属白;N2O3 蓝色(低温);N2O5 白;P 白,红,黑;P2O3 白;P2O5 白;PBr3 黄;PI3 红;PCl5 无色;P4Sx 黄;P2S3 灰黄;P2S5 淡黄;H4P2O7 无色玻璃状;H3PO2 白;As 灰;As2O3 白;As2O5 白;As2S5 淡黄;Sb 银白;Sb(OH)3 白↓;Sb2O3 白(锑白,颜料);Sb2O5 淡黄;SbX3(X≠I) 白;SbI3 红;Sb2S3 橘红↓;Sb2S5 橙黄;Bi 银白略显红;Bi2O3 淡黄;Bi2O5 红棕;BiF3 灰白;BiCl3 白;BiBr3 黄;BiI3 黑↓;Bi2S3 棕黑.液体:N2H4 无色;HN3 无色;NH2OH 无色;发烟硝酸红棕;NO3-(l)无色;王水浅黄,氯气味;硝基苯黄色油状;PX3 无色;纯H3PO4 无色粘稠状;AsX3(X≠I) 无色;.气体:N2 无色;NH3 无色;N2O 无色甜味;NO 无色;NO2 红棕;PH3 无色;P2H6 无色;AsH3 无色;SbH3 无色;BiH3 无色.卤化氮(未注明者均为无色):固体:NBr3•(NH3)6 紫,爆炸性;NI3•(NH3)6 黑,爆炸性;液体:NCl3;无色气体:NF3;无色碳族(英IV A):Solid:C(金刚石) 无色透明;C(石墨) 黑色金属光泽;Si 灰黑色金属光泽;Ge 灰白;Sn 银白;Pb 暗灰;SiO2 无色透明;H2SiO3 无色透明胶状↓;Na2SiF6 白晶;GeO 黑;GeO2 白;SnO 黑;SnO2 白;Sn(OH)2 白↓;PbO黄或黄红;Pb2O3 橙;Pb3O4 红;PbO2 棕;CBr4 淡黄;CI4 淡红;GeI2 橙;GeBr2 黄;GeF4 白;GeBr4 灰白;GeI4 黄;SnF2 白;SnCl2 白;SnBr2 淡黄;SnI2 橙;SnF4 白;SnBr4 无色;SnI4 红;PbF2 无色↓;PbCl2 白↓;PbF4 无色;GeS 红;GeS2 白;PbS 黑↓;PbS2 红褐;Pb(NO3)2 无色;Pb(Ac)2•3H2O 无色晶体;PbSO4 白↓;PbCO3 白↓;Liquid:CCl4 无色;CS2 无色;GeCl4 无色;SnCl4 无色;PbCl4 无色.Gas:CO CO2 CH4 CF4 SiF4 SiH4 均为无色. 硼族(英IIIA):Solid:B(无定型) 棕色粉末;B(晶体) 黑灰;Al 银白;Ga 银白(易液化);In 银灰;Tl 银灰;B2O3 玻璃状;H3BO3 无色片状;BN 白;NaBO2•4H2O 无色晶体;无水NaBO2 黄晶;Al2O3 白晶;AlF3 无色;AlCl3 白;AlBr3 白;AlI3 棕;Al(OH)3 白↓;Ga2O3 白↓;Ga(OH)3 白↓;GaBr3 白;GaI3 黄;In2O3 黄;InBr3 白;InI3 黄;TlOH 黄;Tl2O 黑;Tl2O3 棕黑;TlCl 白↓;TlBr 浅黄↓;TlI 黄↓(与银相似);TlBr3 黄;TlI3 黑.Liquid:BCl3 无色发烟.Gas:硼烷无色;BF3 无色(有窒息气味).碱土金属(英IIA):单质:银白氧化物:均为白色固体.氢氧化物:白色固体Be(OH)2↓,Mg(OH)2↓. 盐:多为无色或白色晶体;BeCl2 浅黄;BaCrO4 黄↓;CaF2 白↓.碱金属(英IA):单质:银白焰色:Li 红;Na 黄;K 紫;Rb 紫红;Cs 紫红. 氧化物、过氧化物、超氧化物、臭氧化物:Li2O 白;Na2O 白;K2O 淡黄;Rb2O 亮黄;Cs2O 橙红;Na2O2 淡黄;KO2橙黄;RbO2深棕;CsO2 深黄;KO3 橘红.氢氧化物:白色,LiOH白↓.盐:多为无色或白色晶体且易溶于水.不溶盐↓(未注明者皆为白色晶体):LiF Li2CO3 Li3PO4LiKFeIO6 Na[Sb(OH)6]NaZn(UO2)3(Ac)9•6H2O 黄绿;M3[Co(NO2)6] 亮黄;MBPh4 MClO4 M2PtCl6 淡黄;(M=K,Rb,Cs)CsAuCl4.铜副族(英IB):单质:Cu 紫红或暗红;Ag 银白;Au 金黄.铜化合物:焰色绿;CuF 红;CuCl 白↓;CuBr黄↓;CuI 棕黄↓;CuCN 白↓;Cu2O 暗红;Cu2S 黑;CuF2 白;CuCl2 棕黄(溶液黄绿);CuBr2 棕;Cu(CN)2 棕黄;CuO 黑↓;CuS黑↓;CuSO4 无色;CuSO4•5H2O 蓝;[Cu(H2O)4]2+ 蓝;[Cu(OH)4]2- 蓝紫;深蓝;炔铜红↓.银化合物:AgOH 白(常温分解);Ag2O 黑;新制AgOH 棕黄(混有Ag2O);蛋白银(AgNO3滴手上) 黑↓;AgF 白;AgCl 白↓;AgBr 淡黄↓;AgI 黄↓(胶体);Ag2S 黑↓;Ag4[Fe(CN)6] 白↓; Ag3[Fe(CN)6] 白↓; Ag+ ,[Ag(NH3)2]+ ,无色[Ag(S2O3)2]3- ,[Ag(CN)2]- 无色.金化合物:HAuCl4•3H2O 亮黄晶体;KAuCl4•1.5H2O 无色片状晶体; Au2O3 黑;H[Au(NO3)4]•3H2O 黄色晶体; AuBr 灰黄↓; AuI 柠檬黄↓.锌副族(I 英IB):单质:均为银白,Hg 在水溶液中的沉淀为黑色.ZnI2 无色; ZnS 白↓;ZnCl2 白色晶体(溶解度极大,水溶液酸性);K3Zn3[Fe(CN)6] 白; Zn3[Fe(CN)6]2 黄褐.镉化合物:CdO 棕灰↓;汞化合物:HgO 红(大晶粒)或黄(小晶粒)↓;HgI2 红或黄(微溶);(奈斯勒试剂产物)Hg2(NO3)2 无色晶体.ZnS 荧光粉:Ag 蓝;Cu 黄绿;Mn 橙.钛副族(英IVB):钛化合物:Ti3+ 紫红;[TiO(H2O2)2]2+ 橘黄;(NH4)2TiCl6 黄色晶体; [Ti(H2O)6]Cl3 紫色晶体;[Ti(H2O)5Cl]Cl2•H2O 绿色晶体; TiCl4 无色发烟液体.锆、铪:MO2,MCl4 白.钒副族(英VB):钒化合物:V2+ 紫;V3+ 绿; VO2+ 蓝; V(OH)4- 黄; VO43- 黄; VO 黑;V2O3 灰黑; V2S3 棕黑; VO2 蓝色固体; VF4 绿色固体; VCl4 暗棕色液体; VBr4 洋红色液体; V2O5 黄或砖红; 水合V2O5 棕红;饱和V2O5溶液(微溶) 淡黄; [VO2(O2)2]3- 黄; [V(O2)3]3- 红棕.铬副族(英VIB):[CrO(O2)2]OEt2 蓝; CrO2Cl2 深红色液体; Na2Cr2O7,K2CrO7 橙红;Ag2CrO4 砖红↓; BaCrO4 黄↓; PbCrO4 黄↓.紫红Cr2(SO4)3•18H2O ; 绿色Cr2(SO4)3•6H2O ; 桃红Cr2(SO4)3;暗绿[Cr(H2O)4Cl2]Cl ; 紫色[Cr(H2O)6]Cl3; 淡绿[Cr(H2O)5Cl]Cl2; [Cr(H2O)6]3+ 紫;[Cr(H2O)4(NH3)2]3+ 紫红; [Cr(H2O)3(NH3)3]3+ 浅红; [Cr(H2O)2(NH3)4]3+ 橙红; [Cr(NH3)5H2O]3+ 橙黄; [Cr(NH3)6]3+ 黄.钼、钨:MoO3 白;棕色MoCl3; 绿色MoCl5; MoS3 棕色↓;•6H2O 黄色晶状↓;H2WO4•xH2O 白色胶体.锰副族(英VIIB):无水锰盐(MnSO4) 白色晶体;六水合锰盐(MnX2•6H2O, X=卤素,NO3,ClO4) 粉红;MnCO3 白↓; Mn3(PO4)2 白↓; KMnO4 紫红;铁系(第四周期VIII 族):黄;FeO 黑; Fe2O3 暗红; Fe(OH)2 白↓; Fe(OH)3 棕红↓; FeCl3 棕红晶体; 无水FeSO4 白; FeSO4•7H2O 绿;K4[Fe(CN)6](黄血盐) 黄色晶体; K3[Fe(CN)6](赤血盐) 红色晶体; Fe4[Fe(CN)6] 普鲁士蓝↓;M2Fe6(SO4)4(OH)12(黄铁矾,M=NH4,Na,K) 浅黄色晶体;CoO 灰绿; Co3O4 黑; Co(OH)3 棕↓; Co(OH)2 粉红↓; Co(CN)2 红;K4[Co(CN)6] 紫色晶体; Co2(CO)8 黄色晶体; [Co(SCN)6]4- 紫;氯化钴脱水变色:粉红CoCl2•6H2O(325K) ;紫红CoCl2•2H2O(3l3K) ; 蓝紫CoCl2•H2O(393K) ; 蓝CoCl2.[Ni(NH3)6]2+ 紫; Ni(OH)2 绿↓; Ni(OH)3 黑↓; 无水Ni(II)盐 黄; Na2[Ni(CN)4] 黄;K2[Ni(CN)4] 橙;Ni(CO)4 无色液体.铂系元素(第五、六周期VIII族):Os 蓝灰色易挥发固体;Pd↓(aq) 黑;Na2PtCl6 橙黄色晶体;M2PtCl6(M=K,Rb,Cs,NH4) 黄色↓.。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1常见物质的颜色:多数气体为无色,多数固体化合物为白色,多数溶液为无色。
2一些特殊物质的颜色:黑色:MnO2、CuO、Fe3O4、C、FeS(硫化亚铁)蓝色:CuSO4•5H2O、Cu(OH)2、CuCO3、含Cu2+ 溶液、液态固态O2(淡蓝色)红色:Cu(亮红色)、Fe2O3(红棕色)、红磷(暗红色)黄色:硫磺(单质S)、含Fe3+ 的溶液(棕黄色)绿色:FeSO4•7H2O、含Fe2+ 的溶液(浅绿色)、碱式碳酸铜[Cu2(OH)2CO3]无色气体:N2、CO2、CO、O2、H2、CH4有色气体:Cl2(黄绿色)、NO2(红棕色)有刺激性气味的气体:NH3(此气体可使湿润pH试纸变蓝色)、SO2有臭鸡蛋气味:H2S3常见一些变化的判断:①白色沉淀且不溶于稀硝酸或酸的物质有:BaSO4、AgCl(就这两种物质)②蓝色沉淀:Cu(OH)2、CuCO3③红褐色沉淀:Fe(OH)3Fe(OH)2为白色絮状沉淀,但在空气中很快变成灰绿色沉淀,再变成Fe(OH)3红褐色沉淀④沉淀能溶于酸并且有气体(CO2)放出的:不溶的碳酸盐⑤沉淀能溶于酸但没气体放出的:不溶的碱常见物质的物理性质归纳1.颜色的规律(1)常见物质颜色①以红色为基色的物质红色:难溶于水的Cu,Cu2O,Fe2O3,HgO等。
碱液中的酚酞、酸液中甲基橙、石蕊及pH试纸遇到较强酸时及品红溶液。
橙红色:浓溴水、甲基橙溶液、氧化汞等。
棕红色:Fe(OH)3固体、Fe(OH)3水溶胶体等。
②以黄色为基色的物质黄色:难溶于水的金、碘化银、磷酸银、硫磺、黄铁矿、黄铜矿(CuFeS2)等。
溶于水的FeCl3、甲基橙在碱液中、钠离子焰色及TNT等。
浅黄色:溴化银、碳酦银、硫沉淀、硫在CS2中的溶液,还有黄磷、Na2O2、氟气。
棕黄色:铜在氯气中燃烧生成CuCl2的烟。
③以棕或褐色为基色的物质碘水浅棕色、碘酒棕褐色、铁在氯气中燃烧生成FeCl3的烟等④以蓝色为基色的物质蓝色:新制Cu(OH)2固体、胆矾、硝酸铜、溶液中淀粉与碘变蓝、石蕊试液碱变蓝、pH试纸与弱碱变蓝等。
浅蓝色:臭氧、液氧等蓝色火焰:硫、硫化氢、一氧化碳的火焰。
甲烷、氢气火焰(蓝色易受干扰)。
⑤以绿色为色的物质浅绿色:Cu2(OH)2CO3,FeCl2,FeSO4•7H2O。
绿色:浓CuCl2溶液、pH试纸在约pH=8时的颜色。
深黑绿色:K2MnO4。
黄绿色:Cl2及其CCl4的萃取液。
⑥以紫色为基色的物质KMnO4为深紫色、其溶液为红紫色、碘在CCl4萃取液、碘蒸气、中性pH试纸的颜色、K+离子的焰色等。
⑦以黑色为基色的物质黑色:碳粉、活性碳、木碳、烟怠、氧化铜、四氧化三铁、硫化亚铜(Cu2S)、硫化铅、硫化汞、硫化银、硫化亚铁、氧化银(Ag2O)。
浅黑色:铁粉。
棕黑色:二氧化锰。
⑧白色物质★无色晶体的粉末或烟尘;★与水强烈反应的P2O5;★难溶于水和稀酸的:AgCl,BaSO3,PbSO4;★难溶于水的但易溶于稀酸:BaSO3,Ba3(PO4)2,BaCO3,CaCO3,Ca3(PO4)2,CaHPO4,Al(OH)3,Al2O3,ZnO,Zn(OH)2,ZnS,Fe(OH)2,Ag2SO3,CaSO3等;★微溶于水的:CaSO4,Ca(OH)2,PbCl2,MgCO3,Ag2SO4;★与水反应的氧化物:完全反应的:BaO,CaO,Na2O;不完全反应的:MgO。
⑨灰色物质石墨灰色鳞片状、砷、硒(有时灰红色)、锗等。
(2)离子在水溶液或水合晶体的颜色①水合离子带色的:Fe2+:浅绿色;Cu2+:蓝色;Fe3+:浅紫色呈黄色因有[FeCl4(H2O)2] 2-;MnO4-:紫色:血红色;:苯酚与FeCl3的反应开成的紫色。
②主族元素在水溶液中的离子(包括含氧酸根)无色。
运用上述规律便于记忆溶液或结晶水合物的颜色。
(3)主族金属单质颜色的特殊性ⅠA,ⅡA,ⅣA,ⅤA的金属大多数是银白色。
铯:带微黄色钡:带微黄色铅:带蓝白色铋:带微红色(4)其他金属单质的颜色铜呈紫红色(或红),金为黄色,其他金属多为银白色,少数为灰白色(如锗)。
(5)非金属单质的颜色卤素均有色;氧族除氧外,均有色;氮族除氮外,均有色;碳族除某些同素异形体(金钢石)外,均有色。
2.物质气味的规律(常见气体、挥发物气味)①没有气味的气体:H2,O2,N2,CO2,CO,稀有气体,甲烷,乙炔。
②有刺激性气味:HCl,HBr,HI,HF,SO2,NO2,NH3•HNO3(浓液)、乙醛(液)。
③具有强烈刺激性气味气体和挥发物:Cl2,Br2,甲醛,冰醋酸。
④稀有气味:C2H2。
⑤臭鸡蛋味:H2S。
⑥特殊气味:苯(液)、甲苯(液)、苯酚(液)、石油(液)、煤焦油(液)、白磷。
⑦特殊气味:乙醇(液)、低级酯。
⑧芳香(果香)气味:低级酯(液)。
⑨特殊难闻气味:不纯的C2H2(混有H2S,PH3等)。
3.熔点、沸点的规律晶体纯物质有固定熔点;不纯物质凝固点与成分有关(凝固点不固定)。
非晶体物质,如玻璃、水泥、石蜡、塑料等,受热变软,渐变流动性(软化过程)直至液体,没有熔点。
沸点指液体饱和蒸气压与外界压强相同时的温度,外压力为标准压(1.01×105Pa)时,称正常沸点。
外界压强越低,沸点也越低,因此减压可降低沸点。
沸点时呈气、液平衡状态。
(1)由周期表看主族单质的熔、沸点同一主族单质的熔点基本上是越向下金属熔点渐低;而非金属单质熔点、沸点渐高。
但碳族元素特殊,即C,Si,Ge,Sn越向下,熔点越低,与金属族相似。
还有ⅢA族的镓熔点比铟、铊低,ⅣA族的锡熔点比铅低。
(2)同周期中的几个区域的熔点规律①高熔点单质C,Si,B三角形小区域,因其为原子晶体,熔点高。
金刚石和石墨的熔点最高大于3550℃,金属元素的高熔点区在过渡元素的中部和中下部,其最高熔点为钨(3410℃)。
②低熔点单质非金属低熔点单质集中于周期表的右和右上方,另有IA的氢气。
其中稀有气体熔、沸点均为同周期的最低者,而氦是熔点(-272.2℃,26×105Pa)、沸点(268.9℃)最低。
金属的低熔点区有两处:IA、ⅡB族Zn,Cd,Hg及ⅢA族中Al,Ge,Th;ⅣA族的Sn,Pb;ⅤA族的Sb,Bi,呈三角形分布。
最低熔点是Hg(-38.87℃),近常温呈液态的镓(29.78℃)铯(28.4℃),体温即能使其熔化。
(3)从晶体类型看熔、沸点规律原子晶体的熔、沸点高于离子晶体,又高于分子晶体。
金属单质和合金属于金属晶体,其中熔、沸点高的比例数很大(但也有低的)。
在原子晶体中成键元素之间共价键越短的键能越大,则熔点越高。
判断时可由原子半径推导出键长、键能再比较。
如熔点:金刚石>碳化硅>晶体硅分子晶体由分子间作用力而定,其判断思路是:①结构性质相似的物质,相对分子质量大,范德华力大,则熔、沸点也相应高。
如烃的同系物、卤素单质、稀有气体等。
②相对分子质量相同,化学式也相同的物质(同分异构体),一般烃中支链越多,熔沸点越低。
烃的衍生物中醇的沸点高于醚;羧酸沸点高于酯;油脂中不饱和程度越大,则熔点越低。
如:油酸甘油酯常温时为液体,而硬脂酸甘油酯呈固态。
上述情况的特殊性最主要的是相对分子质量小而沸点高的三种气态氢化物:NH3,H2O,HF比同族绝大多数气态氢化物的沸点高得多(主要因为有氢键)。
(4)某些物质熔沸点高、低的规律性①同周期主族(短周期)金属熔点。
如Li<Be,Na<Mg<Al②碱土金属氧化物的熔点均在2000℃以上,比其他族氧化物显著高,所以氧化镁、氧化铝是常用的耐火材料。
③卤化钠(离子型卤化物)熔点随卤素的非金属性渐弱而降低。
如:NaF>NaCl>NaBr>NaI。
4.物质溶解性规律(1)气体的溶解性①常温极易溶解的NH3[1(水):700(气)] HCl(1:500)还有HF,HBr,HI,甲醛(40%水溶液—福尔马林)。
②常温溶于水的CO2(1:1) Cl2(1:2)H2S(1:2.6) SO2(1:40)③微溶于水的O2,O3,C2H2等④难溶于水的H2,N2,CH4,C2H2,NO,CO等。
(2)液体的溶解性①易溶于水或与水互溶的如:酒精、丙酮、醋酸、硝酸、硫酸。
②微溶于水的如:乙酸乙酯等用为香精的低级酯。
③难溶于水的如:液态烃、醚和卤代烃。
(3)固体的水溶性(无机物略)有机物中羟基和羧基具有亲水性,烃基具有憎水性,烃基越大,则水溶性越差,反而易I溶于有机溶剂中。
如:甲酸、乙酸与水互溶,但硬脂酸、油酸分子中因—COOH比例过少反而不溶于水而溶于CCl4,汽油等有机溶剂。
苯酚、三溴苯酚、苯甲酸均溶于苯。
(4)从碘、溴、氯的水溶液中萃取卤素的有机溶剂如:苯、汽油、乙醚、乙酸乙酯、CCl4、CS2等。
(5)白磷、硫易溶于CS2(6)常见水溶性很大的无机物如:KOH,NaOH,AgNO3溶解度在常温超过100g(AgNO3超过200g)。
KNO3在20℃溶解度为31.6g,在100℃溶解度为246g。
溶解度随温度变化甚少的物质常见的只有NaCl。
(7)难溶于水和一般溶剂的物质①原子晶体(与溶剂不相似)。
如:C,Si,SiO2,SiC等。
其中,少量碳溶于熔化的铁。
②有机高分子:纤维素仅溶于冷浓H2SO4、铜氨溶液和CS2跟NaOH作用后的溶液中,已热固化的酚醛树脂不溶于水或一般溶剂。
5.常见的有毒物质(1)剧毒物质白磷、偏磷酸、氰化氢(HCN)及氰化物(NaCN,KCN等)砒霜(As2O3)、硝基苯等。
CO(与血红蛋白结合),Cl2,Br2(气),F2(气),HF,氢氟酸等。
(2)毒性物质NO(与血红蛋白结合),NO2,CH3OH,H2S。
苯酚、甲醛、二氧化硫、重铬酸盐、汞盐、可溶性钡盐、可溶性铅盐、可溶性铜盐等。
这些物质的毒性,主要是使蛋白质变性,其中常见的无机盐如:HgCl2,BaCl2,Pb(CHCOO)2;铜盐也使蛋白质凝固变性,但毒性较小,此外铍化合物也有相当的毒性。
钦酒过多也有一定毒性。
汞蒸气毒性严重。
有些塑料如聚氯乙烯制品(含增塑剂)不宜盛放食品等。
(一)固体的颜色1、红色固体:铜,氧化铁2、绿色固体:碱式碳酸铜3、蓝色固体:氢氧化铜,硫酸铜晶体4、紫黑色固体:高锰酸钾5、淡黄色固体:硫磺6、无色固体:冰,干冰,金刚石7、银白色固体:银,铁,镁,铝,汞等金属8、黑色固体:铁粉,木炭,氧化铜,二氧化锰,四氧化三铁,(碳黑,活性炭)9、红褐色固体:氢氧化铁10、白色固体:氯化钠,碳酸钠,氢氧化钠,氢氧化钙,碳酸钙,氧化钙,硫酸铜,五氧化二磷,氧化镁·二)液体的颜色11、无色液体:水,双氧水12、蓝色溶液:硫酸铜溶液,氯化铜溶液,硝酸铜溶液13、浅绿色溶液:硫酸亚铁溶液,氯化亚铁溶液,硝酸亚铁溶液14、黄色溶液:硫酸铁溶液,氯化铁溶液,硝酸铁溶液15、紫红色溶液:高锰酸钾溶液16、紫色溶液:石蕊溶液(三)气体的颜色17、红棕色气体:二氧化氮18、黄绿色气体:氯气19、无色气体:氧气,氮气,氢气,二氧化碳,一氧化碳,二氧化硫,氯化氢气体等大多数气体。
