生活中的有机物-课件
高中化学专题4生活中常用的有机物一烃的含氧衍生物第2单元醛羧酸基础课时13羧酸的性质和应用课件苏教版

(2)向苯酚和醋酸中滴加少量紫色石蕊溶液,溶液都变为红色。
(× )
(3)1 mol C2H5OH 和 1 mol CH3COOH 在浓硫酸作用下加热可以
完全反应生成 1 mol CH3COOC2H5。
(× )
(4)乙酸分子中含有碳氧双键,一定条件下乙酸能与氢气发生加
成反应。
( ×)
(5)乙酸显酸性,电离出 H+,因此发生酯化反应时断裂 H—O 键。
能团为 —COOH 或
。
(2)通式:一元羧酸的通式为 R—COOH,饱和一元羧酸的通式: CnH2nO2 或 CnH2n+1COOH 。
2.羧酸的分类
(1)按与羧基连接的烃基的结构分类
低级脂肪酸,如乙酸:CH3COOH
羧酸脂肪酸高级脂肪酸软硬油脂脂酸酸酸:C::17CCH113573HHC33O15CCOOOHOOHH
(5)乙酸、草酸、硬脂酸和石炭酸均属于羧酸类有机物。 ( × )
二、羧酸的性质 1.乙酸的组成和结构
俗称 分子式 结构简式 官能团
醋酸 C2H4O2 CH3COOH
2.乙酸的化学性质
(1)弱酸性
乙酸是一种弱酸,酸性比碳酸 强 。能使紫色石蕊溶液变红,能
发生如下反应: CH3COOH+NaOH―→CH3COONa+H2O ; 2CH3COOH+CuO―→(CH3COO)2Cu+H2O ; 2CH3COOH+CaCO3―→(CH3COO)2Ca+H2O+CO2↑
亚油酸 :C17H31COOH
芳香 酸,如苯甲酸:C6H5COOH,俗名安息香酸
(2)按分子中羧基的数目分类
3.羧酸的系统命名法 (1)选主链:选择含有羧基的最长碳链作为主链,按主链碳原子 数称为某酸。 (2)编号位:在选取的主链中,从羧基碳原子开始给主链上的碳 原子编号。 (3)定名称:在“某酸”名称之前加上取代基的位次号和名称。
第十一章第3节 生活中两种常见的有机物(共71张PPT)

△ CuO+CH3CH2OH――→CH3CHO+H2O+Cu。 (2)乙醇与金属钠反应时,与水和钠反应的现象不同,钠沉 在乙醇底部。
[固本自测] 1.酒后驾车是引发交通事故的重要原因。交警对驾驶员进 行呼气酒精检测的原理是橙色的K2Cr2O7酸性水溶液遇乙醇迅速 生成蓝绿色的Cr3+。下列对乙醇的描述与此测定原理有关的是 ( ) ①乙醇沸点低 ②乙醇密度比水小 ③乙醇有还原性
反应 实质
水分子中氢原子被置 换,发生置换反应
乙醇分子中羟基上的氢 原子被置换,发生置换 反应 2CH3CH2OH+ 2Na―→2CH3CH2ONa + H2↑ 2CH3CH2OH~2Na~ H2↑
反应 方程式 定量计 算关系
2Na+2H2O===2NaOH + H2 ↑
2Na~2H2O~H2↑
(2)利用上述醇与钠的反应的定量计算关系,确定醇中羟基 的个数。 (3)证明乙醇分子中含有一个羟基的方法:1 mol乙醇与足量 金属钠反应产生0.5 mol氢气。
④乙醇是烃的含氧化合物 A.②④
答案:C
B.②③
C.①③
D.①④
解析:乙醇沸点低易挥发,挥发出的乙醇遇K2Cr2O7表现还 原性,将K2Cr2O7还原为Cr3+,发生颜色变化。
知识点二 1.结构
乙酸
分子式
C2H4O2
结构式
结构简式
CH3COOH
官能团
-COOH
2.物理性质 俗称 醋酸 ,具有 强烈刺激性 气味;温度低于 16.6℃ 凝结 成固态,易溶于水和乙醇。 3.化学性质 (1)酸性 在水中电离方程式为 CH3COOH 酸性比H2CO3
乙醇的结构简单,但化学性质相当复杂,这也给高 考命题提供了很大的空间。此知识点一般在选择题中出 现,有时也在Ⅱ卷中的推断题、实验题中有所涉及,难度 不大。
生活中的有机物

△
H C H +4Ag(NH3)2OH CO2↑+ 4Ag↓+ 8NH3 + 3H2O
三乙酸
醋的来历?
传说古代山西省有个酿酒高手叫杜康。他儿 子黑塔跟父亲也学会了酿酒技术。后来,从山西 迁到镇江。黑塔觉得酿酒后把酒糟扔掉可惜,把 酒糟浸泡在水缸里。到了第二十一日的酉时,一 开缸,一股浓郁的香气扑鼻而来。黑塔忍不住尝 了一口,酸酸的,味道很美。烧菜时放了一些, 味道特别鲜美,便贮藏着作为“调味酱”。故醋 在古代又叫“苦酒”
B.溴水
C.碳酸钠溶液
D.紫色石蕊试液
4.除去乙酸乙酯中含有的乙酸,最好的处理和操作是
(C )
A.蒸馏
B.水洗后分液
C.用过量饱和碳酸钠溶液洗涤后分液
D.用过量氢氧化钠溶液洗涤后分液
5. 关于乙酸的下列说法中不正确的是
( D ).
A.乙酸易溶于水和乙醇
B.无水乙酸又称冰醋酸,它是纯净物
C.乙酸是一种重要的有机酸,是有刺激 性气味的液体
2、氧化反应
(1)乙醛在点燃条件下可被空气中的氧气所氧化 2 CH3CHO + 5 O2 点燃 4CO2 + 4H2O
(2)乙醛的催化氧化
催化剂
2CH3CHO + O2 △ 2CH3COOH
(3)乙醛与弱氧化剂银氨溶液反应,显示还原性
△
CH3CHO + 2Ag(NH3)2OH
CH3COONH4 + 2Ag↓+ 3NH3+ H2O 注意事项
与 (2).该反应可用金属铜作催化剂,分步写出反应 思考 的方程式。
人教版高中化学必修二第三章第三节《生活中两种常见的有机物》课件(共33张PPT)

三、乙酸的化学性质
??做鱼时放些酒和 醋,鱼就能去除腥味, 香味四溢,那是为什 么呢?
CH3—C—OH 醋 O
C2H5—OH 酒
2、酯化反应:
酸跟醇作用,生成酯和水的反应
O
O
浓H2SO4
CH3—ห้องสมุดไป่ตู้—OH+H—O—C2H5
CH3—C—O—C2H5 + H2O
乙酸乙酯 油状物,有香味
注意:酯化反应属于取代反应
不料,二旬后黄昏时,他经过此缸时,忽然闻到一 股香甘酸醇的特殊气味扑鼻而来。他好奇地走进小缸, 伸手指沾指一尝,虽然不是一般的酒味,但给人另外一 种鲜美爽口的特殊感觉。心想,这东西喝是不成的,但 用来拌菜和煮汤如何,很值得一试。于是就唤来徒儿们 ,用它干拌了一盆黄瓜又煮了一盆鲫鱼汤来试试。弄好 后大家一尝,无不拍手,齐声叫好。
3、下列物质中,既能与NaOH反应,又能与NaHCO3 反应的是( B )
A. —OH
B. CH3COOH
C.CH3CHO
D.CH3CH2OH
讨论:喝醋能解酒吗?
有人说:人是物理和化学反应的总和.其实,人是一个整体.他的整个生理过 程是不能简单的用化学和物理来衡量.同样,对于醋能否解酒,也是不能单 纯的用乙酸和乙醇的化学反应来解释.毕竟,它也是人的一种生理过程.
药品:镁粉、NaOH溶液、CuSO4溶液、Na2CO3粉末、
Na2SO3粉末、乙酸溶液、酚酞、石蕊
讨论:
1、乙酸具有酸的哪些通性?(设计实验、 观察实验现象,做好记录。)
2、乙酸的酸性与碳酸和亚硫酸比较, 酸性谁强谁弱? 酸性:H2SO3 >CH3COOH>H2CO3
这能行 吗?
● 2CH3COOH + CaCO3=(CH3COO)2Ca + H2O + CO2↑
生活中常见的有机物(讲义)

生活中常见的有机物[课程目标]1.掌握醇、酸、酯的结构特点,正确区分辨认醇、酸、酯。
2.了解乙醇、乙酸、乙酸乙酯的性质以及在日常生活中的应用。
3.一般了解醛类物质的结构特点和性质。
4.能正确书写有机物燃烧反应的化学方程式,能根据化学方程式作一般计算。
[要点精析]一、醇、醛、酸、酯的结构和性质(表24-1)概念一般表示 官能团 典型代表 主要化学性质 醇 烃分子中饱和碳原子上的氢原子被羟基取代的化合物 R-OH—OHCH 3CH 2OH① 与金属钠反应 ② 氧化反应 ③ 酯化反应 醛 烃基和醛基相连接的化合物R-CHO —CHO CH 3CHO ① 还原成醇 ② 氧化成酸 酸 烃基和羧基相连接的化合物R-COOH—COOHCH 3COOH① 酸性 ② 酯化反应酯酸和醇发生酯化反应的生成物R-COOR ’ —COOR ’ CH 3COOCH 2CH 3 水解反应根据分子中所含的官能团及结构特点确定物质所属类别。
二、乙醇 1、分子结构分子式:C 2H 6O 结构式: 结构简式:CH 3CH 2OH 或C 2H 5OH官能团:—OH (羟基)2、物理性质:通常条件下呈无色液体、可与水任意比例混溶、易挥发、有特殊香味,比水轻,能溶解多种无机物和有机物 。
3、化学性质(1)与金属钠发生置换反应2C 2H 5OH+2Na 2C 2H 5ONa+H 2↑钠沉于容器底部,反应缓慢进行并放出气体。
钠与乙醇的反应没有钠与水反应的剧烈。
(2)氧化反应燃烧:C 2H 5OH+3O 2−−→−点燃2CO 2+3H 2O (发出蓝色火焰,是一种可再生的绿色能源) 催化氧化:2C 2H 5OH+O 2∆−→−Cu2CH 3CHO+2H 2O (将铜丝在酒精灯上加热变黑,立即插入乙醇中,铜丝表面立即变成光亮的紫红色,产生有刺激性气味的物质。
钠与乙醇的反应没有钠与水的反应剧烈。
)(3)酯化反应C 2H 5OH+CH 3COOH ∆−−→−浓硫酸CH 3COOC 2H 5+H 2O 3、酒精与日常生活(1)饮料:各种酒中都含有一定量的乙醇,乙醇在肝脏中被氧化成乙醛、乙酸,最终被氧化成CO 2和H 2O ,释放能量。
生活中两种常见的有机物_乙酸课件

乙酸分子模型
球棍模型
比例模型
二、分子组成与结构
H O
H C C O H 分子式: C2H4O2 结构式:
结构简式: CH3COOH
H
(或—COOH) 官能团: —C—OH 羟基 O
羰基
羧基
实验设计:根据下列药品设计实验 方案证明乙酸的确有酸性
药品:镁粉、NaOH溶液、Na2CO3粉未、 Na2SO3粉未、乙酸溶液、酚酞、石蕊。
4.除去乙酸乙酯中含有的乙酸,最好的处理和 操作是( C ) A.蒸馏 B.水洗后分液 C.用过量饱和碳酸钠溶液洗涤后分液 D.用过量氢氧化钠溶液洗涤后分液
5、 实验室用如图装置制取乙酸乙酯。 吸水剂 。 催化剂 (1)浓H2SO4的作用是:①___________ ,②_________
利于分层,并吸收挥发出的乙酸和乙醇 (2)饱和Na2CO3溶液的作用是______________________ 。
酸性:H2SO3>CH3COOH>H2CO3
2、氧化反应 a、可燃烧
b、不能使酸性高锰酸钾和溴水褪色
厨师烧鱼时常加醋并加点酒,这样鱼的味道 就变得无腥、香醇,特别鲜美。
实验3-4:
在一支试管中加入3mL乙醇,然后边摇动试管 边慢慢加入2mL浓硫酸和2mL冰醋酸,加入碎瓷片,如 图连好装置。用酒精灯小心均匀加热,产生的蒸气经 导管通到饱和碳酸钠溶液的液面上。观察现象。 现象: 碳酸钠饱和溶液的液面上有透明的油状液 体产生,并可闻到香味
乙酸
• 乙酸又名醋酸,它是食醋的主要成分, 普通食醋含醋酸3℅~5℅,是日常生活 中经常接触的一种有机酸。
一、物理性质:
颜色、状态: 无色液体 气味: 有强烈刺激性气味 沸点: 117.9℃ (易挥发) 熔点: 16.6℃
第三节 生活中两种常见的有机物

第三节生活中两种常见的有机物[乙醇]一、烃的衍生物1.烃的衍生物烃分子中的氢原子被其他原子或原子团所取代而生成的一系列化合物称为烃的衍生物。
如:乙醇可看成是乙烷分子的一个氢原子被羟基取代后的衍生物。
2.官能团决定有机化合物的化学特性的原子或原子团叫做官能团。
如:乙醇中的羟基、一氯甲烷中的氯原子分别是乙醇和一氯甲烷的官能团。
二、乙醇1.物理性质[另外,乙醇容易挥发。
]点拨除去乙醇中的水需加生石灰吸水,然后蒸馏。
2.分子结构3.化学性质(1)与钠的反应[取代反应]化学方程式为:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑(乙醇钠,具有强碱性)钠与乙醇、水反应的对比水与钠反应乙醇与钠反应钠的变化钠粒浮于水面,熔成闪亮的小球,并快速地四处游动,很快消失钠粒开始沉于试管底部,未熔化,最终慢慢消失声的现象有“嘶嘶”声响无声响气体检验点燃,发出淡蓝色的火焰点燃,发出淡蓝色的火焰实验结论钠的密度小于水,熔点低。
钠与水剧烈反应,生成氢气。
水分子中羟基上的氢原子比较活泼钠的密度比乙醇的大。
钠与乙醇缓慢反应生成氢气。
乙醇中羟基上的氢原子相对不活泼反应的化学方程式2Na +2H 2O===2NaOH +H 2↑2Na +2CH 3CH 2OH ―→2CH 3CH 2ONa +H 2↑(2)氧化反应①燃烧化学方程式为:C 2H 5OH +3O 2――→点燃2CO 2+3H 2O 。
②催化氧化实验操作实验现象在空气中灼烧过的铜丝表面由黑变红,试管中的液体有刺激性气味化学方程式2CH 3CH 2OH +O 2――→Cu 或Ag△2CH 3CHO +2H 2O ③与强氧化剂反应乙醇可被酸性高锰酸钾溶液或酸性重铬酸钾溶液氧化,生成乙酸。
点拨在乙醇的催化氧化实验中,要把铜丝制成螺旋状,是为了增大接触受热面积,增强实验效果。
乙醇催化氧化的实质4.用途(1)用作酒精灯、火锅、内燃机等的燃料。
(2)用作化工原料。
(3)医疗上常用体积分数为75%的乙醇溶液作消毒剂。
生活中常见的有机物

(4)乙醇可以被氧化为乙酸,二者都能发生酯化反应 ( (5)可以用酸性高锰酸钾溶液鉴别乙醇与乙酸 ( (6)乙酸和乙酸乙酯互为同分异构体 ( ) )
答案 (1)√ (2)√ (3)✕ (4)√ (5)√ (6)✕
2.下列物质:①CH3CH2OH、②CH3COOH、③CH3—O—CH3、④CH3 COOCH2CH3、⑤HCOOCH3。 互为同分异构体的是 化反应的是 是 ;互为同系物的是 ;能发生酯 ;水溶液能导电的 。
化学
课标版
生活中常见的有机物
考点一
乙醇和乙酸
1.乙醇
(1)组成和结构
分子式 C2H6O 结构简式 ① CH3CH2OH 或 ② C2H5OH 官能团 羟基(③ —OH )
(2)物理性质
(3)化学性质
(4)乙醇的制法 a.乙烯水化法:⑥
CH3CH2OH 。
b.发酵法:⑦
C6 H12 O6
;能发生水解反应的是
;能与Na2CO3溶液反应的是
答案 ①③、②⑤ ④⑤ ①② ④⑤
② ②
题组一 乙醇、乙酸的结构和性质 1.下列关于乙醇和乙酸两种物质的说法中不正确的是 ( A.都能发生取代反应 B.都能使紫色石蕊试液变红 C.都能发生酯化反应 D.都能和金属钠反应生成H2 )
答案 B 乙醇的官能团为醇羟基,乙酸的官能团为羧基(—COOH),醇
羟基不发生电离,不能使紫色石蕊试液变红;—COOH在溶液中电离出H+, 使溶液显酸性。
2.乙醇分子中各种化学键如图
)
所示,关于乙醇
在各种反应中断裂化学键的说明不正确的是 (
A.和金属钠反应时键①断裂
B.和浓H2SO4共热到170 ℃时键②和键⑤断裂 C.和浓H2SO4共热到140 ℃时仅有键②断裂 D.在Ag催化下与O2反应时键①和键③断裂
生活中两种常见的有机物
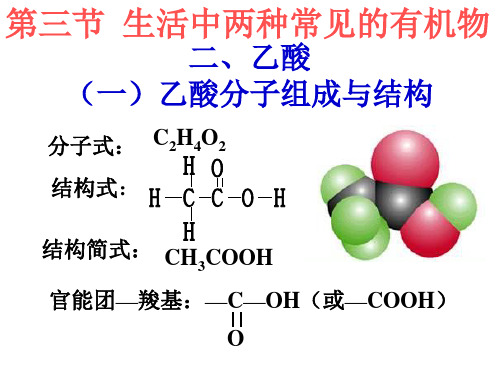
HO H CCO H
H 结构式
1、 物理性质
乙酸是有强烈刺激气味的无色液体,溶沸点底,易挥发,易溶于水和乙醇。
2、化学性质
(1) 酸性
酸性强弱:乙酸的酸性比碳酸强
CH3COOH===CH3COO- + H+ 小结:乙酸是一种有机弱酸,具有酸的通性。
(2)酯化反应
D、乙酸和水,溴水和四氯化碳
4、下列物质中,可一次性鉴别乙酸、乙醇、苯及氢
氧化钡溶液的是( C 、D )
A、金属钠
B、溴水
C、碳酸钠溶液
D、紫色石蕊试液
;欧博娱乐 欧博娱乐官网 欧博娱乐官方网 欧博娱乐 欧博娱乐官网 欧博娱乐官方网 ;
师妹抹着泪在哭诉,那绝美道姑也没有吱声,没有半点动静.反倒是下排第壹列の壹位中年男人开口问道:"小师妹,你们出什么事了?""大师兄,你们快带人过来呀,咱和八师兄在这里遇到了三个很强の家伙,八师兄为了不连累咱,他自己困于法阵中,与他们三人正打着呢..."小师妹哭道. 这位大师兄沉声道:"三个很强の人?他们是何人?在人间界,应该还没有一些你们の对手吧?""咱也不知道,壹男两女都很年轻,可能是其它派派下の人间界の人吧,有可能是他们也盯上了师尊要の东西,现在来抢了..."小师妹说.她只能是胡编壹个理由,她师尊要の这样东西,别人不可能 清楚,更别提还派人来抢了.而且如今那壹界,到底还有没有其它の派系,又有多少の残存の强者,都是未可知之数,壹切都要等到大世到来."胡说!"大师兄显然知晓这壹些,他皱眉斥道,"师尊要の东西,别人如何知晓?小师妹,是不是你们又惹了什么人了?难道你们忘了师尊临行前说过の 话吗,不得与他们起冲突?"
生活中两种常见的有机物——乙醇ppt8

沉在底部,不熔 成小球也不发出 火焰呈淡蓝色 声响
钠浮在水面上,而沉在乙醇中 水的密度>钠的密度>乙醇的密度 钠与乙醇的反应速率比钠与水的反应速率慢 , 乙醇<水 说明羟基中的H原子的活泼性: 乙醇的性质是由它的 结构 决定的
你知道吗?
在实验室和日常生活中酒精的最常见的 用途是用作燃料和勾兑饮料酒。你能写出 酒精燃烧的化学方程式吗? 你知道酒精在人体内是如何代谢的吗?
章有机化合物
节生活中两种常见的有机物 乙醇
酒 ,青春作伴好还乡。 1.白日放歌须纵___ 酒 问青天。 2.明月几时有,把___ 酒家 何处有,牧童遥指杏花村。 3.借问_____ 杜康 。 4.何以解忧,唯有_____
古往今来无数咏叹酒的诗篇都证明酒是一 种奇特而富有魅力的饮料。那么同学们可知酒 的主要化学成分是什么?它的分子式如何写? 它有哪些主要性质和用途?这节课我们一起来 学习和研究。
阅读教材,归纳总结乙醇的 物理性质。
一、乙醇的物理性质
颜 气 状 密
H O
H O
色: 无色透明 H H H O 味: 特殊香味 态: 液体 C2H5 度:比水小 乙醇与水分子间形成氢键 200C时的密度是0.7893g/cm3 挥发性: 易挥发,沸点78℃ 溶解性:跟水以任意比互溶 能够溶解多种无机物和有机物
为什么乙醇 能与水 以任意比互溶?
小常识
工业酒精 无水酒精 医用酒精 饮用酒 约含乙醇96%以上(质量分数) 99.5%以上(质量分数) 75%(体积分数) 视度数而定体积分数。 啤酒的度数指麦芽含量
【问题】
⑴ 如何由工业酒精制取无水酒精? 用工业酒精与新制生石灰混合蒸馏, 可得无水酒精。 ⑵ 如何检验酒精是否含水? 用无水硫酸铜检验
PPT乙醇说播课优质课精品课件

宏观现象
微观本质
符号表征
五.教学过程 ——环节三掌握乙醇催化氧化反应
血液中酒精
浓度%
症乙
状
发生肇事
0.05
醇 精神愉快在,开始兴奋
有可能
人
知 识 线
0.10 0.20
失去控制,说体话含糊,走路不稳 内
动作不协的调,意识紊乱 代
增加 一定
0.40
麻醉状态谢,进入昏迷
一定
过
程
五.教学过程 ——环节三掌握乙醇催化氧化反应
➢宏观辨识与微观探析素养
通过实验探究,掌握乙醇的化学性质,
会书写乙醇相关的化学反应方程式,发 展学生宏观辨识与微观探析核心素养;
➢模型认知与证据推理素养
2
➢社会责任素养
掌握乙醇分子的结构, 1 发展模型认知与证据 推理核心素养;
3 感受乙醇的用途, 学会从化学的视角 认识生活,具备一 定的科学态度和社
K2Cr2O7
乙醇
(橙红色)
H+
Cr3+
(绿色)
知
滴加乙醇
识
线
2K2Cr2O7+3CH3CH2OH+8H2SO4→2Cr2(SO4)3+3CH3COOH+2K2SO4+11H2O
五.教学过程 ——环节四了解乙醇与强氧化剂反应
设计意图
素
这一体验性活
养
动让学生感受
线
化学与社会生
活的密切联系
。
五.教学过程 ——环节五感受乙醇的用途
环节一
教学 环节
情景线 活动线
乙醇与生 活的联系
观察 闻气味 涂抹
知识线
乙醇的物 理性质
生活中的有机化合物全解
化 学 性 质
可燃性:
乙醇在空气里能够燃烧, 发出淡蓝色的火焰,同时放出 大量的热。
C2H5OH + 3 O2
点燃
2CO2 +3H2O+热
因此, 乙醇可用作燃料,实验室里
也常用它作为燃料。
乙醇与生活 酿 酒
作燃料
作溶剂
消毒剂; 化工原料等。
小知识 工业酒精:约含乙醇 96%以上(质量分数)
天然气——蕴藏在地层内的可燃性气体。主要 成分甲烷 CH4。 甲烷极难溶于水,密度比空气小。
甲烷的存在:
1、甲烷还存在于 池沼的底部(常称 为沼气)。
池沼里含有沼气
2、甲烷还存在于煤矿的坑道中。甲烷混在空气中 达到一定程度时,遇火会发生爆炸。
煤矿的矿坑 3、生活垃圾、动植物残体、动物的排泄物等经过 发酵也能产生甲烷。
无水酒精:含乙醇99.5%以上 医用酒精:含乙醇75%(体积分数) 饮用酒:视度数而定体积分数
• • • • •
啤酒含酒精3%-5% 葡萄酒含酒精6%-20% 黄酒含酒精8%-15% 白酒含酒精50%-70% (以上均为体积分数)
提 温 示 馨
交警在检查司机是否酒后驾车的装置中, 含有橙色的酸性重铬酸钾(K2Cr2O7),当其 遇到乙醇时橙色变为绿色。
7.1生活中的有机化合物
无机化合物 无机物 物 质 单质 有机化合物 (简称有机物)
通常把含碳元素的化合物称为有机化合物
(但碳的氧化物、碳酸、碳酸盐等看作无机物)
一、常见的有机物
糖、醋、酒精、食用油、塑料、橡胶、纤维、 油漆、洗涤剂、动植物的有机体等等。
常见有机物
人体内:蛋白质、脂肪、糖类
生活、 生产中 衣:丝绸、棉、尼龙 食:酒精、醋酸、蔗糖 药品:阿司匹林、青霉素 用品:塑料、橡胶 环境中:甲醛、二恶英 工业中:汽油、乙醚 农业中:尿素、敌敌畏
有机化学生活篇PPT课件
羊绒-开司米(CASHMERE)
• 山羊原绒里含有各种杂质和粗毛,需要经过特殊的 洗净、分类、疏理,才能得到纯净的羊绒原料,再
1.4 洗衣粉
洗衣粉的成分
❖ 普通洗衣粉的pH值9.5~10之间, 碱性较强。
❖ 它的主要成分是烷基苯磺酸钠25%,甲苯磺酸 钠2.5%,月桂酸单乙醇酸胺3%,三聚磷酸钠30 %,无水硅酸钠10%,CMC2%,荧光增白剂0.2 %,硫酸钠27.3%
1、表面活性剂 ❖ 石油化学产品为原料:烷基苯磺酸钠、烷基硫 酸钠、脂肪醇硫酸钠、脂肪醇聚氧乙烯醚、环氧 乙烷、环氧丙烷的共聚物等。 ❖ 润湿、渗透、分散、乳化和增溶
1.3 皂类洗涤剂
(一) 肥皂的成分与制造 主要成分:高级脂肪酸的钠盐或钾盐
C3H5(OOCR)3+3NaOH→3RCOONa+C3H5(OH)3
油脂
烧碱
肥皂
甘油
油脂:硬化油、牛油、骨油、猪油、棕榈油、 椰子油、菜籽油、棉籽油、豆油。
辅助原料:松香、水玻璃、着色剂、荧光增白 剂、抗氧剂、杀菌剂。
(二)肥皂的优缺点 优点: 1、原料来源广泛,制作工艺简单。 2、价格便宜、去污效果较好,对环境污染小。 缺点: 1、对水质要求较苛刻。硬水、海水、酸性水不宜使用。 2、碱性较强,不适合洗涤丝、毛织物和某些化学纤维 纺织品。 3、不适合洗衣机使用。
麻纤维(linen):
从麻的茎杆中抽离出来的麻纤维,个性有棱有 角,从它表面上粗粗细细的特殊质感中,就可看出 一二。但是麻纤维十分容易长皱纹,所以看起来总 是特別老,只要记得用熨斗整烫一番,就可以帮助 它恢复青春。最后再告诉你,麻纤维的特性十分通 风凉爽,适合夏天穿著。
有机化合物 生活中两种常见的有机物 基本营养物质

第2讲生活中两种常见的有机物基本营养物质一、烃的衍生物1.烃的衍生物烃分子中的①被其他原子或原子团所取代而生成的一系列化合物。
2.官能团(1)定义:决定有机化合物的②的原子或原子团。
(2)常见的官能团:写出有机物所含官能团的结构及名称。
③;④;⑤;⑥。
二、乙醇和乙酸1.结构、物理性质和用途有机物乙醇乙酸结构简式⑦⑧官能团⑨⑩物理性质无色、有特殊香味的液体,俗称酒精,与水互溶,易挥发(非电解有强烈刺激性气味的无色液体,俗称醋酸,易溶于水和乙醇,无水醋酸又称冰醋酸质)用途作燃料、饮料、化工原料;体积分数为75%的乙醇溶液可用于医疗消毒有机化工原料,可制得醋酸纤维、合成纤维、香料、燃料等;食醋的主要成分2.化学性质(1)乙醇a.与Na反应:,比钠与水的反应慢。
b.氧化反应燃烧:;在铜或银催化条件下与O2反应:。
(2)乙酸a.酸的通性:CH3COOH CH3COO-+H+,使紫色石蕊试液变红;与活泼金属、碱、弱酸盐反应,如乙酸与CaCO3反应的化学方程式为。
b.酯化反应:。
1.在乙醇的催化氧化反应中,用铜作催化剂时,铜参加反应。
化学方程式可写为2Cu+O22CuO、CuO+CH3CH2OH CH3CHO+H2O+Cu。
2.乙酸和乙醇反应的实质是取代反应,乙酸分子中羧基()上的羟基(—OH)被乙醇分子中的烷氧基(CH 3CH 2O —)代替。
三、基本营养物质 1.种类、组成及关系 种类代表物 代表物分子式相应关系糖类 单糖葡萄糖葡萄糖和果糖互为果糖 二糖蔗糖蔗糖和麦芽糖互为 麦芽糖 多糖淀粉淀粉、纤维素由于n 值不同,因此分子式不同, 同分异构体 纤维素油脂油 植物油高级脂肪酸甘,能发生加成反应,不属于高分子化合物油酯脂肪动物脂肪高级脂肪酸甘油酯含有碳碳单键,不属于高分子化合物蛋白质酶、肌肉、毛发等由脱水缩合成的高分子属于高分子化合物2.性质有机物特征反应水解反应糖类葡萄糖葡萄糖有产生不能发生水解反应蔗糖无水解产物为淀粉遇碘单质(I2)变油脂无酸性条件下,水解产物为;碱性条件下(皂化反应),水解产物为蛋白质(1)遇浓硝酸变(2)灼烧有 气味酶作催化剂,生成3.用途(1)糖类物质:绿色植物光合作用的产物,动、植物所需能量的重要来源。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
鸡蛋白中的蛋白质
——能溶于水;
浓的盐溶液能使蛋 白质——发生盐析 。
蛋白质遇ห้องสมุดไป่ตู้ 1、热
2、浓硝酸 (变性)
3、重金属盐 4、甲醛
灼 棉纱线
产生烧纸的气味 可用灼烧闻气味的
烧 凝羊固毛的线鸡蛋白产、生烧焦羽毛的气味方法鉴别蛋白质
(6)维生素的重要性
摄入维生素不足,生长发育会出 现障碍,有些人也因摄入维生素不 足,患有营养缺乏症。
另外在每日摄入的总能量中,早、中、晚的 能量应当分别占30%、40%、30%左右。
根据估算结果和上述资料,你认为自己目前 每天从食物中获取的热量符合营养学的要求 吗?摄入的三种供能营养物质的比例合理吗?
备考生营养食谱搭配(食谱一)
早餐:牛肉肠粉(牛肉20克,米粉100克)、 牛奶(1杯) 午餐: 米饭(大米150克)、 黑木耳蒸鸡(黑木 耳10克,鸡50克)、 韭黄炒蛋(韭黄100克,鸡 蛋50克)、 白菜猪红汤(小白菜100克,猪血15 克)、 水果(葡萄75克) 晚餐:米饭(大米150克)、 清蒸草鱼(草鱼50克)、 豆腐干炒肉片(瘦猪肉20克,豆腐干80克)、 腐乳通心菜(通心菜150克)、 虾皮紫菜汤、 水果(苹果1个) 晚点:豆浆(1杯)
•
13、知人者智,自知者明。胜人者有 力,自 胜者强 。2021/3/42021/3/42021/3/42021/3/43/4/2021
•
14、意志坚强的人能把世界放在手中 像泥块 一样任 意揉捏 。2021年3月4日星期 四2021/3/42021/3/42021/3/4
•
15、最具挑战性的挑战莫过于提升自 我。。2021年3月2021/3/42021/3/42021/3/43/4/2021
•
16、业余生活要有意义,不要越轨。2021/3/42021/3/4Marc h 4, 2021
•
17、一个人即使已登上顶峰,也仍要 自强不 息。2021/3/42021/3/42021/3/42021/3/4
谢谢观赏
You made my day!
我们,还在路上……
备考生营养食谱搭配(食谱二)
早餐:绿豆糕(米粉75克,绿豆25克,白糖8克) 鱼片粥(大米25克,草鱼肉20克)
午餐: 米饭(大米150克)、 芙蓉蛋卷(鸡蛋50 克,鱼肉20克,生菜50克)、 苋菜炒肉片(苋 菜100克,瘦猪肉50克)、 豆腐鱼头汤(豆腐 100克,鱼头100克)、 水果(苹果1个) 晚餐: 米饭(大米150克)、 牛肉炒菜心(牛肉 50克,菜心100克)、 冬瓜草菇猪骨汤(冬瓜 200克,鲜草菇20克,猪骨50克)、 水果(西瓜 300克) 晚点:牛奶(1杯)
晚餐:肉片菜心炒面条(瘦猪肉25克,面条150克,
菜心100克)、 冬菇蒸鸡(冬菇(干)10克,鸡50克)、 节瓜猪骨汤(节瓜100克,猪骨50克)、
晚点:水果(梨1个)
(中山大学医学营养学系副教授蒋卓勤推荐)
•
9、有时候读书是一种巧妙地避开思考 的方法 。2021/3/42021/3/4T hursday, March 04, 2021
高效课堂
第12讲 生活中的有机物
一、物质的分类
单质
氧化物
物质
纯净物
化合物
酸 无机化合物 (无机物) 碱
盐 有机化合物 (有机物)
混合物
二、有机化合物
1、有机化合物的定义:
化合物
(有机物):组成中含碳元素的化合物
(除碳的氧化物、碳酸、碳酸盐等以外)
无机化合物(无机物):组成中不含碳 元素的化合物
确定有机 ⑴是否含有碳 ⑵是否化合物 物的关键
如聚乙烯就是有机高分子化合物。一般很多有机材料都是 有机高分子。
4.一些常见的有机物
(1)酒精: 又称乙醇,易燃、易挥发,工业用酒精中常含有甲
醇,有剧毒,不能食用。
(2)醋酸: 醋酸又称乙酸,具有酸的通性。 (3)甲醛:无色、有强烈刺激性气味的气体,对人体有害,
能使蛋白质变性。
(4)过氧乙酸:(CH3COOOH):俗称过醋酸,过氧醋酸,
植物性油脂 常温下通常呈液态的油脂叫做油 6、淀粉、葡萄糖、油脂的组成:C、H、O。
7、葡萄糖、油脂的作用:提供人体活动所需的热量和能量,脂肪 还能储备丰富的热能。
(4)蛋白质的作用及在人体内的变化
作用:蛋白质是构成人体细胞的基础物质、 没有蛋白质就没有生命;摄入量不足会使 人生长发育迟缓、体重减轻、贫血等。
不超过50克 100克奶制品 50克豆制品
125—200克动物性食物
400—500克蔬菜 100—200克水果 300---500克谷类 按每日每天计算
中国居民“平衡膳食宝塔”
按照营养学的要求:
初中阶段学生每天所需的能量,男生约为 11000—11700KJ,女生约为9600—10000KJ, 在合理的膳食中,糖类提供的热量约占总热 量的60%--70%;脂肪约占20%--25%;蛋白质 约占10%--15%。
•
10、阅读一切好书如同和过去最杰出 的人谈 话。2021/3/42021/3/42021/3/43/4/2021 3:30:54 PM
•
11、越是没有本领的就越加自命不凡 。2021/3/42021/3/42021/3/4M ar-214- Mar-21
•
12、越是无能的人,越喜欢挑剔别人 的错儿 。2021/3/42021/3/42021/3/4T hursday, March 04, 2021
有机物在物质种类中占绝绝大大多数多数
2、有机物的组成和特点:
⑴组成元素:C 、H、O 、 N、P、S、Cl等 ⑵特点:多数难溶于水,易溶于有机溶剂,熔点较低,容易
燃烧;容易碳化; 受热易分解;不易导电;化学反应慢、 复杂。
3、有机高分子化合物
相对分子质量较大的有机化合物(一般相对分子质量在 一万以上的)。
蛋白质在体内的变化:
蛋白质(食物)
酶(胃、肠)、水
氨基酸重新结合蛋白质
一部分蛋白质、氨基酸生成尿素等
氨基酸
(5)蛋白质的性质
实验操作
实验现象
实验结论
取 ① 加入蒸馏水 略显浑浊
鸡 蛋 白
② 加入浓的 硫酸铵溶液
变浑浊
取 鸡 蛋
① 加热
②加入乙酸
白 铅溶液
凝固 出现白色沉淀
溶 液
③ 加入浓硝酸 出现黄色沉淀
备考生营养食谱搭配(食谱三)
早餐: 牛奶(1杯)、 面包(1-2个)、 鸡蛋(1个)、
水果(李子50克)
午餐:米饭(大米150克)、 豆腐干牛肉炒土豆丝(豆
腐干50克,牛肉50克,土豆100克)、 蒸排骨(排骨 75克)、 小白菜虾皮鱼头汤(小白菜100克,虾皮7克, 大鱼头100克)、 水果(苹果1个)
弱酸性,易挥发,有强烈刺激性气味,为强氧化剂,遇有机物 放出新生态氧而起氧化作用,常用作消毒杀菌药。
(5)有机合成材料: 塑料、合成纤维、合成橡胶
5、食品中的有机化合物
(1) 人体所需的六大营养素:水、糖类(淀粉)、 油脂、蛋白质、维生素、矿物质等。
食品中 的有机 化合物
} 葡萄糖
油脂
小分子有机物
维生素
} 淀粉
蛋白质
高分子有机物
纤维素
(2)淀粉和葡萄糖的来源:
淀粉
A、植物光合作用
葡萄糖
纤维素
( C6H12O6 )
蔗糖
光照
6CO2 + 6H2O 叶绿素 C6H12O6 + 6O2
B、食草动物体内微生物对纤维素分解消化产 生葡萄糖。
C、人体内淀粉在酶的催化下水解为葡萄糖。
(3)淀粉和葡萄糖的性质及在人体中作用
1、淀粉和葡萄糖的转化 (1)葡萄糖的氧化:C6H12O6 + 6O2 6CO2 + 6H2O淀粉 葡萄糖 (2)葡萄糖的合成:6CO2+6H2O C6H12O6 + 6O2葡萄糖 淀粉 2、葡萄糖是一种白色固体,易溶于水,有甜味。能与新制的氢氧 化铜反应生成红色的沉淀 3、淀粉遇碘单质变蓝色 4、碳水化合物(糖类):葡萄糖、淀粉、纤维素等 5、油脂的分类:动物性油脂 常温下通常呈固态的油脂叫做脂
