初三化学置换反应共18页
人教版初三下册化学方程式及实验现象汇总

九年级化学方程式及现象汇总(下册课本)一、置换反应(1)金属单质+ 酸------ 盐+ 氢气1、锌和稀硫酸反应:Zn + H2SO4 =ZnSO4 + H2↑2、镁和稀硫酸反应:Mg + H2SO4 =MgSO4 + H2↑3、铝和稀硫酸反应:2Al + 3H2SO4 =Al2(SO4)3 + 3H2↑4、锌和稀盐酸反应:Zn + 2HCl= ZnCl2 + H2↑5、镁和稀盐酸反应:Mg+ 2HCl= MgCl2 + H2↑6、铝和稀盐酸反应:2Al + 6HCl= 2AlCl3+H2↑(1-6)现象:都有气泡产生,但是剧烈程度不相同。
7、铁和稀盐酸反应:Fe + 2HCl=FeCl2 + H2↑8、铁和稀硫酸反应:Fe + H2SO4 = FeSO4 + H2↑铁单质参加置换反应,铁元素由“0”价变为“+2”价,生成“某亚铁”(7-8)现象:有气泡产生,溶液由无色变成浅绿色。
(2)金属单质+ 盐(溶液) --- 另一种金属+ 另一种盐9、铁与硫酸铜反应:Fe + CuSO4=Cu + FeSO4现象:铁条表面覆盖一层红色的物质,溶液由蓝色变成浅绿色。
(古代湿法制铜及“曾青得铁则化铜”所指的是此反应)10、锌片放入硫酸铜溶液中:CuSO4+Zn=ZnSO4+Cu现象:锌片表面覆盖一层红色的物质,溶液由蓝色变成无色。
11、铜片放入硝酸银溶液中:2AgNO3 + Cu = Cu(NO3)2 + 2Ag现象:铜片表面覆盖一层银白色的物质,溶液由无色变成蓝色。
12、锌片放入硝酸银溶液中:2AgNO3 + Zn=Zn(NO3)2+ 2Ag现象:锌片表面覆盖一层银白色的物质13、铁丝放入硝酸银溶液中:2AgNO3 + Fe = Fe(NO3)2+ 2Ag现象:铁丝表面覆盖一层银白色的物质,溶液由无色变成浅绿色。
(3)金属氧化物+木炭或氢气→金属+二氧化碳或水(固体间置换反应)14、焦炭还原氧化铁:3C+ 2Fe2O34Fe + 3CO2↑15、木炭还原氧化铜:C+ 2CuO2Cu + CO2↑16、氢气还原氧化铜:H2 + CuO Cu + H2O现象:黑色粉末变成红色,试管内壁有水珠生成17、氢气与四氧化三铁反应:Fe3O4 + 4H23Fe + 4H2O18、氢气与氧化铁反应:Fe2O3+3H22Fe+3H2O现象:红色(氧化铁)粉末逐渐变成黑色,管内壁有水珠生成。
人教版化学九年级下册8.2知识总结:置换反应

置换反应置换反应有两个突出特点:一是在反应中一种游离态元素将另一种元素从其化合物中替换出来,使其变为游离态,因而在反应物和生成物中必定各有一种单质出现。
例如:Zn+H2SO4(稀)==ZnSO4+H2↑Fe+CuSO4=FeSO4+Cu二是反应的发生必定伴有某些元素化合价的变化,因此属于氧化还原反应。
如上述两例:在初中阶段学习的是发生在水溶液里的置换反应,主要有金属与酸溶液的反应和金属与盐溶液的反应,这两种反应都遵循金属活动性顺序而进行。
1.金属+酸──→盐+氢气金属:必须是位于金属活动性顺序中氢以前的金属,排在氢后面的金属不能跟酸发生置换反应。
金属的位置愈靠前,置换反应愈容易进行。
例如:Mg+H2SO4(稀)=MgSO4+H2↑很快Zn+H2SO4(稀)=ZnSO4+H2↑平稳Fe+H2SO4(稀)=FeSO4+H2↑较慢Cu+H2SO4(稀)不能反应酸:必须是可溶性的非氧化性酸,如盐酸、稀硫酸、磷酸等。
氧化性酸如硝酸、浓硫酸等不能与金属发生置换反应,这种具有强氧化性的酸与金属发生的是另一种类型的反应。
例如:Zn+2H2SO4(浓)ZnSO4+SO2↑+2H2O此外,碳酸(H2CO3)、氢硫酸(H2S)等很弱的酸,虽然能与氢前面的金属发生置换反应,但其反应不够典型或难以进行。
硅酸(H2SiO3)是微溶性酸,难与金属发生置换反应。
盐:反应生成的盐必须是可溶的,否则,生成难溶或微溶的盐会沉积在金属表面,阻碍反应顺利进行。
例如下列反应因生成难溶的硫酸铅,反应很难顺利进行。
Pb+H2SO4(稀)=PbSO4+H2Pb+CuSO4=PbSO4+Cu2.金属+盐──→另一种盐+另一种金属金属:只有在金属活动性顺序中位于前面的金属才能把位于后面的金属从它们的盐溶液中置换出来。
这两种金属的位置相距愈远,反应愈容易进行。
但应注意,K、Ca、Na等很活动的金属在与其它金属的盐溶液发生反应时,是先置换水中的氢,而难以置换盐中的金属。
初三化学反应式大全

初三化学反应式大全一、氧化还原反应(Redox Reactions)1. 金属与非金属氧化物反应:M + O₂ → MO例如:2Na + O₂ → 2Na₂O2. 非金属与非金属氧化物反应:N₂O₅ + H₂O → 2HNO₃例如:CO₂ + H₂O → H₂CO₃3. 金属与酸反应:2Fe + 6HCl → 2FeCl₃ + 3H₂例如:Zn + H₂SO₄ → ZnSO₄ + H₂4. 还原剂与氧化剂的反应:H₂O₂ + 2KI → I₂ + 2KOH例如:KMnO₄ + 5HCl → KCl + MnCl₂ + 3H₂O + Cl₂5. 氧化剂与还原剂的反应:Cl₂ + 2KI → 2KCl + I₂例如:HNO₃ + 3Cu → 3Cu(NO₃)₂ + H₂O + 2NO 二、酸碱反应(Acid-Base Reactions)1. 强酸与强碱的反应:HCl + NaOH → NaCl + H₂O例如:HNO₃ + KOH → KNO₃ + H₂O 2. 强酸与碱性氧化物的反应:HCl + Na₂O → 2NaCl + H₂O例如:HCl + CaO → CaCl₂ + H₂O3. 酸与碱的中和反应:H₂SO₄ + 2NaOH → Na₂SO₄ + 2H₂O例如:HNO₃ + NH₃ → NH₄NO₃4. 酸与金属的反应:2HCl + Zn → ZnCl₂ + H₂例如:2HCl + Mg → MgCl₂ + H₂5. 酸与金属碱的反应:2HNO₃ + Ca(OH)₂ → Ca(NO₃)₂ + 2H₂O 例如:HCl + NaOH → NaCl + H₂O三、沉淀反应(Precipitation Reactions)1. 双盐交换反应:AgNO₃ + NaCl → AgCl + NaNO₃例如:CaCl₂ + Na₂CO₃ → CaCO₃ + 2NaCl2. 酸与相应的盐反应:2HCl + Ba(OH)₂ → BaCl₂ + 2H₂O例如:2HCl + Cu(OH)₂ → CuCl₂ + 2H₂O3. 溶液中的钠盐与其他金属盐反应:Na₂S + Cd(NO₃)₂ → CdS↓ + 2NaNO₃例如:Na₂S + Pb(NO₃)₂ → PbS↓ + 2NaNO₃4. 氨与金属离子反应:2NH₃ + Cu²⁺ → Cu(NH₃)₄²⁺例如:2NH₃ + Fe³⁺ → Fe(NH₃)₆³⁺四、酸、碱、盐的相关反应(Acid, Base, Salt Reactions)1. 酸钠与碳酸钙的反应:2HCl + Na₂CO₃ → 2NaCl + H₂O + CO₂例如:2HCl + CaCO₃ → CaCl₂ + H₂O + CO₂2. 硝酸银与氯化钠的反应:AgNO₃ + NaCl → AgCl + NaNO₃例如:AgNO₃ + KCl → AgCl + KNO₃综上所述,初三化学反应式大全包含了氧化还原反应、酸碱反应、沉淀反应以及酸、碱、盐的相关反应。
【优质】达尔文的置换反应化学方程式-word范文 (4页)

本文部分内容来自网络整理,本司不为其真实性负责,如有异议或侵权请及时联系,本司将立即删除!== 本文为word格式,下载后可方便编辑和修改! ==达尔文的置换反应化学方程式CO2+H2O=CO+H2O+H(电解)这是一种化学方程式中十分简单的配平方式。
世界上有这样一个故事:在中国西南境地,有这样的一户人家。
年长十几岁的叔叔,带着一个小他十来岁的男子生活在一起。
叔叔是一位有文化但是由于生存空间的原因,一直在家照顾小他十几岁的男子,洗衣做饭,清洁卫生。
因为这个年轻男人,工作努力积极上进。
年关跟前,年轻男子带回来一位年轻美貌的年轻女子,女子皮肤白皙,秀发如斯,谈吐文雅,勤快守时。
年轻男子因为跟这位年长的叔叔住在一起,照顾体切,年轻的男子希望给这两位自己终身敬爱的“亲人”一个温暖的家庭环境,在百忙之中,抽出时间给他们以及他自己一个见面的时间和一个温馨的环境。
因为这两位年轻人认识的时间很短,年轻男子,希望给她考虑以及接纳自己的时间。
在大年夜过后,背着行囊借口“工作原因”除去远行,希望给彼此考虑以及接纳的时间。
哪里知道,等到这个年轻的男子回到家里,发现女子不见了,叔叔一个人安静的坐在厨房里吃饭。
灯光,清幽而冷清。
男子失落的脸庞边掩映的从发迹间留下来的一滴湿答答的水珠。
没有问原因。
因为,以自己对双方的长期观察,在他的眼里,这两个人都很重要,都很优秀,所有的疑问影藏在自己的心里。
很久很久,两个相处十几年时间的男人,尽然变成了陌路相逢的陌生人。
过了两年的时间,这个面容消瘦苍白的中年男人在喝了很多很多酒以后,向他的弟弟下跪,哭着诉说了在“他”回来两个月之前的一件难以启齿的事情。
年后热闹的人群四处奔走,寻找更多的生存基础和生存毅力。
在这条阴暗悠然的街道中,留下的只有湿漉漉的背影和曾经温暖的场面。
小晴,那个女子的,温柔善良体贴,因为你的离开,叔叔终于因为常年的坚持而病倒。
小晴在这个属于我们自己的家里,看着你远去的背影怀揣着失落的心情,仍然坚持为她心目中的男人坚持照顾身边这位上了年纪的“大叔”。
初三化学知识点:置换反应的实例类型归纳

初三化学知识点:置换反应的实例类型归纳置换反应的实例类型归纳一、按元素的性质划分,金属与非金属单质间的置换。
1、金属置单质换金属单质2Al+Fe2O3 Al2O3+2Fe(铝热反应。
Al还可与V2O5、CrO3、WO3、MnO2等发生置换) Fe+CuSO4 FeSO4+Cu2、金属单质置换非金属单质2Na+2H2O 2NaOH+H2 2Mg+CO2 2MgO+C 3Fe+4H2O(g) Fe3O4+4H23、非金属单质置换金属单质H2+CuO Cu+H2O C+FeO Fe+CO Si+2FeO 2Fe+SiO24、非金属单质置换非金属单质2F2+2H2O 4HF+O2 2C+SiO2 Si+2COC+H2O CO+H2 2H2+SiCl4 Si+4HCl二、按元素在周期表的位置划分,同族元素单质间的置换与不同族元素单质间的置换。
1、同主族元素单质间的置换Na+KCl NaCl+K 2Na+2H2O 2NaOH+H22H2S+O2 2S+2H2O 2C+SiO2 Si+2COCl2+2HI 2HCl+I2 F2+2HCl 2HF+Cl22、不同主族元素单质间的置换Mg+2HCl MgCl2+H2 2Mg+CO2 2MgO+C2Al+6HCl 2AlCl3+3H2 2F2+2H2O 4HF+O2C+H2O CO+H2 2H2+SiCl4 Si+4HClH2S+Cl2 S+2HCl 3Cl2+8NH3 6NH4Cl+N2 4NH3+3O2 2N2+6H2O3、主族元素单质置换副族元素的单质H2+CuO Cu+H2O 2Al+Fe2O3 Al2O3+2FeC+CuO Cu+CO 2Al+3Hg2+ 2Al3++3Hg Na+TiCl4 4NaCl+Ti4、副族元素的单质置换主族元素单质3Fe+4H2O(g) Fe3O4+4H2 Zn+2H+ Zn2++H25、副族元素的单质置换副族元素的单质Fe+CuSO4 FeSO4+Cu三、按物质类别划分,单质与氧化物间的置换和单质与非氧化物间的置换。
置换反应

浩贤个性化教案学员姓名:年级:初三学校:凤城中学学科:化学课时:1小时教材版本:人教版课题名称:复习置换反应教师姓名:王老师授课时间:2011年1月21 日至教案期数:1101-2教学目标理解置换反应概念掌握置换反应重点难点重点:1理解并掌握置换反应的概念及分类2掌握置换反应原则3熟记金属活动顺序并熟练解题难点:金属活动顺序一、概念置换反应是无机化学反应的基本类型之一,指一种单质和一种化合物生成另一种单质和另一种化合物的反应,可表示为:A+BC→B+AC置换关系是指组成化合物的某种元素被组成单质的元素所替代。
二、分类(一)根据反应物分类(1)金属单质+ 酸-------- 盐+ 氢气(置换反应)1、锌和稀硫酸反应:Zn + H2SO4 === ZnSO4 + H2↑2、镁和稀硫酸反应:Mg + H2SO4 === MgSO4 + H2↑3、铝和稀硫酸反应:2Al + 3H2SO4 === Al2(SO4)3 + 3H2↑4、锌和稀盐酸反应:Zn + 2HCl === ZnCl2 + H2↑5、镁和稀盐酸反应:Mg+ 2HCl === MgCl2 + H2↑6、铝和稀盐酸反应:2Al + 6HCl === 2AlCl3 + 3H2↑1~6的现象:有气泡产生。
7、铁和稀盐酸反应:Fe + 2HCl === FeCl2 + H2↑8、铁和稀硫酸反应:Fe + H2SO4 === FeSO4 + H2↑7~8铁参加的置换反应显+2价,7~8的现象:有气泡产生,溶液由无色变成浅绿色。
要特别注意不能用浓硫酸,硝酸,它们有强氧化性,先将金属氧化成对应氧化物,氧化物再溶于酸中,然后继续氧化,继续溶解,反应得以继续(2)金属单质+ 盐(溶液)----- 另一种金属+ 另一种盐9、铁与硫酸铜反应:Fe+CuSO4 === Cu+FeSO4现象:铁条表面覆盖一层红色的物质,溶液由蓝色变成浅绿色。
(古代湿法制铜及"曾青得铁则化铜"指的是此反应)10、锌片放入硫酸铜溶液中:CuSO4 + Zn == ZnSO4 + Cu现象:锌片表面覆盖一层红色的物质,溶液由蓝色变成无色。
九年级化学常见的化学反应方程式整理(word版)

四大基本反应类型:1、化合反应:多变12、分解反应:1变多3、置换反应:单质+化合物==新单质+新化合物4、复分解反应:两种化合物互相交换成分,生成另外两种化合物(有气体、沉淀或水)。
初中常见化学方程式的书写一、物质与氧气的反应1、单质与氧气的反应(化合反应)(1)镁在空气中的燃烧:2MgO 点燃O 2Mg 2+(2)铁在氧气中燃烧:432O Fe 点燃2O 3Fe +(3)铜在空气中加热:2CuO ΔO 2Cu 2+(4)铝在空气中燃烧:322O 2Al 点燃3O 4Al +(5)氢气在空气中燃烧:O 2H 点燃O 2H 222+(6)红磷在空气中燃烧:522O 2P 点燃5O 4P +(7)硫粉在空气中燃烧:22SO 点燃O S +(8)碳在氧气中充分燃烧:22CO 点燃O C +(9)碳在氧气中不充分燃烧:2CO 点燃O 2C 2+2、化合物与氧气的反应(1)一氧化碳在氧气中燃烧(化合反应):222CO 点燃O 2CO +(2)甲烷在空气中燃烧(氧化反应):O 2H CO 点燃2O CH 2224++(3)酒精在空气中燃烧(氧化反应):O 3H 2CO 点燃3O OH H C 22252++二、几个分解反应1、分解过氧化氢制氧气:↑+22222O 02H MnO O 2H2、加热混有二氧化锰的氯酸钾:↑+==2233O 2KCl ΔMnO 2KClO 3、加热高锰酸钾:↑++22424O MnO MnO 2K Δ2KMnO4、水在直流电的作用下分解:↑+222O O 2H 通电O 2H5、碳酸不稳定而分解:↑+===2232CO O H CO H6、高温煅烧大理石或石灰石:↑+23CO CaO 高温CaCO三、还原金属氧化物的几个反应1、几种单质的还原性(置换反应)(1)氢气还原氧化铜:O H Cu ΔCuO H 22++(2)木炭还原氧化铜:↑++2CO 2Cu 高温2CuO C(3)焦炭还原氧化铁:↑++2323CO 4Fe 高温O 2Fe 3C2、化合物的还原性(氧化还原反应)(1)一氧化碳还原氧化铜:2CO Cu ΔCuO CO ++(2)一氧化碳还原氧化铁:2323CO 2Fe 高温O Fe 3CO ++(3)一氧化碳还原四氧化三铁:2434CO 3Fe 高温O Fe 4CO ++四、单质、氧化物、酸、碱、盐的相互转化1、金属单质+酸→盐+氢气(置换反应)(1)锌和稀硫酸:↑+==+2442H ZnSO SO H Zn(2)铁和稀硫酸:↑+==+2442H FeSO SO H Fe(3)镁和稀硫酸:↑+==+2442H MgSO SO H Mg(4)铝和稀硫酸:↑+==+234242H )(SO Al SO 3H 2Al(5)锌和稀盐酸:↑+==+22H ZnCl 2HCl Zn(6)铁和稀盐酸:↑+==+22H FeCl 2HCl Fe(7)镁和稀盐酸:↑+==+22H MgCl 2HCl Mg(8)铝和稀盐酸:↑+==+233H 2AlCl 6HCl 2Al2、金属单质+盐(溶液)→另一种金属+另一种盐(置换反应)(1)铁和硫酸铜溶液反应:44FeSO Cu CuSO Fe +==+(2)铝和硫酸铜溶液反应:3Cu )(SO Al 3CuSO 2Al 3424+==+(3)铜和硝酸银溶液的反应:2Ag )Cu(NO 2AgNO Cu 233+==+3、某些金属氧化物+酸→盐+水(复分解反应)(1)苛性钠暴露在空气中变质:O H CO Na CO 2NaOH 2322+==+(2)苛性钠吸收三氧化硫气体:O H SO Na SO 2NaOH 2423+==+(3)熟石灰在空气中变质:O H CaCO CO Ca(OH)2322+↓==+5、酸+碱→盐+水(复分解反应)(1)盐酸和烧碱(火碱)起反应:O H NaCl NaOH HCl 2+==+(2)盐酸和氢氧化钙反应:O 2H CaCl Ca(OH)2HCl 222+==+(3)氢氧化铝药物治疗胃酸过多:O 3H AlCl Al(OH)3HCl 233+==+(4)硫酸与烧碱反应:O H SO Na 2NaOH SO H 24242+==+6、酸+部分盐→另一种酸+另一种盐(复分解反应)(1)大理石或石灰石与稀盐酸反应:↑++==+2223CO O H CaCl 2HCl CaCO(2)碳酸钠与稀盐酸反应:↑++==+2232CO O H NaCl 2HCl CO Na(3)碳酸氢钠与稀盐酸反应:↑++==+223CO O H NaCl HCl NaHCO(4)硝酸银与稀盐酸反应:33HNO AgCl HCl AgNO +↓==+(5)硫酸与氯化钡溶液反应:2HCl BaSO BaCl SO H 4242+↓==+7、碱+部分盐→另一种碱+另一种盐(复分解反应)(1)氢氧化钠溶液与硫酸铜溶液反应:↓+==+2424Cu(OH)SO Na CuSO 2NaOH (2)氢氧化钙溶液与碳酸钠溶液反应:2NaOH CaCO CO Na Ca(OH)3322+↓==+ (3)熟石灰与氯化铵混合研磨:O 2H 2NH CaCl Cl 2NH Ca(OH)23242+↑+==+8、盐+部分盐→两种新盐(复分解反应)(1)氯化钠溶液和硝酸盐溶液反应:33NaNO AgCl AgNO NaCl +↓==+(2)硫酸钠溶液和氯化钡溶液:2NaCl BaSO BaCl SO Na 4242+↓==+五、其他反应1、碳还原二氧化碳:2CO 高温CO C 2+2、二氧化碳溶于水中:3222CO H O H CO ==+3、生石灰溶于水:22Ca(OH)O H CaO ==+ 放热4、葡萄糖在酶的催化作用下缓慢氧化:O 6H 6CO 酶6O O H C 2226126++。
置换反应(化学)

置换反应(化学)《置换反应知多少》一、概念:一种单质跟一种化合物生成另一种单质和另一种化合物的化学反应实质:氧化还原反应二、置换反应类型:(一)中学常见的置换反应(1)活泼金属与冷水反应置换出氢气。
(2)碳、铁等在高温下与水蒸气反应置换出氢气。
镁与热水反应置换出氢气。
(3)氟气与水反应置换出氧气。
(4)排在金属活动顺序表氢以前的金属与盐酸稀硫酸等置换出氢气(5)较活泼金属与盐溶液反应置换出不活泼金属。
(6)较活泼的非金属与无氧酸或盐溶液置换出不活泼非金属(7)氢气、碳单质与金属氧化物的置换反应(8)碳单质还原SiO2制粗硅。
(9)铝等活泼金属与金属氧化物的反应(10)镁与CO2的置换反应。
(二)按元素在周期表的位置1、同周期元素之间的置换第二周期:如2F2+2H2O= 4HF+O2第三周期:如Cl2+H2S=2HCl+S2、同主族元素之间的置换第ⅠA族:如2Na+2H2O=2NaOH+H2↑第ⅣA族:如SiO2+2C== Si+2CO↑第ⅥA族:如O2+2H2S=2H2O+2S第ⅦA族:如Cl2+2KBr=2KCl+Br23、不同主族元素单质间的置换Mg+2HCl=MgCl2+H2 ↑ 2Al+6HCl=2AlCl3+3H2 ↑2Mg+CO2 ==2MgO+C 2F2+2H2O= 4HF+O2C+H2O==CO+H2Cl2+H2S=2HCl+S3Cl2+8NH3=6NH4Cl+N24、过渡金属参与的置换Fe+CuSO4 =FeSO4+CuH2+CuO=Cu+H2O 2Al+Fe2O3==Al2O3+2Fe3Fe+4H2O(g)==Fe3O4+4H2Zn+2HCl= ZnCl2+H2 ↑Cu+2AgNO3=Cu(NO3)2+2Ag(三)按单质的类别1、金属单质置换金属单质2Al+Fe2O3==Al2O3+2FeFe+CuSO4 =FeSO4+Cu2、金属单质置换非金属单质2Na+2H2O=2NaOH+H2↑3Fe+4H2O(g)==Fe3O4+4H2Zn+2HCl= ZnCl2+H2 ↑2Mg+CO2 ==2MgO+C2Al+Fe2O3==Al2O3+2Fe 3、非金属单质置换金属单质H2+CuO=Cu+H2OC+FeO==Fe+CO4、非金属单质置换非金属单质2F2+2H2O= 4HF+O2Cl2+H2S=2HCl+SCl2+2KI=2KCl+I23Cl2+8NH3=6NH4Cl+N2 (四)按化合物类别1、氧化物参加:2Mg+CO2 ==2MgO+CSiO2+2C==Si+2CO↑H2+CuO=Cu+H2O 2Al+Fe2O3==Al2O3+2Fe 2、水参加:3Fe+4H2O(g)==Fe3O4+4H22Na+2H2O=2NaOH+H2↑C+H2O==CO+H22F2+2H2O= 4HF+O2Mg+2H2O=Mg(OH)2+H2↑3、酸参加:Mg+2HCl= MgCl2+H2 ↑Cl2+H2S=2HCl+S↓Cl2+2HBr=2HCl+Br24、盐溶液参加:Fe+CuSO4 =FeSO4+CuBr2+2KI=2KBr+I2Cl2+Na2S=2NaCl+S↓三、高考题中的置换反应1、(2006年全国理综I卷—27)置换反应的通式可以表示为:单质(1)+化合物(2)=单质(2)+化合物(2)请写出满足以下要求的3个置换反应的化学方程式:(1)所涉及的元素的原子序数都小于20;(2)6种单质分属于6种不同的主族 2、(2006年全国理综II卷—28)以下一些氧化物和单质之间可以发生如下图所示的反应:其中,氧化物(I)是红棕色固体,氧化物(II)、(III)、(IV)在反应条件下都是气体。
置换反应详细资料大全

置换反应详细资料大全置换反应是单质与化合物反应生成另外的单质和化合物的化学反应,是化学中四大基本反应类型之一,包括金属与金属盐的反应,金属与酸的反应等。
它是一种单质与一种化合物作用,生成另一种单质与另一种化合物的反应。
氧化还原反应不一定为置换反应,置换反应一定为氧化还原反应。
基本介绍•中文名:置换反应•外文名:Single Displacement reaction•类型:无机化学反应•反应公式:AB+C→A+BC•是否放热:部分放热,部分吸热•注意点:必须根据金属活动性顺序表发生基本介绍,反应的吸热与放热,反应类型,根据反应环境分类,根据元素性质分类,根据元素周期表中位置分类,根据物质类别分类,金属活动性顺序表,反应现象,基本介绍置换反应可表示为A+BC=B+AC 或AB+C=AC+B,通常认为置换反应都是氧化还原反应,但是一些特殊的反应,例如金属羰基化合物间的置换,则不是氧化还原反应。
置换反应除此之外,也可以指路易斯酸间的置换反应,此时并不需要单质参与反应。
(出处:高等教育出版社的《无机化学》(第四版)下册第460页正文第3行:“……能将另一个较弱的路易斯酸MnF4从稳定配离子[MnF6] 2-的盐中置换出来”)反应的吸热与放热1、放热的反应(1)金属和酸发生的置换反应(2)金属和盐发生的置换反应(3)铝和金属氧化物发生的置换反应(4)活泼金属和水的置换反应2、吸热的反应(1)不太活泼的金属和水蒸气发生的置换反应(2)碳、氢气还原金属氧化物的反应(3)碳和水蒸气的置换反应反应类型根据反应环境分类根据反应环境的类别,置换反应有以下2种情况:(1)固态置换在加热或高温条件下固体与固体或固体与气体发生的置换反应。
(2)液态置换在水溶液中进行的置换反应。
1、金属跟酸的置换:金属原子与酸溶液中氢离子(H+)之间的反应特别注意:(1)不能用浓硫酸,硝酸等有强氧化性的酸,它们反应时,先将金属氧化成对应氧化物,氧化物再溶于酸中,然后继续氧化、溶解,反应得以继续。
置换反应、氧化反应、还原反应和复分解反应

置换反应、氧化反应、还原反应和复分解反应全文共四篇示例,供读者参考第一篇示例:一、置换反应:置换反应是一种化学反应类型,其中一个元素或原子团取代了另一个元素或原子团。
置换反应的一般形式为:A + BC -> AC + B。
在这种类型的反应中,A取代了B;A和B可能是原子,也可能是原子团。
置换反应可以分为单一置换反应和双重置换反应。
铜与氯气反应生成氯化铜的方程式为:Cu + Cl2 -> CuCl2。
二、氧化反应:氧化反应是一种氧原子或氧分子与其他物质发生化学反应的过程。
在氧化反应中,一种物质失去电子,而另一种物质获得电子。
氧化反应可以非常剧烈,例如发生火灾或爆炸。
一个普遍的氧化反应是金属氧化成金属氧。
氧化反应的一般形式为:A + O2 -> AO。
铁与氧气反应生成氧化铁的方程式为:4Fe + 3O2 -> 2Fe2O3。
三、还原反应:四、复分解反应:总结:置换反应、氧化反应、还原反应和复分解反应是化学反应的四种基本类型。
这些反应在化学领域中起着至关重要的作用,帮助我们理解不同元素之间的化学性质和反应规律。
通过研究这些反应,我们可以更深入地了解化学反应的机理和过程,为化学领域的发展做出贡献。
希望大家能够在学习化学的过程中深入研究这些反应类型,提高对化学知识的理解和掌握。
第二篇示例:置换反应、氧化反应、还原反应和复分解反应是化学反应中常见的几种类型。
这些反应在化学实验室和工业生产中起着重要作用,我们今天就来详细讨论一下这几种反应的定义、特点和实际应用。
首先我们来讨论置换反应。
置换反应是一种化学反应,其中一个化合物中的原子或原子团被另一个原子或原子团取代,形成新的化合物。
置换反应可以分为两种类型:单一置换反应和双置换反应。
在单一置换反应中,一个原子或原子团取代了另一个原子或原子团,而在双置换反应中,两个化合物发生原子或原子团的置换。
一个经典的例子是铜和银的置换反应:Cu + 2AgNO3 → Cu(NO3)2 + 2Ag这个反应中,铜取代了银的位置,形成了铜(II)硝酸盐和银。
初中化学反应类型总结及规律

初中化学反应类型总结及规律一、基础知识(一)化学反应类型1、按照反应物与生成物的种类, 可把化学反应分为四种基本反应类型:化合反应、分解反应、置换反应和复分解反应。
(1)化合反应:由两种或两种以上的物质生成另一种物质的反应。
①金属与非金属的化合反应。
例如:2Na + Cl2点燃2NaCl 3Fe + 2O2点燃Fe3O4②非金属跟非金属的化合反应。
例如:4P + 5O2点燃2P2O5H2 + Cl2点燃2HCl③某些碱性氧化物跟水的化合反应。
例如:CaO + H2O == Ca(OH)2 Na2O + H2O == 2NaOH ④某些酸性氧化物跟水的化合反应。
例如:CO2 + H2O == H2CO3SO3 + H2O == H2SO4⑤酸性氧化物跟碱性氧化物的化合反应。
例如:SiO2 + CaO 高温CaSiO3MgO + SO3 == MgSO4⑥多种物质之间的化合反应。
例如:2Cu + O2 + CO2 + H2O == Cu2(OH)2CO3CaCO3 + CO2 + H2O == Ca(HCO3)2 (2)分解反应:由一种物质生成两种或两种以上其它物质的反应。
①某些氧化物的分解反应。
例如:2H2O 通电2H2↑+ O2↑2HgO∆2Hg + O2↑②某些含氧酸的分解反应。
例如:H2CO3 == H2O + CO2↑2HClO 光照2HCl + O2↑(次氯酸)③难溶性碱的分解反应。
例如:Cu(OH)2∆CuO + H2O 2Fe(OH)3∆Fe2O3 + 3H2O④某些含氧酸盐的分解反应。
例如:CaCO3高温CaO + CO2↑2KMnO4∆K2MnO4 + MnO2 + O2↑(3)置换反应:由一种单质跟一种化合物起反应, 生成另一种单质和另一种化合物的反应。
①金属与酸的置换反应。
例如:Zn + 2HCl == ZnCl2 + H2↑Fe + H2SO4(稀) == FeSO4 + H2↑②金属与盐溶液的置换反应。
初三化学:化学反应基本类型

初三化学:化学反应基本类型
①化合反应:A+B+...=C多变一的反应(符合绿色化学要求)
②分解反应:A=B+C+... 一变多的反应
**分解反应前后元素的化合价发生改变
.......。
③置换反应:A+BC=AC+B一单换一单的反应
**溶液里的置换反应必须符合金属活动性顺序:
金属活动性顺序由强至弱: K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
(按顺序背诵)钾钙钠镁铝锌铁锡铅(氢)铜汞银铂金
*金属位置越靠前的活动性越强,越易失去电子变为离子,反应速率越快
*排在前面的金属,能把排在后面的金属从它们的盐溶液里置换出来。
排在后面的金属跟排在前面的金属的盐溶液不反应。
注意:1、单质铁在置换反应中总是变为+2价的亚铁
2、等质量金属跟足量酸反应,放出氢气由多至少的顺序按相对原子质量/化合价由小到大排列:Al(9)>Mg(12)>>Fe(28)>Zn(32.5)
④复分解反应:两种化合物相互交换成分,生成另外两种化合物的反应,
**复分解反应前后各元素和原子团的化合价都保持不变
........。
**注意事项:复分解反应能否发生,要考虑是否有沉淀、气体或水生成。
有沉淀生成的反应中,反应物中不能有难溶于水的物质。
初中化学只有碳酸盐跟酸反应和碱溶液与铵盐反应有气体生成
中和反应:酸跟碱作用生成盐和水的反应。
中和反应属于复分解反应。
第1 页共1 页。
初三化学方程式总结按反应类型

初三化学方程式总结化学反应基本反应类型(四种):化合反应(A+B→C)、分解反应(A→B+C)、置换反应(AB+C→BC+A)、复分解反应(AB+CD→AD+BC),复分解反应条件:沉淀、气体、水。
一、化合反应1、镁条燃烧:2Mg + O2点燃2MgO现象:发出耀眼的白光、放出热量、生成白色粉2、铝在空气中生成致密氧化膜,铝在空气中不容易生锈的原因:4Al + 3O22Al2O33、细铁丝在纯氧中燃烧:3Fe + 2O2点燃Fe3O4剧烈燃烧火星四射、放出热量、生成黑色固体。
4、铜丝加热变黑:2Cu + O2△2CuO 现象:铜丝变黑。
5、硫燃烧:S + O2点燃SO2现象:在纯氧中明亮的蓝紫火焰、生成一种有刺激性气味的气体。
6、红磷燃烧:4P + 5O2点燃2P2O5 现象:发出白光、放出热量、生成大量白烟。
7、氢气燃烧:2H2+ O2点燃2H2O现象:产生淡蓝色火焰、放出热量、烧杯内壁有水雾。
8、一氧化碳燃烧:2CO + O2点燃2CO29、碳完全燃烧:C + O2点燃CO2现象:发出白光、放出热量、澄清石灰水变浑。
10、碳不完全燃烧:2C + O2点燃2CO11、二氧化碳气体通过炽热的碳层:C + CO2高温2CO12、水和某些非金属氧化物反应,水和二氧化碳气体反应制汽水:CO2 + H2O === H2CO313、水和某些金属氧化物反应,水和生石灰反应制熟石灰:CaO + H2O === Ca(OH)2二、分解反应1、高锰酸钾制取氧气:2KMnO4△K2MnO4 + MnO2 + O2↑2、过氧化氢制取氧气:2H2O MnO2 2H2O+ O2↑3、氯酸钾制取氧气:2KClO3MnO2 2KCl + 3O2 ↑4、水通电分解:2H2O 通电2H2↑+ O2 ↑5、碳酸不稳定分解:H2CO3=== H2O + CO2↑6、煅烧石灰石:CaCO3=== CaO + CO2↑三、置换反应1、碳还原氧化铁:3C+ 2Fe2O3高温4Fe + 3CO2↑2、碳还原氧化铜:H2 + CuO 高温Cu + H2O3、铁丝放入稀盐酸溶液中:Fe + 2HCl=== FeCl2 + H2↑ 有气泡产生,溶液由无色变成浅绿色。
高中化学22种置换反应类型及其意义

1、VIIA元素之间的置换反应说明:F2太活泼,不与其它卤素的盐溶液发生置换反应。
①.氯气与其它卤素盐溶液发生的置换反应:Cl2+2KBr=2KCl+Br2;Cl2+2KI=2KCl+I2②.溴单质与其它卤素盐溶液发生的置换反应:Br2+2KI=2KBr+I2③.氯气与其它氢卤酸溶液发生的置换反应:Cl2+2HBr=2HCl+Br2;Cl2+2HI=2HCl+I2④.溴单质与其它氢卤酸溶液发生的置换反应:Br2+2HI=2HBr+I2意义:根据置换反应判断得出氧化性顺序为:Cl2 >Br2>I2;还原性顺序:I- >Br- >Cl-。
2、VIA元素之间的置换反应①.氧气与氢硫酸的置换反应:O2+2H2S=2H2O+2S↓意义:氧化性:O2 >S;还原性:H2S>H2O 。
3、VIIA元素的单质与VIA元素的氢化物之间的置换反应:①.氟气与水的反应:2F2+2H2O=4HF+O2↑,意义:氧化性:F2 >O2,还原性:H2O>HF②.氢硫酸与卤素单质〔氟气除外〕发生的置换反应:Cl2+H2S=2HCl+S↓;Br2+H2S=2HBr+S↓;I2+ H2S=2HI+S↓意义:氧化性:Cl2>Br2>I2>S;还原性:H2S>HI>HBr>HCl 。
4、VIIA元素的单质与V A元素的氢化物之间的置换反应:2NH3+3Cl2=N2+6HCl氧化性:Cl2 >N2;还原性:NH3 >HCl。
5、VIA元素的单质与V A元素的氢化物之间的置换反应:3O2〔纯〕+4NH3点燃2N2+6H2O;N2H4+ O2点燃2N2+2H2O氧化性:O2 >N2;还原性:NH3 >H2O。
6、IV A元素之间的置换反应:2C+SiO2高温2CO↑+Si。
意义:用焦炭与石英在高温下反应制备粗硅。
7、IV A元素的单质与IB元素的氧化物的置换反应:C+2CuO加热CO2+2Cu意义:碳还原氧化铜制备铜。
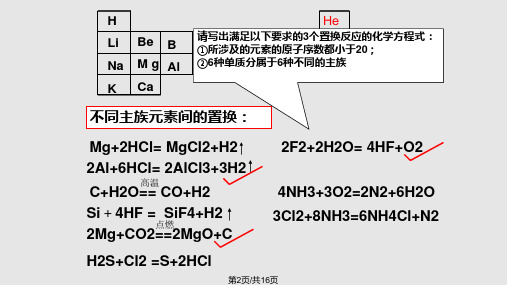
请写出满足以下要求个置换反应化学方程式所涉.pptx
第12页/共16页
返回
金属置换非金属
1、活泼金属置换水或酸中的氢(H+)、醇、酚羟基中的氢
2Na+2H2O=2NaOH+H2↑ 2Na+2CH3CH2OH=2CH3CH2ONa+H2↑ Fe+2HCl=FeCl2+H2↑ Mg+2HCl=MgCl2+H2 2Al+6HCl=2AlCl3+3H2
2 、镁置换CO22中M的g碳+:CO2=点=燃==2MgO+C
H Li Be B Na M g Al K Ca
He
C请 ①写 所出 涉满 及N足 的以 元下素O要的求原的子F 序3个数置N都换e小反于应2的0;化学方程式: S②i6种单P质分属S于6种C不l同的A主r族
不同主族元素间的置换:
Mg+2HCl= MgCl2+H2
2Al+6HCl= 2AlCl3+3H2
(3)若甲,乙均为氧化物,其中甲常温下为气态, 乙是常温下
为固态,则X为 Mg Y为 C
Z为 ____O_2_________
第5页/共16页
同族置换
注意Y 的状态
(4)若甲,乙均为氧化物,其中X常温下为固态, Y常温下为气
态,则X为
晶体(填晶体类型),乙为
氧化物
(选填“酸性”,“碱性” ,“两性”,“不成盐”)
常温下为固体的氧化 物:一般为金属氧化 物,非金属氧化物有:
SiO2、SO3
(化1学)方若程乙式2是H__水2_S_,_+_XO_,_2_Y_点=是_=燃_同_2_S族+元2H素2的O单质,C写+出HX2与O甲高=温=的C反O应+H2
(2)若甲是水,写出甲与X反应的化学方程式方程式_________
