重组蛋白表达系统的选择
细菌的重组蛋白质表达系统

细菌的重组蛋白质表达系统蛋白质是构成生物体及细胞的重要组成部分,也是细胞功能的核心执行者。
为了研究和应用不同类型的蛋白质,科学家发展出了各种蛋白质表达系统。
其中,细菌的重组蛋白质表达系统是最常用的一种方法之一。
本文将详细介绍细菌重组蛋白质表达系统的原理、优势和应用。
一、原理细菌重组蛋白质表达系统利用细菌作为宿主来表达外源蛋白质。
这个系统主要包括以下几个重要组成部分:表达载体、宿主菌株、诱导系统和纯化方法。
1. 表达载体表达载体是指带有外源蛋白质编码序列的质粒。
这些质粒通常包括启动子、反义密码子和终止子等参与蛋白质表达的元件。
其中,启动子通过结合转录因子来启动蛋白质合成的过程。
反义密码子则能够增强蛋白质的长效稳定性,并促进其在细菌中的高效表达。
2. 宿主菌株宿主菌株在蛋白质表达系统中起到重要的作用,通常选择大肠杆菌作为宿主,主要因为大肠杆菌具有较高的生长速度、易于培养和常用的遗传工具。
此外,大肠杆菌本身产生的内切酶活性较低,有利于保护外源蛋白质的稳定性。
3. 诱导系统诱导系统是细菌重组蛋白质表达系统中的一个重要组成部分。
通常使用化学诱导或者温度诱导来启动表达载体中蛋白质编码序列的转录和翻译。
化学诱导通常通过添加一种诱导剂,如异丙基-β-D-硫代半乳糖苷(IPTG),来激活载体中的启动子。
温度诱导则是通过改变培养温度来调节蛋白质表达。
4. 纯化方法纯化是细菌重组蛋白质表达系统中最关键的环节之一。
常用的纯化方法包括亲和纯化、碳水化合物基负载层析和凝胶过滤等。
这些方法能够根据蛋白质的特性和亲和性实现高效纯化。
二、优势与其他蛋白质表达系统相比,细菌重组蛋白质表达系统具有以下优势:1. 高效性细菌重组蛋白质表达系统是目前各种表达系统中最高效的一种方法之一。
通过优化表达条件和使用高效的诱导系统,可以实现高产量的蛋白质表达。
此外,细菌本身的生长速度也有助于高效表达。
2. 便捷性相比其他表达系统,细菌重组蛋白质表达系统的操作更为简便。
重组蛋白的表达系统(详细版)

整理版ppt
20
2.1 常用酵母表达系统(宿主-载体系统)
• 3.1.1 酿酒酵母(Saccharomyces cerevisiae)表 • 由达于系遗统传和生理背景清楚而且安全,酿酒酵母是
最早应用于重组蛋白表达的酵母宿主菌。
• 表达菌株:
• INVSC1是酿酒酵母表达系统的常用菌株,它是一
种双倍体营养缺陷细胞株,在缺少组氨酸、亮氨
• 强启动子中,tac和trc是lac启动子的变体, 其重组蛋白产率能够达到细胞总蛋白量的 15-30%。araBAD启动子的诱导剂是便宜无 毒的L-阿拉伯糖,本底表达量低,启动能力 比tac稍弱。T7则是目前原核表达系统中最 高效的启动子,pET表达系统即是以它为中 心构建的。T7启动子整理版来ppt 源于λ噬菌体,专一 9
• 当重组蛋白不表达时:
• 如果重组蛋白不表达(包含体和可溶蛋白
都没有),首先检查cDNA和质粒是否正确,
蛋白对宿主菌是否有很大毒性,然后尝试
更换菌株、质粒载体和融合标签。原核蛋
白在大肠杆菌中不能表达的情况很少见,
通常是真核蛋白不能表达。不能表达的重
组蛋白,即使在更换了宿主、载体后可以
整理版ppt
15
重组蛋白表达系统
• 1.原核表达系统 • 2.酵母表达系统 • 3.昆虫细胞表达系统 • 4.哺乳动物细胞表达系统 • 5.转基因植物表达系统 • 6.转基因动物表达系统 • 7.表达系统的选择
整理版ppt
1
一、 原核表达系统
• 原核表达系统发展完善、流程简单快速、 成本低、产量高,对大部分蛋白来说都值 得一试白。
• 终止子:
• 转录终止子按照是否依赖和不依赖ρ因子的 作用分为两类,这两类终止子均在终止点 前含有一段7-20bp的回文序列。终止子可以 保护mRNA在核外不被降解,显著延长 mRNA的寿命,由此提高重组蛋白的表达量。 但是对于T7系统来说,由于T7 RNA聚合酶 效率极高,宿主中随时都有充足的mRNA以 供翻译,因此大部分在T7系统中表达的重 组蛋白并不在意质粒上是否有终止子,只 有一些自身带有翻译起始信号的外源基因 需要终止子。
重组蛋白质的这些注意事项需牢记

重组蛋白质的这些注意事项需牢记蛋白质是生物体内功能最为广泛的大分子,其结构和功能的调整对于生物体的正常运作至关重要。
重组蛋白质技术在生物医学和生物工程领域得到广泛应用,可以通过改变蛋白质的结构和功能,为生物研究和工业生产提供有力支持。
然而,在进行重组蛋白质的过程中,需要遵守一些注意事项,以确保实验的可靠性和安全性。
第一,合适的表达系统的选择。
在重组蛋白质的过程中,选择适合的表达系统对于蛋白质的表达量和活性至关重要。
常见的表达系统包括大肠杆菌、酵母、昆虫细胞和哺乳动物细胞等。
不同的表达系统具有不同的特点和适用范围,研究人员需要根据自己的实验目的和样品特点选择合适的表达系统。
第二,蛋白质结构的优化。
在进行蛋白质重组之前,研究人员需要对目标蛋白质的结构进行优化。
这可以通过基因工程手段来实现,包括插入或删除特定的氨基酸序列、构建新的融合蛋白等。
优化蛋白质结构可以提高其稳定性、溶解性和抗原性,在后续的表达和纯化过程中更加容易操作。
第三,遗传转化的优化。
在进行蛋白质表达之前,需要将目标蛋白质的基因导入到表达系统中。
这一步骤被称为遗传转化,可以通过多种方法实现,包括电转化、热激转化、化学转化等。
研究人员需要根据表达系统的要求选择合适的遗传转化方法,并进行优化,以提高蛋白质的表达水平和活性。
第四,适当的培养条件的控制。
在蛋白质表达过程中,适当的培养条件对于蛋白质的表达量和活性至关重要。
这包括温度、氧气浓度、培养基的成分和pH值等。
研究人员需要对培养条件进行优化,以满足蛋白质的表达需求,并确保培养过程的稳定性和可重复性。
第五,蛋白质纯化的选择和优化。
在蛋白质表达后,需要对其进行纯化,以获得高纯度和高活性的蛋白质样品。
常用的蛋白质纯化方法包括亲和层析、离子交换层析、凝胶过滤层析等。
研究人员需要根据目标蛋白质的特性和实验要求选择合适的纯化方法,并进行优化,以提高纯化效率和纯度。
第六,蛋白质结构和功能的分析。
在获得重组蛋白质样品后,需要对其进行结构和功能的分析,以验证其表达和纯化的有效性。
cho细胞表达重组蛋白方案

CHO (Chinese Hamster Ovary) 细胞是常用的哺乳动物细胞系统,用于表达重组蛋白的研究和生产。
以下是一般性的CHO 细胞表达重组蛋白的方案:
1. 购买表达载体:选择适合的表达载体,可以是质粒或病毒载体。
载体应包含适当的启动子、选择标记等。
2. 转染CHO 细胞:将表达载体导入CHO 细胞中。
转染方法可以选择经典的化学或电穿孔法,也可以选择使用特定的转染试剂或转染仪器。
3. 选择稳定转染株:在转染后,使用适当的选择剂(如抗生素) 处理细胞,以选择稳定表达重组蛋白的细胞株。
可通过单克隆分离等方法筛选和扩增单一细胞克隆。
4. 细胞培养条件优化:优化培养基配方和细胞培养条件,包括温度、pH 值、培养基组分等,以提高重组蛋白的产量和纯度。
5. 表达蛋白的诱导:使用适当的诱导剂或方法,例如添加诱导剂(如甲酪酸) 到培养基中,以启动重组蛋白的表达。
6. 重组蛋白的纯化和分析:通过细胞破碎和不同的纯化步骤(如亲和层析、离子交换层析、凝胶过滤等)从培养基或细胞提取物中纯化目标重组蛋白,并使用适当的分析方法验证表达的蛋白的纯度和功能。
在每个步骤中,需要根据具体的重组蛋白和研究目的进行优化和调整。
此外,合理的培养细胞和操作操作也至关重要,以确保产量和纯度的理想达到。
这些方案的细节将根据具体的实验目的和需要进行个体化定制。
重组表达质粒的构建——原核表达载体选择
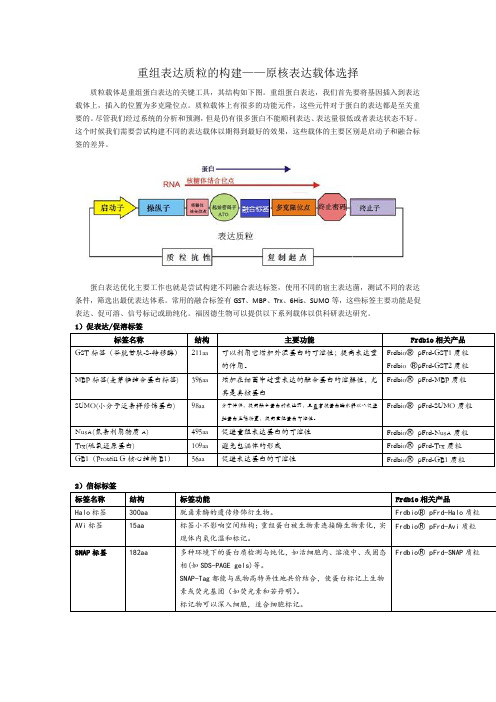
重组表达质粒的构建——原核表达载体选择质粒载体是重组蛋白表达的关键工具,其结构如下图。
重组蛋白表达,我们首先要将基因插入到表达载体上,插入的位置为多克隆位点。
质粒载体上有很多的功能元件,这些元件对于蛋白的表达都是至关重要的。
尽管我们经过系统的分析和预测,但是仍有很多蛋白不能顺利表达、表达量很低或者表达状态不好。
这个时候我们需要尝试构建不同的表达载体以期得到最好的效果,这些载体的主要区别是启动子和融合标签的差异。
蛋白表达优化主要工作也就是尝试构建不同融合表达标签,使用不同的宿主表达菌,测试不同的表达条件,筛选出最优表达体系。
常用的融合标签有GST、MBP、Trx、6His、SUMO等,这些标签主要功能是促表达、促可溶、信号标记或助纯化。
福因德生物可以提供以下系列载体以供科研表达研究。
1)促表达/促溶标签2)信标标签3)纯化标签我们选择表达载体的时候不但要考虑蛋白怎么表达成功,更要考虑蛋白怎么纯化出来,纯化的问题主要是考虑纯化标签和酶切位点的选择,下表我们列举了常见的纯化标签和酶切位点。
4)酶切位点以上为原核表达常用的标签和酶切位点,其性质也都作了简要的介绍,各专业网站或专业书籍已对此做详尽解释,科研工作者可根据具体实验设计方案,组合设计以上标签和酶切位点的使用。
特别值得注意的是,选用和设计蛋白酶切位点的时候首要考虑的是序列内部有没有蛋白酶位点,同时要考虑酶切的效率和蛋白酶试剂成本。
一般商业化载体,在标签蛋白与载体多克隆位点之间都设计有酶切位点。
标签可设计在N-端也可在C-端,设计在N-端的优势是,可通过标签高效翻译起始位点带动插入蛋白的表达,可溶性标签的高效表达更可促进蛋白的可溶性表达;同时,大部分的蛋白内切酶的切割位点在C-端,所以标签设计在N-端可将标签切割完全。
在设计标签序列与酶切位点的时候还要考虑N-端稳定性原则,也就是所谓宿主细胞的N-端规则(N-end rule),这个要避免;同时,还应该检查是否引入了可与别的蛋白相互作用的序列或者蛋白酶切位点。
如何选择合适的蛋白表达系统

如何选择合适的蛋白表达系统?金开瑞拥有原核/真核/无细胞等六大重组蛋白表达系统,提供从基因合成到蛋白表达的一站式蛋白服务,并通过表达载体的改造和实验流程的优化,可在最短时间获得最高的产量,满足您的各项需求。
目前,金开瑞已成功为全球各地客户提供3000余种重组蛋白产品,涵盖人类疾病相关蛋白(细胞因子、激素、酶、病毒抗原)、动植物和微生物蛋白等。
根据您所需要表达蛋白的特点,可选择合适的表达系统:真核酵母细胞经济高效,放大培养基廉价、培养条件简单、生产迅速、可拓展性强、分泌蛋白或细胞内表达的良好选择、蛋白分泌高效且允许简单纯化、广泛的翻译后修饰、无内毒素工业菌种改良、放大自行改造的高效分泌载体和宿主组合,可在最大程度上实现最高质量的蛋白表达;专利的Biobrick技术,可成功用于工业菌种的改良优化杆状病毒-昆虫细胞基因容量大,外源基因表达效率高,有效的细胞折叠、中度可扩展性、广泛的翻译后修饰、糖基化与哺乳动物细胞类似、相对容易地酶促的去糖基化、无内毒素病毒疫苗、信号蛋白、细胞因子、激酶等采用AcNPV-sf9细胞和BmNPV-BmN细胞两种表达系统,多表达系统、多宿主、多载体的选择性极大的提高了蛋白表达的成功率哺乳动物细胞较高的表达水平、中度的可扩展性、细胞的悬浮培养特性可大规模生产、有效的蛋白折叠、适合分泌蛋白、充分的翻译后修饰、无内毒素复杂高等真核生物蛋白采用特有的哺乳动物细胞表达载体和多种转染方法的组合方式,优化表达条件,提高转染效率,大大缩短实验周期,显著提高表达量。
重组蛋白质的表达与纯化技术

重组蛋白质的表达与纯化技术蛋白质是生命体活动的重要组成部分,对于生命体的生长、繁殖和免疫功能起着至关重要的作用。
而重组蛋白质则是利用基因工程技术,将人工合成的外源基因导入到特定的宿主细胞中,通过细胞表达和纯化技术得到的转录翻译产物。
这种技术不仅可以生产天然蛋白质,还可以生产人工合成的新型蛋白质,对于疾病的治疗和新药的研发有着重要的意义。
一、蛋白质表达技术蛋白质表达是获得大量重组蛋白质的重要方法。
选择适当的宿主细胞和表达载体是获得高水平表达的关键。
常用的宿主细胞包括大肠杆菌、酵母菌、昆虫细胞、哺乳动物细胞等。
1.大肠杆菌表达系统大肠杆菌表达系统具有生长快、表达量高等优点,广泛应用于重组蛋白质的表达和纯化。
其表达载体主要有pET和pBAD两种,pET系统一般用于产生可以形成包涵体的重组蛋白,pBAD系统用于在分泌表达中产生滞留蛋白。
2.昆虫细胞表达系统昆虫细胞表达系统包括SF9、Sf21、HighFive等细胞系,常用的表达载体为pIB/V5-His、pFastBac等。
昆虫细胞表达系统通常用于表达大分子蛋白质,如糖蛋白、膜蛋白等。
3.哺乳动物细胞表达系统哺乳动物细胞表达系统是目前表达规模最大、表达产物最接近人体蛋白质的一种表达系统。
其表达载体主要有pCDNA3.1、pCI 等,常用于表达与人体有关的蛋白质,如抗体、生长因子等。
二、蛋白质纯化技术蛋白纯化是重组蛋白质生产的重要环节,其目的是得到高质量的、纯度较高的蛋白质样品。
常见的纯化方法包括亲和层析法、离子交换层析法、凝胶过滤层析法、逆流式层析法等。
1.亲和层析法亲和层析法是指因与载体中固定的亲和剂相互结合而纯化目标蛋白质的一种方法。
亲和剂通常是与目标蛋白质有特异性结合作用的化合物,如亲和标签、酶底物、抗体等。
常见的亲和层析方法有亲和柱层析、亲和膜层析等。
2.离子交换层析法离子交换层析法是根据蛋白质带有正或负电荷的差异性进行分离的一种方法。
离子交换层析的柱填充物常为离子交换树脂,其一般分为阴离子交换树脂和阳离子交换树脂两种。
重组蛋白的大量表达

一、原理
1、E . coli 表达系统
E . coli 是重要的原核表达体系。
在重组基因转化入E . coli 菌株以后,通过温度的控制,诱导其在宿主菌内表达目的蛋白质,将表达样品进行SDS-PAGE 以检测表达蛋白质。
2、外源基因的诱导表达
提高外源基因表达水平的基本手段之一,就是将宿主菌的生长与外源基因的表达分成两个阶段,以减轻宿主菌的负荷。
常用的有温度诱导和药物诱导。
本实验采用异丙基硫代-β-D-半乳糖昔(IPTG)诱导外源基因表达。
不同的表达质粒表达方法并不完全相同,因启动子不同,诱导表达要根据具体情况而定。
二、步骤
1、一活:从-80℃取菌株,50 mL LB+50 uL抗生素(pet32:AMP,pet28:Kana)+50uL菌种(根据菌活性可多加),置于恒温振荡器中(37℃,150 rpm)培养过夜(约12 小时)。
2、二活:1 L LB+1 mL抗生素+50mL菌种,于恒温振荡器上(37℃,200 rpm)培养2小时。
3、取1.5 mL诱导前菌种,标记,加1 mL IPTG至二活后的LB培养基中根据相应条件诱导表达(低温(125rpm),高温(150rpm),8h,12h,20h)
4、诱导后取1.5mL菌,12000rpm离心2min,弃上清,加100uL PBS(可根据情况加50uL),吹打均匀(诱导前保留的菌也同样处理),煮样,跑电泳。
利用原核和真核系统在重组蛋白质表达中的比较

利用原核和真核系统在重组蛋白质表达中的比较当今生物科学领域中,蛋白质表达技术的发展一直备受关注。
利用原核和真核系统来重组蛋白质,是常见的两种方法。
这两种系统在蛋白质表达中有着各自的优势和适用范围。
一、原核系统的蛋白质表达原核系统主要指大肠杆菌(Escherichia coli,简称E.coli)等细菌,并且是最常用的蛋白质表达系统之一。
原核细胞具有复制速度快、易于培养、表达量高等特点,使其成为研究人员的首选。
在原核系统中,通常使用表达载体质粒将目标基因插入到细菌细胞中,并利用细菌自身的转录、翻译系统来实现蛋白质的合成。
在表达载体上,一般包含启动子、转录终止子、选择性标记等功能元件,以控制目标基因的表达和纯化。
原核系统的蛋白质表达具有高效、简便、经济等优势。
然而,由于原核细胞的风险素材含量高,存在内源性的蛋白质翻译后修饰机制有限等局限,某些复杂蛋白质的表达可能会受到限制。
二、真核系统的蛋白质表达真核系统主要指哺乳动物细胞(如CHO细胞)、昆虫细胞(如Sf9细胞)等,相对于原核系统,真核系统具有更接近生物体内蛋白质表达的环境,更能实现复杂蛋白质的表达。
在真核系统中,常用的蛋白质表达包括稳定转染和瞬时转染两种方式。
稳定转染是将目标基因整合到宿主细胞的基因组中,从而实现长期稳定的表达。
而瞬时转染则是将目标基因引入宿主细胞的质粒中,通过短时间高表达来获得大量蛋白质。
真核系统的蛋白质表达能够实现更多的翻译后修饰,如糖基化、磷酸化、乙酰化等。
这些修饰对于某些蛋白质功能的发挥至关重要。
此外,真核细胞中包含更多复杂的蛋白翻译机制和分子伴侣蛋白,有利于蛋白正确折叠和纯化。
然而,真核系统的蛋白质表达过程更为复杂,所需时间和成本也相对较高。
此外,真核细胞具有更严格的质控机制和蛋白降解系统,蛋白质的表达稳定性较差。
三、原核与真核系统的比较原核和真核系统的选择应根据具体的研究目的和需求。
如果目标是表达小分子量、水溶性和结构简单的蛋白质,原核系统是较好的选择。
生物制品考试题及答案

生物制品考试题及答案一、单项选择题(每题2分,共20分)1. 细胞培养中常用的培养基是:A. 肉汤培养基B. 琼脂培养基C. 液体培养基D. 固体培养基答案:B2. 以下哪种物质不属于生物制品?A. 疫苗B. 抗生素C. 化学药品D. 血清答案:C3. 细胞凋亡的英文缩写是:A. PCDB. ADCC. BCDD. NCD答案:A4. 以下哪种细胞器不含膜结构?A. 线粒体B. 内质网C. 高尔基体D. 核糖体5. 基因工程中常用的运载体是:A. 质粒B. 病毒C. 细菌D. 酵母答案:A6. 以下哪种技术不是用于基因克隆?A. PCR技术B. DNA测序C. 电泳D. 转化答案:B7. 重组蛋白的表达系统不包括:A. 原核表达系统B. 真核表达系统C. 植物表达系统D. 动物细胞培养系统答案:C8. 以下哪种细胞是终末分化细胞?A. 干细胞B. 肝细胞C. 肌细胞D. 神经细胞答案:D9. 以下哪种生物制品可用于治疗糖尿病?B. 干扰素C. 红细胞生成素D. 血小板生成素答案:A10. 以下哪种技术用于检测基因突变?A. PCRB. DNA测序C. 基因芯片D. 以上都是答案:D二、多项选择题(每题3分,共15分)1. 以下哪些因素会影响细胞培养?A. 温度B. pH值C. 营养物质D. 氧气供应答案:ABCD2. 以下哪些是生物制品的常见类型?A. 疫苗B. 抗体C. 激素D. 细胞因子答案:ABCD3. 以下哪些是细胞凋亡的特征?A. 细胞体积缩小B. 细胞核凝聚C. 细胞膜破裂D. 细胞内容物释放答案:AB4. 以下哪些是基因工程中常用的工具酶?A. 限制性内切酶B. DNA连接酶C. 反转录酶D. 聚合酶答案:AB5. 以下哪些是重组蛋白表达的影响因素?A. 表达系统B. 启动子C. 密码子优化D. 表达载体答案:ABCD三、填空题(每空1分,共20分)1. 细胞培养的基本原则包括无菌操作、__________和__________。
重组蛋白的表达

重组蛋白的表达1.概述分离纯化组成了基因工程的下游处理(downstream processing)时期,这一过程又和上游过程紧密相联系,上游过程的诸方面阻碍到下游的分离纯化,因此在进行目标蛋白质表达纯化时要统一考虑和整体设计,并充分考虑上游因素对下游的阻碍,如是否带有亲和标签,是否进行分泌表达。
目前应用最广泛的表达系统有三大类,分别是大肠杆菌表达系统、酵母表达系统和CHO细胞表达系统,不同的表达系统和培养方法显著阻碍下游的处理过程,目标蛋白表达是否形成包涵体,目标蛋白表达的定位(胞内、细胞内膜、周质空间和胞外),蛋白表达的量都依靠于所选择的表达系统。
选择将所表达的蛋白分泌到细胞外或周质空间能够幸免破裂细胞的步骤,同时由于蛋白质种类少,目标蛋白容易纯化;而在细胞质内表达蛋白,可能是可溶性表达,可能形成包涵体,可溶性的蛋白往往需要复杂的纯化步骤,而包涵体易于分离,纯度较高,但回收具有生物活性的蛋白却变的相当困难,需要对集合的蛋白进行变复性,通常活性蛋白的得率比较低,表1列出了不同策略对表达、纯化的阻碍,关于其中的有些缺点能够通过一定的方法进行克服和幸免,如利用DNA重组技术给外源蛋白加上一个亲和纯化的标签,有助于可溶性外源蛋白的选择性纯化,并能爱护目标蛋白不被降解(96)。
表 1 重组蛋白不同表达策略的优点和缺点表达策略优点缺点分泌表达至细胞外增强正确二硫键的形成降低蛋白酶对表达蛋白的降解可获得确定的N末端显著减少杂蛋白水平,简化纯化不需要细胞破裂表达水平低多数蛋白不能进行分泌表达表达蛋白需要进行浓缩细胞周质空间表达增强正确二硫键的形成可获得确定的N末端显著减少杂蛋白水平,简化纯化好些蛋白不能分泌进入周质空间没有大规模选择性的开释周质空间蛋白的技术周质蛋白酶可引起重组蛋白酶解胞内包涵体表达包涵体易于分离爱护蛋白质不被降解蛋白质不具有活性对宿主细胞生长没有大的阻碍,通常可获得高的表达水平需要体外的折叠和溶解,得率较低具有不确定N末端胞内可溶性蛋白表达不需要体外溶解和折叠一样具有正确的结构和功能高水平的表达常难以得到需要复杂的纯化可发生蛋白质的酶解具有不确定的N末端在细胞的提取物中,除了目标蛋白外,还含有其它各种性质的蛋白、核酸、多糖等。
重组蛋白的高效表达及纯化技术研究

重组蛋白的高效表达及纯化技术研究随着生物技术的发展,蛋白表达与纯化技术在医疗、工业以及科学研究等领域中扮演着越来越重要的角色。
其中,重组蛋白的高效表达及纯化技术是蛋白质学研究的关键环节之一。
本文旨在探讨目前被广泛应用的几种重组蛋白表达及纯化技术,以及它们的新进展与应用前景。
一、背景介绍重组蛋白指的是通过基因重组技术将人工合成的DNA片段引导到细胞中,使其在受到特定刺激后大量表达特定功能蛋白的一种新型蛋白质。
由于其具有高度专一性、易制备性以及更高的效力和安全性,越来越多的药物被开发为基于重组蛋白的生物制剂。
二、重组蛋白表达技术1. 原核表达系统原核表达系统是将DNA片段导入大肠杆菌等细菌中,在其形成菌落的过程中进行表达。
该系统的优点在于表达速度快、操作简便、表达产量高。
但同时,由于原核表达与真核细胞中的表达相比,它对于蛋白翻译辅助因子和蛋白修饰等生物特征的模拟程度较差,不利于蛋白的正确折叠,因此该系统表达的蛋白质通常需要经过重新折叠处理。
2. 原核表达系统与原核表达系统相比,真核表达系统更接近真实情况中的表达方式,对于全长的蛋白大多数时候能够实现正确的折叠。
在真核表达系统中,常用的系统包括昆虫细胞、哺乳动物细胞以及酵母菌表达系统等。
其中,哺乳动物细胞表达系统能够实现高产量、高质量的蛋白质表达,因此被广泛应用于蛋白质制备。
三、重组蛋白纯化技术1. 亲和层析法亲和层析法是一种将目标蛋白质从混合物中分离出来的技术。
该技术的依据是一种特定的与目标蛋白质具有相互作用的配体分离柱。
在该技术中,目标蛋白质与配体分离柱上的特定功能团结合,非特异性的蛋白质能够在洗脱过程中被去除。
2. 总体分离法总体分离法是将目标蛋白从混合物中分离出来,采用离心、可溶性和非可溶性的分离方法。
其中,在采用可溶性分离的方式时,常用的方法有两相法、分配层析等。
四、新兴技术及应用前景近年来,3D打印技术的应用逐渐渗透到生物医疗领域,并开始用于制备组织工程器官和人造蛋白质等领域。
重组蛋白的表达与纯化技术研究

重组蛋白的表达与纯化技术研究随着基因工程和生物技术的发展,重组蛋白的表达及纯化技术在生物医药领域得到了广泛应用。
重组蛋白是通过将目标基因转移到宿主表达系统中,利用宿主细胞表达并合成特定蛋白的技术。
表达后的蛋白需要经过纯化、鉴定和活性分析,以确保获得高纯度和高活性的蛋白。
本文将介绍重组蛋白的表达与纯化技术研究的相关内容。
重组蛋白表达技术是通过将目标基因克隆到表达载体中,然后将表达载体转入宿主细胞中进行表达。
常用的表达系统包括大肠杆菌、酿酒酵母、昆虫细胞和哺乳动物细胞等。
在选择表达载体时,需要考虑载体的复制数、启动子的强度和宿主细胞的适应性。
而在选择宿主细胞时,需要考虑宿主细胞的生长特性、表达能力以及宿主细胞的酶切位点等因素。
表达载体和宿主细胞的选择将直接影响重组蛋白的表达水平和纯化效果。
在重组蛋白的表达过程中,除了选择适合的表达系统外,还需要优化培养条件和表达工艺。
培养基的组成、培养温度、培养时间、诱导条件等因素都会影响蛋白的表达水平和纯度。
常见的优化方法包括调整培养基的成分、优化培养条件和诱导条件、构建工程菌株以及使用辅助因子等。
通过合理的优化,可以提高蛋白的表达水平和纯度,为后续的纯化工作奠定基础。
重组蛋白的纯化是确保蛋白质高纯度和高活性的关键步骤。
常见的纯化方法包括亲和层析、离子交换层析、凝胶过滤层析、逆流色谱和层流洗脱等技术。
亲和层析是通过目标蛋白与特异性结合剂之间的亲和力选择性地捕获目标蛋白。
离子交换层析是利用蛋白质与带电离子交换剂间的相互作用进行纯化。
凝胶过滤层析则是根据蛋白分子大小进行分离纯化。
逆流色谱和层流洗脱则是利用目标蛋白与静电荷间的相互作用进行分离。
通过合理选择和组合这些方法,可以获得高纯度和高活性的重组蛋白。
在纯化过程中,还需要进行蛋白质的结构鉴定和活性分析。
结构鉴定可以通过质谱分析、核磁共振、X射线晶体学等技术来实现。
活性分析则是通过特定的活性测定方法来验证蛋白的功能和活性。
原核表达系统三大要素的选择及优化
原核表达系统是目前使用最广泛、最完善的重组蛋白表达系统,具有遗传背景清晰、表达周期快、表达量高、成本低等优势,缺点是无法进行蛋白的翻译后修饰,得到具有生物活性蛋白的几率较小。
原核表达系统适用于表达原核来源的蛋白或不需要翻译后修饰的真核来源蛋白。
在原核蛋白表达过程中,需要综合考虑表达菌株、质粒载体、表达条件三大因素,以获得最满意的表达效果。
下面为大家一一介绍这三大因素的选择和优化。
1. 表达菌株菌株的选择往往是大家最容易忽视的,大多数人会选择使用自己实验室有的或用过的表达菌株。
当蛋白表达效果不佳时,大多会在质粒载体或表达条件上找原因,而不会考虑菌株的选择是否合适。
但作为表达宿主,菌株一定会对外源基因表达蛋白产生影响。
图1 大肠杆菌原核表达系统常用的菌株包括大肠杆菌、芽孢杆菌和链霉菌。
其中运用最为广泛的就是大肠杆菌表达系统。
以下为大家列出了一些常用的大肠杆菌表达菌株,可根据不同的需求进行选择。
2. 质粒载体质粒表达载体上的重要元件包括启动子,多克隆位点,终止子,复制子,信号肽,融合标签,筛选标记等。
根据载体上这些元件的特性,有多种质粒可供选择。
图2 大肠杆菌表达质粒pET-22b(+)图谱启动子:根据启动子的强弱考虑,强启动子可以提高蛋白表达量;弱启动子可以降低本底表达、增加可溶表达、表达小量伴侣蛋白等。
根据启动子的作用方式考虑,组成型启动子使宿主不停的表达重组蛋白;诱导型启动子使宿主在特定诱导条件下表达重组蛋白。
终止子:终止子的作用在于保护mRNA在核外不被降解,延长mRNA的寿命,以提高重组蛋白表达量。
对于T7系统来说,由于T7 RNA聚合酶效率非常高,保证一直有充足的mRNA 提供翻译,所以终止子对其影响不大,只有一些自身带有起始密码子的外源基因需要终止子。
~复制子:复制子决定质粒载体拷贝数,拷贝数越高,重组蛋白表达量就越高。
表达载体通常会选用高拷贝的复制子,但过高的拷贝数会影响质粒稳定性和宿主生长。
重组蛋白的表达系统详细版

优化培养条件:优化 培养温度、pH、营养 物质等条件,提高重 组蛋白的表达水平。
开发更高效的亲和层析技术,提高目标蛋白的纯度和回收率。 引入连续层析技术,缩短纯化时间和降低成本。 利用蛋白质结晶技术,提高重组蛋白的结晶效率和纯度。 开发新型的蛋白去垢剂和清洗剂,减少对重组蛋白的损害和污染。
添加标题
添加标题
添加标题
添加标题
常用方法:离心、过滤、沉淀、亲 和层析等
注意事项:避免蛋白降解和活性丧 失
重组蛋白用于蛋白质晶体学研究,解析蛋白质结构 重组蛋白表达系统能够高效表达和纯化蛋白质,提高晶体学研究效率 通过重组蛋白表达系统,可以生产具有生物活性的蛋白质,用于药物筛选和开发 重组蛋白表达系统在蛋白质晶体学研究中具有广泛的应用前景,为生命科学研究提供有力支持
载体构建:选择合适的载体分子,将重组DNA分子插入到载体分子中,形成重组载体。
转化:将重组载体导入受体细胞中,使目的基因在受体细胞中复制和表达。
克隆筛选:通过筛选和鉴定,从众多的转化子中选育出含有目的基因的阳性克隆。
宿主细胞类型:原核细胞、真核细胞、昆虫细胞等 选择依据:表达产物的纯度、表达量、安全性等 转化方法:电击法、化学法、显微注射法等 转化后筛选:抗性筛选、互补筛选等
重组蛋白表达系统用于生产抗 体药物
高效、可重复的抗体药物研发 过程
重组蛋白表达系统在抗体药物 研发中的优势
抗体药物的种类和应用领域
用于研究病毒结构、功能和 传播机制
重组蛋白表达系统在疫苗生 产中的应用
用于开发新型疫苗和治疗策 略
提高疫苗产量和纯度,降低 生产成本
用于研究蛋白质 之间的相互作用, 帮助科学家更好 地理解生命活动 的本质和疾病的
发生机制。
重组蛋白的表达载体和表达方式

什么是重组蛋白?
重组蛋白(recombinant protein)是指应用重组 DNA 或重组 RNA 技术而获得的蛋白质。
重组蛋白工程先应用基因克隆或化学合成技术获得目的基因(gene of interest,GOI),连接到适合的表达载体,导入到特定的宿主细胞,利用宿主细胞的遗传系统,表达出有功能的蛋白质分子。
什么是表达载体?
表达载体(expression vector)是一种可以携带外源基因并在宿主细胞中进行表达的工具,它通常是一种质粒或病毒。
表达载体除了包含外源基因外,还需要包含一些必要的元件,如启动子、终止子、选择标记、筛选标记等。
重组蛋白的表达方式有哪些?
按重组蛋白的表达方式,表达载体大致可分为以下几种:
•单独表达:指目的基因单独编码一个蛋白质,在宿主细胞中以自由形式存在。
这种方式适用于大多数不需要翻译后修饰或结构域相互作用的蛋白质。
•融合表达:指目的基因与其他基因(如伴侣蛋白、纯化标签等)相连接,编码一个含有多个功能区域的融合蛋白,在宿主细胞中
以结合形式存在。
这种方式可以增加目的蛋白的溶解度、稳定性、纯化效率和活性检测等。
•分泌表达:指目的基因与一个信号肽基因相连接,编码一个含有信号肽的前体蛋白,在宿主细胞中经过分泌途径被运输到胞外或胞器内。
这种方式可以避免目的蛋白在胞质中形成包涵体或受到降解酶的作用,也可以实现一些翻译后修饰,如糖基化等。
重组蛋白表达和表征

重组蛋白表达和表征重组蛋白表达和表征随着现代生物技术的发展,重组蛋白技术已经成为了生物学和医学领域的重要研究工具。
通过表达目标蛋白,可以用于研究特定蛋白的结构、功能和作用机制等方面。
本文将着重介绍重组蛋白表达和表征的相关知识。
一、重组蛋白表达重组蛋白表达是指利用现代生物技术手段,将目标蛋白基因克隆入载体并表达出来的过程。
在这个过程中,需要选择一个适合的表达载体并将目标基因插入其中,然后通过合适的表达条件,使得目标蛋白在细胞中得到充分表达。
一般情况下,表达载体可以是大肠杆菌、酵母菌、哺乳动物细胞等不同的表达宿主。
1. 选择表达载体选择适合的表达载体是重组蛋白表达的关键。
不同的表达宿主具有不同的优点和不足。
例如,大肠杆菌表达系统具有高效和简单的操作特点,但是在表达复杂蛋白时容易出现折叠和溶解问题;哺乳动物细胞表达可以在分泌型和细胞内型进行,但是由于表达时间周期长,表达量低等原因,通常用于大规模生产。
2. 克隆目标基因在选定适合的表达载体后,需要将目标基因克隆到载体中。
一般有PCR 扩增、限制性内切酶切割等方法实现。
此外,还需要选择合适的启动子、选择子、标签等元素,以便完成高效稳定的表达。
3. 利用不同表达系统实现重组蛋白表达具体地,可以使用原核表达体系、酵母表达体系、哺乳细胞表达体系及昆虫表达体系等实现重组蛋白表达。
其中,原核表达体系中最常用的是大肠杆菌,酵母表达体系中最常用的是毕赤酵母,而哺乳细胞表达体系中最常用的则是CHO细胞等。
二、重组蛋白表征重组蛋白表征是指对已经表达出来的重组蛋白进行检测、纯化、鉴定等过程。
这个过程中需要采用多种手段,如SDS-PAGE蛋白电泳、Western blot检测、质谱分析、生物活性检测等。
1. SDS-PAGE蛋白电泳SDS-PAGE蛋白电泳是常用的蛋白质分析方法,可以用来确定蛋白分子量、纯度等,以及检查蛋白的电泳性质等。
通过对目标蛋白的去氧核糖核酸和蛋白质的标记,可以检测到蛋白质的表达和纯化情况。
重组蛋白的表达系统

添加 标题
昆虫细胞表达系统:以Sf9和Bm5细胞为代表优点是 能够进行真核翻译后修饰表达的蛋白具有生物活性; 缺点是操作较为复杂且表达量有限。
添加 标题
哺乳动物细胞表达系统:以CHO和HEK293为代表 优点是能够高度模拟真核生物的翻译后修饰表达的蛋 白具有高度生物学活性;缺点是操作复杂成本高且表 达量有限。
宿主细胞的选择与培养
宿主细胞的选择:根据重组蛋白的特性选择适合的宿主细胞如大肠杆菌、酵母、昆虫细胞和哺 乳动物细胞等。
宿主细胞的培育:通过培养基和生长条件的优化提高宿主细胞的生长速率和蛋白表达水平。
宿主细胞的遗传改造:通过基因敲除、基因沉默等技术手段对宿主细胞进行遗传改造以实现重 组蛋白的高效表达。
重组蛋白表达系统的分类
添加 标题
原核表达系统:以大肠杆菌为代表优点是操作简便、 成本低适用于大规模生产;缺点是表达的蛋白缺乏真 核生物特有的翻译后修饰且表达量不稳定。
添加 标题
酵母表达系统:以酿酒酵母和毕赤酵母为代表优点是 能够进行真核翻译后修饰表达的蛋白具有生物活性; 缺点是表达量相对较低且产物大多为包涵体。
宿主细胞的反应条件:通过调节温度、pH、营养物质等反应条件实现对重组蛋白表达过程的精 细控制。
重组蛋白的表达诱导与检测
诱导方法:使用诱导剂诱导目的基因的表达 检测方法:通过免疫印迹法、荧光检测等技术检测目的蛋白的表达情况 目的:验证重组蛋白表达系统的可行性 意义:为进一步研究重组蛋白的结构和功能奠定基础
重组蛋白表达系统的改进方向
优化宿主细胞:选择更合适的宿主细胞以提高重组蛋白的表达水平和产量。 基因工程改造:通过基因工程手段对重组蛋白进行改造以提高其表达效率和稳定性。 添加分子伴侣:利用分子伴侣的作用提高重组蛋白的折叠效率和分泌能力。 开发新型表达系统:不断探索和开发新型的表达系统以克服现有表达系统的限制和不足。
-重组蛋白疫苗的原理

-重组蛋白疫苗的原理
重组蛋白疫苗是通过将病原体特定的蛋白质基因导入表达系统中,利
用表达系统产生的复制病原体表面抗原蛋白质来诱导机体产生刺激免疫应
答的新型疫苗。
其原理大致如下:
1.确定目标蛋白:针对某一种病原体,需要确定其特定的蛋白质。
2.基因克隆:获得并克隆目标蛋白的基因,进行基因测序等操作。
3.表达系统选择:选择一个合适的表达系统来生产目标蛋白,如细菌
表达系统、酵母表达系统、哺乳动物细胞表达系统等。
4.表达目标蛋白:将目标蛋白质的基因导入到表达系统中,促使表达
系统将其转录和翻译成蛋白质。
5.纯化目标蛋白:将表达系统中产生的蛋白质纯化出来,去除杂质。
6.制备疫苗:将纯化的目标蛋白质形成疫苗,如植入或注射到机体中,诱导机体产生针对这种蛋白质的免疫应答。
7.提高免疫性:可添加佐剂等物质提高免疫应答。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
重组蛋白表达系统的选择、表达策略和方法学研究宁1. 前言在生命科学的很多研究和应用领域中,如何获得大量、均一、高纯、有活性的蛋白质都是一个关键问题。
现代重组蛋白表达技术为我们提供了多种选择:传统的大肠杆菌、酵母、昆虫和哺乳动物细胞表达系统以及较新的植物和体外表达系统。
每种表达系统都有很多成功的例子,但重组蛋白的个性不尽相同,没有任何一个系统和方法是普遍适用的,为目的蛋白选择一个恰当的表达系统也就成为表达工作的重中之重。
关于目的蛋白的一切信息,对表达系统的选择都是有帮助的,有几个最基本的问题一定要在表达之前回答清楚:目的蛋白的来源是原核还是真核生物?具有什么样的功能?分子量和聚合状态?是膜蛋白还是水溶蛋白?胞表达还是分泌表达?是否需要以及需要何种翻译后修饰?有没有配体、底物或产物类似物可以利用?对蛋白酶是否敏感?有多少分子及分子间二硫键?对目的蛋白的表达量、活性、表达速度和成本有怎样的要求?除了摸清目的蛋白的脾性,还要清楚各个表达系统的特点、优势和局限性,才能找到表达工作的大略方向,要获得最适合目的蛋白的表达方案,还需要在具体实验中调整优化。
表1比较了目前常用的表达系统的特点,并给出了粗略的适用围。
大肠杆菌酵母昆虫细胞哺乳动物细胞流程简单简单复杂复杂培养基简单简单复杂复杂成本低低中高产率高中中低表达量高高较高较低蛋白折叠中较好较好好胞外表达周质空间分泌至培养基分泌至培养基分泌至培养基细胞增殖周期30min 90min 18H 24H 折叠常有错误折叠偶有不当折叠正确折叠正确二硫键难以形成有有有N-糖基化无甘露糖残基,高无唾液酸,简单复杂O-糖基化无有有有磷酸化无有有有酰化无有有有γ-羧基化无无无有适用原核蛋白、简单真核蛋白真核蛋白、分泌表达蛋白真核蛋白、分泌表达蛋白复杂高等真核生物蛋白表1:常用表达系统比较2. 原核表达系统原核表达系统发展完善、流程简单快速、成本低、产量高,对大部分蛋白来说都值得一试,尤其适宜于表达原核来源的以及不需要翻译后修饰的真核蛋白。
2.1 表达菌株原核表达系统刚用的宿主菌有E. coli,Bacillus等。
其中革兰式阳性的Bacillus更适宜在其周质空间分泌表达重组蛋白;革兰氏阴性的E. coli能够广谱表达异源蛋白。
大肠杆菌表达系统是目前发展最完善的重组蛋白表达系统。
常用大肠杆菌菌株有BL21(DE3)、BL21(DE3)Star、B834(DE3)等,这些菌株都敲除了蛋白酶,并溶源了噬菌体DE3。
DE3是的一种衍生λ噬菌体,带有噬菌体21抗性区和lacI基因,lac UV5启动子,以及T7 RNA聚合酶基因。
这一区段被插入int基因,因此阻止了DE3在没有辅助噬菌体时整合到染色体上或从染色体切出。
一旦形成DE3溶原状态,就只有受IPTG诱导的lac UV5启动子指导T7 RNA聚合酶基因转录,在溶原培养体系中加入IPTG诱导T7 RNA聚合酶生产,继而质粒上的目的DNA开始转录。
同时,还有一些特殊设计的菌株以表达有特殊需要的重组蛋白,如甲硫氨酸营养缺陷型表达硒代甲硫氨酸蛋白,溶解性增强的菌株表达毒性蛋白,补充了稀有密码子的菌株表达真核蛋白等,表2给出了常用的大肠杆菌表达菌株。
常用表达菌株应用抗生素抗性B834 met营养缺陷性,对照株,不能使用T7启动子,蛋白酶敲除无B834(DE3) met营养缺陷性,蛋白酶敲除无BL21 对照株,不能使用T7启动子,蛋白酶敲除无BL21(DE3) 常规表达宿主菌,蛋白酶敲除无BL21(DE3) 高严紧表达宿主菌,蛋白酶敲除氯霉素(34μg/ml)BL21trxB(DE3) 常规表达宿主菌,在E.coli胞质中形成二硫键,蛋白酶敲除卡那霉素(15μg/ml)BL21trxB(DE3)pLysS 高严紧表达宿主菌,在E.coli胞质形成二硫键,蛋白酶敲除卡那霉素(15μg/ml)氯霉素(34μg/ml)Origami 对照株,不能使用T7启动子四环素(12.5μg/ml)卡那霉素(15μg/ml)Origami(DE3) 常规表达宿主菌,更好的在E.coli中形成二硫键四环素(12.5μg/ml)卡那霉素(15μg/ml)Origami(DE3)pLysS 高严紧表达宿主菌,更好的在E.coli中形成二硫键四环素(12.5μg/ml)卡那霉素(15μg/ml)氯霉素(34μg/ml)Rosetta 对照株,不能使用T7启动子,蛋白酶敲除氯霉素(34μg/ml)Rosetta(DE3)常规表达宿主菌,lac透性酶突变,可以控制表达水平,提供稀有密码子tRNAs,蛋白酶敲除氯霉素(34μg/ml)Rosetta(DE3)pLysS 高严紧表达宿主菌,lac透性酶突变,可以控制表达水平,提供稀有密码子tRNAs,蛋白酶敲除氯霉素(34μg/ml)Rosetta-gami 对照株,不能使用T7启动子四环素(12.5μg/ml)卡那霉素(15μg/ml)氯霉素(34μg/ml)Rosetta-gami(DE3) 常规表达宿主菌,更好的在E.coli胞质形成二硫键,提供稀有密码子tRNAs四环素(12.5μg/ml)卡那霉素(15μg/ml)氯霉素(34μg/ml)Rosetta-gami(DE3)pLysS高严紧表达宿主菌,更好的在E.coli胞质形成二硫键,提供稀有密码子tRNAs四环素(12.5μg/ml)卡那霉素(15μg/ml)氯霉素(35μg/ml)表2:常用E. coli表达菌株2.2 质粒载体:大肠杆菌表达系统采用质粒为表达载体,质粒上的重要元件包括复制子,启动子,终止子,多克隆位点,信号肽,融合标签,筛选标记等(图1)。
原核表达载体已经发展得比较完善,有多种质粒可供选择(表4)。
复制子:复制子决定着质粒载体在宿主中的拷贝数。
通常情况下质粒拷贝数越高,重组蛋白的表达量就越高,但是高拷贝的质粒也会严重影响宿主的生长,质粒本身也不稳定,容易丢失和突变。
克隆载体常采用拷贝数低、严谨复制的复制子,如pSC101;表达载体通常选用高拷贝的复制子,如pCoE1,pMBI(pUC),等。
如果需要进行多个质粒的共转化,就要根据复制子的相容性选用不同复制系统的复制子,如pSC101和pUC共表达。
启动子:表达重组蛋白时,我们需要考虑启动子的强弱、作用方式、调控方式和本底表达水平。
表达载体通常选用强启动子以提高表达量,但弱启动子也有其优点,如降低本底表达、增加可溶表达、表达小量伴侣蛋白等。
按照作用方式,启动子可以分为两类:组成型表达的启动子使宿主不停地表达重组蛋白,常用于工业生产,如σS等;诱导型表达的启动子使宿主仅在受到诱导(诱导剂、温度等)时表达目的蛋白,诱导型启动子使重组蛋白的表达容易控制,同时降低了外源蛋白对细菌生长的影响。
图1:大肠杆菌表达质粒pET-22b(+)图谱及多克隆位点早期大肠杆菌表达体系中,常见的启动子是lac和lac UV5。
lac是一个弱启动子,很难使外源基因得到高表达。
目前使用的含有需要小量共表达的蛋白(如分子伴侣,蛋白抑制剂等)的载体,有很多都采用了经典的lac启动子。
强启动子中,tac和trc是lac启动子的变体,其重组蛋白产率能够达到细胞总蛋白量的15-30%。
araBAD启动子的诱导剂是便宜无毒的L-阿拉伯糖,本底表达量低,启动能力比tac 稍弱。
T7则是目前原核表达系统中最高效的启动子,pET表达系统即是以它为中心构建的。
T7启动子来源于λ噬菌体,专一与T7启动子结合的T7 RNA聚合酶则被整合在宿主菌的基因组中。
在λ噬菌体溶源的表达宿主菌,如BL21(DE3)中,lacI抑制T7 RNA聚合酶的表达,IPTG的加入可以解除这种抑制。
当受到诱导时,T7 RNA聚合酶开始表达并结合在T7启动子上,启动重组蛋白的表达。
T7 RNA聚合酶活性很高,转录速度比大肠杆菌RNA 聚合酶快5倍,使其下游的重组蛋白得到高效表达,其产率可以达到细菌总蛋白量的50%以上。
T7lac启动子则在T7启动子下游加入了一个lac操纵子,其中带有一个常规启动子和lac阻遏蛋白的编码序列。
lac阻遏蛋白可以抑制宿主合成T7 RNA聚合酶,并阻断T7 RNA 聚合酶导致的目的基因转录,从而降低重组蛋白的本底表达水平。
P L、cspA启动子使宿主菌能够进行温度依赖型的表达。
在温度敏感型突变体菌株中,P L等启动子使得宿主在30℃时抑制重组蛋白表达,而在42 ℃时诱导重组蛋白表达;cspA启动子则被高温(37℃)抑制,低温(10℃)启动。
温度诱导型的启动子避免了诱导剂的引入,降低了使用成本,同时也降低了诱导剂对细胞的伤害。
终止子:转录终止子按照是否依赖和不依赖ρ因子的作用分为两类,这两类终止子均在终止点前含有一段7-20bp的回文序列。
终止子可以保护mRNA在核外不被降解,显著延长mRNA的寿命,由此提高重组蛋白的表达量。
但是对于T7系统来说,由于T7 RNA聚合酶效率极高,宿主中随时都有充足的mRNA以供翻译,因此大部分在T7系统中表达的重组蛋白并不在意质粒上是否有终止子,只有一些自身带有翻译起始信号的外源基因需要终止子。
启动子受细胞类型的限制,在不同的细胞系中有很大不同,因此需根据宿主细胞(尤其是真核宿主)的类型选择不同的启动子以便于目的基因的高效表达。
融合标签:融合标签是与目的蛋白共表达的一段多肽,方便重组蛋白的纯化、固定和检测,表3给出了常用的重组标签。
如果不需要对重组蛋白进行纯化,尽量不要引入融合标签,以免影响蛋白性质;如果重组蛋白本身能够结合某种亲和柱,如某些金属结合蛋白可以结合Ni-NTA,某些糖结合蛋白能够特异识别糖类,也不必引入标签。
融合标签的引入能够大大简化重组蛋白的纯化流程,并提高蛋白溶解度。
商业化表达质粒,如pET、pGEX等提供了各种纯化标签和融合蛋白供选,应根据蛋白具体情况进行选择。
His-tag是最常用的纯化标签,它具有很多优点:标签较短(10-20个氨基酸残基),不带电(pH8.0),免疫原性差,通常不影响重组蛋白的结构和功能,Ni2+亲和力高,能够通过一步纯化达到60%-90%的纯度。
如果蛋白质溶解度不高,导致折叠困难、表达量低,可以选择较大的融合标签(GST、MBP、Trx等)帮助重组蛋白表达和折叠,提高重组蛋白溶解度,从而提高表达量。
较大的融合标签有时也会导致翻译困难甚至提前中止,纯化后发现大部分都是标签蛋白也是常见现象。
翻译的提前中止会大大影响重组蛋白产率和后续纯化,所以在短标签能够达到目的的时候,尽量不要选择大的融合标签。
标签位置的选择也很重要:N端标签(短的或长的)自身带有启动子和适应宿主偏好的密码子,可以帮助目的蛋白表达,提高表达量,但是提前中止翻译的蛋白片段也会被一并纯化出来,降低重组蛋白纯度,对蛋白酶敏感的、自身容易降解的以及一级序列中有集中的疏水残基区的蛋白尤其要避免使用N端标签;C端标签则可以保证只有完整蛋白得到纯化。
