王镜岩核酸的物理化学性质
[王镜岩生物化学第三版笔记]第六章 核酸
![[王镜岩生物化学第三版笔记]第六章 核酸](https://img.taocdn.com/s3/m/356f964aa6c30c2259019eb8.png)
第六章 核酸核酸是遗传物质1868年瑞士Miesher.从脓细胞的细胞核中分离出可溶于碱而不溶于稀酸的酸性物质。
间接证据:同一种生物的不同种类的不同生长期的细胞,DNA含量基本恒定。
直接证据:T2噬菌体DNA感染E.coli用35S标记噬菌体蛋白质,感染E.coli,又用32P标记噬菌体核酸,感染E.coliDNA、RNA的分布(DNA在核内,RNA在核外)。
第一节核酸的化学组成核酸是一种线形多聚核苷酸,基本组成单位是核苷酸。
结构层次:核酸核苷酸组成核酸的戊糖有两种::D-核糖和D-2-脱氧核糖,据此,可以将核酸分为两种:核糖核酸(RNA)和脱氧核糖核酸(DNA)P330 表5-1 两类核酸的基本化学组成一、 碱基1. 嘌呤碱:腺嘌呤鸟嘌呤2. 嘧啶碱:胞嘧啶尿嘧啶胸腺嘧啶P331 结构式3. 修饰碱基植物中有大量5-甲基胞嘧啶。
E.coli噬菌体中,5-羟甲基胞嘧啶代替C。
稀有碱基:100余种,多数是甲基化的产物。
DNA由A、G、C、T碱基构成。
RNA由A、G、C、U碱基构成。
二、 核苷核苷由戊糖和碱基缩合而成,糖环上C1与嘧啶碱的N1或与嘌呤碱的N9连接。
核酸中的核苷均为β-型核苷P332 结构式腺嘌呤核苷胞嘧啶脱氧核苷DNA 的戊糖是:脱氧核糖RNA 的戊糖是:核糖三、 核苷酸核苷中戊糖C3、C5羟基被磷酸酯化,生成核苷酸。
1、构成DNA、RNA的核苷酸P333表5-32、细胞内游离核苷酸及其衍生物①核苷5’-多磷酸化合物A TP、GTP、CTP、ppppA、ppppG在能量代谢和物质代谢及调控中起重要作用。
②环核苷酸cAMP(3’,5’-cAMP) cGMP(3’,5’-cGMP)它们作为质膜的激素的第二信使起作用,cAMP调节细胞的糖代谢、脂代谢。
③核苷5’多磷酸3’多磷酸化合物ppGpp pppGpp ppApp④核苷酸衍生物HSCoA、 NAD+、NADP+、FAD等辅助因子。
GDP-半乳糖、GDP-葡萄糖等是糖蛋白生物合成的活性糖基供体。
王镜岩《生物化学》第三版考研笔记(提要版本071页)

王镜岩《生物化学》第三版考研笔记(提要版本071页)内容提要:1、氨基酸与蛋白质氨基酸分类:常见蛋白质氨基酸,不常见蛋白质氨基酸,非蛋白氨基酸;氨基酸的酸碱化学,氨基酸两性解离,氨基酸的等电点;氨基酸的旋光性和紫外吸收。
蛋白质的共价结构:蛋白质的化学组成和分类,蛋白质功能,蛋白质的形状和大小,蛋白质构象和组织层次。
肽:肽键结构,肽的物理化学性质,活性多肽。
蛋白质一级结构测定:Sanger试剂,DNS及Edman降解,二硫桥位置确定。
蛋白质的三维结构:XRD原理;稳定蛋白质三维结构的作用力,肽平面和两面角;蛋白质的二级结构:α-螺旋,β-折叠片,β-转角;超二级结构和结构域;球状蛋白的三级结构;亚基缔合和四级结构。
蛋白质结构与功能的关系:肌红蛋白和血红蛋白的结构与功能,镰刀状细胞贫血病;免疫球蛋白。
蛋白质的分离、纯化和表征:蛋白质分子量测定,沉降分析及沉降系数,沉降系数单位,凝胶过滤及SDS-PAGE法测分子量;蛋白质的沉淀;电泳:区带电泳、薄膜电泳、等电聚焦电泳、毛细管电泳。
2、酶和辅酶酶催化作用特点:反应温合、高效、专一、可调节控制;酶活性调节控制:调剂酶浓度、激素调节、反馈抑制调节、抑制剂激活剂调节、别构调控、酶原激活,可逆共价修饰;酶的化学本质及其组成,辅酶和辅基,单体酶,寡聚酶和多酶复合体。
酶的命名和分类:习惯命名法;国际系统命名法及酶的编号,六大类酶的特征。
酶的专一性:“锁与钥匙”学说;诱导楔合假说;过渡态理论,过渡态类似物与医药和农药的设计,催化抗体。
酶的活力测定:酶活力单位,比活力。
酶工程:化学修饰酶,固定化酶,人工模拟酶。
酶促反应动力学:底物浓度与酶反应速度,酶促反应动力学方程式及推导,米氏常数的意义和求法。
酶的抑制作用:不可逆抑制和可逆抑制及动力学判断,一些重要的抑制剂,有机磷农药和磺胺药作用机制。
温度、PH、激活剂对酶反应影响。
酶的作用机制:酶活性部位及研究方法;影响酶催化效率的有关因素:临近和定向效应、底物形变和诱导契合、酸碱催化、共价催化、金属离子催化、多元催化和协同效应、微环境影响;溶菌酶作用机制和胰凝乳蛋白酶。
王镜岩-生物化学(第三版)配套练习及详解

第一章蛋白质化学I 主要内容一、蛋白质的生物学意义蛋白质是生物体内最为重要的有机化学物质之一,它几乎参与了生物体所有的生命活动,如生物体的构成、机体的运动、化学催化、机体的免疫保护、生物遗传信息的传递与表达等等,可以说蛋白质是一切生命活动的重要支柱,没有蛋白质就没有生命现象的存在,因此,蛋白质化学是生物化学中一个重要的研究方面。
二、蛋白质的元素组成蛋白质是由C、H、O、N、S等几种元素构成,其中C 50-55%、H 6-8%、O 20-30%、 N 15-17%、S 0-4%,且含量基本相同,因此通过测定蛋白质样品中元素含量就可以推测出样品中蛋白质的含量。
三、蛋白质的氨基酸组成(一)氨基酸的结构及特点一般的蛋白质都是由20种氨基酸构成,这些氨基酸都是在蛋白质的合成过程中直接加进去的,并有专门的遗传密码与其对应,这些构成蛋白质的基本氨基酸称为天然氨基酸(通用氨基酸)。
天然氨基酸具有如下特点:1. 20种天然氨基酸均有专门的遗传密码与其对应,它们在蛋白质的合成中是直接加上去的。
2. 除甘氨酸外,其它氨基酸至少含有一个手性碳原子。
3. 除脯氨酸外,其它氨基酸均为 -氨基酸。
4. 氨基酸虽有D、L–型之分,但存在于天然蛋白质中的氨基酸均为L-型氨基酸。
(二)天然氨基酸的分类1.根据氨基酸分子中氨基和羧基的相对数量进行分类2.根据氨基酸分子结构分类3.根据氨基酸侧链基团极性分类氨基酸根据其侧链基团在近中性的pH条件下是否带电荷以及带电荷的种类分成四类:非极性氨基酸、极性不带电荷氨基酸、极性带正电荷氨基酸、极性带负电荷氨基酸。
(三)稀有蛋白质氨基酸这部分主要是指虽然在蛋白质中有所存在,含量却较少的一类氨基酸。
蛋白质中的稀有氨基酸是在蛋白质合成后的加工过程中通过化学的方法在天然氨基酸的基础上增加某些基团而形成的。
(四)非蛋白质氨基酸非蛋白质氨基酸是细胞中不参与天然蛋白质合成的一类氨基酸。
(五)氨基酸的重要理化性质1. 一般理化性质2. 氨基酸的酸碱性质与等电点3. 氨基酸的主要化学性质(1)茚三酮反应(2)桑格反应(Sanger reaction)(3)埃德曼反应(Edman reaction )4. 氨基酸的光学性质由于氨基酸分子中除甘氨酸外都有不对称碳原子的存在,因此,天然氨基酸中除甘氨酸外均有旋光现象的存在。
生物化学(王镜岩第三版)经典笔记

生物化学 王镜岩第三版 完整笔记
第一章 一、 糖的概念 糖类物质是多羟基 (2 个或以上 ) 的醛类 (aldehyde) 或酮类 (Ketone)化合物, 以及它们的衍生物或聚合物。 据此可分为醛糖 (aldose)和酮糖 (ketose)。 糖 糖
还可根据碳层子数分为丙糖 (triose),丁糖 (terose),戊糖 (pentose)、己糖 (hexose)。 最简单的糖类就是丙糖 (甘油醛和二羟丙酮 ) 由于绝大多数的糖类化合物都可以用通式 Cn (H2O)n 表示,所以过去人们一直认为糖类是碳与水的 化合物,称为碳水化合物。现在已经这种称呼并恰当,只是沿用已久,仍有许多人称之为碳水化合物。 二、 糖的种类 根据糖的结构单元数目多少分为: ( 1)单糖:不能被水解称更小分子的糖。 ( 2)寡糖: 2-6 个单糖分子脱水缩合而成,以双糖最为普遍,意义也较大。 ( 3)多糖: 均一性多糖:淀粉、糖原、纤维素、半纤维素、几丁质 (壳多糖 ) 不均一性多糖:糖胺多糖类 (透明质酸、硫酸软骨素、硫酸皮肤素等 ) ( 4)结合糖 (复合糖,糖缀合物, glycoconjugate):糖脂、糖蛋白 (蛋白聚糖 )、糖 -核苷酸等 ( 5)糖的衍生物:糖醇、糖酸、糖胺、糖苷 三、 糖类的生物学功能 (1) 提供能量。植物的淀粉和动物的糖原都是能量的储存形式。 (2) 物质代谢的碳骨架,为蛋白质、核酸、脂类的合成提供碳骨架。 (3) 细胞的骨架。纤维素、半纤维素、木质素是植物细胞壁的主要成分,肽聚糖是细胞壁的主要成分。 (4) 细胞间识别和生物分子间的识别。 细胞膜表面糖蛋白的寡糖链参与细胞间的识别。一些细胞的细胞膜表面含有糖分子或寡糖链,构成 细胞的天线,参与细胞通信。 红细胞表面 ABO 血型决定簇就含有岩藻糖。
静态生物化学时期静态生物化学时期静态生物化学时期静态生物化学时期1920年以前年以前年以前年以前动态生物化学时期动态生物化学时期动态生物化学时期动态生物化学时期1950年以前年以前年以前年以前这是一个飞速发展的辉煌时期随着同位素示踪技术色谱技术等物理学手段的广泛应用生物化学从单纯的组成分析深入到物质代谢途径及动态平衡能量转化光合作用生物氧化糖的分解和合成代谢蛋白质合成核酸的遗传功能酶维生素激素抗生素等的代谢都基本搞清
生物化学(王镜岩版)第三章核酸化学

遗传信息储存和传递媒介
DNA作为遗传物质
01
DNA以双螺旋结构储存遗传信息,通过复制传递给下一代。
RNA作为遗传信息传递媒介
02
RNA以单链形式存在,通过转录将DNA的遗传信息传递给蛋白
质。
核酸序列变异与进化
03
核酸序列的变异是生物进化的基础,为生物多样性提供了遗传
基础。
生物技术应用领域拓展
01
DNA与RNA结构差异
DNA(脱氧核糖核酸)和RNA(核糖核酸)在化学结构上存在差异,主要体现在五碳糖和 碱基的不同。
DNA的五碳糖是脱氧核糖,而RNA的五碳糖是核糖;DNA的碱基包括腺嘌呤(A)、鸟嘌 呤(G)、胸腺嘧啶(T)和胞嘧啶(C),而RNA的碱基则是腺嘌呤(A)、鸟嘌呤(G) 、尿嘧啶(U)和胞嘧啶(C)。
生物化学(王镜岩版)第 三章核酸化学
目 录
• 核酸概述与分类 • DNA结构与性质 • RNA结构与性质 • 核酸合成与降解途径 • 核酸生物功能与应用 • 实验方法与技术手段介绍
01
核酸概述与分类
核酸定义及功能
01
核酸是由核苷酸组成的大分子生 物聚合物,是生命体系中的重要 遗传物质。
02
核酸在生物体内主要承担遗传信 息的存储、传递和表达等功能, 是生物体正常生长和发育的基础 。
THANKS
感谢观看
03
RNA结构与性质
tRNA三叶草结构
反密码环
与mRNA上的密码子进行碱基 互补配对。
可变环
序列和大小在不同tRNA中有 所变化,可能与tRNA的特异 性识别有关。
氨基酸接受臂
负责识别和携带特定的氨基酸 。
TΨC环
含有保守序列和修饰碱基,与 tRNA的生物活性有关。
生物化学笔记(王镜岩)
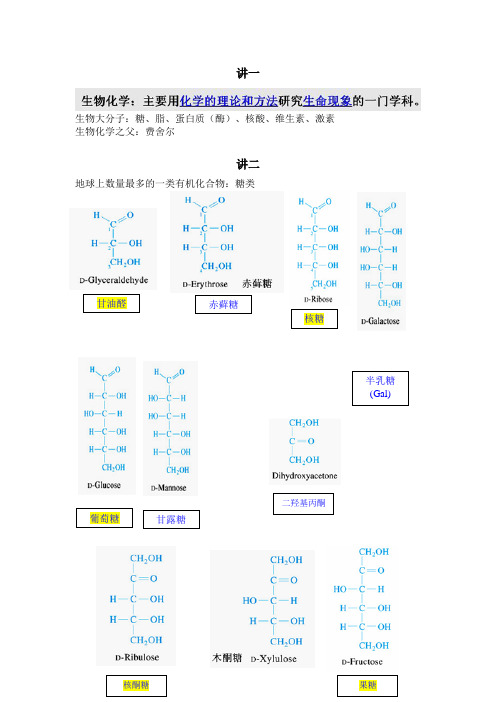
赤藓糖葡萄糖甘油醛核糖甘露糖半乳糖(Gal)((Gal)二羟基丙酮核酮糖果糖讲一生物大分子:糖、脂、蛋白质(酶)、核酸、维生素、激素生物化学之父:费舍尔讲二地球上数量最多的一类有机化合物:糖类α和β吡喃葡萄糖(羟基在下为α型,在上为β型)糖原高度分支的生理意义:第三章、蛋白质20种氨基酸英文名等电点掌握氨基酸的用途、现象DNFB法PITCCys半胱氨酸Ellman反应,DTNB,二硫硝基苯甲酸Ellman反应(二硫硝基苯甲酸,DTNB)Cys与二硫硝基苯甲酸(DTNB) 或称Ellman 试剂发生硫醇-二硫化物交换反应。
反应中1 分子的Cys引起1分子的硫硝基苯甲酸的释放。
它在pH 8.0 时, 在412nm 波长处有强烈的光吸收, 因此可利用分光光度法定量测定-SH。
肽平面(酰胺平面)——由肽键周围的6个原子组成的刚性平面3.6蛋白质的纯化注:用尽可能少的步骤、尽可能短的时间。
1.前处理阶段物理法——冻融法,超声波法,均浆法,研磨法等。
酶裂解法——就是利用水解酶将细胞壁和细胞膜消化的方法,常用的水解酶有溶菌酶、葡聚糖酶、蛋白酶、糖苷酶、壳多糖酶、细胞壁溶解酶等。
其中溶菌酶主要对细菌类有作用,其他酶对酵母作用显著。
2.粗分级/粗分离根据蛋白质的①溶解性质、②大小不同、③带电状态不同/电荷多少④净化方法根据与其他化合物相互作用的蛋白质(部分蛋白质对..有特定的..)②:凝胶过滤层析常用凝胶过滤介质Sephadex:交联葡聚糖,是采用环氧氯丙烷作交联剂将右旋葡聚糖交联而成。
干粉容易膨胀,在水、盐溶液、有机溶液、碱和弱酸中化学性质稳定,可高压灭菌。
高交联度的Sephadex,其颗粒坚硬,适于高流速下操作。
Sephacryl : 烯丙基葡聚糖同N、Nˊ—甲叉双丙烯酰胺共价交联而成。
颗粒坚硬,性质比Sephadex更为稳定,可高压灭菌,在pH3~11条件下稳定,可用有机溶剂洗脱,也可用SDS、尿素及盐酸胍洗脱。
王境岩生物化学笔记

第一章糖第一节概述一、糖的命名糖类是含多羟基的醛或酮类化合物,由碳氢氧三种元素组成的,其分子式通常以Cn(H2O)n 表示。
因为一些糖分子中氢和氧原子数之比往往是2:1,与水相同,过去误认为此类物质是碳与水的化合物,所以称为"碳水化合物"(Carbohydrate)。
实际上这一名称并不确切,如脱氧核糖、鼠李糖等糖类不符合通式,而甲醛、乙酸等虽符合这个通式但并不是糖。
只是"碳水化合物"沿用已久,一些较老的书仍采用。
我国将此类化合物统称为糖,而在英语中只将具有甜味的单糖和容易的寡糖称为糖(sugar)。
二、糖的分类按照分子的构成,糖可分为单糖、寡糖、多糖、结合糖和衍生糖。
1.单糖单糖是不能水解为更小分子的糖。
葡萄糖,果糖都是常见单糖。
按照羰基在分子中的位置,单糖可分为醛糖和酮糖。
按照碳原子数目,可分为丙糖,丁糖,戊糖,己糖和庚糖。
2.寡糖寡糖由2-6个单糖分子构成,其中以双糖最普遍。
寡糖和单糖都可溶于水,多数有甜味。
3.多糖多糖由多个单糖聚合而成,又可分为同聚多糖和杂聚多糖。
同聚多糖由同一种单糖构成,杂聚多糖由两种以上单糖构成。
4.结合糖糖链与蛋白质或脂类物质构成的复合分子称为结合糖。
其中的糖链普通是杂聚寡糖或杂聚多糖。
如糖蛋白,糖脂,蛋白聚糖等。
5.衍生糖由单糖衍生而来,如糖胺、糖醛酸等。
三、糖的分布与功能1.分布糖在生物界中分布很广,几乎所有的动物,植物,微生物体内都含有糖。
糖占植物干重的80%,微生物干重的10-30%,动物干重的2%。
糖在植物体内起着重要的结构作用,而动物则用蛋白质和脂类代替,所以行动更灵便,适应性强。
动物中惟独昆虫等少数采用多糖构成外骨胳,其形体大小受到很大限制。
在人体中,糖主要以三种形式存在:(1)以糖原形式贮藏在肝和肌肉中。
糖原代谢速度很快,对维持血糖浓度衡定,满意机体对糖的需求有重要意义。
(2)以葡萄糖形式存在于体液中。
细胞外液中的葡萄糖是糖的运输形式,它作为细胞的内环境条件之一,浓度相当衡定。
王镜岩-生物化学-第13章-核酸的结构全
修饰核苷
核酸中还存在少量修饰 核苷,有三种:
➢ 由稀有碱基参与,如: 5-甲基脱氧胞苷,
次黄嘌呤核苷 ➢ 由稀有戊糖参与,如:
2-O-甲基胞苷 ➢ 碱基与戊糖连接方式特
殊,如:
假尿苷(ψ)C1-C5
DNA的甲基化导致基因沉默
5-甲基脱氧胞苷 2’-O-甲基胞苷
次黄嘌呤核苷 假尿苷(ψ)
DNA,RNA中主要的碱基、核苷
(2)DNA的碱基组成(Chargaff定则):
①在所有的DNA中,A=T,G=C 即A+G=T+C; ②DNA的碱基组成具有种的特异性,即不同生物物种的DNA具有
自己独特的碱基组成(以不对称比率A+T/G+C表示),但 同一生物体内没有组织和器官的特异性。
A=T,G=C这一规律的发现,提示了A与T,G与C之间碱基互补 的可能性。
(35y)
(25y)
(1)DNA双螺旋结构的研究背景
碱基组成分析 Chargaff 规则:[A] = [T]
[G] = [C] 碱基的理化数据分析 A-T、G-C以氢键配对较合理
DNA纤维的X-线衍射图谱分析
(2)DNA双螺旋结构的特 点
①两条反向平行的 多脱氧核苷酸链围 绕同一中心轴以右 手盘绕成双螺旋结 构,螺旋表面 具大沟和小沟。
第13章 核酸的结构
N H2 N
N
N H
N
一、核酸的组成p223
核酸
磷酸 核苷酸
核苷
核糖
戊糖
脱氧核糖 嘌呤碱
含氮碱
嘧啶碱
(一)核酸的元素组成
基本元素:C H O N P 核酸的元素组成有两个特点:
1. 一般不含S。 2. P含量较多,并且恒定(9%-10%)。
【考研必备】王镜岩生物化学笔记 第六章 核酸

第六章核酸核酸是遗传物质1868年瑞士Miesher.从脓细胞的细胞核中分离出可溶于碱而不溶于稀酸的酸性物质。
间接证据:同一种生物的不同种类的不同生长期的细胞,DNA含量基本恒定。
直接证据:T2噬菌体DNA感染E.coli用35S标记噬菌体蛋白质,感染E.coli,又用32P标记噬菌体核酸,感染E.coliDNA、RNA的分布(DNA在核内,RNA在核外)。
第一节核酸的化学组成核酸是一种线形多聚核苷酸,基本组成单位是核苷酸。
结构层次:核酸核苷酸组成核酸的戊糖有两种::D-核糖和D-2-脱氧核糖,据此,可以将核酸分为两种:核糖核酸(RNA)和脱氧核糖核酸(DNA)P330 表5-1 两类核酸的基本化学组成一、碱基1. 嘌呤碱:腺嘌呤鸟嘌呤2. 嘧啶碱:胞嘧啶尿嘧啶胸腺嘧啶P331 结构式3. 修饰碱基植物中有大量5-甲基胞嘧啶。
E.coli噬菌体中,5-羟甲基胞嘧啶代替C。
稀有碱基:100余种,多数是甲基化的产物。
DNA由A、G、C、T碱基构成。
RNA由A、G、C、U碱基构成。
二、核苷核苷由戊糖和碱基缩合而成,糖环上C1与嘧啶碱的N1或与嘌呤碱的N9连接。
核酸中的核苷均为β-型核苷P332 结构式腺嘌呤核苷胞嘧啶脱氧核苷DNA 的戊糖是:脱氧核糖RNA 的戊糖是:核糖三、核苷酸核苷中戊糖C3、C5羟基被磷酸酯化,生成核苷酸。
1、构成DNA、RNA的核苷酸P333表5-32、细胞内游离核苷酸及其衍生物①核苷5’-多磷酸化合物A TP、GTP、CTP、ppppA、ppppG在能量代谢和物质代谢及调控中起重要作用。
②环核苷酸cAMP(3’,5’-cAMP)cGMP(3’,5’-cGMP)它们作为质膜的激素的第二信使起作用,cAMP调节细胞的糖代谢、脂代谢。
③核苷5’多磷酸3’多磷酸化合物ppGpp pppGpp ppApp④核苷酸衍生物HSCoA、NAD+、NADP+、FAD等辅助因子。
GDP-半乳糖、GDP-葡萄糖等是糖蛋白生物合成的活性糖基供体。
王镜岩生物化学知识点整理版

教学目标:1.掌握蛋白质的概念、重要性和分子组成。
2.掌握α-氨基酸的结构通式和20种氨基酸的名称、符号、结构、分类;掌握氨基酸的重要性质;熟悉肽和活性肽的概念。
3.掌握蛋白质的一、二、三、四级结构的特点及其重要化学键。
4.了解蛋白质结构与功能间的关系。
5.熟悉蛋白质的重要性质和分类第一节蛋白质的分子组成一、蛋白质的元素(化学)组成主要有 C(50%~55%)、H(6%~7%)、O(19%~24%)、N(13%~19%)、S(0%~4%)。
有些蛋白质还含微量的P、Fe、Cu、Zn、Mn、Co、Mo、I等。
各种蛋白质的含氮量很接近,平均为16%。
因此,可以用定氮法来推算样品中蛋白质的大致含量。
每克样品含氮克数×6.25×100=100g样品中蛋白质含量(g%)二、蛋白质的基本组成单位——氨基酸蛋白质在酸、碱或蛋白酶的作用下,最终水解为游离氨基酸(amino acid),即蛋白质组成单体或构件分子。
存在于自然界中的氨基酸有300余种,但合成蛋白质的氨基酸仅20种(称编码氨基酸),最先发现的是天门冬氨酸(1806年),最后鉴定的是苏氨酸(1938年)。
(三)氨基酸的重要理化性质1.一般物理性质α-氨基酸为无色晶体,熔点一般在200 oC以上。
各种氨基酸在水中的溶解度差别很大(酪氨酸不溶于水)。
一般溶解于稀酸或稀碱,但不能溶解于有机溶剂,通常酒精能把氨基酸从其溶液中沉淀析出。
芳香族氨基酸(Tyr、Trp、Phe)有共轭双键,在近紫外区有光吸收能力,Tyr、Trp的吸收峰在280nm,Phe在265 nm。
由于大多数蛋白质含Tyr、Trp残基,所以测定蛋白质溶液280nm的光吸收值,是分析溶液中蛋白质含量的快速简便的方法。
2.两性解离和等电点(isoelectric point, pI)氨基酸在水溶液或晶体状态时以两性离子的形式存在,既可作为酸(质子供体),又可作为碱(质子受体)起作用,是两性电解质,其解离度与溶液的pH有关。
王镜岩-生物化学-第14章__核酸的物理化学性质

第一节
核酸的水解
核酸的水解
核酸
水
核苷酸
解
磷酸 核苷
戊糖
碱基
一、酸水解
• 水解特点:
• 1.糖苷键和磷酸酯键都能被酸水解 • 2.但糖苷键比磷酸酯键更易被酸水解 • 3.嘌呤碱的糖苷键比嘧啶碱的糖苷键对酸 更不稳定
二、碱水解
• 水解特点: • 1. RNA的磷酸酯键易被碱水解;而DNA对碱稳定
2. Cot l/2
• 衡量复性反应的速度快慢的指标 • Co为变性DNA复性时的初始浓度,以核 苷酸的摩尔浓度表示, • t为时间,以秒表示, • Cot l/2表示复性一半的Cot值
•在DNA浓度相同的情况下, Cot l/2与基因组的大小成正比
三、核酸的杂交 (hybridization)
(3) 限制性内切酶
限制性核酸内切酶,是一类能够识别双链DNA 分子中的某种特定核苷酸序列,并由此切割 DNA双链结构的核酸内切酶。它们主要是从原 核生物中分离纯化出来的。 根据 1994 年美国出版的《分子生物学百科 全书》的统计数字,仅Ⅱ型核酸内切限制酶一 项迄今就已从各种不同的微生物当中,分离出 了2300种以上。
• 1. 定义: • 将不同来源的DNA放在试管里,经热变 性后,慢慢冷却,让其复性。若这些异 源DNA之间在某些区域有相同的序列, 则复性时,会形成杂交DNA分子。 • DNA与互补的RNA之间也可以发生杂交。 是分子生物学和分子遗传学的研究中应 用极广的技术。
2. 常见杂交的类型
• (1)Southern blotting • (2)Northern blotting • (3)Western blotting
• 能够识别由4~8个核苷酸组成的特定的 核苷酸序列; • 切割位点的一个共同特点是,它们具有 双重旋转对称的结构形式,换言之,这 些核苷酸对的顺序是呈回文结构。
考研复习王镜岩生物化学之核酸化学

2核酸化学1 考试大纲涉及王镜岩版生物化学第11、12、27章 + 分子生物学(一)核酸的结构与功能1生物大分子有四类:核酸、蛋白质、多糖和脂质。
最重要的生物大分子是DNA、RNA和蛋白质。
2核酸的研究史:(1)1868年,瑞士青年科学家F.Miescher由脓细胞分离得到细胞核,并从中提取出一种含磷酸很高的酸性物质,称为核素。
他又转向研究鲑鱼精子头部的物质,除了分离到酸性高含磷酸化合物外,还提取出一种碱性化合物称为鱼精蛋白。
Miescher被认为是细胞核化学的创始人和DNA的发现者。
(2)R.Altmann他发展了从酵母和动物组织中制备不含蛋白质的核酸的方法,核酸这个名称是由他在1889年最先提出来的。
(3)胸腺的细胞核特别大,酵母的细胞质很丰富,这是两种容易提取核酸的材料,因此这两种核酸也就研究的最多。
(4)核酸中的碱基大部分是由A.Kossel及其同事所鉴定的,1910年,因其在核酸化学研究中的成就而被授予诺贝尔医学奖,但他却认为决定染色体功能的是蛋白质,在获奖后转而研究染色体蛋白质。
(5)1953年Watson和Crick提出了DNA双螺旋结构模型。
(6)1956年A.Kornbery发现了DNA聚合酶可以在体外复制DNA。
(7)1958年,Crick总结了当时分子生物学的成果,提出了中心法则,即及遗传信息从DNA传到RNA,再传到蛋白质,一旦传递给蛋白质就不再传递。
(8)W.Arber最早发现细菌细胞中存在DNA限制性内切酶。
DNA重组技术的出现。
(9)1981年T.Cech发现四膜虫rRNA前体,能够通过自我剪切切除内含子,表明RNA也具有催化功能称为核酶。
(10)1983年R.Simons和T.Mizuno发现反义RNA,表明RNA具有调节作用。
(11)1986年W.Gilbert提出RNA世界的假说,这对DNA中心的观点是一次有力的冲击。
1987年,阐述了核糖体移码,说明遗传信息的解码也是可以改变的。
王镜岩生物化学知识点整理版

教学目标:1.掌握蛋白质的概念、重要性和分子组成。
2.掌握α-氨基酸的结构通式和20种氨基酸的名称、符号、结构、分类;掌握氨基酸的重要性质;熟悉肽和活性肽的概念。
3.掌握蛋白质的一、二、三、四级结构的特点及其重要化学键。
4.了解蛋白质结构与功能间的关系。
5.熟悉蛋白质的重要性质和分类第一节蛋白质的分子组成一、蛋白质的元素(化学)组成主要有 C(50%~55%)、H(6%~7%)、O(19%~24%)、N(13%~19%)、S(0%~4%)。
有些蛋白质还含微量的P、Fe、Cu、Zn、Mn、Co、Mo、I等。
各种蛋白质的含氮量很接近,平均为16%。
因此,可以用定氮法来推算样品中蛋白质的大致含量。
每克样品含氮克数×6.25×100=100g样品中蛋白质含量(g%)二、蛋白质的基本组成单位——氨基酸蛋白质在酸、碱或蛋白酶的作用下,最终水解为游离氨基酸(amino acid),即蛋白质组成单体或构件分子。
存在于自然界中的氨基酸有300余种,但合成蛋白质的氨基酸仅20种(称编码氨基酸),最先发现的是天门冬氨酸(1806年),最后鉴定的是苏氨酸(1938年)。
(三)氨基酸的重要理化性质1.一般物理性质α-氨基酸为无色晶体,熔点一般在200 oC以上。
各种氨基酸在水中的溶解度差别很大(酪氨酸不溶于水)。
一般溶解于稀酸或稀碱,但不能溶解于有机溶剂,通常酒精能把氨基酸从其溶液中沉淀析出。
芳香族氨基酸(Tyr、Trp、Phe)有共轭双键,在近紫外区有光吸收能力,Tyr、Trp的吸收峰在280nm,Phe在265 nm。
由于大多数蛋白质含Tyr、Trp残基,所以测定蛋白质溶液280nm的光吸收值,是分析溶液中蛋白质含量的快速简便的方法。
2.两性解离和等电点(isoelectric point, pI)氨基酸在水溶液或晶体状态时以两性离子的形式存在,既可作为酸(质子供体),又可作为碱(质子受体)起作用,是两性电解质,其解离度与溶液的pH有关。
生物化学--(王镜岩)精心整理 精要知识点速览

生物化学精要速览(希望对广大生化初学者有助)第一章绪论一、生物化学的的概念:生物化学(biochemistry)是利用化学的原理与方法去探讨生命的一门科学,它是介于化学、生物学及物理学之间的一门边缘学科。
二、生物化学的发展:1.叙述生物化学阶段:是生物化学发展的萌芽阶段,其主要的工作是分析和研究生物体的组成成分以及生物体的分泌物和排泄物。
2.动态生物化学阶段:是生物化学蓬勃发展的时期。
就在这一时期,人们基本上弄清了生物体内各种主要化学物质的代谢途径。
3.分子生物学阶段:这一阶段的主要研究工作就是探讨各种生物大分子的结构与其功能之间的关系。
三、生物化学研究的主要方面:1.生物体的物质组成:高等生物体主要由蛋白质、核酸、糖类、脂类以及水、无机盐等组成,此外还含有一些低分子物质。
2.物质代谢:物质代谢的基本过程主要包括三大步骤:消化、吸收→中间代谢→排泄。
其中,中间代谢过程是在细胞内进行的,最为复杂的化学变化过程,它包括合成代谢,分解代谢,物质互变,代谢调控,能量代谢几方面的内容。
3.细胞信号转导:细胞内存在多条信号转导途径,而这些途径之间通过一定的方式方式相互交织在一起,从而构成了非常复杂的信号转导网络,调控细胞的代谢、生理活动及生长分化。
4.生物分子的结构与功能:通过对生物大分子结构的理解,揭示结构与功能之间的关系。
5.遗传与繁殖:对生物体遗传与繁殖的分子机制的研究,也是现代生物化学与分子生物学研究的一个重要内容。
第二章蛋白质的结构与功能一、氨基酸:1.结构特点:氨基酸(amino acid)是蛋白质分子的基本组成单位。
构成天然蛋白质分子的氨基酸约有20种,除脯氨酸为α-亚氨基酸、甘氨酸不含手性碳原子外,其余氨基酸均为L-α-氨基酸。
2.分类:根据氨基酸的R基团的极性大小可将氨基酸分为四类:①非极性中性氨基酸(8种);②极性中性氨基酸(7种);③酸性氨基酸(Glu和Asp);④碱性氨基酸(Lys、Arg和His)。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
核
苷
酸离
的
子 化
解
程 度
离
曲
线
鸟嘌呤核苷酸
pK2 = 3.7
含氮环 pK3 = 6.1
pK1 = 0.7
第二磷酸基
第一磷酸基
烯醇式羟基
pK2 = 4.3 含氮环
胞嘧啶核苷酸
pK1 = 0.8 第一磷酸基
pK3 = 6.3 第二磷酸基
pK1 = 1.0 第一磷酸基
尿嘧啶核苷酸
pK3 = 6.4 第二磷酸基
2020/9/22
影响DNA的Tm值的因素
①DNA均一性 。 均一性高,变性的温度范围越窄,据此可分析DNA 的均一性 。 ②G-C含量与Tm值成正比。 测定Tm,可推知G-C含量。 G-C%=(Tm-69.3)×2.44
2020/9/22
③介质中离子强度 离子强度高,Tm高。
2020/9/22
利用酸水解可以研究核酸的碱基组成
2020/9/22
(二)碱水解
RNA的磷酸酯键对碱敏感
室温,0.3~1mol/L KOH,24h,可将RNA完全水解, 得到2′-或3′-核苷酸的混合物。
DNA抗碱水解 生理意义:
DNA更稳定 ,遗传信息。 RNA是DNA的信使,完成任务后迅速降解。
2020/9/22
或:40ug/mL单链DNA(或RNA) 或:20ug/mL寡核苷酸 3、判断DNA是否变性 在DNA的变性过程中,摩尔吸光系数增大(增色效应) 在DNA的复性过程中,摩尔吸光系数减小(减色效应)
2020/9/22
四、核酸的变性、复性及杂交
(一)变性
核酸变性指核酸双螺旋区的氢键断裂,变成单链, 不涉及共价键断裂。
(三)酶水解
非特异的磷酸二酯酶:
蛇毒磷酸二酯酶水解DNA(RNA)得5′-核苷酸 牛脾磷酸二酯酶水解DNA(RNA)得3′-核苷酸
特异的磷酸二酯酶: 核酸酶
2020/9/22
1、核酸酶的分类
★底物专一性:
核糖核酸酶 RNase 脱氧核糖核酸酶 DNase
★作用方式:
核酸外切酶(exonuclease)、核酸内切酶 (endonuclease) 单链核酸酶、双链核酸酶、杂链核酸酶
★RNase T1
耐热、耐酸 产物:3′-鸟苷酸或以其为结尾的寡核苷酸,专一性更高
★RNase T2
产物:将tRNA完全水解为以3′-腺苷酸结尾的寡核苷酸
2020/9/22
3、DNase
★核酸酶S1 作用于单链DNA部分 ★牛胰脱氧核糖核酸酶,DNase I 切断双链或单链DNA,产物:以5′-磷酸为末端的寡 核苷酸 ★牛脾脱氧核糖核酸酶,DNase Ⅱ 产物:以3′-磷酸为末端的寡核苷酸 ★DNA限制性内切酶
第十四章 核酸的物理化学性质
一、核酸的水解 二、核酸的酸碱性质 三、核酸的紫外吸收 四、核酸的变性、复性及杂交
2020/9/22
一、核酸的水解
(一)酸水解
对酸的敏感性:糖苷键>磷酸酯键
嘌呤糖苷键>嘧啶糖苷键 脱嘌呤:
pH1.6,37℃,对水透析 pH2.8,100℃,1h
脱嘧啶:
98-100%甲酸,175℃,2h 三氟乙酸,155℃,60min(DNA)或 80min(RNA)
烯醇式羟基
pH
小牛胸腺DNA 的滴定曲线
pH
三、核酸的紫外吸收
碱基、核苷、核苷酸和核酸在240~290nm的紫外 波段有强烈的光吸收, λmax=260nm
2020/9/22
1、鉴定纯度 纯DNA的A260/A280应为1.8(1.65-1.85) 纯RNA的A260/A280应为2.0。 若溶液中含有杂蛋白或苯酚,则A260/A280比值明显降 低。 2、含量计算 1ABS值相当于:50ug/mL双螺旋DNA
★磷酸二酯键的断裂方式:
5′-(寡)核苷酸 3′-(寡)核苷酸
2020/9/22
2、RNAase
★RNase H
作用于DNA-RNA中的RNA链
★牛胰核糖核酸酶(pancreatic ribonuclease) , RNase I
最适pH :7.0-8.2 产物:3′-嘧啶核苷酸或以其为结尾的寡核苷酸。高度专一的 内切酶
(二)复性
变性DNA在适当(一般低于 Tm20 ~ 25℃ ) 条 件 下 , 两 条链重新缔合成双螺旋结构。
★复性机制:10~20bp成拉链 ★热变性DNA在缓慢冷却时可以复 性,快速冷却不能复性。
★DNA片段越大,复性越慢; ★DNA浓度越大,复性越快。
★复性速度可用Co·t衡量。 Co 为 变 性 DNA 原 始 浓 度 mol·L-1 , t为时间,以秒表示。
20●20/根9/22据复性动力学可以测定基因组的大小和重复序列的拷 贝数
波长(nm)
★DNA的变性是爆发式的,变性作用发生在一个很 窄的温度范围内。
DNA的双螺旋结构失去一半时对应的温度称为解链 温度(Tm)。
浓 度 50ug/mL 时 , 双 链 DNA A260=1.00,完全 变 性 ( 单 链 ) , A260= 1.37。当A260增加到最大 增大值一半时,即1.185 时,对应的温度即为Tm。 DNA 的 Tm 一 般 在 82 ~ 95℃之间。
2020/9/22
●1个核苷酸对(A.U),若浓度为Co=1.0mmol/L,则 50%复性时, Cot1/2=4×10-6mol.s/L,t=0.004秒 全部复性, Cot=10-4, t=0.1秒 ●E.coli 4.2×106碱基对,若浓度Co=1.0 umol/L,则 复性50%, Cot1/2=10 mol.s/L,t=107秒,约115天。 复性100%,Cot=500 mol.s/L,t=5×108秒,5758天。
4、N-糖苷酶
2020/9/22
二、 核酸的酸碱性质
磷酸和碱基均能发生两性解离。 DNA等电点 4~4.5 RNA等电点 2~2.5 1、碱基的解离 P504 2、核苷的解离 P505 3、核苷酸的解离
2020/9/22
pK2 = 3.7
腺嘌呤核苷酸
含氮环 pK3 = 6.2
pK1 = 0.9
第二磷酸基
2020/9/22
★变性因素:
热变性
酸碱变性(pH小于4或
大于11)
0.4
变性剂(尿素、盐酸胍、
甲醛)
0.3
光
吸
★变性后的理化性质: 260nm吸收值升高。
收
0.2
粘度降低,浮力密度升 0.1 高。
二级结构改变,部分失
活。
220
1 天然DNA 2 变性DNA 3 核苷酸总吸收值
3 2 1
240 260 280
