南京工业大学分析化学试卷2
南京工业大学无机分析化学题库试题2

南京工业大学无机分析化学题库试题2一、选择题1. 配位化合物的内界,若有多种无机配体和有机配体,其命名顺序为:(A) 无机阴离子-无机分子-有机配体(B) 无机分子-无机阴离子-有机配体(C) 有机配体-无机分子-无机阴离子(D) 有机配体-无机阴离子-无机分子2. [Cu(NH3)4]2+为内轨型配合物、平面四方形构型,其磁矩为:(A) 5.75?SUB>B (B) 3.87?SUB>B (C) 1.73?SUB>B (D) 0?SUB>B3. Fe2+有6个3d电子,配合物[Fe(CN)6]4-,△o= 395kJ·mol-1;Ep=213kJ·mol-1。
则晶体场稳定化能CFSE等于(kJ·mol-1):(A) -522 (B) -470.4 (C) -948 (D) -3094. 在等年度的Ca2+、Mg2+、Al3+、Fe3+溶液中,加入EDTA溶液,首先与EDTA形成配合物的是:(A) Ca2+ (B) Mg2+ (C) Al3+ (D) Fe3+5. 在pH = 12.00的溶液中,用EDTA滴定Ca2+和Mg2+混合液,测定的是:(A) Mg2+的量(B) Ca2+的量(C) Ca2+-Mg2+的量(D) Ca2++Mg2+的量6. 物质Fe3O4中的Fe的氧化数是(A) +2 (B) +3 (C) +4/3(D) +8/37. 已知: Fe3++ e = Fe2+φo = 0.77V;Zn2++ 2e = Zn φo = -0.76 VFe2++ 2e = Fe φo = -0.44V;Al3++ 3e = Al φo = -1.66 V 上述物质中还原性最强的是(A) Zn (B) Fe2+(C) Fe (D) Al8. 人们规定标准电极在标准状态下的电极电位为0。
标准电极是:(A) 甘汞电极(B) 银电极(C) 氢电极(D) 铂电极9. 用能斯特方程φ=φθ+ (0.0592/n)lgC(氧化型)/C(还原型)计算φCr2O72-/Cr3+的电极电位时,说法不正确的是:(A) 温度应为298 K (B) Cr3+浓度增大则φ减小(C) H+浓度的变化对φ无影响(D) Cr2O72-浓度增大,则φ增大10. φo MnO4-/ Mn2+ = 1.45V,φoSn4+/Sn2+= 0.15V,以MnO4-滴定Sn2+,([H+]=1mol·L-1)其化学计量点的电极电位为:(A) 0.80V (B) 1.48V (C) 1.30V(D) 1.08V11. 可以直接配制的标准溶液是:(A) K2Cr2O7 (B) K2S2O8 (C) Na2S2O3 (D) Ce(SO4)212. 碘量法用纯Cu标定Na2S2O3标准溶液,将Cu溶解说Cu2+所用的溶剂为:(A) HNO3 (B) HCl (C) 浓H2SO4 (D) HCl + H2O213. 下列说法正确的是:(A) 聚集速度越大越易形成晶体沉淀(B) 过饱和度越大,定向速度越大(C) 聚集速度越小越易形成晶体沉淀(D) 过饱和度越小,定向速度越大14. 在下列措施中,不能增加ZnS沉淀溶液中Zn2+浓度(mol·L-1)的措施是:(A) 加HNO3 (B) 加水(C) 加Cu2+ (D) NaCl15. 下列说法不正确的是:(A) 称量形式的组成必须单一(B) 沉淀形式溶度积一定要小(C) 沉淀剂不纯对重量分析法无影响(D) 加入的沉淀剂的量不必准确16. 法扬司法测定Cl-时,使用的指示剂是:(A) Ag2CrO4 (B) 二氯荧光黄(C) Fe(NH4)2(SO4)2 (D) FeNH4(SO4)217. 工业上五氧化二钒的主要用途是做(A) 吸附剂(B) 表面活性剂(C)催化剂(D)氧化剂18. 下列离子的颜色为粉红色的是(A) [Fe(H2O)6]2+ (B) [Ni(H2O)6]2+ (C) [Ni(NH3)6]2+ (D) [Co(H2O )6]2+19. 阴离子交换树脂可分离下列哪组物质?(A) 氯化钠和氯化钾(B) 苯酚和醋酸(C) 氯化钠和溴化钠(D) 水和NaOH20. 用薄层层析法,以苯-乙酸乙酯为展开剂分离黄连素时,已知比移值为0.41,溶剂前沿距离为24.5 cm,则斑点中心只原点的距(A) 10.0cm (B) 14.5cm (C)10.3cm (D) 无法确定二、填充题1. 配离子[Co(NH3)4(NO2)Cl]+的名称为_____________________(若有多个答案,用”;“号间隔。
无机分析化学试卷B卷

南京工业大学无机与分析化学试卷(下、B)(一页开卷)2012—2013学年第二学期使用班级:全校相关专业学院专业学号姓名题号一二三四五六七总分得分一、每题只有一个答案是正确的,请选择(每题2分,将答案填入答题表中)题号12345678910答案题号11121314151617181920答案1. 在酸性溶液中,以0.1000 mo l•L-1的Ce4+溶液滴定0.1000 mo l•L-1的Fe2+溶液,化学计量点的电位为1.06V,对此滴定最适宜的指示剂是:(A) 次甲基蓝(φo=0.53V)(B) 二苯胺磺酸钠(φo=0.84V)(C) 邻二氮菲亚铁(φo=1.06V)(D) 硝基邻二氮菲亚铁(φo=1.25V)2. 配离子[FeEDTA]-中Fe3+配位数为:(A) 2 (B) 4 (C) 5 (D) 63. 已知lgK MY=9.65,[M] = 0.01000mol/L。
pH=7.0,lgαY(H) = 3.32;pH=8.0,lgαY(H) = 2.27;pH=9.0,lgαY(H) = 1.28;pH=10.0,lgαY(H) = 0.45。
对M进行准确滴定的最低pH为:(A) 7.0 (B) 8.0 (C) 9.0 (D) 10.04. 在间接碘量法中,最后以淀粉为指示剂,用Na2S2O3标准溶液滴定生成的I2。
加入淀粉指示剂最适宜的时间是:(A) 滴定开始时(B) 溶液变为浅黄色时(C) 溶液变为无色时(D) 溶液变为蓝色时5. 若配制EDTA溶液时所用的水中含有Ca2+,在pH =12.00下,以CaCO3为基准物质标定EDTA溶液。
然后用此标准溶液在pH = 2左右滴定试样中的Fe3+,Fe3+测定结果:(A) 偏低(B) 偏高(C) 正常(D) 不确定6. 已知:φo Fe3+/Fe2+=0.77 V,φo I2/I-=0.535 V,φo BrO3-/Br-=1.44 V,φo Cu2+/Cu+=0.17 V,K sp(CuI) = 1.1×10-12。
南京工业大学分化期末试卷

南京工业大学分化期末试卷光学分析概论(一)判断题()1.从本质上而言,质谱应属于波谱范畴。
()2.化合物的可见-紫外吸收光谱,主要是由分子中价电子的跃迁而产生。
(二)单选题1.属于非光谱分析法的是()A.UV B.IR C.X-ray D.AAS E.NMR2.属于光谱分析法的是()A.比浊法B.折射法C.旋光法D.红外吸收法E.X-射线衍射法3.某化合物受电磁辐射作用后,振动能级发生变化,所产生的光谱波长范围是()A.紫外光B.X射线C.微波D.红外线E.可见光4.不同波段的电磁波具有不同的能量,其大小顺序是()A.无线电波>红外光>可见光>紫外光>X射线B.X射线>红外光>可见光>紫外光>无线电波C.X射线>红外光>可见光>紫外光>微波D.X射线>紫外光>可见光>红外光>微波E.微波>X射线>紫外光>可见光>红外光5.电子能级间隔越小,跃迁时吸收光子的()A.数目越多B.波长越长C.能量越大D.波数越大E.频率越高6.分子吸收了外来辐射后,外层价电子跃迁时所产生的光谱波长范围通常在()A.无线电波区B.微波区C.X射线区D.红外光区E.可见-紫外光区7.复合光变成单色光的过程称为()A.散射B.折射C.衍射D.色散E.激发(三)多选题1.真空紫外、近紫外、可见光谱的能级跃迁方式是()A.内层电子跃迁B.中层电子跃迁C.外层电子跃迁D.分子振动跃迁E.价电子跃迁2.属于光谱法的是()A.UV B.IR C.AAS D.MS E.X-ray3.属于非光谱分析法的是()A.UV B.IR C.X-ray D.CD E.AES(四)填空题1.当光照射到物质上时,光与物质之间便产生光的、、、等现象。
2.按产生光谱的方式不同,光谱法可以分为、、。
(五)名词解释1.吸收光谱法2.发射光谱法3.原子光谱法4.分子光谱法三、参考答案(一)判断题1.×2.√(二)单选题1.C 2.D 3.D 4.D 5.B 6.E 7.D(三)多选题1.CE 2.ABC 3.CD(四)填空题1.反射、散射、折射、吸收。
化学分析二级试题及答案

化学分析二级试题及答案一、选择题(每题2分,共20分)1. 以下哪种物质不属于碱?A. NaOHB. KOHC. NH4ClD. Ca(OH)22. 根据化学计量学,1摩尔物质的质量等于:A. 1克B. 其相对原子质量或相对分子质量的克数C. 1千克D. 其相对原子质量或相对分子质量的千克数3. 以下哪种元素的原子序数为2?A. 氢B. 氦C. 锂D. 铍4. 以下哪种化合物属于共价化合物?A. NaClB. MgOC. HClD. Fe5. 以下哪种物质是强酸?A. 醋酸B. 柠檬酸C. 碳酸D. 硫酸6. 以下哪种物质是强碱?A. 氢氧化钠B. 氢氧化钾C. 氢氧化铵D. 氢氧化镁7. 以下哪种物质是强电解质?A. 醋酸B. 乙醇C. 硫酸D. 蔗糖8. 以下哪种物质是弱电解质?A. 硫酸B. 氯化钠C. 醋酸D. 蔗糖9. 以下哪种物质是难溶性盐?A. NaClB. CaCO3C. KClD. Na2SO410. 以下哪种物质是可溶性盐?A. 硫酸钡B. 氯化银C. 氯化钠D. 碳酸钙二、填空题(每题2分,共20分)1. 化学方程式中,表示反应物和生成物的量的关系是______。
2. 摩尔质量的单位是______。
3. 元素周期表中,原子序数为1的元素是______。
4. 化学中,表示物质的量的单位是______。
5. 化学中,表示物质的量的单位是摩尔,其符号是______。
6. 氧化还原反应中,失去电子的物质被称为______。
7. 氧化还原反应中,获得电子的物质被称为______。
8. 根据化学计量学,1摩尔物质的质量等于其相对原子质量或相对分子质量的______。
9. 强酸是指在水溶液中完全电离的酸,例如______。
10. 强碱是指在水溶液中完全电离的碱,例如______。
三、简答题(每题10分,共30分)1. 描述什么是化学平衡,并举例说明。
2. 解释什么是酸碱中和反应,并给出一个具体的反应方程式。
南京工业大学无机与分析化学试卷(下、A)

南京工业大学 无机与分析化学 试卷(下、下、A)A)(一页开卷一页开卷))2012—2013学年第二学期学年第二学期 使用班级使用班级 :全校相关专业:全校相关专业学院学院 专业专业 学号学号 姓名姓名题号题号 一 二 三 四 五 六 七 总分总分 得分得分一 、每题只有一个答案是正确的,请选择(每题2分,将答案填入答题表中)将答案填入答题表中)题号题号12 3 4 5 6 7 8 9 10 答案答案 题号题号 11 12 13 14 15 16 17 18 19 20 答案答案1. 取同浓度的Zn 2+-EDTA 配合物的溶液两份,分别用A :用NaOH 溶液控制pH=10.0,其条件稳定常数记作K'ZnY ZnY,A ,A ,B :用氨-氯化铵缓冲溶液控制pH= 10.0,条件稳定常数记作K'ZnY ZnY,B ,B ,。
正确的关系式是:正确的关系式是:2. 佛尔哈德法测定Cl -时,使用的指示剂是:时,使用的指示剂是:(A) Ag 2CrO 4 (B) 二氯荧光黄二氯荧光黄 (C) 甲基橙 (D) FeNH 4(SO 4)2 3. 在下列物质中,不能将KI 氧化成I 2的是:的是: (A) KIO 3 (B) FeNH 4(SO 4)2 (C) Fe(NH 4)2(SO 4)2 (D) CuSO 44. 下列说法正确的是:下列说法正确的是:(A) 非构晶离子的盐浓度越大,沉淀溶解度越大非构晶离子的盐浓度越大,沉淀溶解度越大 (B) 非构晶离子的盐浓度越大,沉淀溶解度越小非构晶离子的盐浓度越大,沉淀溶解度越小(C) 两种沉淀的溶度积相比,溶度积小的溶解度也小两种沉淀的溶度积相比,溶度积小的溶解度也小 (D) 不同种类沉淀的溶解度越大,溶度积也越大不同种类沉淀的溶解度越大,溶度积也越大5. 从磷元素的电位图φo (V) H 2PO 2-____-2.25V ____P 4_______________PH 3 |_____________-1.23V -1.23V____________| 可计算电对P 4/ PH 3的标准电极电位φo P4/PH3为:为:(A) -1.02V (B) -1.74V (C) -0.89V (D) -1.16V 6. 在配离子[Co(C 2O 4)2(en)]-中(en 为H 2N-CH 2-CH 2-NH 2),中心离子Co 3+的配位数是:的配位数是:(A) 3 (B) 4 (C) 5 (D) 6 7. 用Na 2C 2O 4标定KMnO 4,加入第一滴KMnO 4时,KMnO 4的紫红色不会立即退去,这是因为反应速度不够快,若使第一滴KMnO 4很快退色,最有效的措施是:很快退色,最有效的措施是:(A) 加大H 2C 2O 4浓度浓度(B) 加大酸度加大酸度 (C) 事先加入Mn 2+ (D) 加快滴KMnO 4的速度的速度opH lgαY(H)pH lgαY(H)pH lgαY(H)0.0 23.64 5.0 6.45 10.0 0.45 1.0 18.01 6.0 4.65 11.0 0.07 2.0 13.51 7.0 3.32 12.0 0.01 3.0 10.60 8.0 2.27 4.0 8.44 9.0 1.28 17. 碘量法中所用的指示剂为:碘量法中所用的指示剂为: (A) 淀粉溶液淀粉溶液 (B) 二甲酚橙二甲酚橙 (C) 亚甲基蓝亚甲基蓝 (D) 二苯胺磺酸钠二苯胺磺酸钠18. 晶形沉淀陈化的主要目的是:晶形沉淀陈化的主要目的是:(A) 增大沉淀的溶解度增大沉淀的溶解度 (B) 小颗粒长大,使沉淀更纯净小颗粒长大,使沉淀更纯净 (C) 避免后沉淀现象避免后沉淀现象 (D) 形成非晶型沉淀形成非晶型沉淀19. 当含有Mg 2+、Na +、Ag +、Al 3+离子混合液流过阳离子交换树脂时,最先流出和最后流出的离子分别是:的离子分别是:(A) Na +,Mg 2+(B) Ag +,Al 3+(C) Na +,Al 3+(D) Mg 2+,Ag +20. 已知M 与EDTA(Y)的lg K MY = 13.2,在pH = 5.0的HAc-NaAc 缓冲溶液中,αY(H) =106.45;αM(L) =102.4;αM(OH) =100.4;则在此条件下,lgK’MY 为:为: (A) 6.75 (B) 4.35 (C) 3.95 (D) 2.95 二、填空和简单计算(每题2分) 1. 称取0.3581g 的ZnO(M = 81.38)定容250.00mL ,吸取该溶液20.00mL ,用EDTA 溶液滴定。
南京工业大学无机分析化学题库试题1

南京工业大学无机分析化学题库试题1第二学期模拟试卷一、选择题1. 配合物[Cu(NH3)4]SO4的导电性和加入Ba2+后的现象是:(A) 导电、有沉淀(B) 导电、无沉淀(C) 不导电、有沉淀(D) 不导电、无沉淀2. 当0.01mol氯化铬(III)(CrCl3·6H2O)在水溶液中用过量的硝酸银处理时,有0.02mol 氯化银沉淀析出,此样品的分子式应表示为:(A) [Cr(H2O)6]Cl3 (B) [CrCl(H2O)5]Cl2 (C) [CrCl2(H2O)4]Cl (D)[CrCl3(H2O)3]3. 根据晶体场理论,形成高自旋配合物的理论判据是:(A) 晶体场分裂能>电子成对能(B) 电离能>电子成对能(C) 晶体场分裂能>成键能(D) 电子成对能>晶体场分裂能4. 有关EDTA酸效应的叙述中,正确的是:(A) pH越大,αY(H)越大(B) pH越大,αY(H)越小(C) pH值愈大,酸效应系数愈大(D) 酸度越大,酸效应系数愈小5. 关于EDTA滴定法滴定突跃的说法不正确的是(忽略金属离子的水解):(A) pH越大,突跃范围越小(B) KMY越大,突跃范围越大(C) M或Y浓度约达,突跃范围越大(D) pH越大,突跃范围越大6. 在化学反应Mn(NO3)2 + PbO2 + HNO3→HMnO4 + Pb(NO3)2中,还原剂是:(A) Pb(NO3)2 (B) PbO2 (C) Mn(NO3)2 (D) HMnO47. 原电池(-)Zn│Zn2+(mo l?L-1 )‖Ag+(mo l?L-1 )│Ag(+),已知:φoAg+/Ag=0.80V,φoZn2+/Zn=-0.76V,在298.15 K 时,该电池的反应平衡常数lgKθ为:(A) 26.4 (B) 52.9 (C) 63.3 (D) 79.8. Cr2O72- + 14H+ + 6e = 2Cr3+ + 7H2O;能斯特方程表达式是:(A) φCr2O72-/Cr2+ = φoCr2O72-/Cr3+ + 0.059lg [Cr2O72-](B) φCr2O72-/Cr2+ = φoCr2O72-/Cr3+ + 0.059/3 lg [Cr2O72-][H+]14/[ Cr3+](C) φCr2O72-/Cr2+ = φoCr2O72-/Cr3+ + 0.059/3 lg [Cr2O72-][H+]14/[ Cr3+]2(D) φCr2O72-/Cr2+ = φoCr2O72-/Cr3+ + 0.059/6 lg [Cr2O72-]/[ Cr3+]29. 用Na2C2O4标定KMnO4,加入第一滴KMnO4时,KMnO4的紫红色不会立即退去,这是因为反应速度不够快,若使第一滴KMnO4很快退色,有效的措施是:(A) 加大H2C2O4浓度(B) 加大酸度(C) 加快滴KMnO4的速度(D) 加热10. φo Cr2O72-/ Cr3+ = 1.33V,φoFe3+/Fe2+= 0.68V,以K2Cr2O7滴定Fe2+,([H+]=1mol·L-1)滴淀突跃范围为:(A) 0.86~1.15V (B) 0.86~1.33V (C) 0.68~1.33V (D) 0.68~1.14V11. 可以用作标定Na2S2O3标准溶液的基准物质是:(A) KBrO3 (B) K2S2O8 (C) ZnO (D) 无水Na2CO312. 下列测定中需要加热的有:(A) KMnO4溶液测定H2O2 (B) KMnO4法测定MnO2(C) 碘量法测定Na2S (D) 溴量法测定苯酚13. 晶形沉淀陈化的目的是:(A) 增大沉淀的溶解度(B) 小颗粒长大,使沉淀更纯净(C) 避免后沉淀现象(D) 形成非晶型沉淀14. BaSO4在稀硫酸、氯化钠、EDTA和水中溶解度从大到小的顺序为:(A) EDTA>NaCl> H2O>稀H2SO4 (B) EDTA>NaCl>稀H2SO4>H2O(C) NaCl>稀H2SO4>H2O> EDTA (D) 稀H2SO4>NaCl>EDTA>H2O15. 进行重量法分析,下列说法正确的是:(A) 欲使沉淀净化,洗涤水量越多越好(B) 非晶型沉淀,一定用热溶液洗涤(C) 沉淀的洗涤剂只能是蒸馏水(D) 沉淀的体积越大越易洗净16. 下列哪组试剂是佛尔哈德法测定Cl-时全需使用?(A) FeNH4(SO4)2、K2CrO4 (B) KSCN、FeNH4(SO4)2(C) Fe(NH4)2(SO4)2 、硝基苯(D) K2CrO4、硝基苯17. 锰形成多种氧化态的化合物,其中最稳定的是:(A) 酸性介质中的Mn (Ⅱ) (B) 酸性介质中的Mn (Ⅶ)(C) 中性介质中的Mn (Ⅳ) (D) 中性介质中的Mn (Ⅵ)18. 下列混合离子能用氨水分离的是:(A) Cr3+和Cu2+ (B) Cu2+和Zn2+ (C) Fe3+和Cr3+ (D) Cr3+和Zn2+19. K+与四苯硼钠可以形成晶体沉淀,这种沉淀是:(A) 离子化合物(B) 螯合物(C) 分子晶体化合物(D) 离子对化合物20. 用等体积萃取并要求一次萃取率不小于99%,则分配比最小为:(A) 50 (B) 100 (C) 99 (D) 199二、填充题1. 配合物[Co(en)3]Cl3(en为乙二胺简写符号)的名称为______________________。
无机分析化学试卷B卷

南京工业大学无机与分析化学试卷(下、B)(一页开卷)2012—2013学年第二学期使用班级:全校相关专业学院专业学号姓名题号一二三四五六七总分得分一、每题只有一个答案是正确的,请选择(每题2分,将答案填入答题表中)题号12345678910答案题号11121314151617181920答案1. 在酸性溶液中,以0.1000 mo l•L-1的Ce4+溶液滴定0.1000 mo l•L-1的Fe2+溶液,化学计量点的电位为1.06V,对此滴定最适宜的指示剂是:(A) 次甲基蓝(φo=0.53V)(B) 二苯胺磺酸钠(φo=0.84V)(C) 邻二氮菲亚铁(φo=1.06V)(D) 硝基邻二氮菲亚铁(φo=1.25V)2. 配离子[FeEDTA]-中Fe3+配位数为:(A) 2 (B) 4 (C) 5 (D) 63. 已知lgK MY=9.65,[M] = 0.01000mol/L。
pH=7.0,lgαY(H) = 3.32;pH=8.0,lgαY(H) = 2.27;pH=9.0,lgαY(H) = 1.28;pH=10.0,lgαY(H) = 0.45。
对M进行准确滴定的最低pH为:(A) 7.0 (B) 8.0 (C) 9.0 (D) 10.04. 在间接碘量法中,最后以淀粉为指示剂,用Na2S2O3标准溶液滴定生成的I2。
加入淀粉指示剂最适宜的时间是:(A) 滴定开始时(B) 溶液变为浅黄色时(C) 溶液变为无色时(D) 溶液变为蓝色时5. 若配制EDTA溶液时所用的水中含有Ca2+,在pH =12.00下,以CaCO3为基准物质标定EDTA溶液。
然后用此标准溶液在pH = 2左右滴定试样中的Fe3+,Fe3+测定结果:(A) 偏低(B) 偏高(C) 正常(D) 不确定6. 已知:φo Fe3+/Fe2+=0.77 V,φo I2/I-=0.535 V,φo BrO3-/Br-=1.44 V,φo Cu2+/Cu+=0.17 V,K sp(CuI) = 1.1×10-12。
南京工业大学分析化学试卷2

一、选择题(每题2分,共30分)1 下列数据中有效数字是3位的是( )(A) 1.003 mol/L (B) pH = 12.003 (C) 1.230 mol/L (D) pH = 1.23 2 可以减小偶然误差的有效措施为( )(A) 增加平行测定的次数 (B) 采用高纯水和高纯试剂(C) 对测量仪器进行校正 (D) 做对照试验3 用高锰酸钾法测定Ca 2+,Ca 2+与MnO 4-之间的化学计量关系为n (Ca)/n (KMnO 4)为( )(A) 2 (B) 5/2 (C) 5 (D) 2/54 下列物质不能直接用NaOH 标准溶液准确滴定的是( )(A) 邻苯二甲酸氢钾 (B) HAc (C) NH 4+ (D) H 2C 2O 4 5欲配制pH=3左右的缓冲溶液,应选择下列何种酸和它的共轭碱( )(A) HAc (pK a =4.74) (B) 甲酸 (pK a =3.74)(C) 一氯乙酸 (pK a =2.86) (D) 二氯乙酸(pK a =1.30)6 欲用EDTA 标准溶液滴定Bi 3+、Pb 2+混合液中的Bi 3+而使Pb 2+不干扰,下列哪种方法较好(94.27lg =BiY K ,04.18lg =PbY K ,4.303)(,=O H Bi sp pK ,93.143)(,=O H Bi sp pK )( )(A) 适当降低pH 值,利用酸效应进行分别滴定(B) 适当提高pH 值,利用酸效应进行分别滴定(C) 将Bi 3+沉淀为Bi(OH)3,过滤分离出Bi(OH)3,用酸溶解后滴定Bi 3+(D) 将Pb 2+沉淀为Pb(OH)2,过滤分离出Pb(OH)2后,滴定Bi 3+7 已知69.10lg =CaY K , pH 6.0 7.0 8.0 9.0 10.0 11.0 12.0 )(lg H Y α 4.65 3.32 2.27 1.28 0.45 0.07 0.01用0.02mol/L EDTA 滴定0.02 mol/L Ca 2+,允许相对误差为0.1%,则最低允许pH 值为( )(A) pH ≈6 (B) pH ≈8 (C) pH ≈10 (D) pH ≈127 以MgY-EBT 为指示剂用EDTA 滴定Ca 2+,终点时的颜色变化为( )(A) MgY → Mg-EBT (B) Ca-EBT → EBT(C) Mg-EBT → EBT (D) EBT → Ca-EBT8 在含有Fe 3+和Fe 2+的溶液中,加入下述何种溶液,Fe 3+/Fe 2+电对的实际电位将上升( )(A) 稀H 2SO 4 (B) 三乙醇胺 (C) NH 4F (D) K 2Cr 2O 79 已知在1 mol/L HCl 溶液中,V 68.0E '0Fe /Fe 23=++,V 14.0E '0Sn/Sn 24=++。
南师期末分析化学试卷2(含答案)

南师期末分析化学试卷2(含答案)-CAL-FENGHAI.-(YICAI)-Company One121.下列论述中,最能说明偶然误差小的是( ) A .高精密度 B .标准偏差大C .仔细校正过所有砝码和容量仪器D .与已知含量的试样多次分析结果的平均值一致 2.采用什么方法可以减小分析测试中的偶然误差( )A .仪器校正B .空白试验C .对照试验D .增加平行测定次数 3.以0.4000 mol/L NaOH 滴定0.4000 mol/L 柠檬酸(H 3A)可以准确滴定到终点(K a1=7.4×10-4, K a2=1.7×10-5, K a3=4.0×10-7)( ) A .H 2A - B .HA 2- C .A 3- D . HA 2- 及 H 2A -4.与缓冲溶液的缓冲容量大小有关的因素是( )A .缓冲溶液的pH 范围B .缓冲溶液的总浓度和组分的浓度比200 年 月江苏省高等教育自学考试 284634201定量分析化学(二)一、 单项选择题(每小题 1 分,共 20分)在下列每小题的四个备选答案中选出一个正确的答案,并将其字母标号填入题干的括号内。
C.外加的酸量 D.外加的碱量5.以HCl滴定一碱溶液,先用酚酞作指示剂,滴定至终点时体积为V1,加入甲基橙后继续滴定,至变橙色时体积为V2,结果是V1=V2≠0,所以碱液的组成物质为 ( )A.NaOH+Na2CO3 B.纯Na2CO3C.NaHCO3+ Na2CO3 D.纯NaHCO36. 0.1 mol/L NaOH滴定0.1 mol/L HCOOH(K a=1.8×10-4)的滴定曲线同用0.1 mol/L NaOH滴定0.1 mol/L HAc(K a=1.8×10-5)的滴定曲线相比,滴定曲线的不同处是( )A.在计量点以前的曲线部分pH值更大B.在计量点以前的曲线部分pH值更小C.在计量点以后的曲线部分pH值更大D.在计量点以后的曲线部分pH值更小7. 0.2 mol/L HCl滴定0.2 mol/L NH3·H2O(K b=1.8×10-5)的滴定曲线同用0.02 mol/LHCl滴定0.02 mol/L NH3·H2O的滴定曲线相比,滴定曲线的不同处是( )A.在计量点以前的曲线部分pH值更大B.在计量点以前的曲线部分pH值更小C.在计量点以后的曲线部分pH值更大D.在计量点以后的曲线部分pH值更小38.用铈量法测定铁时,滴定至50%时的电位是多少()[已知此条件时EФ’(Ce4+/Ce3+)=1.44V,EФ’(Fe3+/Fe2+)=0.68V] A.0.68V B.1.44V C.1.06V D.0.86V9. 0.05 mol/LSnCl2溶液10 mL与0.10 mol/LFeCl3溶液20 mL相混合,平衡体系的电位是多少?()[已知此条件时EФ’(Fe3+/Fe2+)=0.68V,EФ’(Sn4+/Sn2+)=0.14V] A.0.14V B.0.32V C.0.50V D.0.68V10.用EDTA直接滴定金属离子,终点所呈现的颜色是 ( )A.指示剂—金属离子络合物的颜色B.游离指示剂的颜色C.EDTA—金属离子络合物的颜色D.上述B与C的混合颜色11.在Ca2+、Mg2+的混合溶液中,用EDTA法测定Ca2+,要消除Mg2+的干扰,宜用()A.控制酸度法 B.络合掩蔽法C.氧化还原掩蔽法 D.沉淀掩蔽法12.在含有Fe3+和Fe2+的溶液中,加入下述何种溶液,Fe3+/Fe2+电对的电位将降低(不考虑离子强度的影响)( )A.稀H2SO4 B.HCl C.NH4F D.邻二氮菲4513.当两电对的电子转移数均为2时,为使反应完全度达到99.9%,两电对的条件电位差至少应大于( )A .0.09VB .0.18VC .0.27VD .0.36V 14.用佛尔哈德法测定Ag +,滴定剂是什么( )A .NaClB .NaBrC .NH 4SCND .Na 2S15.在重量分析法中,待测物质中含的杂质与待测的离子半径相近,在沉淀过程中往往形成( )A .混晶B .吸留C .表面吸附D .后沉淀 16.下列阴离子的水溶液,若浓度(单位:mol/L )相同,则碱度最强的是( )A .CN - (HCN K a =6.2×10-10)B .S 2- (H 2S K a1=1.3×10-7 K a2=7.1×10-15 )C .F - (HF K a =1.8×10-4)D .Cl - (K HC l ≥1)17.1 mol/LHAc 与1 mol/LNaAc 等体积混合溶液的H +浓度(单位:mol/L )的计算公式是( )A .[]c K H a •=+1 B .[]21a a K K H •=+ C .[]bwK cK H =+ D .[]盐酸c c K H a =+18.关于Na 2CO 3在水溶液中质子条件是( )6A .[][][][]--++=++OH HCO Na H 32B .[][][][]--+=++OH HCO CO H H 3322C .[][][][]--+=++OH HCO CO H H 332D .[][][][]---++=++2332CO OH HCO H19.下列这些物质中,不能用标准强酸溶液直接滴定的是( ) A .Na 2CO 3 (H 2CO 3 K a1=4.2×10-7 K a2=5.6×10-10) B .Na 2B 4O 7·10H 2O (H 3BO 3 K a =5.8×10-10) C .NaAc (HAc K a =1.8×10-5)D .Na 3PO 4 (H 3PO 4 K a1=7.6×10-3 K a2=6.3×10-8 K a3=4.4×10-13 20.下列有关沉淀操作的叙述,正确的是( ) A .沉淀BaSO 4时不需陈化 B .用纯水洗涤AgCl C .用稀HCl 洗涤H 2SiO 3 D .在400℃下灼烧CaC 2O 4沉淀21.NH 3的K b =1.8×10-5 ,ph-COO -的K a =6.2×10-5,CO 32-的K a1=4.2×10-7, K a2=5.6×10-11,HC 2O 4-的K a1=5.9×10-2, K a2=6.4×10-5,其碱性由强到弱为 (1) ; (2) ; (3) ; (4) 。
(完整word版)南京工业大学2010-2011年分析化学试卷1.doc

一、选择题(每小题 2 分,共 40 分)1(A)(B)(C)(D)23(A) 1.030 mol/L (B) pH = 12.023(C) 1.023 mol/L (D) pH = 1.233(A) (B)(C)(D)4 NaOH(A)K b = 4.6× 10-10 (B) NH 4NO 3 NH 3 K b = 1.8× 10-5(C)K a =1.4×10-4(D) Na 2SO 45 pH 3(A) HAc pK =4.74(B) pKa =3.74a(C)pK a =2.86 (D)pK a =1.306 H 3PO 42.12 7.20 12.36NaOHpH(A) 2.12(B) 5.66(C) 7.20(D) 9.787nn(A)(C)Y(H)Y(H)1K a i[ H]i(B)i 1niH[ H ] i1(D)i1Y(H)Y(H)1[ H ] ii 1n [H ]i 1K a ii 18EDTABi 3+ Pb 2+ Bi 3+Pb 2+lg K BiY27.94 lg K PbY 18.04 pK sp,Bi(OH) 3 30.4 pK sp,Bi(OH) 3 14.93(A) pH(B) pH(C) Bi 3+Bi(OH) 3Bi(OH) 3Bi 3+(D) Pb 2+Pb(OH) 2Bi 3+9lg K ZnY16.5pH45 67lgY(H)8.44 6.454.563.200.02000 mol/L EDTA0.02 mol/L Zn2+0.1%(A) pH 4(B) pH 6(C) pH8(D) pH 1010Fe 3+ Fe 2+Fe 3+/Fe 2+(A)H SO4(B)(C) NHF(D) K Cr O7242 211E 0' 4/Ce 31.44 V E 0' 3/Fe 20.68VCe 4++ Fe 2+ = Ce 3+ + Fe 3+CeFeFe 3+ Fe 2+(A) 1.08 × 10-18 (B) 92.5(C) 36.2(D) 2.76 × 106(A) [Fe 3+ ]=[Cr 3+ ], [Fe 2+2-] (B) 3+ 3+2+2- ]]=[Cr 2 O 73[Fe ]=[Cr] , [Fe]=6[Cr 2O 7(C) [Fe 3+]=3[Cr 3+], [Fe 2+]=6[Cr 2O 72- ] (D) [Fe 3+]=3[Cr 3+] , 6[Fe 2+]=[Cr 2O 72- ]13 间接碘量法的主要误差来源是 ()(A) 碘的挥发和空气中的氧对碘离子的氧化 (C) 淀粉指示剂对大量碘的吸附(B) 碘的溶解度较小,易在溶液中析出(D) 碘的黄色褪去不易观察14 在不另加试剂的情况下, 可以用莫尔法直接滴定的含氯试样是()(A) FeCl3(B) BaCl2(C) NaCl + NaS (D) NaCl + Na SO42215 某荧光吸附指示剂 HFl 形式为黄色,游离的 Fl -形式呈蓝色, Fl -被吸附后显紫红色。
南京工业大学无机分析化学试题

南京工业大学无机分析化学试题一、选择题1.可与Cu2+形成螯合物的配体是(A) CN- (B) EDTA (C) -NO2 (D) CO2. [FeF6]3-为外轨型配合物。
其中心原子的杂化轨道类型和磁矩为:(A) 4s14p34d2;5.75μB (B) 3d24s14p3;1.73μB(C) 4s14p34d2;1.73μB (D) 3d24s14p3;5.75μB3. Cr2+有4个3d电子,配位体为水时,△o = 13876cm-1;Ep = 27835cm-1。
则[Cr(H2O)6]2+自旋状态和磁矩的正确结论是:(A) 高自旋;2.83μB (B) 低自旋;2.83μB (C) 高自旋;4.90μB (D) 低自旋;4.90μB4. EDTA与Ca2+、Mg2+、Al3+配合物稳定常数的次序是:(A) Al3+>Ca2+>Mg2+ (B) Ca2+>Mg2+>Al3+ (C) Mg2+>Al3+>Ca2+ (D) Al3+>Mg2+>Ca2+5. 若配制EDTA溶液时所用的水中含有Ca2+,以ZnO为基准物质标定EDTA溶液(pH =4.50),然后用此标准溶液在pH = 10.00左右滴定试样中的Zn2+,测定结果:(A) 偏高(B) 偏低(C) 正常(D) 不确定6. 在氧化还原反应中,产物中氧原子数比反应物增加,反应介质为:(A) 酸性(B) 碱性(C) 中性(D) 酸性或碱性均可7. 为了明显提高铜锌原电池的电动势,采取的正确措施是:(A) 在ZnSO4溶液中加固体酸(B) 在CuSO4溶液中加水(C) 在ZnSO4溶液中加氨水(D) 在CuSO4溶液中加氨水8. Cr2O72- + 14H+ + 6e = 2Cr3+ + 7H2O;下列哪个措施可提高φCr2O72-/Cr3+?(A) 提高pH (B) 提高酸度(C) 提高Cr3+的浓度(D) 将Cr2O72-转化为CrO42-9. 用KMnO4定量氧化还原性物质时,调节溶液酸度使用的是:(A) HAc (B) HCl (C) HNO3 (D) H2SO410. φo MnO4-/ Mn2+ = 1.45V,φoSn4+/Sn2+= 0.15V,以KMnO4滴定Sn2+,([H+]=1mol·L-1)滴至50%时的电极电位为:(A) 0.73V (B) 0.15V (C) 0.80V (D) 0.65V11. 可以用作标定KMnO4标准溶液的基准物质是:(A) CaCO3 (B) Fe(NH4)2(SO4)2 (C) K2S2O8 (D) SnCl212. 用KMnO4溶液滴定H2O2时,发现有沉淀生成,原因是:(A) pH太大,生成MnO2沉淀(B) 溶液酸度太大,形成HMnO4沉淀(C) H2O2生成了沉淀物(D) pH太大,生成Mn(OH)2沉淀13. 下列说法正确的是:(A) 聚集速度越大越易形成晶体沉淀(B) 过饱和度越大,定向速度越大(C) 聚集速度越小越易形成晶体沉淀(D) 过饱和度越小,定向速度越大14. 在CaC2O4沉淀中加入同体积、同浓度的液体,溶解度最大的是:A) NH3(B) KNO3 (C) EDTA (D) NaCl15. 进行重量法分析,下列说法正确的是:(A) 沉淀必须在灼烧后才能称量(B) 沉淀只能在烘干后称量(C) 氢氧化物必须在灼烧后才能称量(D) 氢氧化物可在烘干后称量16. 佛尔哈德法测定Cl-时,使用的指示剂是:(A) Ag2CrO4 (B) 二氯荧光黄(C) Fe(NH4)2(SO4)2 (D) FeNH4(SO4)217. 实验室用来洗涤玻璃仪器的洗液组成是:(A) 浓盐酸和硝酸(B) 浓硫酸和重铬酸钾(C) 硝酸和重铬酸钾(D) 硝酸和硫酸18. 碱性BaCl2溶液与K2Cr2O7溶液混合生成的沉淀是:(A) 黄色BaCrO4 (B) 橙色BaCrO4 (C) 黄色BaCr2O7 (D) 橙色BaCr2O719. 阴离子交换树脂可分离下列哪组物质?(A) 氯化钠和氯化钾(B) 苯酚和醋酸(C) 氯化钠和溴化钠(D) 水和NaOH20. 用等体积萃取并要求一次萃取率不小于99%,则分配比最小为:(A) 50 (B) 100 (C) 99 (D) 199二、填充题1. 配合物[Co(en)3]Cl3(en为乙二胺简写符号)的名称为______________________。
南京工业大学无机与分析化学第一学期模拟试卷

第一学期模拟试卷一、选择题1、已知NaOH的浓度为0.0010 mol/L,其pH值表达正确的是:(A) 3 (B) 3.0 (C) 11.00 (D) 11.02、下列哪一项是铝的基态电子层结构?(A) 1s22s22p63s3 (B) 1s22s22p63s23p1(C) 1s22s22p63s13p4 (D) 1s22s22p63s23p43、表示电子运动状态的四个量子数(依次为n、l、m、ms)不合理的是:(A) 2、1、0、-1/2 (B) 2、1、0、-1/2(C) 3、0、0、+1/2 (D) 2、2、0、+1/24、A原子电子排布为1s22s22p53s1;B原子电子排布为1s22s22p63s1。
A和B状态是:(A) A激发态;B基态 (B) A、B均为激发态(C) B激发态;A基态 (D) A、B均为基态5、最外电子层的电子排布为3s23p6的元素的原子序数是:(A) 14 (B) 16 (C) 18 (D) 206、下列物质中,没有离子键,只有共价键的是:(A) SiO2 (B) (NH4)2SO4(C) NaCl (D) BaO7、下列分子中,键角最小的是:(A) AlCl3 (B) H2O (C) 金刚石 (D) MgCl28、 O2、H2S、NH3、NaCl化学键极性从强到弱顺序为:(A) O2> H2S> NH3> NaCl (B) H2S> NH3> NaCl> O2(C) NH3> NaCl> O2> H2S (D) NaCl> NH3> H2S> O29、空间构型是四面体的分子是:(A) C2H4(B) SF6(C) GeCl4(D) CO210、下列关于σ键和π键的说法不正确的是:(A) 共价键既可以是σ键,也可以是π键(B) s轨道和p轨道之间只能形成σ键(C) 三键的键能是单键键能的三倍(D) p轨道和p轨道之间既可形成σ键,也可形成π键11、已知HgCl2的中心原子Hg的杂化方式是:(A) sp杂化 (B) sp2杂化 (C) 等性sp3杂化 (D) 不等性sp3杂化12、在极性分子中存在哪些偶极矩?(A) 瞬间偶极矩 (B) 诱导偶极矩 (C) 固有偶极矩 (D) 以上都存在13、下列物质的熔点由高到低的顺序为:(A) C(金刚石) > CuCl2 > H2O > H2S (B) CuCl2> C(金刚石) > H2O > H2S(C) C(金刚石) > CuCl2 > H2S > H2O (D) CuCl2> C(金刚石) > H2S > H2O14、反应2HgO(s) = 2Hg(g) + O2(g) 是一个吸热反应,此反应的标准平衡常数K,说法正确的是:(A) 温度升高K增加 (B) 压力升高K增加(C) 温度升高K降低 (D) K与T、P无关15、化学反应 Sn (s)+2Cl2(g)= SnCl4(g)已达平衡,该反应是放热反应。
南京工业大学无机与分析化学模拟卷2

模拟卷二一、单项选择题1. 元素N的核外电子正确排布是:(A) 1s22s22p x1p y1p z1(B) 1s22s12p x2p y1p z1(C) 1s22s22p x2p y1(D) 1s22s22p x1p y22. 下列那种物质可作为基准物质标定NaOH?(A) 1mol/L的HCl(B) 无水Na2CO3(C) FeSO4(D) 邻苯二甲酸氢钾3. 已知HAc的浓度为0.12 mol/L,其pH值表达正确的是:(A) 2.8 (B) 2.83 (C) 2.833 (D) 2.83284. 实验数据的精密度不好,最可能的引起原因是:(A) 系统误差所致(B) 实验操作不熟练(C) 偶然误差太大(D) 实验次数太少5. 下列完全正确的4个量子(依次为n,l,m,m s)数组合是:(A) 3、3、-2、+1/2 (B) 3、2、5、+1/2 (C) 3、2、-1、-1/2 (D) 3、1、-1、+16. 下列化学键中具有“键角”参数的物质是:(A) 金属Zn (B) KCl (C) HCl (D) H2S7. CO2中碳原子C中的2s和2p轨道采取:(A) sp杂化(B) sp2杂化(C) 等性sp3杂化(D) 不等性sp3杂化8. O2、H2S、NH3、NaCl化学键极性从强到弱顺序为:(A) O2> H2S> NH3> NaCl (B) H2S> NH3 > NaCl> O2(C) NH3> NaCl> O2> H2S (D) NaCl> NH3 > H2S> O29. BaS、BaO、NaCl、NaF晶体的熔点从高到低的顺序为:(A) BaS>BaO>NaCl>NaF (B) BaO>NaF>BaS>NaCl(C) BaO>BaS>NaF>NaCl (D) NaF>NaCl>BaS>BaO10. 下列那组物质是共轭酸碱(A) H2O和OH- (B)H3PO4和HPO42- (C)NaOH和HCl (D)H2SO4和H2SO311. 第29号元素为Cu,其亚铜离子溶液为无色,其核外电子排布式应为:(A) [Ar]3d104s1(B) [Ar]3d94s2(C) [Ar]3d105s1(D)[Ar]3d54p612. 欲配制pH=9~10的缓冲溶液,最好使用选择那种体系:(A) KH2PO4+K2HPO4 (K a2= 6.30×10-3) (B)NH3+NH4Cl (K b=1.8×10-5)(C) NaAc+HAc (K a=1.8×10-5) (D) KHSO3+H2SO3 (K a=1.3×10-2)13. HCl滴定某碱,突跃范围为pH=4.3~3.6,化学计量点的pH=3.95,且知溴甲酚绿的变色范pH=4.0~5.6 (黄~蓝,中间色为绿色),酚酞的变色范围为pH=8.0~10.0 (无色~红色),下列指示剂的选择及滴定终点的颜色均正确的是:(A) 溴甲酚绿,黄色(B) 溴甲酚绿,绿色(C) 酚酞,无色(D) 酚酞,红色14. 在下列物质中,能用强碱NaOH溶液直接滴定的溶液是:(A) NH4Cl (NH3的K b=1.8×10-5) (B) NH2OH (NH2O-的K b=9.1×10-9)(C) 苯酚(K a=1.1×10-10) (D) HCN (CN-的K b= 1.5×10-5)15. 下列分子中,键角最小的是:(A) AlCl3(B) PH3(C) CH4(D) MgBr216. 在化学反应中,催化剂的作用是:(A) 增大平衡常数K (B) 增大活化能(C) 降低活化能(D) 增加分子能量17. 根据离子极化和离子变形学说,下列物质在水中溶解度从大到小的顺序为:(A) CuI>CuCl>CuF>CuBr (B) CuI>CuBr>CuCl>CuF(C) CuF>CuI>CuCl>CuBr (D) CuF>CuCl>CuBr>CuI18. 已知下列反应的平衡常数:H2(g) + S(s) = H2S(s) K1、S(s) + O2(g) = SO2(g) K2则反应:H2(g) + SO2(g) = O2(g) + H2S(g) 的平衡常数K等于:(A) K1 + K2(B) K1-K2(C) K1·K2(D) K1/K219. 放热反应2NO(g) + O2(g) = 2NO2(g) 达平衡后,若分别采取:①增加反应的总压力;②用吸附剂吸附NO2,减少NO2的量;③减少O2的量;④升高温度(假设K不变);⑤加入催化剂。
南京工业大学 无机与分析化学 试卷(下、A)

南京工业大学无机与分析化学试卷(下、A)(一页开卷)2012—2013学年第二学期使用班级:全校相关专业学院专业学号姓名一1. 取同浓度的Zn2+-EDTA配合物的溶液两份,分别用A:用NaOH溶液控制pH=10.0,其条件稳定常数记作K'ZnY,A,B:用氨-氯化铵缓冲溶液控制pH= 10.0,条件稳定常数记作K'ZnY,B,。
正确的关系式是:2. 佛尔哈德法测定Cl-时,使用的指示剂是:(A) Ag2CrO4(B) 二氯荧光黄(C) 甲基橙(D) FeNH4(SO4)23. 在下列物质中,不能将KI氧化成I2的是:(A) KIO3 (B) FeNH4(SO4)2(C) Fe(NH4)2(SO4)2(D) CuSO44. 下列说法正确的是:(A) 非构晶离子的盐浓度越大,沉淀溶解度越大(B) 非构晶离子的盐浓度越大,沉淀溶解度越小(C) 两种沉淀的溶度积相比,溶度积小的溶解度也小(D) 不同种类沉淀的溶解度越大,溶度积也越大5. 从磷元素的电位图φo(V) H2PO2-____-2.25V____P4_______________PH3|_____________-1.23V____________|可计算电对P4/ PH3的标准电极电位φo P4/PH3为:(A) -1.02V (B) -1.74V (C) -0.89V (D) -1.16V6. 在配离子[Co(C2O4)2(en)]-中(en为H2N-CH2-CH2-NH2),中心离子Co3+的配位数是:(A) 3 (B) 4 (C) 5 (D) 67. 用Na2C2O4标定KMnO4,加入第一滴KMnO4时,KMnO4的紫红色不会立即退去,这是因为反应速度不够快,若使第一滴KMnO4很快退色,最有效的措施是:(A) 加大H2C2O4浓度(B) 加大酸度(C) 事先加入Mn2+(D) 加快滴KMnO4的速度8. 下列混合离子能用氨水分离的是:(A) Cr3+和Cu2+(B) Cu2+和Zn2+(C) SO42-和Cl-(D) Fe3+和Al3+9. φo Cr2O72-/ Cr3+ = 1.33V,φo Fe3+/Fe2+= 0.68V,以K2Cr2O7滴定Fe2+,([H+] = 2mol·L-1)滴至70%时,溶液的电极电位为:(A) 0.70V (B) 1.01V (C) 1.35V (D) 0.67V10. 已知lgK MY =14.51,[M] = 0.010mol·L-1。
分析化学2试题及答案

分析化学2试题及答案一、选择题(每题2分,共20分)1. 下列哪种物质不是分析化学中常用的缓冲溶液?A. 盐酸B. 醋酸C. 磷酸D. 硼酸答案:A2. 滴定分析中,滴定终点的判断依据是:A. 颜色变化B. 体积变化C. 温度变化D. 压力变化答案:A3. 原子吸收光谱法中,测定元素含量的基本原理是:A. 吸收光谱B. 散射光谱C. 荧光光谱D. 拉曼光谱答案:A4. 以下哪种仪器不适用于液相色谱分析?A. 紫外检测器B. 质谱检测器C. 红外光谱仪D. 荧光检测器答案:C5. 在电位滴定中,指示电极的作用是:A. 测量溶液的电导率B. 测量溶液的pH值C. 测量溶液的电位D. 测量溶液的电流答案:C6. 红外光谱分析中,用于识别分子中官能团的特征吸收峰是:A. 指纹区B. 吸收峰C. 反射峰D. 散射峰答案:A7. 质谱分析中,用于确定分子离子峰的是:A. 单电荷离子B. 双电荷离子C. 多电荷离子D. 负离子答案:A8. 以下哪种方法不是色谱分离技术?A. 纸色谱B. 薄层色谱C. 气相色谱D. 离心分离答案:D9. 在酸碱滴定中,如果滴定剂的浓度未知,可以通过:A. 标准溶液B. 空白试验C. 预滴定D. 后滴定答案:C10. 以下哪种物质不是分析化学中常用的指示剂?A. 酚酞B. 甲基橙C. 硫酸铜D. 溴酚蓝答案:C二、填空题(每空1分,共20分)1. 在酸碱滴定中,滴定剂的浓度通常是_________的。
答案:已知2. 原子吸收光谱法中,样品原子化的方法有_________、_________和_________。
答案:火焰、石墨炉、氢化物发生3. 高效液相色谱(HPLC)中,常用的检测器有_________、_________和_________。
答案:紫外、荧光、质谱4. 质谱分析中,分子离子峰的符号是_________。
答案:M+5. 在红外光谱分析中,_________区是用于鉴定分子中官能团的区域。
南京工业大学无机与分析化学试卷下A

南京工业大学无机与分析化学试卷(下、A)(一页开卷)2012—2013学年第二学期使用班级:全校相关专业学院专业学号姓名一1. 取同浓度的Zn2+-EDTA配合物的溶液两份,分别用A:用NaOH溶液控制pH=10.0,其条件稳定常数记作K'ZnY,A,B:用氨-氯化铵缓冲溶液控制pH= 10.0,条件稳定常数记作K'ZnY,B,。
正确的关系式是:2. 佛尔哈德法测定Cl-时,使用的指示剂是:(A) Ag2CrO4(B) 二氯荧光黄(C) 甲基橙(D) FeNH4(SO4)23. 在下列物质中,不能将KI氧化成I2的是:(A) KIO3 (B) FeNH4(SO4)2(C) Fe(NH4)2(SO4)2(D) CuSO44. 下列说法正确的是:(A) 非构晶离子的盐浓度越大,沉淀溶解度越大(B) 非构晶离子的盐浓度越大,沉淀溶解度越小(C) 两种沉淀的溶度积相比,溶度积小的溶解度也小(D) 不同种类沉淀的溶解度越大,溶度积也越大5. 从磷元素的电位图φo(V) H2PO2-____-2.25V____P4_______________PH3|_____________-1.23V____________|可计算电对P4/ PH3的标准电极电位φo P4/PH3为:(A) -1.02V (B) -1.74V (C) -0.89V (D) -1.16V6. 在配离子[Co(C2O4)2(en)]-中(en为H2N-CH2-CH2-NH2),中心离子Co3+的配位数是:(A) 3 (B) 4 (C) 5 (D) 67. 用Na2C2O4标定KMnO4,加入第一滴KMnO4时,KMnO4的紫红色不会立即退去,这是因为反应速度不够快,若使第一滴KMnO4很快退色,最有效的措施是:(A) 加大H2C2O4浓度(B) 加大酸度(C) 事先加入Mn2+(D) 加快滴KMnO4的速度8. 下列混合离子能用氨水分离的是:(A) Cr3+和Cu2+(B) Cu2+和Zn2+(C) SO42-和Cl-(D) Fe3+和Al3+9. φo Cr2O72-/ Cr3+ = 1.33V,φo Fe3+/Fe2+= 0.68V,以K2Cr2O7滴定Fe2+,([H+] = 2mol·L-1)滴至70%时,溶液的电极电位为:(A) 0.70V (B) 1.01V (C) 1.35V (D) 0.67V10. 已知lgK MY =14.51,[M] = 0.010mol·L-1。
南京工业大学有机化学期末试卷2.docx
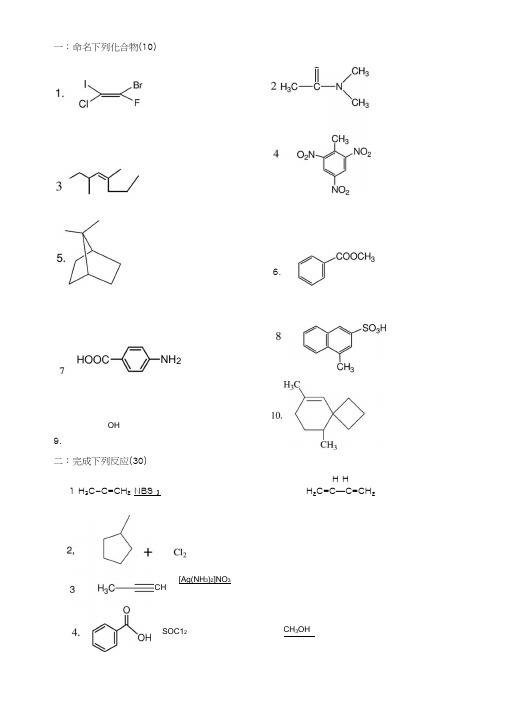
一:命名下列化合物(10)NH2OH9.二:完成下列反应(30)1 H3C-C=CH2 NBS 】CHSOC12[Ag(NH3)2]NO36.H HH2C=C—C=CH2CH3OH「NaOH 溶湮ClOHNaOH ---------------- JNaOH C2H5OH稀 NaOH+ H 2C=CHCH 3酸性+CH 3NaOH + Br 22 CH3OH干HCIHQ 丁 Zn/HAC(NH 4)2SNO 2KOHNHC 2H 5OHNaNO» HC1 0-5 °CCl(1) LiAlHj⑵水(CH 3)三:排序 (10 )1. 将下列化合物对亲电取代反应的容易程度排列成序2. 比较下列化合物的碱性(气态条件下)氨 甲胺二甲胺3. 将下列化合物中拨基与同一亲核试剂加成反应的活性排列成序POCH 3CH 3CH 2CHOCH3COCH34. 比较下列化合物的酸性C 6H 5OH CH3COOH CICH2COOH5. 比较下列卤代桂按S N I 反应的速度大小CH 3CH 2CH 2CH 2Br (CH3)3C Br四、区别下列各组化合物:(6)1丙烷,丙烯,丙烘2 2 ■丁醇节醇正丙醇五 用化学方法分离下列各组化合物(10)1. 苯、苯酚2. 2—丁醇与2—丁酮六 立体化学问题:用R/S 标出下列手性碳原子的构型(4分)9H3CH 3CH 2CHBr七、简答题(10分)1. 写出下述反应的机理:2.分子式为C 4H 6的三个异构体A,B,C 能发生如下反应:(1) 三个异构体都能和漠反应,对于等摩尔的样品而言,与B,C 反应的漠量是A 的两倍. (2) 三个都能和氯化氢发生反应,而B,C 在Hg+催化下得到同一产物 (3) B,C 能和硫酸汞的硫酸溶液作用,得到C 4H 8O 的化合物 (4) B 能和硝酸银的氨溶液作用牛成白色沉淀.试推测A,B,C 的结构,并写出有关反应的方程式.八用指定的原料合成下列各化合物(小分子试剂任选)(20)1以丙烯为原料合成1 一氯一 2, 3—二漠丙烷+———CH 3+2Br3.Br4. CH 3COCH 2COOC 2H 5COOH一:命名1. (E) 一1 一氟一2—氯一1—漠一2 —碘乙烯3. 3,5 —二甲基一4一辛烯5. 7,7—二甲基双环[221]庚烷7. 4-氨基苯甲酸9.甘油二:完成反应参考答案HI BrH2C—C=CH23. H3C ----------------- CHAg7.6OH11.10. CH3CH2NH2、甲ZOCH3OCH3—CHOo\^CHO2. N, N二甲基乙酰胺4. 2, 4, 6■三硝基甲苯6.苯甲酸甲酯8. 4■甲基・2■蔡磺酸10. 6, 9-二甲基螺[3,5]-5一壬烯三:排序2.二甲胺〉甲胺〉氨3.45.四:区别化合物1. 用硝酸银的钱溶液,酸性高猛酸钾溶液区别2. 卢卡斯试剂3.五:分离1. 加入NaOH 溶液,油层为苯,然后萃取。
最新南京工业大学 无机与分析化学 样2

南京工业大学无机与分析化学样21. Pb-EDTA(无色)、Pb-二甲酚橙(红色)、二甲酚橙(黄色)。
用EDTA滴定Pb2+,终点时,溶液的颜色如何突变?(A) 无色→红色 (B) 黄色→红色 (C) 红色→黄色 (D) 红色→无色2. 可与Cu2+形成螯合物的配体是:(A) CN- (B) EDTA (C) NO2- (D) CO3. 欲使BaCO3在水溶液中溶解度增大,可采用的方法是:(A) 加入1.0 mol·L-1NaOH (B) 加入1.0mol·L-1Na2CO3(C) 加入0.10 mol·L-1BaCl2(D) 降低溶液的pH值4. EDTA与Ca2+、Fe2+、Fe3+配合物稳定常数的次序是:(A) Ca2+>Fe2+>Fe3+ (B) Fe3+>Ca2+>Fe2+ (C) Fe2+>Fe3+>Ca2+ (D) Fe3+>Fe2+>Ca2+5. 碘量法中所用的指示剂为:(A)二甲酚橙 (B) 淀粉溶液 (C) 亚甲基蓝 (D) 二苯胺磺酸钠6. [FeF6]3-为外轨型配合物。
其中心原子的杂化轨道类型和理论磁矩为:(A) 4s14p34d2;5.92 µB (B)3d24s14p3;1.73 µB(C) 4s14p34d2;1.73 µB (D)3d24s14p3;5.92 µB7. 在pH = 12.00的溶液中,用EDTA滴定Ca2+和Mg2+混合液,测定的是:(A) Mg2+的量 (B) Ca2+的量 (C) Ca2+-Mg2+的量 (D) Ca2++Mg2+的量8. 从氧元素的电位图φo(V) O2 0.682V H2O2? H2O| 1.23V |求φo(H2O2/H2O)为:(A) 1.912V (B) 0.956V (C)0.548V (D) 1.778V9. 已知M的lg KMY =13.2,pH=5的氨缓冲溶液中,αY(H)=106.45;αM(L) =102.4;αM(OH) =100.4;则在此条件下,lgK'MY为:(A) 6.75 (B) 4.35 (C)3.95 (D) 2.9510. 在下列物质中,哪一个不能将KI氧化成I2:(A)KBrO3 (B)FeNH4(SO4)2(C)Fe(NH4)2(SO4)2(D)CuSO411. Cr2+有4个3d电子,配位体为水时,△o = 13876cm-1;E p = 27835cm-1。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
一、选择题(每题2分,共30分)
1 下列数据中有效数字是3位的是( )
(A) mol/L (B) pH = (C) mol/L (D) pH =
2 可以减小偶然误差的有效措施为( )
(A) 增加平行测定的次数 (B) 采用高纯水和高纯试剂
(C) 对测量仪器进行校正 (D) 做对照试验
3 用高锰酸钾法测定Ca 2+,Ca 2+与MnO 4-之间的化学计量关系为n (Ca)/n (KMnO 4)为( )
(A) 2 (B) 5/2 (C) 5 (D) 2/5
4 下列物质不能直接用NaOH 标准溶液准确滴定的是( )
(A) 邻苯二甲酸氢钾 (B) HAc (C) NH 4+ (D) H 2C 2O 4
5欲配制pH=3左右的缓冲溶液,应选择下列何种酸和它的共轭碱( )
(A) HAc (pK a = (B) 甲酸 (pK a =
(C) 一氯乙酸 (pK a = (D) 二氯乙酸(pK a =
6 欲用EDTA 标准溶液滴定Bi 3+、Pb 2+混合液中的Bi 3+而使Pb 2+不干扰,下列哪种方法较好(94.27lg =BiY K ,04.18lg =PbY K ,4.303)(,=OH Bi sp pK ,93.143)(,=OH Bi sp pK )( )
(A) 适当降低pH 值,利用酸效应进行分别滴定
(B) 适当提高pH 值,利用酸效应进行分别滴定
(C) 将Bi 3+沉淀为Bi(OH)3,过滤分离出Bi(OH)3,用酸溶解后滴定Bi 3+
(D) 将Pb 2+沉淀为Pb(OH)2,过滤分离出Pb(OH)2后,滴定Bi 3+
7 已知69.10lg =CaY K , pH
)(lg H Y α
用L EDTA 滴定 mol/L Ca 2+,允许相对误差为%,则最低允许pH 值为( )
(A) pH ≈6 (B) pH ≈8 (C) pH ≈10 (D) pH ≈12
7 以MgY-EBT 为指示剂用EDTA 滴定Ca 2+,终点时的颜色变化为( )
(A) MgY → Mg-EBT (B) Ca-EBT → EBT
(C) Mg-EBT → EBT (D) EBT → Ca-EBT
8 在含有Fe 3+和Fe 2+的溶液中,加入下述何种溶液,Fe 3+/Fe 2+电对的实际电位将上升( )
(A) 稀H 2SO 4 (B) 三乙醇胺 (C) NH 4F (D) K 2Cr 2O 7
9 已知在1 mol/L HCl 溶液中,V 68.0E '0Fe /Fe 23=++,V 14.0E '0Sn /Sn 24=+
+。
若20 mL mol/L Fe 3+的HCl 溶液与40 mL L SnCl 2溶液相混合,平衡时体系的电位是( )
(A) (B) (C) (D)
10 已知V 44.1E '0Ce /Ce 34=++, V 68.0E '0Fe /Fe 23=+
+,则下列反应:Ce 4+ + Fe 2+ = Ce 3+ + Fe 3+在达到化学计量点时,溶液中++23Fe Fe c /c 值为( )
(A) ×10-18 (B) (C) (D) ×106
11某荧光吸附指示剂HFl 形式为黄色,Fl -形式为黄绿色,。
Fl -的被吸附后显粉红色。
碱性条件下,将其加入用NaCl 滴定AgNO 3的体系中,化学计量点后,应呈现的颜色是( )
(A) 黄色 (B) 黄绿色 (C) 粉红色 (D) 不变色
12 移取FeCl 3溶液,用含HCl 的乙醚溶液萃取,已知FeCl 3在乙醚和水中的分配比D=100,则上
述操作中FeCl 3的萃取百分率为( )
(A) % (B) % (C) % (D) %
13 用纸层析上行法分离物质A 与B 时,已知两组分的比移值R f (A) = ,R f (B) = 。
欲使分离后A
与B 的斑点中心距离为2.0 cm ,那么层析滤纸条的长度(cm)至少为( )
(A) 6 (B) 8 (C) (D) 25
14 完成一项酸碱滴定问题的合理步骤是( )
① 根据指示剂变色范围部分与滴定突跃范围重叠的原则选择指示剂;
② 写出反应方程式,确定化学计量比和滴定终点的产物;
③ 根据浓度等具体条件估算滴定终点产物的pH 值和滴定突跃范围;
④ 估算终点误差以检验滴定方法是否合理。
(A) ②①③④ (A) ②③①④ (C) ①②③④ (D) ③①②④
15 做空白试验可以在一定程度上消除( )
(A) 试剂中的杂质和实验用水对测定结果的影响
(B) 玻璃仪器容积不准确所引起的偏差
(C) 操作不稳定所引起的偏差
(D) 实验方法所引入的系统误差
二、填空题(共10分)
1 根据标定与测定条件相近的原则,以二甲酚橙为指示剂,用EDTA测定废水中的Pb2+时,所用的EDTA标准溶液宜用标定(填“高纯CaCO3”或“ZnO”,1分);若将在弱酸性条件下标定的EDTA用于在强碱性条件下测定金属离子,则所得结果。
(填“不受影响”、“偏高”或“偏低”,2分)
2 酸碱、络合或氧化还原三种滴定分析中,滴定突跃的大小受被测物浓度影响最小的
是。
(1分)
3 用分光光度法测定合金钢试样中的微量铜,为使Cu2+与Fe3+分离,可以用过量NaF掩蔽Fe3+
后,在弱酸性条件下经强型离子交换柱,使Cu2+留存于流出液中加以测定。
(填“酸”或“碱”、“阴”或“阳”,2分)
4 写出(c1 mol/L NaAc + c2 mol/L NaOH)水溶液的质子条件式
(2分)写出二元弱碱Na2CO3水溶液中HCO3-的分布系数计算公式
(2分)
三、问答题(每题5分,共20分)
1 平均值的置信区间具有什么含义?如何表达?要比较两组数据的准确度和精密度分别可以进
行什么检验?说出一种可疑值取舍的方法。
2 以BaCl2为沉淀剂,用BaSO4重量法分析钢管酸洗废水中的SO42-时,如果沉淀经灼烧后发现含有少量Fe2(SO4)3,则该原因造成结果偏低还是偏高?为什么?已知Ar(Fe)=;Ar(Ba)=;Ar(S)=;Ar(O)=。
3 某样品溶液含有常量的Fe3+、Al3+、Ca2+、Mg2+离子,简述测定该混合样中各组分的方法(包、滴定剂、pH条件、指标剂和掩蔽剂等)。
4 沉淀的溶解度有哪些影响因素?为了得到便于分离的沉淀,则晶形沉淀和无定形沉淀的条件各是什么?
四、计算题(共40分)
1 称取 0 g 某纯一元弱酸HA ,溶于适量水后,稀释至 mL ,用 0 1
L mol -⋅ NaOH 溶液进行电位滴定,滴定终点时NaOH 溶液的用量为 mL , 试计算:
(1)该一元弱酸的摩尔质量;
(2)化学计量点时的pH 值。
已知:该一元弱酸的K a = ×10-5。
2 称取三聚磷酸钠(Na 5P 3O 10)样品0.3627g ,溶于水,加酸分解为PO 43-,在NH 3-NH 4Cl 缓冲溶液中,加入L 的Mg 2+溶液,形成MgNH 4PO 4沉淀,过滤、洗涤。
沉淀灼烧成Mg 2P 2O 7,称重为0.3192g ,滤液和洗涤液混合后用EDTA 滴定多余的Mg 2+,终点时,消耗EDTA(c=L)多少毫升?三聚磷酸钠的质量百分含量为多少?已知Mr(Na 5P 3O 10)=,Mr(Mg 2P 2O 7)=。
3 称取含有PbO 、PbO 2的试样1.242g ,加入浓度为L 的草酸(H 2C 2O 4)溶液,将PbO 2还原为Pb 2+,然后以氨水中和,Pb 2+以PbC 2O 4形式沉淀。
(1)过滤、洗涤,将滤液酸化后用浓度为.04000mol/L 的KMnO 4标准溶液滴定,用掉。
(2)再将滤渣PbC 2O 4沉淀溶于酸中,也用同浓度的KMnO 4标准溶液滴定,消耗。
计算原试样中PbO 和PbO 2的质量百分含量。
已知M(PbO)=223.2g/mol ,M(PbO 2)=239.2g/mol
4 已知lg K CaY =,pH = 时,lg αY(H) = ,EBT 的p K a 1 = ,p K a 2 = ,lg K Ca-EBT =。
在pH=的氨性溶液中,以铬黑T(EBT)为指示剂,用 mol/L EDTA 滴定 mol/L Ca 2+溶液,计算终点误差。
5 已知CaCO 3 的K sp = ×10-9,H 2CO 3的p K a 1 = ,p K a 2 = 。
计算CaCO 3在pH=的水中的溶解度。
