高三专题复习 晶体密度相关计算
高三化学高考备考专题复习有关晶体的各类计算

位置 的原子数 例1、铝单质为面心立方晶体,其晶胞参数a=0.405nm,列式表示铝单质的密度
g·cm-3(不径必计的算关出结系果)
②若合金的密度为d g/cm3,晶胞参数a=________nm。
*(2)分数坐标:(0,0,0)-顶点
(1/2,1/2,0)
3、边长(晶胞参数)和半径关系
空间利用率
3 Po 顶10点0%
球半径r 与晶胞边长 a 的关系:
3、边长(晶胞参数)和半径关系
(1)球数:8×1/8 + 6×1/2 = 4
1 、 晶 体 中 的 微 粒 数 、 化 学 式 其中,密度公式中共有四个未知量:密度,微粒摩尔质量,晶 胞体积,NA,知道3个可求另一个,因此可能围绕密度出现4种题型。
在面心立方基础上,再插入4个球,分别占据8个小立 方体中4个互不相邻的体心,
S a a sin 60 3 a2 2
V晶胞 3 a2 2 6 a
2
3
2a3 8 2r3
V球球)
V球 V晶胞 100% 74.05%
7、空间利用率
(4)金刚石空间利用率:球体积占晶胞体积的百分比
8 4 πr 3 8 4 πr 3
3
3 100% 34%
实例
NaCl 型
AB CsCl 型
Na+:6 Na+:6 Cl-: 6 Cl-: 6
Cs+:8 Cs+:8 Cl-: 8 Cl-: 8
Na+:4 Cl-: 4 Cs+:1 Cl-:1
KBr AgCl、 MgO、CaS、 BaSe
CsCl、CsBr、 CsI、TlCl
ZnS型
Zn2+:4 Zn2+:4 Zn2+:4 ZnS、AgI、 S2-: 4 S2-: 4 S2-:4 BeO
高考微专题复习——晶体密度计算(附参考答案)
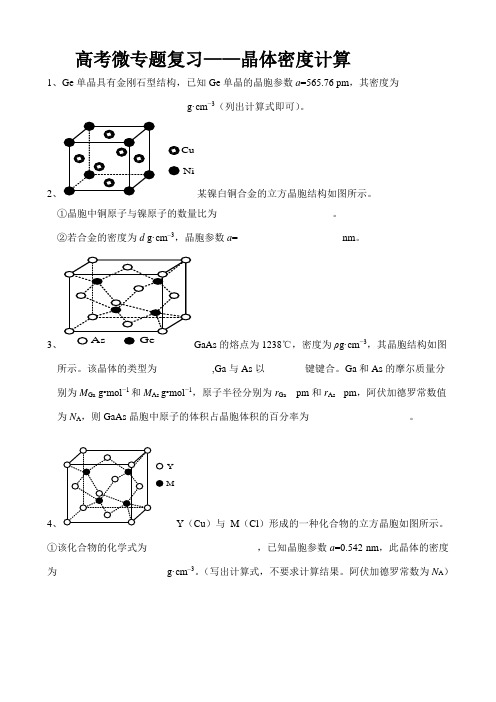
高考微专题复习——晶体密度计算1、Ge单晶具有金刚石型结构,已知Ge单晶的晶胞参数a=565.76 pm,其密度为_________________________g·cm−3(列出计算式即可)。
2、CuNi某镍白铜合金的立方晶胞结构如图所示。
①晶胞中铜原子与镍原子的数量比为_______________________。
②若合金的密度为d g·cm–3,晶胞参数a=_____________________nm。
3、GaAs的熔点为1238℃,密度为ρg·cm−3,其晶胞结构如图所示。
该晶体的类型为___________,Ga与As以________键键合。
Ga和As的摩尔质量分别为M Ga g•mol−1和M As g•mol−1,原子半径分别为r Ga pm和r As pm,阿伏加德罗常数值为N A,则GaAs晶胞中原子的体积占晶胞体积的百分率为____________________。
4、YMY(Cu)与M(Cl)形成的一种化合物的立方晶胞如图所示。
①该化合物的化学式为______________________,已知晶胞参数a=0.542 nm,此晶体的密度为______________________g·cm–3。
(写出计算式,不要求计算结果。
阿伏加德罗常数为N A)5、(O)和B(Na)能够形成化合物F,其晶胞结构如图所示,晶胞参数,a=0.566nm,F的化学式为____________;晶胞中A原子的配位数为____________;列式计算晶体F的密度(g·c m¯3)___________________________________。
6、Al单质为面心立方晶体,其晶胞参数a=0.405nm,晶胞中铝原子的配位数为_________,列式表示Al单质的密度为________________________g·cm¯3(不必计算出结果)7、金刚石晶胞含有_______个碳原子。
人教版《物质结构-晶体密度的计算》

1、顶点:1/8. 2、面:1/2
1、顶点:1/8. 2、面:1/2 3、棱: 1/4
1、顶点:1/8 2、面:1/2 3、棱: 1/4
4、体内:1
例如
ClNa+ 氯化钠晶胞 Cl- 有 81/8+61/2=4 个 Na+有 121/4+1=4 个 故氯化钠化学式为 NaCl .
7
二、专题突破-晶胞密度计算
【2016 ·全国新课标Ⅰ卷节选】
已知Ge单晶的晶胞参数a=565.76 pm,其 密度为__________g· cm-3(列出计算式即可)。
1 1 1.确定晶胞中的粒子数:N(Ge) 8 6 4 8 8 2
2.确定晶胞体积:
V (565.76pm)3 (565.76 1010 cm)3 565.763 1030 cm3
3.代入公式进行计算:
8 73 3 g / cm 6.02 10 23 565.76 3 10 30 8 73 7 3 10 g / cm 6.02 565.76 3
【2016 ·全国新课标Ⅱ卷节选】
某镍白铜合金的立方晶胞结构如图所示。 ①晶胞中铜原子与镍原子的数量比为________。 ②若合金的密度为d g· cm–3,晶胞参数a=______nm。 ① N(Cu) 6 1 3
• 晶胞密度计算公式:
8
例:已知NaCl晶胞的边长为acm ,计算NaCl晶胞的密度 2.计算晶胞体积为 V=a3cm3
Cl-
Na+ 氯化钠晶胞
435.5+423 NA a3
g/cm-3
1.确定晶胞中的粒子数 Cl- 有 81/8+61/2=4 个 Na+有 121/4+1=4 个
晶体密度的计算

1 1 1.确定晶胞中的粒子数:N(Ge) 定晶胞体积:
V (565.76pm)3 (565.76 1010 cm)3 565.763 1030 cm3
解得:
251 a 6.02 102 d
3
高考化学第35题之
晶体密度的计 算
开平市开侨中学 姜 姝
晶体密度的计算
一、计算公式:
m晶胞 V晶胞
M晶胞 NA
N1M1 N2M2 Nn Mn
N1M1 N 2 M 2 N n M n N A V晶胞
晶体密度的计算
一、计算公式:
二、计算步骤: 1.确定晶胞中的粒子数
1 4
1 2
1
晶体密度的计算
三、晶胞中粒子数的确定(均摊法):
【例题】确定下图晶胞中各原子个数
1 1 绿色: 8 6 =4 8 2 1 灰色: 12 1=4 4
晶体密度的计算
三、晶胞中粒子数的确定(均摊法):
【真题感知】【2013· 新课标全国卷Ⅰ】 单质硅存在与金刚石结构类似的晶体,其晶胞中共
3.代入公式进行计算:
NGe M Ge 8 73 3 g / cm 23 3 30 N A V晶胞 6.02 10 565.76 10
8 73 7 3 10 g / cm 6.02 565.76 3
晶体密度的计算
五、实战演练: 【2016 ·全国新课标Ⅱ卷】
N1M1 N 2 M 2 N n M n N A V晶胞
2.确定晶胞体积
3.代入公式进行计算
晶体密度的计算.

最新高考化学专题复习——晶体密度计算解析

高考微专题复习——晶体密度计算1、Ge单晶具有金刚石型结构,已知Ge单晶的晶胞参数a=565.76 pm,其密度为_________________________g·cm−3(列出计算式即可)。
2CuNi某镍白铜合金的立方晶胞结构如图所示。
①晶胞中铜原子与镍原子的数量比为_______________________。
②若合金的密度为d g·cm–3,晶胞参数a=_____________________nm。
3、GaAs的熔点为1238℃,密度为ρg·cm−3,其晶胞结构如图所示。
该晶体的类型为___________,Ga与As以________键键合。
Ga 和As的摩尔质量分别为M Ga g•mol−1和M As g•mol−1,原子半径分别为r Ga pm和r As pm,阿伏加德罗常数值为N A,则GaAs晶胞中原子的体积占晶胞体积的百分率为____________________。
4YMY(Cu)与M(Cl)形成的一种化合物的立方晶胞如图所示。
①该化合物的化学式为______________________,已知晶胞参数a=0.542 nm,此晶体的密度为______________________g·cm–3。
(写出计算式,不要求计算结果。
阿伏加德罗常数为N A)5、(O)和B(Na)能够形成化合物F,其晶胞结构如图所示,晶胞参数,a=0.566nm,F的化学式为____________;晶胞中A原子的配位数为____________;列式计算晶体F的密度(g·c m¯3)___________________________________。
6、Al单质为面心立方晶体,其晶胞参数a=0.405nm,晶胞中铝原子的配位数为_________,列式表示Al单质的密度为________________________g·cm¯3(不必计算出结果)7、金刚石晶胞含有_______个碳原子。
晶体密度的计算范文

晶体密度的计算范文晶体密度(也称为晶胞密度或晶体比重)是指晶体中其中一种元素或化合物的质量与其体积的比值,是晶体性质的一个重要参数。
晶体密度的计算可以通过实验测定或者理论计算两种方法来进行。
一、实验测定晶体密度实验测定晶体密度的方法通常有密度瓶法、比重和天平法、浸法等。
1.密度瓶法密度瓶法是一种常用的测量固体密度的方法,适用于大部分固体物质。
首先称取一定质量的晶体样品,并记录其质量(m1)。
然后将晶体样品放入一瓶中,记录瓶的质量(m2)。
然后向瓶中加满溶液,将晶体完全浸没并将装有晶体的瓶口盖严实。
再次称量瓶及溶液的总质量(m3)。
计算公式如下:晶体密度=(m1-m2)/(m3-m2)2.比重和天平法比重和天平法是一种测量固体密度的简单方法。
首先称取晶体样品的质量(m1),然后将晶体样品挂于天平的轻轻之处并记录其质量(m2)。
然后将晶体样品放入已知体积的液体中并完全浸没。
再次称量液体和晶体样品的总质量(m3)。
计算公式如下:晶体密度=(m1-m2)/(m3-m2)3.浸法浸法是一种常用的测量小颗粒物质密度的方法。
首先称取物质的质量(m1),然后浸入一定质量的溶液中并搅拌均匀。
浸入前后称取溶液的总质量(m2),计算公式如下:晶体密度=m1/(m2-m1)二、理论计算晶体密度理论计算晶体密度通常基于晶体的结构和元素组成,通过晶胞参数和晶体化学式来进行。
1.密度=(晶胞中原子总质量)/(晶胞体积)原子总质量可以通过取晶胞中所有原子的质量之和来计算。
晶胞体积可以通过晶胞参数来计算,其中包括晶胞的长度、宽度和高度。
2.密度=(晶体的摩尔质量)/(晶胞体积)晶体的摩尔质量可以通过分子式中各元素的原子质量乘以其相应的个数之和来计算。
3. 密度 = (晶体的摩尔质量) / (Avogadro常数 * 晶胞体积)Avogadro常数是一个统计常数,代表1摩尔物质中的分子或离子个数。
以上是一些晶体密度的计算方法,实验测定法适用于已经合成或存在的晶体样品,而理论计算法则适用于已知晶体结构和化学组成的情况下。
2020届高三化学二轮专题复习——晶体密度计算

高考微专题复习——晶体密度计算1、Ge单晶具有金刚石型结构,已知Ge单晶的晶胞参数a=565.76 pm,其密度为_________________________g·cm−3(列出计算式即可)。
2CuNi某镍白铜合金的立方晶胞结构如图所示。
①晶胞中铜原子与镍原子的数量比为_______________________。
②若合金的密度为d g·cm–3,晶胞参数a=_____________________nm。
3、GaAs的熔点为1238℃,密度为ρg·cm−3,其晶胞结构如图所示。
该晶体的类型为___________,Ga与As以________键键合。
Ga 和As的摩尔质量分别为M Ga g•mol−1和M As g•mol−1,原子半径分别为r Ga pm和r As pm,阿伏加德罗常数值为N A,则GaAs晶胞中原子的体积占晶胞体积的百分率为____________________。
4YMY(Cu)与M(Cl)形成的一种化合物的立方晶胞如图所示。
①该化合物的化学式为______________________,已知晶胞参数a=0.542 nm,此晶体的密度为______________________g·cm–3。
(写出计算式,不要求计算结果。
阿伏加德罗常数为N A)5、(O)和B(Na)能够形成化合物F,其晶胞结构如图所示,晶胞参数,a=0.566nm,F的化学式为____________;晶胞中A原子的配位数为____________;列式计算晶体F的密度(g·c m¯3)___________________________________。
6、Al单质为面心立方晶体,其晶胞参数a=0.405nm,晶胞中铝原子的配位数为_________,列式表示Al单质的密度为________________________g·cm¯3(不必计算出结果)7、金刚石晶胞含有_______个碳原子。
晶体密度的计算

有不同的衍射花样。
晶体结构对晶体的物理和化学性质有着重要影响,如硬度、熔
03
点、导电性等。
密度的定义与计算公式
01
密度是指物质的质量与其所占体积的比值,单位为克
/立方厘米。
02 计算公式为:密度 = (质量 / 体积) = g / cm³。
03
对于晶体,密度计算需要考虑其内部原子或分子的排
列方式以及晶胞参数。
晶体密度是评估材料性能的重要参数,如金属、陶瓷、玻璃等材料 的力学、热学、电学等性能都与晶体密度有关。
材料合成与制备
在材料合成与制备过程中,晶体密度可用于优化合成条件和制备工 艺,提高材料的纯度和结晶度。
材料检测与表征
通过测量晶体密度,可以对材料进行成分分析、结构表征和缺陷检测 等。
在化学中的应用
04 晶体密度与其他物理量的 关系
与晶体熔点、沸点的关系
总结词
晶体密度与熔点和沸点之间存在一定的 关系。
VS
详细描述
晶体密度通常随着熔点和沸点的升高而增 加。这是因为随着温度的升高,原子或分 子的振动幅度增大,导致晶格结构膨胀, 密度随之增大。因此,通过测量晶体密度 可以推测其熔点和沸点的大致范围。
研究新的计算方法,减少计算过程中 的近似处理,提高计算精度。
未来研究的方向与展望
• 考虑温度和压力的影响:研究温 度和压力对晶体密度的影响,发 展适用于不同温度和压力下的计 算方法。
未来研究的方向与展望
拓展应用领域
将晶体密度计算方法应用于更多领域,如材料科学、化学、生物 学等。
促进学科交叉
加强物理学、化学、材料科学等学科的交叉融合,推动晶体密度 计算方法的创新发展。
计算中的误差来源与控制方法
体心立方晶格致密度

体心立方晶格致密度
体心立方晶格是一种晶体结构,其中每个原子都位于一个正八面体的顶点上,并且一个额外的原子位于正中央。
这种结构在三个方向上都有相等的原子密排列,因此具有一定的密度。
要计算体心立方晶格的密度,我们首先需要知道晶体的化学成分和晶体常数。
晶体常数是指晶体中最小重复单元的尺寸,通常用a表示。
对于体心立方晶格,晶胞中的原子占据了体心位置,因此晶胞中有两个原子。
假设每个原子的原子量为M,那么晶体的摩尔质量就是2M。
晶体的密度可以通过以下公式计算:
密度 = (晶体的摩尔质量) / (晶胞的体积)。
对于体心立方晶格,晶胞的体积可以通过以下公式计算:
体积 = a³。
将晶体的摩尔质量和晶胞的体积代入上面的公式,就可以计算
出体心立方晶格的密度。
需要注意的是,这只是一个理论上的计算方法。
在实际应用中,晶体的密度可能会受到其他因素的影响,比如晶体的缺陷或者杂质等。
因此,在实际应用中,可能需要进行更复杂的实验来确定晶体
的密度。
计算晶胞密度的公式

计算晶胞密度的公式晶胞密度是晶体中的晶元的数量的度量,它可以用来衡量晶体的尺寸大小。
晶体结构中的晶元尺寸有时会变化,但是晶元密度通常是一个常量,可以用于估算晶体容积。
晶元密度也可以作为材料性质的指示,用于研究超导、磁性和光学性质。
计算晶胞密度的公式计算晶体中的晶元密度有几种方法,最常用的是Bohr公式:晶胞密度 = N/V其中,N为晶体中的晶元数量,V为晶体的体积。
实验方法对于计算晶胞密度,首先需要测量晶体的大小,以确定晶体的体积。
针对有规律的晶体,可以使用定向投射(XRD)来测量晶体的大小,而且平行定向投射(PDI)可以测得晶元的尺寸。
接下来,必须统计晶体中的晶元数量,这样才能用Bohr公式计算出晶胞密度。
此时,必须对晶体进行X射线衍射,以获取晶元结构的详细资料。
最后,可以计算出晶元密度,这样就可以测定晶体的性质。
晶胞密度的应用晶胞密度与晶体的性质有着密切的关系,已经应用于能源材料,光学材料和电子材料等方面。
燃料电池材料。
晶胞密度可以用来测定燃料电池材料的porosity,以估算燃料电池的热性能和性能。
电子材料。
晶胞密度可以用来测定半导体材料的尺寸大小,以确定其电子性质。
光学材料。
通过晶胞密度,可以得知晶体的衍射和折射性质,以此作为纤维光学材料的表征指标。
总结晶胞密度是晶体结构中晶元的数量的度量,也是材料的一种度量。
Bohr公式可以用来测定晶胞密度,实验方法是先测量晶体尺寸,再使用X射线衍射统计晶体中晶元数量,最后计算晶胞密度。
晶胞密度可以用于研究能源、电子、光学材料的性质。
2021年高考化学复习《晶胞的有关计算》

2 2
,设晶胞
棱长为 a pm,则该晶胞的质量为65×4N+A32×4 g=ρ g·cm-3×(a×10-10 cm)3,解
3 得 a=
4×97 ρNA
×1010,故两个 S 原子之间的距离为
2 2
3 ×
4×97 ρNA
×1010 pm。
答案:(1)4
(2)(1,21 ,12 )
(3)
2 2
3 ×
4×97 ρNA
命题角度 3:微粒间距的相关计算
【典例 3】(2019·全国卷Ⅰ节选)图(a)是 MgCu2 的拉维斯结构,Mg 以金刚石
方式堆积,八面体空隙和半数的四面体空隙中,填入以四面体方式排列的 Cu。图
(b)是沿立方格子对角面取得的截图。可见,Cu 原子之间最短距离
x=
pm,Mg 原子之间最短距离 y=
答案:
2 4
a
3 8×24+16×64 4 a NAa3×10-30
【归纳总结】微粒间距的计算方法
命题角度 4:晶体中空间利用率的计算
【典例 4】(2016·全国卷Ⅲ)GaAs 的熔点为 1 238 ℃,密度为 ρ g·cm-3,其晶胞
结构如图所示。该晶体的类型为
,Ga 与 As 以
键键合。
Ga 和 As 的摩尔质量分别为 MGa g·mol-1 和 MAs g·mol-1,原子半径分别为 rGa pm
nm , 晶 体 的 密 度
m ρ=V
=
4×62 g·mol-1
6.02×1023 mol-1 (0.566×10-7cm)3
≈2.27
g·cm-3。
答案:Na2O 8 4×62 g·mol-1
(0.566×10-7cm)3×6.02×1023 mol-1 ≈2.27
相求晶体密度例题

相求晶体密度例题
摘要:
1.晶体密度计算的基本步骤
2.晶体密度计算的公式
3.具体实例:NaCl晶体密度计算
正文:
一、晶体密度计算的基本步骤
1.首先找出晶胞,因为晶胞是晶体的基本单位。
2.确定晶胞内所有的原子或离子的种类和位置。
3.搞清每个原子或离子是完全在晶胞内部(不被不同晶胞共用)还是被不同晶胞共用。
4.按第三步,把一晶胞所有的原子或离子在考虑共用后加起来。
二、晶体密度计算的公式
晶体密度(ρ)= 晶体质量(m)/ 晶体体积(V)
其中,晶体质量是指单位晶胞内的原子或离子的质量之和,晶体体积是指晶胞的体积。
三、具体实例:NaCl晶体密度计算
1.首先,确定NaCl晶体的晶胞结构。
NaCl是面心立方晶系,每个晶胞中含有4个Na+离子和4个Cl-离子。
2.计算单位晶胞的质量:Na+离子的摩尔质量为23g/mol,Cl-离子的摩尔质量为35.5g/mol。
所以,单位晶胞的质量为(23g/mol + 35.5g/mol)*
4 = 170g。
3.计算晶体密度:已知NaCl晶体的晶胞边长a=3.869 nm,将其转换为厘米(1 nm = 10^-7 cm)。
然后,计算晶胞体积V=a= (3.869 nm) =
4.276 x 10^-22 cm。
晶体密度ρ = 晶体质量/晶体体积= 170g / 4.276 x 10^-22 cm ≈ 4.02 g/cm。
所以,NaCl晶体的密度约为4.02 g/cm。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
8
2
2.确定晶胞体积: 4b 3a a 4b pm 3
3.代入公式计算:
N(R) 4
V ( 4b pm)3 ( 4b 10 10 cm)3
3
3
N (O) M (O) N (R) M (R) N A V (晶胞)
4 16 NA (
4 M (R) 4b 1010 )3
3
g/cm3
dg/cm3
人教版高三专题复习课系列
晶体密度相关计算
学校:XXXXXXXXXX 授课:X X X
教学 内容
1 直接计算密度 2 通过密度求参数a 3 通过密度求相对原子质量 4 通过密度求原子半径
01
直接计算密度
实战 2016全国 (节选) Ge(锗)的单质的晶胞参数a=565.76pm,其密
演练 新课标Ⅰ卷 度为
g/cm3 (列出计算式即可)
1.确定晶胞中的粒子数目:
N (Ge) 8 1 6 1 4 8 82
2.确定晶胞体积:
V (565.76pm) 3 (565.76 1010cm)3 565.763 1030cm3
3.代入公式计算:
N (Ge) M (Ge) N A V (晶胞)
6.02 1023
。 nm。
1.确定晶胞中的粒子数目:
N (Cu) 6 1 3
2
2.确定晶胞体积:
N (Ni) 8 1 1
8
V (anm)3 (a 10 7 cm)3 a3 10 21cm3
3.代入公式计算:
N (Cu) M (Cu) N (Ni) M (Ni) N A V (晶胞)
364 159 6.021023 a3 1021
8 73 565.763
10 30
g/cm3
8 73 6.02 565.763
107 g/cm3
1 确定晶胞中的粒子数目(均摊法)
2 确定晶胞体积
3 代入公式计算
m NM
V NA V (晶胞)
02
通过密度求参数a
镍白铜合金的立方晶胞结构如图所示。
实战 演练
通过密度 求参数a
(1)晶胞中的铜原子与镍原子的数量比为 (2)若合金的密度为d g/cm3 ,晶胞参数a=
6.021023mol 13.08108cm3 4108cm3 2
1308pm
=3.4g/cm3
400pm
400pm
m
NM
1
V N A V (晶胞)
课堂 小结
2 直接计算密度
3 通过密度求参数a
4 通过密度求相对原子质量
5 通过密度求原子半径
3.代入公式计算:
N (Fe) M (Fe) N A V (晶胞)
2 56 g / cm3 dg / cm3
N
A
(
4r 3
)3
r
3 3
256 cm
4 d NA
头脑 风暴
(2013全国卷II) F、K和Ni三种元素组成的一种化合物的晶胞如
下图。列式计算该晶体的密度
g/cm3 。
259 239 419g / mol
g/cm3
dg/cm3
a3
251 6.02 102 d
03
通过密度求相对原子质量
实战 通过密度求 R的氧化物晶胞结构如下图。该晶体密度为d g/cm3 , 演练 相对原子质量 距离最近的两个原子的距离为b pm ,则R的相对原子质量为 。
1.确定晶胞中的粒子数目:
N (O) 8 1 6 1 4
M
(R)
1 4
d
N
A
(
4b 3
10 10 )3
16
04
通过密度求原子半径
实战 通过密度 铁单质的晶胞如下图所示,为
cm。(列出计算式即可)
1.确定晶胞中的粒子数目:
N
(Fe)
8
1 8
1
2
2.确定晶胞体积:
4r
3a
V
(acm)3 ( 4r )3 cm3 3
