胺与酰胺
第八章 胺和酰胺

宁德职业技术学院
宁德职业技术学院
(3) 叔胺 脂肪族叔胺由于氮原子上没有氢原子, 只能与亚硝酸 作用, 生成不稳定的水溶性亚硝酸盐(无名显现象). 此盐 用碱处理后, 又重新得到游离的脂肪族叔胺.
芳香族叔胺与亚硝酸作用, 不生成盐, 而是在芳环上引 入亚硝基, 生成有色的对亚硝基芳叔胺. 如对位被其它基团 占据,则亚硝基在邻位上取代.
宁德职业技术学院
“摇头丸”是冰毒的衍生物,名为3,4-亚甲二氧基甲基 苯丙胺英文缩写为 MDMA ,属中枢神经兴奋剂. 我国从 1990 年起, 摇头丸开始在舞厅流行 , 通常以 60~120 毫克的药丸或 胶囊形式服用. 服用后会使人有快乐的感觉,出现幻觉,进而 使人多话而不知停止, 头颈左右摇摆不止等中枢神经系统高度 兴奋的症状. “摇头丸” 对健康的损害是相当严重而且无法预 期的,服用摇头丸会诱发突发性的恶性高血压、自发性脑出血 或脑血管阻塞、胸痛、肝炎及肝衰竭等疾病的发生,导致严重 的后果,并可能诱发潜在的精神疾病.
宁德职业技术学院
苯胺能与稀盐酸、硫酸等成盐, 但不能和乙酸成 盐,二苯胺只能与浓的盐酸、硫酸成盐,但形成的盐遇 水立即水解,三苯胺则接近中性,不能和浓盐酸等成盐. 芳脂胺的碱性,由于氨基氮原子上孤对电子对不 能和苯环发生P-π共轭, 所以碱性一般比苯胺强些. 如 苄胺的碱性强于苯胺.
宁德职业技术学院
第八章 胺和酰胺
第一节 胺
宁德职业技术学院
NH3(氨)分子中的氢原子被R-或Ar-取代后的衍生 物叫做胺. 胺类广泛存在于生物界, 许多生物碱具有生理 或药理作用.
宁德职业技术学院
一.胺的分类和命名 1.胺的分类 (1) 根据分子中与氮原子连接的烃基数来分
胺与醇的分级依据不同. 胺的分级着眼于氮原子上烃 基的数目;醇的分级立足于 羟基所连的碳原子的级别 .
有机化学中的胺和酰胺的反应

有机化学中的胺和酰胺的反应胺和酰胺是有机化学中常见的两类化合物,在许多化学反应中发挥着重要作用。
本文将探讨胺和酰胺的反应机理和一些重要的反应类型。
一、胺的反应1. 亲电取代反应胺可以作为亲电试剂参与取代反应。
在这类反应中,氨基(NH2)基团可以与带有亲电中心的化合物发生取代反应。
例如,胺可以与卤代烃反应,形成相应的胺类化合物。
这类反应可以通过氨基团中的孤对电子攻击带有亲电性的碳原子实现。
2. 缩合反应胺还可以参与缩合反应,形成脲、胸腺嘧啶等化合物。
在这类反应中,胺的氨基团与酮或醛的羰基进行缩合,形成C-N键。
缩合反应通常需要使用酸催化剂或碱催化剂来促进反应的进行。
3. 氧化反应胺是一种容易氧化的化合物,可以参与氧化反应。
在这类反应中,胺的氨基团会被氧化剂(如过氧化氢或过氧化苯甲酰)氧化为亚胺、亚胺氧化物等。
氧化反应通常需要在酸性或碱性条件下进行。
二、酰胺的反应1. 羟胺化反应酰胺可以与羟胺反应,形成羟基酰胺。
在这类反应中,酰胺的羰基与羟胺发生加成反应,形成新的羟基和酰胺的酰胺化合物。
这类反应在生物体内广泛存在,参与许多重要生物分子的合成过程。
2. 加氢反应酰胺可以参与加氢反应,将羰基还原为羟基。
这类反应通常需要使用氢化试剂(如氢气和催化剂)催化。
加氢反应对于合成醇和醛的羰基还原具有重要意义。
3. 脱酰反应酰胺可以发生脱酰反应,生成相应的胺和酰基化合物。
在这类反应中,酰胺的酰基与碱性条件下断裂,形成胺和酰基化合物。
这类反应在有机合成中常被用于制备新的胺类化合物。
总结起来,胺和酰胺在有机化学中具有广泛的应用。
胺可以参与亲电取代、缩合和氧化等反应,而酰胺主要参与羟胺化、加氢和脱酰等反应。
对这些反应的深入研究可以为新的有机合成方法的开发和有机化学的进一步应用提供重要的基础。
胺和酰胺的知识点总结

胺和酰胺的知识点总结一、胺。
1. 定义与结构。
- 胺可以看作是氨(NH_3)分子中的氢原子被烃基取代后的产物。
- 根据胺分子中氮原子上所连接的烃基数目不同,可分为伯胺(R - NH_2,氮原子上连接1个烃基)、仲胺(R_2NH,氮原子上连接2个烃基)和叔胺(R_3N,氮原子上连接3个烃基)。
当氮原子上连接4个烃基时形成季铵盐(R_4N^+X^-)或季铵碱(R_4N^+OH^-)。
2. 命名。
- 简单胺的命名:以胺为母体,在烃基名称后面加上“胺”字。
例如,CH_3NH_2称为甲胺;(CH_3)_2NH称为二甲胺;(CH_3)_3N称为三甲胺。
- 当烃基相同时,用二、三表示烃基的数目;当烃基不同时,将简单的烃基写在前面,复杂的烃基写在后面。
例如,CH_3CH_2NHCH_3称为甲乙胺。
- 对于芳香胺,若- NH_2直接连在苯环上,命名时在“胺”字前面加上芳基的名称。
例如,C_6H_5NH_2称为苯胺。
3. 物理性质。
- 低级胺(如甲胺、二甲胺、三甲胺等)为气体,丙胺以上为液体,高级胺为固体。
- 胺具有特殊的气味,低级胺有类似于氨的气味,有的还有鱼腥味。
- 胺分子间能形成氢键,但由于氮的电负性比氧小,所以胺形成的氢键比醇弱,其沸点比相对分子质量相近的醇低,但比相对分子质量相近的烃高。
4. 化学性质。
- 碱性。
- 胺分子中氮原子上有孤对电子,能接受质子,所以胺具有碱性。
- 胺的碱性强弱顺序为:脂肪族仲胺>脂肪族伯胺>脂肪族叔胺>氨>芳香胺。
脂肪族胺的碱性比氨强,是因为脂肪烃基为推电子基,使氮原子上的电子云密度增大,更容易接受质子;而芳香胺的碱性比氨弱,是因为苯环的吸电子作用,使氮原子上的电子云密度降低。
- 与酸反应。
- 胺能与酸反应生成盐。
例如,甲胺与盐酸反应生成甲胺盐酸盐:CH_3NH_2+HCl→CH_3NH_3^+Cl^-。
胺盐为离子化合物,一般为白色固体,易溶于水而不溶于有机溶剂。
有机化学11胺与酰胺

RNH2 R’X RNHR’ R’X RR’2N R’X RR’3N+X-
伯胺
仲胺
叔胺
季铵盐
胺作为亲核试剂与卤代烃发生取代反应,生 成仲胺、叔胺和季铵盐。此反应可用于工业上 生产胺类。但往往得到的是混合物。
烷基化后,碱性增强,再次烷基化容易。
3、酰化、Hinsberg反应
伯胺、仲胺易与酰氯或酸酐等酰基化剂作用生
3、酰胺的化学性质
1)酰胺的酸碱性; 2)与亚硝酸反应; 3)还原反应; 4)霍夫曼降级反应。
本章思考题和作业
一、习题:10.1,10.4; 二、习题:10.3; 作业:习题: 10.2,10.5,10.6,10.7。
季铵碱为强碱,其碱性与氢氧化钠或 氢氧化钾相当。卤化季铵盐的水溶液用氧 化银处理时则生成季铵碱。
R 4 N + C l+A g 2 OH 2 OR 4 N + O H+ A g C l
比较碱性(给电子能力):
(1)芳胺 < NH3 < 脂肪胺 (2)脂肪胺:
气态:NH3<CH3NH2<(CH3)2NH<(CH3)3N 水溶液: NH3< (CH3)3N < CH3NH2
2、胺的命名
❖简单的胺:用“胺”作官能团,把它所含烃基 的名称和数目写在前面,按简单到复杂先后列出, 后面加上“胺”字。
CH3 N
CH2CH3
甲(基)乙(基)环丙胺
❖复杂的胺:作为烃类的衍生物来命名
❖季铵化合物:作为铵的衍生物来命名
氢氧化四甲铵
溴化四乙铵
§1.3 胺的物理性质
低级脂胺是气体或易挥发的液体,具有难闻的臭 味。高级胺为固体。胺的沸点比分子量相近的烃类 高,但比醇或羧酸的沸点低。叔胺氮原子上无氢原 子,分子间不能形成氢键,因此沸点比其异构体的 伯、仲胺低。伯、仲、叔胺都能与水分子形成氢键, 低级的胺易溶于水。胺的溶解度随分子量的增加而 迅速降低,从6个碳原子的胺开始就难溶于水。一 般胺能溶于醚、醇、苯等有机溶剂。
《胺和酰胺》 讲义

《胺和酰胺》讲义一、胺胺是一类含有氮原子的有机化合物,在有机化学中具有重要的地位。
胺可以看作是氨(NH₃)分子中的氢原子被烃基取代后的产物。
根据胺分子中氮原子上所连接的烃基种类和数目不同,胺可以分为以下几类:1、脂肪胺脂肪胺是指氮原子与脂肪烃基相连的胺。
例如,甲胺(CH₃NH₂)、乙胺(CH₃CH₂NH₂)等。
脂肪胺的化学性质较为活泼,能与酸发生反应生成盐。
2、芳香胺芳香胺是指氮原子与芳香烃基相连的胺。
比如苯胺(C₆H₅NH₂)。
芳香胺通常具有特殊的气味,且在化学性质上与脂肪胺有所不同。
胺的物理性质也有一定的特点。
低级脂肪胺在常温下是气体,随着碳原子数的增加,逐渐变为液体或固体。
胺的沸点比相对分子质量相近的醇低,这是因为胺分子间的氢键作用较弱。
胺的化学性质丰富多样。
胺具有碱性,这是由于氮原子上有孤对电子,可以接受质子。
其碱性强弱与氮原子上电子云密度有关。
一般来说,脂肪胺的碱性大于芳香胺。
胺还能发生酰化反应。
例如,与酰氯或酸酐反应,生成酰胺。
胺的制备方法也有多种。
氨的烷基化是一种常见的方法,即将氨与卤代烃在一定条件下反应。
此外,硝基化合物的还原也是制备胺的重要途径。
二、酰胺酰胺是羧酸中的羟基被氨基(或胺基)取代而形成的化合物。
酰胺的结构特点使得其具有独特的性质。
从物理性质来看,除了少数低级酰胺为液体外,多数酰胺为固体。
由于酰胺分子间可以形成氢键,因此其熔点和沸点通常较高。
在化学性质方面,酰胺具有水解性。
在酸或碱的催化下,酰胺可以水解为羧酸和氨(或胺)。
酰胺的制备通常通过羧酸与胺的缩合反应来实现。
在一定条件下,羧酸和胺反应脱去一分子水,生成酰胺。
酰胺在有机合成和生物化学中都具有重要的意义。
在有机合成中,酰胺是重要的中间体,可以通过进一步的反应转化为其他化合物。
在生物化学中,许多生物大分子如蛋白质,其结构中就包含酰胺键。
三、胺和酰胺的关系胺和酰胺之间存在着密切的联系。
一方面,胺可以通过与羧酸或其衍生物反应转化为酰胺。
《胺和酰胺》 讲义

《胺和酰胺》讲义一、胺胺是一类含有氮原子的有机化合物,在有机化学中具有重要的地位。
胺可以根据氮原子上所连接的烃基数目分为一级胺(伯胺)、二级胺(仲胺)和三级胺(叔胺)。
如果氮原子上连接了一个烃基,就是一级胺;连接了两个烃基,就是二级胺;连接了三个烃基,就是三级胺。
胺的命名通常采用习惯命名法和系统命名法。
习惯命名法是在烃基名称后面加上“胺”字。
比如甲胺、乙胺等。
系统命名法则是把胺看作是烃的氨基衍生物,以烃为母体,氨基作为取代基。
胺具有碱性,这是由于氮原子上的孤对电子能够接受质子。
不同的胺碱性强弱有所不同。
一般来说,脂肪胺的碱性强于芳香胺。
这是因为芳香胺中氮原子上的孤对电子与苯环存在共轭作用,使得电子云密度降低,碱性减弱。
胺在生活和工业中有着广泛的应用。
例如,甲胺是合成许多农药和药物的重要原料;乙二胺常用于制造纤维和塑料等。
胺的制备方法有多种。
比如通过卤代烃与氨的反应,可以得到不同级别的胺。
此外,腈的还原也是制备胺的常用方法。
二、酰胺酰胺是羧酸中的羟基被氨基(或胺基)取代而形成的化合物。
酰胺的结构中,氮原子与羰基通过双键相连,形成了一个比较稳定的结构。
酰胺的命名通常是根据相应的羧酸和胺来命名的。
例如,乙酰胺是由乙酸和氨反应生成的。
酰胺具有较高的熔点和沸点,这是因为酰胺分子之间可以形成氢键,增加了分子间的作用力。
酰胺在化学性质上相对较为稳定,但在一定条件下也能发生水解反应。
水解可以在酸性条件下进行,也可以在碱性条件下进行。
在酸性条件下,水解生成羧酸和铵盐;在碱性条件下,水解生成羧酸盐和氨。
酰胺在生物体内也有着重要的作用。
例如,蛋白质中的肽键就是一种酰胺键,它对于维持蛋白质的结构和功能起着关键作用。
在工业上,酰胺也是许多聚合物的重要组成部分,如尼龙等。
三、胺和酰胺的相互转化胺和酰胺之间在一定条件下可以相互转化。
例如,通过羧酸和胺的缩合反应可以生成酰胺。
而酰胺在一定条件下(如强还原剂的作用)也可以被还原为胺。
高中化学选择性必修三3-4-3胺与酰胺

B.烟酰胺在酸性条件下水解生成
和铵盐
C.烟酰胺在碱性条件下水解生成 D.烟酰胺分子中含有酰基和酰胺基
和氨气
BD
2.下列说法不正确的是( ) A.胺和酰胺都是烃的含氧衍生物 B.胺和酰胺都含有 C、N、H 元素 C.胺可以认为烃中氢原子被氨基取代产物 D.酰胺中一定含酰基
A [胺分子中不含氧原子,不是含氧衍生物,A 错误。]
高二化学组 王吉伟
2.酰胺 (1)结构 酰胺是羧酸分子中羟基被氨基所替代得到的化合物。结构一般表 示如下:
常见的酰胺有乙酰胺(
)、苯甲酰胺
(
)、N,N-二甲基甲酰胺[
]等。
(2)酰胺(
)的水解反应
酰胺在酸或碱存在并加热的条件下可以发 生水解反应。
①与盐酸:RCONH2+H2O+HCl RCOOH+NH4Cl。
酰胺(乙酰胺) 铵盐(NH4Cl) C、N、O、H N、H、Cl
结构式
水解反应:酸性
与酸反应生 化学性质
成铵盐
与酸反应生 成盐
时生成羧酸与 与碱反应生
铵盐,碱性时生 成盐和 NH3
成羧酸盐和
用途
化工原料
化工原料
NH3 化工原料和溶 剂
化工原料、化 肥
练习:1、(双选)最近几年烟酰胺火遍了全网,它 的美白功效一直以来都广受好评。烟酰胺的结构 简式如图,下列有关叙述正确的是( ) A.烟酰胺属于胺
3.(双选)下列关于胺、酰胺的性质和用途中正确的是( ) A.胺和酰胺都可以发生水解 B.胺具有碱性可以与酸反应生成盐和水 C.酰胺在碱性条件下水解可生成 NH3 D.胺和酰胺都是重要的化工原料 CD [胺不能发生水解反应,胺与酸反应没有水生成,A、B 项 不正确。]
第十七章 胺和酰胺教材
N+ ≡N Cl-
氯化重氮苯 (重氮盐)
D H2O
OH + N2
+ HCl
仲胺与亚硝酸的反应 生成黄色油状物或黄色固体N-亚硝基胺。
(CH3)2NH + HNO2 ——> (CH3)2N-NO + H2O
N-亚硝基二甲胺(90%)
CH3 N—H
NaNO2 + HCl
(2) 酰化反应和磺酰化反应 伯胺、仲胺易与酰氯、酸酐或羧酸等酰化剂作
用,氨基中的氢原子被酰基取代,生成N-取代酰 胺。叔胺N上没有氢原子,不发生酰化 。
-CH2CH2NH2 +
吡啶 -CO-Cl
-CH2CH2NHCO-
89%~98%
-CO-Cl + HN
NaOH
——>
-CO— N
酰化剂 R3N ——— O
CONH
H2C
CO
CONH
丙二酰脲存在酮式-烯醇式的互变异构现
象,其烯醇式呈酸性所以又称巴比妥酸。
O NH O NH
O
HO N
OH
N HO
R—NH—R’
R’’ R—N—R’
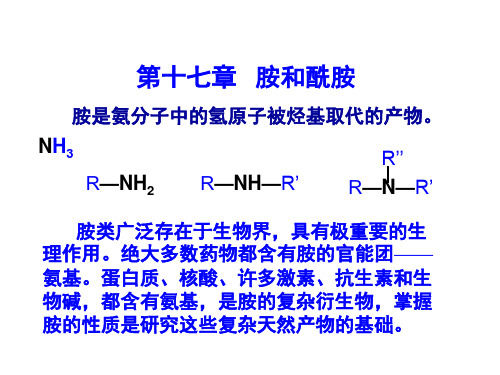
胺类广泛存在于生物界,具有极重要的生 理作用。绝大多数药物都含有胺的官能团—— 氨基。蛋白质、核酸、许多激素、抗生素和生 物碱,都含有氨基,是胺的复杂衍生物,掌握 胺的性质是研究这些复杂天然产物的基础。
一、胺的分类
(1) 根据NH3分子中H被烃基取代的数目将胺分为:
N-甲基乙酰胺
O
CH3
CH3
C
N C2H5
N-甲基-N-乙基乙酰胺
二、酰胺的物理性质
胺和酰胺——精选推荐

第十一章 胺和酰胺
第一节 胺
三、胺的性质
(二)化学性质
3.胺的化学反应
(1)胺具有碱性,能与酸反应生成盐。 (2)伯胺和仲胺能发生酰化反应。 (3)芳香胺苯环上能发生取代反应。 (4)季铵碱能与酸反应。
第十一章 胺和酰胺
第一节 胺
化学反应式
胺与氨相似,胺分子中氮原子上的未共用电子对能接受 质子,因此胺在水溶液中显弱碱性。胺能与酸反应生成盐。
胺和酰胺
胺是氨的烃基衍生物。酰胺是氨分子或胺分子中的氢 原子被酰基取代后的化合物 。
第一节 胺 第二节 酰胺
第十一章 胺和酰胺
第一节 胺
学习要求
1.理解胺的结构和分类 2.掌握胺的命名 3.了解胺的物理性质 4.掌握胺的主要化学性质
第十一章 胺和酰胺
第一节 胺
一、胺的结构和分类
(一)结构
从结构上看,胺可以看作是氨分子中一个H原子或多 个H原子被烃基取代后的化合物。
第二节 酰胺
三、尿素
(三)化学性质
1.尿素的结构特征 O
尿素分子中既有官能团羰基 C ,又有两 个官能团氨基-NH2,羰基与两个氨基相连形成尿 素。
第十一章 胺和酰胺
第二节 酰胺
三、尿素
(三)化学性质 2.尿素的化学性质特征 尿素的化学性质与酰胺相似。由于两个氨基与 羰基相连,又有类似于氨或胺的性质 。
第十一章 胺和酰胺
第一节 胺
二、胺的命名
1.简单伯胺的命名
结构简单的伯胺可以根据烃基的名称命名,即在 烃基的名称后加上“胺”字,省略 “基”字。 【例如】
CH3 CH2 NH2
NH2
NH2
乙胺
环已胺
苯胺
第十一章 胺和酰胺
有机化学胺类和酰胺的性质和反应

有机化学胺类和酰胺的性质和反应有机化学中,氨基基团(-NH2)是常见的官能团之一。
氨基基团可以连接到碳骨架上的不同位置,形成胺类和酰胺。
本文将详细描述胺类和酰胺的性质和反应。
一、胺类的性质和反应1. 胺类的命名与分类胺类按照氨基基团的数量和位置可以分为一级胺、二级胺和三级胺。
一级胺指的是一个碳原子与一个氢原子通过一个键连接,二级胺指的是一个碳原子与两个氢原子通过一个或两个键连接,三级胺指的是一个碳原子与三个氢原子通过一个或两个键连接。
胺类的命名通常使用它们在有机分子中的名称,例如甲胺、乙胺等。
如果一个有机分子中含有多个氨基基团,将其位置和数量用前缀表示,如乙二胺表示乙醇胺。
2. 胺类的物理性质由于氨基基团的电子给予性质,胺类通常呈碱性。
一级胺和二级胺可形成氢键,使它们的沸点和溶解度较高。
与醇类相比,胺类的沸点和溶解度较低,主要是由于胺分子之间较弱的分子间作用力。
3. 胺类的化学性质和反应(1)胺的碱性反应由于氨基基团的弱碱性,胺类可以与酸反应,形成盐。
例如,乙胺与盐酸反应生成乙胺盐酸盐(C2H5NH3Cl)。
(2)胺的氧化反应一级胺在氧化剂的存在下可被氧化为亚硝胺。
例如,乙胺与亚硝酸反应生成亚硝基乙胺(C2H5NHOH)。
(3)胺的磷酸化反应胺类可与磷酰氯反应生成相应的磷酰胺。
例如,乙胺与磷酰氯反应生成乙基磷酰胺(C2H5NHP=OCl)。
(4)胺的取代反应胺类可发生取代反应,取代活泼氢原子的官能团可进一步反应。
例如,氯化乙酰与胺反应生成N-乙酰基乙胺(C2H5NHCOCH3)。
二、酰胺的性质和反应1. 酰胺的命名与分类酰胺是由酰基与胺基形成的化合物,通常按照胺基的数量和位置进行分类。
一级酰胺指的是一个碳原子与一个氨基基团通过一个键连接,二级酰胺指的是一个碳原子与两个氨基基团通过一个或两个键连接,三级酰胺指的是一个碳原子与三个氨基基团通过一个或两个键连接。
2. 酰胺的物理性质酰胺通常具有较高的沸点和溶解度,与醇类和胺类相比,酰胺分子之间的分子间作用力更强。
《胺和酰胺》 知识清单

《胺和酰胺》知识清单一、胺胺是一类重要的有机化合物,在化学和生物领域都有着广泛的应用。
(一)胺的定义与分类胺可以看作是氨(NH₃)分子中的氢原子被烃基取代而形成的化合物。
根据取代氢原子的烃基数量不同,胺可以分为一级胺(伯胺)、二级胺(仲胺)和三级胺(叔胺)。
如果胺分子中含有一个烃基取代基,就是一级胺,例如甲胺(CH₃NH₂);含有两个烃基取代基的是二级胺,像二甲胺((CH₃)₂NH);含有三个烃基取代基的则为三级胺,比如三甲胺((CH₃)₃N)。
此外,按照胺分子中氮原子所连接的烃基种类,胺还可以分为脂肪胺和芳香胺。
脂肪胺中的氮原子连接的是脂肪烃基,比如乙胺;芳香胺中的氮原子连接的是芳香烃基,例如苯胺。
(二)胺的物理性质胺在常温下的状态与分子中所含烃基的结构和碳原子数有关。
低级脂肪胺,如甲胺、二甲胺和三甲胺等,通常为气体;中级脂肪胺,如乙胺和丙胺等,一般是液体;而高级脂肪胺和芳香胺多为固体。
胺的沸点比相对分子质量相近的非极性化合物要高,这是因为胺分子之间可以形成氢键。
但氮原子上所连接的烃基越多,形成氢键的能力就越弱,沸点也就越低。
胺在水中的溶解度与它们和水形成氢键的能力有关。
低级胺可溶于水,随着烃基的增大,其在水中的溶解度逐渐降低。
(三)胺的化学性质1、碱性胺具有碱性,这是因为氮原子上有孤对电子,可以接受质子。
脂肪胺的碱性比氨强,芳香胺的碱性则比氨弱。
在水溶液中,胺的碱性强弱顺序一般为:一级胺<二级胺<三级胺。
2、酰化反应胺可以与酰卤、酸酐等发生酰化反应,生成酰胺。
酰化反应可以用于保护氨基,也可以用于鉴别和分离胺。
3、磺酰化反应胺与苯磺酰氯反应生成相应的磺酰胺。
通过观察反应产物是否溶解于碱,可以鉴别一级胺、二级胺和三级胺。
4、与亚硝酸反应不同级别的胺与亚硝酸反应会生成不同的产物,这个反应可以用于鉴别胺的级别。
(四)胺的制备方法1、氨或胺的烃基化通过氨或胺与卤代烃在一定条件下反应,可以制备一级胺、二级胺和三级胺。
《胺和酰胺》 讲义

《胺和酰胺》讲义一、胺胺是一类含有氮原子的有机化合物,在有机化学中具有重要地位。
胺可以看作是氨(NH₃)分子中的氢原子被烃基取代后的产物。
根据氮原子上所连接的烃基种类和数目不同,胺可以分为以下几类:1、伯胺(一级胺)氮原子上连接一个烃基的胺称为伯胺。
例如,甲胺(CH₃NH₂)就是一种简单的伯胺。
2、仲胺(二级胺)氮原子上连接两个烃基的胺叫做仲胺。
像二甲胺((CH₃)₂NH)就属于仲胺。
3、叔胺(三级胺)氮原子上连接三个烃基的胺则为叔胺。
三甲胺((CH₃)₃N)就是常见的叔胺。
胺具有碱性,这是由于氮原子上的孤对电子能够接受质子。
胺的碱性强弱与氮原子上所连接的烃基结构有关。
一般来说,烃基给电子能力越强,胺的碱性就越强。
例如,脂肪胺的碱性通常比芳香胺强,因为脂肪烃基的给电子能力大于芳香烃基。
胺在有机合成中是非常重要的中间体。
例如,通过胺的酰化反应可以制备酰胺;胺还可以与卤代烃发生亲核取代反应,用于增长碳链。
胺在生物体内也发挥着重要作用。
许多生物活性分子,如氨基酸、生物碱等都含有胺的结构。
二、酰胺酰胺是羧酸中的羟基被氨基或胺基取代后形成的化合物。
它可以看作是羧酸和胺反应的产物。
酰胺具有以下一些重要的性质:1、物理性质酰胺分子间可以通过氢键形成较强的相互作用,因此其沸点通常比相应的羧酸和胺都要高。
大多数酰胺是固体,具有较高的熔点。
2、化学性质酰胺的化学性质相对稳定,在一般条件下不易发生水解反应。
但在强酸或强碱以及长时间加热的条件下,酰胺可以水解为羧酸和胺。
酰胺在有机合成中也有广泛的应用。
例如,通过酰胺的霍夫曼降解反应可以制备少一个碳原子的胺。
在生物体内,蛋白质就是由氨基酸通过酰胺键(肽键)连接而成的大分子。
三、胺和酰胺的相互转化胺和酰胺之间可以通过一系列反应相互转化。
1、胺制备酰胺胺与羧酸或其衍生物(如酰氯、酸酐)在一定条件下反应,可以生成酰胺。
例如,乙胺(CH₃CH₂NH₂)与乙酸酐反应,生成乙酰胺(CH₃CONHCH₂CH₃)。
化学教学:胺类与醯胺类

本章摘要
7-6 醇类、醚类与酚类 11. 将水分子的两个氢原子以烃基取代则可得醚,醇
与醚可为结构异构物。 12. 羟基直接连结于苯环上的化合物称为酚,
呈弱酸性。 13. 具酚结构的化合物与铁离子结合,产生紫色的错
离子,常用于酚的检验。
7-7 醛类与酮类
14. 醛与酮皆为含羰基的有机化合物,羰基的碳以 sp2 混成轨域参与键结。
7-9.1 胺类与酰胺类的结构及命名
二.酰胺类
羧酸分子中的羟基被胺基取代的有机化合物称 为酰胺, 例如: 甲酰胺 (HCONH2): 乙酰胺 (CH3CONH2): 苯甲酰胺 (C6H5CONH2):
7-9.1 胺类与酰胺类的结构及命名
羧酸的羟基被氯基取代则为酰氯, 例如: 甲酰氯 (HCOCl): 乙酰氯 (CH3COCl):
苯胺 (C6H5NH2):
7-9.1 胺类与酰胺类的结构及命名
两个氢原子被取代的胺类称为 二级胺 。 二甲胺 ((CH3)2NH): 甲乙胺 ((CH3)(C2H5)NH):
三个氢原子全部被取代的胺类称为 三级胺 。 例如:三甲胺 ((CH3)3N)
胺类均为极性物质,且一级胺及二级胺均具有 分子间氢键。
7-9
胺类与酰胺类
7-9.1 胺类与酰胺类的结构及命名 7-9.2 胺类与酰胺类的制备
7-9
胺类与酰胺类
学习目标:
了解胺类与酰胺类的结构、性质及常见 的化学反应
7-9.1 胺类与酰胺类的结构及命名
一.胺类
氨分子中,氢原子被烃基取代所得的有机化合物 称为胺类。
只有一个氢原子被取代的胺类称为 一级胺。 甲胺 (CH3NH2): 乙胺 (C2H5NH2):
7-2 烷类与环烷 2. 烷类 CnH2n+2 与环烷 CnH2n 为饱和烃,其碳原子均 以 sp3 混成轨域参与键结。 3. 烷类与环烷的典型反应为取代反应。
七章节胺和酰胺

命名
1.氮原子上连着两个或三个相同烃基时, 需表明烃基的数目;
2.所连烃基不同时,则将简单的放在前面; 3.芳香仲胺和芳香叔胺命名时,一般以芳
香胺为母体,脂肪烃为取代基,并在脂 肪基名称前以字母“N”,表示该脂肪烃 基是直接连在氮原子上。
CH3 NH2
NH2 CH2 CH2 NH2
CH2NH2
甲胺
1.名词解释:缩二脲反应 2.掌握胺、酰胺的系统命名(书中例题及课后复习思 考题第1题)。 3.掌握重要的胺(腐胺、苯胺、胆碱)、酰胺(尿素、 胍、磺胺)的结构。 4.掌握胺(碱性)、酰胺(水解及尿素生成缩二脲) 的重要化学性质(课后复习思考题第3、4题)。
CH2
CH3
N
C12H25
CH3
+
Br
第二节 酰胺
一、酰胺的结构和命名
酰胺(amide)在结构上可看作是羧酸分 子中的 羟基被氨基(-NH2)或羟氨基(-NHR、 ห้องสมุดไป่ตู้NRR’)取代后的产物;也可看作是氨或胺分 子中的氢原子被酰基取代后的产物。
通式是:
O
O
O
R'
R
C
NH2 R
C
NH R' R
C
N
R''
三、重要的酰胺及其衍生物
1.尿素:简称脲。
O H2N - C - NH2
• 尿素 的化学性质:
(1)弱碱性:
O H2N - C - NH2
HNO3 COOH COOH
O
[H2N - C - NH3]+ NO3O
(硝酸尿素)
[(H2N - C - NH3)2]2+ (C2O4)2 - (草酸尿素)
胺和酰胺

R ' RN H 2 RN HR ' RNR ''
官 能
氨基
团
亚氨基
次氨基
(二)胺的分类
(1) 根据分子中与氮原子连接的烃基数来分
R ' RN H 2 RN HR ' RNR ''
伯胺(1°胺) 仲胺(2°胺) 叔胺(3°胺) 胺与醇的分级依据不同. 胺的分级着眼于氮
原子上烃基的数目;醇的分级立足于羟基所连的 碳原子的级别 .
② CH3—C—ONH—CH2CH3 N-乙基乙酰胺
==
③
C—NHCH3
N-甲基苯甲酰胺
O
④
C—N
CH2CH3 CH2CH3 N,N-二乙基苯甲酰胺
二.酰胺的性质
(一)酸碱性
酰胺分子中,虽然有氮原子,由于酰基的影响致使 其碱性减弱,酰胺一般为中性化合物。
(二)水解反应
酰胺在酸、碱或酶的作用下可以发生水解反应,得
OH CH CH CH3
NH CH3
麻 黄碱
N CH3
CH2 CH CH3 NH CH3
甲基 苯 丙胺 (去 氧 麻黄 碱即 冰 毒)
阿托 品
H O
O C CH
HO CH2
一、胺的结构和分类
(一)胺的结构
胺可以看作是氨(NH3)分子中的氢原子被烃基 取代的产物。根据取代烃基数目不同,胺有三种结 构通式:
NH2
NH2
练习 根据结构写命名或者是根据名称写结构
① H2C-CH2-CH2-CH2-CH2-CH2
NH2
NH2
1,6-己二胺
② 邻苯二胺
NH2
NH2
三、胺的性质
胺和酰胺

(6)铵盐或氢氧化铵分子中四个氢原子被烃基取代后的化合物称为季 铵盐和季铵碱。
季铵盐和季铵碱的命名:与无机铵类化合物的命名相同。
NH4OH 氢氧化铵
R4N+OH-
NH4Cl 氯化铵
R4N+X-
季铵碱 [ (CH3) 3 N+CH2 CH 3 ]OH-
氢氧化三甲基乙基铵
季铵盐 (CH3)4 N+Cl-
R' R N R'' 叔胺(3° 胺)
(3)根据分子中氨基的数目,可把胺分为一元 胺和多元胺。
CH3CH2NH2
NH2CH2CH2NH2
乙胺(一元胺) 乙二胺(二元胺)
(二) 胺的命名
(1)简单伯胺的命名:结构简单的伯胺可以根 据烃基的名称命名,即在烃基的名称后加上 “胺”字,“基”字省略。
CH3 CH2NH2
NH2
乙胺
苯胺CH2CH2NH2 NhomakorabeaNH2 CH3
苯乙胺
邻甲基苯胺
(2)脂肪族仲胺和叔胺的命名:若氮原子上所 连脂肪烃基相同,用二或三表明烃基的数目; 若氮原子上所连脂肪烃基不同,则按基团的次 序规则由小到大写出其名称,“基”字一般可 省略。
CH3NH2 甲胺
(CH3)2 NCH2 CH3 二甲乙胺
CH3 CH2 CH CH3 NH2
CH3 CH CH2 CH CH3
CH3
NH2
2-氨基丁烷
2-甲基-4-氨基戊烷
(5)多元胺的命名:与多元醇的命名相仿。 H2NCH2CH2NH2 1,2-乙二胺
H2NCH2CH2CH2CH2CH2CH2NH2 1,6-已二胺
H2NCH2CH2 CH2 CH2 NH2 1,4-丁二胺
胺和酰胺(教案)高二化学(苏教版2019选择性必修第三册)

5.2胺和酰胺一、教学目标1.通过与氨的类比认识胺的结构和性质。
2.能对胺类化合物进行命名。
3.能运用胺的性质解释某些制药工艺。
4.认识酰胺的结构特征,能类比酯说明酰胺的主要性质。
5.能举例说明胺、酰胺类化合物在药物合成中的重要作用。
二、教学重难点重点:1.胺的性质;2.酰胺的性质。
难点:酰胺的性质。
三、教学方法总结归纳法、分组讨论法等四、教学过程【导入】展示常见感冒药主要成分【生】对乙酰氨基酚一、胺的结构与应用【讲解】1.胺的定义:氨分子中的氢原子被烃基取代而形成的一系列的衍生物称为胺。
胺的分子结构:与氨气类似,都是三角锥形。
2.胺的分类(1)根据氢上被烷基取代的数目,胺可分为一级胺(伯胺)RNH2,二级胺(仲胺)R2NH,三级胺(叔胺) R3N。
(2)根据胺分子中含有氨基的数目,可以将胺分为一元胺、二元胺、三元胺等。
(3)根据烃基的不同,胺可分为脂肪胺和芳香胺。
如乙胺CH3CH2NH2、苯胺C6H5NH2。
胺类广泛存在于生物界, 许多生物碱具有生理或药理作用。
3.结构简单的胺常用普通命名法,在烃基后直接加“胺”,如乙胺、二甲胺、苯胺等。
更多的胺类化合物则采用系统命名法,以烃为母体,氨基或烃氨基(—NHR,—NR2)作为取代基。
仲胺和叔胺, 当烃基相同时, 在烃基名称之前加词头“二”或“三”。
【生】单独完成胺类的命名【讲解】命名胺类化合物时应注意“氨”“胺”“铵”字的用法。
表示基团时用“氨”,如甲氨基(CH3NH—);表示氨的烃类衍生物时用“胺”;表示胺的盐时用“铵”。
伯、仲、叔胺中分别含有氨基(—NH2)、亚氨基(—NH—) 和次氨基()。
【讲解】4.胺的物理性质状态:低级脂肪胺,如甲胺、二甲胺和三甲胺等,在常温下是气体,丙胺以上是液体,十二胺以上为固体. 芳香胺是无色高沸点的液体或低熔点的固体,并有毒性.水溶性:低级的伯、仲、叔胺都有较好的水溶性。
随着碳原子数的增加,胺的水溶性逐渐下降。
【讲解】5.胺的化学性质与应用1、胺的碱性(1)与氨气结构相似,也具有碱性,可以与酸反应生成类似的铵盐。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
pKb 3.22
3.37
4.20 4.76 9.40 13.0
季铵碱是离子型化合物,是强碱,其碱性与氢氧化钠相当。
各类胺的碱性顺序:季铵碱>脂肪胺>氨>芳香胺
胺类一般为弱碱, 可与酸成盐, 但遇强碱又可重新游离析出来。 乙胺盐酸盐
苯胺盐酸盐 实验室中常常利用胺的盐易溶于水而遇强碱又重新游离析出的性质 来分离和提纯胺。
NH3 伯胺 RNH2
CH3NH2
仲胺
叔胺 季铵盐
R2NH
R3N
R4N+X-
(CH3)2NH (CH3)3N (CH3)4N+Cl-
NH2 氨基
NH
N
亚氨基 次氨基
注意:伯、仲、叔胺的区别与伯、仲、叔醇或卤代烃不同。
CH3 CH3—C—OH
CH3 叔丁醇
叔醇
CH3 CH3—C—Cl
CH3 叔丁基氯
sp3 杂化,但含更多 p 成分
N
H H
NH2
N上孤对电子离域到苯 环, 使苯环电子云密度升 高, N 上电子云密度降低
三、胺的性质 (一)胺的物理性质
伯胺、仲胺可以形成分子间氢键,其沸点高于相对分子质量相近的烷 烃,而低于相应的醇。叔胺不能形成分子间氢键,其沸点比相应的伯胺和仲 胺低 。低级胺能与水分子形成氢键而易溶于水。
医药上常将难溶于水的胺类药物制成盐,以增加其水溶性和稳定性。
2.酰化反应:伯胺、仲胺与酰化试剂作用,氮原子上的氢原子被酰 基(RCO—)取代生成N-取代或N,N-二取代酰胺
NHCH3 + (CH3CO)2O
N-乙基乙酰胺
O N CCH3 + CH3COOH CH3
N-甲基乙酰苯胺
酰化反应在医药上具有重要意义。在许多胺类药物的分子中引入酰基, 可以降低其毒副作用。
NO
N,N-二甲基-4-亚硝基苯胺 (绿色晶体 mp 86℃)
四、重要的胺及其衍生物
CH3CHCH2CHCH3 NH2 CH3
2-甲基-4-氨基戊烷
CH3CH2CHCH2CH2CHCH2CH3 CH2NH2 NHCH3
3-氨甲基-6-甲氨基辛烷
多元胺的命名类似于多元醇,例如:
H2NCH2CH2NH2
CH3CH2CHCH2CHCH3 NH2 NH2
乙二胺
2,4-己二胺
NH2 NH2
邻苯二胺
3.季铵类化合物命名:与无机铵盐及氢氧化物的命名相似 氯化四甲铵(季铵盐) 氢氧化四甲铵(季铵碱)
二、胺的结构
胺的结构与氨相似,具有棱锥形空间构型。氮原子为不等性 sp3杂化。
N H
H H
N
H
H
CH3
N
CH3 H3C
CH3
苯胺中的氮原子仍为不等性 sp3 杂化,但孤对电子所占据的 轨道含有更多 p 轨道的成分。
H N
H
R
H R
NH
H N
H
R
H R
NH
H N
H
R
H R
NH
(二)胺的化学性质
胺分子中氮原子上具有的孤对电子使胺具有碱性和亲核性。由 于p-π供电子共轭效应,芳香胺具有较高的亲电取代反应活性。
碱性 亲核性
芳香胺亲电取代 反应活性增高
—NH2
1.碱性:胺分子中氮原子上的孤对电子能接受质子呈碱性
NH3 + H2O
NH4 + OH
R N +H
RNH
N上的电子云密度↑,接受质子的能力↑,碱性↑。 碱性顺序 :脂肪胺 > 氨 > 芳香胺
胺的碱性强弱是电子效应、立体效应和溶剂化效应综合影响的结 果。胺的碱性强弱通常用pKb来表示,pKb越小,其碱性越强。
胺 (CH3)2NH>CH3NH2>(CH3)3N>NH3>C6H5NH2>(C6H5)2NH
O
HO
NH2 + (CH3CO)2O
HO
NHCCH3 + CH3COOH
对羟基苯胺
N-对羟基乙酰苯胺(扑热息痛)
胺的酰化反除应用于合成重要的酰胺类化合物外,还常用于保护氨基。
NH2
NHCOCH3
NHCOCH3
NH2
(CH3CO)2O
KMnO4
H+
CH3
CH3
COOH
COOH
3.与亚硝酸反应:胺与亚硝酸作用, 伯、仲、叔胺各不相同, 脂肪 胺和芳香胺也有差异。可用于鉴别。
苯胺
苄胺
芳香仲胺和芳香叔胺命名时,以芳香伯胺为母体,脂肪烃基 作为取代基,并在取代基名称前冠以“N-”或“N,N-”,表示这 些基团与氮原子直接相连,而不是连在芳环上。
NHCH3
N(CH3)2
N-甲基苯胺 N,N-二甲基苯胺
NCH2CH3 CH3
N-甲基-N-乙基苯胺
2.复杂胺命名:ห้องสมุดไป่ตู้以烃基为母体,氨基作为取代基进行命名
叔卤代烃
CH3 CH3—C—NH2
CH3 叔丁胺
伯胺
相应于氢氧化铵和铵盐的四烃基取代物, 分别称为季铵碱 和季铵盐。
季铵盐
胆碱 (季铵碱)
(二)胺的命名
1.简单胺命名:以胺为母体,烃基作为取代基,称为“某胺”
CH3CH2NH2 乙胺
CH3NHCH3 二甲胺
CH3NHCH2CH3 甲乙胺
甲乙异丙胺
胺类化合物具有多种生理作用,在医药上用作退热、镇痛、局 部麻醉、抗菌、驱虫等药物 。
(一)胺的分类
1.根据氮原子上所连烃基的种类不同,胺可分为脂肪胺和芳香胺
脂肪胺 芳香胺
CH3CH2NH2 NH2
CH3NHCH3 NHCH3
CH3CH2N
CH3 CH3
N(CH3)2
伯胺
仲胺
叔胺
2. 根据氮原子上所连烃基的数目不同,胺可分为伯胺(1º胺)、 仲胺(2º胺)和叔胺(3º胺)
•脂肪伯胺:定量放出N2,氨基酸和多肽定量分析
•芳香伯胺:低温下生成芳香重氮盐 重氮化(diazotization)反应
•脂肪或芳香仲胺:与亚硝酸作用都形成不溶于水的黄色油状物 N-亚硝基胺
(CH3CH2)2N-H + HO-NO
(C2H5)2N-NO + H2O
N-亚硝基二乙胺
NHCH3 + HNO2
N=O N CH3 + H2O
N-甲基-N-亚硝基苯胺
•脂肪叔胺 :与亚硝酸作用形成不稳定的水溶性亚硝酸盐。
(CH3)3N
NaNO2/HCl 室温
[(CH3)3NH]+NO22--
•芳香叔胺:与 HNO2 作用生成对亚硝基胺。
N(CH3)2 + NaNO2 +HCl 8℃
N(CH3)2 + H2O + NaCl
目录
第一节 胺 第二节 酰胺
学习目标
掌握 胺与酰胺的结构、命名及主要化学性质。 熟悉 胺的分类。 了解 重要的胺、酰胺及其衍生物。
第一节 胺
一、胺的分类和命名 二、胺的结构 三、胺的性质 四、重要的胺及其衍生物
一、胺的分类和命名
胺(amine)可以看作氨的烃基衍生物,即氨分子中的氢原子 被烃基取代后所形成的化合物 。
