新药申请表
新特药申请表&评审表

新特药申请表商品名剂型规格医保类型甲类招标类型中标品种中标价格乙类非中标品种非中标价自费中标编码:生产企业业务联系人联系电话主要用途与适应症与本院同类药品比较情况建议淘汰品种药物性价比申请人(临床医师)签名:年月日临床科室意见临床科室主任签字:年月日药剂科意见科室主任签字:年月日医院药事管理委员会意见业务院长签字:年月日集团药管部意见集团主管领导审批填表要求:字迹工整清楚,填写完整,对填写不完整的不予以受理。
备注:申请人申购产品,如在三个月发生产品滞销等现象,所剩产品直接由申请人负责清货,无法清货的直接扣除申请人绩效。
新药、特药形式筛查(评审)1.合法经营:□营业执照□许可证□委托书□身份证□GMP(GSP)证2.报备文件合法:□新药证书□生产批件□批准文号□注册商标批件□包装□标签说明书□价格批准文件(□企业□国家零售价:实价:扣率%:)3.质量文件齐全:□《药品质量保证书》、□法定质量标准、□法定检验报告4.是否有失效的证书、批件等文件:□有□无;与年月日补其。
5.品种费别等:□自费、□甲类、□乙类、□()线抗菌药物、□招标品种6.查HIS系统同类品种名称与规格:结论:□符合要求□资料不齐全□不能提供有效资料签名:年月日优选品种:①医保品种;②质优价廉;③仿制药质量标准有提高;④优选国家批准的新药,“增加规格的品种”次选;⑤与医院有长期合作且未发生过任何不良事件的。
严控品种:①质量标准有缺项的。
②药名、外观与医院的同类品种极其相似,易混淆的;③辅助药品、同类品种多的。
④严格管理的二~三线抗菌药物。
不采用品种:①曾发生过严重质量事件的厂商生产的品种;②疗效不确切,作用机理不清楚的;③国家通报有严重不良反应;④外国禁用的;⑤厂家、业务人员或供应商在我院有不良记录。
结论:□是优选品种第项;□是严控品种第项;□是不采用品种第项签名:年月日。
海南省中医院新药申请表

海南省中医院
临床科室药品引进申请表[通用名] [商品名]
[处方组成]
[生产厂家]
[包装规格及零售价]
[英文名] [批准文号或进口证号] [医保情况]甲类()、乙类()、自费()[是否挂网] [是否基药]
[是否国家谈判药品] [是否本地企业生产] [配送公司]
[申请理由]
(1)[该药在国内外应用情况]
(2)[该药的优势特点与同类药比较文献报道情况]
(3)[该药的临床不良反应与同类药比较文献报道情况]
备注:以上申请理由请详细提供相关资料
[参考文献]
[申请数量(1个月的用量)]
[用药可行性分析(能否按计划用完)]
[申请科室] 科主任签名:年月日(以上内容由临床科室主任填写,如填写不完请另附纸填写)
[初审情况汇报]
年月日。
新药申请表
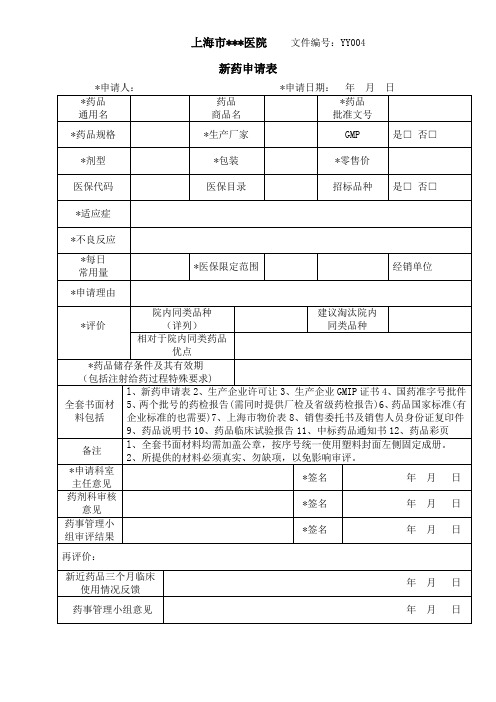
优点
*药品储存条件及其有效期
(包括注射给药过程特殊要求)
全套书面材
料ቤተ መጻሕፍቲ ባይዱ括
l、新药申请表2、生产企业许可让3、生产企业GMIP证书4、国药准字号批件5、两个批号的药检报告(需同时提供厂检及省级药检报告)6、药品国家标准(有企业标准的也需要)7、上海市物价表8、销售委托书及销售人员身份证复印件9、药品说明书10、药品临床试验报告11、中标药品通知书12、药品彩页
备注
l、全套书面材料均需加盖公章,按序号统一使用塑料封面左侧固定成册。
2、所提供的材料必须真实、勿缺项,以免影响审评。
*申请科室
主任意见
*签名
年月日
药剂科审核
意见
*签名
年月日
药事管理小
组审评结果
*签名
年月日
再评价:
新近药品三个月临床
使用情况反馈
年月日
药事管理小组意见
年月日
上海市***医院文件编号:YY004
新药申请表
*申请人:*申请日期:年月日
*药品
通用名
药品
商品名
*药品
批准文号
*药品规格
*生产厂家
GMP
是□否□
*剂型
*包装
*零售价
医保代码
医保目录
招标品种
是□否□
*适应症
*不良反应
*每日
常用量
*医保限定范围
经销单位
*申请理由
*评价
院内同类品种
(详列)
建议淘汰院内
同类品种
表1 新药引进申请表2019
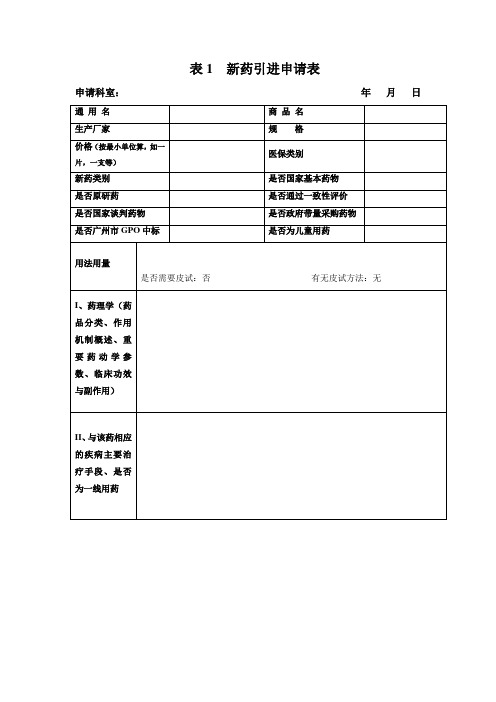
表1 新药引进申请表
申请科室:年月日
填写说明
1、请各位科室谨慎填写,申请科室对所填信息真实性负责,一旦将新药申请表
交给药学部,则不允许更换。
2、如是医保品种,注明医保类别,如不是则填“否”;如属国家新药品种注明几
类新药,如不是则填“否”;是原研厂家生产的品种填“是”,如不是则填“否”;
3、I-Ⅲ项需提供参考资料或相关指南,并清楚标识资料编号。
4、临床科室行政主任组织本专科专家对申请的药品进行集体讨论填写本表,并
由科室民主管理小组(科主任,副主任,护长,支部书记组成)亲笔签名,纸质版递交药学部临床药学科(饭堂旁边3D打印实验室2楼),电子版由行政主任通过OA发送给“药学部/新药申请”。
5、申请科室行政主任在新药遴选会上陈述申请理由,每个品种限时1.5分钟,
建议PPT主要内容不超过5页。
陈述PPT请和本表电子版一并发送至“药学部-新药申请”。
如果行政主任不能参会,可由行政主任安排人代陈述。
新药申请表

XX医院新药申请表
发表人签字及发表日期:申请受理编号:
《XX新药申请表》填写说明
一、我院引进的药品都必须能够经湖南省药品集中采购交易平台采购(除国家实行特殊管理的麻醉药品、第一、二类精神药品、医疗用毒性药品、放射性药品及中药材、中药饮片以外)。
二、以下申请材料不予受理:
1、上次申请未通过的药品(隔年可以申请);
2、同一品种已申请两次未获得通过的品种;
3、已被XX医院淘汰的品种
4、近年来发生过药品销售违规或不正当竞争行为的生产企业的产品。
三、临床科室递交新药引进申请时应同时提供以下材料,材料不全的新药申请不予受理:
1、新药申请表;
2、药品说明书,必须是国家药监局批准的正式说明书(销售包装内说明书和药监局批件复印件均可,产品宣传彩页不予受理);
3、文献证据(指南推荐、系统评价、随机对照试验等)。
四、新引进药品的采购价格和零售价格严格按省物价主管部门确定并在省交易平台公布的价格执行。
五、药品采购办公室每月两次集中受理新药申请,时间为每月第一个和第三个星期五。
其它时间不予办理新药引进工作。
六、药品采购办公室只接受与我院有业务往来的医药公司所提交的新药资料,不接受厂家及个人提交的新药材料。
七、药品采购办公室工作人员发放本表时应在左上角相应位置签名,并注明发表日期。
八、本申报表从领取之日起,七个工作日内必须交回药品采购办公室。
Welcome To Download !!!
欢迎您的下载,资料仅供参考!。
XXX医院新药引进申请表

XXXX医院新药引进申请表医院新药、特药药学评估评估日期:年月日医院新药、特药审批一、药剂科主任意见二、药事管理委员会意见三、院长或主管副院长意见医院新药、特药临床使用观察医院新药、特药临床使用期药学评估药品名称:规格:单价:生产厂家:供货单位:1.疗效及安全性评估2.制剂稳定性评估3.评价人:评价日期:年月日医院特殊药品引进申请表医院药品安全性再评价药品名称:规格:生产厂家:供货单位:一、ADR核实及临床调查(预警编号:)二、安全性再评价与处理意见:评价日期:年月日医院新药、特药形式筛查1.合法经营:□营业执照□许可证□委托书□身份证□GMP(GSP)证2.报备文件合法:□新药证书□生产批件□批准文号□注册商标批件□包装□标签说明书□价格批准文件(□企业□国家零售价:实价:扣率%:)3.质量文件齐全:□《药品质量保证书》、□法定质量标准、□法定检验报告4.是否有失效的证书、批件等文件:□有□无;与年月日补其。
5.品种费别等:□自费、□甲类、□乙类、□()线抗菌药物、□招标品种6.查HIS系统同类品种名称与规格:结论:□符合要求□资料不齐全□不能提供有效资料签名:年月日优选品种:①医保品种;②质优价廉;③仿制药质量标准有提高;④优选国家批准的新药,“增加规格的品种”次选;⑤与医院有长期合作且未发生过任何不良事件的。
严控品种:①质量标准有缺项的。
②药名、外观与医院的同类品种极其相似,易混淆的;③辅助药品、同类品种多的。
④严格管理的二~三线抗菌药物。
不采用品种:①曾发生过严重质量事件的厂商生产的品种;②疗效不确切,作用机理不清楚的;③国家通报有严重不良反应;④外国禁用的;⑤厂家或供应商在我院有不良记录。
结论:□是优选品种第项;□是严控品种第项;□是不采用品种第项签名:年月日。
北京世纪坛医院新药申请表

北京世纪坛医院新药申请表
附件1 北京世纪坛医院新药申请表
联系人姓名: 联系方式: 录入时间: 药品名称剂型规格、包装 (通用名) 北京市医保中标价格元零售价元报销范围
药典?
原料药主要质量标准部颁? 生产企业辅料成分
企业内控标准?
中标手册页码备案采购批件有无
收入指南名称: 药典?
具体内容: 所有数据来源杂志?
本厂?
药品检验生产厂家报告单正在使用医院
说明书中要求成分含量药品保存条件用法用量每日治疗费用元疗程
注射剂:溶解度、PH值、复配后稳定性、不溶性微粒等产品特点
药剂学特点
药代动力学特点
批准文号国药准字注射用溶媒选择:
适应症
主要不良反应
市场同类
产品比较
药剂科初审意见
专科主任意见并签字
质量委员会主任意见并签字。
医院新药申请表格模板

用法、用量及疗程:*****
临床推荐理由(药学的主要特点,如有同类品种性能价格的比较):
1、治疗优势:*****
2、剂型优势:方便
3、药物依从性:患者依从性高。
4、联合用药:对乙酰氨基酚、非布司他、非甾体消炎药
5、安全优势:*****
指南推荐情况:《*****诊疗指南》
科
新药申请单
通用名:*****
商品名:/
剂型:*****
规格:*****
给药途径:口服
主要成分:*****
生产厂家:*****
供货企业:*****
品种类型:相同品种 相似品种 新药品种√
医保类型:甲类 乙类√自费
医保编号:*****
基药情况:国基 省补 非基药√
价格 *****
挂网情况:挂网√非挂网
挂网质量层次:挂网限价
室
意
见
申请人意见:
申请人签字:
科室讨论意见:
科室负责人签字:
申请时间年月日
某某人民医院
新药申请表

年 月 日
********医院特殊用药申请表
申请科室: 日期: 年 月 日
药品通用名
商品名
药品剂型
规 格
用法用量
生产厂家
药品类别
(按院用药目录或药典2010版目录)
适应症
医保类别
甲类□
乙类□
自费□
国家基本药物
是□ 否□
基药补充药物
是□ 否□
申请数量
申请新药理由
申意见
药事管理与药物治疗学委员会讨论意见
罗田县第二人民医院新药申请表
药品通用名
商品名
零售价格
剂型
规格
适应症
用法用量
医保类别
甲类□
乙类□
自费□
平台挂网
是□否□
批准文号
生产厂家
报送公司
药品类别
(按院用药目录或药典2010版目录)
医院已有同类药品名称(无则不填)
名称
规格、剂型
生产厂家
剂型
申请科室
申请新药理由
申请医生
科主任签字
药剂科意见
药事管理与药物治疗学委员会讨论意见
西安交大二附院新药申请表【模板】

申请科室:
通用名
(商品名)
规格
生产企业
是否基药
是□否□
是否为医保品种
是□__________否□
是否中标
是□否□
有无同类药品
有□__________无□
价格(元)பைடு நூலகம்
价格依据
申请理由
循证医学证据
(可另附相关支持文献)
临床科室意见
科室三名以上副高签字:
临床主任签字:_________年 月 日
有无淘汰品种建议
有□(建议淘汰品种药品名称:)__________________________
无□
备注
注:1.本表仅限于本院临床科室新药申请使用,提交药学部汇总
2.多科室使用的药品可联合申请
3.本表用于药事会新药引进前的资料准备
临床新药申请表全部

新药申请规程为加强对新药申请的管理,规范新药申请行为,保障军地患者用药安全、有效,根据《医院药材采购管理办法(试行)》第一条、第二十二条、第二十三条,第三十一条规定,制定《新药申请规程》如下:1、填写《新药申请查询单》(表1)。
药剂科新药初审小组根据对医院现有药品情况的检索,判断申请引进药品是“新药品种”、“相似品种”、“相同品种”或“恢复品种”。
2、药剂科新药初审小组填写《新药查询登记表》(表2),对提出申请引进的药品按顺序编号。
3、由各科室行政主任填写《医院使用新药申请表》(表3,简称为《新药申请表》),根据《新药申请查询单》查询结论和临床需要,填写申请理由。
4、由药品供货公司填写《申请新药引进形式审查表》(表4),由药剂科新药初审小组进行形式审查,审查通过后,申请资料上交医院药事管理委员会。
5、根据上报资料,简明、扼要填写各申请引进药品的《新药申请汇报表》(表5)。
6、药事委员会例会前,将《参评新药汇总明细表》(表6)和《参评新药投票汇总》(表7)送药事会负责人审核;申请引进药品的药品说明书提前送达各委员预览。
7、药事委员会例会,各委员在《参评新药投票汇总》(表7)投票。
8、根据投票结果,作出《药事委员会新药审评意见》(表8)。
9、根据《药事委员会新药审评意见》,药剂科向申请新药引进公司发出《新药品种报价表》(表9),申请公司填写后送交药库。
由医院组织,随机抽选专家评审,产生中选公司。
药品的引进工作由药剂科按规定具体实施。
10、新药引进3个月在院内未使用,药剂科根据规定退药;对保留药品,药事委员会向申请科室和其他科室发出《新药引进使用反馈调查表》(表10),对该药有效性、安全性、经济性进行综合评价。
表1 新药申请查询单送达地点:药库(表1)新药申请查询单填写说明1.新药申请查询单用于新药申请初筛,为医院、药事会、临床、医药公司、药厂、药库所进行的新药申请评审提供参考。
2.处方成份填写药品活性成份,根据药品说明书填写。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
XX医院新药申请表
《XX新药申请表》填写说明
一、我院引进的药品都必须能够经湖南省药品集中采购交易平台采购(除国家实行特殊管理的麻醉药品、第一、二类精神药品、医疗用毒性药品、放射性药品及中药材、中药饮片以外)。
二、以下申请材料不予受理:
1、上次申请未通过的药品(隔年可以申请);
2、同一品种已申请两次未获得通过的品种;
3、已被XX医院淘汰的品种
4、近年来发生过药品销售违规或不正当竞争行为的生产企业的产品。
三、临床科室递交新药引进申请时应同时提供以下材料,材料不全的新药申请不予受理:
1、新药申请表;
2、药品说明书,必须是国家药监局批准的正式说明书(销售包装内说明书和药监局批件复印件均可,产品宣传彩页不予受理);
3、文献证据(指南推荐、系统评价、随机对照试验等)。
四、新引进药品的采购价格和零售价格严格按省物价主管部门确定并在省交易平台公布的价格执行。
五、药品采购办公室每月两次集中受理新药申请,时间为每月第一个和第三个星期五。
其它时间不予办理新药引进工作。
六、药品采购办公室只接受与我院有业务往来的医药公司所提交的新药资料,不接受厂家及个人提交的新药材料。
七、药品采购办公室工作人员发放本表时应在左上角相应位置签名,并注明发表日期。
八、本申报表从领取之日起,七个工作日内必须交回药品采购办公室。
