高考化学推断题专题整理(精)
高中化学推断题总结经典+全)
无机推断题复习无机推断题是在化学学科的历次高考改革中始终保留的一种基本题型,是高考的热点题型。
它以无机物的结构、性质和相互转化为载体,不仅能全面检查学生对元素及其化合物、物质结构、元素周期律等基础知识的掌握情况,检查学生灵活运用知识的能力,而且能考查学生抽象、求异、发散、收敛,逻辑推理,知识迁移,信息处理等方面的能力,也能很好地与化学实验、计算、基本化学用语,化学基础理论、元素及化合物,有机知识等学科内综合考查,对考生有很好的区分度,预计在今后的理科综合能力考查中,它将依然是化学学科的一种重要题型。
一、无机推断题复习方法和策略。
推断题融元素化合物、基本概念和理论于一体,侧重考查学生思维能力和综合应用能力。
在解无机推断题时,读题、审题相当重要,在读题审题过程中,要认真辩析题干中有关信息,抓住突破口,分析无机推断中的转化关系,仔细推敲,挖掘出隐含条件。
(一)基本思路读题(了解大意)→审题(寻找明显条件、挖掘隐含条件与所求)→解题(抓突破口)→推断(紧扣特征与特殊)→得出结论→正向求证检验读题:读题的主要任务是先了解题目大意,寻找关键词、句,获取表象信息。
切勿看到一点熟悉的背景资料就匆匆答题,轻易下结论,这样很容易落入高考试题中所设的陷阱。
审题:对读题所获信息提炼、加工,寻找明显的或潜在的突破口,更要注意挖掘隐含信息-“题眼”。
“题眼”常是一些特殊的结构、状态、颜色,特殊的反应、反应现象、反应条件和用途等等。
审题最关键的就是找出”题眼”。
解题:找到“题眼”后,就是选择合适的解题方法。
解无机推断题常用的方法有:顺推法、逆推法、综合推理法、假设法、计算法、实验法等。
通常的思维模式是根据信息,大胆猜想,然后通过试探,验证猜想;试探受阻,重新阔整思路,作出新的假设,进行验证。
一般来说,先考虑常见的规律性的知识,再考虑不常见的特殊性的知识,二者缺一不可。
验证:不论用哪种方法推出结论,都应把推出的物质代入验证。
如果与题设完全吻合,则说明我们的结论是正确的。
高考化学有机推断题集锦

2
4. A 、 B、C、 D 四种芳香族化合物的结构简式如下所示:
A
B
C
D
请回答下列问题:
( 1)写出 A 中无.氧.官能团的名称
, C中含氧官能团的结构简式为
。
( 2)用 A、 B、 C、 D 填空:能发生银镜反应的有
,既能与 FeCl3 溶液发生显色反应又能
化合物的结构简式是: B___________,C__________。反应④所用试剂和条件是 ________________ 。
10.为扩大现有资源的使用效率,在一些油品中加入降凝剂
J,以降低其凝固点,扩大燃料油品的使用范
围。丁是一种高分子聚合物,它的合成路线可以设计如下,其中
A 的氧化产物不发生银镜反应:
65 %,
则Y的分子式为 ______________ A的结构简式为 _______________ 。
( 2)第①②步反应类型分别为 ① _________________ ②_____________________ 。
( 3)化合物B具有的化学性质(填写字母代号)是
__________________________
( 4) G、 H和 D 互为同分异构体,它们具有如下特点:
① G 和 H 都是苯的二元取代物,这两个取代基分别为羟基和含有-
② G 和 H 苯环上的一氯代物有两种不同结构;
③ G 可以发生银镜反应, H 分子中苯环不与取代基碳原子直接相连
写出 G和 H的结构简式: G:
; H:
。
COO-结构的基团;
A. H2O B . CO2 C . O2 D . H2 答案:第 1 题答案 C 第 2 题答案 CD。第 3 题答案 A 第 4 题答案 A。
高考化学推断题综合题专题复习【认识有机化合物】专题解析及答案

高考化学推断题综合题专题复习【认识有机化合物】专题解析及答案一、认识有机化合物练习题(含详细答案解析)1.(1)的系统名称是_________;的系统名称为__________。
(2)2,4-二甲基-3-乙基戊烷的结构简式是_____,1mol该烃完全燃烧生成二氧化碳和水,需消耗氧气_______mol。
(3)键线式表示的物质的结构简式是__________________。
【答案】3,4-二甲基辛烷 1,2,3-三甲苯 14mol CH3CH2CH=CH2【解析】【分析】(1)命名烷烃时,先确定主链碳原子为8个,然后从靠近第一个取代基的左端开始编号,最后按取代基位次—取代基名称—烷烃名称的次序命名。
命名苯的同系物时,可以按顺时针编号,也可以按逆时针编号,但需体现位次和最小。
(2)书写2,4-二甲基-3-乙基戊烷的结构简式时,先写主链碳原子,再编号,再写取代基,最后按碳呈四价的原则补齐氢原子,1mol该烃耗氧量,可利用公式312n进行计算。
(3)键线式中,拐点、两个端点都是碳原子,再确定碳原子间的单、双键,最后依据碳呈四价的原则补齐氢原子,即得结构简式。
【详解】(1) 主链碳原子有8个,为辛烷,从左端开始编号,最后按取代基位次—取代基名称—烷烃名称的次序命名,其名称为3,4-二甲基辛烷。
命名时,三个-CH3在1、2、3位次上,其名称为1,2,3-三甲苯。
答案为:3,4-二甲基辛烷;1,2,3-三甲苯;(2)书写2,4-二甲基-3-乙基戊烷的结构简式时,主链有5个碳原子,再从左往右编号,据位次再写取代基,补齐氢原子,得出结构简式为;1mol该烃耗氧量为3912⨯+mol=14mol 。
答案为:;14mol ;(3)键线式中,共有4个碳原子,其中1,2-碳原子间含有1个双键,结构简式为CH 3CH 2CH=CH 2。
答案为:CH 3CH 2CH=CH 2。
【点睛】给有机物命名,确定主链时,在一条横线上的碳原子数不一定最多,应将横线上碳、取代基上碳综合考虑,若不注意这一点,就会认为的主链碳原子为7个,从而出现选主链错误。
高考化学必背推断题知识

高考化学必背推断题知识考生在准备化学复习的过程中,明确重点细化考点,要特别重视必考的知识点,理解并记熟。
下面小编给大家整理了关于高考化学必背推断题知识,欢迎大家阅读!高考化学必背推断题知识一、位置与结构1、Li是周期序数等于族序数2倍的元素。
2、S是最高正价等于最低负价绝对值3倍的元素。
3、Be、Mg是最外层电子数与最内层电子数相等的元素。
4、Li、Na是最外层电子数是最内电子数的1/2的元素。
5、最外层电子数是最内层电子数的2倍的是C、Si;3倍的是O、S;4倍的是Ne、Ar。
6、Be、Ar是次外层电子数等于最外层电子数的元素。
6、Mg是次外层电子数等于最外层电数4倍的元素。
7、Na是次外层电子数等于最外层电子数8倍的元素。
8、H、He、Al是原子最外层电子数与核外电子层数相等。
9、He、Ne各电子层上的电子数都满足2n2的元素。
10、H、He、Al是族序数与周期数相同的元素。
11、Mg是原子的最外层上的电子数等于电子总数的1/6的元素。
12、最外层上的电子数等于电子总数的1/3的是Li、P;1/2的有Be;相等的是H、He。
13、C、S是族序数是周期数2倍的元素。
14、O是族序数是周期数3倍的元素。
15、C、Si是最高正价与最低负价代数和为零的短周期元素。
16、O、F是最高正价不等于族序数的元素。
17、子核内无中子的原子氢( H)18、形成化合物种类最多的元素碳19、地壳中含量前三位的元素 O、Si、Al20、大气中含量最多的元素 N21、最外层电子数为次外层2倍的元素(或次外层电子数为最外层1/2的元素)C22、最外层电子数为次外层3倍的元素(或次外层电子数为最外层1/3的元素) O23、最外层电子数为次外层4倍的元素(或次外层电子数为最外层1/4的元素)Ne24、最外层电子数为次外层电子数1/2的元素Li、Si25、最外层电子数为次外层电子数1/4的元素 Mg25、最外层电子数比次外层电子数多3个的元素N26、最外层电子数比次外层电子数多5个的元素 F27、最外层电子数比次外层电子数少3个的元素P28、最外层电子数比次外层电子数多5个的元素 Al29、核外电子总数与其最外层电子数之比为3:2的元素C30、内层电子总数是最外层电子数2倍的原子有Li 、P31、电子层数跟最外层电子数数相等的原子有H 、Be、 Al32、核外电子总数与其最外层电子数之比为4:3的元素 O33、最外层电子数是电子层数2倍的原子有关He、 C、 S34、最外层电子数跟次外层电子数相等的原子有Be、Ar35、X、Y两元素可形成X2Y和X2Y2两种化合物(或形成原子个数比2:1与1:1的化合物 Na2O、Na2O2 、H2O、H2O2二、含量与物理性质1、O是地壳中质量分数最大的元素,Si次之,Al是地壳中质量分数最大的金属元素。
高考化学无机化学常考题型:无机化学推断题精选【答案+解析】

高考高高高高高高高高高高高高高高高高高高精选一、单选题(本大题共20小题,共40分)1.甲乙丙丁戊是中学常见的无机物,他们的转化关系如图所示(某些条件和部分产物已略去).下列说法错误的是()A. 若戊为一种强碱且焰色反应为黄色,则反应①②可能都属于氧化还原反应B. 常温下,若丙为无色气体,戊为红棕色气体,则甲、乙是铜和稀硝酸C. 若甲为硫磺燃烧产物,丁为水,则戊可用于干燥甲D. 若甲为浓盐酸,乙为MnO2,则戊可能使品红褪色2.甲、乙、丙、丁均为中学化学中常见的单质或化合物,它们之间的转化关系如下图所示(部分产物已略去),如表各组物质中不能按图示关系转化的是()选项物质转化关系甲乙丙丁A NaOH NaHCO3Na2CO3CO2B C CO CO2O2C Fe Fe(NO3)3Fe(NO3)2HNO3D AlCl3NaAlO2Al(OH)3NaOHA. AB. BC. CD. D3.元素A、B、C、D分别位于三个不同短周期,且原子序数依次增大.只有D为金属元素,它们可形成x、y、z、w四种常见的二元化合物及p、q两种常见三元化合物,它们之间存在如下转化关系;,,其中z 为液体、w为气体,其余均为固体.下列有关说法正确的是()A. 原子半径大小顺序:D>C>B>AB. y、p 中均只含有离子键C. B、D两元素最高价氧化物对应水化物分别为强酸、强碱D. p能抑制水的电离而q能促进水的电离4.A、B、C、D、E五种物质均含有同一元素,且A为单质,有如图所示的转化关系.则下列判断不正确的是()A. 若ABCDE中同一元素的价态均不相同,则A为气态单质B. 若A 为金属钠,则由ImolD 完全反应生成C 时,一定有1mol 电子转移C. 若A 为非金属硫,则④的反应类型既可以是氧化还原反应又可以是复分解反应D. 若A 为金属铁,则化合物C 和D 均可以由化合反应生成5. A 、B 、C 、D 是中学化学常见物质,其中A 、B 、C均含有同一种元素.在一定条件下相互转化关系如图,下列判断正确的是( )A. 若D 为H 2O ,A 为碳,则A 和C 反应生成1 mol B 转移的电子数为N AB. 若D 为Fe ,A 为CI 2,则B 溶液蒸干后可得到纯净的B 固体C. 若D 为O 2,A 为碱性气体,则以上转化只涉及两个氧化还原反应D. 若D 为HCl ,A 为Na 2CO 3,则B 溶液中c(Na +)=c(HCO 3−)+2c(CO 32−+c(H 2CO 3)6. 在给定的条件下,下列选项所示的物质间转化均能实现的是( ) A.漂白粉 B.C. Al →NaOH 溶液NaAlO 2→过量盐酸Al(OH)3D. 饱和NaCl 溶液→NH 3,CO 2NaHCO 3→△Na 2CO 37. 工业上用铝土矿(主要成分为Al 2O 3,含SiO 2、Fe 2O 3等杂质)为原料冶炼铝的工艺流程如下,对下述流程中的判断正确的是( )A. 试剂X 为稀硫酸,沉淀中含有硅的化合物B. 反应II 中生成Al(OH)3的反应为:CO 2+AlO 2−+2H 2O =Al(OH)3↓+HCO 3−C. 结合质子(H +)的能力由弱到强的顺序是OH −>CO 32−>AlO 2−D. Al 2O 3熔点很高,工业上还可采用电解熔融AlCl 3冶炼Al。
高考化学无机推断题大汇总

高考化学(huàxué)无机推断题大汇总高考化学无机(wújī)推断题大汇总全国名校高三化学调研精选(jīnɡ xuǎn)汇编1〔8分〕某、Y、Z为三种由短周期元素(yuán sù)构成的粒子,每mol粒子都有10mol电子,其结构特点如下:原子核数粒子(lìzǐ)的电荷数物质A由某、Z构成,B、C、D、K都是单质,反响①~⑤都是用于工业生产的反响,各有关物质之间的相互反响转化关系如以下图所示:请答复以下问题:(1)A的化学式为;D的结构式为。
(2)完成以下反响的离子方程式:反响①。
反响④。
(3)假设J气体浓度过高可导致高铁血红蛋白血症,且污染大气等。
但J也有不少的用途,如〔举出一例〕2.物质之间的转化关系如以下图所示,A〔只含两种元素〕可作为工业生产J的原料,B、C、H、I为非金属单质,某的水溶液为一种常见的无色医用消毒液,F为常见的红棕色防锈油漆颜料的主要成分,O是常见氮肥,且反响⑦中L 与M的物质的量之比为1∶2,A、E、J、N中含有同一种元素。
CAB高温①某单核1个单位正电荷Y四核0Z双核1个单位负电荷EFGH某③J高温④足量Ba(NO过滤32)溶液白色沉淀KLM高压⑦ND高温②OD设备ⅠI⑤设备ⅡH+I⑥答复以下问题:⑴某的化学式为_______________,C+D的反响方程式为___________________⑵考虑到综合经济效益,工业生产M时,可采取的措施有_______________(填字母序号)。
a.使用催化剂b.适当降低温度c.选择适宜的温度d.适度增大压强e.及时别离出产物f.对原料进行循环利用g.充分利用反响本身放出的热量h.工厂地址尽可能选择在交通兴旺的城市i.工厂地址可选择在盛产天然气的地区;设备Ⅰ的名称是_______________。
工业生产中为了节约资源、降低本钱和保护环境,常对某些物质进行循环利用。
高中化学推断题100题
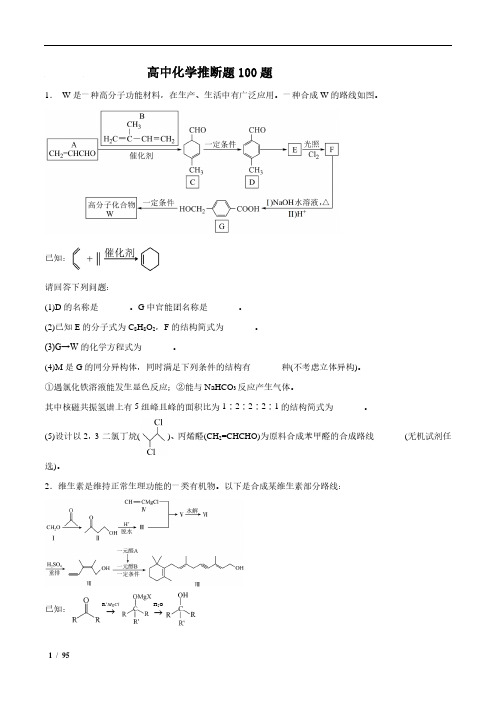
高中化学推断题100题1. W 是一种高分子功能材料,在生产、生活中有广泛应用。
一种合成W 的路线如图。
已知:请回答下列问题:(1)D 的名称是_______。
G 中官能团名称是_______。
(2)已知E 的分子式为C 8H 8O 2,F 的结构简式为_______。
(3)G→W 的化学方程式为_______。
(4)M 是G 的同分异构体,同时满足下列条件的结构有_______种(不考虑立体异构)。
①遇氯化铁溶液能发生显色反应;②能与NaHCO 3反应产生气体。
其中核磁共振氢谱上有5组峰且峰的面积比为1∶2∶2∶2∶1的结构简式为_______。
(5)设计以2,3-二氯丁烷()、丙烯醛(CH 2=CHCHO)为原料合成苯甲醛的合成路线_______(无机试剂任选)。
2.维生素是维持正常生理功能的一类有机物。
以下是合成某维生素部分路线:已知:R MgCl'→2H O→(1)化合物Ⅶ的分子式为________,该分子中处在同一平面的碳原子数为________。
(2)分析一元醛A 的结构特征,预测其可能的化学性质,完成下表 序号 结构特征 反应的试剂 反应形成的新结构 反应类型① -CHO Ag(NH 3)2OH _____ _____ ②_____________________(3)写出由化合物Ⅲ和Ⅳ反应生成化合物V 的方程式:________。
(4)化合物Ⅱ的同分异构体中能发生银镜反应但不能发生水解反应的共________种,其中核磁共振氢谱有3组峰,且峰面积比为6:1:1的同分异构结构简式为________。
(5)聚苯乙烯树脂是一种良好的保温材料,请以苯甲醛为原料,设计路线合成其单体苯乙烯____,其他试剂任选。
3.化合物H 是用于合成某种镇痛药的医药中间体,利用烃A 合成H 的某路线如下图所示:已知:Fe/HCl22R NO R NH ⎯−−⎯⎯→ 回答下列问题:(1)A 的化学名称为___________;D 中的官能团名称为___________。
高中化学推断题专题训练附详细答案

高中化学推断题专题训练附详细答案一.选择题(共4小题)1.某物质的实验式为PtCl4•2NH3,其水溶液不导电,加入AgNO3溶液反应也不产生沉淀,以强碱处理并没有NH3放出,则关于此化合物的说法中正确的是()A.配合物中中心原子的电荷数和配位数均为6B.该配合物可能是平面正方形结构C.4个Cl﹣和2个NH3分子均与Pt4+配位D.配合物中4个Cl﹣与Pt4+配位,而2个NH3分子与Pt4+不配位2.向盛有硫酸铜溶液的试管中加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到深蓝色透明溶液.下列对此现象的相关说法不正确的是()A.沉淀溶解后,生成深蓝色的配离子为[Cu(NH3)4]2+B.向反应后的溶液中加入乙醇,有沉淀析出C.在[Cu(NH3)4]2+离子中,Cu2+提供空轨道,NH3提供孤电子对D.反应前后,Cu2+浓度不变3.如图所示,装置在常温下工作(溶液体积变化忽略不计).闭合K,灯泡发光.下列叙述中不正确的是()A.当电路中有1.204×1022个电子转移时,乙烧杯中溶液的C(H+)约为0.1mol•L﹣1B.电池工作时,盐桥中的K+移向甲烧杯C.电池工作时,外电路的电子方向是从a到bD.乙池中的氧化产物为SO42﹣4.有4种燃料电池下面是工作原理示意图,其中正极反应的产物为水的是()A.固体氧化物燃料电池B.碱性氢氧燃料电池C.质子交换膜燃料电池D.熔融盐燃料电池二.填空题(共5小题)5.NH3分子中∠HNH键角为107°,而配离子[Zn(NH3)6]2+中∠HNH的键角为109,5°,配离子[Zn(NH3)6]2+中∠HNH键角变大的原因是。
6.(1)微粒间作用有多种,则CH3COONH4不同于CuSO4•5H2O的微粒间作用有(填字母).a.氢键b.配位键c.极性共价键d.非极性共价键(2)无水CrCl3和氨作用能形成两种配合物,组成相当于CrCl3•6NH3及CrCl3•5NH3,加入AgNO3溶液能从第一种配合物水溶液中将几乎所有的氯沉淀为AgCl,而从第二种配合物水溶液中仅能沉淀出相当于组成中含氯量2/3的AgCl,加入NaOH并加热时两种溶液都无味.则两种配合物的化学式分别为:、.(3)硝化甘油(C3H5N3O9)分解的产物为N2、CO2、O2和H2O,已知20℃时,2.27g 硝化甘油分解放出热量为15.4kJ,则其热化学方程式为,每生成1mol气体伴随放出的热量为kJ.7.推断下列化合物的化学式:(1)X、Y两元素能形成XY2型化合物,XY2中共有38个电子,若XY2是离子化合物,其化学式是;若XY2是共价化合物其化学式是.(2)第三周期内,X、Y两元素的原子序数之差为4,它们组成的XY型化合物,其化学式为.(3)1mol某物质含有不同周期三种元素的原子各1mol,其质子总数为20mol,该物质的化学式为.(4)某非金属X的最高正价为+m,它的最高价氧化物对应的水化物中有b个氧原子,则这种酸的化学式是.(5)X元素的最高正价和负价绝对值之差为6,Y元素和X元素原子的次外电子层上都有8个电子,X和Y形成的化合物在水溶液中能电离出电子层结构相同的离子,则该化合物是.8.为确认HCl、H2CO3、H2SiO3的酸性强弱,某学生设计了如图所示的装置,一次实验即可达到目的(不必选其他酸性物质).请据此回答:(1)锥形瓶中装某可溶性正盐溶液,分液漏斗中所盛试剂应为.(2)装置B所盛的试剂是,其作用是.(3)装置C所盛的试剂是,C中反应的离子方程式.(4)由引得出的结论是:酸性>>.9.25℃时,将体积Va,pH=a的某一元强碱与体积为V b,pH=b的某二元强酸混合.(1)若所得溶液的pH=11,且a=13,b=2,则Va:Vb=.(2)若所得溶液的pH=7,且已知Va>Vb,b=0.5a,b值可否等于4(填“可”或“否”)(3)为了更好的表示溶液的酸碱性,科学家提出了酸度(AG)的概念,AG的定义为AG=lg.25℃时,若溶液呈中性,则AG=,溶液的pH与AG的换算公式为AG=(要简化).三.实验题(共2小题)10.某兴趣小组利用图1实验装置研究铁发生腐蚀的条件。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
高考化学推断题专题整理(精)化学推断题专题高考化学推断题包括实验推断题、有机物推断题和无机物推断题,它对考生的思维能力和知识网络构造提出了较高的要求,即要求考生有较深厚的化学功底,知识网络清晰,对化学的所有知识点(如元素、化合物的性质了如指掌。
一、找到突破口进行联想:推断题首先要抓住突破口,表现物质特征处大都是突破口所在,所以考生在掌握化学知识概念点上,要注意总结它的特征。
在推断题的题干中及推断示意图中,都明示或隐含着种种信息。
每种物质都有其独特的化学性质,如物质属单质还是化合物,物质的颜色如何,是固体、液体还是气体,有怎样的反应条件,反应过程中有何现象,在生活中有何运用等,同时还要注意表述物质的限制词,如最大(小、仅有的等。
考生看到这些信息时,应积极联想教材中的相关知识,进行假设重演,一旦在某一环节出错,便可进行另一种设想。
二、在训练中找感觉:一般而言,推断题的思维方法可分三种:一是顺向思维,从已有条件一步步推出未知信息;第二种是逆向思维,从问题往条件上推,作假设;第三种则是从自己找到的突破口进行发散推导。
解推断题时,考生还可同时找到几个突破口,从几条解题线索着手,配合推断。
可以说化学推断题没有捷径可谈,它需要考生在训练中总结经验、寻找规律,发现不足后再回归课本,再进行训练,螺旋上升。
如此而为,做推断题便会有“感觉”。
无机推断题既能考查元素及其化合物知识的综合应用,又能对信息的加工处理、分析推理、判断等方面的能力加以考查,因此此类题型应是考查元素及其化合物知识的最佳题型之一。
无机物的综合推断,可能是对溶液中的离子、气体的成分、固体的组成进行分析推断,可以是框图的形式,也可以是文字描述的形式(建议考生有时可以先在草稿纸上把文字描述转换成框图形式,这样可以一目了然。
不管以哪种方式出题,解题的一般思路都是:迅速浏览→产生印象→寻找突破口→注意联系→大胆假设→全面分析(正推和逆推→验证确认。
解题的关键是依物质的特性或转移特征来确定突破口(题眼,顺藤摸瓜,进而完成全部未知物的推断。
因此首先应熟练掌握各种常见元素及其常见化合物之间相互转化的基础知识,并能够形成网络,其次就是要善于抓住题目的突破口。
一、无机物知识网络:1、重要的非金属及其化合物:2、重要的金属及其化合物:二、常见的突破口:抓住题目的突破口,是解决无机推断题的关键。
题目中的突破口可能是显性的,也可能是隐性的。
显性的突破口通常是指物质特殊的物理、化学性质、用途以及一些特征的反应现象;而隐性的突破口则往往是一些特殊的反应类型或者物质之间的转化关系。
1、物质颜色红色:Fe2O3、Fe(OH3、FeSCN2+、Cu2O、Cu、NO2、Br2(g、P;橙色:Br2的溶液;黄色:S、Na2O2、AgBr、AgI、Ag3PO4、Fe3+(aq、久置浓HNO3;绿色:Fe2+( aq、绿矾、铜绿、浓CuCl2、Cu+浓HNO3;蓝色:Cu2+(aq、胆矾、Cu(OH2;紫色:石蕊、KMnO4、I2(g、Fe3++C6H5OH;黑色:多数过渡金属的氧化物以及硫化物、C、Fe等;白色:CaCO3、BaSO4、A gCl、Mg(OH2、Al(OH3、MgO、Al2O3。
2、物质状态液态单质:Br2、Hg;液态化合物:H2O、H2O2、H2SO4、HNO3等;气态单质:H2、N2、O2、F2、Cl2等;气态化合物:C、N、S的氢化物及氧化物等。
3、反应现象或化学性质(1焰色反应:黄色—Na;紫色(钴玻璃—K。
(2与燃烧有关的现象:火焰颜色:苍白色:H2在Cl2中燃烧; (淡蓝色:H2、CH4、CO 等在空气中燃烧;黄色:Na在Cl2或空气中燃烧;烟、雾现象:棕(黄色的烟:Cu或Fe在Cl2中燃烧;白烟:Na在Cl2或P在空气中燃烧;白雾:有HX等极易溶于水的气体产生;白色烟雾:P在Cl2中燃烧。
(3沉淀特殊的颜色变化:白色沉淀变灰绿色再变红褐色:Fe(OH2→Fe(OH3;白色沉淀迅速变棕褐色:AgO H→Ag2O。
(4使湿润的红色石蕊试纸变蓝的气体:NH3;(5能使品红溶液褪色加热后又复原的气体:SO2;(6在空气中迅速由无色变成红棕色的气体:NO;(7使淀粉溶液变蓝的物质:I2;(8能漂白有色物质的淡黄色固体:Na2O2;(9在空气中能自燃的固体:P4;(10遇SCN-变红色、OH-产生红褐色沉淀、苯酚显紫色的离子:Fe3+;(11不溶于强酸和强碱的白色沉淀:AgCl、BaSO4;(12遇Ag+生成不溶于硝酸的白色、浅黄色、黄色沉淀的离子分别是:Cl-、Br-、I-。
(13可溶于NaOH的白色沉淀:Al(OH3、H2SiO3;金属氧化物:Al2O3;(14可溶于HF的酸性氧化物:SiO2;(15能与NaOH溶液反应产生气体的单质:Al、Si、;化合物:铵盐;(16能与浓硫酸、铜片共热产生红棕色气体的是:硝酸盐;(17通入二氧化碳产生白色胶状沉淀且不溶于任何强酸的离子:SiO32-;(18溶液中加酸产生的气体可能是:CO2、SO2、H2S;溶液中存在的离子可能是:CO32-、HCO3-;SO32-、HSO3-;S2-、HS-;(19同一元素的气态氢化物和最高价氧化物对应水化物能反应生成盐的元素:N;(20与酸、碱都能反应的无机物:Al、Al2O3、Al(OH3、弱酸酸式盐、弱酸弱碱盐等;(21能与水反应生成气体的物质:K、Na、NaH;Na2O2、CaC2及Mg3N2、Al2S 3等;(22既有气体又有沉淀生成的反应:Ba(OH2、Ca(OH2与NH4HCO3、(NH42SO 4等;(23先沉淀后溶解的反应:Ca(OH2+CO2、AgNO3+氨水、Al3++OH-、AlO2-+ OH-、Ba(OH2+H3PO4 等;(24见光易分解的物质:HClO、HNO3、AgCl、AgBr、AgI;(25使用催化剂的反应:合成氨、三氧化硫的生成、氨的催化氧化、制氧气等。
4、特殊的反应类型:往往是题目的隐性突破口。
(1单质A + 化合物B →单质C + 化合物D即置换反应,可以是金属置换出金属(最常见的是铝热反应或金属置换出非金属(被置换出来的非金属应该是还原产物,而还原产物在一定条件下具有一定的还原性,故通常是H2或C,也可以是非金属置换出非金属(常见的是卤素单质之间的置换或F2置换出O2、当然卤素都能置换出S,另外C可以置换出Si、H2或非金属置换出金属(此时的非金属必作还原剂,而常见的还原性非金属只有C和H2。
(2A 的化合物 + A的化合物→ A 的单质 + 化合物B该反应通常是一个归中到单质的反应,该单质必为非金属单质,常见的是S、Cl2、N2。
(3单质A + 强碱→两种含A 元素的化合物该反应是一个碱性歧化反应,单质A 通常是X2或S;(4单质A + 单质B →化合物C ;C + 单质A →化合物D综合以上两个反应,可知A、B两种元素可以形成C、D两种以上的化合物,其中必定有一种元素有变价。
若有变价的元素是金属,则必为Fe;若有变价的元素为非金属则该元素通常是C、N、S或O等,故以上C、D分别是NO、NO2或CO、CO2、或SO2、SO3或Na2O、Na2O2等。
(5一种物质分解得到两种以上产物:常见的有KMnO4、NaHCO3、NH4HCO3、(NH42CO3、NH4I、Cu2(OH2C O3等的分解。
(6多种物质化合得到一种物质:如Fe(OH2+O2+H2O;NOx+O2+H2O等(7电解类型(惰性电极:生成两种产物:电解质分解型或电解水型或熔融的NaCl等。
生成三种产物:放氧生酸型或放氢生碱型。
生成三种气体:电解氨水或NH4Cl溶液。
(8与化工生产有关的反应:如制漂白粉、制生石灰、工业合成氨、氯碱工业、硫酸工业、硝酸工业、玻璃工业等。
三、例题解析[例题1]:X、Y、Z为常见的三种单质,常温下X为固体,Y是液体,Z是无色气体。
其反应关系如下图所示,其中B的溶液显强酸性。
请回答下列问题:(1根据上述关系,确定X、Y、Z的化学式:X 、Y 、Z ;(2Y元素在周期表中的位置是;(3写出A溶于水后加X的离子方程式:;(4写出C溶液中通入过量氯气的离子方程式:。
[解析]:突破口错误!未找到引用源。
:“Y是液体(单质”,则Y可能是液溴或汞,应为液溴;突破口错误!未找到引用源。
:“Z是无色气体(单质,B的溶液为强酸性”则Z为H2、B为HBr;突破口错误!未找到引用源。
:“B(HBr+X(单质→C+Z(H2”该反应是一个从酸中置换出H2的反应,X必为金属,C为金属溴化物;突破口错误!未找到引用源。
:“C(金属溴化物+Y(溴→A”,A必为金属X的另一种溴化物,故X必为有变价的金属,应为Fe。
答案:见解析[例题2]:下图中A是一种无色液体,G是一种极易溶于水的碱性气体,Y是胃酸的主要成分,K是不溶于稀硝酸的白色沉淀,反应5是工业制X的主要反应之一。
请按要求填空:(1写出下列物质的化学式A 、E 、F 、Y ;(2写出反应5的化学方程式;(31molB通过反应2得到1molF,B中F的质量分数为72%,则B的化学式为。
[解析]:突破口错误!未找到引用源。
:“Y是胃酸的主要成分”,则为HCl;突破口错误!未找到引用源。
:“K为不溶于稀硝酸的白色沉淀”,必为BaSO4或Ag Cl,应为AgCl,故I为AgNO3、X为HNO3,再由反应4可推出F为Ag,结合反应1可进一步得知A为H2O,H为NO2;突破口错误!未找到引用源。
:“G为碱性气体”,则必为NH3,结合反应1、3、5可知C、D、E、J分别为O2、H2、N2、NO;突破口错误!未找到引用源。
:“1molB得到1molF”,则B的化学式为AgNx,结合质量分数可以算出x=3。
答案:见解析[例题3]:A、B、C是常见的单质,X、Y、Z是氧化物,它们之间有如右图所示的转化关系:请写出符合下列要求的化学方程式(1若X为CO2、B为红色固体,则:反应1:;反应2:;(2若X为Fe3O4、A为银白色固体,则:反应1:;反应2:。
[解析]:由“A、B、C是单质,X、Y、Z是氧化物”可知反应1、2都是有有氧化物参加的置换反应。
(1“X为CO2”且A单质能在其中燃烧,则A为Mg,C为C、Y为MgO。
“B为红色固体(单质”,必为Cu,故Z为CuO。
(2“X为Fe3O4、A为银白色固体”,则反应1为金属单与金属氧化物之间的置换反应,常见的是铝热反应,故A、Y、C分别为Al、Fe、Al2O3;C(铁通过反应2得到X(Fe3O4,常见生成Fe3O4的反应只有两个,其中属于置换反应的只有一个,故Z、B分别是H2O、H2。
答案:见解析[例题4]:如图所示,A、B、C、D、G是五种常见单质,其中A、G为气体。
