高考化学无机推断题集锦
高考化学无机非金属材料推断题综合题汇编及详细答案

高考化学无机非金属材料推断题综合题汇编及详细答案一、无机非金属材料练习题(含详细答案解析)1.某混合物X由Na2O、Fe2O3、Cu、SiO2中的一种或几种物质组成.某校兴趣小组以两条途径分别对X进行如下实验探究.下列有关说法不正确的是()A.由Ⅱ可知X中一定存在SiO2B.无法判断混合物中是否含有Na2OC.1.92 g固体成分为CuD.15.6 g混合物X中m(Fe2O3):m(Cu)=1:1【答案】B【解析】途径a:15.6gX和过量盐酸反应生成蓝色溶液,所以是铜离子的颜色,但是金属Cu和盐酸不反应,所以一定含有氧化铁,和盐酸反应生成的三价铁离子可以和金属铜反应,二氧化硅可以和氢氧化钠反应,4.92g固体和氢氧化钠反应后,固体质量减少了3.0g,所以该固体为二氧化硅,质量为3.0g,涉及的反应有:Fe2O3+6H+=2Fe3++3H2O;Cu+2Fe3+=2Fe2++Cu2+,SiO2+2NaOH=Na2SiO3+H2O,又Cu与NaOH不反应,1.92g固体只含Cu;结合途径b可知15.6gX和足量水反应,固体质量变为6.4g,固体质量减少15.6g﹣6.4g=9.2g,固体中一定还有氧化钠,其质量为9.2g,A.由以上分析可知X中一定存在SiO2,故A正确;B.15.6gX和足量水反应,固体质量变为6.4g,只有氧化钠与水反应,混合物中一定含有Na2O,故B错误;C.Cu与NaOH不反应,1.92g固体只含Cu,故C正确;D.设氧化铁的物质的量是x,金属铜的物质的量是y,由Fe2O3+6H+=2Fe3++3H2O、Cu+2Fe3+=2Fe2++Cu2+得出:Fe2O3~2Fe3+~Cu,则160x+64y=6.4,64y﹣64x=1.92,解得x=0.02mol,y=0.05mol,所以氧化铁的质量为0.02mol×160g/mol=3.2g,金属铜的质量为0.05mol×64g/mol=3.2g,则原混合物中m(Fe2O3):m(Cu)=1:1,故D正确;【点评】本题考查了物质的成分推断及有关化学反应的简单计算,侧重于学生的分析和计算能力的考查,为高考常见题型,注意掌握检验未知物的采用方法,能够根据反应现象判断存在的物质,注意合理分析题中数据,根据题中数据及反应方程式计算出铜和氧化铁的质量,难度中等.2.下列说法中正确的是A.水玻璃和石英的主要成分都是SiO2B.Si、SiO2和SiO32-等均可与NaOH 溶液反应C.二氧化硅属于酸性氧化物,不溶于任何酸D.高岭石[Al2(Si2O5)(OH)4]可表示为Al2O3·2SiO2·2H2O【答案】D【解析】【分析】【详解】A.水玻璃的主要成分是硅酸钠,石英的主要成分是SiO2,故A错误;B.Si、SiO2均可与NaOH溶液反应,但SiO32-不能与NaOH溶液反应,故B错误;C.二氧化硅属于酸性氧化物,二氧化硅能溶于氢氟酸,故C错误;D.用氧化物的形式表示硅酸盐的组成时,各氧化物的排列顺序为:较活泼金属的氧化物→较不活泼金属的氧化物→二氧化硅→水,则高岭石[Al2(Si2O5)(OH)4]可表示为Al2O3·2SiO2·2H2O,故D正确;答案选D。
高考化学高无机综合推断-经典压轴题附答案

高考化学高无机综合推断-经典压轴题附答案一、无机综合推断1.已知C、D、G、I为短周期元素形成的单质,D、G、I常温下为气态,且G为黄绿色;形成D的元素原子的最外层电子数是次外层的3倍;B的焰色反应呈紫色(透过蓝色钴玻璃);K为红棕色粉末。
其转化关系如图。
请回答:(1)工业上制C用A不用H的原因______________________。
(2)写出C与K反应的化学方程式_________________,该反应的反应物总能量___________(填“大于”或“小于”)生成物总能量。
(3)L是目前应用最广泛的金属,用碳棒作阳极,L作阴极,接通电源(短时间)电解E水溶液的化学方程式___________________。
(4)写出E物质的电子式___________________。
(5)J与H反应的离子方程式为________________________。
(6)写出G与熟石灰反应制取漂白粉的化学方程式_______________________。
【答案】氯化铝是共价化合物,熔融状态下不导电 2Al+Fe2O3高温Al2O3+2Fe 大于2KCl+2H2O2KOH+H2↑+Cl2↑ Al3++3AlO2-+6H2O=4Al(OH)3↓2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O【解析】【分析】【详解】形成D的元素的原子最外层电子数是次外层的3倍,原子只能有2个电子层,最外层电子数为6,则D为O2;K为红棕色固体粉末,K为Fe2O3;由于电解A得到C与D,则C与K 生成A的反应为铝热反应,故A为Al2O3,L为Fe,C为Al;黄绿色气体G为Cl2,与C反应得到H为AlCl3;B的焰色反应呈紫色(透过蓝色钴玻璃),B中含有K元素,B在催化剂、加热条件下反应生成氧气,则B为KClO3,E为KCl,电解KCl溶液生成KOH、H2和Cl2,过量的F与氯化铝反应得到J,则I为H2,F为KOH,J为KAlO2;(1)H为AlCl3,氯化铝是共价化合物,熔融状态下不导电,故工业上制Al用氧化铝不用氯化铝,故答案为氯化铝是共价化合物,熔融状态下不导电;(2)C与K反应的化学方程式为:2Al+Fe2O3高温Al2O3+2Fe,该反应为放热反应,故该反应的反应物总能量大于生成物总能量,故答案为2Al+Fe2O3高温Al2O3+2Fe;大于;(3)Fe是目前应用最广泛的金属,用碳棒作阳极,Fe作阴极,接通电源(短时间)电解KCl水溶液的化学方程式为:2KCl+2H2O 电解2KOH+H2↑+Cl2↑,故答案为2KCl+2H2O 电解2KOH+H2↑+Cl2↑;(4)E为KCl,KCl的电子式为,故答案为;(5)J与H反应的离子方程式为:Al3++3AlO2-+6H2O=4Al(OH)3↓,故答案为Al3++3AlO2-+6H2O=4Al(OH)3↓;(6)G为Cl2,G与熟石灰反应制取漂白粉的化学方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,故答案为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O。
高考化学无机化学推断题专题复习
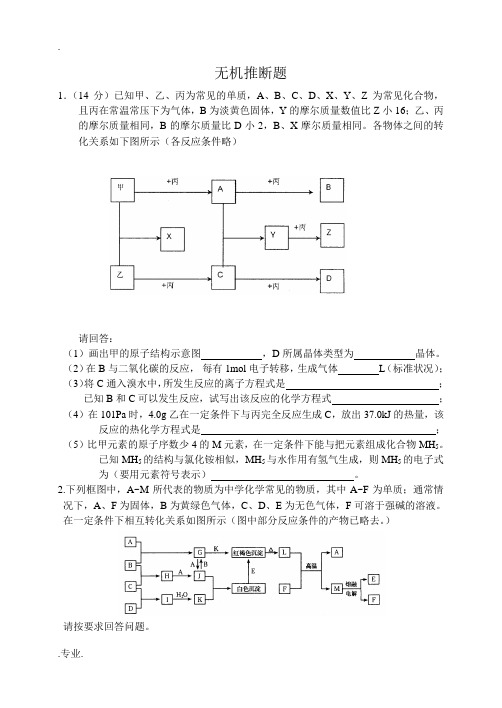
无机推断题1.(14分)已知甲、乙、丙为常见的单质,A、B、C、D、X、Y、Z为常见化合物,且丙在常温常压下为气体,B为淡黄色固体,Y的摩尔质量数值比Z小16;乙、丙的摩尔质量相同,B的摩尔质量比D小2,B、X摩尔质量相同。
各物体之间的转化关系如下图所示(各反应条件略)请回答:(1)画出甲的原子结构示意图,D所属晶体类型为晶体。
(2)在B与二氧化碳的反应,每有1mol电子转移,生成气体L(标准状况);(3)将C通入溴水中,所发生反应的离子方程式是;已知B和C可以发生反应,试写出该反应的化学方程式;(4)在101Pa时,4.0g乙在一定条件下与丙完全反应生成C,放出37.0kJ的热量,该反应的热化学方程式是;(5)比甲元素的原子序数少4的M元素,在一定条件下能与把元素组成化合物MH5。
已知MH5的结构与氯化铵相似,MH5与水作用有氢气生成,则MH5的电子式为(要用元素符号表示)。
2.下列框图中,A~M所代表的物质为中学化学常见的物质,其中A~F为单质;通常情况下,A、F为固体,B为黄绿色气体,C、D、E为无色气体,F可溶于强碱的溶液。
在一定条件下相互转化关系如图所示(图中部分反应条件的产物已略去。
)请按要求回答问题。
(1)写出代学式:A ,B ,C ,D 。
(2)I的电子式为,I与E在催化剂(如铂等)存在的条件下,发生反应的化学方程式为。
(3)将G的水溶液加热、蒸干、灼烧,最后得到的固体是;G与K反应的离子方程式为。
(4)写出下列反应的化学方程式:①L+F→A+M 。
②M→E+F 。
3.设X、Y、Z、A、B分别代表五种短周期元素,已知:①Y m-和Z n-两种离子具有相同的电子层结构;②Y和X可以形成原子个数比为1:1的化合物甲和原子个数比为1:2的化合物乙,甲和和乙都是共价化合物;③Z和X可以形成原子个数比为1:1的化合物丙,其分子与乙的分子所含质子数相同;④Y和A是同周期相邻的两种元素,Y 和B是同主族相邻的两种元素;⑤Y、A、B三种元素的原子序数之和为31。
高中化学10道无机推断练习题(附答案)

高中化学10道无机推断练习题_一、推断题1.某课外学习小组对日常生活中不可缺少的调味品M进行探究。
已知C可在D中燃烧发出苍白色火焰。
M与其他物质的转化关系如下图所示(部分产物、反应条件已略去):(1)常温下,用惰性电极电解M溶液(足量)发生反应的离子方程式为___________________,电解一段时间后,让溶液复原的方法为______________________,若M溶液为0.5L,电解一段时间后,两极共生成气体1.12L(已折算为标准状况下的体积),则电解后溶液的pH为________(忽略溶液的体积变化)。
(2)若A是一种常见的难溶于水的酸性氧化物,可用于制造玻璃,则E溶液的俗称是_____________。
(3)若A是CO2气体,将一定量的A通入B溶液,得到溶液W,再向溶液W中滴入盐酸,相关量如图所示,则溶液W中的溶质及其物质的量分别为__________________、______________________。
(4)若A是一种化肥。
A和B反应可生成气体E,E与D相遇产生白烟,工业上可利用E与D的反应检查输送D的管道是否泄漏,是因为E与D可发生反应:____________________(写化学方程式)。
2.已知A为淡黄色固体,T为生活中使用最广泛的金属单质,D是具有磁性的黑色晶体,C是无色无味的气体,H是白色沉淀。
(1)物质A的化学式为 ________。
(2)H在潮湿空气中变成M的实验现象是_____________________,化学方程式为______________________。
(3)A和水反应生成B和C的离子方程式为_______________,列出A的一种重要用途_________。
(4)反应①的离子方程式为________________________。
3.A-I分别表示中学化学中的常见物质,它们之间的相互转化关系如下图所示(部分反应物、生成物没有列出),且已知G是一种两性氧化物,A、B、C、D、E、F六种物质中均含有同一种元素,F 为红褐色沉淀。
高考化学复习各地无机推断题集锦.doc

高考化学复习各地无机推断题集锦1、对从太空某星球外层空间取回的气体样品分析如下:(1)将样品溶于水,发现其主要成分气体A 极易溶于水,水溶液呈酸性;(2)将A 的浓溶液与KMnO 4反应产生一种黄绿色气体单质B ,将B 通入石灰乳可生成两种钙盐的混合物D 。
(3)A 的稀溶液与锌粒反应生成气体C ,C 与B 的气体充分混合经光照发生爆炸又生成气体A ,实验测得反应前后气体体积不变。
据此回答下列问题:(1)写出A 、B 、C 、D 的化学式: A________;B________C_________D___________。
(2)气体B 与Ca(OH)2的化学反应方程式____________________,混合物D 俗名是__________________,它的有效成分是____________________,其有效成分与空气里的二氧化碳和水蒸气反应的方程式是________________________________。
2、列物质间有如下转化关系浅黄色固体WE③②气体甲E①气体乙白色悬浊液C固体A溶液B点燃液B 溶 ④液体E 气体丙 液D溶溶液B(1)W 为__________(2)固体A 是一种重要的工业原料,1mol 气体乙完全燃烧时生成1molE 和2mol 丙,则乙的分子式为____________(3)C 溶液中的溶质和丙以物质的量之比1:2反应时,离子方程式为 __________________________________________________________。
(4)利用图中有关物质实现C →B 的转变,该物质是___________(填化学式) (5)若甲和乙恰好完全反应,则A 和W 的物质的量之比为__________3、有A 、B 、C 、D 、E 、F 、G 七种常见物质,它们满足下图所示转化关系。
已知:○1A 、B 、C 、D 含同一种元素;○2A 、B 、C 、D 、E 、F 、G 都不是氧化物; ○3D 、G 是钠盐; ○4A 、E 、F 、G 含同一种元素,且F 为单质, E 在常温下为气体。
高考化学无机非金属材料推断题综合经典题含答案

高考化学无机非金属材料推断题综合经典题含答案一、无机非金属材料练习题(含详细答案解析)1.甲、乙、丙、丁、戊五种物质是中学化学常见的物质,其中甲、乙均为单质,它们的转化关系如图所示(某些条件和部分产物已略去)。
下列说法正确的是A .若甲可以与NaOH 溶液反应放出H 2,则丙一定是两性氧化物B .若甲为短周期中最活泼的金属,且戊为碱,则丙生成戊一定是氧化还原反应C .若丙、丁混合产生大量白烟,则乙可能具有漂白性D .若甲、丙、戊都含有同一种元素,则三种物质中,该元素的化合价由低到高的顺序可能为甲<丙<戊【答案】D【解析】【详解】A .甲为单质,若甲可以与NaOH 溶液反应放出2H ,则甲为Al 或Si ,所以丙可能是氧化铝,也可能是二氧化硅,不一定是两性氧化物,故A 错误;B .若甲为短周期中最活泼的金属,且戊为碱,则甲为Na ,乙为氧气,所以丙可以为氧化钠或过氧化钠,当丙为氧化钠时,丙生成戊不是氧化还原反应,故B 错误;C .丙、丁混合产生白烟,则丙、丁可为HCl 和3NH 或3HNO 和3NH 等,甲、乙均为单质,则乙可能是氯气或氢气或氮气,都不具有漂白性,故C 错误;D .若甲、丙、戊含有同一种元素,当甲为S ,乙为氧气,丙为二氧化硫,丁为HClO 等具有强氧化性的物质,戊为硫酸,则含S 元素的化合价由低到高的顺序为甲<丙<戊,故D 正确;故答案为D 。
2.某一固体粉末含有SiO 2、Fe 2O 3、Al 2O 3,加入足量NaOH 溶液充分反应后,过滤,向所得溶液中加入过量盐酸,过滤,将所得滤渣洗涤并灼烧至恒重,最终固体成份为 A .SiO 2B .Fe 2O 3、SiO 2C .SiO 2、Al 2O 3D .Fe 2O 3【答案】A【解析】SiO 2、Fe 2O 3、Al 2O 3,加入足量NaOH 溶液充分反应后,过滤,向所得溶液中含有硅酸钠、偏铝酸钠,加入过量盐酸,生成硅酸沉淀,将所得滤渣洗涤并灼烧生成二氧化硅,故A 正确。
高考化学无机化学常考题型:无机化学推断题精选【答案+解析】

高考高高高高高高高高高高高高高高高高高高精选一、单选题(本大题共20小题,共40分)1.甲乙丙丁戊是中学常见的无机物,他们的转化关系如图所示(某些条件和部分产物已略去).下列说法错误的是()A. 若戊为一种强碱且焰色反应为黄色,则反应①②可能都属于氧化还原反应B. 常温下,若丙为无色气体,戊为红棕色气体,则甲、乙是铜和稀硝酸C. 若甲为硫磺燃烧产物,丁为水,则戊可用于干燥甲D. 若甲为浓盐酸,乙为MnO2,则戊可能使品红褪色2.甲、乙、丙、丁均为中学化学中常见的单质或化合物,它们之间的转化关系如下图所示(部分产物已略去),如表各组物质中不能按图示关系转化的是()选项物质转化关系甲乙丙丁A NaOH NaHCO3Na2CO3CO2B C CO CO2O2C Fe Fe(NO3)3Fe(NO3)2HNO3D AlCl3NaAlO2Al(OH)3NaOHA. AB. BC. CD. D3.元素A、B、C、D分别位于三个不同短周期,且原子序数依次增大.只有D为金属元素,它们可形成x、y、z、w四种常见的二元化合物及p、q两种常见三元化合物,它们之间存在如下转化关系;,,其中z 为液体、w为气体,其余均为固体.下列有关说法正确的是()A. 原子半径大小顺序:D>C>B>AB. y、p 中均只含有离子键C. B、D两元素最高价氧化物对应水化物分别为强酸、强碱D. p能抑制水的电离而q能促进水的电离4.A、B、C、D、E五种物质均含有同一元素,且A为单质,有如图所示的转化关系.则下列判断不正确的是()A. 若ABCDE中同一元素的价态均不相同,则A为气态单质B. 若A 为金属钠,则由ImolD 完全反应生成C 时,一定有1mol 电子转移C. 若A 为非金属硫,则④的反应类型既可以是氧化还原反应又可以是复分解反应D. 若A 为金属铁,则化合物C 和D 均可以由化合反应生成5. A 、B 、C 、D 是中学化学常见物质,其中A 、B 、C均含有同一种元素.在一定条件下相互转化关系如图,下列判断正确的是( )A. 若D 为H 2O ,A 为碳,则A 和C 反应生成1 mol B 转移的电子数为N AB. 若D 为Fe ,A 为CI 2,则B 溶液蒸干后可得到纯净的B 固体C. 若D 为O 2,A 为碱性气体,则以上转化只涉及两个氧化还原反应D. 若D 为HCl ,A 为Na 2CO 3,则B 溶液中c(Na +)=c(HCO 3−)+2c(CO 32−+c(H 2CO 3)6. 在给定的条件下,下列选项所示的物质间转化均能实现的是( ) A.漂白粉 B.C. Al →NaOH 溶液NaAlO 2→过量盐酸Al(OH)3D. 饱和NaCl 溶液→NH 3,CO 2NaHCO 3→△Na 2CO 37. 工业上用铝土矿(主要成分为Al 2O 3,含SiO 2、Fe 2O 3等杂质)为原料冶炼铝的工艺流程如下,对下述流程中的判断正确的是( )A. 试剂X 为稀硫酸,沉淀中含有硅的化合物B. 反应II 中生成Al(OH)3的反应为:CO 2+AlO 2−+2H 2O =Al(OH)3↓+HCO 3−C. 结合质子(H +)的能力由弱到强的顺序是OH −>CO 32−>AlO 2−D. Al 2O 3熔点很高,工业上还可采用电解熔融AlCl 3冶炼Al。
高考化学无机推断题大汇总

高考化学无机推断题大汇总高考化学无机推断题大汇总高考化学中,无机推断题是一种常见的题型。
在这类题目中,考生需要根据所给的实验现象和化学知识进行推断和判断,从而确定物质的性质、反应方式或溶液中所含物质的种类。
下面是一些常见的无机推断题,供考生参考。
1. 实验室中有一个无色溶液,加入酸性钾高锰酸钾溶液后,溶液的颜色变为粉红色。
这时,我们可以推断原来溶液中是铁离子、铬离子还是锰离子?答案:由于酸性高锰酸钾溶液与铁离子和铬离子无反应,而与锰离子反应生成棕黑色固体,所以可以推断原来溶液中是铁离子。
2. 实验室中有一个无色气体X,能让红色石蕊试纸变蓝和黄色湿润性试纸变红,加入氢氧化钠溶液后溶液变浑浊,并生成一种白色固体Y。
这时,我们可以推断气体X是氯气、二氧化硫还是二氧化氮?答案:气体X能让红色石蕊试纸变蓝和黄色湿润性试纸变红,这表明它具有酸性。
而气体X与氢氧化钠反应生成白色固体Y,所以可以推断气体X是二氧化硫。
3. 实验室中有一个无色固体,热解后生成红色气体,与盐酸反应产生氯气。
这时,我们可以推断无色固体是碘化钠、碘化铅还是碘化汞?答案:无色固体热解后生成红色气体,说明它本身含有硫元素。
而与盐酸反应产生氯气,可以推断无色固体是碘化铅。
4. 实验室中有一个无色气体,不可燃,无味,能使湿润性试纸变红,能与二氧化锰反应生成紫红色物质。
这时,我们可以推断无色气体是氢气、氮气还是氧气?答案:无色气体能使湿润性试纸变红,表明它具有酸性。
而与二氧化锰反应生成紫红色物质,可以推断无色气体是氮气。
5. 实验室中有一种无色溶液,与氯气反应生成浑浊物。
这时,我们可以推断无色溶液是盐酸溶液、硫酸溶液还是硝酸溶液?答案:无色溶液与氯气反应生成浑浊物,这表明无色溶液中有一种物质具有还原性,所以可以推断无色溶液是硫酸溶液。
以上只是一些常见的高考化学无机推断题,希望对考生有所帮助。
在解答无机推断题时,需要考生熟练掌握化学常识和实验现象,构建正确的推理链条,准确推断出物质的性质和反应方式。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2014高考化学无机推断题集锦“无机框图推断题”题眼知识准备:物质颜色1.有色固体:白色:Fe(OH)2、CaCO3、BaSO4、AgCl、BaSO3、铵盐,白色或黄色腊状固体:白磷淡黄色或黄色:S 黄或浅黄、FeS2 黄、AgI 黄、Au 黄、Na2O2 浅黄、AgBr 浅黄、Ag3PO4浅黄等。
红色或红棕色:Cu 紫红、Cu2O 红、Fe2O3 红棕色、Fe(OH)3红褐色。
黑色:C、CuS、Cu2S 、FeS 、MnO2、FeO、Fe3O4(磁性物质)、CuO、PbS 、Ag2O棕黑紫黑色:I2 紫黑、KMnO4 紫黑。
2.有色溶液:Cu2+蓝、MnO4紫红、Fe2+ 浅绿、Fe3+ 棕黄、Fe(SCN)3 血红、NO2浅黄。
--氯水浅黄绿色、溴水橙黄色、碘水棕黄色、溴的有机溶液橙红—红棕、I2的有机溶液紫红3.气体小结1、有颜色的气体:F2(淡黄绿色),Cl2(黄绿色),NO2(棕色),溴蒸气(红棕色)、I2(紫色)、O3(淡蓝色)。
其余均为无色气体。
2、有刺激性的气体:HF,HCl,HBr,HI,NH3,SO2,NO2,F2,Cl2,溴蒸气。
有臭鸡蛋气味的气体:H2S3、易溶于水的气体:HF,HCl,HBr,HI,NH3,SO2和NO2。
能溶于水的气体:CO2,Cl2,H2S和溴蒸气。
4、易液化的气体:NH3,SO 2,Cl25、有毒的气体:F2,HF,Cl2,H2S,SO2,CO,NO,NO2和溴蒸气。
6、在空气中易形成白雾的气体:HF,HCl,HBr,HI7、常温下由于发生化学反应而不能共存的气体:H2S和SO2,H2S和Cl2,HI和Cl2,NH3和HCl,NO和O2,F2和H28、其水溶液呈酸性且能使紫色石蕊试液变红色的气体:HF,HCl,HBr,HI,H2S,SO2,CO2,NO2和溴蒸气。
可使紫色石蕊试液先变红后褪色的气体:Cl2。
可使紫色石蕊试纸变蓝且水溶液呈弱碱性的气体:NH39、有漂白作用的气体:Cl2(有水时)和SO2。
10、能使澄清石灰水变浑浊的气体:CO2,SO2,HF。
11、能使无水CuSO4变蓝的气体:水蒸气。
12、在空气中可燃的气体:H2,CH4,C2H2,C2H4,CO,H2S。
在空气中点燃后火焰呈淡蓝色的气体:H2S,CH4,CO,H2。
13、具有氧化性的气体:F2,Cl2,溴蒸气,NO2,O2。
具有还原性的气体:H2S,H2,CO,NH3,HI,HBr,HCl,NO。
SO2和N2通常既可显示氧化性又可显示还原性。
14、与水可发生反应的气体:Cl2,F2,NO2,溴蒸气,CO2,SO2,NH3。
其中Cl2,F2,NO2,溴蒸气和水的反应属于氧化还原反应。
15、在空气中易被氧化变色的气体:NO。
16、能使湿润的KI淀粉试纸变蓝的气体:Cl2,NO2,溴蒸气。
17、遇AgNO3溶液可产生沉淀的气体:H2S,Cl2,溴蒸气,HCl,HBr,HI,NH3。
其中NH3通入AgNO3溶液产生的沉淀当NH3过量时会溶解。
18、能使溴水和酸性KMnO4溶液褪色的气体:H2S,SO2,C2H2,C2H4。
19、由于化学性质稳定,通常可作为保护气的气体:N2和Ar。
20、制得的气体通常为混合气的是:NO2和N2O4。
4.物质的状态、气味硬度等:呈液态的金属单质:Hg 呈液态的非金属单质:Br2 呈液态的化合物:H2O 常温呈气态的单质:H2、O2、Cl2、N2、F2、稀有气体等。
地壳中元素的含量:O、Si、Al、Fe、硬度最大的单质:C(金刚石)形成化合物种类最多的元素:C方法二、根据特征反应现象推断知识准备:特征反应现象1.焰色反应:Na+(黄色)、K+(紫色)2.能使品红溶液褪色的气体可能是:加热恢复原颜色的是SO2,不恢复的是Cl2、NaClO、Ca(ClO)2等次氯酸盐、氯水、过氧化钠、过氧化氢、活性碳等3.白色沉淀[Fe(OH)2]空气红褐色[Fe(OH)3](由白色→灰绿→红褐色)4.能在空气中自燃:P45.在空气中变为红棕色:NO6.能使石灰水变浑浊:CO2、SO27.通CO2变浑浊:石灰水(过量变清)、Na2SiO3、饱和Na2CO3、浓苯酚钠、NaAlO28.气体燃烧呈苍白色:H2在Cl2中燃烧;在空气中点燃呈蓝色:CO、H2、CH49.遇酚酞显红色或湿润红色石蕊试纸变蓝的气体:NH3(碱性气体)10.使湿润的淀粉碘化钾试纸变蓝:Cl2、Br2、FeCl3、碘水等。
11.加苯酚显紫色或加SCN-显血红色或加碱产生红褐色沉淀,必有Fe3+12.遇BaCl2生成不溶于硝酸的白色沉淀,可能是:SO42、Ag+、SO32 ——13.遇HCl生成沉淀,可能是:Ag+、SiO32、AlO2、S2O32 ———14.遇H2SO4生成沉淀,可能是:Ba2+、Ca2+、S2O32、SiO32、AlO2 ———15.与H2S反应生成淡黄色沉淀的气体有Cl2、O2、SO2、NO216.电解时阳极产生的气体一般是:Cl2、O2,阴极产生的气体是:H217.两种气体通入水中有沉淀的是2H2S+SO2=3S+2H2O ;同一元素的气态氢化物和最高价氧化物对应的水化物生成盐的元素一定是氮(NH4NO3)18.两种溶液混合生成沉淀和气体,这两种溶液的溶质可能是①Ba(OH)2与(NH4)2SO4或(NH4)2CO3或(NH4)2SO3②强烈双水解③可溶性铁盐与可溶性碳酸盐或碳酸氢盐④Na2S2O3溶液与强酸H2O CO32HCO3CO2Al OH3H2OAl3与S2HS H2S Al OH3H2O Al OH3AlO219.能使溴水褪色的物质:H2S和SO2及它们相对应的盐、活泼金属、不饱和烃、醛、酚、碱20.两物质反应先沉淀后溶解的有:CO2与Ca(OH)2或Ba(OH)2、NaOH与铝盐、氨水与AgNO3、强酸与偏铝酸盐知识准备:依据特征结构1.正四面体型分子:CH4、SiH4、CCl4、SiCl4、P4等。
2.直线型分子:乙炔、二氧化碳、二硫化碳等。
3.平面型分子: 苯、乙烯等。
4.含有非极性共价键的离子化合物:过氧化钠(Na2O2)、二硫化亚铁(FeS2)、CaC2等。
5.含有10个电子的粒子:离子:O2 、F、Ne、Na+、Mg2+、Al3+、NH4+、H3O+、OH、NH2 分子:————CH4、NH3、H2O、HF6.电子总数为18的粒子:分子:Ar、F2、SiH4、PH3、H2S、HCl、H2O2、C2H6、CH3OH、CH3NH2、CH3F、NH2 OH、NH2—NH2 等;离子:K+、Ca2+、HS—、S2—、Cl—、O22—7.9个电子的粒子:—OH、—CH3、—NH2、F方法三、根据特殊反应条件推断知识准备:熟悉具有特殊反应条件的反应,多数是重要工业生产反应1、高温条件C+H2OCO2+2H2,3Fe+4H2OFe3O4+4H2,CaCO3CaO+CO2,高温高温SiO2+CaCO3CaSiO3+CO2,SiO2+2CSi+2CO↑,SiOCaSiO3,2+CaO 高温高温4FeS2+11O22FeNa2SiO3+CO2 2O3+8SO2,SiO2+Na2CO32、高温高压催化剂:N2+3H23、催化剂、加热:催化剂高温高压H2+CO,C+2H2O2NH3催化剂4NH3+5O24NO+6H2O 2SO2+O2△MnO 2H2O2 2H2O+O2↑ △催化剂加热2SO3 2KClO3MnO △2KCl+3O2↑4、放电:N2+O22NO 3O22O3方法四、根据特征转化关系推断知识准备:1、一般思路是找出特别的变化关系,用可能的几种情况试探,得出合理答案.2、掌握一些特别的连续变化关系(1)O2O22OA B C H D(酸或碱)OOHO222(气体)NO NO2HNO3 ①NH3222②H2S(气体)SO2SO3H2SO4 OOHO222CO CO2H2CO3 ③C(固体)OOHO222Na2O Na2O2NaOH ④Na(固体)OOHO(2)A与强酸或强碱的反应A为弱酸的铵盐:(NH4)2CO3或NH4HCO3;(NH4)2S或NH4HS;(NH4)2SO3、NH4HSO33、注意几个典型转化关系三角转化:4、置换反应:或H2O 1.金属盐金属盐活泼金属(Na、Mg、Fe)H H2(1)金属→金属(2)金属→非金属点燃2.铝热反应2MgO C2Mg CO22F22H2O4HF O2高温Si2CO(3)非金属→非金属2C SiO2高温CO H2C H2OCl(Br、I)HS S2HCl(HBr、HI)2222H2金属氧化物高温金属H2O(4)非金属→金属高温金属CO2C金属氧化物5、与碱反应产生气体Al、Si OH H2碱⑪单质2Al2NaOH2HO2NaAlO3H⑫铵盐:NH4NH3H2O 222Si2NaOH H2O Na2SiO32H26、与酸反应产生气体HCl H2浓H2SO4SO2金属HNO3NO2、NO⑪⑫浓HSO4单质SO2、CO22C浓HNO3NO2、CO2非金属浓HSO4SO22S浓HNO3SO2、NO2H CO32HCO3CO2H化合物S2HS H2S2H SOHSO SO23 37、既能酸反应,又能与碱反应Al、Al2O3、Al(OH)3、弱酸的酸式盐(NaHCO3、NaHSO3、NaHS等)、弱酸的氨盐[NH4HCO3、(NH4)2CO3、NH4HSO3、(NH4)2SO3、(NH4)2S、NH4HS等]、氨基酸等;8、与水反应产生气体2Na2O22H2O4NaOH O22Na2H2O2NaOH H2Mg3N23H2O3Mg OH22NH3(1)单质(2)化合物2F22H2O4HF O2Al2S36H2O2Al OH33H2S CaC2HO Ca OH CH222229、气体反应特征(1)苍白色:H2在Cl2中燃烧;(2)蓝色:CO在空气中燃烧;(3)淡蓝色:H2S、H2、CH4、CH3CH2OH、S等在空气中燃烧;(4)明亮的蓝紫色:S在纯氧中燃烧;(5)金属的焰色反应烟、雾(1)在空气中形成白雾的:HCl、HBr、HI、NH3等气体及浓盐酸、浓硝酸;(2)相遇形成白烟或固体的:NH3+HCl、NH3+HBr、NH3+HNO3、H2S+SO2、H2S+Cl2;(3)燃烧时出现白色烟雾的:(P+Cl2);(4)燃烧时出现棕黄色烟的:(CuCl2)。
10、受热分解产生2种或3种气体的反应:NH4HCO3[(NH4)2CO3]NH3CO2H2O2Cu(NO3)22CuO4NO2O2(1)铵盐NHHSO[(NH)SO](2)硝酸盐NH SO HO434233222Ag2NO2O22AgNO3 NH3H2S NH4HS[(NH4)2S](3)硝酸:4HNO3==2H2O+4NO2↑+O2↑(4)碱式碳酸铜:Cu2 (OH)2CO3== 2CuO + CO2↑ + H2O (5)碳酸氢盐:2NaHCO △2CO3+H2O+CO2;Ca(HCO3)2高温CaO+H2O+2CO2方法五、根据特殊工业生产推断知识准备:重要工业生产反应1、煅烧石灰石2、煅烧黄铁矿3、二氧化硫的催化氧化4、氨的催化氧化5、合成氨6、电解饱和食盐水7、工业制盐酸8、高炉炼铁9、工业制取漂粉精10、工业制水煤气11、硅酸盐工业方法六、根据特征数据推断知识准备:近两年计算型推断题成为高考热点之一,解这类题时要善于抓住物质转化时相对分子质量的变化(例CO→CO2,NO → NO2,SO2→SO3转化时分子中都增加1个氧原子,相对分子质量变化均为16 );放出气体的体积或生成沉淀的量;化合物中各元素的含量;气体的相对密度;相对分子质量;离子化合物中离子个数比;反应物之间的物质的量比;电子总数;质子总数等重要数据。
