药物制剂CTD申报资料(4、52类)模板
CTD格式申报资料目录、化学药品申报资料项目(附件二格式)(5篇范例)

CTD格式申报资料目录、化学药品申报资料项目(附件二格式)(5篇范例)第一篇:CTD格式申报资料目录、化学药品申报资料项目(附件二格式)附件:原料药CTD格式申报资料目录管理信息资料:审查意见表/受理通知书(进口申请);药品注册现场核查报告;药品注册现场检查报告;药品注册检验报告申请表;药品研制情况申报表;药品注册现场检查申请表综述资料(文件夹名)1.药品名称。
2.证明性文件。
3.立题目的与依据。
4.对主要研究结果的总结及评价。
5.药品说明书、起草说明及相关参考文献。
6.包装、标签设计样稿。
信息汇总表(文件夹名)信息汇总表资料药学资料(文件夹名)1.基本信息(3.2.S.1)生产信息(3.2.S.2)3.特性鉴定(3.2.S.3)4.原料药的质量控制(3.2.S.4)5.对照品(3.2.S.5)6.包装材料和容器(3.2.S.6)7.稳定性(3.2.S.7)药理毒理研究资料(文件夹名)16.药理毒理研究资料综述。
17.主要药效学试验资料及文献资料。
18.一般药理学的试验资料及文献资料。
19.急性毒性试验资料及文献资料。
20.长期毒性试验资料及文献资料。
21.过敏性(局部、全身和光敏毒性)、溶血性和局部(血管、皮肤、粘膜、肌肉等)刺激性等特殊安全性试验资料和文献资料。
22.复方制剂中多种成份药效、毒性、药代动力学相互影响的试验资料及文献资料。
23.致突变试验资料及文献资料。
24.生殖毒性试验资料及文献资料。
25.致癌试验资料及文献资料。
26.依赖性试验资料及文献资料。
27.非临床药代动力学试验资料及文献资料。
临床试验资料(文件夹名)案。
30.临床研究者手册。
31.知情同意书样稿、伦理委员会批准件。
32.临床试验报告。
二、制剂CTD格式申报资料电子提交目录管理信息资料:审查意见表/受理通知书(进口申请);药品注册现场核查报告;药品注册现场检查报告;药品注册检验报告申请表;药品研制情况申报表;药品注册现场检查申请表综述资料(文件夹名)1.药品名称。
药品研发与CTD格式申报资料

12
(三)存在的主要问题
1. 2. 3. 4. 5. 6. 研究的目标不明确 申报工艺的大生产可行性 杂质的控制 研究的系统性 自我评价与完善 申报资料质量差
CDE SFDA
13
1.研究的目标不明确
• 药品研发的目标 目标药品质量概况(QTPP):需考虑到如给药 途径,剂型,生物利用度,规格和稳定性等内 容;创新药研发的目标。 药品的关键质量属性(CQA):以使那些对药 品质量有影响的药品特性能得以研究和控制; 国内仿制药研发的不足之处。实例 确定原料药、辅料等的关键质量属性,并选择 要达到药品预期质量所用的辅料类型和用量;
32
起草过程与特点
• 2009年开始启动 • 周密安排、全员参与 制定了详细的工作计划(中心与各小组 层面),全体化药药学人员参与讨论 • 广泛征求意见 多种形式多方征求意见 • 2010年9月正式发布 国食药监注 〔2010〕 387 号
CDE SFDA
33
国家局对有关事项的通知
一、化药注册分类3、4、5和6的生产注册申请的 药学部分申报资料,可参照CTD格式提交,同 时提交电子版。 二、化药注册分类1和2的药学资料,暂不按CTD 格式提交资料。 三、为鼓励CTD格式提交,并稳步推进: (一)按《药品注册管理办法》附件2申报资料 要求提交的生产注册申请申报资料仍予接收。 (二)技术审评部门将对提交CTD格式申报资 料的注册申请单独按序进行审评。
CDE SFDA
30
(3)ICH的CTD格式申报资料要求
• 目的 统一三方申报资料的格式要求,避免重复劳动 • 资料结构 第一部分:各国的特殊要求(证明材料等) 第二部分:各专业的综述 第三部分:具体的研究资料与图片等 • 特点 条理清晰、资料编码科学、方便审评与国际间的 交流
ctd格式申报资料模板

(3)ICH的CTD格式申报资料要求
• 目的 统一三方申报资料的格式要求,避免重复劳动 • 资料结构 第一部分:各国的特殊要求(证明材料等) 第二部分:各专业的综述 第三部分:具体的研究资料与图片等 • 特点 条理清晰、资料编码科学、方便审评与国际间的 交流
2.国内起草背景
• 国内存在的问题 对申报资料的要求不够细化 企业水平参差不齐 申报资料的质量总体较差 审评人员的工作量大,且包括很多不必要的 打字工作。 审评报告的重点信息缺失 • 解决的思路 照国外,规范申报资料,提倡电子提交, 审评报告与综述资料有机结合。
质控:分析方法的验证与对照品的标定
稳定性:样品情况、结果的表述
综述中关键点(2)
• 制剂 处方工艺:研发过程、变化情况及批次 汇总表(代表性批次 ) 质量控制 :放行标准、有关物质方法学 验证应针对已知杂质、列明产品中可能 含有的杂质、对照品的标定 稳定性:上市后的承诺和方案、使用中 产品稳定性、相容性试验
三、总结
• 满足临床治疗与患者需求是药品研发立题 的主要依据。 • 质量源于设计:药品研发的质量决定了药 品的质量。 • 申报资料是注册时证明药品安全有效、质 量可控的重要依据。 • CTD格式的申报资料充分体现了药品研发 的系统性,对指导研发、注册申报,提高 审评的质量与效率均有重要意义。
国内外质量标准杂质检查项对比
起草过程与特点
• 2009年开始启动 • 周密安排、全员参与 制定了详细的工作计划(中心与各小组 层面),全体化药药学人员参与讨论 • 广泛征求意见 多种形式多方征求意见 • 2010年9月正式发布 国食药监注 〔2010〕 387 号
国家局对有关事项的通知
一、化药注册分类3、4、5和6的生产注册申请的 药学部分申报资料,可参照CTD格式提交,同 时提交电子版。 二、化药注册分类1和2的药学资料,暂不按CTD 格式提交资料。 三、为鼓励CTD格式提交,并稳步推进: (一)按《药品注册管理办法》附件2申报资料 要求提交的生产注册申请申报资料仍予接收。 (二)技术审评部门将对提交CTD格式申报资 料的注册申请单独按序进行审评。
第二部分:注册分类4、5.2类申报资料要求试行

第二部分注册分类4、5.2类申报资料要求(试行)目录一、申报资料项目 (4)二、申报资料项目说明 (5)(一)概要部分 (5)1.药品名称 (5)2.证明性文件 (5)2.1注册分类4类证明性文件 (5)2.2注册分类5.2类证明性文件 (6)3.立题目的与依据 (7)4.自评估报告 (7)5.上市许可人信息 (7)5.1资质证明性文件 (7)5.2药品质量安全责任承担能力相关文件 (7)6.原研药品信息 (8)7.药品说明书、起草说明及相关参考文献。
(8)8.包装、标签设计样稿。
(8)(二)原料药部分 (8)9.(2.3.S)药学研究信息汇总表 (8)10.(3.2.S)原料药药学申报资料 (9)10.1.(3.2.S.1)基本信息 (9)10.2.(3.2.S.2)生产信息 (9)10.3.(3.2.S.3.)特性鉴定 (12)10.4.(3.2.S.4)原料药的质量控制 (13)10.5.(3.2.S.5)对照品 (16)10.6.(3.2.S.6)包装材料和容器 (16)10.7.(3.2.S.7)稳定性 (17)(三)制剂部分 (20)11.(2.3.P)制剂药学研究信息汇总表 (20)12.(3.2.P)制剂药学申报资料 (20)12.1.(3.2.P.1)剂型及产品组成 (20)12.2.(3.2.P.2)产品开发 (20)12.3.(3.2.P.3)生产信息 (23)12.5.(3.2.P.5)制剂的质量控制 (25)12.6.(3.2.P.6)对照品 (29)12.7.(3.2.P.7)稳定性 (29)13.(2.4.P.)非临床研究信息汇总表 (32)14. 制剂非临床研究申报资料 (32)15. (2.5.P.)制剂临床试验信息汇总表 (32)16. 临床试验资料 (33)一、申报资料项目(一)概要1.药品名称。
2.证明性文件。
2.1注册分类4类证明性文件2.2注册分类5.2类证明性文件3.立题目的与依据。
CTD格式申报资料范本

药品注册分类:化学药品六类注册申请分类:仿制药品注册申请药品名称:苯磺酸氨氯地平片(XX g、XX g)资料项目名称:药学研究CTD格式申报资料研究机构名称:XXX制药有限公司研究机构地址:XXXXXXXXX研究机构主要研究者:XXX研究机构电话:XXX注册申请联系人姓名:XXX原始资料的保存地点:XXX制药有限公司注册申请机构联系电话:XXXXXXXXX药品注册申请人:XXX制药有限公司苯磺酸氨氯地平片申报资料(药学部分)目录3.2.P.1 剂型及产品组成 (3)3.2.P.2 产品开发 (4)3.2.P.2.1 处方组成 (4)3.2.P.2.1.1 原料药 (4)3.2.P.2.1.2 辅料 (5)3.2.P.2.2 制剂研究 (5)3.2.P.2.2.1 处方开发过程 (5)3.2.P.2.3 生产工艺的开发 (20)3.2.P.2.4 包装材料/容器 (23)2.3.P.2.5 相容性 (23)3.2.P.3 生产 (23)3.2.P.3.1生产商 (23)3.2.P.3.2批处方 (23)3.2.P.3.3 生产工艺和工艺控制 (24)3.2.P.3.4 关键步骤和中间体的控制 (25)3.2.P.3.5 工艺验证和评价 (26)3.2.P.4 原辅料的控制 (31)3.2.P.5 制剂的质量控制 (31)3.2.P.5.1质量标准 (31)3.2.P.5.2 分析方法 (31)3.2.P.5.3 分析方法的验证 (34)3.2.P.5.4 批检验报告 (93)3.2.P.5.5 杂质分析 (97)3.2.P.6 对照品 (100)3.2.P.7 稳定性 (101)3.2.P.7.1稳定性总结 (101)3.2.P.7.2上市后的稳定性承诺和稳定性方案 (102)3.2.P.7.3 稳定性数据 (102)申报资料正文3.2.P.1 剂型及产品组成苯磺酸氨氯地平片是一种独特的具有高度血管选择性的长效二氢吡啶类钙离子拮抗剂,是心血管治疗药物中比较理想的长效降压药,也是近几年来世界处方量最大的高血压和心绞痛治疗药物。
CTD格式申报资料撰写格式(制剂)带实例

CTD格式申报资料撰写格式(制剂)3.2.P.1 剂型及产品组成3.2.P.2 产品开发3.2.P.2.1 处方组成3.2.P.2.1.1 原料药3.2.P.2.1.2 辅料3.2.P.2.2 制剂3.2.P.2.2.1 处方开发过程3.2.P.2.2.2 制剂相关特性3.2.P.2.3 生产工艺的开发3.2.P.2.4 包装材料/容器3.2.P.2.5 相容性3.2.P.3 生产3.2.P.3.1 生产商3.2.P.3.2 批处方3.2.P.3.3 生产工艺和工艺控制3.2.P.3.4 关键步骤和中间体的控制3.2.P.3.5 工艺验证和评价3.2.P.4 原辅料的控制3.2.P.5 制剂的质量控制3.2.P.5.1 质量标准3.2.P.5.2 分析方法3.2.P.5.3 分析方法的验证3.2.P.5.4 批检验报告3.2.P.5.5 杂质分析3.2.P.5.6 质量标准制定依据3.2.P.6 对照品3.2.P.7 稳定性3.2.P.7.1 稳定性总结3.2.P.7.2 上市后的稳定性研究方案及承诺3.2.P.7.3 稳定性数据二、申报资料正文及撰写要求3.2.P.1 剂型及产品组成(1)说明具体的剂型,并以表格的方式列出单位剂量产品的处方组成,列明各成分在处方中的作用,执行的标准。
如有过量加入的情况需给予说明。
对于处方中用到但最终需去除的溶剂也应列出。
(2)如附带专用溶剂,参照以上表格方式列出专用溶剂的处方。
(3)说明产品所使用的包装材料及容器。
Eg:3.2.P.2 产品开发提供相关的研究资料或文献资料来论证剂型、处方组成、生产工艺、包装材料选择和确定的合理性,具体为:3.2.P.2.1 处方组成3.2.P.2.1.1 原料药参照《化学药物制剂研究的技术指导原则》,提供资料说明原料药和辅料的相容性,分析与制剂生产及制剂性能相关的原料药的关键理化特性(如晶型、溶解性、粒度分布、吸湿性等)。
Eg:格列苯脲的粒度研究3.2.P.2.1.2 辅料说明辅料种类和用量选择的依据,分析辅料用量是否在常规用量范围内,是否适合所用的给药途径,(符合药用要求,注射剂辅料应符合注射液要求;不予主药发生不良相互作用;根据剂型选择必要的辅料)并结合辅料在处方中的作用分析辅料的哪些性质会影响制剂特性。
药物制剂CTD申报资料(4、52类)模板
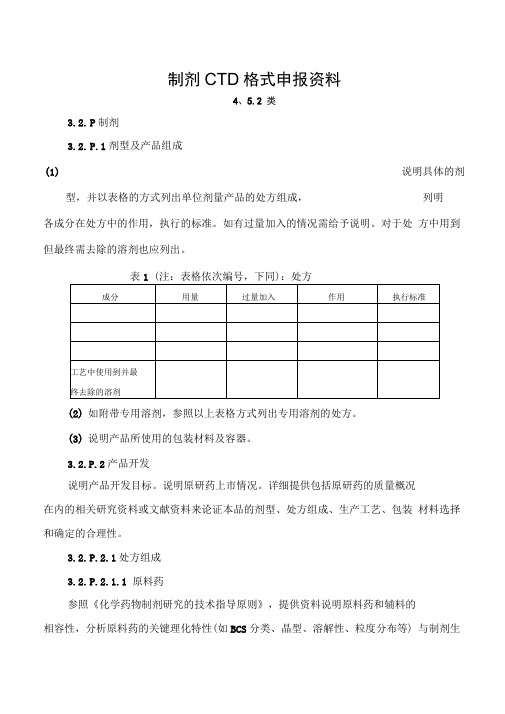
制剂CTD格式申报资料4、5.2 类3.2.P制剂3.2.P.1剂型及产品组成(1)说明具体的剂型,并以表格的方式列出单位剂量产品的处方组成,列明各成分在处方中的作用,执行的标准。
如有过量加入的情况需给予说明。
对于处方中用到但最终需去除的溶剂也应列出。
表1 (注:表格依次编号,下同):处方(2)如附带专用溶剂,参照以上表格方式列出专用溶剂的处方。
(3)说明产品所使用的包装材料及容器。
3.2.P.2产品开发说明产品开发目标。
说明原研药上市情况。
详细提供包括原研药的质量概况在内的相关研究资料或文献资料来论证本品的剂型、处方组成、生产工艺、包装材料选择和确定的合理性。
3.2.P.2.1处方组成3.2.P.2.1.1 原料药参照《化学药物制剂研究的技术指导原则》,提供资料说明原料药和辅料的相容性,分析原料药的关键理化特性(如BCS分类、晶型、溶解性、粒度分布等) 与制剂生产及制剂性能的相关性,并提供相关的研究资料与文献。
3.2.P.2.1.2 辅料说明辅料是否适合所用的给药途径结合辅料在处方中的作用分析辅料的哪些性质会影响制剂特性,提供相关的研究资料与文献。
3.2.P.2.2 制剂研究3.2.P.2.2.1处方开发过程参照《化学药物制剂研究的技术指导原则》,提供处方的研究开发过程和确定依据,包括文献信息(如对照药品的处方信息)、研究信息(包括处方设计,处方筛选和优化、处方确定等研究内容)、辅料种类和用量选择的依据、分析辅料用量是否在常规用量范围内,以及自制样品与原研药的质量特性对比研究结果(需说明原研药的来源、批次和有效期,自研样品批次,对比项目、采用方法),并重点说明在药品开发阶段中处方组成的主要变更、原因以及支持变化的验证研究。
如生产中存在过量投料的问题,应提供过量投料的必要性和合理性的相关研究资料。
3.2.P.2.2.2制剂相关特性对与制剂性能相关的理化性质,如pH、离子强度、溶出度、再分散性、复溶、粒径分布、聚合、多晶型、流变学等进行分析。
CTD申报资料模版

CTD申报资料模版1. 介绍本文档提供了CTD申报资料的模版,帮助申请人编写CTD 申报资料。
CTD,即Common Technical Document,是国际上通用的药品注册申报文档格式。
CTD申报资料是药品注册申请的核心文档,用于向药品监管机构提交药品的安全性、有效性和质量等相关信息。
2. CTD申报资料的结构与内容CTD申报资料包含5个模块,分别是:质量部分(Quality)、非临床部分(Nonclinical)、临床部分(Clinical)、申请人概述部分(Applicant’s Overview)和审核员概述部分(Module 5)。
2.1 质量部分质量部分包括了药品的质量控制和生产工艺方面的信息,主要内容包括:•药品的质量规范(Specifications)•药品的制造工艺(Manufacturing Process)•药品的成分(Composition)•药品的稳定性研究(Stability Studies)•药品的包装和标签(Packaging and labeling)2.2 非临床部分非临床部分包含了药物的非临床研究数据,主要内容包括:•药物的药理学和毒理学研究(Pharmacology and Toxicology Studies)•药物代谢与药物动力学研究(Metabolism and Pharmacokinetics Studies)2.3 临床部分临床部分包含了药物的临床试验数据,主要内容包括:•临床试验设计(Clinical Trial Design)•临床试验结果(Clinical Trial Results)•药物在人群中的疗效(Efficacy)•药物的安全性(Safety)2.4 申请人概述部分申请人概述部分是申请人对药物的总结和解释,主要内容包括:•药物的概述和用途(Overview and Uses of the Drug)•为什么该药物是安全和有效的(Why the Drug is Safe and Effective)•药物的剂量和给药途径(Dosage andAdministration)•药物的不良反应(Adverse Reactions)2.5 审核员概述部分审核员概述部分是药品审评机构对申请资料的总结和评价,主要内容包括:•药物的总结和评价(Summary and Assessment of the Drug)•对申请人的要求和建议(Recommendations for the Applicant)•对药物的批准或拒绝的意见(Opinion on Approval or Rejection of the Drug)3. 编写CTD申报资料的注意事项在编写CTD申报资料时,需要注意以下几点:•按照CTD的结构和内容编写,确保包含了所有必要的信息。
药物制剂CTD申报资料(4、52类)模板

制剂CTD格式申报资料4、5.2类3.2.P 制剂3.2.P.1 剂型及产品组成(1)说明具体的剂型,并以表格的方式列出单位剂量产品的处方组成,列明各成分在处方中的作用,执行的标准。
如有过量加入的情况需给予说明。
对于处方中用到但最终需去除的溶剂也应列出。
表1(注:表格依次编号,下同):处方(2)如附带专用溶剂,参照以上表格方式列出专用溶剂的处方。
(3)说明产品所使用的包装材料及容器。
3.2.P.2 产品开发说明产品开发目标。
说明原研药上市情况。
详细提供包括原研药的质量概况在内的相关研究资料或文献资料来论证本品的剂型、处方组成、生产工艺、包装材料选择和确定的合理性。
3.2.P.2.1处方组成3.2.P.2.1.1原料药参照《化学药物制剂研究的技术指导原则》,提供资料说明原料药和辅料的相容性,分析原料药的关键理化特性(如BCS分类、晶型、溶解性、粒度分布等)与制剂生产及制剂性能的相关性,并提供相关的研究资料与文献。
3.2.P.2.1.2辅料说明辅料是否适合所用的给药途径结合辅料在处方中的作用分析辅料的哪些性质会影响制剂特性,提供相关的研究资料与文献。
3.2.P.2.2 制剂研究3.2.P.2.2.1处方开发过程参照《化学药物制剂研究的技术指导原则》,提供处方的研究开发过程和确定依据,包括文献信息(如对照药品的处方信息)、研究信息(包括处方设计,处方筛选和优化、处方确定等研究内容)、辅料种类和用量选择的依据、分析辅料用量是否在常规用量范围内,以及自制样品与原研药的质量特性对比研究结果(需说明原研药的来源、批次和有效期,自研样品批次,对比项目、采用方法),并重点说明在药品开发阶段中处方组成的主要变更、原因以及支持变化的验证研究。
如生产中存在过量投料的问题,应提供过量投料的必要性和合理性的相关研究资料。
3.2.P.2.2.2制剂相关特性对与制剂性能相关的理化性质,如pH、离子强度、溶出度、再分散性、复溶、粒径分布、聚合、多晶型、流变学等进行分析。
CTD格式-药品研发与CTD格式申报资料

11
研究中正确使用
• 熟悉掌握指导原则的基本要求,如手性药物药 学研究指导原则重点在构型与立体异构体。
• 结合原则中的具体方法进一步加深了解 • 根据情况指导具体的研发工作 • 决不能拘泥于已有的方法。僵化地使用指导原
则做不好药品研发,尤其是创新药的研发。
CDE SFDA
12
(三)存在的主要问题
Impurity)和总杂质的规定。 • 特定杂质的限度应根据自主研究或质量
对比研究的结果确定。 • 非特定杂质的限度应符合杂质研究指导
原则中鉴定限度的要求。
CDE SFDA
20
4.研究的系统性
• 研究缺乏系统性
加强学科间的沟通与协调。如杂质限度的确 定应综合药学、毒理与临床研究的结果。
工艺研究
杂质分析
限度
稳定性
毒理
临床
CDE SFDA
21
5.自我评价与完善
• 缺乏自我评价意识、不能及时纠偏与完 善研究工作
• 应设立关键控制点,强化研发过程中的 自我评价
• 自我评价不能一厢情愿,应客观:从治 疗需求、患者与评价者的角度进行
CDE SFDA
22
6.申报资料质量差
• 主观不重视、甚至有意瞒报,客观上水平不够, 缺乏系统性、重点不突出。
1. 研究的目标不明确 2. 申报工艺的大生产可行性 3. 杂质的控制 4. 研究的系统性 5. 自我评价与完善 6. 申报资料质量差
CDE SFDA
13
1.研究的目标不明确
• 药品研发的目标
✓ 目标药品质量概况(QTPP):需考虑到如给药
途径,剂型,生物利用度,规格和稳定性等内 容;创新药研发的目标。
ctd申报资料格式

ctd申报资料格式篇一:CTD格式申报资料范本药品注册分类:化学药品六类注册申请分类:仿制药品注册申请药品名称:苯磺酸氨氯地平片(XXg、XXg)资料项目名称:药学研究CTD格式申报资料研究机构名称:XXX制药有限公司研究机构地址:XXXXXXXXX 研究机构主要研究者:XXX 研究机构电话:XXX 注册申请联系人姓名:XXX原始资料的保存地点:XXX制药有限公司注册申请机构联系电话:XXXXXXXXX药品注册申请人:XXX制药有限公司苯磺酸氨氯地平片申报资料(药学部分)目录3.2.P.1 剂型及产品组成 ................................................3 3.2.P.2 产品开发 ................................................ (4)3.2.P.2.1 处方组成 ................................................43.2.P.2.1.1 原料药 (4)3.2.P.2.1.2 辅料 (5)3.2.P.2.2 制剂研究 (5)3.2.P.2.2.1 处方开发过程 (5)3.2.P.2.3 生产工艺的开发 (20)3.2.P.2.4 包装材料/容器 (23)2.3.P.2.5 相容性 .................................................23 3.2.P.3 生产 ................................................ (23)3.2.P.3.1生产商 ................................................ .. 23 3.2.P.3.2批处方 .................................................. 23 3.2.P.3.3 生产工艺和工艺控制 (24)3.2.P.3.4 关键步骤和中间体的控制 ................................. 25 3.2.P.3.5 工艺验证和评价.. (26)3.2.P.4 原辅料的控制 ................................................31 3.2.P.5 制剂的质量控制...............................................31 3.2.P.5.1质量标准 ................................................ (31)3.2.P.5.2 分析方法...............................................31 3.2.P.5.3 分析方法的验证 (34)3.2.P.5.4 批检验报告 (93)3.2.P.5.5 杂质分析...............................................97 3.2.P.6 对照品 ................................................ ...... 100 3.2.P.7 稳定性 ................................................ (101)3.2.P.7.1稳定性总结 (101)3.2.P.7.2上市后的稳定性承诺和稳定性方案 ......................... 102 3.2.P.7.3 稳定性数据 .. (102)申报资料正文3.2.P.1 剂型及产品组成苯磺酸氨氯地平片是一种独特的具有高度血管选择性的长效二氢吡啶类钙离子拮抗剂,是心血管治疗药物中比较理想的长效降压药,也是近几年来世界处方量最大的高血压和心绞痛治疗药物。
ctd格式申报资料模板

05
CTD格式申报资料模板的未 来发展与展望
国际发展趋势
统一化
随着国际药品监管机构之间的合作日益紧密,CTD格式申报资料模板将逐渐实现统一化,减少不同国家或地区的差异 ,提高资料的可比性和可操作性。
电子化
随着信息技术的发展,电子化的CTD格式申报资料模板将逐渐成为主流,通过电子化方式提交资料可以更加方便快捷 ,同时也有利于资料的保存和检索。
模块化
CTD格式将申报资料划分为多个 模块,每个模块包含特定的技术 内容,方便申报资料的整理和审 查。
CTD格式的重要性
促进国际药品注册合作
采用CTD格式可以方便不同国家和地区之间 药品注册信息的交流和合作,加速药品在全 球范围内的上市进程。
提高审查效率
CTD格式规范了申报资料的内容和技术要求,有助 于审查机构快速、准确地评估申请资料的技术合规 性。
目的
通过采用CTD格式,确保药品注册申请的技术资料具有一致性和规范性,提高 药品注册审批的效率和可靠性。
CTD格式的特点
标准化
CTD格式采用统一的章节结构和 内容要求,确保技术资料的规范 性和一致性。
灵活性
CTD格式允许申报资料按照不同 国家和地区的注册要求进行个性 化展示,以满足不同监管机构的 要求。
未来发展方向与建议
完善法规体系
建立健全CTD格式申报资料模板的相关法 规和标准,明确资料的要求和规范,为资
料模板的制定和应用提供有力保障。
推进信息化建设
加强信息化建设,提高CTD格式申报资料 模板的电子化和智能化水平,提升资料的
管理和利用效率。
加强培训与指导
加强对企业和申报人员的培训和指导,提 高他们对CTD格式申报资料模板的认识和 应用能力,促进资料的规范化和标准化。
CTD申报资料模版

CTD申报资料模版1. 引言本文档旨在为CTD(药物临床试验数据)申报提供一个标准化的资料模板,以便帮助申请人整理和准备相关文件。
本模板按照国家药监局的要求进行编写,并参考了相关指南和标准。
2. 资料清单下面是CTD申报资料的清单:1.申请表2.药物研究概况3.临床研究计划4.药物化学和药学附件5.其他相关附件3. 申请表在申请表中,需要填写以下信息:•申请人信息:包括申请人姓名、单位、联系方式等。
•药物信息:包括药物名称、剂型、规格、批号等。
•申报内容:包括申报的研究阶段、测试目标、研究计划等。
•相关声明:包括研究过程中的伦理和合规问题的声明。
4. 药物研究概况药物研究概况需要提供以下信息:•药物研究的背景和目的•相关研究基础和先行研究•临床试验方案的设计和方法•参与者招募和纳入标准•数据收集和统计分析方法•预期研究结果5. 临床研究计划临床研究计划需要提供以下信息:•研究设计与方法:包括研究类型、研究中心、样本大小、随机化方案等。
•研究过程的伦理和合规问题:包括伦理委员会审查、知情同意和机密保护等问题。
•数据收集和管理:包括数据收集时间点、数据管理计划等。
•统计分析计划:包括主要的统计分析方法和假设检验等。
6. 药物化学和药学附件药物化学和药学附件需要提供以下信息:•药物的化学结构和化学性质•药物的制备方法和工艺•药物的质量标准和分析方法(如鉴别、含量测定等)•药物的稳定性研究和储存条件7. 其他相关附件除了上述资料,申请人还需要提供其他相关附件,如:•急救方案和不良事件报告•临床试验结果和分析报告•相关专家和机构的鉴定或推荐信•其他与申报相关的文件8. 结论本文档提供了一个CTD申报资料的模版,帮助申请人整理和准备相关文件。
申请人应根据具体情况进行调整和补充,以确保申报资料的完整和准确。
努力准备好CTD申报资料,将有助于快速获得批准,并推动药物研究的进展。
注意:本文所提供的模版仅供参考,申请人需要根据实际需求和相关法规进行适当的调整和修改。
CTD格式申报资料

申报资料的关键点(1)
• 原料药 制备工艺:物料与中间体质控方法的必 要验证、关键起始原料的制备工艺、工 艺验证的分类要求 结构确证:杂质的结构确证与溯源 包材:检验报告、选择依据、相容性研 究
申报资料的关键点(2)
• 制剂 处方工艺研究:与对照药品对比研究结 果(包括f2相似因子的比较 )、批分析 汇总表、包材的相容性研究 生产工艺:详略要求、主要设备的技术 参数、大生产规模的要求(10倍以内)、 工艺验证的要求与内容 稳定性:中试以上规模的样品、使用中 的稳定性、上市后的稳定性承诺与方案
质控:分析方法的验证与对照品的标定
稳定性:样品情况、结果的表述
综述中关键点(2)
• 制剂 处方工艺:研发过程、变化情况及批次 汇总表(代表性批次 ) 质量控制 :放行标准、有关物质方法学 验证应针对已知杂质、列明产品中可能 含有的杂质、对照品的标定 稳定性:上市后的承诺和方案、使用中 产品稳定性、相容性试验
(二)重点解读
1.资料结构与特点 2.关键点
1.资料结构与特点
• 资料结构 主要研究信息汇总表(原料药、制剂) 相当于CTD第二部分的综述资料 申报资料撰写要求(原料药、制剂) 相当于CTD第三部分的研究资料 • 特点 与国外CTD基本一致(编码与资料) 综述与申报资料相互映证(包括编码)、互为 补充 适合电子提交,与审评报告结合能够方便审评, 提高效率、保证质量
三、总结
• 满足临床治疗与患者需求是药品研发立题 的主要依据。 • 质量源于设计:药品研发的质量决定了药 品的质量。 • 申报资料是注册时证明药品安全有效、质 量可控的重要依据。 • CTD格式的申报资料充分体现了药品研发 的系统性,对指导研发、注册申报,提高 审评的质量与效率均有重要意义。
CTD申报资料模版

*********C T D格式申报资料一、目录剂型及产品组成产品开发处方组成原料药辅料制剂研究处方开发过程制剂相关特性生产工艺的开发包装材料/容器相容性生产生产商批处方生产工艺和工艺控制关键步骤和中间体的控制工艺验证和评价原辅料的控制制剂的质量控制质量标准分析方法分析方法的验证批检验报告杂质分析质量标准制定依据对照品稳定性 稳定性总结上市后的稳定性研究方案及承诺 稳定性数据二、申报资料正文剂型及产品组成(1)本品为淡黄色或类白色片,规格为50mg ,单位剂量产品的处方组成,各(2)本品无专用溶剂。
(3)本品采用PVC 铝塑包装,外加聚酯/铝/聚乙烯复合膜袋。
产品开发*********是德国拜耳开发上市的首个口服苷酶抑制剂,1990年首先在德国上市。
于1998年进入我国,商品名为“*********”。
我公司以“*********”为对照药品,研制了*********片,规格为50mg ,按照国家药品注册分类,属于化学药第6类已有国家标准品种。
处方组成 原料药*********化学名称为: 化学结构式为: 分子式: 分子量:*********为白色或类白色无定形粉末,在水中极易溶,在甲醇中溶解,在乙醇中极成 分 用量 百分重量作用 执行标准 微晶纤维素淀粉6026适量填充剂 填充剂 黏合剂中国药典2010年版 中国药典2010年版 中国药典2010年版********* 二氧化硅50活性成分 助流剂中国药典2010年版 中国药典2010年版微溶解,在乙腈和丙酮中不溶。
本品应密封、避光、在阴凉处保存。
辅料“*********”处方中所用的辅料为:微晶纤维素、淀粉、硬脂酸镁、二氧化硅。
本品处方参照“*********”,除加入粘合剂羟丙甲基纤维素外,其他辅料均与上市对照药“*********”一致,辅料相容性试验结果显示羟丙甲基纤维素对活性成分无明显影响。
制剂研究处方开发过程为尽量保证研制品与上市药品安全、有效性一致,我们对上市样品进行了全面的考察及评价,并全面考察原料的性质。
CTD申报模版

*********C T D格式申报资料一、目录剂型及产品组成产品开发处方组成原料药辅料制剂研究处方开发过程制剂相关特性生产工艺的开发包装材料/容器相容性生产生产商批处方生产工艺和工艺控制关键步骤和中间体的控制工艺验证和评价原辅料的控制制剂的质量控制质量标准分析方法分析方法的验证批检验报告杂质分析质量标准制定依据对照品稳定性稳定性总结上市后的稳定性研究方案及承诺 稳定性数据二、申报资料正文剂型及产品组成(1)本品为淡黄色或类白色片,规格为50mg ,单位剂量产品的处方组成,各 (2)本品无专用溶剂。
(3)本品采用PVC 铝塑包装,外加聚酯/铝/聚乙烯复合膜袋。
产品开发*********是德国拜耳开发上市的首个口服苷酶抑制剂,1990年首先在德国上市。
于1998年进入我国,商品名为“*********”。
我公司以“*********”为对照药品,研制了*********片,规格为50mg ,按照国家药品注册分类,属于化学药第6类已有国家标准品种。
处方组成 原料药*********化学名称为: 化学结构式为: 分子式: 分子量:*********为白色或类白色无定形粉末,在水中极易溶,在甲醇中溶解,在乙醇中极微溶解,在乙腈和丙酮中不溶。
本品应密封、避光、在阴凉处保存。
辅料“*********”处方中所用的辅料为:微晶纤维素、淀粉、硬脂酸镁、二氧化硅。
本品处方参照“*********”,除加入粘合剂羟丙甲基纤维素外,其他辅料均与上市对照药成 分 用量 百分重量 作用 执行标准 微晶纤维素 淀粉 60 26 适量 69.40 30.08 0.52填充剂 填充剂 黏合剂中国药典2010年版 中国药典2010年版 中国药典2010年版********* 二氧化硅50 2.535.71 1.79活性成分 助流剂中国药典2010年版 中国药典2010年版“*********”一致,辅料相容性试验结果显示羟丙甲基纤维素对活性成分无明显影响。
药品研发--CTD格式申报资料

Manufecturer
Impurities detected by HPLC
Retention Time 2.8min 6.0min 9.2min 11.2min Sum
Roche(Switzerl <0.1% and)
<0.1%
Standard Organics(India)
<0.1% <0.1% <0.2%
• 国内申报情况(均不含补充资料)
仿制药 新药 进口药 全 部
2003 2887
5428
996
9324
2004 6664
6440
971
14115
2005 9723
6403
718
19368
2006 7050 14636
4264
588
国家药品审评中心
美国FDA仿制药概况
历年申报数量: 1999 2000 2001 2002 2003 2004 2005 296 365 320 392 479 635 777
国家药品审评中心
综述中关键点(1)
• 原料药 ➢制备工艺:研发过程、工艺变化情况
及批次汇总表 ➢结构确证:杂质的定性研究与溯源 ➢质控:分析方法的验证与对照品的标
定 ➢稳定性:样品情况、结果的表述
国家药品审评中心
综述中关键点(2)
• 制剂 ➢处方工艺:研发过程、变化情况及批
次汇总表(代表性批次 ) ➢质量控制 :放行标准、有关物质方法
Dong Wha(Korea)Biblioteka <0.17% 0.17%
China 1 <0.1% 0.95%
0.95%
China 2
0.95%
CTD格式申报资料撰写格式(制剂)带实例

CTD格式申报资料撰写格式(制剂)带实例CTD格式申报资料撰写格式(制剂)3.2.P.1 剂型及产品组成3.2.P.2 产品开发3.2.P.2.1 处方组成3.2.P.2.1.1 原料药3.2.P.2.1.2 辅料3.2.P.2.2 制剂3.2.P.2.2.1 处方开发过程3.2.P.2.2.2 制剂相关特性3.2.P.2.3 生产工艺的开发3.2.P.2.4 包装材料/容器3.2.P.2.5 相容性3.2.P.3 生产3.2.P.3.1 生产商3.2.P.3.2 批处方3.2.P.3.3 生产工艺和工艺控制3.2.P.3.4 关键步骤和中间体的控制3.2.P.3.5 工艺验证和评价3.2.P.4 原辅料的控制3.2.P.5 制剂的质量控制3.2.P.5.1 质量标准3.2.P.5.2 分析方法3.2.P.5.3 分析方法的验证3.2.P.5.4 批检验报告3.2.P.5.5 杂质分析3.2.P.5.6 质量标准制定依据3.2.P.6 对照品3.2.P.7 稳定性3.2.P.7.1 稳定性总结3.2.P.7.2 上市后的稳定性研究方案及承诺3.2.P.7.3 稳定性数据二、申报资料正文及撰写要求3.2.P.1 剂型及产品组成(1)说明具体的剂型,并以表格的方式列出单位剂量产品的处方组成,列明各成分在处方中的作用,执行的标准。
如有过量加入的情况需给予说明。
对于处方中用到但最终需去除的溶剂也应列出。
(2)如附带专用溶剂,参照以上表格方式列出专用溶剂的处方。
(3)说明产品所使用的包装材料及容器。
ctd申报模板

ctd申报模板
CTD申报模板是用于向监管机构提交化学药物临床试验申请的表格,通常包括以下内容:
1. 封面页:包括药物名称、申请人信息、申请类型、申报单位等信息。
2. 目录:列出整个申报材料的内容清单,便于审评人员快速了解申报材料的内容。
3. 概述:简要介绍药物的研发背景、目的、主要研究内容、技术方法等。
4. 药学研究总结:详细描述药物的剂型、处方组成、生产工艺、质量标准、稳定性等方面的研究结果。
5. 药理毒理研究总结:详细描述药物的初步药理、毒理、药效学等方面的研究结果。
6. 临床研究总结:详细描述临床试验的设计、实施过程、数据分析、结果评价等方面的研究结果。
7. 风险评估和安全有效性总结:对整个研发过程进行风险评估,并对药物的安全性和有效性进行总结。
8. 药品包装材料和标签说明:详细描述药品的包装材料、标签、说明书等方面的内容。
9. 参考文献:列出所有引用的文献。
以上是CTD申报模板的一般内容,具体内容可能因药物类型、申报目的和监管机构的要求而有所不同。
在编写申报材料时,建议仔细阅读相关法规和指导原则,遵循监管机构的要求,确保申报材料的质量和完整性。
CTD格式申报资料撰写格式(制剂)

CTD格式申报资料撰写格式(制剂)3.2.P.1 剂型及产品组成3.2.P.2 产品开发3.2.P.2.1 处方组成3.2.P.2.1.1 原料药3.2.P.2.1.2 辅料3.2.P.2.2 制剂3.2.P.2.2.1 处方开发过程3.2.P.2.2.2 制剂相关特性3.2.P.2.3 生产工艺的开发3.2.P.2.4 包装材料/容器3.2.P.2.5 相容性3.2.P.3 生产3.2.P.3.1 生产商3.2.P.3.2 批处方3.2.P.3.3 生产工艺和工艺控制3.2.P.3.4 关键步骤和中间体的控制3.2.P.3.5 工艺验证和评价3.2.P.4 原辅料的控制3.2.P.5 制剂的质量控制3.2.P.5.1 质量标准3.2.P.5.2 分析方法3.2.P.5.3 分析方法的验证3.2.P.5.4 批检验报告3.2.P.5.5 杂质分析3.2.P.5.6 质量标准制定依据3.2.P.6 对照品3.2.P.7稳定性3.2.P.7.1 稳定性总结3.2.P.7.2上市后的稳定性研究方案及承诺3.2.P.7.3 稳定性数据二、申报资料正文及撰写要求3.2.P.1 剂型及产品组成(1)说明具体的剂型,并以表格的方式列出单位剂量产品的处方组成,列明各成分在处方中的作用,执行的标准。
如有过量加入的情况需给予说明。
对于处方中用到但最终需去除的溶剂也应列出。
(2)如附带专用溶剂,参照以上表格方式列出专用溶剂的处方。
(3)说明产品所使用的包装材料及容器。
要求:列出所有辅料的组成和用量(若含增塑剂,需说明增塑剂用量的合理性),包括包衣辅料等;3.2.P.2 产品开发提供相关的研究资料或文献资料来论证剂型、处方组成、生产工艺、包装材料选择和确定的合理性,具体为:技术要求:简要说明产品开发目标,包括剂型/规格选择依据;简要描述背景资料,市场导向,国内外上市情况,专利、产品说明书,制剂处方组成、相关标准等资料的调研;并以列表的形式提出开发目标(QTTP),包含:(1)预期的临床用途,给药途径、剂型、给药系统;(2)剂量规格(3)容器密闭系统(4)影响药代动力学和质量的关键属性(如:溶出度)(5)适合于拟上市产品的药品质量标准(如:纯度、稳定性和药物溶出);参考下表:3.2.P.2.1 处方组成3.2.P.2.1.1 原料药参照《化学药物制剂研究的技术指导原则》,提供资料说明原料药和辅料的相容性,分析与制剂生产及制剂性能相关的原料药的关键理化特性(如晶型、溶解性、粒度分布等)要充分。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
制剂格式申报资料4、5.2类3.2 制剂3.2.1剂型及产品组成(1)说明具体的剂型,并以表格的方式列出单位剂量产品的处方组成,列明各成分在处方中的作用,执行的标准。
如有过量加入的情况需给予说明。
对于处方中用到但最终需去除的溶剂也应列出。
表1(注:表格依次编号,下同):处方(2)如附带专用溶剂,参照以上表格方式列出专用溶剂的处方。
(3)说明产品所使用的包装材料及容器。
3.2.2 产品开发说明产品开发目标。
说明原研药上市情况。
详细提供包括原研药的质量概况在内的相关研究资料或文献资料来论证本品的剂型、处方组成、生产工艺、包装材料选择和确定的合理性。
3.2.2.1处方组成3.2.2.1.1原料药参照《化学药物制剂研究的技术指导原则》,提供资料说明原料药和辅料的相容性,分析原料药的关键理化特性(如分类、晶型、溶解性、粒度分布等)与制剂生产及制剂性能的相关性,并提供相关的研究资料与文献。
3.2.2.1.2辅料说明辅料是否适合所用的给药途径结合辅料在处方中的作用分析辅料的哪些性质会影响制剂特性,提供相关的研究资料与文献。
3.2.2.2 制剂研究3.2.2.2.1处方开发过程参照《化学药物制剂研究的技术指导原则》,提供处方的研究开发过程和确定依据,包括文献信息(如对照药品的处方信息)、研究信息(包括处方设计,处方筛选和优化、处方确定等研究内容)、辅料种类和用量选择的依据、分析辅料用量是否在常规用量范围内,以及自制样品与原研药的质量特性对比研究结果(需说明原研药的来源、批次和有效期,自研样品批次,对比项目、采用方法),并重点说明在药品开发阶段中处方组成的主要变更、原因以及支持变化的验证研究。
如生产中存在过量投料的问题,应提供过量投料的必要性和合理性的相关研究资料。
3.2.2.2.2制剂相关特性对与制剂性能相关的理化性质,如、离子强度、溶出度、再分散性、复溶、粒径分布、聚合、多晶型、流变学等进行分析。
提供自研产品与原研药品的理化性质、质量特性对比研究结果,例如有关物质等。
如为口服固体制剂,需提供详细的自研产品与原研药在不同溶出条件下的溶出曲线比较研究结果,推荐采用f2相似因子的比较方式。
如为手性药物,详细提供光学纯度和构型稳定性的研究控制情况。
3.2.2.3生产工艺的开发提供详细的工艺研究资料(包括实验数据及图谱),说明在开发阶段对哪些工艺步骤以何质量指标进行了工艺条件的优选与放大研究。
该资料应能充分证明申报的工艺有充足的研究与放大的数据支持,保证现有的申报工艺的规模、物料控制、操作流程及主要设备均已基本与大生产一致,已生产的批数与各批产品的质量均能反映出工艺具备一定的重现性,进而证明该申报工艺的合理性与大生产的可行性。
详细说明在工艺开发过程中生产工艺的主要变化(包括批量、设备、工艺参数、中间体控制等的变化)及相关的支持性验证研究。
汇总研发过程中代表性批次(应包括但不限于临床试验批、中试放大批、生产现场检查批、工艺验证批等)的样品情况,包括:批号、生产时间及地点、生产工艺、批量、用途(如用于稳定性试验,用于生物等效性试验等)、分析结果(例如有关物质、溶出度以及其他主要质量指标)。
示例如下:表:批分析汇总注:表中所列批次的生产工艺如不一致,应注明各工艺的编号,并在表格下另行说明各工艺的不同点。
3.2.2.4包装材料/容器(1)包材类型、来源及相关证明文件:表:包材类型、来源及相关证明文件注1例如,五层共挤膜输液袋,规格为内层:改性乙烯/丙烯聚合物,第二层:聚乙烯,第三层:聚乙烯,第四层:乙烯甲基丙烯酸酯聚合物,第五层:多酯共聚物;聚丙烯输液瓶,规格为250;铝塑泡罩包装,组成为:铝、铝、铝;复合膜袋包装,组成为:聚酯/铝/聚乙烯复合膜袋、聚酯/低密度聚乙烯复合膜袋。
注2:表中的配件一栏应包括所有使用的直接接触药品的包材配件。
如:塑料输液容器用组合盖、塑料输液容器用接口等。
提供包材的检验报告(可来自包材生产商或供应商)。
(2)阐述包材的选择依据说明原研药所使用的内包材,并说明本品的内包材是否与原研药一致,如不一致,应提供充分的试验与文献依据。
(3)对包材选择的支持性研究详细提供本品与内包材相容性研究的资料,包括相容性试验的内容、每一项研究内容采用的试验设计、考察指标、检测方法及方法学验证、样品制备方法、试验结果及对结果的分析等。
相容性研究可以参考国内外相关指导原则进行。
如未进行包材相容性研究,应说明理由,并提供充分的文献依据。
3.2.2.5相容性提供详细的研究资料,说明制剂和附带溶剂或者给药装置的相容性。
3.2.3生产信息3.2. P.3.1生产商详细提供生产商的全称、地址、电话、传真以及生产线的具体地址、电话、传真等。
上述信息应与申请表、证明文件、生产现场检查报告中的地址与生产线完全一致。
3.2.3.2 批处方以表格的方式列出典型生产规模产品的批处方组成,列明各成分执行的标准。
如有过量加入的情况需给予说明并论证合理性。
对于处方中用到但最终需去除的溶剂也应列出。
表:典型生产批的处方3.2.3.3 生产工艺和工艺控制(1)工艺流程图:按制备工艺步骤提供完整、直观、简洁的工艺流程图,应涵盖所有的工艺步骤、各物料的加入顺序,并标明关键步骤以及进行中间体检测的环节。
(2)工艺描述:以目前生产的最大批量为例,按单元操作过程描述工艺(包括包装步骤),明确操作流程、工艺参数和范围。
在描述各单元操作时,应结合不同剂型的特点关注各关键步骤与参数。
如大输液品种的原辅料的预处理、直接接触药品的内包装材料等的清洗、灭菌、去热原等;原辅料的投料量(投料比),配液的方式、温度和时间,各环节溶液的值范围;活性炭的处理、用量,吸附时浓度、温度、搅拌或混合方式、速度和时间;初滤及精滤的滤材种类和孔径、过滤方式、滤液的温度与流速;中间体质控的检测项目及限度,药液允许的放置时间;灌装时药液的流速,压塞的压力;灭菌温度、灭菌时间和目标F0值。
生产工艺描述的详略程度应能使本专业的技术人员根据申报的生产工艺可以完整地重复生产过程,并制得符合标准的产品。
(3)主要的生产设备:列表提供本品实际生产线的主要生产设备的相关信息,如型号、操作原理、规格、正常的批量范围、生产厂、用于的工艺步骤等,并说明与现有最大的生产批量的匹配性。
如现有最大的生产批量所用主要生产设备与实际生产线的不一致,应提供相应的放大研究与验证的试验依据,以证明在实际生产线上能采用工艺验证报告或空白的批生产记录上的工艺稳定地生产出合格的药品。
如输液制剂生产中的灭菌柜型号、生产厂、关键技术参数;轧盖机类型、生产厂、关键技术参数;过滤滤器的种类和孔径;配液、灌装容器规格等。
(4)拟定的大生产规模及依据:说明商业大生产的拟定批量及其制定依据。
通常可以结合生产设备情况、处方工艺研究放大情况、验证情况、临床试验试验样品的生产规模等拟定大生产规模。
如拟定的大生产的批量范围超出了研究开发过程中的最大生产批量(包括临床试验试验样品的批量),应提供充分的放大研究与验证的依据。
3.2.3.4 关键步骤和中间体的控制列出所有关键步骤及其工艺参数控制范围。
详细提供界定关键工艺步骤和工艺参数的研究资料,以支持关键步骤确定的合理性以及工艺参数控制范围的合理性。
提供中间体的质量控制标准(包括项目、方法和限度)及质量标准拟定的依据,并提供必要的方法学验证资料。
3.2.3.5 工艺验证和评价提供无菌工艺步骤的工艺验证报告(编号:,版本号:),工艺必须在预定的参数范围内进行。
工艺验证内容包括:批号;批量;设备的选择和评估;工艺条件/工艺参数及工艺参数的可接受范围;分析方法;抽样方法及计划;工艺步骤的评估;可能影响产品质量的工艺步骤及可接受的操作范围、关键工艺步骤和工艺参数的确认等。
对于非无菌工艺步骤,可提交工艺验证报告(编号:,版本号:),也可仅提供工艺验证方案(编号:,版本号:)和上市后对前三批商业生产批进行验证的承诺书。
所有制剂均应提供空白的批生产记录样稿。
该样稿应是针对本品的实际生产线按照申报的工艺进行的操作规程,应与今后正常生产本品的保持一致。
验证方案、验证报告、空白的批生产纪录等应有编号及版本号,且应由合适人员(例如、、质量及生产负责人等)共同签署。
3.2.3.6临床试验试验样品的生产情况提供临床试验试验样品的批生产记录和自检报告的复印件,包括相应的图谱。
3.2.4 原辅料的控制提供原辅料的来源、相关证明文件以及执行标准。
表:原辅料的信息者制剂给药途径的需要精制而得,例如精制为注射给药途径用,需提供精制工艺选择依据、详细的精制工艺及其验证资料、精制前后的质量对比研究资料、精制产品的注射用内控标准及其起草依据。
如制剂生产商对原料药、辅料制定了内控标准,应分别提供制剂生产商的内控标准以及原料药/辅料生产商的质量标准。
提供原料药、辅料生产商的检验报告复印件以及制剂生产商对所用原料药、辅料的检验报告复印件。
提供是否有风险的声明。
3.2.5 制剂的质量控制应提供充分的试验资料与文献资料,证明仿制品的质量与已上市原研药的质量是一致的,仿制品的货架期标准是合理可行的,且不低于现行的技术指导原则与各国现行版药典的要求。
3.2.5.1 质量标准按下表提供质量标准的分析方法与限度(方法不必详细描述,可简述为,或中国药典方法等),并与其他药典标准(如,、、等)进行比较。
如具有放行标准和货架期标准,应分别进行说明。
表:质量标准比较3.2.5.2 分析方法详细提供质量标准中各项目的检查方法及其筛选、优化的过程,并对其他药典收载的主要项目(如有关物质、溶出度、含量等)的方法列表进行比较。
示例可参考原料药项下。
3.2.5.3 分析方法的验证按照《化学药物质量控制分析方法验证技术指导原则》、《化学药物质量标准建立的规范化过程技术指导原则》、《化学药物杂质研究技术指导原则》、《化学药物残留溶剂研究技术指导原则》以及现行版《中华人民共和国药典》附录中有关的指导原则,逐项提供详细的方法学验证资料,并提供相关验证数据和图谱。
可采用表格形式整理验证结果,示例如下:表:有关物质检查方法——法的建立表:有关物质方法学验证结果有关物质分析方法的验证应采用拟控制的杂质的对照品与供试品进行验证,以充分证明该分析方法确实能有效地检出相应的杂质。
3.2.5.4 批检验报告提供不少于三批连续生产的验证批或生产批样品的检验报告。
提供临床试验试验样品的检验报告。
3.2.5.5 杂质谱分析以列表的方式列明产品中可能含有的杂质,分析杂质的产生来源,结合相关指导原则要求,对于已知杂质给出化学结构并提供结构确证资料,并提供控制限度。
可以表格形式整理,示例如下:表:杂质谱分析说明各杂质在最终质量标准中是否进行控制以及控制的限度,并提供充分的依据。
