保健食品液体制剂生产记录
维生素B6注射液批生产记录20130122
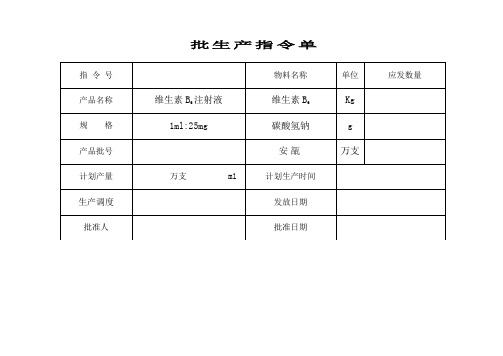
2.记录操作区温度:18-26℃湿度:45%-65%压差≥10Pa
温Байду номын сангаас:℃湿度: %压差:Pa
3.配剂室无与本批生产无关的物料,设备清洁合格。
□符合要求□不符合要求
4.配剂所用容器具已清洁并在有效期内。
□符合要求□不符合要求
5.检查配剂用本批记录文件齐全。
□齐全□不齐全
6.本批生产的房间状态标志牌已换挂。
□已挂标识牌□未挂标识牌
2.滤前气泡点试验
按气泡点试验方法对0.45µm、0.22µm的滤芯做气泡点试验,要求如下:0.45µm压力:≥0.20Mpa
0.22µm压力:≥0.25Mpa并附打印记录
0.45µm:压力:Mpa
0.22µm:压力:Mpa
3.药液管道的配剂前清洗
配剂罐、药液管道及过滤系统的配剂前清洁按SOP-CLP 309进行操作。清洗时间为30分钟以上。
□ 已清洗清洗时间:-
□ 未清洗
4.配剂操作
1.配剂罐内加配剂量约90%的注射用水,水温室温(10~30℃)
加注射用水ml水温:℃
岗位:
QA:
2.将维生素B6投入注射用水中,搅拌3+1分钟。
□按要求操作□未按要求操作
3.补加注射用水至全量。
注射用水加至ml
4.用5%碳酸氢钠溶液40ml-45ml缓慢加入上述溶液中,搅拌循环5分钟后测PH值在2.8—3.3。
3.灌封室设备清洁合格。
□符合要求□不符合要求
4灌封所用器具已清洁并在有效期内。
□符合要求□不符合要求
5.灌注系统及管道已清洗/灭菌并在有效期内。
□符合要求□不符合要求
6.检查灌封用本批记录文件齐全。
XXX版GMP口服液制剂全套批生产记录

XXX版GMP口服液制剂全套批生产记录产品名称:XXX版GMP口服液制剂生产批号:XXXXX生产日期:XXXX年XX月XX日一、原辅材料准备及检查1.原辅材料准备:(1)主要原料清单:原料名称供应商批号用量xxx xxx公司 xxx xxxxxx xxx公司 xxx xxx(2)辅料清单:辅料名称供应商批号用量xxx xxx公司 xxx xxxxxx xxx公司 xxx xxx2.原辅材料检查:(1)主要原料:按照相关要求进行外观、标识、包装、规格等检查,检查记录见附件1(2)辅料:按照相关要求进行外观、标识、包装、规格等检查,检查记录见附件2二、制剂生产过程1.准备制剂设备和容器:(1)根据工艺要求,准备好所需的制剂设备和容器,洗净并消毒。
2.准备生产用水:(1)检查生产用水的水质,并记录相关数据。
3.准备制剂溶剂:(1)按工艺要求,准备好制剂所需的溶剂。
4.配制制剂溶液:(1)按照工艺要求,将制剂原料逐一加入搅拌容器中,适当加热并搅拌至均匀。
5.过滤制剂溶液:(1)将配制好的制剂溶液通过过滤器过滤,去除悬浮物等杂质。
6.灭菌处理:(1)将过滤好的溶液进行灭菌处理,确保产品的微生物指标符合要求。
7.装瓶包装:(1)将灭菌好的制剂液体装入瓶中,按规定数量进行包装。
9.封瓶:10.封装包装:三、质量控制及分析1.进行质检样品的取样及标记。
2.根据质检样品的检验项目和方法,进行质检操作。
3.记录质检结果,并进行分析。
4.对合格的产品进行包装交接。
四、记录1.生产批次报告:记录生产过程中的设备、操作、环境等要点,检查合格项目等,附件32.温度记录:记录生产过程中的各个环节的温度,附件43.湿度记录:记录生产过程中的各个环节的湿度,附件54.净化度验证记录:记录净化设备的验证情况,附件65.灭菌验证记录:记录灭菌设备的验证情况,附件76.质量检查记录:记录质量检查的结果,附件8以上内容为生产批次记录的基本内容,详细操作和检验项目及方法需根据具体工艺和要求进行调整。
保健食品液体制剂生产记录
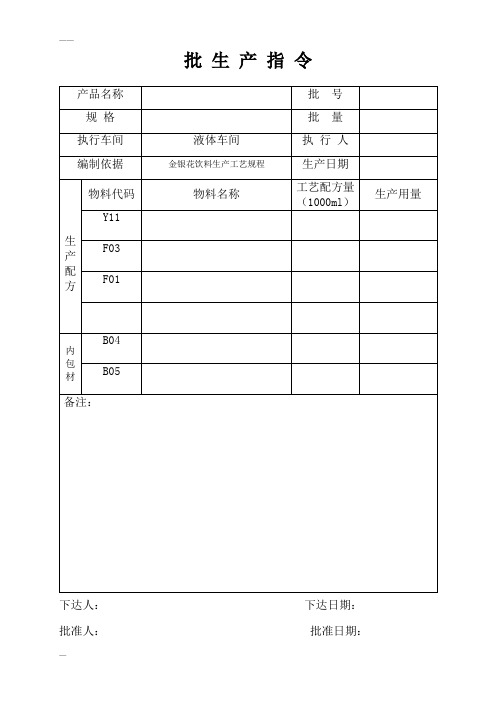
3.检查设备是否完好。
4.按生产工艺取规定量30-40%纯化水置夹层锅,加热至沸腾。
5.将配方中的金银花加入夹层锅进行煎煮提取(时间为30分钟)后进行过滤至贮罐中备用。
6.将、和贮罐中的料液放入调配罐中进行搅拌溶解,过滤后备用。
有□ 无□
是□ 否□
投料记录
:
::
升温
开始
时间
到达
时间
灭菌温度 ℃
115℃
灭菌
开始
时间
结束
时间
灭菌总数:瓶
破 损:瓶
操作人:复核人:
4.清场:设备容器具是否已清洁并挂好相应状态牌,操作间有无遗留物。
已清洁 是□ 否□
遗留物 有□ 无□
清场人:
QA: 日期:
5.现场监视监控记录
复核人:
灯检岗位操作记录
生产日期:
品名:
规格:
批号:
批量:
平衡率= ×100%
总配制量
平衡率范围99±2%
是□ 否□
是□ 否□
10ml玻璃瓶:
铝盖:
待灌装料液: L
试灌装装量检测结果: QA:
灌装总数:瓶
灌装合格瓶数:瓶
收率=
是否符合规定:是□ 否□
平衡率=
有无偏差:有□ 无□
操作人:复核人:
8.清场:设备容器具是否已清洁并挂好相应状态牌,操作间有无遗留物。
□完好
□已煎煮提取
□已加热沸腾
□已溶解、搅拌均匀
□加全量
得溶液:
操作人: 复核人:
7.QA取样送检(中间产品报告单附后)
□已取样
取样量: QA:
口服液体制剂批生产记录(全套)

XXXX制药有限公司
XXXX口服液批生产记录
产品批号:
生产日期:
有效期至:
包装规格:
投料总数:
成品数量:
XXXX口服液批生产记录汇总表
填表日期:年月日填表人:
中药材净选、水洗、干燥生产记录
岗位清场记录
粉碎岗位生产记录
岗位清场记录
渗漉工序记录
XXXX制药有限公司岗位清场记录
XXXX制药有限公司
乙醇回收岗位生产记录
XXXX口服液批生产记录,第9页
岗位清场记录
XXXX制药有限公司配料称量记录
XXXX制药有限公司配制岗位记录
XXXX制药有限公司岗位清场记录
内包装(分装)记录
岗位清场记录
XXXX制药有限公司灭菌岗位生产记录
岗位清场记录
灯检岗位生产记录
岗位清场记录
岗位清场记录。
GMP口服液制剂全套批生产记录

GMP口服液制剂全套批生产记录一、生产前准备生产日期:(填写具体日期)生产序号:(填写具体序号)1.设备和工具准备:a)检查所有设备和工具是否干净、完好无损,并进行必要的校准。
b)检查设备操作按钮和控制仪表是否正常运行。
2.准备原材料:a)核对所需原材料及数量,确保无误。
b)检查原材料是否符合要求,并进行必要的测试和检验。
3.校准仪器和设备:a)校准所有用到的仪器和设备,确保准确度和精确性。
4.检查和清洁生产区域:a)检查生产区域是否干净整洁,并进行必要的清洁和消毒。
b)检查生产区域的温湿度是否符合要求,如有需要,进行调整。
5.审核和签署相关文件:a)审核各项相关文件,确保生产记录的准确性和完整性。
b)签署相关文件,确认批生产过程开始。
二、生产过程记录1.生产前操作:a)检查生产区域的温湿度是否符合要求,如有需要,进行调整。
b)核对原材料及数量,确保无误。
2.制备药液:a)根据生产工艺和配方,将所需原材料按照准确的配比和方法加入制剂容器中。
b)确认加入原材料的准确性和完整性,并记录下来。
3.混合和搅拌:a)启动混合和搅拌设备,并按照工艺要求进行混合和搅拌操作。
b)监测混合和搅拌设备的运行状况,并记录下来。
4.过滤和清洁:a)将药液进行过滤处理,去除杂质和固体颗粒。
b)检查过滤设备的过滤效果和运行状况,并记录下来。
c)对过滤后的药液进行必要的清洁处理。
5.灭菌处理:a)对药液进行灭菌处理,确保产品的安全性和无菌性。
b)监测灭菌设备的运行状况,并记录下来。
6.填充和包装:a)将灭菌处理后的药液装入符合要求的容器中。
7.质检和检验:a)取样进行质量检验,确保产品符合要求。
b)监测质检设备和检验方法的准确性和稳定性,并记录下来。
8.封标和入库:a)对通过质检的产品进行封标处理。
b)按照规定的程序和要求,将封标的产品入库。
三、生产结束及记录1.生产结束操作:a)关闭设备和工具,确保安全和无损坏。
b)对生产区域进行清洁和消毒处理,确保干净卫生。
口服液批生产记录1

口服液批生产记录产品名称____________________批号____________________规格____________________配置量____________________理论产量_____________________成品量_____________________包装规格______________________ 生产周期:年月日至年月日批生产记录目录1 批生产指令书2 批领料记录3 制水岗位生产指令4 制水岗位生产记录(附上批清场合格证)5 纯化水检测检验记录6 制水岗位清场记录(附本批生产状态指示牌“生产证”)7 配料岗位生产指令8 配料岗位生产记录(附上批清场合格证)9 配料岗位清场记录(附本批生产状态指示牌“生产证”)10 理瓶岗位生产指令11 理瓶岗位生产记录(附上批清场合格证)12 理瓶岗位清场记录(附本批生产状态指示牌“生产证”)13洗瓶烘瓶岗位生产指令14洗瓶烘瓶岗位生产记录(附上批清场合格证)15洗瓶烘瓶岗位清场记录(附本批生产状态指示牌“生产证”)16灌封岗位生产指令17灌封岗位生产记录(附上批清场合格证)18灌封质量监测记录19灌封岗位清场记录(附本批生产状态指示牌“生产证”)20灭菌岗位生产指令21灭菌岗位生产记录(附上批清场合格证)22灭菌岗位清场记录(附本批生产状态指示牌“生产证”)23灯检岗位生产指令24灯检岗位生产记录(附上批清场合格证)25灯检岗位清场记录(附本批生产状态指示牌“生产证”)26批包装指令书27批配料记录28外包装岗位生产指令29外包装岗位生产记录(附上批清场合格证)30外包装岗位清场记录(附本批生产状态指示牌“生产证”)31物料平衡分析汇总表32工序收得率分析汇总表33生产过程监控记录34成品检验报告单口服液批生产指令书批领料记录领料人:日期:配料人:日期:制水岗位生产指令书制水岗位生产记录纯化水监测检验记录QA签名:制水岗位清场记录配料岗位生产指令书配料岗位清场记录理瓶岗位生产指令书理瓶岗位生产记录理瓶岗位清场记录洗瓶烘瓶岗位生产指令书洗瓶烘瓶岗位生产记录洗瓶烘瓶岗位清场记录。
五子衍宗口服液批生产记录(100盒)

五子衍宗口服液批生产审核单
口服液准备岗位容器具处理及灭菌操作记录
五子衍宗口服液洗瓶岗位生产指令单
口服液洗瓶岗位操作记录
格式号:YL·Z02-02-002-01
口服液车间洗瓶岗位清洁记录
五子衍宗口服液配液、灌封指令单
五子衍宗口服液配液岗位操作记录
岗位负责人:工艺员:
五子衍宗口服液灌装岗位操作记录
口服液生产线中转岗位操作记录
中转岗半成品进、出记录
五子衍宗口服液灭菌岗位操作记录
五子衍宗口服液灯检岗位生产指令单
口服液车间一般生产区清洁记录
五子衍宗口服液包装岗位生产指令
五子衍宗口服液批包装记录
五子衍宗口服液批包装记录
岗位负责人:工艺员:
五子衍宗口服液批包装记录
岗位负责人:工艺员:
包装工包装产量明细
包 装 工 包 装 产 品 明 细。
口服干混悬剂批生产记录模板

口服干混悬剂批生产记录模板口服干混悬剂的批生产记录模板通常包含以下内容:1. 产品信息:记录口服干混悬剂的通用名称、规格、批号等基本信息。
2. 原辅料准备:列出所使用的原辅料的名称、批号、供应商信息等,并记录其准备数量和使用数量。
3. 设备清单:列出用于生产口服干混悬剂的设备清单,包括混合器、称量器等,并记录其校准情况。
4. 生产工艺:详细描述生产过程中的每个步骤,包括原辅料的称量、混合、搅拌时间、温度控制等。
5. 生产记录:记录每个生产步骤的实际操作情况,包括操作员、操作时间、操作步骤、操作结果等。
6. 质量控制:记录在生产过程中进行的质量控制检验,包括原辅料的检验、中间产品的检验、最终产品的检验等,并记录检验结果。
7. 清洁记录:记录清洁过程,包括设备和容器的清洗、消毒等。
8. 备注:记录生产过程中的特殊情况、异常情况、操作员的签名等。
以下是一个口服干混悬剂批生产记录模板的示例:批号:20210101日期:2021年1月1日产品信息:通用名称:口服干混悬剂规格:10mg/袋批号:001原辅料准备:原辅料名称批号供应商准备数量(g) 使用数量(g)甲 202012 A公司 50 48乙 202011 B公司 30 28设备清单:混合器:型号A,校准日期:2020年12月1日称量器:型号B,校准日期:2020年11月15日生产工艺:1. 将甲按配方要求称量48g,将乙按配方要求称量28g。
2. 将甲、乙放入混合器中,搅拌10分钟。
3. 控制温度在25°C,继续搅拌5分钟。
4. 完成混合后,将混合物装袋,每袋10mg。
生产记录:操作员操作时间操作步骤操作结果张三 08:00 称量甲 48g李四 08:05 称量乙 28g王五 08:10 混合搅拌完成质量控制:- 甲的检验结果:符合要求- 乙的检验结果:符合要求- 最终产品检验结果:符合要求清洁记录:设备清洗:使用清洁剂X进行设备清洗,消毒剂Y进行消毒。
保健食品GMP质量体系RD0204000醇沉岗位生产记录

保健食品GMP质量体系RD0204000醇沉岗位生产记录日期:YYYY年MM月DD日岗位:醇沉岗位工作人员:XXX、XXX、XXX1.岗位背景醇沉岗位是保健食品GMP质量体系中的重要环节,负责醇沉工艺的生产操作。
醇沉是一种常用于提取保健食品中活性成分的工艺方法,通过溶剂提取和醇沉的步骤,将保健食品中的目标成分分离出来。
该岗位的任务是根据工艺要求,进行准确、规范的操作,确保产品质量和生产效率。
2.生产记录本次生产记录的产品为XX保健食品,下面将详细记录醇沉岗位的生产工作。
2.1原材料准备a.检查原材料的质量,确保原材料符合要求。
b.准备好所需的溶剂和醇沉剂,确保溶剂和醇沉剂的质量和纯度符合要求。
c.确保工作区域的清洁,准备好所需的工具和容器。
将容器进行清洗、消毒,并在工作台上摆放好。
2.2生产操作a.根据配方和工艺要求,准确称取所需原料,并进行记录。
b.将原料按照配方和工艺要求添加到容器中,确保添加的顺序、比例和方法准确无误。
c.搅拌原料混合物,确保搅拌的时间、速度和方式符合要求。
d.将容器移至醇沉设备中,进行沉淀操作。
根据工艺要求设置沉淀时间,并确保沉淀的效果达到要求。
e.在沉淀过程中,及时检查沉淀物的形态和质量,并做好记录。
f.醇沉完成后,根据工艺要求将上清液和沉淀进行分离。
确保分离的过程规范、完整,并记录分离的效果。
g.对分离后的上清液进行过滤、除杂等处理,确保上清液质量达到要求。
h.整理并清洁工作区域,将废弃物进行妥善处理。
2.3记录与数据a.在操作过程中,及时记录关键步骤的操作时间、温度、压力等重要参数,并进行签名确认。
b.记录操作过程中可能出现的异常情况、处理措施和结果。
c.记录工艺设备的运行情况、维护记录等信息。
d.记录原材料的批号、生产日期、失效日期等信息。
e.将记录的数据整理成周报、月报等形式,进行归档保存。
3.结束与总结本次醇沉岗位的生产操作顺利完成,工艺步骤和操作均符合GMP质量体系的要求。
保健食品GMP质量体系RD0208900水沉岗位生产记录

保健食品GMP质量体系RD0208900水沉岗位生产记录日期:2024年1月1日生产线:水沉岗位操作人员:张三、李四、王五生产记录:1.原料准备1.1张三负责查询并核对所需原料清单,确保所使用原料完全符合生产要求。
1.2张三根据清单准备所需原料,并进行称量,确保原料的准确性和精确度。
1.3李四负责核对和签署原料称量记录,确保原料准备过程的准确性和可追溯性。
2.生产操作2.1张三按照工艺要求将准备好的原料加入生产设备中,并设置合适的参数。
2.2张三启动生产设备,确保设备运行正常,并记录设备启动时间。
2.3张三定期对生产设备进行检查和维护,确保设备的运行稳定和安全性。
2.4张三根据生产工艺要求,进行工艺操作,包括加热、搅拌等。
2.5李四负责对生产过程进行监控,确保操作的规范性和符合GMP要求。
2.6王五负责记录生产操作的各项参数和数据,包括温度、时间、搅拌速度等。
3.抽样检验3.1张三、李四根据抽样计划,定期对生产过程中的产品进行抽样。
3.2张三、李四进行抽样,确保样品的平均性和代表性。
3.3张三、李四将抽样样品送至质检部门进行检验,确保产品质量符合标准要求。
4.包装4.1张三、李四负责将生产完毕的产品进行包装,确保包装的完整性和卫生性。
4.2张三、李四将包装好的产品进行记录,包括产品数量、批次号等信息。
4.3张三、李四将包装好的产品送至成品库存区,并进行入库记录。
5.清洁和消毒5.1张三、李四负责对生产设备和生产环境进行定期清洁和消毒。
5.2张三、李四按照清洁和消毒程序进行操作,并记录清洁和消毒的日期和时间。
5.3张三、李四将清洁和消毒记录交给质量部门进行审核和存档。
备注:本次生产过程中未发生异常情况和质量问题,所有操作符合GMP质量体系要求,并按照相关标准操作程序进行。
生产完毕后,生产区域清洁整齐,无任何残留物。
小儿咳喘灵口服溶液批生产记录
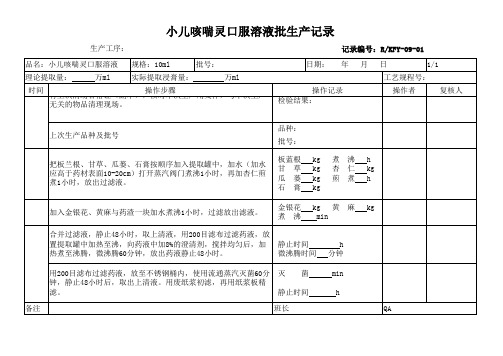
生产工序: 品名:小儿咳喘灵口服溶液 理论提取量: 时间 万ml 规格:10ml 实际提取浸膏量: 批号: 万ml 操作记录 检验结果: 日期: 记录编号:R/KFY-09-01 年 月 日 操作者 1/1 复核人
工艺规程号:
操作步骤 有上次清场合格证(副本),核对本次生产用文件,与本次生产 无关的物品清理现场。 上次生产品种及批号
品种: 批号: 板蓝根 甘 草 瓜 蒌 石 膏 金银花 煮 沸 kg kg kg kg 煮 杏 煎 沸 仁 煮 h kg h
把板兰根、甘草、瓜蒌、石膏按顺序加入提取罐中,加水(加水 应高于药材表面10-20cm)打开蒸汽阀门煮沸1小时,再加杏仁煎 煮1小时,放出过滤液。
加入金银花、黄麻与药渣一块加水煮沸1小时,过滤放出滤液。 合并过滤液,静止48小时,取上清液,用200目滤布过滤药液,放 置提取罐中加热至沸,向药液中加8%的澄清剂,搅拌均匀后,加 热煮至沸腾,微沸腾60分钟,放出药液静止48小时。 用200目滤布过滤药液,放至不锈钢桶内,使用流通蒸汽灭菌60分 钟,静止48小时后,取出上清液。用废纸浆初滤,再用纸浆板精 滤。 备注
kg 黄 min麻kg静止时间 微沸腾时间 灭 菌
h 分钟 min h QA
静止时间 班长
小儿止咳糖浆剂批生产记录
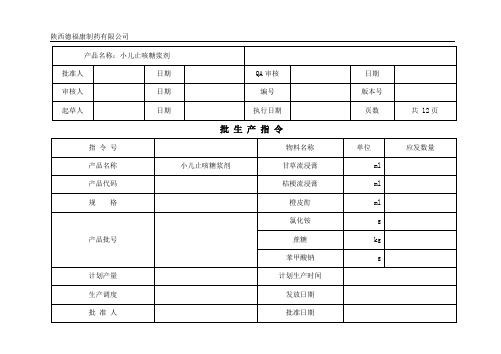
陕西德福康制药有限公司产品名称:小儿止咳糖浆剂批准人日期QA审核日期审核人日期编号版本号起草人日期执行日期页数共 12页批生产指令指令号物料名称单位应发数量产品名称小儿止咳糖浆剂甘草流浸膏ml产品代码桔梗流浸膏ml规格橙皮酊ml产品批号氯化铵g 蔗糖kg 苯甲酸钠g计划产量计划生产时间生产调度发放日期批准人批准日期批号操作时间年月日第2页共21页生产日汇总表品名:小儿止咳糖浆剂批号:规格:年月日物料中间产品备注含量原辅料名称批号代号化验单号投料量(kg)项目含量(%)甘草流浸膏桔梗流浸膏橙皮酊氯化铵蔗糖苯甲酸钠配液体积回收液体积玻璃瓶用量标签用量小纸盒用量中纸盒用量纸箱用量灌装数(瓶)理论数(瓶) 生产数(瓶)灯检成品灯检数(瓶)合格品数(瓶)合格率(%)成品数(瓶)合格率(%)入库数(瓶)QA:复核人:填表人:批号操作时间年月日第3页共21页原辅料领料单名称物料编号批号上批留用实发数量检验报告号发料人领料人领料日期甘草流浸膏ml ml桔梗流浸膏ml ml橙皮酊ml ml氯化铵g g蔗糖kg kg苯甲酸钠g g批 号操作时间 年 月 日 第4页 共21页称 量 工 序 记 录操作步骤规定工艺要求实际操作1.称量前检查房间号: 清场合格,有上批清场合格副本。
□符合要求 □不符合要求操作时间:操作人:复核人:电子称表面无粉尘、污渍;在校验有效期内,使用前已用标准砝码校正。
□符合要求 □不符合要求墙壁无粉尘、污渍,地面无积水,无物料残渍。
□符合要求 □不符合要求 容器具内外表面无粉尘,污渍。
□符合要求 □不符合要求 房间压差为相对负压□负压 房间压差 Pa有生产状态标示卡,内容填写完全。
□已挂标识牌 □挂标识牌 2.领取物料 从原辅料暂存间领取原辅料,并同时核对名称、数量,批号、外观等相关信息。
□符合要求 □不符合要求操作时间:操作人:复核时间:复核人:3.称量物料电子称型号:编号: 名称 标准量 批号 领用量 使用量 复核数量 剩余量 甘草流浸膏 30万ml 桔梗流浸膏 6万ml橙皮酊 4万ml 氯化铵 2万g 蔗糖 1300kg 苯甲酸钠4000g4.退回物料 将剩余的物料密封,称重,贴上标签后,退回原辅料暂存间,填写记录。
GMP质量管理体系文件 消斑口服液洗瓶生产记录
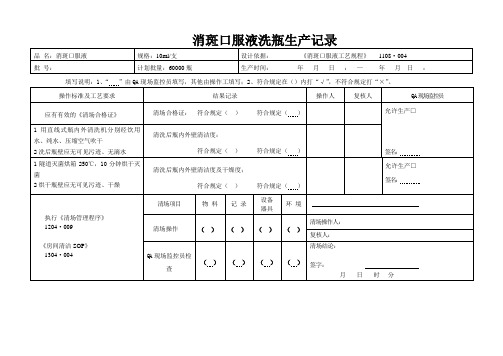
品名:消斑口服液
规格:10ml/支
设计依据:《消斑口服液工艺规程》1108·004
批号:
计划批量:60000瓶
生产时间:年月日:—年月日:
填写说明:1、“”由QA现场监控员填写,其他由操作工填写;2、符合规定在()内打“√”,不符合规定打“×”。
操作标准及瓶内外壁清洁度及干燥度;
符合规定( ) 符合规定()
允许生产□
签名:
执行《清场管理程序》
1204·009
《房间清洁SOP》
1304·004
清场项目
物料
记录
设备
器具
环境
清场操作
()
()
()
()
清场操作人:
复核人:
QA现场监控员检查
()
()
()
()
清场结论:
签字:
月日时分
复核人
QA现场监控员
应有有效的《清场合格证》
清场合格证: 符合规定( ) 符合规定()
允许生产□
签名:
1用直线式瓶内外清洗机分别经饮用水、纯水、压缩空气吹干
2洗后瓶壁应无可见污迹、无滴水
清洗后瓶内外壁清洁度:
符合规定( ) 符合规定()
1隧道灭菌烘箱250℃,10分钟烘干灭菌
2烘干瓶壁应无可见污迹、干燥
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
已清洁 是□ 否□
遗留物 有□ 无□
清场人:
QA:日期:
6.现场监视监控记录
监控记录:
QA:
配制岗位操作记录
生产日期:
品名:
规格:
批号:
批量:
编 制 依 据
1、生产工艺规程
2、配制岗位标准操作记录
生 产 指 令
操 作 结 果
1.操作间有 “清场合格证”, “已清洁”合格证。
2.检查设备是否完好。
3.核对包材名称、数量并做记录。
4.按灌装机标准操作规程操作。
5.调整装量经QA确认合格后开始后灌装。
6.在灌装过程中每20分钟测量一次装量,同时做好记录
7.理论灌装量= 领用料液数量 ×100﹪
每瓶灌装数量
合格瓶数
料液收率= ×100%
配制液÷标示量
收率范围95~99%
灌装瓶数×平均装量+废弃液+剩余液
批生产指令
产品名称
批 号
规 格
批 量
执行车间
液体车间
执 行 人
编制依据
金银花饮料生产工艺规程
生产日期
生
产
配
方
物料代码
物料名称
工艺配方量(1000ml)
生产用量
Y11
F03
F01
内
包
材
B04
B05
备注:
下达人: 下达日期:
批准人: 批准日期:
称量备料岗位生产记录
生产日期:
品名:
规格:
批号:
批量:
编 制 依 据
□符合
送检量: QA:
5.清场:设备容器具是否已清洁并挂好相应状态牌,操作间有无遗留物。
已清洁 是□ 否□
遗留物 有□ 无□
清场人:
QA: 日期:
6.现场监视监控记录
监控记录:
QA:
批包 装指令
产品名称
批 号
规 格
批 量
执行车间
液体车间
料)生产工艺规程
2.核对物料的品名、批号、数量是否一致。
3.检查设备是否完好。
4.按生产工艺取规定量30-40%纯化水置夹层锅,加热至沸腾。
5.将配方中的金银花加入夹层锅进行煎煮提取(时间为30分钟)后进行过滤至贮罐中备用。
6.将、和贮罐中的料液放入调配罐中进行搅拌溶解,过滤后备用。
有□ 无□
是□ 否□
投料记录
:
::
合格数+不良品数
平衡率=×100%
领用数
平衡率:98±2%
是□ 否□
操 作 人
灯检产量
不良品数
01
02
03
04
05
灯检总量:瓶
不合格品数:瓶
灯检合格率=
是否符合规定:是□ 否□
灯检平衡率=
有无偏差: 有□ 无□
不合格品分类情况表:
分 类
装量不合格
异 物
松 盖
其 它
数 量
4.取样送检(中间产品报告单附后)
洗瓶(烘干)岗位操作记录
生产日期:
品名:
规格:
批号:
批量:
编 制 依 据
1、生产工艺规程
2、洗瓶(烘干)岗位标准操作记录
生 产 指 令
操 作 结 果
1.检查操作间有无 “已清洁”“清场合格证”
2.核对包材数量是否一致
3.检查设备是否完好
4.10ml玻璃瓶、铝盖用自来水初洗,再用纯化水精洗。
5.将10ml玻璃瓶和铝盖放入烘箱内,干燥灭菌。
批量:
编 制 依 据
1、工艺规程 2、灭菌岗位标准操作规程
生 产 指 令
操 作 记 录
1.检查操作间有无 “已清洁”“清场合格证”。
有□ 无□
2.复核灭菌物的品种、批号、数量应与传递卡一致。
是□ 否□
领取瓶
3.按灭菌岗位标准操作程序操作。
灭菌温度115℃
压力:0.2KPa
灭菌时间30分钟
是□ 否□
灭 菌 记 录
6.清场:设备容器具是否已清洁并挂好相应状态牌,操作间有无遗留物。
已清洁 是□ 否□
遗留物 有□ 无□
清场人:
QA: 日期:
7.现场监视监控记录
监控记录:
QA:
灌装岗位操作记录
生产日期:
品名:
规格:
批号:
批量:
编 制 依 据
1、生产工艺规程
2、灌装岗位标准操作记录
生 产 指 令
操 作 结 果
1.检查操作间有无 “已清洁”“清场合格证”、核对品名、批号是否相符。
编 制 依 据
1、生产工艺规程2、灯检岗位标准操作规程
生 产 指 令
操 作 记 录 及 结 果
1.检查操作间有无 “已清洁”和“清场合格证”
有□ 无□
2.核对灯检的品种、批号、数量是否一致。
是□ 否□
数量瓶
3.按灯检标准操作规程灯检。
记录个人产量及不良品数:
合格数
合格率= ×100%
领入数
范围≥96%
平衡率= ×100%
总配制量
平衡率范围99±2%
是□ 否□
是□ 否□
10ml玻璃瓶:
铝盖:
待灌装料液: L
试灌装装量检测结果: QA:
灌装总数:瓶
灌装合格瓶数:瓶
收率=
是否符合规定:是□ 否□
平衡率=
有无偏差:有□ 无□
操作人:复核人:
8.清场:设备容器具是否已清洁并挂好相应状态牌,操作间有无遗留物。
已清洁 是□ 否□
遗留物 有□ 无□
清场人:
QA: 日期:
9.现场监视监控记录
监控记录:
QA:
附表:灌装装量检查表
品 名
批 号
装量检查
装量为250ml/支;每20分钟抽查一次,每次抽查4瓶
编号
时间
1
2
3
4
:
:
:
:
:
:
:
:
:
:
:
:
:
:
:
:
:
:
:
:
:
:
:
:
结论
灭菌岗位操作记录
生产日期:
品名:
规格:
批号:
生产工艺规程
2、称量备料岗位标准操作规程
生 产 指 令
操 作 记 录
1.操作间有“已清洁”和“清场合格证”。
2.计量器具是否在有效期内。
是□ 否□
是□ 否□
3.物料经缓冲间脱包清洁并做记录
4.核对待称量物料的品种、批号、数量是否一致
是□ 否□
称 量 备 料 单
物料名称
编 号
备料量
剩余量
称量人: 复核人:
合格瓶数
收率=×100%
领用数量-剩余数量
收率范围≥95%
合格瓶数+剩余数量+废瓶数
平衡率= ×100%
领用数量
范围:≥98%
有□ 无□
是□ 否□
10ml玻璃瓶:
铝盖:
完好□
□已清洗
□已干燥、灭菌
合格玻璃瓶数:
不合格玻璃瓶数:
铝盖数:
收率=
是否符合规定:是□ 否□
平衡率=
有无偏差:有□ 无□
操作人: 复核人:
升温
开始
时间
到达
时间
灭菌温度 ℃
115℃
灭菌
开始
时间
结束
时间
灭菌总数:瓶
破 损:瓶
操作人:复核人:
4.清场:设备容器具是否已清洁并挂好相应状态牌,操作间有无遗留物。
已清洁 是□ 否□
遗留物 有□ 无□
清场人:
QA: 日期:
5.现场监视监控记录
复核人:
灯检岗位操作记录
生产日期:
品名:
规格:
批号:
批量:
□完好
□已煎煮提取
□已加热沸腾
□已溶解、搅拌均匀
□加全量
得溶液:
操作人: 复核人:
7.QA取样送检(中间产品报告单附后)
□已取样
取样量:QA:
8.清场:设备容器具是否已清洁并挂好相应状态牌,操作间有无遗留物。
已清洁 是□ 否□
遗留物 有□ 无□
清场人:
QA: 日期:
9.现场监视监控记录
监控记录:
QA: 日期:
