CAR-T免疫治疗
CAR-T细胞治疗的挑战

CAR-T细胞治疗的挑战化疗、放疗和外科手术是最传统的癌症治疗方法,但它们的疗效较低,副作用严重。
因此,在过去的十年中,研究人员已经开发了新的策略,从而实现疾病的完全缓解。
目前,免疫疗法已经成为革命性的癌症治疗方法,有几种类型的免疫疗法用于治疗癌症,其中包括过继细胞疗法(ACT)。
嵌合抗原受体(CAR)T细胞疗法是一种ACT,自体T细胞通过基因工程表达CAR以特异性杀死肿瘤细胞。
CAR-T细胞疗法是治疗对其他一线癌症治疗无反应患者的一个机会,并且已经在血液恶性肿瘤的治疗中展现出优越的抗肿瘤效果。
然而,这类疗法作为一线临床治疗仍有许多挑战需要克服。
从药学的角度来看,这项新兴技术仍然被归类为先进疗法,因此,要应用这项技术,必须首先满足医药监管的某些要求。
因此,有必要分析CAR-T细胞技术的要素和挑战,并将基础、临床和实践等方面的因素考虑在内,采取应对策略,从而使CAR-T技术能够成为可负担的治疗模式。
CAR-T细胞发展简史回顾CAR-T的发展史,首先要提到1957年Thomas及其同事报告的首次白血病患者骨髓移植以及随后Miller等人发现了T细胞的起源。
然而,直到1986年Steven Rosenberg 报告了一项关于肿瘤浸润淋巴细胞(TIL)的研究,这才让人们将目光锁定在“患者自身的免疫细胞可以对抗自身癌症”的理念上。
1992年,Sadelain等人成功地建立了逆转录病毒介导的基因转移到T淋巴细胞的方法,使基因修饰成为在实验或治疗环境中控制免疫的手段。
几乎与此同时,ZeligEshhar及其同事利用抗体结合域和T细胞受体上免疫球蛋白的γ或ζ亚单位,通过嵌合单链设计了细胞毒性淋巴细胞的特异性激活,从而开发出第一代CAR-T细胞。
五年后,Sadelain博士的研究小组证明,将CD28等共刺激信号整合到CAR-T中可增强生存、增殖并保持活性,从而开发出第二代CAR。
随后,携带靶向CD19的CAR-T细胞被开发出来,并启动了慢性淋巴细胞白血病(CLL)和急性淋巴细胞白血病(ALL)的I期临床试验。
cd7cat原理

cd7cat原理
CD7-CAR-T(Chimeric Antigen Receptor T cell)是一种免疫治疗方法,旨在利用患者自身的T细胞来攻击癌症。
其原理如下:
首先,从患者体内提取T细胞,然后通过基因工程技术将CD7基因导入T
细胞,使T细胞表达CD7蛋白。
接着,通过CAR-T技术对T细胞进行改造,使其能够特异性地识别和攻击表达CD7的癌细胞。
改造后的T细胞被重新
输回到患者体内,与癌细胞结合并激活免疫反应,最终杀灭癌细胞。
CD7-CAR-T疗法的原理基于T细胞表面表达的CD7蛋白的特异性。
CD7
是一种在T细胞表面稳定表达的标志物,几乎所有的T细胞肿瘤患者都会表达CD7,因此CD7成为了一个理想的靶点。
通过利用CD7-CAR-T疗法,可以直接针对T细胞肿瘤进行精确打击,而不影响正常的T细胞。
然而,CD7-CAR-T疗法也存在一些挑战。
例如,由于正常T细胞和恶性T
细胞之间共有的抗原性,目前仍然缺乏针对T细胞恶性肿瘤的获批CAR-T
疗法。
此外,大量清除T细胞后可能使患者出现严重相关的T细胞免疫缺陷,从而导致感染的风险增加。
因此,为了克服这些挑战,目前正在研究制备不表达CD7的CAR-T或其他替代方法。
总的来说,CD7-CAR-T是一种具有潜力的免疫治疗方法,但还需要进一步的研究和改进才能更好地应用于临床治疗。
kymriah原理 -回复

kymriah原理-回复Kymriah(中文名:唐可替)是一种由瑞士诺华制药公司(Novartis)开发的CAR-T细胞疗法。
它是第一种通过基因工程将T细胞与抗原受体(CAR)融合的疗法,用于治疗一种罕见但具有巨大破坏性的白血病——急性淋巴细胞白血病(ALL)。
本文将详细介绍Kymriah的原理,并逐步回答您的问题。
一、CAR-T疗法的基本原理1. 什么是CAR-T细胞疗法?CAR-T细胞疗法是一种免疫治疗方式,利用基因工程技术将患者自身的T 细胞(免疫系统的一种细胞)改造成携带具有高度亲和力的抗原受体(CAR),以增强T细胞对癌细胞或病原体的识别和杀伤能力。
2. CAR的结构和功能是什么?CAR(Chimeric Antigen Receptor)是一个融合蛋白,由外部的单链抗体结构域、连接桥梁区和内部的信号传导区组成。
外部的单链抗体可以通过特异性识别白血病细胞表面的特定抗原。
连接桥梁区使得抗原识别和信号传导区联系在一起,而内部的信号传导区则启动T细胞的杀伤机制。
3. CAR-T细胞疗法的基本流程是什么?CAR-T细胞疗法的基本流程包括T细胞采集、基因改造、增殖扩增、药物治疗与回输等步骤。
首先,医生从患者的体内采集T细胞,并将其送往实验室进行基因改造。
然后,将获得的CAR基因导入T细胞中,使其表达CAR蛋白。
接下来,改造后的T细胞在实验室内被增殖扩增,以获得足够数量的CAR-T细胞。
最后,这些CAR-T细胞通过输注的方式回输给患者,使其免疫系统获得更强的攻击白血病细胞能力。
二、Kymriah的特点和原理1. 什么是Kymriah?Kymriah是一种基于CAR-T细胞疗法的治疗方法,具有针对急性淋巴细胞白血病的能力。
它是由从患者体内提取的T细胞经过基因改造和扩增后制备而成的。
2. Kymriah的治疗原理是什么?Kymriah的治疗原理是利用CAR-T细胞疗法的基本原理。
首先,医生从患者体内采集T细胞,并将其送往实验室进行基因改造。
有效率100﹪,中国CAR-T癌症免疫治疗团队成ASCO最闪亮的新星 临床大发现

有效率100﹪,中国CAR-T癌症免疫治疗团队成ASCO最闪亮的新星临床大发现目前,癌症治疗中,化疗反应率大约是10%-30%,免疫系统药物最高的反应率在35%-40%,即便是靶向药物,反应率也就是70%-80%。
然而在芝加哥举行的美国临床肿瘤学会(ASCO)年会上传来了惊人的消息——来自中国的研究团队,在采用CAR-T治疗难治性或复发性的多发性骨髓瘤临床试验中,客观反应率为100%![1]更为重要的是,这项临床研究中,一共有35名患者接受了CAR-T治疗,所有患者都对CAR-T治疗有反应,客观响应率达到惊人的100%。
让人振奋的是,有19名患者中位随访时间为6个月,其中18名患者病情完全缓解,1名患者部分缓解,CAR-T治疗有效率也是100%。
该结果实力碾压美国的Bluebird Bio公司,成为ASCO的焦点。
因为后者在临床试验中,只招募了21名患者,有18人的治疗时间足够长,可供评价,其中只有15人对CAR-T治疗有反应[2]。
此次CAR-T治疗反应率能达到100%,这让美国癌症协会副首席医务官Leonard Lichtenfeld博士非常震惊,他表示:“达到100%实在是太难了,这些结果真是令人印象深刻!”[3]这项研究是由西安交通大学二附院与南京传奇生物(Nanjing Legend Biotech)联合开展的。
在接受CAR-T治疗的35名晚期复发或难治性的多发性骨髓瘤患者中,全部患者都有反应,在初次注射CAR-T细胞后的第10天,患者就表现出治疗效果。
其中19名患者的随访时间已超过4个月,能够进行有效评估:14名患者(74%)达到严格完全缓解(sCR)标准,没有任何患者出现复发;4名患者(21%)达到非常好的部分缓解(VgPR)标准,1名患者(5%)达到部分缓解(PR)标准。
在安全性方面,这次的CAR-T治疗也是非凡的。
细胞因子释放综合征是CAR-T治疗中的常见的危险副作用,在接受CAR-T治疗时,有85%的患者出现了这一副作用,但只是暂时的。
car t免疫疗法原理

car t免疫疗法原理CAR-T免疫疗法是一种新型的免疫治疗技术,它利用改造的CAR(chimeric antigen receptor)T细胞来识别和攻击肿瘤细胞。
CAR-T细胞疗法的基本原理是将病人的自体T细胞提取出来,并通过基因工程技术改造,使其表达具有特异性的CAR。
CAR是由抗原识别结构域和信号传导结构域组成的融合受体,抗原识别结构域可以与肿瘤细胞特异性抗原结合,信号传导结构域可以激活T细胞杀伤功能。
首先,病人的T细胞会被提取出来,并通过特定的生物技术手段进行基因改造,使其携带CAR基因。
然后,经过一系列体外培养和扩增的步骤,大量改造后的CAR-T细胞会被重新注入到患者体内。
一旦重新注入到患者体内,CAR-T细胞会识别并结合到肿瘤细胞表面的特异性抗原上。
这一结合会激活CAR-T细胞内的信号传导通路,进而激发CAR-T细胞的杀伤功能。
CAR-T细胞会释放出细胞毒性物质,如穿孔素和细胞因子,进而导致肿瘤细胞的凋亡和死亡。
CAR-T免疫疗法的优势在于其特异性和高效性。
CAR-T细胞通过识别特异性抗原与肿瘤细胞发生特异性结合,因此可以避免对正常细胞的损伤。
此外,CAR-T细胞具有极高的杀伤能力,即使在低浓度下也能有效杀伤肿瘤细胞。
然而,CAR-T免疫疗法也存在一些挑战和风险。
一方面,由于CAR-T细胞具有强大的杀伤能力,可能会导致严重的不良反应,如细胞因子释放综合征和神经毒性反应。
另一方面,CAR-T疗法的制备过程需要耗费大量的时间和资源,并且成本较高。
尽管存在一些挑战,CAR-T免疫疗法仍然被认为是一种有前景的肿瘤治疗技术。
随着科学技术的不断进步和临床实践的深入,CAR-T免疫疗法有望在未来为患者带来更好的治疗效果。
肿瘤细胞免疫治疗之CAR-T技术:技术优势、风险与几大应用场景

肿瘤细胞免疫治疗之CAR-T技术:技术优势、风险与几大应用场景动脉网2018-10-04 11:36:35一、CAR-T技术原理(一)过继性细胞治疗过继性细胞治疗是细胞的免疫治疗一个主要研究方向。
过继免疫细胞输注(adoptive cell transfer, ACT)属于肿瘤的被动免疫疗法,指的是分离肿瘤患者自体肿瘤浸润淋巴细胞( tumor-infiltrating lymphocytes,TIL)或者外周血淋巴细胞,在体外加以分选、扩增、活化,并回输至患者体内。
在恶性黑色素瘤和肾细胞癌,TIL是常用的ACT治疗。
TIL是浸润于肿瘤中的淋巴细胞,分离后在IL-2等因子作用下进行体外扩增,最后再回输到患者体内。
然而,多数情况下无法应用TIL:有些患者缺乏肿瘤标本或肿瘤和转移灶中TIL很少;获得新鲜的肿瘤组织并分离和扩增TIL 具有难度;回输的TIL 细胞功能受损,在体内往往不能有效识别肿瘤细胞; 肿瘤中强大的免疫抑制微环境降低回输细胞的杀伤能力。
这些问题限制了TIL的广泛应用,仅对如恶性黑色素瘤和肾细胞癌的少数肿瘤有一定疗效,对大多数肿瘤疗效欠佳。
在这种情况下,ACT需要使用外周血淋巴细胞。
目前使用外周血淋巴细胞的ACT包括淋巴因子激活的杀伤细胞(lymphokine activated killer cells,LAK)、细胞因子诱导的杀伤细胞(cytokine-induced killer,CIK)、树突细胞-细胞因子诱导杀伤细胞(dendritic cells-cytokine induced killer,DC-CIK)、抗CD3抗体诱导的活化杀伤细胞(anti-CD3 antibody-induced activated killer cells, CD3-AK cells)等。
然而CIK等是非特异性活化的淋巴细胞,缺乏肿瘤特异性反应能力。
在这种情况下,科学家开始通过基因修饰,将识别肿瘤抗原的T细胞受体(T cell receptor, TCR)或CAR基因导入淋巴细胞使之成为TCR基因修饰T淋巴细胞(TCR-T)或CAR-T细胞,使之具备肿瘤抗原靶向识别能力。
CAR-T治疗
CAR-T治疗01、什么是CAR-T治疗?嵌合抗原受体(CAR)T细胞免疫疗法是通过整合后基因修饰的T细胞来抵抗肿瘤细胞的有效过继细胞治疗。
研究已证实其在B细胞急性淋巴细胞白血病 (B-ALL) 患者中的显著疗效,并被FDA认定为“突破性治疗”。
随后在CD 19-CAR-T治疗复发性/难治性B细胞非霍奇金淋巴瘤(B-NHL)的研究中也显示出了良好疗效。
目前全球有3款CAR-T产品获得FDA批准被用于血液瘤的治疗,已在多个国家开展实体瘤治疗临床研究。
02、它是怎样发挥作用的?CD19是一种在B细胞表面表达的B细胞受体相关蛋白。
由于其在恶性B细胞上均匀表达,且仅在B细胞谱系中表达,因此被认为是最佳的治疗靶点。
抗CD19CAR是一种重组分子,由三部分组成:源自抗CD19单克隆抗体的单链可变区(scFv)、跨膜区、T细胞受体(TCR)的信号转导区(CD3ζ)。
为了改善CAR-T细胞扩增能力,进一步增强杀伤力和精准度,CAR的结构也在逐渐完善中,目前进展到第四代CAR的探索阶段。
正常T细胞与抗原呈递细胞(APC)(如树突状细胞)相互作用,通过T细胞受体(TCR)和其他共刺激结构域被激活(a)。
TCR 介导的抗原识别依赖于主要组织相容性复合体(MHC)分子上的多肽。
然而,CAR-T可以通过抗原识别结构域识别靶抗原,并且不依赖于MHC(b)。
当CAR-T识别特异性抗原时,细胞通过细胞内信号转导结构域被激活,发挥靶细胞毒性。
(i) 通过白细胞单采采集患者的单核细胞(ii) T细胞被分离、激活和扩增(iii) 使用逆转录病毒或慢病毒载体将CAR基因转染至T细胞中(iv)细胞克隆扩增(v) 将新创的CAR-T细胞产品输注到已接受淋巴细胞耗竭化疗的患者体内03CAR-T治疗会带来哪些风险?一旦T细胞被激活,他们的细胞毒性可能会导致副作用:(i) 靶向肿瘤毒性:即使在CAR-T细胞通过其在肿瘤组织上表达的靶点特异性激活的最佳情况下也会导致毒性。
car-t成功案例

car-t成功案例
以下是一些Car-T成功案例的例子:
1. CAR-T治疗白血病:在2017年,FDA批准了一款名为Kymriah的CAR-T细胞疗法,用于治疗一种罕见的急性淋巴细胞白血病(ALL)。
这是世界上第一款获得批准的CAR-T 治疗药物。
在临床试验中,Kymriah显示出对于治疗复发或难治性ALL的患者有显著的疗效,使得许多患者能够获得长期的缓解或无病生存。
2. CAR-T治疗淋巴瘤:CAR-T细胞疗法也已成功用于治疗一种名为B细胞淋巴瘤的癌症。
在临床试验中,CAR-T细胞疗法显示出对于治疗难以治愈的B细胞淋巴瘤患者具有显著的疗效。
目前有一些CAR-T疗法已经获得了FDA的批准,用于治疗不同类型的淋巴瘤。
3. CAR-T治疗多发性骨髓瘤:多发性骨髓瘤是一种恶性血液肿瘤,目前没有可治愈的方法。
然而,CAR-T细胞疗法已经在临床试验中显示出在治疗多发性骨髓瘤中的潜力。
在一项临床试验中,患者接受了一种名为bb2121的CAR-T细胞治疗,结果显示有70%的患者对治疗有积极的反应。
这些案例只是展示了Car-T治疗在不同类型的癌症中的潜力和疗效。
随着技术的进步和进一步的研究,相信会有更多的成功案例涌现。
car-t 案例

car-t 案例摘要:1.什么是CAR-T 疗法2.CAR-T 疗法的原理3.CAR-T 疗法的发展历程4.CAR-T 疗法的应用领域5.CAR-T 疗法的优势与挑战6.我国在CAR-T 疗法方面的研究进展7.结论正文:1.什么是CAR-T 疗法CAR-T 疗法,全称为嵌合抗原受体T 细胞疗法,是一种免疫治疗技术。
通过基因工程技术,将具有识别特定肿瘤抗原的受体基因导入T 细胞中,使T 细胞能够特异性地识别和攻击肿瘤细胞。
2.CAR-T 疗法的原理CAR-T 疗法的原理是利用T 细胞对肿瘤细胞的天然识别和杀伤能力,通过基因工程技术给T 细胞安装一个能够识别特定肿瘤抗原的“导航系统”,从而使T 细胞能够更加精准地识别和攻击肿瘤细胞。
3.CAR-T 疗法的发展历程CAR-T 疗法的发展经历了几个阶段:从最早的单个受体结构,到第二代、第三代的多个受体结构,再到现在的第四代、第五代CAR-T 疗法。
每一代CAR-T 疗法都在特异性、安全性和有效性等方面有所提升。
4.CAR-T 疗法的应用领域CAR-T 疗法主要应用于血液肿瘤的治疗,如急性淋巴细胞白血病、淋巴瘤等。
随着研究的深入,CAR-T 疗法在实体瘤治疗领域的应用也在逐步拓展。
5.CAR-T 疗法的优势与挑战CAR-T 疗法的优势在于它能够精准识别和攻击肿瘤细胞,具有较高的特异性和有效性。
然而,CAR-T 疗法也面临着一些挑战,如制备过程复杂、成本高昂,以及可能出现的严重副作用等。
6.我国在CAR-T 疗法方面的研究进展近年来,我国在CAR-T 疗法方面的研究取得了显著进展。
多个研究团队在国内外发表了重要的研究成果,一些CAR-T 疗法产品也进入了临床试验阶段。
7.结论CAR-T 疗法是一种具有巨大潜力的肿瘤治疗技术。
CAR-T治疗的安全性

CAR-T治疗的安全性
CAR-T(嵌合抗原受体T细胞)是一种新型的免疫治疗方式,
被广泛应用于肿瘤治疗领域。
然而,CAR-T治疗在提供疗效的同时,也存在一定的安全性问题。
1. 急性毒性反应
CAR-T治疗可能引发急性毒性反应,包括发热、寒战、低血压、呼吸急促等症状。
这些反应往往发生在CAR-T细胞输注后的数小
时内,可能严重影响患者的生命体征和器官功能。
2. 慢性毒性反应
除了急性反应外,CAR-T治疗还可能导致慢性毒性反应。
长期使用CAR-T细胞可能对正常细胞和组织造成损害,引发各种慢性
毒性反应,如免疫不耐受、细胞凋亡等。
3. 细胞增殖与转移
CAR-T细胞治疗过程中,CAR-T细胞的不受控制增殖可能导致治疗效果上的波动,甚至引发白血病等恶性疾病。
此外,CAR-T 细胞的转移也是安全性问题之一,转移到其他部位可能导致非预期的副作用。
4. 免疫系统副作用
CAR-T治疗采用自身免疫细胞改造而成的CAR-T细胞,对免疫系统产生一定程度的影响。
免疫系统副作用可能包括免疫过度激活、自身免疫反应、感染等,需要特别注意。
综上所述,CAR-T治疗虽然具有突破性的疗效,但安全性问题不可忽视。
在进行CAR-T治疗时,应该充分评估患者的安全性,并采取适当的措施来监测和减轻治疗过程中可能出现的副作用和安全隐患。
car-t 原理

car-t 原理
CAR-T细胞疗法(Chimeric Antigen Receptor T-cell Therapy)是
一种细胞免疫治疗方法,可以将患者的T细胞重编程以识别和攻击癌细胞。
该治疗方法主要依靠组成性的CAR受体来实现。
1.收集T细胞:从患者体内收集外周血中的T细胞。
2.重编程T细胞:通过人工合成的CAR基因,将其植入到T细胞中,
改变其表观特性,让其对癌细胞更加敏感。
3.批量培养:将重编程的T细胞运往实验室进行批量生产和培养,从
而形成大量的CAR-T细胞。
4.注射CAR-T细胞:将生产好的CAR-T细胞注射到患者体内,让其攻
击和杀死癌细胞。
CAR-T细胞疗法通过增强T细胞的功能,来对抗癌细胞。
由于其治疗
效果、可控性和安全性等方面的优势,已成为当前最具有前途的癌症治疗
手段之一。
CAR-T细胞免疫疗法临床研究伦理审查指南

CAR-T细胞免疫疗法临床研究伦理审查指南在细胞治疗探索研究发展中,CAR-T细胞免疫疗法(chimeric antigen recepto r T-cell immunotherapy,CAR-T细胞免疫疗法)显示出良好的应用前景。
但目前CAR-T技术仍属于新兴领域,其技术标准、临床疗效与潜在风险尚需更多评估数据,临床研究监管存在诸多挑战。
为指导北京地区医疗卫生机构在现行政策下对CAR-T临床研究进行科学、规范地伦理审查,充分评估研究的风险与获益比,落实受试者权益,特制定本指南。
一、适用范围本指南适用于医疗卫生机构开展的CAR-T临床研究伦理审查,包括药物临床试验及研究者发起的探索性临床研究。
二、CAR-T细胞免疫疗法的定义CAR-T细胞免疫疗法,指从受试者血液中分离T淋巴细胞,通过基因工程技术导入含有特异性抗原识别片段、T细胞受体活化分子、共刺激信号分子的CAR 基因修饰T细胞,使其不仅获得识别肿瘤细胞表面特异性抗原的能力,又能获得细胞激活能力。
将构建的这种CAR-T细胞经体外扩增、纯化后回输至受试者体内,从而达到靶向杀伤肿瘤细胞,治疗疾病的目的。
三、研究机构及伦理委员会要求开展临床研究的医疗卫生机构应当具备相应资质与条件,建议参照《药物临床试验质量管理规范》(GCP)、《细胞治疗产品研究与评价技术指导原则(试行)(2017)》、《干细胞临床研究管理办法(试行)》,研究项目已按要求完成药物临床试验或临床研究项目备案,并在备案项目范围内开展研究。
药物、器械临床试验应在具有临床试验资格的机构中进行。
医疗机构承担研究的主体责任,应当建立完备的细胞制备及临床研究全过程质量管理体系、数据信息管理及相关风险管理机制。
开展CAR-T临床研究的机构不得向受试者收取任何研究相关费用,且应购买第三方保险,对于发生与研究相关的损害或死亡的受试者承担治疗费用及相应的经济补偿或赔偿。
研究机构应具有与开展CAR-T临床研究相适应的、由高水平专家组成的独立伦理委员会。
细胞原理的CAR-T疗法

细胞原理的CAR-T疗法标题: 突破医学边界:细胞原理的CAR-T疗法导言:在当今医学领域中,细胞疗法已经成为一种备受关注的先进治疗方法。
而细胞原理的CAR-T疗法更是近年来备受瞩目和推崇的创新疗法。
本文将以直观且易懂的方式探讨CAR-T疗法的基本原理、治疗应用和前景展望,帮助读者深入了解这一引人注目的医学突破。
一、基础概念和原理1. CAR-T疗法的定义和概念- CAR-T全称为Chimeric Antigen Receptor-T cell,是一种细胞免疫疗法。
- CAR是由人工合成的嵌合抗原受体,结合了抗原识别和T细胞激活功能。
2. CAR-T疗法的原理- 提取患者自身免疫细胞,如T细胞。
- 通过基因工程技术将CAR引入T细胞,使其获得识别癌细胞的能力。
- 改造后的CAR-T细胞通过扩增培养后重新注入患者体内。
- CAR-T细胞识别并攻击体内的癌细胞,从而达到治疗目的。
二、CAR-T疗法的应用1. 临床应用和成果- CAR-T疗法在治疗B细胞相关的血液恶性肿瘤上取得了显著的突破,如急性淋巴细胞白血病(ALL)。
- 持续的临床研究和临床试验证实CAR-T疗法在其他癌症类型,如非霍奇金淋巴瘤和多发性骨髓瘤中也表现出潜力和效果。
2. 挑战和限制- 治疗过程中可能出现严重的副作用,如细胞因子释放综合征(CRS)和神经毒性。
- 高昂的成本限制了CAR-T疗法的普及和可及性。
三、前景展望和未来发展1. 研究进展和新技术- 进一步优化CAR结构和细胞工程技术,以提高CAR-T细胞的效果和安全性。
- 开发针对其他癌症类型和抗原的CAR-T疗法,拓展治疗范围。
2. 个体化治疗和组合疗法- 进一步了解不同癌症类型的免疫特点,实现个体化的CAR-T疗法。
- 组合CAR-T疗法与其他治疗方法,如免疫检查点抑制剂的联合应用,以增强治疗效果。
结论:CAR-T疗法作为一项创新的细胞免疫治疗方法,展示了取得突破性进展的潜力。
嵌合抗原受体T细胞(CAR-T)在疾病治疗中的研究进展

孙强等嵌合抗原受体T细胞(CAR-T)在疾病治疗中的研究进展第22期嵌合抗原受体T细胞(CAR-T)在疾病治疗中的研究进展孙强金宇亭黄晶(吉林大学第一医院,长春130000)中图分类号R730.51文献标志码A文章编号1000-484X(2021)22-2815-04[摘要]嵌合抗原受体T细胞(CAR-T)免疫疗法是一种细胞免疫治疗方法,是以CAR为基础的治疗恶性肿瘤的新模式。
此技术将抗原抗体的高度亲和性和T细胞杀伤作用相结合,通过基因修饰的手段,使T细胞能特异性识别并杀死肿瘤抗原,且不受主要组织相容性复合体(MHC)限制。
近几年来,CAR-T免疫疗法除了在治疗急性白血病、非霍奇金淋巴瘤中取得较好的疗效,也被用来治疗实体瘤、自身免疫性疾病和心脏病。
本文就目前CAR-T细胞免疫疗法的现状及其在疾病治疗中的应用进行综述。
[关键词]嵌合抗原受体T细胞;免疫治疗;恶性肿瘤Research progress of chimeric antigen receptor T cells(CAR-T)in disease treatmentSUN Qiang,JIN Yu-Ting,HUANG Jing.First Hospital of Jilin University,Changchun130000,China [Abstract]Chimeric antigen receptor T-cell immunotherapy is a therapeutic method of cellular immunity,which is a new mode of treatment of malignant tumor based on CAR.This technique combines the high affinity of antigen and antibody with the killing effect of T cells.By means of gene modification,T cells can specifically recognize and kill tumor antigens without being restricted by the major histocompatibility complex(MHC).In recent years,CAR-T immunotherapy has achieved good results not only in the treat‐ment of acute leukemia and non-Hodgkin's lymphoma,but also in the treatment of solid tumors,autoimmune diseases and heart dis‐ease.This article reviews the current status of CAR-T immunotherapy and its application in the treatment of malignant tumors.[Key words]CAR-T;Immunotherapy;Malignant tumor嵌合抗原受体T细胞(chimeric antigen receptor T-cell,CAR-T)免疫疗法自产生以来,在临床治疗中发挥重要作用,尤其对血液系统肿瘤及实体瘤来说是一种有效的治疗手段[1-2]。
CAR—T细胞免疫疗法的研究进展

CAR—T细胞免疫疗法的研究进展嵌合抗原受体(CAR)-T细胞免疫疗法是过继性细胞免疫疗法中最具有研究前景的方法,它是利用基因技术,在T细胞内导入一个可以将CAR表达于其表面的基因,并使T细胞发挥作用,克服肿瘤局部免疫抑制微环境、打破宿主免疫耐受状态,靶向杀伤肿瘤细胞。
本综述主要探讨CAR-T细胞免疫疗法及其原理、临床应用、存在的安全性问题和应对措施。
标签:嵌合抗原受体;T淋巴细胞;肿瘤免疫治疗嵌合抗原受体(CAR,Chimeric antigen receptor)-T细胞免疫疗法是一种肿瘤过继细胞免疫疗法,基本原理是利用基因工程修饰T淋巴细胞,使其表达嵌合抗原受体,以非MHC(major histocompatibility complex,主要组织相容性复合体)限制性的方式杀伤肿瘤细胞。
CAR的优点在于能非MHC依赖性识别肿瘤蛋白质和脂类抗原,不需要经过抗原递呈细胞(antigen-presenting cell,APC),目前已經发展到第四代,早期主要用于治疗B细胞急性淋巴细胞白血病(B-ALL),慢性淋巴细胞性白血病和B细胞非霍奇金淋巴瘤[2],近年来也用于治疗实体瘤、HIV等。
虽然CAR-T细胞在临床试验中取得了显著的效果,但同时也出现了诸多安全性问题,包括细胞因子释放综合征、肿瘤溶解综合征、神经毒性和脱靶效应等[3]。
1 CAR-T细胞免疫疗法及原理1.1 CAR-T设计原理正常T细胞的活化有赖于双信号:第一信号由TCR识别APC表面的抗原肽-MHC复合物(p-MHC)启动;第二信号由T细胞和APC间共刺激分子的相互作用启动(即B7/CD28协同刺激信号)[4]。
而CAR-T细胞技术的设计原理是使T细胞不需要依赖MHC分子和APC,将识别肿瘤相关抗原(TAA)的单链抗体(scFv)、跨膜的共刺激结构域(如CD28和CD4-1BB)和T细胞的活化基序结合为一体,通过基因转导的方法转染T淋巴细胞,经基因修饰的T细胞通过表达单链抗体增强结合肿瘤细胞的能力,同时激活T细胞,使其增殖并激活其细胞毒活性,使其能特异性地识别和杀伤肿瘤细胞[5]。
肿瘤免疫治疗的新方法CAR-T 细胞治疗
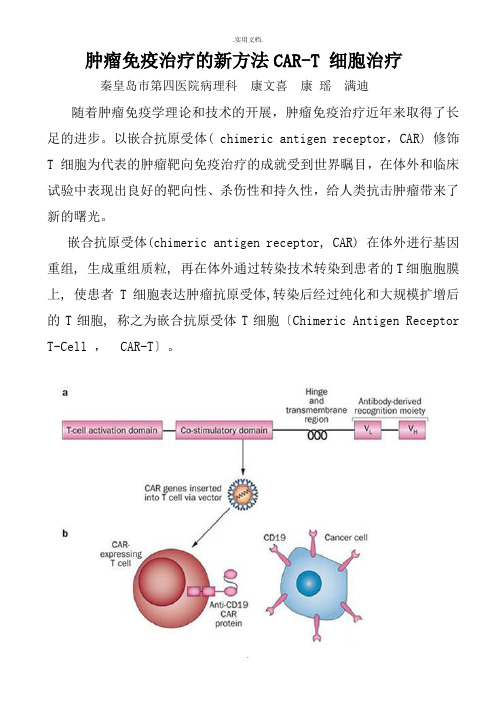
肿瘤免疫治疗的新方法CAR-T 细胞治疗秦皇岛市第四医院病理科康文喜康瑶满迪随着肿瘤免疫学理论和技术的开展,肿瘤免疫治疗近年来取得了长足的进步。
以嵌合抗原受体( chimeric antigen receptor,CAR) 修饰T 细胞为代表的肿瘤靶向免疫治疗的成就受到世界瞩目,在体外和临床试验中表现出良好的靶向性、杀伤性和持久性,给人类抗击肿瘤带来了新的曙光。
嵌合抗原受体(chimeric antigen receptor, CAR) 在体外进行基因重组, 生成重组质粒, 再在体外通过转染技术转染到患者的T细胞胞膜上, 使患者T细胞表达肿瘤抗原受体,转染后经过纯化和大规模扩增后的T细胞, 称之为嵌合抗原受体T细胞〔Chimeric Antigen Receptor T-Cell , CAR-T〕。
1989年Grooss等首次提出CAR-T细胞这一概念,多年来科学家经过不断的深入研究,CAR-T细胞技术已经研制出三代。
第一代CAR 由识别肿瘤外表抗原的单链抗体和免疫受体酪氨酸活化基序〔ITAM〕组成。
然而,ITAM 发出的激活信号只能引起 T 细胞短暂的分裂和较低水平的细胞因子分泌,不能提供长时间的多克隆扩增和持续的体内抗肿瘤效应。
给患者输注第一代 CAR-T细胞2天后, CAR-T细胞在体内可大量繁殖, 但1个月后迅速下降至难以检测的水平, 也没有观察到对肿瘤的免疫应答反响。
虽然对第一代CAR-T细胞的研究较多, 但是大多数试验在细胞扩增、体内存活时间、细胞因子分泌等方面还存在很多问题, 没有到达预期的临床效果。
研究说明, T细胞的完全活化有赖于双信号和细胞因子的作用。
其中第一信号为特异性信号, 由 TCR识别抗原递呈细胞外表的抗原肽-MHC 复合物所启动;第二信号为协同刺激信号, 通过CD28/B7等重要的共刺激分子, 促进IL-2合成, 并使T细胞充分活化及免于凋亡。
对于初始型T细胞(未与抗原接触的T细胞), 如果只有信号1而没有信号2, T 细胞就不能发挥正常作用;即使T细胞与抗原接触, 假设没有协同刺激信号, 细胞也不能发挥正常功能。
car-t各种不良反应的分级标准

Car-T各种不良反应的分级标准
Car-T细胞疗法是一种先进的免疫治疗方法,但也会引发不良反应。
下面是Car-T 各种不良反应的分级标准:
1. 细胞因素相关的不良反应
•一级:轻度发热、头痛等症状
•二级:高热、低血压、呼吸困难等症状
•三级:需住院治疗的重度不良反应
•四级:威胁生命的危重症状,需密切监护和紧急治疗
2. 免疫因素相关的不良反应
•一级:轻度皮疹、恶心、呕吐等症状
•二级:中度瘙痒、腹泻、发热等症状
•三级:重度过敏反应、肺炎等症状
•四级:严重的免疫相关毒性反应,可能导致死亡
3. 组织相关的不良反应
•一级:注射部位疼痛、红肿等症状
•二级:组织坏死、感染等症状
•三级:需手术治疗的严重不良反应
•四级:系统性并发症,需紧急处理。
CAR-T治疗有关问题

Q1:CAR-T的原理是什么?Z(张隆基教授):CAR-T它是基因修改T细胞的治疗方案,换句话说就是一个免疫细胞治疗方案。
它的机理是应用我们身体免疫系统里面主要的两个记忆性细胞的功能,B细胞和T细胞功能做一个修改,我们采用B细胞的抗体基因跟T细胞表面受体基因结合,我们造成一个新的叫做嵌合性的抗体T细胞受体基因chimeric antigen receptor(嵌合抗原受体)这个技术,来把T细胞修改成为一个靶向性的T细胞,所有的T细胞基本上都可以一次性的把它作为一个靶向性的T细胞的修改的一种治疗方案,所以它是一种靶向T细胞的治疗方案。
Q2:CAR-T如何达到抗肿瘤的作用?Z:针对肿瘤,不同的肿瘤我们把肿瘤表面抗原给找到,根据这个肿瘤表面抗原的特异性,我们把T细胞给它靶向到肿瘤层去,所以有一个非常针对性的靶向治疗的特性,即CAR-T 细胞的治疗效果。
如果靶向特异性高的话,治疗效果是非常好的,如果靶向特异性不高的话,它可能有副作用,可能会打到其他的组织细胞,那我们要非常注意。
Q3:CAR-T技术具体到淋巴瘤和白血病是如何让肿瘤快速消亡的?Z:我们讲白血病现在应用比较多,尤其是B细胞急性淋巴瘤的白血病,B急淋因为它表面都是B细胞的抗原,叫做CD19,有的CD20、CD22,CD19的Car现在用的是最多的,主要以CD19的Car为主,那它怎么样有效呢?是因为我们可以把T细胞改变成为针对CD19 B细胞攻击的一个”杀手”细胞,所以可以在很有效的时间之内,大量扩增T细胞,把CD19细胞包括B细胞肿瘤全部杀掉,所以它效果非常好,由于B细胞急淋这是一种叫做血液肿瘤,它是一种瘤体的细胞,这个效果是特别好的,对于淋巴瘤、实体瘤目前也正在开展,它的数据还有病人量比较少,但是初步看的效果也是非常好。
因为淋巴瘤很多也是B细胞的淋巴瘤,表面抗原是一样的,所以目前看来,这个是很有前景的一个细胞治疗方案。
Q4:国际上几个研究中心及国内的相关进展如何?Z:国际上现在还是以美国做的比较多一些临床方面,科研大概在过去十几二十年对Car 的技术的发展已经做了很多了。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
CAR T细胞表面的嵌
合抗原受体
单链抗体ScFv 目前能获得的最小的具有 特异性识别功能的分子, 大小为28KD
CAR-T通过外源基因转染技术,把识别肿瘤相关抗原的单链抗体(scFv)和T细胞活化序列 的融合蛋白表达到T细胞表面,这样scFv通过精品跨PP膜T 区与T细胞胞内的活化增殖信号域偶联,经 回输患者体内后大规模扩增,表现强效的抗癌作用
精品PPT
➢ 慢病毒:表达持久,效率较高;
安全问题,费用较贵。
➢ 电穿孔:适用性广,更加安全;
效率较低,不够持久。
精品PPT
1、早期杀伤力与特异性不强 2、转录方式的选择问题 3、副作用仍不能忽视(细胞因子风暴)
精品PPT
精品PPT
目前制药公司、生物科技公司、大学以及合作 组织都在进行CAR-T细胞的研究,已有公司制 备好可应用于白血病、淋巴瘤、多发性骨髓瘤、 胃癌、肠癌、肺癌、乳腺癌、胰腺癌等多种适 应症的CAR-T技术体系
精品PPT
原理:通过基因转导使患者的T细胞能够表达嵌合抗原受体CAR,将改造后
的T细胞回输至患者体内,生成大量特异性识别肿瘤的CAR-T细胞从而杀死 肿瘤细胞(通过加强自身免疫力和特异性识别来达到杀伤肿瘤的效果)。
CAR-T疗法在会议中大放异彩,会中多项 报告发布了CAR-T疗法最新的喜人进展
目前,国外从事CAR-T疗法研发的公司主要包括诺华、Juno、
Bellicum、Kite Pharma等。2014年7月FDA授予诺华公司开发的个
性化CAR-T癌症疗法CTL019突破性药物认证,并希望借此推动这种
疗法研究
Chimeric Antigen Receptor T-Cell Immunotherapy (CAR-T)
嵌合抗原受体T细胞免疫疗法
精品PPT
2014年12月6号-9号在旧金山举 行的美国血液学会年会(ASH) 上,会议现场的巨型"T细胞"
小女孩Emily Whitehead
第一批吃CAR-T这个螃蟹的人,治愈两 年多了,复查体内仍然没有任何癌细胞
CD28
CD134/ CD137
精品PPT
1、CAR能非MHC依赖性识别肿瘤抗原, 不需要经过APC。
2、肿瘤表面蛋白类和脂类抗原都可以作为 靶点
3、有共刺激分子(如CD28),能有效增 强T细胞增殖
精品PPT
➢ 首次临床应用的报道是2008年,在Nature medicine上 报道了使用CART细胞治疗11例儿童成纤维神经瘤,6例好 转的报道。 ➢ 目前的临床应用,主要集中在白血病上,针对的是CD19、 CD20、CD22三个靶向位点。
