纤维蛋白 纤维蛋白原降解产物测定试剂盒(乳胶免疫比浊法)产品技术要求sjwd
纤维连接蛋白测定试剂盒(免疫比浊法)产品技术要求九强

纤维连接蛋白测定试剂盒(免疫比浊法)适用范围:用于体外定量测定人血清或血浆中纤维连接蛋白的含量。
1.1 包装规格包装规格见表1。
表1 包装规格1.2 主要组成成分主要组成成分见表2。
表2 主要组成成分2.1 外观试剂1为无色澄清液体,目测不得有任何沉淀及絮状悬浮物;试剂2为无色澄清液体,目测不得有任何沉淀及絮状悬浮物;校准品为黄色澄清液体,目测不得有任何沉淀及絮状悬浮物;质控品为黄色澄清液体,目测不得有任何沉淀及絮状悬浮物。
试剂盒标签标识清晰,外包装完整无损。
2.2 净含量试剂的净含量应不少于标称量。
2.3 试剂空白吸光度A340nm下测定空白吸光度应≤ 0.5000。
2.4 准确度与已上市产品进行比对试验:相关系数r≥0.975,在[20.0,100.0] mg/L 区间内测定的偏差应不超过±10 mg/L,在(100.0,600.0] mg/L区间内测定的偏差应不超过±10%。
2.5 分析灵敏度样本浓度为150 mg/L时,其吸光度变化在0.0200~0.1500之间。
2.6 线性范围在[20.0,600.0] mg/L区间内,线性相关系数r≥0.990,在[20.0,100.0] mg/L区间内测定的线性偏差应不超过±10 mg/L,在(100.0,600.0] mg/L区间内测定的线性偏差应不超过±10%。
2.7 测量精密度2.7.1 重复性对不同浓度的同一血清样本或质控品重复测定10次,其测定值的变异系数(CV%)应不大于10%。
2.7.2 批间差随机抽取三批试剂盒的批间相对极差(R)应不大于10%。
2.8 稳定性试剂盒在2℃~8℃密封避光保存,有效期为12个月。
在试剂盒有效期满后一个月以内,应符合2.1、2.3、2.4、2.5、2.6、2.7.1的要求。
纤维蛋白(原)降解产物定值质控品产品技术要求wf

纤维蛋白(原)降解产物定值质控品
产品名称
纤维蛋白(原)降解产物定值质控品
型号、规格
低值:3×0.5 mL、6×0.5 mL 、3×1.0 mL、6×1.0 mL;高值:3×0.5 mL、6×0.5 mL 、3×1.0 mL、6×1.0 mL。
结构及组成
含不同浓度纤维蛋白(原)降解产物重组抗原的缓冲液冻干品。 低值:纤维蛋白(原)降解产物重组抗原,5μg/mL;Tris 缓冲液50mM/L; 高值:纤维蛋白(原)降解产物重组抗原,40μg/mL;Tris 缓冲液50mM/L。 注:不同批次的质控品的靶值及靶值范围参见其靶值单。
产品适用范围/预期用途
适用于纤维蛋白(原)降解产物测定试剂盒(化学发光免疫分析法)试剂配套的检测系统,对该校准项目检测时的室内质量控制。
2
2.1外观
外观应符合如下要求:
a)质控品应为外观均匀,成形完整,呈乳白色的冻干品,复溶后较清亮,无浑浊及沉淀;
b)质控品各组分应齐全、完整,液体无渗漏;
c)中文包装标签清晰,无磨损。
2.2瓶内均一性
变异系数CV≤8.0%。
2.3瓶间均一性
变异系数CV≤5及配套试剂组成的检测系统,对质控品进行上机测定,重复3
次测试,测试结果应在质控品靶值范围内。
1
纤维蛋白(原)降解产物测定试剂盒(胶乳免疫比浊法)产品技术要求meigaoyi

纤维蛋白(原)降解产物测定试剂盒(胶乳免疫比浊法)适用范围:用于体外定量测定人血清中纤维蛋白(原)降解产物的浓度。
1.1包装规格a) 试剂1:1×18ml,试剂2:1×6ml;b) 试剂1:1×30ml,试剂2:1×10ml;c) 试剂1:2×30ml,试剂2:2×10ml;d) 试剂1:1×15ml,试剂2:1×5ml;e)试剂1:2×150ml,试剂2:2×50ml;f)试剂1:1×16.8ml,试剂2:1×5.6ml。
1.2主要组成成分试剂1主要成份Tris缓冲液(pH 6.0-9.0) 30 mmol/L试剂2主要成份鼠抗FDP单克隆抗体胶乳微粒适量2.1 外观和性状2.1.1 试剂盒各组分应齐全、完整、液体无渗漏;外包装完好、无破损,标签完好、字迹清晰。
2.1.2 试剂1应为无色透明溶液;试剂2应为乳白色溶液。
2.2 净含量应不低于试剂瓶标示装量。
2.3 试剂空白测定试剂空白吸光度,应<1.8。
2.4 分析灵敏度测试100ug/ml的被测物时,吸光度变化(ΔA)应不低于0.01。
2.5 准确性与比对试剂盒同时测试40例线性范围内的不同浓度的血清样本,样本浓度在[2.5,120]ug/ml范围内,测定结果相关性(r)≥0.975 样本浓度在[7.0,120]ug/ml相对偏差≤15%;样本浓度[2.5,7.0)ug/ml绝对偏差≤2 ug/ml。
2.6 重复性变异系数(CV)应不超过5%。
2.7 线性2.7.1在[2.5,120]ug/ml范围内,线性回归的确定系数应不低于0.990;2.7.2 [7.0,120]ug/ml相对偏差≤15%;或[2.5,7.0)ug/ml绝对偏差≤1ug/ml。
2.8 批间差对同一份样品进行重复测定,相对偏差<10%2.9 稳定性该产品在2℃~8℃条件下贮存有效期为24个月,取效期末的产品进行检测,应符合2.1、2.2、2.3、2.4、2.5、2.6、2.7之规定。
纤维蛋白原测定试剂盒(免疫比浊法)产品技术要求丹大
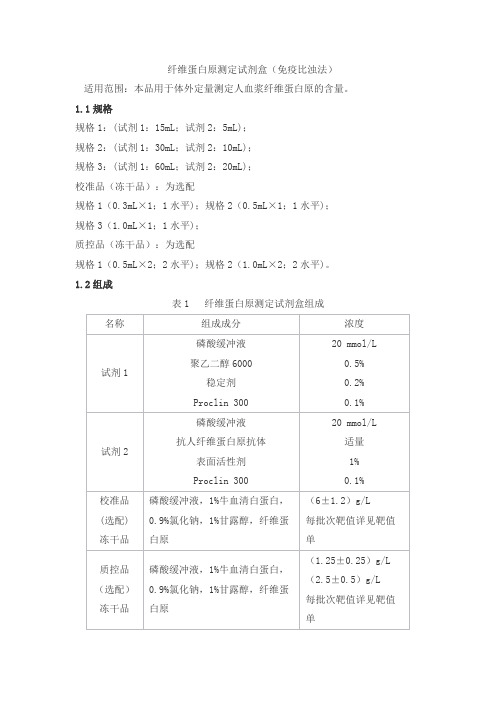
纤维蛋白原测定试剂盒(免疫比浊法)适用范围:本品用于体外定量测定人血浆纤维蛋白原的含量。
1.1规格规格1:(试剂1:15mL;试剂2:5mL);规格2:(试剂1:30mL;试剂2:10mL);规格3:(试剂1:60mL;试剂2:20mL);校准品(冻干品):为选配规格1(0.3mL×1;1水平);规格2(0.5mL×1;1水平);规格3(1.0mL×1;1水平);质控品(冻干品):为选配规格1(0.5mL×2;2水平);规格2(1.0mL×2;2水平)。
1.2组成表1 纤维蛋白原测定试剂盒组成2.1试剂2.1.1外观试剂盒外观应整洁,文字符号标识清晰;试剂1、试剂2为透明液体,不得有沉淀和絮状物。
2.1.2装量每瓶不少于标示值。
2.1.3试剂空白吸光度用指定的空白样品测试试剂(盒),在光径1cm下,在A340nm处测定试剂空白吸光度A≤0.2。
2.1.4分析灵敏度测定3.0g/L被测物,吸光度差值△A≥0.2。
2.1.5线性范围2.1.5.1在[0.1,8]g/L内,相关系数R≥0.990。
2.1.5.2在[0.1,2]g/L内,线性绝对偏差不超过±0.2g/L;(2,8] g/L内,线性相对偏差不超过±10%。
2.1.6 重复性重复测试(1.25±0.25)g/L和(2.5±0.5)g/L样本,所得结果的变异系数(CV%)应不大于8%。
2.1.7批间差测定(1.25±0.25)g/L和(2.5±0.5)g/L样本,所得结果的批间相对极差(R)应不大于10%。
2.1.8准确度)中加入一定体积高于8 g/L的纤维蛋白在正常浓度范围的临床样本(C)或由其配制的标准溶液,回收率应在90%-110%范围内。
原样品(Cs2.2校准品2.2.1外观校准品为冻干品。
2.2.2瓶间差瓶间差CV≤10%2.2.3准确度与配套试剂组成测试系统,指标要求同2.1.8。
纤维蛋白(原)降解产物测定试剂盒(胶乳免疫比浊法)产品技术要求zhongshengbeikong

纤维蛋白(原)降解产物测定试剂盒(胶乳免疫比浊法)适用范围:本试剂用于体外定量测定人血浆中纤维蛋白(原)降解产物的含量。
1.1规格液体双剂型试剂1(R1):60mL×2, 试剂2(R2):20mL×2;试剂1(R1):45mL×2, 试剂2(R2):15mL×2;试剂1(R1):15mL×2, 试剂2(R2):10mL×1;选配校准品:冻干粉型:1mL×1;选配质控品:冻干粉型 (2个水平):1mL×2。
1.2规格划分说明根据净含量、复溶体积划分规格。
1.3主要组成成分试剂盒由试剂1(R1)液体、试剂2(R2)液体、选配校准品冻干粉和选配质控品冻干粉组成。
1.3.1 试剂1(R1)液体:三羟甲基氨基甲烷缓冲液 20mmol/L1.3.2 试剂2(R2)液体:FDP抗体包被胶乳颗粒浓度随效价而定1.3.3 校准品冻干粉:人血浆基质纤维蛋白(原)降解产物 75μg/mL~100μg/mL(每批定值)1.3.4 质控品冻干粉:人血浆基质纤维蛋白(原)降解产物水平1:2μg/mL~10μg/mL;水平2:10μg/mL~50μg/mL。
(每批定值)2.1 外观试剂盒中各组件的外观应满足:a)试剂1(R1)应为无色透明溶液,无杂质、无絮状物,外包装完整无破损;b)试剂2(R2)应为白色乳浊液,无杂质、无絮状物,外包装完整无破损;c) 校准品应为白色或淡黄色冻干粉,复溶后应为白色或淡黄色溶液,无混浊,无未溶解物,外包装完整无破损;d) 质控品应为白色或淡黄色冻干粉,复溶后应为白色或淡黄色溶液,无混浊,无未溶解物,外包装完整无破损。
2.2 试剂空白吸光度在主波长570nm(540nm~600nm)(光径1cm)处,试剂空白吸光度(A)应≤1.800。
2.3.准确度测定纯品物质,回收率应在80%~120%范围内。
2.4分析灵敏度对应于浓度为10μg/mL的FDP所引起的吸光度差值(△A)的绝对值应在0.020~0.080的范围内。
纤维蛋白(原)降解产物(FDP)测定试剂盒(胶乳免疫比浊法)产品技术要求sainuopu

纤维蛋白(原)降解产物(FDP)测定试剂盒(胶乳免疫比浊法)产品技术要求sainuopu纤维蛋白(原)降解产物(FDP)测定试剂盒(胶乳免疫比浊法)适用范围:用于体外定量测定人体血浆中纤维蛋白/纤维蛋白原降解产物(FDP)的浓度。
1.1试剂盒包装规格试剂1:1×15ml,试剂2:1×5ml;试剂1:2×45ml,试剂2:2×15ml;试剂1:2×300ml,试剂2:1×200ml。
校准品(选配,冻干品):4×0.5ml(四水平);4×1ml(四水平);质控品(选配,冻干品):1×0.5ml;1×1ml;稀释液(选配):1×4ml,2×4ml。
1.2试剂盒主要组成成分2.1 外观液体双试剂:试剂1无色澄清液体;试剂2乳白色悬浊液。
校准品:冻干品,溶解后为无色至浅黄色透明液体。
质控品:冻干品,溶解后为无色至浅黄色透明液体。
稀释液:无色液体。
2.2 净含量液体试剂的净含量不得低于标示体积。
2.3 试剂空白吸光度在37℃、600nm波长、1cm光径条件下,试剂空白吸光度应不大于2.0。
2.4 分析灵敏度测定浓度为40mg/L样本时,吸光度变化的绝对值(|ΔA|)应在(0.01,0.5)范围内。
2.5 线性范围在(2.5,80)mg/L范围内,线性相关系数r不小于0.990;在(8,80)mg/L 区间内线性相对偏差应不大于±15%,(2.5,8] mg/L区间内线性绝对偏差不大于±1.2mg/L。
2.6 重复性重复测试两份高低浓度的样本,所得结果的变异系数(CV%)应不大于8%。
2.7 批间差不同批号试剂测试同一份样本,测定结果的批间相对极差应不大于10%。
2.8 准确度回收试验:回收率应在85%~115%。
2.9 质控品赋值有效性测定结果在靶值范围内。
2.10瓶间差(均一性)校准品和质控品瓶间变异系数(CV%)应不大于5%。
纤维蛋白原测定试剂盒(凝固法)产品技术要求万孚

纤维蛋白原测定试剂盒(凝固法)
型号、规格
以1人份/袋为基础包装,通用包装规格为:12人份/盒、24人份/盒、48人份/盒、100人份/盒、200人份/盒。
结构及组成
1.试剂盒由检测卡、ID芯片及使用说明书组成。检测卡由塑料基片、转子和基片反应区的凝血试剂组成。2.凝血试剂成分:由凝血酶和缓冲液组成,其比例为1:4。
2.4线性:
FIB试剂卡在测试范围内(1.5~6g/L),线性相关系数应大于0.98。
2.5重复性
用质控品重复测试所得结果的变异系数(CV)应不超过8%。
2.6批间差
用质控品重复测试不同批号试剂,所得结果变异系数(CV)应不超过15%。- 1 -
产品适用范围/预期用途
适用于体外检测人静脉全血中纤维蛋白原浓度。临床上主要用于弥散性血管内凝血、原发性纤溶症的辅助诊断以及溶栓疗效的监测。
2.性能指标
2.1外观
a)试剂盒外观应整洁,文字符号标识清晰;
b)各组分齐全,试剂卡无破损。
2.2装量
试剂卡份数应不少于标示量。
确度
用内控品测量,相对偏差应不超过±15%。
纤维蛋白(原)降解产物(FDP)测定试剂盒(胶乳免疫比浊法)产品技术要求百奥康泰

纤维蛋白(原)降解产物(FDP)测定试剂盒(胶乳免疫比浊法)适用范围:该产品用于体外定量测定人血清或血浆中的纤维蛋白(原)降解产物浓度。
1.1产品规格1.2 组成成分1.2.1 试剂组成试剂1:Tris缓冲液(pH=8.5) 50mmol/L 。
试剂2:抗人纤维蛋白(原)降解产物抗体包被的胶乳悬浊液<0.5%1.2.2校准品的组成五个水平的校准品,1号校准品为液体, 2-5号校准品为冻干品,校准品组成是在牛血清中(50g/L)加入含不同浓度的纤维蛋白(原)降解产物纯品,稳定剂<5%。
定值范围:0.0mg/L;(3-15)mg/L;(10-30)mg/L;(30-50)mg/L;(60-100)mg/L。
1.2.3质控品的组成单水平冻干质控品,在牛血清(50g/L)中加入纤维蛋白(原)降解产物纯品,稳定剂<5%。
目标浓度范围:(5-25)mg/L。
2.1 外观液体双试剂:试剂1:无色至淡黄色澄清液体;试剂2:乳白色液体。
校准品:1号校准品为无色或浅黄色液体;2号-5号校准品冻干品,溶解后为无色至浅黄色透明液体。
质控品:冻干品,溶解后为无色至浅黄色透明液体。
2.2 净含量液体试剂、校准、质控品的净含量不得低于标示体积。
2.3 试剂空白吸光度试剂空白吸光度应≤1.5。
2.4 分析灵敏度浓度为40mg/L时,吸光度差值的绝对值在≥0.01。
2.5 线性在[2.5,80]mg/L范围内,线性相关系数r应≥0.990;在[2.5,30]mg/L范围内绝对偏差不超过4 .5mg/L,在(30,80]mg/L范围内相对偏差不超过±15%。
2.6 精密度变异系数(CV)应≤8%。
2.7 批间差不同批号之间测定结果的相对极差应≤10%。
2.8 准确度:回收试验:回收率应在90%-110%之间。
2.9质控品赋值有效性测定值在质控靶值范围内2.10 批内瓶间差(均一性)校准品(2号-5号)瓶间重复性CV≤5%。
纤维蛋白(原)降解产物测定试剂盒(胶乳免疫比浊法)产品技术要求赛科希德

纤维蛋白(原)降解产物测定试剂盒(胶乳免疫比浊法)适用范围:本产品用于体外定量测定人血浆中纤维蛋白(原)降解产物(FDP)含量。
1.1 包装规格见表1。
表1 包装规格1.2 主要组成成分本产品由FDP试剂1、FDP试剂2组成。
FDP试剂1主要成分为2%三羟甲基氨基甲烷缓冲液、1‰苯甲酸钠;FDP试剂2主要成分为0.25%鼠抗人FDP单克隆抗体胶乳颗粒、0.5%牛血清白蛋白。
2.1 外观2.1.1 试剂盒包装完整,标签应清晰易识别。
2.1.2 FDP试剂1应为无色均匀液体,FDP试剂2应为白色均匀乳液。
2.2 空白吸光度试剂空白吸光度差值(△A)≤0.02。
2.3 灵敏度FDP 10μg/mL时,吸光度差值(△A)应≥0.100。
2.4 线性范围2.4.1在[2.5,40]μg/mL线性范围内,相关系数γ≥0.98。
2.4.2线性偏差:[2.5,5]μg/mL时绝对偏差不超过±0.5μg/mL,(5,40]μg/mL 时相对偏差不超过±10%。
2.5 准确度与已上市产品作比对,取40个[2.5,40]μg/mL浓度范围内不同浓度的人源样本,计算相关系数应≥0.975。
[2.5,5]μg/mL的样本绝对偏差不超过±0.5μg/mL,(5,40]μg/mL的样本相对偏差不超过±10%。
2.6 重复性用同一批号FDP试剂盒重复水平Ⅰ、水平Ⅱ两个水平的质控品,所得结果变异系数(CV)≤10%。
2.7 批间差批间极差≤8%。
2.8 装量FDP试剂盒中液体性状试剂的装量不少于其试剂瓶瓶签的标称量。
2.9 稳定性FDP试剂盒在2℃~8℃密闭的贮存条件下保存至有效期12个月后3个月内,产品的性能应符合2.1、2.2、2.3、2.4、2.5、2.6条规定的要求。
纤维蛋白(原)降解产物测定

纤维蛋白(原)降解产物测定纤维蛋白降解产物(fibrinogen degradation produce,FDP)是反映原发性和继发性纤溶的重要指标。
(一)检验原理乳胶凝集法。
用抗纤维蛋白(原)降解产物抗体包被的乳胶颗粒与待检血浆混合,阳性者出现肉眼可见的凝集物。
(二)检验方法学1.试剂及器材(1)鼠抗人FDP单抗包被的乳胶颗粒悬浮液。
(2)甘氨酸缓冲液。
(3)FDP阳性、阴性对照溶液。
(4)专用纸片反应板。
(5)混匀用塑料小棒。
2.检验方法(1)标本稀释:待检标本需先作两个稀释度:①1∶2:血浆50μl加甘氨酸缓冲液50μl。
②1∶8:血浆50μl加甘氨酸缓冲液350μl。
(2)加待检标本:每个稀释度各取20μl,加于纸片板的相邻环形圈内。
(3)加对照品:各取20μl阴、阳性对照品于各自环形圈内。
(4)加单克隆抗体:每个环形圈内各加20μl单抗抗体。
(5)混匀:每个环形圈各取一根混匀搅拌棒将2液混合,然后轻轻地旋转纸片板3分钟。
3.观察结果待测标本与阴、阳性对照比较,若2个稀释度均与阴性对照一样不产生凝集,则纤维蛋白(原)降解产物小于5mg/L;若1∶2出现凝集而1∶8不凝集,则5~20mg/L之间;若2个稀释度均出现凝集,则大于20mg/L。
(三)方法学评价本法的纤维蛋白(原)降解产物检测的阈值为2.5mg/L,超过1∶8阳性时,则其浓度大于2.5×8(稀释倍数);类风湿因子强阳性时可出现假阳性结果。
(四)质量保证1.试剂试剂应储存于2~8℃,用前取出置于室温5分钟方可使用;使用包被抗体的乳胶悬液用前须充分混匀。
2.标本保存待检血浆室温保存8小时,2~8℃24小时,-20℃1个月。
(五)参考范围<5mg/L。
(六)临床意义FDP增高见于原发性纤溶亢进时,也可见于高凝状态、弥散性血管内凝血、肺栓塞、器官移植后的排异反应、妊娠期高血压疾病、恶性肿瘤、心、肝、肾疾病及静脉血栓、溶栓治疗等所致的继发性纤溶亢进。
纤维蛋白原降解产物测定试剂盒 (胶乳免疫比浊法)产品技术要求lepu

纤维蛋白原降解产物测定试剂盒 (胶乳免疫比浊法)适用范围:用于体外定量测定人血浆中纤维蛋白(原)降解产物的浓度。
1.1规格试剂1: 1×60mL,试剂2: 1×60mL;试剂1: 4×60mL,试剂2: 4×60mL;试剂1:2×45mL,试剂2:2×15mL;试剂1:1×45mL,试剂2:1×15mL。
1.2主要组成成分试剂1主要组分:试剂2主要组分:2.1 净含量应不低于试剂瓶标示装量。
2.2 外观试剂1:无色透明溶液,试剂2:乳白色溶液。
外包装完好、无破损,标签完好、字迹清晰。
2.3 试剂空白在570nm处测定试剂空白吸光度,应<1.8。
2.4 分析灵敏度测试100μg/mL的被测物时,吸光度变化(ΔA)应不低于0.01。
2.5 准确度参照EP9-A2的方法,用比对试剂盒同时测试40例线性区间内的不同浓度的血浆样本。
其相关系数(r)不小于0.990。
每个浓度点[2.5,18]μg/mL区间内绝对偏差不超过±2.7μg/mL;(18,120]μg/ml区间内相对偏差不超过±15%。
2.6 重复性变异系数(CV)应不超过13%。
2.7 线性2.7.1 在[2.5,120]μg/mL区间内,线性回归的相关系数r应不低于0.990;2.7.2 [2.5,18]μg/mL区间内绝对偏差不超过±2.7μg/mL;(18,120]μg/ml 区间内相对偏差不超过±15%。
2.8 批间差对同一份样品进行重复测定,相对极差<15%。
2.9 稳定性取在2℃~8℃条件下贮存达到12个月后的试剂进行检测,应符合本标准2.2、2.3、2.4、2.5、2.6、2.7之规定。
纤维蛋白原降解产物测定试剂盒(胶乳免疫比浊法)产品技术要求haifeng

纤维蛋白原降解产物测定试剂盒(胶乳免疫比浊法)适用范围:本产品适用于体外定量测定人血浆中的纤维蛋白原降解产物含量。
1.1 产品规格1.2主要组成成分注:校准品、质控品具有批间、赋值特异性,具体值详见靶值单。
2.1外观2.1.1试剂盒标签标识清晰,外包装完整无破损;2.1.2试剂1为无色澄清液体,目测不得有任何沉淀及絮状悬浮物;2.1.3试剂2为乳白色液体,目测不得有任何沉淀及絮状悬浮物;2.1.4校准品:无色或浅黄色干粉,复溶后不得有任何沉淀及絮状悬浮物;2.1.5质控品:无色或浅黄色干粉,复溶后不得有任何沉淀及絮状悬浮物。
2.2净含量净含量不低于标示值。
2.3空白吸光度在波长570nm、37℃条件下,试剂空白吸光度A≤1.5。
2.4线性范围(2,80)μg/mL范围内,相关系数r≥0.990;(2,20]μg/mL范围内,绝对偏差不超过±3μg/mL;(20,80)μg/mL范围内,相对偏差不超过±15.0%。
2.5分析灵敏度在产品说明书规定参数设定条件下,测定浓度为20μg/mL的样本, 吸光度变化△A≥0.01。
2.6 精密度2.6.1批内重复性CV≤10.0%。
2.6.2 批间差相对极差R≤10.0%。
2.7 准确度与已上市产品比对:(2,80)μg/mL范围内,相关系数r≥0.990;(2,20] μg/mL范围内,绝对偏差不超过±3μg/mL;(20,80)μg/mL范围内,相对偏差不超过±15.0%。
2.8 校准品2.8.1 均一性:CV≤5.0%。
2.8.2 瓶间差:CV≤5.0%。
2.8.3 开瓶稳定性:开瓶后3天,相对偏差不超过±10.0%。
2.9 质控品2.9.1赋值有效性:测定值在质控靶值范围内。
2.9.2 均一性:CV≤10.0%。
2.9.3 瓶间差:CV≤10.0%。
2.9.4 开瓶稳定性:开瓶后3天,测定值在质控靶值范围内。
纤维蛋白(原)降解产物(FDP)测定试剂盒(免疫散射比浊法)产品技术要求参考版

医疗器械产品技术要求编号:
纤维蛋白(原)降解产物(FDP)测定试剂盒
(免疫散射比浊法)
1. 产品型号/规格及其划分说明
1.1 型号规格
6600A
1.2 型号规格划分说明
由缓冲液、抗血清、质控品(选购)、校准品(选购)、磁卡、搅拌子(选配)组成。
1.3 适用范围
用于体外定量测定人血浆中纤维蛋白(原)降解产物(FDP)的含量。
2性能指标
2.1外观和性状
外观和性状应符合表2要求
表 2 试剂盒内各组成的外观性状
2.2装量
液体试剂的净含量应不少于下表各包装规格试剂盒上的标示值。
2.3空白限
试剂空白限不大于2.5 mg/L。
2.4线性范围
2.4.1试剂盒在2.5 mg/L~80 mg/L 区间范围内,其回归系数r ≥ 0.990。
2.4.2线性的相对偏差或绝对偏差应符合表3 的要求。
表 3 线性相对偏差或绝对偏差
2.5测量精密度
2.5.1试剂盒批内精密度CV ≤ 10%。
2.5.2试剂盒批间相对极差R ≤ 10%。
2.6准确度
相对偏差(Bias%)应在参考物质靶值±15%范围以内。
2.7校准品准确度
相对偏差(Bias%)应在±15%以内。
2.8质控品预期结果
质控品的测试结果应在质控范围内。
2.9校准品均一性
CV 应≤ 10% 。
2.10质控品均匀性
CV 应≤ 10% 。
以下内容为空白。
纤维蛋白(原)降解产物(FDP)测定试剂盒(乳胶免疫比浊法)产品技术要求meichuang

纤维蛋白(原)降解产物(FDP)测定试剂盒(乳胶免疫比浊法)适用范围:用于体外定量检测人血浆中的纤维蛋(原)降解产物(FDP)的浓度。
1.1 包装规格乳胶试剂:1×3ml、Tris缓冲液:1×7ml、氯化钠溶液:1×5ml;乳胶试剂:2×3ml、Tris缓冲液:2×7ml、氯化钠溶液:2×5ml;乳胶试剂:1×4.5ml、Tris缓冲液:1×10ml、氯化钠溶液:1×10ml;乳胶试剂:2×4.5ml、Tris缓冲液:2×10ml、氯化钠溶液:2×10ml;乳胶试剂:1×6ml、Tris缓冲液:1×12ml、氯化钠溶液:1×12ml;乳胶试剂:2×6ml、Tris缓冲液:2×12ml、氯化钠溶液:2×12ml。
1.2 主要成份2.1 外观a)试剂盒外观应该整洁,文字符号标识清晰,包装无破损。
b)乳胶试剂为乳白色悬浊液。
c)Tris缓冲液为无色透明液体。
d)氯化钠溶液为无色透明液体。
2.2 装量各组成成分的装量应不低于产品标示量。
2.3 准确性比对试验,待测试剂盒与比对试剂盒做线性回归,其线性相关系数r>0.98,并满足以下条件:(2.5, 10]ug/ml浓度区间绝对偏差不大于±1ug/ml,[10, 120)ug/ml浓度区间相对偏差不大于±10%。
2.4 线性测定试剂在(2.5,120)ug/ml范围内,线性相关系数应r>0.98。
2.5 重复性用低值质控血浆和高值质控血浆重复测定所得结果的变异系数(CV)应≤10%。
2.6 批间差用三个不同批号的试剂测试低质控血浆,所得结果的变异系数(CV)≤14%。
2.7 稳定性a)开瓶稳定性:开瓶后样品在2℃~8℃条件下,保存24小时,取该样品检测外观、准确性应符合2.1、2.3的要求。
纤维蛋白 纤维蛋白原降解产物测定试剂盒(乳胶免疫比浊法)产品技术要求sjwd

纤维蛋白/纤维蛋白原降解产物测定试剂盒(乳胶免疫比浊法)适用范围:用于体外定量测定血浆中纤维蛋白/纤维蛋白原降解产物(FDP)的含量。
1.1包装规格校准品(选配): 1.0mL×1;1.0mL×2;1.0mL×5质控品(选配): 1.0mL×1;1.0mL×2;1.0mL×51.2主要组成成分2.1 外观试剂1为无色或淡黄色澄清液体,试剂2为乳白色液体;校准品、质控品为白色冻干品,复溶后为无色澄清液体;试剂盒标签标识清晰,外包装完整无损。
2.2 装量试剂液体成分的装量不少于瓶签标示量。
2.3 试剂空白在546nm处测定试剂空白吸光度应≤1.8。
2.4 分析灵敏度测试10mg/L的被测物时,吸光度变化(ΔA)应≥0.002。
2.5 空白限试剂盒的空白限≤0.2mg/L。
2.6 准确度待检系统与比对系统测值的相关系数(r)不小于0.975;在[1,14] mg/L区间内,绝对偏差不超过±1.68mg/L;在(14,120]mg/L区间内,相对偏差应不超过±12%。
2.7 线性2.7.1在[1,120]mg/L区间内,线性相关系数r≥0.990;2.7.2在[1,14]mg/L区间内,线性绝对偏差应不超过±1.68mg/L;在(14,120]mg/L区间内,线性相对偏差应不超过±12%。
2.8 精密度2.8.1 重复性测试高、低两浓度样本,其结果的变异系数CV≤10%。
2.8.2 批间差随机抽取三批试剂盒测试同一份样本,批间相对极差(R)≤10%。
2.8.3 瓶内均匀性校准品、质控品的瓶内变异系数CV≤10%。
2.8.4 瓶间均匀性校准品、质控品瓶间变异系数CV≤10%。
2.9质控品的赋值有效性质控品检测结果应在其质控范围内。
2.10 校准品溯源性按照GB/T 21415-2008《体外诊断医疗器械生物样品中量的测量校准物和控制物质赋值的计量学溯源性》及有关规定建立溯源性,提供校准品的来源、赋值过程及测量不确定度等内容,溯源至公司内部工作校准品,并与已上市产品比对赋值。
纤维蛋白(原)降解产物测定试剂盒(胶乳免疫比浊法)产品技术要求jiuqiang

纤维蛋白(原)降解产物测定试剂盒(胶乳免疫比浊法)适用范围:用于体外定量测定人血浆或血清中纤维蛋白(原)降解产物的含量。
1. 产品型号/规格及其划分说明包装规格见表1。
表1 包装规格2.1 外观试剂1为无色澄清液体,目测不得有任何沉淀及絮状悬浮物;试剂2为乳白色液体,目测不得有任何沉淀及絮状悬浮物;校准品稀释液为无色或淡黄色澄清液体,目测不得有任何沉淀及絮状悬浮物;校准品为白色或黄色粉末状物质,复溶后为无色或黄色澄清液体,目测不得有任何沉淀及絮状悬浮物;质控品为白色或黄色粉末状物质,复溶后为无色或黄色澄清液体,目测不得有任何沉淀及絮状悬浮物。
试剂盒标签标识清晰,外包装完整无损。
2.2 净含量试剂的净含量应不少于标称量。
2.3 试剂空白吸光度A600nm下测定空白吸光度应≤ 2.0000。
2.4 准确度与已上市产品进行比对试验:相关系数r≥0.975,在[2.5,15]μg/ml 区间内测定的偏差应不超过±1.5 μg/ml,在(15,80]μg/ml区间内测定的偏差应不超过±10%。
2.5 分析灵敏度样本浓度为20 μg/ml时,其吸光度变化在0.0100~0.1000之间。
2.6 线性范围在[2.5,80]μg/ml区间内,线性相关系数r≥0.99,在[2.5,15]μg/ml区间内测定的线性偏差应不超过±1.5 μg/ml,在(15,80]μg/ml区间内测定的线性偏差应不超过±10%。
2.7 测量精密度2.7.1 重复性对不同浓度的同一血清样本或质控品重复测定10次,其测定值的变异系数(CV%)应不大于10%。
2.7.2 批间差随机抽取三批试剂盒的批间相对极差(R)应不大于10%。
2.8 瓶间精密度校准品、质控品的瓶间精密度应≤10%。
2.9 稳定性2.9.1 试剂稳定性试剂盒在2℃~8℃密封避光保存,有效期为12个月。
在试剂盒有效期满后一个月以内,应符合2.1、2.3、2.4、2.5、2.6、2.7.1的要求。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
纤维蛋白/纤维蛋白原降解产物测定试剂盒(乳胶免疫比浊法)
适用范围:用于体外定量测定血浆中纤维蛋白/纤维蛋白原降解产物(FDP)的含量。
1.1包装规格
校准品(选配): 1.0mL×1;1.0mL×2;1.0mL×5
质控品(选配): 1.0mL×1;1.0mL×2;1.0mL×5
1.2主要组成成分
2.1 外观
试剂1为无色或淡黄色澄清液体,试剂2为乳白色液体;
校准品、质控品为白色冻干品,复溶后为无色澄清液体;
试剂盒标签标识清晰,外包装完整无损。
2.2 装量
试剂液体成分的装量不少于瓶签标示量。
2.3 试剂空白
在546nm处测定试剂空白吸光度应≤1.8。
2.4 分析灵敏度
测试10mg/L的被测物时,吸光度变化(ΔA)应≥0.002。
2.5 空白限
试剂盒的空白限≤0.2mg/L。
2.6 准确度
待检系统与比对系统测值的相关系数(r)不小于0.975;
在[1,14] mg/L区间内,绝对偏差不超过±1.68mg/L;
在(14,120]mg/L区间内,相对偏差应不超过±12%。
2.7 线性
2.7.1在[1,120]mg/L区间内,线性相关系数r≥0.990;
2.7.2在[1,14]mg/L区间内,线性绝对偏差应不超过±1.68mg/L;
在(14,120]mg/L区间内,线性相对偏差应不超过±12%。
2.8 精密度
2.8.1 重复性
测试高、低两浓度样本,其结果的变异系数CV≤10%。
2.8.2 批间差
随机抽取三批试剂盒测试同一份样本,批间相对极差(R)≤10%。
2.8.3 瓶内均匀性
校准品、质控品的瓶内变异系数CV≤10%。
2.8.4 瓶间均匀性
校准品、质控品瓶间变异系数CV≤10%。
2.9质控品的赋值有效性
质控品检测结果应在其质控范围内。
2.10 校准品溯源性
按照GB/T 21415-2008《体外诊断医疗器械生物样品中量的测量校准物和控制物质赋值的计量学溯源性》及有关规定建立溯源性,提供校准品的来源、赋值过程及测量不确定度等内容,溯源至公司内部工作校准品,并与已上市产品比对赋
值。
2.11 稳定性
2.11.1效期稳定性
该产品在2℃~8℃条件下贮存有效期为12个月,取有效期满后2个月内产品进行检测,应符合2.1、2.3、2.4、2.5、2.6、2.7、2.8.1、2.8.3、2.9的规定。
2.11.2复溶稳定性
复溶后校准品、质控品在2℃~8℃条件下密闭贮存,可稳定7天。
在有效期满后2天内,校准品的检测结果应符合2.6、2.7的规定,质控品的检测结果应符合2.9的规定。
