高考化学高无机综合推断(大题培优)
高考化学 高无机综合推断 培优易错试卷练习(含答案)含答案(1)
高考化学高无机综合推断培优易错试卷练习(含答案)含答案(1)一、无机综合推断1.中学化学中的一些常见物质有如图转化关系。
其中A、H为空气中的主要成分,气体B 能使湿润的红色石蕊试纸变蓝,气体D遇到A很快变成红棕色E,C是黑色金属氧化物,I 是紫红色金属单质。
X为常见液体(部分反应条件及生成物没有全部列出)。
回答下列问题:(1)B的化学式为________ C的化学式为___________D的化学式为___________(2)B的实验室制法的化学方程式____________________(3)写出反应①的化学方程式_______________________。
(4)写出反应②的离子方程式_______________________。
【答案】NH3 CuO NO 2NH4Cl+Ca(OH)2CaCl2+2NH3↑+2H2O4NH3+5O24NO+6H2O 3Cu+8H++2NO3—=3Cu2++NO↑+4H2O【解析】【分析】A、H为空气中主要成分,分别为N2、O2中的一种,气体B能使湿润的红色石蕊试纸变蓝,则B为NH3,A能与氨气反应生成D与X,X为常见液体,气体D遇到A很快变成红棕色E,可推知A为O2,H为N2,D为NO,X为H2O,E为NO2,E与X反应生成F,I是紫红色金属单质,应为Cu,F与Cu反应得到G、X(水)、D(NO),故为HNO3,G为Cu(NO3)2.C属于氧化物,与B(NH3)反应得到X(水)、H(氮气)、I(Cu),根据元素守恒可知C 为CuO,据此解答。
【详解】A、H为空气中主要成分,分别为N2、O2中的一种,气体B能使湿润的红色石蕊试纸变蓝,则B为NH3,A能与氨气反应生成D与X,X为常见液体,气体D遇到A很快变成红棕色E,可推知A为O2,H为N2,D为NO,X为H2O,E为NO2,E与X反应生成F,I是紫红色金属单质,应为Cu,F与Cu反应得到G、X(水)、D(NO),故为HNO3,G为Cu(NO3)2.C属于氧化物,与B(NH3)反应得到X(水)、H(氮气)、I(Cu),根据元素守恒可知C 为CuO;(1)由上述分析可知,B的化学式为NH3;C的化学式为CuO;D的化学式为NO;(2)实验室利用氯化铵和氢氧化钙固体混合加热制NH3,发生反应的化学方程式为2NH4Cl+Ca(OH)2CaCl2+2NH3↑+2H2O;(3)反应①为氨的催化氧化,发生反应的化学方程式为4NH3+5O24NO+6H2O;(4)反应②为Cu溶于稀硝酸生成NO,发生反应的离子方程式为3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O。
2020-2021高考化学培优(含解析)之高无机综合推断含答案解析

2020-2021高考化学培优(含解析)之高无机综合推断含答案解析一、无机综合推断1.固体X由四种元素组成,为探究其组成和性质,设计并完成如下实验:(1)固体X中含有H、O、______和______元素。
(2)写出固体X受热分解的化学方程式______。
(3)取少量固体B溶于稀硫酸,加入适量的KI溶液,反应后溶液显棕黄色,同时产生一种白色的碘化物沉淀,写出产生该现象的离子方程式______。
【答案】C Cu Cu3(OH)2(CO3)23CuO+H2O+2CO2↑ 2Cu2++4I-=2CuI↓+I2【解析】【分析】由固体隔绝空气加热生成1.8g水可知,含H原子的物质的量n=1.8g/18g∙mol-1×2=0.2mol,质量为0.2g;气体A与石灰水反应生成白色沉淀为碳酸钙,其物质的量n=20.0g/100g∙mol-1=0.2mol,所以碳原子的物质的质量为m=0.2mol×12g/mol=2.4g;固体B与CO反应生成紫红色固体为Cu,则B为CuO,其物质的量为24.0g/80g∙mol-1=0.3mol,所以铜的质量为m=0.3mol×64g/mol=19.6g;剩余质量为34.6g-0.2g-2.4g-19.6g=12.4g,所以X中含O为n=12.4g/16g∙mol-1=0.8mol,则n(Cu):n(C):n (H):n(O)=3:2:2:8,X为Cu3(OH)2(CO3)2,以此来解答。
【详解】(1)由上述分析可知,固体X中含有H、O、C、Cu元素,故答案为:C;Cu;(2)固体X受热分解的化学方程式为Cu3(OH)2(CO3)23CuO+H2O+2CO2↑,故答案为:Cu3(OH)2(CO3)23CuO+H2O+2CO2↑;(3)取少量固体B溶于稀硫酸,生成硫酸铜,加入适量的KI溶液,反应后溶液显棕黄色,同时产生一种白色的碘化物沉淀,可知生成碘和CuI,产生该现象的离子方程式为2Cu2++4I-=2CuI↓+I2,故答案为:2Cu2++4I-=2CuI↓+I2。
高考化学高无机综合推断(大题培优)及答案解析

高考化学高无机综合推断(大题培优)及答案解析一、无机综合推断1.X、Y、Z三种主族元素,原子序数依次增大且原子序数小于10,它们的单质在常温下都是常见的无色气体,在适当条件下,三者之间可以两两发生反应生成分别是双原子、三原子和四原子的甲、乙、丙三种分子,且乙、丙分子中含有X元素的原子个数比为2∶3。
请回答下列问题:(1)元素X的名称是______,丙分子的电子式为______。
(2)若甲与Y单质在常温下混合就有明显现象,则甲的化学式为________。
丙在一定条件下转化为甲和乙的反应方程式为____________________________________________。
(3)化合物丁含X、Y、Z三种元素,丁是一种常见的强酸,将丁与丙按物质的量之比1∶1混合后所得物质戊的晶体结构中含有的化学键为________(选填序号)。
a.只含共价键 b.只含离子键 c.既含离子键,又含共价键【答案】氢 NO 4NH3+5O24NO+6H2O C【解析】【分析】由X、Y、Z三种主族元素,原子序数依次增大且原子序数小于10,它们的单质在常温下都是常见的无色气体可知,三种气体单质为氢气、氮气、氧气,X为H元素、Y为N元素、Z 为O元素,由在适当条件下,三者之间可以两两发生反应生成分别是双原子、三原子和四原子的甲、乙、丙三种分子,且乙、丙分子中含有X元素的原子个数比为2∶3可知,甲为NO、乙为H2O、丙为NH3。
【详解】(1)元素X为H元素,名称为氢;丙为共价化合物NH3,电子式为,故答案为氢;;(2)甲为无色气体NO,NO与氧气反应生成红棕色的二氧化氮;氨气与氧气发生催化氧化反应生成一氧化氮和水,反应的化学方程式为4NH3+5O2 4NO+6H2O,故答案为4NH3+5O24NO+6H2O;(3)由化合物丁是一种含H、O、N三种元素的强酸可知,丁为HNO3,HNO3与NH3按物质的量之比1:1混合反应生成NH4NO3,NH4NO3为离子化合物,含有离子键和共价键,故答案为C。
高考化学高无机综合推断(大题培优)及答案(1)

高考化学高无机综合推断(大题培优)及答案(1)一、无机综合推断1.下列各物质是中学化学中常见的物质,甲为常见金属单质,乙、丙、丁是非金属单质,其它为化合物,B、D分别为黑色粉末和黑色晶体,G为淡黄色固体,J为生活中常见的调味品,I为红褐色固体,①是实验室制取丁的反应之一,F为棕黄色溶液。
各物质间的转化如下图所示,回答下列各问题(部分生成物未列出):(1)A的电子式:___________________;(2)写出甲与C反应的化学方程式:________________________________;(3)在F和E的混合溶液中用___________试剂(填化学式)检验E中阳离子;(4)整个转换过程中属于氧化还原反应的有___________个;(5)写出反应③E与G按物质的量之比2:1的反应的离子方程式___________________。
【答案】3Fe + 4H2O(g) Fe3O4 + 4H2KMnO46个6Fe2+ + 3Na2O2 + 6H2O = 4Fe(OH)3↓ + 2Fe3+ + 6Na+【解析】【分析】由题意可知,G为淡黄色固体化合物,J为生活中常见的调味品,则G是Na2O2, J为NaCl;I为红褐色固体,则I是氢氧化铁,甲是Fe单质;B、D分别为黑色粉末和黑色晶体,Fe与物质C发生置换反应生成另一种非金属单质,根据Fe与水蒸气在高温条件下反应生成氢气和黑色固体四氧化三铁可知C是水,乙是氢气,D是Fe3O4;A与B反应生成水和一种非金属单质,且①是实验室制取丁的反应之一,判断A是过氧化氢,B是二氧化锰,过氧化氢在二氧化锰做催化剂作用下发生分解反应生成水和氧气,所以丁是氧气;四氧化三铁与K反应生成两种物质E、F,可以相互转化,则K是盐酸,盐酸与四氧化三铁反应生成氯化亚铁和氯化铁,F与Fe反应生成E,则F是氯化铁,E是氯化亚铁,氯化铁与过氧化钠反应生成氢氧化铁、氯化钠、氧气,氯化亚铁与一定量的过氧化钠反应生成氯化铁、氢氧化铁、氯化钠。
高考化学 高无机综合推断 培优练习(含答案)含详细答案

高考化学高无机综合推断培优练习(含答案)含详细答案一、无机综合推断1.某新型无机材料A3M4由两种非金属元素组成,元素M位于第二周期V A族。
D、E、H 均为难溶于水的白色固体:化合物C、E均含A元素。
其余物质均为中学化学中常见物质。
请回答:(1)写出H的化学式:________________。
(2)化合物A3M4中含有的化学键类型为:________________。
(3)写出反应②的离子方程式:________________。
【答案】AgCl共价键SiO2+2OH- = SiO32-+H2O【解析】根据题中各物质转化关系,D受热得E,E能与氢氧化钠反应生成F,F与过量的二氧化碳反应生成D,说明D为弱酸且能受热分解;新型无机材料A3M4由两种非金属元素组成,元素M位于第二周期VA族,应为N元素,A元素为四价元素,C、E均为含A元素,可知A3M4应为Si3N4,可以确定A为Si,E为SiO2,F为Na2SiO3,则D为H2SiO3,G与硝酸银反应生成不溶于稀硝酸的沉淀H,则可知G中有Cl-,H为AgCl,故C为SiCl4,B为Cl2;由SiCl4+3H2═4HCl+H2SiO3,生成G:HCl;(1)H的化学式为AgCl;(2)化合物Si3N4中含有的化学键类型为共价键;(3)SiO2溶解于NaOH溶液发生反应的离子方程式为SiO2+2OH- = SiO32-+H2O。
2.现有稀硫酸、纯碱、二氧化碳、铜片、食盐、生石灰、铁片和木炭粉8种物质。
(1)在这8种物质中,属于电解质的有_____________(用相应的化学式表示,下同)。
(2)这8种物质中的某5种存在下面的相互关系,选择适当的物质填入①~⑤,使有连线的两种物质能发生反应,并回答下列问题。
①它们的化学式分别为:①______________;③____________;⑤______________。
②如果连线对应的反应分别用A、B、C、D、E表示。
高考化学培优(含解析)之高无机综合推断含答案

高考化学培优(含解析)之高无机综合推断含答案一、无机综合推断1.A、B、C、W均为中学常见的物质,它们之间有如图所示的转化关系(其他产物及反应条件已略去,反应可以在水溶液中进行)。
X、Y、Z、W均为中学化学的常见物质,一定条件下它们之间有如下转化关系:(1)若A、B、C三种物质都含有一种金属元素,且B为两性物质,W俗称苛性钠。
①A、B、C三种物质中所含有的金属元素单质与W反应的化学方程式为_______________。
②A溶液一步转化为C溶液的反应离子方程式为________________。
(2)若X是一种黄绿色的气体,Y的饱和溶液滴入沸水中能生成红褐色胶体。
①检验溶液Z是否变质最灵敏的一种试剂是____________________(名称);②一定条件下W与水反应的化学方程式_______________________________。
(3)X常温下为气体化合物,Z是一种红棕色气体,X气体的检验方法____________________,X转化为Y的化学方程式为______________________;(4)X为一元强碱溶液,W是形成酸雨的主要气体。
①则Y到Z的离子方程式为________________________________________;②请画出向含0.01molX和0.01molY的溶液中逐滴加入0.1mol/L稀盐酸的体积和生成气体的物质的量的关系的图像___________。
【答案】2Al+2NaOH+2H2O =2NaAlO2 +H2 Al3-+ 4OH- =AlO2- + 2H2O 硫氰化钾溶液 3Fe + 4H2O(g) === Fe3O4 + 4H2使湿润的红色石蕊试纸变蓝(或遇蘸有浓盐酸的玻璃棒产生白烟)4NH3+5O24NO+6H2O SO32-+SO2+H2O=2HSO3-【解析】【分析】W为NaOH。
B为两性物质且含有一种金属元素,确定该金属元素为铝元素,因在溶液中产生了B,所以B为Al(OH)3。
高考化学高无机综合推断(大题培优 易错 难题)

高考化学高无机综合推断(大题培优易错难题)一、无机综合推断1.现有H、N、O、Na、S、Cl、Fe、Cu八种常见元素,回答下列问题:(1)Cl在周期表中的位置____________________;(2)Na+离子的结构示意图为__________________;(3)能说明非金属性Cl比S强的事实是_____________(用化学方程式表示);(4)物质A~L是由上述八种元素中的一种、二种或三种组成,A的摩尔质量166g·mol-1,其焰色反应呈黄色;B是最常见的液体;C中两元素的质量比为96∶7; D、E都为氢氧化物,E呈红褐色。
F、G、H、I为单质,其中F、G是无色气体,H是紫红色固体,I是黄绿色气体;L是常见的强酸。
它们有如下图所示的关系(部分反应条件及产物已略去):①C的化学式为____________________;②D的电子式为____________________;③L的稀溶液与H反应的离子方程式为_________________;④反应(a)的化学方程式为_______________。
【答案】第3周期ⅦA族 Cl2+H2S=S↓+2HCl Cu3N 3Cu + 8H++2NO3-=3Cu2++2NO↑+4H2O 4Na2FeO4 +10H2O = 4Fe(OH)3↓+8NaOH + 3O2↑【解析】【分析】前三问考查了元素周期表中“位构性”三者关系,后一问为无机推断大题,其推导思路: B 是最常见的液体则为水;E呈红褐色为氢氧化铁,D、E属同类物质,且D应该也含有钠元素故为氢氧化钠;F、G、H、I为单质,其中F、G是无色气体,H是紫红色固体即为Cu,C 中两元素的质量比为96:7,C分解得到G和H,可知生成Cu和氮气,故C为Cu3N,G为氮气;氮气与氧气放电生成NO,故F为氧气,J为一氧化氮,与氧气反应生成K为二氧化氮,二氧化氮与水反应生成L是常见的强酸硝酸;I是黄绿色气体则为氯气;A的摩尔质量为166g·mol-1,其焰色反应呈黄色,则含有钠元素,结合D、E、F可推知A为Na2FeO4。
高考化学 高无机综合推断 培优练习(含答案)及答案

高考化学高无机综合推断培优练习(含答案)及答案一、无机综合推断1.已知A、B、C、D是元素周期表中的四种短周期元素,A分别与B、C、D结合生成三种化合物:甲、乙、丙。
甲、乙、丙三种化合物的分子中含有相同数目的电子;丙与甲、乙均能发生化学反应,且甲、丙为无色有不同刺激性气味的物质,化合物丁与C的某种单质在常温下反应可生成红棕色气体;B、C、D三种元素的单质与甲、乙、丁三种化合物之间存在如图所示的转化关系(反应条件已略去):(1)D在元素周期表中的位置为________________。
(2)B、C、D的原子半径的大小关系为________(用元素符号表示)。
(3)丁与C的单质在常温下反应的化学方程式为______________。
(4)甲、乙、丙分子中的电子数均为________,实验室如何检验丙_______ 。
(5)C的单质+丙→乙+丁的化学方程式为_______________。
【答案】第2周期ⅤA族 N>O>F 2NO+O2===2NO2 10 能使湿润的红色石蕊试纸变蓝色 5O2+4NH36H2O+4NO【解析】【分析】本题有几个重要的突破口:①甲、乙、丙三种化合物的分子中含有相同数目的电子;②丙为无色有不同刺激性气味的物质;③化合物丁与C的某种单质在常温下反应可生成红棕色气体,说明丁为NO,C的某种单质可能为O2。
【详解】A、B、C、D是元素周期表中的四种短周期元素,A分别与B、C、D结合生成三种化合物:甲、乙、丙。
化合物丁与C的某种单质在常温下反应可生成红棕色气体,则丁为NO、C为O元素;丙与甲、乙均能发生化学反应,且甲、丙为无色有不同刺激性气味的物质,由图中信息可知,丙与O元素的单质反应生成NO,也可以由O的单质与D的单质化合而得,则丙为NH3、D为N元素,乙为H2O;甲、乙、丙三种化合物的分子中含有相同数目的电子,则其都有10个电子,结合图中信息,B的单质可以与H2O反应生成甲和O 元素的单质,故甲为HF、B为F元素。
高考化学二轮高无机综合推断专项培优附详细答案
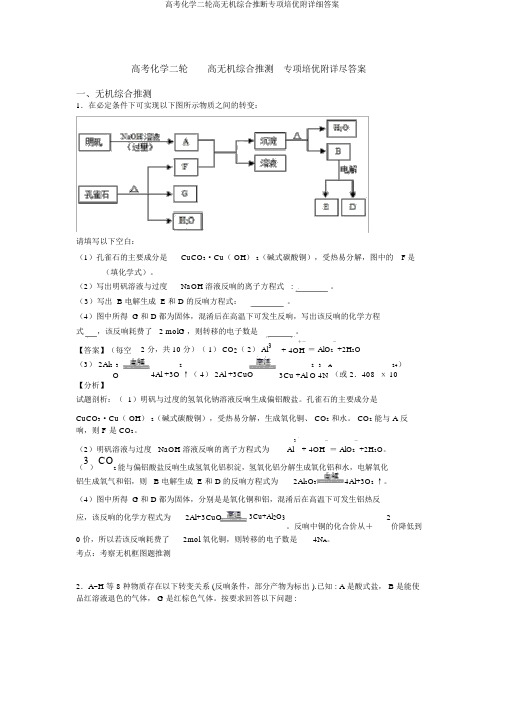
高考化学二轮高无机综合推测专项培优附详尽答案一、无机综合推测1.在必定条件下可实现以下图所示物质之间的转变:请填写以下空白:(1)孔雀石的主要成分是CuCO3·Cu( OH)2(碱式碳酸铜),受热易分解,图中的 F 是______(填化学式)。
(2)写出明矾溶液与过度NaOH 溶液反响的离子方程式 :。
(3)写出 B 电解生成 E 和 D 的反响方程式:。
(4)图中所得 G 和 D 都为固体,混淆后在高温下可发生反响,写出该反响的化学方程式,该反响耗费了 2 molG ,则转移的电子数是。
【答案】(每空 2 分,共 10 分)( 1) CO2( 2) Al3+--+ 4OH= AlO2 +2H2O(3) 2Al2 32 2 3A24)O4Al +3O ↑( 4) 2Al +3CuO3Cu +Al O 4N(或 2.408х 10【分析】试题剖析:( 1)明矾与过度的氢氧化钠溶液反响生成偏铝酸盐。
孔雀石的主要成分是CuCO3·Cu( OH)2(碱式碳酸铜),受热易分解,生成氧化铜、 CO2和水。
CO2能与 A 反响,则 F 是 CO2。
(2)明矾溶液与过度 NaOH 溶液反响的离子方程式为3+--Al+ 4OH= AlO2 +2H2O。
(3)CO2 能与偏铝酸盐反响生成氢氧化铝积淀,氢氧化铝分解生成氧化铝和水,电解氧化铝生成氧气和铝,则 B 电解生成 E 和 D 的反响方程式为2Al2O34Al+3O2↑。
(4)图中所得 G 和 D 都为固体,分别是是氧化铜和铝,混淆后在高温下可发生铝热反应,该反响的化学方程式为2Al+3CuO3Cu+Al2O32价降低到。
反响中铜的化合价从+0 价,所以若该反响耗费了2mol 氧化铜,则转移的电子数是4N A。
考点:考察无机框图题推测2.A~H 等 8 种物质存在以下转变关系 (反响条件,部分产物为标出 ).已知 : A 是酸式盐, B 是能使品红溶液退色的气体, G 是红棕色气体。
高考化学高无机综合推断(大题培优)及详细答案
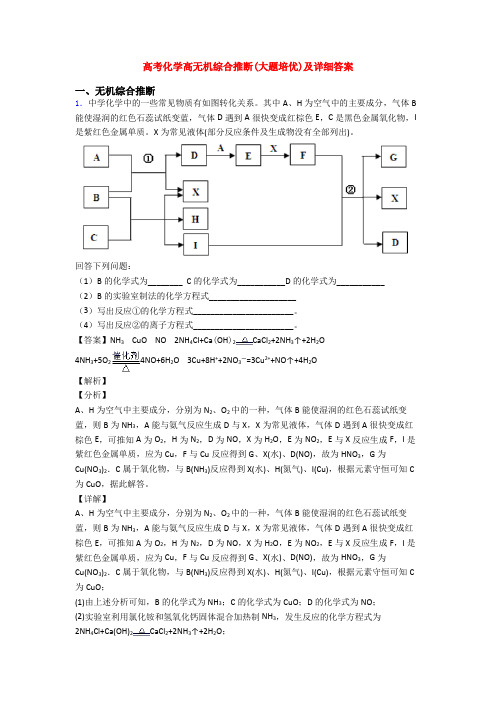
高考化学高无机综合推断(大题培优)及详细答案一、无机综合推断1.中学化学中的一些常见物质有如图转化关系。
其中A、H为空气中的主要成分,气体B 能使湿润的红色石蕊试纸变蓝,气体D遇到A很快变成红棕色E,C是黑色金属氧化物,I 是紫红色金属单质。
X为常见液体(部分反应条件及生成物没有全部列出)。
回答下列问题:(1)B的化学式为________ C的化学式为___________D的化学式为___________(2)B的实验室制法的化学方程式____________________(3)写出反应①的化学方程式_______________________。
(4)写出反应②的离子方程式_______________________。
【答案】NH3 CuO NO 2NH4Cl+Ca(OH)2CaCl2+2NH3↑+2H2O4NH3+5O24NO+6H2O 3Cu+8H++2NO3—=3Cu2++NO↑+4H2O【解析】【分析】A、H为空气中主要成分,分别为N2、O2中的一种,气体B能使湿润的红色石蕊试纸变蓝,则B为NH3,A能与氨气反应生成D与X,X为常见液体,气体D遇到A很快变成红棕色E,可推知A为O2,H为N2,D为NO,X为H2O,E为NO2,E与X反应生成F,I是紫红色金属单质,应为Cu,F与Cu反应得到G、X(水)、D(NO),故为HNO3,G为Cu(NO3)2.C属于氧化物,与B(NH3)反应得到X(水)、H(氮气)、I(Cu),根据元素守恒可知C 为CuO,据此解答。
【详解】A、H为空气中主要成分,分别为N2、O2中的一种,气体B能使湿润的红色石蕊试纸变蓝,则B为NH3,A能与氨气反应生成D与X,X为常见液体,气体D遇到A很快变成红棕色E,可推知A为O2,H为N2,D为NO,X为H2O,E为NO2,E与X反应生成F,I是紫红色金属单质,应为Cu,F与Cu反应得到G、X(水)、D(NO),故为HNO3,G为Cu(NO3)2.C属于氧化物,与B(NH3)反应得到X(水)、H(氮气)、I(Cu),根据元素守恒可知C 为CuO;(1)由上述分析可知,B的化学式为NH3;C的化学式为CuO;D的化学式为NO;(2)实验室利用氯化铵和氢氧化钙固体混合加热制NH3,发生反应的化学方程式为2NH4Cl+Ca(OH)2CaCl2+2NH3↑+2H2O;(3)反应①为氨的催化氧化,发生反应的化学方程式为4NH3+5O24NO+6H2O;(4)反应②为Cu溶于稀硝酸生成NO,发生反应的离子方程式为3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O。
高考化学高无机综合推断(大题培优)附答案

高考化学高无机综合推断(大题培优)附答案一、无机综合推断1.下列各物质中只有A、B、C三种单质,A的焰色反应为黄色,主要以G形式存在于海水中,F是一种淡黄色的固体,H是一种常见的无色液体,I是造成温室效应的“元凶”,各物质间的转化关系图如下:回答下列问题:(1)A是:_____,C是:_____,L是:______,I是:____(填化学式)。
(2)写出反应①②③的化学反应方程式:①:____________________________________;②:____________________________________;③:____________________________________;【答案】Na Cl2HCl CO22Na+2H2O=2NaOH+H2↑2Na2O2+2H2O=4NaOH+O2↑2NaHCO3Na2CO3+CO2↑+H2O【解析】【分析】焰色反应为黄色的单质是钠,钠元素在自然界主要以氯化钠的形式存在,淡黄色固体是过氧化钠,常见的无色液体是水,造成温室效应的“元凶”是二氧化碳。
因此,A是钠,B是氧气,C是氯气,D是氢氧化钠,E是氧化钠,F是过氧化钠,G是氯化钠,H是水,I是二氧化碳,J是碳酸氢钠,K是碳酸钠,L是盐酸。
【详解】(1)A是钠,化学式为Na,C是氯气,化学式为Cl2,L是氯化氢,化学式为HCl,I是二氧化碳,化学式为CO2;(2)①是钠与水的反应,化学方程式为:2Na+2H2O=2NaOH+H2↑;②是过氧化钠与水的反应,化学方程式为:2Na2O2+2H2O=4NaOH+O2↑;③是碳酸氢钠的受热分解,化学方程式为:2NaHCO3Na2CO3+CO2↑+H2O;【点睛】无机框图推断题要找出题眼,关键点,熟记特殊物质的颜色,特殊的反应,工业生产等等,找出突破口,一一突破。
2.已知A、B、C、D原子序数依次递增的短周期主族元素,常温常压下AB2是一种红棕色气体,B与C同主族,则:(1)C元素在周期表中的位置____________。
高考化学 高无机综合推断 培优 易错 难题练习(含答案)含答案(1)

高考化学高无机综合推断培优易错难题练习(含答案)含答案(1)一、无机综合推断1.已知A、B、C、D是元素周期表中的四种短周期元素,A分别与B、C、D结合生成三种化合物:甲、乙、丙。
甲、乙、丙三种化合物的分子中含有相同数目的电子;丙与甲、乙均能发生化学反应,且甲、丙为无色有不同刺激性气味的物质,化合物丁与C的某种单质在常温下反应可生成红棕色气体;B、C、D三种元素的单质与甲、乙、丁三种化合物之间存在如图所示的转化关系(反应条件已略去):(1)D在元素周期表中的位置为________________。
(2)B、C、D的原子半径的大小关系为________(用元素符号表示)。
(3)丁与C的单质在常温下反应的化学方程式为______________。
(4)甲、乙、丙分子中的电子数均为________,实验室如何检验丙_______ 。
(5)C的单质+丙→乙+丁的化学方程式为_______________。
【答案】第2周期ⅤA族 N>O>F 2NO+O2===2NO2 10 能使湿润的红色石蕊试纸变蓝色 5O2+4NH36H2O+4NO【解析】【分析】本题有几个重要的突破口:①甲、乙、丙三种化合物的分子中含有相同数目的电子;②丙为无色有不同刺激性气味的物质;③化合物丁与C的某种单质在常温下反应可生成红棕色气体,说明丁为NO,C的某种单质可能为O2。
【详解】A、B、C、D是元素周期表中的四种短周期元素,A分别与B、C、D结合生成三种化合物:甲、乙、丙。
化合物丁与C的某种单质在常温下反应可生成红棕色气体,则丁为NO、C为O元素;丙与甲、乙均能发生化学反应,且甲、丙为无色有不同刺激性气味的物质,由图中信息可知,丙与O元素的单质反应生成NO,也可以由O的单质与D的单质化合而得,则丙为NH3、D为N元素,乙为H2O;甲、乙、丙三种化合物的分子中含有相同数目的电子,则其都有10个电子,结合图中信息,B的单质可以与H2O反应生成甲和O 元素的单质,故甲为HF、B为F元素。
2020-2021备战高考化学 高无机综合推断 培优练习(含答案)及详细答案
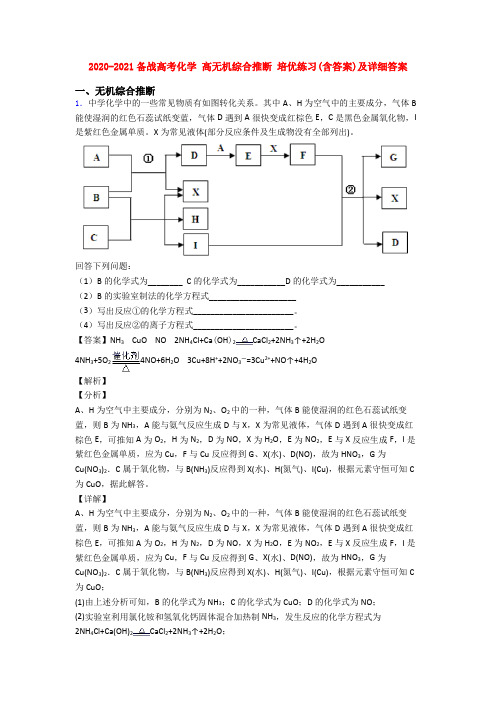
2020-2021备战高考化学高无机综合推断培优练习(含答案)及详细答案一、无机综合推断1.中学化学中的一些常见物质有如图转化关系。
其中A、H为空气中的主要成分,气体B 能使湿润的红色石蕊试纸变蓝,气体D遇到A很快变成红棕色E,C是黑色金属氧化物,I 是紫红色金属单质。
X为常见液体(部分反应条件及生成物没有全部列出)。
回答下列问题:(1)B的化学式为________ C的化学式为___________D的化学式为___________(2)B的实验室制法的化学方程式____________________(3)写出反应①的化学方程式_______________________。
(4)写出反应②的离子方程式_______________________。
【答案】NH3 CuO NO 2NH4Cl+Ca(OH)2CaCl2+2NH3↑+2H2O4NH3+5O24NO+6H2O 3Cu+8H++2NO3—=3Cu2++NO↑+4H2O【解析】【分析】A、H为空气中主要成分,分别为N2、O2中的一种,气体B能使湿润的红色石蕊试纸变蓝,则B为NH3,A能与氨气反应生成D与X,X为常见液体,气体D遇到A很快变成红棕色E,可推知A为O2,H为N2,D为NO,X为H2O,E为NO2,E与X反应生成F,I是紫红色金属单质,应为Cu,F与Cu反应得到G、X(水)、D(NO),故为HNO3,G为Cu(NO3)2.C属于氧化物,与B(NH3)反应得到X(水)、H(氮气)、I(Cu),根据元素守恒可知C 为CuO,据此解答。
【详解】A、H为空气中主要成分,分别为N2、O2中的一种,气体B能使湿润的红色石蕊试纸变蓝,则B为NH3,A能与氨气反应生成D与X,X为常见液体,气体D遇到A很快变成红棕色E,可推知A为O2,H为N2,D为NO,X为H2O,E为NO2,E与X反应生成F,I是紫红色金属单质,应为Cu,F与Cu反应得到G、X(水)、D(NO),故为HNO3,G为Cu(NO3)2.C属于氧化物,与B(NH3)反应得到X(水)、H(氮气)、I(Cu),根据元素守恒可知C 为CuO;(1)由上述分析可知,B的化学式为NH3;C的化学式为CuO;D的化学式为NO;(2)实验室利用氯化铵和氢氧化钙固体混合加热制NH3,发生反应的化学方程式为2NH4Cl+Ca(OH)2CaCl2+2NH3↑+2H2O;(3)反应①为氨的催化氧化,发生反应的化学方程式为4NH3+5O24NO+6H2O;(4)反应②为Cu溶于稀硝酸生成NO,发生反应的离子方程式为3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O。
2020-2021高考化学高无机综合推断(大题培优)及详细答案

2020-2021高考化学高无机综合推断(大题培优)及详细答案一、无机综合推断1.已知A、B、C、D是元素周期表中的四种短周期元素,A分别与B、C、D结合生成三种化合物:甲、乙、丙。
甲、乙、丙三种化合物的分子中含有相同数目的电子;丙与甲、乙均能发生化学反应,且甲、丙为无色有不同刺激性气味的物质,化合物丁与C的某种单质在常温下反应可生成红棕色气体;B、C、D三种元素的单质与甲、乙、丁三种化合物之间存在如图所示的转化关系(反应条件已略去):(1)D在元素周期表中的位置为________________。
(2)B、C、D的原子半径的大小关系为________(用元素符号表示)。
(3)丁与C的单质在常温下反应的化学方程式为______________。
(4)甲、乙、丙分子中的电子数均为________,实验室如何检验丙_______ 。
(5)C的单质+丙→乙+丁的化学方程式为_______________。
【答案】第2周期ⅤA族 N>O>F 2NO+O2===2NO2 10 能使湿润的红色石蕊试纸变蓝色 5O2+4NH36H2O+4NO【解析】【分析】本题有几个重要的突破口:①甲、乙、丙三种化合物的分子中含有相同数目的电子;②丙为无色有不同刺激性气味的物质;③化合物丁与C的某种单质在常温下反应可生成红棕色气体,说明丁为NO,C的某种单质可能为O2。
【详解】A、B、C、D是元素周期表中的四种短周期元素,A分别与B、C、D结合生成三种化合物:甲、乙、丙。
化合物丁与C的某种单质在常温下反应可生成红棕色气体,则丁为NO、C为O元素;丙与甲、乙均能发生化学反应,且甲、丙为无色有不同刺激性气味的物质,由图中信息可知,丙与O元素的单质反应生成NO,也可以由O的单质与D的单质化合而得,则丙为NH3、D为N元素,乙为H2O;甲、乙、丙三种化合物的分子中含有相同数目的电子,则其都有10个电子,结合图中信息,B的单质可以与H2O反应生成甲和O 元素的单质,故甲为HF、B为F元素。
高考化学培优 易错 难题(含解析)之高无机综合推断含答案解析

高考化学培优易错难题(含解析)之高无机综合推断含答案解析一、无机综合推断1.A、B、C、W均为中学常见的物质,它们之间有如图所示的转化关系(其他产物及反应条件已略去,反应可以在水溶液中进行)。
(1)若A、B、C三种物质的焰色反应均为黄色,A俗称苛性钠,W为无色无味气体,C受热分解可转化为B。
①向B溶液中通入W生成C的离子方程式为__________________________________。
②A溶液与C溶液反应的化学方程式为______________________________________。
(2)若A、B、C三种物质都含有一种金属元素,且B为两性物质,W俗称苛性钠。
①A、B、C三种物质中所含有的金属元素单质与W反应的化学方程式为_____________。
②A溶液一步转化为C溶液的反应离子方程式为________________________________。
(3)若A、B、C、W四种物质均为气体,其中A、W为单质,C的摩尔质量为46g·mol-1。
①B的化学式为________________。
②实验室制取B时,_____________(填“能”或“不能”)用向上排空气法收集B。
③一定条件下B与CO反应的化学方程式为_____________________________。
(4)若A为淡黄色固体单质,W为气体单质,B、C均为酸性氧化物。
则C溶于水形成化合物D,在加热的情况下,D的浓溶液与A反应的化学方程式为________________________。
【答案】CO32-+H2O+CO2=2HCO3- NaOH+NaHCO3=Na2CO3+H2O 2Al+2NaOH+2H2O =2NaAlO2 +3H2↑ Al3-+ 4OH- =AlO2- + 2H2O NO 不能 2NO+2CO2CO2+N2S+2H2SO4(浓)3SO2↑+2H2O【解析】【分析】(1) 若A、B、C 三种物质的焰色反应均为黄色,均含Na元素,A俗称苛性钠,则A为NaOH,W为无色无味气体,C受热分解可转化为B,则W为CO2、B为Na2CO3,C为NaHCO3;(2)若A、B、C三种物质都含有一种金属元素,且B为两性物质,W俗称苛性钠,则B为Al(OH)3,A为AlCl3、C为NaAlO2;(3) 若A、B、C、W四种物质均为气体,其中A、W为单质,C的摩尔质量为46g•mol-1,则A为N2、W为O2、B为NO、C为NO2;(4) 若A 为淡黄色固体单质,W 为气体单质,B、C均为酸性氧化物,则A为S,W为O2、B为SO2、C为SO3 。
高考化学 高无机综合推断 培优 易错 难题练习(含答案)附详细答案
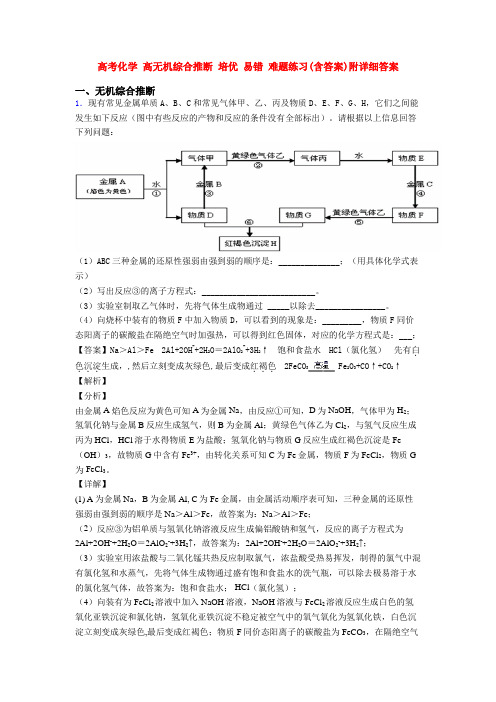
高考化学高无机综合推断培优易错难题练习(含答案)附详细答案一、无机综合推断1.现有常见金属单质A、B、C和常见气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。
请根据以上信息回答下列问题:(1)ABC三种金属的还原性强弱由强到弱的顺序是:______________;(用具体化学式表示)(2)写出反应③的离子方程式:__________________________。
(3)实验室制取乙气体时,先将气体生成物通过_____以除去________________。
(4)向烧杯中装有的物质F中加入物质D,可以看到的现象是:_________,物质F同价态阳离子的碳酸盐在隔绝空气时加强热,可以得到红色固体,对应的化学方程式是:___;【答案】Na>Al>Fe2Al+2OH-+2H2O=2AlO2-+3H2↑饱和食盐水HCl(氯化氢)先有白.色沉淀...2FeCO3Fe2O3+CO↑+CO2↑...生成,,然后立刻变成灰绿色,最后变成红褐色【解析】【分析】由金属A焰色反应为黄色可知A为金属Na,由反应①可知,D为NaOH,气体甲为H2;氢氧化钠与金属B反应生成氢气,则B为金属Al;黄绿色气体乙为Cl2,与氢气反应生成丙为HCl,HCl溶于水得物质E为盐酸;氢氧化钠与物质G反应生成红褐色沉淀是Fe (OH)3,故物质G中含有Fe3+,由转化关系可知C为Fe金属,物质F为FeCl2,物质G 为FeCl3。
【详解】(1) A为金属Na,B为金属Al, C为Fe金属,由金属活动顺序表可知,三种金属的还原性强弱由强到弱的顺序是Na>Al>Fe,故答案为:Na>Al>Fe;(2)反应③为铝单质与氢氧化钠溶液反应生成偏铝酸钠和氢气,反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;(3)实验室用浓盐酸与二氧化锰共热反应制取氯气,浓盐酸受热易挥发,制得的氯气中混有氯化氢和水蒸气,先将气体生成物通过盛有饱和食盐水的洗气瓶,可以除去极易溶于水的氯化氢气体,故答案为:饱和食盐水; HCl(氯化氢);(4)向装有为FeCl2溶液中加入NaOH溶液,NaOH溶液与FeCl2溶液反应生成白色的氢氧化亚铁沉淀和氯化钠,氢氧化亚铁沉淀不稳定被空气中的氧气氧化为氢氧化铁,白色沉淀立刻变成灰绿色,最后变成红褐色;物质F同价态阳离子的碳酸盐为FeCO3,在隔绝空气时加强热,得到红色固体为Fe2O3,化学方程式为2FeCO3Fe2O3+CO↑+CO2↑,故答案为:先有白色沉淀生成,,然后立刻变成灰绿色,最后变成红褐色;2FeCO3Fe2O3+CO↑+CO2↑。
高考化学二轮 高无机综合推断 专项培优含详细答案

高考化学二轮高无机综合推断专项培优含详细答案一、无机综合推断1.已知A、B、C、D是元素周期表中的四种短周期元素,A分别与B、C、D结合生成三种化合物:甲、乙、丙。
甲、乙、丙三种化合物的分子中含有相同数目的电子;丙与甲、乙均能发生化学反应,且甲、丙为无色有不同刺激性气味的物质,化合物丁与C的某种单质在常温下反应可生成红棕色气体;B、C、D三种元素的单质与甲、乙、丁三种化合物之间存在如图所示的转化关系(反应条件已略去):(1)D在元素周期表中的位置为________________。
(2)B、C、D的原子半径的大小关系为________(用元素符号表示)。
(3)丁与C的单质在常温下反应的化学方程式为______________。
(4)甲、乙、丙分子中的电子数均为________,实验室如何检验丙_______ 。
(5)C的单质+丙→乙+丁的化学方程式为_______________。
【答案】第2周期ⅤA族 N>O>F 2NO+O2===2NO2 10 能使湿润的红色石蕊试纸变蓝色 5O2+4NH36H2O+4NO【解析】【分析】本题有几个重要的突破口:①甲、乙、丙三种化合物的分子中含有相同数目的电子;②丙为无色有不同刺激性气味的物质;③化合物丁与C的某种单质在常温下反应可生成红棕色气体,说明丁为NO,C的某种单质可能为O2。
【详解】A、B、C、D是元素周期表中的四种短周期元素,A分别与B、C、D结合生成三种化合物:甲、乙、丙。
化合物丁与C的某种单质在常温下反应可生成红棕色气体,则丁为NO、C为O元素;丙与甲、乙均能发生化学反应,且甲、丙为无色有不同刺激性气味的物质,由图中信息可知,丙与O元素的单质反应生成NO,也可以由O的单质与D的单质化合而得,则丙为NH3、D为N元素,乙为H2O;甲、乙、丙三种化合物的分子中含有相同数目的电子,则其都有10个电子,结合图中信息,B的单质可以与H2O反应生成甲和O 元素的单质,故甲为HF、B为F元素。
高考化学 高无机综合推断 培优易错试卷练习(含答案)及答案(1)

高考化学高无机综合推断培优易错试卷练习(含答案)及答案(1)一、无机综合推断1.黑色固体物质A有如下图所示的转化关系。
每个方框表示有一种反应物或生成物(反应条件及生成的水已略去),其中C、F常温下为无色气体,D、E有共同的阳离子。
⑴写出B和C的化学式:B______________;C______________。
⑵写出反应④的离子方程式______________【答案】FeSO4 H2S 2Fe3++SO2+2H2O=2Fe2++SO42-+4H+【解析】【分析】从框图中可以看出,反应②是解题的突破口。
因为它的已知信息多,不仅有“D、E有共同的阳离子”,而且有Cl2这种具有强氧化性的特殊物质。
【详解】(1)由反应②知,B物质具有还原性;由反应④知,E物质具有氧化性,F气体具有还原性。
综合分析反应②和④,可得出B中的阳离子具有还原性,从而得出其为亚铁盐。
结合反应③,可得出F气体为SO2,C气体为H2S。
再回到反应④,F为SO2,氧化产物必然为H2SO4,从而得出E为Fe2(SO4)3、B为FeSO4、G为H2SO4。
由反应①,很容易得出A为FeS。
由反应②,可得出D为FeCl3。
答案为:B是FeSO4、C是H2S。
(2) 反应④的化学方程式为:Fe2(SO4)3+SO2+2H2O=2FeSO4+2H2SO4,离子方程式为:2Fe3++SO2+2H2O=2Fe2++SO42-+4H+。
答案为:2Fe3++SO2+2H2O=2Fe2++SO42-+4H+【点睛】无机框图题是难度较大的一类题,因为它要求我们必须熟练掌握元素及其化合物的性质,尤其是一些具有特殊性质的物质。
比如Cu、Cl2、Fe2O3、CuO、FeS等物质的颜色,需要高温、通电、催化剂等条件的反应,具有较强氧化性的金属离子(比如Fe3+),具有较强还原性的气体(比如SO2)等。
解题时,条件特殊、已知条件多、具有特殊性的反应,常常是解题的切入点和突破口。
高考化学 高无机综合推断 培优练习(含答案)附答案解析
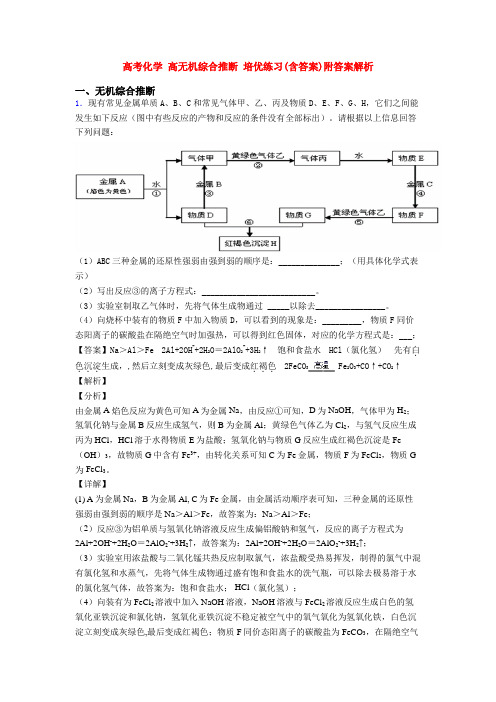
高考化学高无机综合推断培优练习(含答案)附答案解析一、无机综合推断1.现有常见金属单质A、B、C和常见气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。
请根据以上信息回答下列问题:(1)ABC三种金属的还原性强弱由强到弱的顺序是:______________;(用具体化学式表示)(2)写出反应③的离子方程式:__________________________。
(3)实验室制取乙气体时,先将气体生成物通过_____以除去________________。
(4)向烧杯中装有的物质F中加入物质D,可以看到的现象是:_________,物质F同价态阳离子的碳酸盐在隔绝空气时加强热,可以得到红色固体,对应的化学方程式是:___;【答案】Na>Al>Fe2Al+2OH-+2H2O=2AlO2-+3H2↑饱和食盐水HCl(氯化氢)先有白.色沉淀...2FeCO3Fe2O3+CO↑+CO2↑...生成,,然后立刻变成灰绿色,最后变成红褐色【解析】【分析】由金属A焰色反应为黄色可知A为金属Na,由反应①可知,D为NaOH,气体甲为H2;氢氧化钠与金属B反应生成氢气,则B为金属Al;黄绿色气体乙为Cl2,与氢气反应生成丙为HCl,HCl溶于水得物质E为盐酸;氢氧化钠与物质G反应生成红褐色沉淀是Fe (OH)3,故物质G中含有Fe3+,由转化关系可知C为Fe金属,物质F为FeCl2,物质G 为FeCl3。
【详解】(1) A为金属Na,B为金属Al, C为Fe金属,由金属活动顺序表可知,三种金属的还原性强弱由强到弱的顺序是Na>Al>Fe,故答案为:Na>Al>Fe;(2)反应③为铝单质与氢氧化钠溶液反应生成偏铝酸钠和氢气,反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;(3)实验室用浓盐酸与二氧化锰共热反应制取氯气,浓盐酸受热易挥发,制得的氯气中混有氯化氢和水蒸气,先将气体生成物通过盛有饱和食盐水的洗气瓶,可以除去极易溶于水的氯化氢气体,故答案为:饱和食盐水; HCl(氯化氢);(4)向装有为FeCl2溶液中加入NaOH溶液,NaOH溶液与FeCl2溶液反应生成白色的氢氧化亚铁沉淀和氯化钠,氢氧化亚铁沉淀不稳定被空气中的氧气氧化为氢氧化铁,白色沉淀立刻变成灰绿色,最后变成红褐色;物质F同价态阳离子的碳酸盐为FeCO3,在隔绝空气时加强热,得到红色固体为Fe2O3,化学方程式为2FeCO3Fe2O3+CO↑+CO2↑,故答案为:先有白色沉淀生成,,然后立刻变成灰绿色,最后变成红褐色;2FeCO3Fe2O3+CO↑+CO2↑。
高考化学 高无机综合推断 培优练习(含答案)附答案
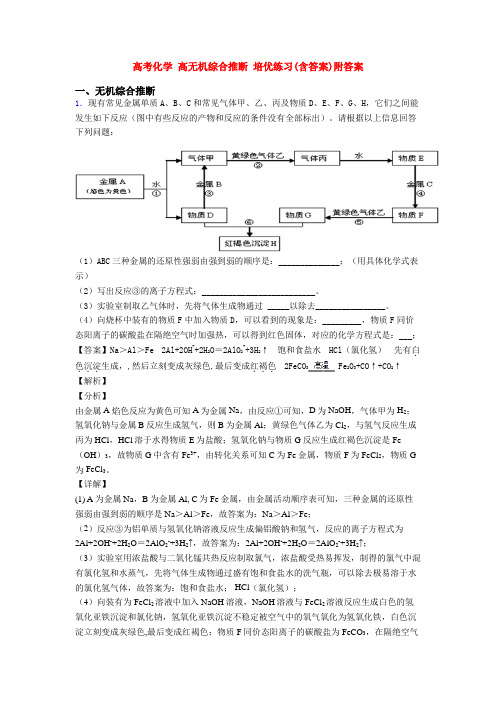
高考化学高无机综合推断培优练习(含答案)附答案一、无机综合推断1.现有常见金属单质A、B、C和常见气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。
请根据以上信息回答下列问题:(1)ABC三种金属的还原性强弱由强到弱的顺序是:______________;(用具体化学式表示)(2)写出反应③的离子方程式:__________________________。
(3)实验室制取乙气体时,先将气体生成物通过_____以除去________________。
(4)向烧杯中装有的物质F中加入物质D,可以看到的现象是:_________,物质F同价态阳离子的碳酸盐在隔绝空气时加强热,可以得到红色固体,对应的化学方程式是:___;【答案】Na>Al>Fe2Al+2OH-+2H2O=2AlO2-+3H2↑饱和食盐水HCl(氯化氢)先有白.色沉淀...2FeCO3Fe2O3+CO↑+CO2↑...生成,,然后立刻变成灰绿色,最后变成红褐色【解析】【分析】由金属A焰色反应为黄色可知A为金属Na,由反应①可知,D为NaOH,气体甲为H2;氢氧化钠与金属B反应生成氢气,则B为金属Al;黄绿色气体乙为Cl2,与氢气反应生成丙为HCl,HCl溶于水得物质E为盐酸;氢氧化钠与物质G反应生成红褐色沉淀是Fe (OH)3,故物质G中含有Fe3+,由转化关系可知C为Fe金属,物质F为FeCl2,物质G 为FeCl3。
【详解】(1) A为金属Na,B为金属Al, C为Fe金属,由金属活动顺序表可知,三种金属的还原性强弱由强到弱的顺序是Na>Al>Fe,故答案为:Na>Al>Fe;(2)反应③为铝单质与氢氧化钠溶液反应生成偏铝酸钠和氢气,反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;(3)实验室用浓盐酸与二氧化锰共热反应制取氯气,浓盐酸受热易挥发,制得的氯气中混有氯化氢和水蒸气,先将气体生成物通过盛有饱和食盐水的洗气瓶,可以除去极易溶于水的氯化氢气体,故答案为:饱和食盐水; HCl(氯化氢);(4)向装有为FeCl2溶液中加入NaOH溶液,NaOH溶液与FeCl2溶液反应生成白色的氢氧化亚铁沉淀和氯化钠,氢氧化亚铁沉淀不稳定被空气中的氧气氧化为氢氧化铁,白色沉淀立刻变成灰绿色,最后变成红褐色;物质F同价态阳离子的碳酸盐为FeCO3,在隔绝空气时加强热,得到红色固体为Fe2O3,化学方程式为2FeCO3Fe2O3+CO↑+CO2↑,故答案为:先有白色沉淀生成,,然后立刻变成灰绿色,最后变成红褐色;2FeCO3Fe2O3+CO↑+CO2↑。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
高考化学高无机综合推断(大题培优)一、无机综合推断1.现有稀硫酸、纯碱、二氧化碳、铜片、食盐、生石灰、铁片和木炭粉8种物质。
(1)在这8种物质中,属于电解质的有_____________(用相应的化学式表示,下同)。
(2)这8种物质中的某5种存在下面的相互关系,选择适当的物质填入①~⑤,使有连线的两种物质能发生反应,并回答下列问题。
①它们的化学式分别为:①______________;③____________;⑤______________。
②如果连线对应的反应分别用A、B、C、D、E表示。
五个反应中属于氧化还原反应的有________________个;反应A的离子方程式为________________________,反应D的化学方程式为_________________________。
【答案】(1)Na2CO3、NaCl、CaO;(2)①Fe ②H2SO4③CO2④CaO ⑤Na2CO3②1 Fe+2H+===Fe2++H2↑不属于 H2SO4+Na2CO3===Na2SO4+H2O+CO2↑【解析】试题分析:(1)电解质指的是在水溶液或熔融状态下能够导电的化合物,因此属于电解质的有Na2CO3、NaCl、CaO;(2)单质①能够和酸②,则单质①为Fe,酸②为H2SO4;盐⑤能够和H2SO4反应,因此盐⑤为Na2CO3;氧化物④能够和H2SO4反应,因此氧化物④为碱性氧化物CaO;氧化物③能够和CaO反应,则氧化物③为CO2;故答案:①Fe②H2SO4③CO2④CaO ⑤Na2CO3;②有化合价升降的反应为氧化还原反应,在五个反应中,只有反应A为氧化还原反应;反应A的离子方程式为Fe+2H+===Fe2++H2↑;反应B 为CO2和CaO的反应,不属于离子反应;反应D是Na2CO3和H2SO4的反应,反应的化学方程式为:H2SO4+Na2CO3===Na2SO4+H2O+CO2↑。
考点:考查物质的分类与性质。
2.氢能源是一种重要的清洁能源。
现有两种可产生H2的化合物甲和乙。
将6.00g甲加热至完全分解,只得到一种短周期元素的金属单质和6.72LH2(已折算成标准状况),甲与水反应也能产生H2,同时还产生一种白色沉淀物,该白色沉淀可溶于NaOH溶液。
化合物乙在催化剂存在下可分解得到H2和另一种单质气体丙,丙在标准状态下的密度为1.25g/L。
请回答下列问题:(1)甲的化学式是__________;乙的电子式是__________。
(2)甲与水反应的化学方程式是__________。
(3)气体丙与金属镁反应的产物是__________(用化学式表示)。
(4)乙在加热条件下与CuO反应可生成Cu和气体丙,写出该反应的化学方程式__________。
有人提出产物Cu中可能还含有Cu2O,请设计实验方案验证之__________(已知Cu2O+2H+=Cu+Cu2++H2O)。
【答案】AlH3 AlH3+3H2O=Al(OH)3↓+3H2↑ Mg3N2 2NH3+3CuO3Cu+N2+3H2O 将固体溶于稀硫酸中,如果溶液变蓝,说明产物中含有Cu2O,反之则无Cu2O【解析】【分析】将6.00g甲加热至完全分解,只得到一种短周期元素的金属单质和6.72L的H2(已折算成标准状况),甲与水反应也能产生H2,同时还产生一种白色沉淀物,该白色沉淀可溶于NaOH溶液,因此白色沉淀是Al(OH)3,则金属单质是铝,因此甲是AlH3。
化合物乙在催化剂存在下可分解得到H2和另一种单质气体丙,丙在标准状况下的密度为1.25g·L-1,则丙的相对分子质量是1.25×22.4=28,因此丙是氮气,则乙是氨气NH3,据此解答。
【详解】(1)根据以上分析可知甲的化学式是AlH3。
乙是氨气,含有共价键的共价化合物,电子式为;(2)甲与水反应生成氢气和氢氧化铝,反应的化学方程式是AlH3+3H2O=Al(OH)3↓+3H2↑。
(3)氮气与金属镁反应的产物是Mg3N2。
(4)氨气在加热条件下与CuO反应可生成Cu和氮气,根据原子守恒可知该反应的化学方程式为2NH3+3CuO3Cu+N2+3H2O。
铜与稀硫酸不反应,则根据Cu2O+2H+=Cu+Cu2++H2O可知,要检验产物Cu中可能还混有Cu2O可以将固体溶于稀硫酸中,如果溶液变蓝,说明产物中含有Cu2O,反之则无Cu2O。
3.为探究某无结晶水的正盐X(仅含有两种短周期元素)的组成和性质,设计并完成下列实验。
(气体体积已转化为标准状况下的体积)已知:B 是空气的主要成分之一;C 是一种强碱,且微溶于水 ,载人宇宙飞船内常用含 C 的过滤网吸收宇航员呼出的CO 2,以净化空气;D 遇湿润的红色石蕊试纸变蓝。
(1)X 的化学式为 __________________ 。
(2)图中B 的组成元素在元素周期表中的位置是______________。
(3)A 的电子式为 ____________。
(4)X 受热分解转变成 A 和 B 的化学反应方程式为 ____________。
【答案】LiN 3 第2周期VA 族 3LiN 3ΔLi 3N+4N 2↑ 【解析】【分析】B 是空气的主要成分之一,B 为氮气或氧气;C 是一种强碱,且微溶于水,C 为LiOH ,载人宇宙飞船内常用含 C 的过滤网吸收宇航员呼出的CO 2,以净化空气,LiOH 与反应生成Li 2CO 3;D 遇湿润的红色石蕊试纸变蓝,D 是NH 3,确定B 为氮气,NH 3是2.24L 合0.1mol ,A 中N 为14g·mol -1×0.1mol=1.4g 。
A 为Li 3N ,3.5g 中Li 为3.5-1.4=2.1g ,14.7gX 中Li 为 2.1g ,n(Li)=12.17?g g mol-=0.3mol ,n(N)=114.7 2.114?g g g mol --=0.9mol,n(Li):n(N)=0.3:0.9=1:3,X 的化学式为:LiN 3。
【详解】(1)由分析可知:X 的化学式为LiN 3。
故答案为:LiN 3;(2)B 为氮气,组成元素N 在元素周期表中的位置是第2周期VA 族。
故答案为:第2周期VA 族;(3)A 为Li 3N ,Li 最外层只有1个电子,显+1价,N 最外层5个电子,得三个电子,显-3价,电子式为。
故答案为:;(4)由分析X 的化学式为:LiN 3,X 受热分解转变成 Li 3N 和 N 2,由质量守恒:化学反应方程式为 3LiN 3ΔLi 3N+4N 2↑。
故答案为: 3LiN 3ΔLi 3N+4N 2↑。
4.A 是一种红棕色金属氧化物;B 、D 是金属单质;J 是一种难溶于水的白色化合物,受热易分解。
回答下列问题:(1)A、E、J、G的化学式分别为___、___、___、___。
(2)C转化为I的离子方程式为___。
(3)H和I反应生成J的离子方程式为___。
(4)如何检验E溶液中大量存在的阳离子?___。
【答案】Fe2O3 FeCl2 Al(OH)3 Fe(OH)3 Al2O3+2OH-═2AlO2-+H2O Al3++3AlO2-+6H2O═4Al(OH)3↓取E溶液2mL于试管中,滴入几滴KSCN溶液,无现象,再滴入几滴氯水,溶液呈血红色,则含有Fe2+【解析】【分析】A是一种红棕色金属氧化物,则A是Fe2O3,红褐色沉淀G为Fe(OH)3,分解可以生成氧化铁,则F是 Fe(OH)2.B、D是金属单质,Fe2O3和B在高温下能反应生成金属单质D,则该反应是铝热反应,B是Al,D是Fe,C是Al2O3,J是一种不溶于水的白色化合物,受热容易分解成C,则J是Al(OH)3,由转化关系可知,I是NaAlO2,H是AlCl3;铁和盐酸反应生成氯化亚铁和氢气,E和氨水反应生成 Fe(OH)2,则E是 FeCl2,以此解答该题。
【详解】(1)由以上分析可知,则A为Fe2O3,E是FeCl2,J是Al(OH)3,G是Fe(OH)3;(2)氧化铝是两性氧化物,与氢氧化钠反应生成偏铝酸钠与水,反应离子方程式为:Al2O3+2OH-═2AlO2-+H2O;(3)铝离子和偏铝酸根之间双水解而不共存,反应的离子方程式为Al3++3AlO2-+6H2O═4Al(OH)3↓;(4)E是FeCl2,检验亚铁离子,可取E溶液2mL于试管中,滴入几滴KSCN溶液,无现象,再滴入几滴氯水,溶液呈血红色,则含有Fe2+。
5.探究无机盐X(仅含三种短周期元素)的组成和性质,设计并完成如下实验:请回答:(1)X的化学式是____。
(2)白色粉末溶于氢氧化钠溶液的离子方程式是____。
(3)高温条件下白色粉末与焦炭发生置换反应,写出该反应的化学方程式____。
【答案】Mg2SiO4或2MgO·SiO2 SiO2+2OH-=SiO32-+H2O SiO2+2C 高温Si+2CO↑【解析】【详解】无机盐X(仅含三种短周期元素),加入过量盐酸溶解,离心分离得到白色胶状物沉淀和无色溶液,白色胶状沉淀为硅酸,白色沉淀充分灼烧得到白色粉末1.80g为SiO2,物质的量=1.8g÷60g/mol=0.03mol,溶于氢氧化钠溶液得到无色溶液为硅酸钠溶液,说明无机盐中含硅酸根离子或原硅酸根离子,物质的量为0.03mol,若为硅酸根离子其质量=0.03mol×76g/mol=2.28g,金属质量=4.20g-2.28g=1.92g,无色溶液中加入过量氢氧化钠溶液生成白色沉淀则判断为Mg(OH)2,金属离子物质的量=3.48g÷58g/mol=0.06mol,质量为0.06mol×24g/mol=1.44g,不符合,则应为原硅酸根,物质的量为0.03mol,质量=0.03mol×92g/mol=2.76g,金属质量4.20g-2.76g=1.44g,物质的量=1.44g÷24g/mol=0.06mol,得到X为Mg2SiO4,则(1)X的化学式是Mg2SiO4或2MgO·SiO2。
(2)白色粉末溶于氢氧化钠溶液的离子方程式是SiO2+2OH-=SiO32-+H2O。
(3)高温条件下白色粉末与焦炭发生置换反应,该反应的化学方程式SiO2+2C 高温Si+2CO↑。
6.生氢材料甲由X、Y两种元素组成,两元素的原子最外层电子数相等。
为确定甲的组成,进行了如下实验:①称取1.2g甲固体与一定量的水蒸气刚好完全反应,生成标准状况下1.12L可燃性单质气体乙,同时得到2g化合物丙。
②用0.05mol甲与0.8g氧气恰好发生化合反应,得到2g丙。
请回答:(1)乙的分子式____。
