第14章细胞增殖调控与癌细胞
细胞增殖与癌症关系的研究报告

细胞增殖与癌症关系的研究报告摘要:本研究旨在探讨细胞增殖与癌症之间的关系。
通过对细胞增殖的机制、癌症发展的过程以及两者之间的相互作用进行综合分析,我们发现细胞增殖在癌症的发展中起到了重要的作用。
本文以细胞增殖与癌症关系的研究为出发点,对该领域的研究现状和未来发展方向进行了探讨。
1. 引言癌症是一种严重威胁人类健康的疾病,其发病机制至今尚未完全阐明。
细胞增殖作为生物体内细胞数量增加的重要过程,对癌症的发展起到了重要的推动作用。
因此,深入研究细胞增殖与癌症之间的关系对于癌症的预防和治疗具有重要意义。
2. 细胞增殖的机制细胞增殖是指细胞数量增加的过程,主要通过细胞分裂来实现。
细胞分裂包括有丝分裂和无丝分裂两种形式。
有丝分裂是指通过有丝分裂纺锤体的形成和消失来实现染色体的准确分离,从而产生两个与母细胞基因组完全相同的子细胞。
无丝分裂则是指细胞核直接分裂,没有明显的纺锤体形成。
3. 癌症的发展过程癌症的发展是一个复杂的过程,涉及到多个细胞生物学过程的紊乱。
癌症的发展过程包括癌前病变、原位癌、浸润癌和转移癌四个阶段。
癌前病变是指正常细胞发生遗传变异和表观遗传变化,逐渐演变为癌细胞前体。
原位癌是指癌细胞仅局限于原发病灶,没有浸润到周围组织。
浸润癌是指癌细胞侵犯周围组织和器官。
转移癌是指癌细胞通过血液循环或淋巴系统迁移到其他部位。
4. 细胞增殖与癌症的关系细胞增殖在癌症的发展中起到了重要的作用。
癌细胞的异常增殖导致肿瘤的形成和扩大。
细胞增殖过程中的遗传变异和表观遗传变化是癌症发展的重要驱动力。
癌细胞通过激活增殖信号通路和抑制凋亡信号通路,促进自身的不受控制的增殖。
此外,癌细胞还可以通过改变细胞周期调控、增加血管生成和抑制免疫应答等机制来促进细胞增殖和肿瘤的发展。
5. 结论与展望细胞增殖与癌症之间存在着密切的关系。
深入研究细胞增殖的机制和癌症的发展过程,有助于揭示癌症发生发展的机制,并为癌症的预防和治疗提供新的思路和方法。
细胞学作业第十四章 细胞增殖调与癌细胞

一、简述p34^cdc2/cyclin B蛋白激酶的发现过程。
Tim Hunt 为代表的科学家以海胆卵为材料,对细胞周期调控进行了深入研究。
JR.Evans 等人于1983年报道,在海胆卵细胞中含有两种特殊蛋白,它们的含量随周期过程变化而变化,一般在细胞间期内积累,在细胞分裂期内消失,在下一个周期有重复这一过程,因而它们将其命名为周期蛋白。
随后的研究证明:周期蛋白为诱导蛋白进入M期所必须。
各种生物之间的周期蛋白在功能上有着广泛的互补性。
将海胆cyclin B的mrna引入到非洲爪蟾卵非细胞系中,其翻译产物可诱导该非细胞体系进行多种细胞周期循环。
接下来的一系列实验提示周期蛋白可能参与MPF的功能调节。
二、举例说明CDK在细胞周期中是如何执行调节功能的?细胞周期调控包括正调控、负调控和信号反应。
CDK激酶是正调控因子,它是细胞沿周期运行的引擎蛋白。
以MPF为例阐述:MPF是一种使多种底物磷酸化的蛋白激酶,即CDK1激酶,由p34蛋白和周期蛋白B结合而成。
CDK1激酶活性首先依赖于周期蛋白B含量的积累。
周期蛋白B一般在G1期的晚期开始合成,通过S期,其含量不断增加,达到G2期,其含量达到最大值,CDK1激酶的活性随着周期蛋白B浓度变化而变化。
CDK1激酶的活化还受到激酶与磷酸酶的调节。
活化的CDK1激酶可使更多的CDK1激酶活化。
随着周期蛋白B 含量达到一定程度,CDK1激酶活性开始出现,到G2晚期阶段,CDK1激酶活性达到最大值并一直维持到M期的中期阶段。
活化的CDK1激酶促使分裂期细胞在分裂前期执行下列生化事件:(1)染色质开始浓缩形成有丝分裂染色体;(2)细胞骨架解聚,有丝分裂纺锤体开始组装;(3)高尔基复合体、内质网等细胞器解体,形成小的膜泡。
在有丝分裂的后期,活化的后期促进因子APC主要介导两类蛋白降解:后期抑制因子和有死分裂周期蛋白。
前者维持姐妹染色单体粘连,抑制后期启动;后者的降解意味着CDK1激酶失去活性,有死分裂即将结束,即染色体开始去凝集,核膜重建。
第十四章 细胞增殖调控与癌细胞

二、p34cdc2激酶的发现及其与MPF的关系
温度敏感株 cdc基因调控酵母细胞分裂和细胞周期(cdc2, cdc25, cdc28等) MPF催化亚单位(p32) cdc2基因突变导致细胞停留在G2/M期交界处
p34cdc2 p34cdc28
cdc28基因突变导致细胞停留在G1/S期交界处 或G2/M期交界处
17
The pathogenesis of cancer metastasis
18
二、癌基因与抑癌基因
癌症主要是由携带遗传信息的DNA的病理变化而引起的疾病 遗传病:生殖细胞DNA突变 癌症:体细胞DNA突变 (生殖细胞某些基因位点的突变会加大癌变的可能性) 癌基因(oncogene):控制细胞生长和分裂的一类正常基因,其突变能引起 正常细胞发生癌变。
ATR/CHK1介导 DNA复制检验点
15
六、其他因素在细胞周期调控中的作用
癌基因 抑癌基因 (p53, Rb)
细胞和机体的外在因素 离子辐射、化学物质作用、病毒感染、温度变化、PH变化等
16
第二节 癌细胞
一、癌细胞的基本特征
动物体内因细胞分裂调节失控而无限增殖的细胞称为肿瘤细胞(tumor cell); 具有转移能力的肿瘤细胞称为恶性肿瘤(malignancy); 源于上皮组织的恶性肿瘤称为癌 (目前已成为恶性肿瘤细胞的通称)。
抑癌基因或其编码的蛋白质的主要功能可概括为3类: ① 偶联细胞周期与DNA损伤 ② 与细胞凋亡有关 ③ 与细胞黏着有关
21
原癌基因- 显性突变
抑癌基因- 隐性突变
22
控制细胞生长和增殖,并与肿瘤发生相关的7类蛋白
23
细胞信号调控网络及肿瘤发生相关的主要调控因子
第14章+细胞增殖调控与癌细胞

33
六、细胞周期运转调控
1. G2/M期转化与CDK1激酶的关键性调控作用 2. M期周期蛋白与分裂中期向后期转化 3. G1/S期转化与G1期周期蛋白依赖性Cdk激酶 4. S/G2期转化与DNA复制检验点
34
1. G2/M期转化与CDK1激酶的关键性调控作用
• CDK1激酶即MPF,由p34cdc2蛋白和周期 蛋白B结合而成。p34cdc2蛋白在细胞周期中 的含量相对稳定,而周期蛋白B一般在G1 期的晚期开始合成,S期含量不断增加, 到G2期含量达到最大。因此,CDK1激酶 活性在G2期晚期达到最大并一直维持到M 期的中期阶段。
Cyclin B-Cdk1 (Cdc2)
G1 Substrates
S Substrates
G2/M Substrates
Growth and Morphogenesis
DNA Replication
Mitosis 26
五、Cdk激酶抑制因子
• 哺乳动物Cdk抑制因子 (Cdk inhibibitors, CKIs) ,包括Cip/Kip家族和INK4家族。
13
14
三、细胞周期蛋白(cyclin)
1983年Evans等报道在海胆卵细胞中存在一种特 殊蛋白质,这种蛋白含量随细胞周期进程变化 而变化,将这种蛋白称为周期蛋白(cyclin)。
已从多种生物体发现细胞周期蛋白,如酵母的 Cln1、Cln2、Cln3、Clb1~Clb6,高等动物的周 期蛋白A1、A2、B1、B2、B3、C、D1、D2、 D3、E1、E2、F、G、H、L1蛋白在细胞周期 调控中的作用
在DNA出现损伤时,P53 作为转录激活因子诱导 P21基因的表达,P21蛋白 能够同CDK-周期蛋白复合 物结合并将细胞阻止在G1 期或G2期。同时,P21蛋 白与增殖细胞核抗原
植物生理学第十四章 细胞增殖及其调控

第二节 癌细胞
癌细胞的基本特征 癌基因与抑癌基因 肿瘤干细胞
动物体内因分裂调节失控而无限增殖的细胞称为肿瘤细 胞。
具有转移能力的肿瘤称为恶性肿瘤;上皮组织的恶性肿 瘤称为癌。
癌细胞与正常分化细胞明显不同的一点: 正常分化细胞:细胞类型各异,但都具有相同的基因组; 癌细胞:细胞类型相近,但基因组却发生不同形式的改变。
肿瘤的发生频率会高吗?
第一、绝大数基因突变位点不会致癌 第二、单一基因的突变不会发生癌症,多个基因突变逐 渐形成癌细胞的特征
癌症会遗传吗?
生殖细胞中原癌基因或肿瘤抑制因子发生致 癌突变——癌变发生所需要的基因突变数积 累时间减少,家族成员更易患癌症
白血病:血细胞恶性增生——少数基因发生 突变,便可导致癌症发生,患病年龄较早
Dr. Folkman’s War: endostatin(内皮他丁)
研究细胞增殖调控的意义
G1
S
G2
Cytokinesis
M
基于细胞周期的癌症治疗药物研发进展
本章小结
促成熟因子(MPF)=p34cdc2(周期蛋白依赖性激酶) +clyclin B (周期蛋白)
周期蛋白:不同的周期蛋白在细胞周期中表达的时间不同 ,与不同的CDK结合调节其活性
植物生理学第十四章 细胞增殖及其 调控
重点:MPF的组成及作用;细胞周期运 转调控;癌细胞的基本特征;癌基因与 抑癌基因;肿瘤干细胞
难点:细胞周期运转调控
第一节 细胞增殖调控
MPF(mitosis promoting factor)发现及其作用 p34cdc2激酶的发现及其与MPF的关系 周期蛋白 CDK激酶(cyclin-dependent kinase)和CDK抑制因子 细胞周期运转调控
第十四章 细胞增殖调控与癌细胞-yan

• • • the 32(34) kDa protein and the Cdc2 Cell, 54, 433-439 , 1988
非洲爪蟾:MPF : 裂殖酵母:P34cdc28 芽殖酵母 P34cdc2
P32+P45
+P56cdc13
CDK1
海胆卵:cyclinA cyclinB
MPF主要 成分
SCF底物特异性的识别是由F-box 蛋白来决定的
SCF通过降解不同时期不同底物从而在 整个细胞周期中都发挥作用
确保每一周期DNA只复制一次的机制
在G1期ORC(复制 起始点识别复合物)结 合起始复制点,Cdc6和 Cdt1被募集到ORC上, 在ATP供能下,促进6个 亚单位构成的Mcm复合 体和其他一些蛋白结合 到ORC上,形成前复制 复合体(pre-RC), DNA复制获得执照。 Mcm 实际上就是 DNA解旋酶。随着DNA 的复制, Mcm逐渐减少, 复制结束消失。 Mcm存在于细胞质 中,只有在M期细胞核 膜破裂时才有机会和染 色质结合。
(二)M期周期蛋白与分裂中期向分裂后期转化
① M期周期蛋白A和B在分裂中期与CDK1分离,在激活APC (Anaphase Promoting Complex)的介导下,通过泛素依赖性途径降解)。 ② CDK1激酶活性消失,细胞由中期向后期转化,完成一个细胞周期。
。
APC至少由15种成分组成,分别为APC1-APC15。在人体和酵 母中都分别鉴定出13种. APC 正调控因子: Cdc20/Fizzy和Cdh1/Fzy; 负调控因子:Emi1、 Emi2、Mad2、BubR1等。 Cdc20 和Mad2蛋白位于动粒上,在微管与动粒结合以前,不 能从动粒上释放。 • 当微管正确结合到动粒上时,可能改变着丝粒相关蛋白的构象,从 而影响BubR1 等的活性,使Mad2 与Cdc20脱离动粒,这时APC才有活 性,启动细胞向后期转换.
第十四章细胞增殖调控与癌细胞

第十四章细胞增殖调控与癌细胞细胞周期的有序运转第十四章细胞增殖调控与癌细胞第一节细胞增殖调控Clock Theory Domino Theory一、MPF的发现及其作用研究背景1970s Rao和Johnson发现与M期细胞(Hela)融合的间期细胞染色体发生凝缩,称为早熟凝集染色体(prematurelycondensed chromosome,PCC)。
–G1期PCC为单线状,因DNA未复制。
–S期PCC为粉末状,因DNA由多个部位开始复制。
–G2期PCC为双线染色体,说明DNA复制已完成。
甚至不同类的M期细胞也可诱导PCC产生,说明M期细胞具有促进间期细胞进行分裂的因子,即成熟促进因子(maturation promoting factor,MPF)。
G期细胞与M期细胞融合S期细胞与M期细胞融合1G 2期细胞与M期细胞融合PCC成熟促进因子(maturation promoting factor,MPF ),早期称为M-期促进因子(M-phase promoting factor, MPF),是指M期细胞中存在的促进细胞分裂的因子MPF的发现及组成卵细胞提取物注射实验把M 期细胞的细胞质注射到卵细胞,发现可以促进卵细胞成熟分裂,继续用该卵细胞细胞质诱导新的卵细胞,仍然可以促进卵细胞成熟分裂。
因而他们推测M 期细胞中必然有一种物质可以诱导卵细胞成熟分裂,即促细胞成熟因子(maturation promoting factor, MPF )。
1960s Leland Hartwell,1970s Paul Nurse 以芽殖酵母和裂殖酵母为实验材料,利用温度敏感突变株,发现许多与细胞分裂有关的基因(cell division cycle gene, CDC)。
如:–裂殖酵母cdc2、芽殖酵母cdc28突变型在限制温度下无法分裂;–wee1突变型则提早分裂,cdc25突变型细胞体积增大而不分裂;–cdc2和cdc28都编码一个34KD的蛋白激酶,促进细胞周期的进行,weel和cdc25分别表现为抑制和促进CDC2的活性。
第十四章 细胞增殖调控与癌细胞

结果 找到cdc基因,如cdc28,表达蛋白为 34kDa,称为p34cdc28
结论 第二个被分离出来的cdc基因; 突变后细胞停留在G1/S或G2/M期 。
cdc2: 第一个被分离出来的cdc基因,表达蛋白为p34cdc2 特点:突变后裂殖酵母细胞停留在G2/M期
cdc28: 第二个被分离出来的cdc基因,表达蛋白为p34cdc28 特点:突变后芽殖酵母细胞停留在G1/S或G2/M期
结论
在成熟的卵母细胞中,必定有一种物质,能诱导卵 母细胞成熟,这种物质称为成熟促进因子(MPF)
卵细胞细 胞质移植 实验
成熟卵母细胞中 的物质能诱导卵 母细胞成熟
实验三 时间 研究者 步骤
1988 Maller et al
以2和p45两种蛋白。p32和p45结合后, 表现出蛋白激酶活性,能使多种蛋白质底物磷酸化
1、CDK
通过Pdc2同类基因,不同物种的cdc2基因编 码的蛋白质都含有一段相似序列,并且都能和周期蛋白结合, 将其作为调节亚基,进而表现出激酶活性。它们被统称为周 期蛋白依赖性蛋白激酶(cyclin-dependent kinase),简称 CDK。
A: G1期DNA未复制,超前染色体为单线性; B:S期DNA正在复制,超前染色体为点状,很多复制起始点;
C:G2期DNA复制完毕,超前染色体为双线性。
实验二 时间
研究者
1971 Masui和Markert
步骤
用解剖的方法分离非洲爪蟾第IV期卵母细胞, 孕酮诱导成熟后进行细胞质移植实验
结果
孕酮诱导成熟的卵母细胞的细胞质 能诱导其他卵母细胞的成熟
已经发现CDK1-CDK13等CDK激酶。
(1)与不同类型的周期蛋白相结合的CDK
细胞生物学:第14章 细胞增殖调控与癌基因

一、癌细胞的基本特征
1.细胞生长与分裂失去控制,具有无限增殖能力, 成为“永生”细胞,破坏正常组织的结构与功能;
2.具有侵润性和转移性 良性肿瘤仅存在于某些组织的特定部位,不会转移 恶性肿瘤的细胞间粘着性下降,容易转移到身体的 其它部位增殖,产生次级肿瘤(转移灶)
肝癌细胞的扩散性
转移灶
3. 细胞间相互作用改变 正常细胞通过相互识别,形成特定组织和器官;癌 细胞异常表达某些膜受体蛋白,与别处细胞粘着与 生长
调节亚基:周期蛋白(cyclin)
催化亚基: 丝氨酸/苏氨酸型蛋白激酶 其活性有赖于周期蛋白,故称周期依赖性蛋白激酶 (cyclin-dependent protein kinases, Cdks),
•CDK蛋白至少有12种:CDK1~CDK12 •周期蛋白也有多种:cyclin A1 A2 A3 B1 B2 B3 C D1等
第二节 癌细胞(Cancer cell)
癌症是一种严重威胁人类生命安全的疾病。动物体 内细胞分裂调节失控而无限增殖的细胞称为肿瘤细 胞(tumor cell)。具有转移能力的肿瘤称为恶性肿瘤 (malignancy)。上皮组织的恶性肿瘤称为癌。
正常细胞通过分化形成组织器官;而癌细胞的细胞 类型趋于一致,破坏有机体的组织器官,并且基因 组也发生不同形式的突变
第14章 细胞增殖调控与癌细胞
重点内容
•MPF的实质以及检验点 •癌细胞的基本特征 •癌基因与抑癌基因
第一节 细胞周期调控
一、MPF的发现及其作用
MPF( maturation promoting factor,卵细胞促成 熟因子)或M期促进因子,是M期细胞中存在的促进 细胞分裂的因子
MPF的发现
4.mRNA表达谱及蛋白表达谱或蛋白活性改变
细胞13.细胞增殖调控与癌细胞

细胞13.细胞增殖调控与癌细胞●细胞增殖调控●调控因子●mitosis-promoting factor, MPF 细胞有丝分裂促进因子定义:也称卵细胞成熟促进因子或M期促进因子,是催化亚基cdc2蛋白和调节亚基周期蛋白共同组成的蛋白质复合物,具有蛋白激酶活性,促进细胞从G_2期进入M期●(1970年)Johnson&Rao将Hela细胞的M期细胞与间期细胞融合,发生了形态各异的早熟染色体凝缩(premature chromosome condensation, PCC)早熟凝缩染色体定义:将M期细胞与G_1、S、G_2期细胞融合并继续培养一定时间后,融合细胞的染色体提前凝缩,形态各异G_1期PCC为细单线S期PCC为粉末状G_2期PCC为双线染色体状提示可能存在诱导染色体凝缩的因子●(1971年)Masui&Markert,非洲爪蟾卵,孕酮刺激生发泡破裂注射诱导卵母细胞成熟●p34^{Cdc2}激酶(MPF的催化亚单位)●Cdc2:CDC基因调控酵母细胞分裂和细胞周期,Cdc2是第一个被分离出来的CDC基因,Cdc2基因突变导致细胞停留在G_2/M期交界处●p34^{Cdc2}是Cdc2基因的表达产物,具有蛋白激酶活性,在裂殖酵母细胞周期调控过程中促进G_2/M期转换●Cdc28:芽殖酵母中的一个关键性CDC基因,其产物p34^{Cdc28}也是一种蛋白激酶,调节G_2/M期和G_1/M期转换●验证得知p34^{Cdc2}是MPF的同源物●本身不具有激酶活性,只有当其与有关蛋白质结合后,其激酶活性才能够表现出来●cyclin 周期蛋白(MPF的调节亚单位)定义:在细胞中的含量随细胞周期进程变化而变化的蛋白质,对细胞周期循环具有调节作用●分类●G_1期周期蛋白定义:某些只在G_1期表达并只在G_1期和S期转化过程中执行调节功能的周期蛋白,如cyclin C、D、E、Cln1、Cln2、Cln3等●M期周期蛋白定义:某些虽然在间期表达和积累,但到M期时才表现出调节功能的周期蛋白,如cyclin A、B等●特点●存在时间:G_1期周期蛋白在细胞周期中存在的时间相对较短,M期周期蛋白在细胞周期中则相对稳定●结构●均含有一段相当保守的氨基酸序列,成为cyclin box 周期蛋白框,其功能是介导周期蛋白与CDK结合●M期周期蛋白近N端含有一段由9个氨基酸残基组成的特殊序列,称为destruction box 破坏框,参与泛素依赖性的cyclin A、B的降解●G_1期周期蛋白分子中不含破坏框,但其C端含有一段特殊的PEST序列,与G_1期周期蛋白的更新有关●与CDK结合特点:不同的周期蛋白在细胞周期中表达的时期不同,并与不同的CDK结合,调节不同的CDK活性●cyclin A在G_1期的早期即开始表达并逐渐积累,到达G_1/S期交界处,其含量达到最大值并一直维持到G_2/M期●cyclin B从G_1期的晚期开始表达并逐渐积累,到G_2期后期阶段达到最大值并一直维持到M期的中期阶段,然后迅速降解●cyclin D在细胞周期中持续表达●cyclin E在M期的晚期和G_1期早期开始表达并逐渐积累,到达G_1期的晚期其含量达到最大值,然后逐渐下降,到达G_2期的晚期,其含量降到最低值●cyclin-dependent kinase, CDK 周期蛋白依赖性蛋白激酶、(CKI)CDK抑制因子●CDK定义:可以与周期蛋白结合,并以周期蛋白作为调节亚单位,表现出蛋白激酶活性●mitosis-promoting factor, MPF 细胞有丝分裂促进因子是一种CDK(CDK1)●特点●各种CDK分子均含有一段类似的CDK激活结构域●不同的CDK所结合的周期蛋白不同,在细胞周期中执行的调节功能也不相同●细胞内存在多种因子,修饰CDK的分子结构,参与CDK活性的调节●CKI:对CDK活性起负调控的蛋白质●细胞周期运转调控●G_2/M期检查点(cyclin B-Cdk1)●Cdk1(MPF)由p34^{Cdc2}和cyclin B(A)结合而成●p34^{Cdc2}在细胞周期中的含量相对稳定,主要变化在于周期蛋白含量●(主)cyclin B(A)的含量呈现周期性变化在G_1期的晚期开始合成,通过S期,其含量不断增加,到达G_2期,其含量达到最大值●(副)进一步的修饰:在Wee1/Mik1激酶和CDK活化激酶作用下发生3次磷酸化,在蛋白磷酸水解酶Cdc25C作用下发生2次去磷酸化三个磷酸化位点:Thr14、Tyr15、Thr161 Thr161位点保持磷酸化使Cdk1活性表现所必需的●下游作用使某些底物蛋白磷酸化,改变其下游的某些靶蛋白的结构和启动其功能,实现其调控细胞周期的作用●磷酸化组蛋白H1:促进染色质凝缩●磷酸化核纤层蛋白:促使核纤层解聚●磷酸化核仁蛋白:促使核仁解体●磷酸化p60^{c-Src}蛋白:促使细胞骨架重排●磷酸化c-Abl蛋白:促使细胞形态调整●中/后期检查点(APC)●anaphase-promoting complex, APC 后期促进复合物●定义:在分裂间期表达,M期表现出活性,可以调节M期周期蛋白泛素化依赖降解途径,以及其他一些与细胞周期调控有关的非周期蛋白类蛋白质的降解●在APC的作用下,M期cyclin A&B通过泛素化依赖途径被蛋白酶体降解这一过程中破坏框起着重要的调节作用●Mad2的负调控作用(有丝分裂中后期转换)Cdc20能活化APC并降解抑制分离酶的securin,进而导致中后期转换●Mad2定位在早中期和错误排列的中期染色体的动粒上,纺锤体组装不完全,动粒不能被动粒微管捕捉,Mad2则不能从动粒上解离下来●当纺锤体组装完成以后,动粒全部被动粒微管捕捉,Mad2从动粒上消失,从而解除对Cdc20的抑制作用,促使APC活化,导致M期周期蛋白降解●G_1/S期检查点(cyclin E/A-Cdk2、cyclin D-Cdk4/6)●主要的G_1期周期蛋白-CDK●cyclin D-Cdk4/6●cyclin D为细胞G_1/S期转化所必需●Cdk4/6的底物Rb蛋白是转录因子E2F的抑制因子,是G_1/S期转化的负调控因子,在G_1期的晚期阶段通过磷酸化而失活如果细胞Rb突变,失去对E2F的抑制,使细胞无法停留在G_1期,会导致细胞过度增殖●cyclin E-Cdk2●主要出现在G_1期晚期到S期的早期阶段,为S期启动所必需●transforming growth factor β, TGFβ 转化生长因子β可以有效地抑制cyclin E-Cdk2活性,进而将细胞阻止在G_1期●cyclin E-Cdk2与类Rb蛋白p107和E2F结合形成复合物,Cdk2催化p107磷酸化,使其不能抑制E2F,E2F促进有关基因的转录,促使细胞周期由G_1期向S期转化●cyclin A-Cdk2●cyclin A的合成开始于G_1/S期转化时期●进入S期后,cyclin A-Cdk2激酶成为该时期主要的CDK●cyclin A-Cdk2与DNA复制有关,位于DNA复制中心●G_1期周期蛋白通过SCF泛素化途径降解●同时需要G_1期CDK活性的参与●SCF具有E3泛素连接酶的功能,它可以被F-box蛋白活化,进而催化底物蛋白的泛素化●其他DNA复制起始活动的调控●DNA复制起始点的识别(ORC、Cdc6、Cdc45)●DNA复制执照因子学说(Mcm蛋白)●S/G_2/M期转换与DNA复制检查点将细胞停滞在S期和G_2/M期●intra-S phase checkpoint S期内部检查点定义:在S期内发生DNA损伤如DNA双链发生断裂时,S期内部检查点被激活,从而抑制复制起始点的启动,使DNA复制速度减慢,S期延长,同时激活DNA修复和复制叉的恢复等机制●通过染色体结构维持蛋白Smc1的磷酸化,从而实现S期的延长●通过ATM/ATR介导的Cdc25A磷酸酶过磷酸化而降解,从而抑制cyclinE/A-Cdk2活性●replication checkpoint DNA复制检查点由于停滞的复制叉导致的S期的延长的机制,主要是由ATR/Chk1激活来介导的●ATR/Chk1介导Cdc25A降解进而抑制cyclin E/A-Cdk2的通路,减缓整体DNA复制的效率●DNA损伤检查点p53含量提高→ p21表达→ cyclin E-CDK2失活●抑癌基因p53表达产物p53蛋白对细胞增殖起负调节作用●调控机制:p53本在细胞中含量极少(被Mdm2泛素化降解),DNA受损后,Chk1&Chk2使p53磷酸化并与Mdm2解离,p53蛋白浓度上升,作为转录因子调控p21表达,使cyclin E-Cdk2失活,不能进入S期●多细胞生物:若DNA无法修复,则发生p53介导的细胞凋亡●癌细胞●cancer cell 癌细胞●定义:脱离了细胞社会制约,表现出细胞增殖失控,并且有侵袭和转移等特征的细胞,癌细胞会破坏组织和器官的正常生理功能●分类●tumor cell 肿瘤细胞动物体内因细胞分裂调节失控而无限增殖的细胞●malignancy 恶性肿瘤具有转移能力的肿瘤●cancer 癌源于上皮组织的恶性肿瘤●benign tumor 良性肿瘤分裂缓慢,具有结缔组织包膜而不扩散的肿瘤●基本特征●细胞生长与分裂失去控制癌细胞失去控制,称为“不死”的细胞,核质比例增大,分裂速度加快,破坏了正常组织的结构与功能●具有浸润性和扩散性癌细胞细胞间黏着性下降,易于浸润周围健康组织,或通过血液循环和淋巴途径转移并在其他部位黏着和增殖。
细胞增殖与癌症治疗

细胞增殖与癌症治疗细胞增殖是生物体生长和修复组织的关键过程之一,同时也是引发癌症发展的重要因素之一。
癌症是一种由异常细胞不受控制地增殖而引起的严重疾病。
因此,研究细胞增殖与癌症治疗之间的关系对于癌症的预防和治疗具有重要意义。
一、细胞增殖的基本机制细胞增殖是指细胞按照一定的规律进行繁殖和分裂的过程。
正常情况下,细胞增殖是受到严格的调控,包括细胞周期调控、生长因子的影响等。
细胞周期包括G1期、S期、G2期和M期四个阶段,细胞在不同的阶段执行不同的功能。
在细胞增殖中,细胞周期调控蛋白激酶和检查点蛋白等起着重要的调控作用。
这些蛋白能够判断细胞是否准备好进入下一个细胞周期阶段,以保证细胞增殖的正常进行。
此外,生长因子通过与细胞表面受体的结合,可以促进或抑制细胞增殖。
二、细胞增殖与癌症的关系细胞增殖异常是癌症发展的主要特征之一。
在肿瘤中,癌细胞的增殖速度明显快于正常细胞,而且无法受到细胞周期调控的约束。
癌细胞能够突破细胞周期阻滞点和生长因子抑制,导致无限制的细胞增殖。
这种异常的细胞增殖过程可能涉及多个信号通路的紊乱。
例如,癌细胞可以通过突变或过度表达细胞周期调控蛋白来促进细胞增殖。
此外,失活细胞凋亡通路、激活血管生成通路等也可以为癌细胞提供增殖的有利条件。
三、癌症治疗中的细胞增殖干扰针对癌症治疗中的细胞增殖异常,研究者们积极探索干预方法,以期阻断癌细胞的异常增殖。
1. 细胞周期调控蛋白靶向治疗细胞周期调控蛋白在癌症治疗中成为了重要的靶点。
通过针对不同的细胞周期调控蛋白进行药物靶向干预,可以有效地抑制癌细胞的增殖。
例如,CDK抑制剂、p53激活剂等药物已经用于临床治疗,显示出了潜在的抗肿瘤活性。
2. 生长因子信号通路干扰生长因子信号通路在肿瘤发展中起着关键作用。
通过干扰生长因子信号通路,可以抑制癌细胞的增殖。
目前,许多抗癌药物已经被开发出来,针对过度表达的受体酪氨酸激酶进行抑制。
3. 细胞凋亡诱导剂的应用细胞凋亡是机体对异常细胞进行规范性消除的重要途径。
细胞增殖与癌症治疗的关系

细胞增殖与癌症治疗的关系随着医学科技的不断发展和人们健康意识的提高,癌症已经成为当今社会最重要的健康问题之一。
癌症是一种细胞增殖异常的疾病,而细胞增殖是指体内生物在生长发育和修复组织的过程中进行的一项重要功能。
在正常情况下,细胞增殖是有一定调控和限制的,但在一些情况下,如某些基因变异或蛋白质表达异常,细胞就可能失控增殖,进而导致癌症的发生。
因此,研究细胞增殖与癌症的关系,对于癌症的预防和治疗具有重要意义。
本文将从细胞增殖机制和癌症治疗两个方面探讨这一问题。
一、细胞增殖的机制细胞增殖是细胞分裂和增生的过程,分为三个阶段:G1阶段、S阶段和G2/M阶段。
其中,S阶段是DNA合成期,细胞在此期间进行DNA复制,从而让细胞能够分裂。
细胞增殖过程是由一系列蛋白质信号通路调控的,涉及到细胞周期检查点控制系统、细胞自噬和凋亡途径等多种调控机制。
细胞周期检查点控制系统是细胞增殖调控的一个重要组成部分。
它包括两个检查点(G1/S和G2/M)、三个关键控制因子(cyclin-dependent kinases,CDKs)和诸多辅助因子,通过调节CDK活性和裂解酶的调控作用,通过对细胞周期的调控来维持正常的细胞增殖。
同时,细胞因子、激素、生长因子等各种信号分子也可以通过调节这些检查点来影响细胞增殖。
细胞自噬是细胞通过降解细胞内部的蛋白质分子和囊泡组分来维持细胞稳态的一种重要反应。
细胞自噬在调控细胞增殖和凋亡中也扮演着关键角色。
在正常情况下,细胞自噬可以清除受损或老化的细胞器和细胞成分,同时也可以降解细胞周期相关因子,并在某些情况下调控细胞凋亡等信号通路,以维持正常的细胞增殖和细胞稳态。
细胞凋亡是指当细胞暴露在危险环境或者细胞自身存在重大问题时,细胞会受到死亡信号,引发细胞自我消化和死亡。
细胞凋亡对于维持正常细胞增殖有着重要的调节作用。
在正常情况下,细胞凋亡通路会清除乏味,过时或者有问题的细胞。
在某些癌症类型中,凋亡途径会被一些信号调节,以促进癌细胞增殖。
细胞增殖调控与癌细胞
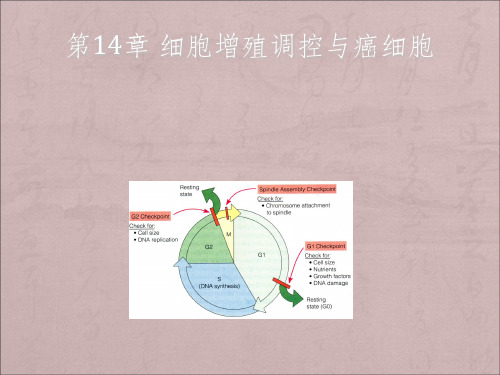
细胞周期中的主要的检验点
G1/S检验点 :启动DNA的复制 S期检验点:检验DNA复制是否完毕 G2/M检验点:能否开始分裂 中-后期检验点:纺锤体组装的检验
细胞周期调控系统
+ 细胞周期调控系统的关键组分
周期性活化和失活的蛋白激酶
+ MPF的发现及其作用 + MPF与 CDK激酶 (周期蛋白依赖性蛋白激酶) + 细胞周期蛋白(cyclin)的作用
5)体外培养的恶性转化细胞特征
体外培养的恶性转化细胞的特征
+ 恶性转化细胞同癌细胞一样具有无限增殖 的潜能;
+ 在体外培养时贴壁性下降; + 失去接触抑制; + 培养时对血清依赖性降低; + 当将恶性转化细胞注入易感动物体内,往
往会形成肿瘤。
二、癌基因与抑癌基因——肿瘤形成的 内因
涉及到两大类与细胞增殖相关的基因的突变: ●促进细胞增殖相关基因突变: 原癌基因(proto-oncogene)突变形成癌基因(oncogene) ●抑制细胞增殖相关基因突变: 肿瘤抑制基因(tumor-suppressor gene),抑癌基因 细胞癌变是基因突变累积和自然选择的结果,所以患者
多为年长者。 原癌基因与肿瘤抑制基因产物协调作用,避免细胞癌变
1、癌基因( oncogenes)
+ 癌基因 oncogenes, onc :可引起细胞癌变的基因,是调 控细胞增殖、分裂和生长的正常基因(原癌基因)的突 变形式。
+ 原癌基因proto-oncogenes:细胞中调控细胞增殖、分裂 和生长的一类正常基因(促进因子),当其突变会促进 癌症的发生(即变成癌基因)。
四、肿瘤干细胞
判断依据 + 肿瘤细胞异种移植实验——需要一定数量 + 化疗药物不能彻底杀死种肿细胞 实验证明 1977年分离白血病肿瘤干细胞(Cancer stem cell) 既具有干细胞自我更新和无限增殖的特性,又失去
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
Amphibian oocytes and early embryos of frogs
(引自翟中和等,2011)
Masui and Markert’s experiments (J. Exp. Zool. 1971, 177: 142)
What’s the role of hormone? Trigger protein synthesis
By cyclin
mitosis
mitosis
Cyclin concentration
interphase
interphase
By phosphatase and Kinase
Cell-cycle control system: cyclically activated protein kinases
2. MPF: transition from G2 to M
Maturation-promoting factor / Mitosis-promoting factor
(引自翟中和等,2011)
1978, MPF activity undergoes dramatic fluctuations in cleaving eggs that correlate with changes in the cell cycle
Mitosis
Mitosis
Mitosis
MPF activity
Cdc2
MPF has protein kinase activity
cyclin
M phase Cyclin-Cdk (MPF) (Cyclin-dependent protein kinase)
cyclin-dependent kinase (Cdk)
MPF的发现
• HeLa细胞融合:有丝分裂促进因子
(1) Discovery Does the cytoplasm of cells contain regulatory factors that affect cell cycle activities?
(引自翟中和等,2011)
M phase HeLa cell with a rat kangaroo PtK2 cell, 1974, Humangenetik
cdc2-
Cdc2 encodes a protein kinase with 34kD whose activity is required for cells to enter M phase.(p34cdc2)
Hartwell found cdc28
• What is the relationship between cyclins or cdc2 and MPF? MPF purification: 1988 (Xenopus egg) MPF=32kD+45kD Cyclin B Cdc2
Interphase Interphase High Low
➢Tim Hunt found cyclin in 1983: sea urchin eggs
When the gel was developed on Friday 23 July 1982, I found that the strongest band early on suddenly got very much weaker at about the time when the eggs were about to divide in two. This was a stunning, startling discovery.“
35S-Met: Fertilized eggs
16 min 60 min 85 min 120 min
Samples after fertilized
Cyclin: in sea urchin eggs that is destroyed at each cleavage division.
Cell, 1983, 33:389-396
➢Nurse found cdc2
• In the mid-1970s as a postdoc studying the fission yeast S. pombe.
• Divide before they had reached full size: Mutants – wee:
Wee1,wee2
Regulation of cell proliferation
and cancer cells
细胞增殖调控与癌细胞
Section 1 Regulation of Cell Proliferation
1. Cell-cycle control system
and Checkpoints
Cell-cycle control system safely guides the cell through the events of the cell cycle
In most eucaryotic cells, the cell-cycle control system triggers cell-cycle progression at three major regulatory transitions, or checkpoints
(From the World of the Cell, 2000)
• 非洲爪蟾卵细胞提取物注射:MPF概念提 出
• 酵母温度敏感突变株:cdc基因,p34cdc2, Cdc28
• 海胆卵细胞:Cyclin的发现 •thMe P20F0生1 N化o成be分l P:rizCedfoc2r P和hyCsiyocloligny or Medicine
(2) Activation of MPF
• The wee2 gene was later
(University of Oxford)
renamed cell division cycle 2
(CDC2 is identical in function to
CDC28 from budding yeast 1982).
cdc2D
Normal
