定量分析计算例题
定量分析方法

Max(140,160,75)=160万元
最后,160万元对应的方案是B,就是被选中的决策方案;因 此,选择全部更新,购进新设备。
管理学
(2)悲观法。也称小中取大法。这种方法决策是建立在 决策者对未来形势估计非常悲观的基础上的,故从最坏的结 果中选最好的。
仍以上题为例。 A方案(改造原有设备):Min(100,75,20)=20万元 B方案(全部购进新设备):Min(160,65,10)=10万元
状态方案 较好 (0.5) 30 一般 (0.3) 20 较差 (0.2) 8
购置新机器
改造旧机器
25
21
16
管理学
第一步,绘制决策树。首先从左端决策点出发,按备选 方案引出相应的方案枝,每条方案枝上注明所代表的方案; 然后,每条方案枝到达一个方案的结点,再由各方案结点引 出各个状态枝,并在每个状态枝上注明状态内容及其概率; 最后,在状态枝末端注明不同状态下的损益值。决策树完成 后,再在下面注明时间长度。如图7-6所示。
表7-6
各方案在不同情况下的损益值 销路好 销路一般 75 65 55
单位:万元 销路差 20 10 35
管理学
A方案 B方案 C方案
140 160 75
A方案(改造原有设备):Max(140,75,20)=140万元
B方案(全部购进新设备):Max(160,65,10)=160万元
C方案(购进关键设备):Max(75,55,35)=75万元 从三个方案的最大收益值中选择一个最大的收益值:
管理学
在上例中,在销路好自然状态下,B方案的收益最大,为 160万元。在将来发生的自然状态是销路好的情况下,如果管 理者恰好选择了这一方案,他就不会后悔,即后悔值为0。如 果他选择的不是B方案,而是其他方案,他就会后悔(后悔没 有选择B方案)。比如,他选择的是C方案,该方案在销路好时 带来的收益是75万元,比选择B方案少带来85万元的收益,即 后悔值为85万元。各个后悔值的计算结果见表7-7。
定量分析化学概论

第一章 定量分析化学概论 习题1. 某矿石的最大颗粒直径为10 mm ,若k 值为0.1 kg·mm -2,问至少应采取多少试样才具代表性?若将该试样破碎,缩分后全部通过10号筛,应缩分几次?若要求最后获得的分析试样不超过100 g ,应使试样通过几号筛?解:(1)m Q ≥kd 2 = 0.1 kg·mm -2 × (10mm)2 = 10kg ;至少应采10kg 试样才具代表性。
(2)10号筛筛孔直径d = 2.00mm (见51页表1-1);最小取样量为:kd 2 = 0.1kg·mm -2 × (2.00mm)2 = 0.4kg ;设:缩分次数为n ,10/2n ≥0.4, 解得n ≤4;所以应缩分4次。
(3)据m Q ≥kd 2,得d ≤k m Q= 1.0101003-⨯ = .1.0mm ; 查51页表1-1得:10号筛d = 2.00mm ,20号筛d = 0.83mm ;所以应使试样通过20号筛,可满足其要求。
2. 用氧化还原滴定法测得FeSO 4·7H 2O 中铁的质量分数为20.01%,20.03%,20.04%,20.05%。
计算:a.平均值;b.中位数;c.单次测量值的平均偏差;d.相对平均偏差;e.极差;f.相对极差。
解:a. ∑==n1i i x n 1x = 4%05.20%04.20%03.20%01.20+++ = 20.03%; b. x M = (x 2+x 3)/2 = (20.03%+20.04%)/2 = 20.04%;c. ∑=-=n1i i x x n 1d = 4%02.0%01.0%00.0%02.0+++ = 0.012%; d. Rd = %100xd ⨯= %100%03.20%012.0⨯= 0.06%; e. R = x max -x min = 20.05%-20.01% = 0.04%;f. %100xR ⨯= %100%03.20%04.0⨯= 0.2%3. 用沉淀滴定法测定纯NaCl 中氯的质量分数,得到下列结果:59.82%,60.06%,60.46%,59.86%,60.42%。
定量分析方法课程综合练习题
定量分析方法课程综合练习题说明:为了帮助大家巩固所学的定量分析基本方法,建立定量分析思维,特给出一下练习题,其中有些问题已列出了参考答案,没有给出参考答案的问题主要供大家讨论完成。
1. 为研究气温的变化情况,气象局对北方某城市1—2月份各天气的气温进行了记录,结果如下:-3 2 -4 -7 -11 -1 6 8 9 -6-14 -18 -15 -9 -6 -1 0 5 -4 -9-6 -8 -12 -16 -19 -15 -22 -25 -24 -19-8 -6 -15 -11 -12 -19 -25 -24 -18 -17-14 -22 -13 -10 -6 0 -1 5 -4 -9-3 2 -4 -4 -16 -1 7 3 -6 -5(1)指出上面的数据属于什么类型?(2)对上面的数据进行适当的分组;(3)作一个直方图,说明该城市气温分布的特点。
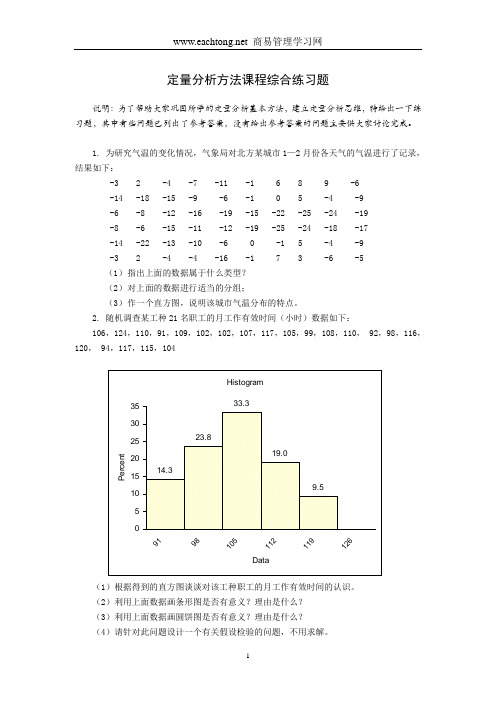
2. 随机调查某工种21名职工的月工作有效时间(小时)数据如下:106,124,110,91,109,102,102,107,117,105,99,108,110, 92,98,116,120, 94,117,115,104(1)根据得到的直方图谈谈对该工种职工的月工作有效时间的认识。
(2)利用上面数据画条形图是否有意义?理由是什么?(3)利用上面数据画圆饼图是否有意义?理由是什么?(4)请针对此问题设计一个有关假设检验的问题,不用求解。
3.某机关采购部的一个员工称他和少数其他几个员工几乎要干所有的活。
为了支持他的观点,他收集了以下的数据,即该部门在一个具有代表性的星期中16个员工每人处理的采购单数目。
计算该数据的集中趋势及离散程度所有测度指标。
对该员工的主张进行评论,是否少数员工几乎在做全部工作?12 22 8 14 15 32 17 24 20 37 15 23 16 40 19 21(均数=20.94,中位数=19.5,众数=15,标准差=8.55。
3-4 事故树的定量分析二

(3-20)
2
当求出一个事故树的最小割集后, 可直接运用 布尔代数的运算定律及式(3-21) 将相交和化为不 交和。但当事故树的结构比较复杂时, 利用这种直 接不交化算法还是相当烦琐。 而用以下不交积之和定理可以简化计算, 特别 是当事故树的最小割集彼此间有重复事件时更具优 越性。 不交积之和定理: 命题 1 集合 Er 和 Es 如不包含共同元素 , 则 应 Es 可用不交化规则直接展开。 命题 2 若集合 Er 和 Es 包含共同元素, 则
要度最大。
(2) 仅在同一最小割(径)集中出现的所有基本
事件结构重要度相等。
21
(3) 两个基本事件仅出现在基本事件个数相等 的若干最小割(径)集中, 这时在不同最小割 ( 径)集 中出现次数相等的基本事件其结构重要度相等; 出 现次数多的结构重要度大, 出现次数少的结构重要 度小。 (4) 两个基本事件仅出现在基本事件个数不等 的若干最小割(径)集中。在这种情况下, 基本事件 结构重要度大小依下列不同条件而定:
不变时, 顶事件状态也由不发生变为发生的情况。
17
用结构函数表示为:
φ(0i, Xj )=0; φ(1i, Xj )=1; φ(1i, Xj )-φ(0i, Xj )=1; 此时, 基本事件Xi发生直接引起顶事件发生, 基本
事件Xi 这一状态所对应的割集叫“危险割集”。若
改变除基本事件Xi以外的所有基本事件的状态,并取
7
⑴最小割集逼近法:
在式 (3-18) 中, 设:
则得到用最小割集求顶事件发生概率的逼近公 式, 即:
8
式 (3-22)中的F1,F1-F2,F1-F2+F3,……等 , 依 此给出了顶事件发生概率P(T)的上限和下限, 可根 据需要求出任意精确度的概率上、下限。 用最小割集逼近法求解 [ 例 3-8] 。 由式 (3-22) 可得 :
定量分析化学习题-推荐下载

第一章定量分析概论习题一1.将下列数据修约为两位有效数字3.667;3.651;3.650;3.550;3.649;pK a=3.664解:3.7;3.7;3.6;3.6;3.6;3.662.根据有效数字运算规则计算下列结果:(1)2.776+36.5789-0.2397+6.34(2)(3.675×0.0045)- (6.7×10-2)+(0.036×0.27)(3)50.00×(27.80-24.39)×0.11671.3245解:(1)45.46;(2)-0.040;(3)15.13. 测定镍合金的含量,6次平行测定的结果是34.25%、34.35%、34.22%、34.18%、34.29%、34.40%,计算(1)平均值;中位值;平均偏差;相对平均偏差;标准偏差;平均值的标准偏差。
(2)若已知镍的标准含量为34.33%,计算以上结果的绝对误差和相对误差。
解:(1)34.28%;34.27%;0.065%;0.19%;0.082%;0.034%(2)-0.05%;;-0.15%4. 分析某试样中某一主要成分的含量,重复测定6次,其结果为49.69%、50.90%、48.49%、51.75%、51.47%、48.80%,求平均值在90%、95%和99%置信度的置信区间。
解:置信度为90%的置信区间μ=(50.18±1.15)%置信度为95%的置信区间μ=(50.18±1.46)%置信度为99%的置信区间μ=(50.18±2.29)%14.用某法分析汽车尾气中SO2含量(%),得到下列结果:4.88,4.92,4.90,4.87,4.86,4.84,4.71,4.86,4.89,4.99。
(1)用Q检验法判断有无异常值需舍弃?(2)用格鲁布斯法判断有无异常值需舍弃?解:(1)无(2)4.71、4.99应舍去第二章滴定分析习题二1.市售盐酸的密度为1.19g/mL,HCl含量为37%,欲用此盐酸配制500mL0.1mol/L的HCl溶液,应量取市售盐酸多少毫升?(4.15mL)2.已知海水的平均密度为1.02g/mL,若其中Mg2+的含量为0.115%,求每升海水中所含Mg2+的物质的量n(Mg2+)及其浓度c(Mg2+)。
《定量分析简明教程》习题一参考答案

一、 选择题1、用同一NaOH 滴定相同浓度和体积的两种弱一元酸,则a K Θ较大的弱一元酸(B ) A 消耗NaOH 多;B 突跃范围大;C 计量点pH 较低;D 指示剂变色不敏锐。
2、滴定分析要求相对误差±0.1%,万分之一的分析天平绝对误差为±0.0001g ,则一般至少称取试样质量为(B )A0.1g ;B0.2g ;C0.3g ;D0.4g.3、以HCl 溶液滴定某碱样,滴定管的初读数为0.25±0.01ml ,终读数为32.25±0.01ml ,则用去HCl 溶液的准确体积为(D )A32.0ml ;B32.00ml ;C32.00±0.01ml ;D32.00±0.02ml 。
4、指示剂的变色范围越窄,则(A )A 滴定越准确;B 选择指示剂越多;C 变色敏锐;D 滴定越不准确。
5、溶液pH 降低,EDTA 的配位能力会(B ) A 升高;B 降低;C 不变;D 无法确定。
6、用KMnO 4法测定Ca 2+离子,所采用的滴定方式是(B )法 A 直接滴定法;B 间接滴定法;C 返滴定法;D 置换滴定法。
7、不同波长的电磁波,具有不同的能量,其波长与能量的关系为(B ) A 波长愈长,能量愈大;B 波长愈长,能量愈小;C 波长无能量无关。
8、在酸性条件下,莫尔法测Cl -,其测定结果(B ) A 偏低;B 偏高;C 正好;D 无法确定。
9、下列有关配体酸效应叙述正确的是(B ) A 酸效应系数越大,配合物稳定性越大;B 酸效应系数越小,配合物稳定性越大;CpH 越高,酸效应系数越大。
10、酸性介质中,用草酸钠标定高锰酸钾溶液,滴入高锰酸钾的速度为(B ) A 同酸碱滴定一样,快速进行;B 开始几滴要慢,以后逐渐加快; C 始终缓慢;D 开始快,然后逐渐加快,最后稍慢。
11、酸碱滴定中,选择指示剂可不考虑的因素是(D )ApH 突跃范围;B 要求的误差范围;C 指示剂的变色范围;D 指示剂的结构。
定量分析计算

标示量%
ms 标示量
100 %
第6页/共13页
(2)剩余滴定法
T(V0 V)F 平均片重
标示量%
ms 标示量
100 %
第7页/共13页
2. 紫外分光光度法 (1)吸收系数法
A E11c%ml 100
D V
平均片重
标示量%
ms 标示量
100%
第8页/共13页
(2)对照法
c对
A供 A对
第11页/共13页
2. 紫外分光光度法
(1)吸收系数法
标示量%
A E11c%ml 100
D
100%
c标示第1ຫໍສະໝຸດ 页/共13页(2)对照法标示量%
c对
A供 A对
D
100%
c标示
第13页/共13页
第六节 定量分析有关计算
一、原料药百分含量的计算 (一)滴定分析法 1.直接滴定法 含量% =V×T×F/m ×100% T(滴定度):指每毫升标准溶液相当于待
测组分的质量(g或mg)。 F(浓度校正因子):实际浓度/规定浓度
第1页/共13页
第六节 定量分析有关计算
2.剩余滴定法 含量% =(V0-V)×T×F×10-3/m ×100% T(滴定度):指每毫升标准溶液相当于待
测组分的质量(g或mg)。 F(浓度校正因子):实际浓度/规定浓度 例题:教材93-94页
第2页/共13页
第六节 定量分析有关计算
(二)分光光度法
1.对照品法 含量%=C对×
AA对样×V×D/m×100%
V:初次配制体积 D:稀释倍数
第3页/共13页
第六节 定量分析有关计算
2.吸收系数法
定量分析化学习题

第一章定量分析概论习题一1.将下列数据修约为两位有效数字=3.6643.667;3.651;3.650;3.550;3.649;pKa解:3.7;3.7;3.6;3.6;3.6;3.662.根据有效数字运算规则计算下列结果:(1)2.776+36.5789-0.2397+6.34(2)(3.675×0.0045)-(6.7×10-2)+(0.036×0.27)(3)50.00×(27.80-24.39)×0.11671.3245解:(1)45.46;(2)-0.040;(3)15.13. 测定镍合金的含量,6次平行测定的结果是34.25%、34.35%、34.22%、34.18%、34.29%、34.40%,计算(1)平均值;中位值;平均偏差;相对平均偏差;标准偏差;平均值的标准偏差。
(2)若已知镍的标准含量为34.33%,计算以上结果的绝对误差和相对误差。
解:(1)34.28%;34.27%;0.065%;0.19%;0.082%;0.034%(2)-0.05%;;-0.15%4. 分析某试样中某一主要成分的含量,重复测定6次,其结果为49.69%、50.90%、48.49%、51.75%、51.47%、48.80%,求平均值在90%、95%和99%置信度的置信区间。
解:置信度为90%的置信区间μ=(50.18±1.15)%置信度为95%的置信区间μ=(50.18±1.46)%置信度为99%的置信区间μ=(50.18±2.29)%14.用某法分析汽车尾气中SO含量(%),得到下列结果:4.88,4.92,4.90,24.87,4.86,4.84,4.71,4.86,4.89,4.99。
(1)用Q检验法判断有无异常值需舍弃?(2)用格鲁布斯法判断有无异常值需舍弃?解:(1)无(2)4.71、4.99应舍去第二章滴定分析习题二1.市售盐酸的密度为1.19g/mL,HCl含量为37%,欲用此盐酸配制500mL0.1mol/L的HCl溶液,应量取市售盐酸多少毫升?(4.15mL)2.已知海水的平均密度为1.02g/mL,若其中Mg2+的含量为0.115%,求每升海水中所含Mg2+的物质的量n(Mg2+)及其浓度c(Mg2+)。
物流管理定量分析方法试题答案

物流管理定量分析方法试题答案IMB standardization office【IMB 5AB- IMBK 08- IMB 2C】《物流管理定量分析方法》期末复习题一、线性规划法 1. 设⎥⎦⎤⎢⎣⎡-=⎥⎦⎤⎢⎣⎡---=011101,132031B A ,求:AB T . 解:⎥⎦⎤⎢⎣⎡--=⎥⎥⎥⎦⎤⎢⎢⎢⎣⎡-⎥⎦⎤⎢⎣⎡---=1121011011132031T AB 2.已知矩阵⎥⎦⎤⎢⎣⎡-=⎥⎥⎥⎦⎤⎢⎢⎢⎣⎡--=⎥⎦⎤⎢⎣⎡-=2101111412210101C B A ,,,求:AB +C. 解:⎥⎦⎤⎢⎣⎡-=⎥⎦⎤⎢⎣⎡-+⎥⎦⎤⎢⎣⎡-=⎥⎦⎤⎢⎣⎡-+⎥⎥⎥⎦⎤⎢⎢⎢⎣⎡--⎥⎦⎤⎢⎣⎡-=+3702210116012101111412210101C AB 3.已知矩阵⎥⎥⎥⎦⎤⎢⎢⎢⎣⎡--=⎥⎥⎥⎦⎤⎢⎢⎢⎣⎡--=131211203012011B A ,,求:AB. 解:⎥⎥⎥⎦⎤⎢⎢⎢⎣⎡--=⎥⎥⎥⎦⎤⎢⎢⎢⎣⎡--⎥⎥⎥⎦⎤⎢⎢⎢⎣⎡--=531421131211203012011AB 4. 已知矩阵⎥⎥⎥⎦⎤⎢⎢⎢⎣⎡=⎥⎥⎥⎦⎤⎢⎢⎢⎣⎡--=600540321201110011B A ,,求:B T A. 解:⎥⎥⎥⎦⎤⎢⎢⎢⎣⎡--=⎥⎥⎥⎦⎤⎢⎢⎢⎣⎡--⎥⎥⎥⎦⎤⎢⎢⎢⎣⎡=1723422011201110011653042001T A B 5.设110012212601A B ⎡⎤-⎡⎤⎢⎥==-⎢⎥⎢⎥⎣⎦⎢⎥⎣⎦,,求:(1) 2B T -A ;(2) AB . 解:12000122121126TB A -⎡⎤⎡⎤-=-⎢⎥⎢⎥-⎣⎦⎣⎦240001241242126164-⎡⎤⎡⎤⎡⎤=-=⎢⎥⎢⎥⎢⎥---⎣⎦⎣⎦⎣⎦6. 已知矩阵⎥⎥⎥⎦⎤⎢⎢⎢⎣⎡=⎥⎥⎥⎦⎤⎢⎢⎢⎣⎡--=600540321201110011B A ,,求:AB. 解: ⎥⎥⎥⎦⎤⎢⎢⎢⎣⎡⎥⎥⎥⎦⎤⎢⎢⎢⎣⎡--=600540321201110011AB 7. 已知矩阵⎥⎥⎥⎦⎤⎢⎢⎢⎣⎡=⎥⎥⎥⎦⎤⎢⎢⎢⎣⎡-=321212113101012111B A ,,求:AB .解:⎥⎥⎥⎦⎤⎢⎢⎢⎣⎡=⎥⎥⎥⎦⎤⎢⎢⎢⎣⎡⎥⎥⎥⎦⎤⎢⎢⎢⎣⎡-=434014646321212113101012111AB 二、导数方法1.设y =(x 2-3) ln x ,求:y '解:xx x x x x x x y 3ln 2)(ln )3(ln )3(22-+='⋅-+⋅'-=' 2.设y =(1+x 3) ln x ,求:y '解:22331ln 3)(ln )1(ln )1(x xx x x x x x y ++='⋅++⋅'+=' 3.设y =(1+x 2)ln x ,求:y '解:xx x x x x x x y 2221ln 2))(ln 1(ln )1(++='++'+='4. 设xx y e 4=,求:y '解:x x x x x x x y )e 4()e (e )(4344+='⋅+⋅'=' 5.设31ln xxy +=,求:y ' 解:23232333)1(ln 31)1()1()(ln )1()(ln x x x x x x x x x x y +-+=+'+⋅-+⋅'='6.设xy x+=1e ,求:y '解:22)1(e )1()1(e )1()e (x x x x x y xx x +=+'+-+'='7.设y =x 3ln x ,求:y '解:2233ln 3)(ln ln )(x x x x x x x y +='⋅+⋅'='三、微元变化累积 1.计算定积分:⎰+1d )e 3(x x x解:25e 3)e 321(d )e 3(|1021-=+=+⎰x x x x x 2.计算定积分:⎰+312d )2(x xx解:3ln 2326|)|ln 231(d )2(|313312+=+=+⎰x x x x x3.计算定积分:⎰+103d )e 24(x x x 解: 1e 2)e 2(d )e 24(|1413-=+=+⎰x x x x x4.计算定积分:⎰+13d )e 2(x x x解:47e 2)e 241(d )e 2(|1413-=+=+⎰x x x x x5.计算定积分:⎰+21d )12(x xx解:2ln 3|)|ln (d )12(|21221+=+=+⎰x x x xx6..计算定积分:⎰+21d )1e (x xx解:2ln e e |)|ln e (d )1e (22121|+-=+=+⎰x x xx x7.计算定积分:⎰+212d )1(x xx解:2ln 37|)|ln 31(d )1(|213212+=+=+⎰x x x x x 四、表上作业法1.某公司从三个产地A1,A2,A3运输某物资到三个销地B1,B2,B3,各产地的供应量(单位:吨)、各销地的需求量(单位:吨)及各产地到各销地的单位运价(单位:百元/吨)如下表所示:(1)在下表中写出用最小元素法编制的初始调运方案:(2)检验上述初始调运方案是否最优,若非最优,求最优调运方案,并计算最低运输总费用。
定量资料案例分析 (统计)

案例1 欲了解某年某市正常成年男性的平均血铅含量,有研究者随机调查了当 。 年该市200名正常成年男性的血铅含量。将所获血铅值整理成频率分布表,据此 认为该地正常成年男性血铅值资料不服从正态分布,应先对数据进行对数变换, 再用式 X 1.96S X 来估计当年正常成年男性平均血铅含量的95%置信区间。 表1 某年某市200名正常成人血铅含量(μg/L)分布 频率(%) 组段 频数 40~ 25 12.5 80~ 32 16.0 120~ 36 18.0 160~ 30 15.0 200~ 25 12.5 240~ 22 11.0 280~ 11 5.5 320~ 8 4.0 360~ 4 2.0 400~ 4 2.0 440~ 1 0.5 480~ 1 0.5 520~560 1 0.5 合计 200 100.0
t=4.78,查表可得,P=0.001,治疗前后血红蛋白 差别有统计学意义,治疗后高于治疗前。
t=(d –0)/(Sd/ √ n) n=9 d =34.5g/l v=8
Sd=21.67g/l
案例四
研究2种单味中药对小鼠细胞免疫功能的影响,并设一个空白对 照组,将30只小鼠随机分为3组,每组10只,雌雄各半,用药15 天后,测定E-玫瑰结形成率(%),结果如下。
案例五
• 某研究所研制了3个降血脂中药复方制剂,现拟对 3个复方与标准降脂药(安妥明)的疗效进行比较, 取品种相同,健康的雄性家兔16只,按其体重大 小分为4个组,各组动物均饲以同样高脂饮食,并 每日分别灌以不同药物,第45天处死动物,观察 冠状动脉硬化斑块面积,见下表。研究者用完全 随机设计资料的方差分析对资料进行了假设检验, F=56.952,P=0.000,故认为3个降血脂中药复方制 剂疗效不全相同。
山西专版2020中考化学复习方案题型突破10定量分析计算试题20200317224

题型突破(十) 定量分析计算类型一文字叙述题1.[2019·山西]碱式碳酸铜是孔雀石的主要成分,俗称铜绿,化学式为Cu2(OH)2CO3,受热可分解生成CuO、水和二氧化碳。
(1)碱式碳酸铜的相对分子质量是。
(2)铜绿分解生成22 g的二氧化碳的同时,生成CuO的质量是多少?2.[2018·山西]黄铜(铜锌合金)的外观与黄金极为相似,容易以假乱真。
小红同学想测定黄铜中锌的含量,她称取20 g黄铜样品放入烧杯中,加入足量稀硫酸充分反应后,测得生成氢气的质量为0.2 g。
(1)该反应属于(填基本反应类型)。
(2)求黄铜样品中锌的质量分数(写计算过程)。
3.[2019·长沙]为了测定某石灰石矿中碳酸钙的含量,进行了如下实验:称取10 g石灰石样品,反复灼烧至质量不再改变,称得剩余固体质量为6.7 g(假设杂质不参与反应)。
请计算:(1)反应生成的CO2的质量为g。
(2)求该石灰石样品中碳酸钙的质量分数(写出计算过程)。
4.[2019·新疆兵团]将8.0 g三氧化二铁加入100.0 g的稀硫酸中,恰好完全反应。
试计算:(1)硫酸的相对分子质量是。
(2)稀硫酸中溶质的质量分数(计算结果精确到0.1%)。
5.[2017·山西]在一次实验课上,同学们用加热氯酸钾和二氧化锰混合物的方法制取氧气。
他们取了24.5 g的混合物,其中二氧化锰的质量分数为20%,加热到完全分解。
通过计算,得出他们制得氧气的质量是多少?6.[2012·山西]某化学兴趣小组的同学采集了一些大理石样品,为测定该样品中碳酸钙的质量分数,取样品 6 g粉碎成粉末状置于烧杯中,向其中加入10%的稀盐酸并不断搅拌,恰好不再有气泡产生时(已知杂质不与稀盐酸反应),共用去稀盐酸36.5 g。
(1)该实验中能否用稀硫酸代替稀盐酸(填“能”或“不能”)。
(2)用质量分数为36%的浓盐酸100 g能配制所需10%的稀盐酸g。
药物定量分析

3.剩余滴定法
含量% T (V空白-V供) F S 100%
V空白 V供试
与药物反应消耗的试液
未反应的试液
空白
供试
空白试验的作用: 1. 求出滴定液与药物反应的消耗量
2. 校正操作上的误差(供试与空白液
必/碘口服液
I ~ Na2 S 2O3 ~ I ~ AgNO3
nI nNa2 S2O3 nAgNO3 ( NaI )
T V F I%= 100% S
KI%
(C AgNO3 VAgNO3-C Na2S 2O 3 VNa2S 2O 3 ) M KI W
100%
m X供试 ( AX / AS ) 供试 ( AR / AS ) 对照 m R对照
C X供试
( AX / AS ) 供试 ( AR / AS ) 对照
C R对照
(供试品与对 照品体积相同)
R:对照品
S:内标物
X:供试品
c) 校正因子法(常用)
(A内标 / C内标 ) ) 对照 (A内标 / C内标 供试 f ( A对 / C 对 )对照 ( A供 / C X )供试
=198.17。
( 9.8-0 ) 100 198.17 含量%= 100%=11.3% 52.75 2 90 180.16
样品分析的前处理方法
一、不经有机破坏的前处理方法
1. 水解法:酸水解、碱水解
2. 还原法
二、经有机破坏的前处理方法
1. 湿法破坏
(1) 硝酸-高氯酸法 (2) 硝酸-硫酸法
λ2
λ1
测定波长 λ1下:A样1 = A药1 + A杂1
05 定量分析方法的应用

定量分析方法的应用一、学习任务(1)了解定量实验研究方法在化学科学发展中的作用。
(2)能通过化学实验收集有关数据和事实,并运用科学方法加以处理,形成实验探究结论。
(3)在化学问题解决中能运用所掌握的化学知识与技能进行必要的分析、归纳、类比、推理或计算,并形成结论。
二、知识框架(一)定量分析知识简介1.定量分析的实验步骤2.定量分析方法(二)滴定分析型计算——化学式的确定1. 微粒形式的化学式确定【典例1】硫酸亚铁铵(NH4)aFe b(SO4)c•dH2O又称莫尔盐,是浅绿色晶体。
称取11.76g新制莫尔盐,溶于水配成250mL 溶液。
取25.00 mL该溶液加入足量的BaCl2溶液,得到白色沉淀1.398 g;另取25.00 mL该溶液用0.0200 mol/L KMnO4酸性溶液滴定,当MnO-4恰好完全被还原为Mn2+时,消耗溶液的体积为30.00mL。
试确定莫尔盐的化学式。
小结:解题步骤、解题关键。
2. 复盐形式的化学式确定【典例2】白钠镁矾(mNa2SO4·nMgSO4·xH2O)俗称硝板,为测定其组成进行下列实验:①取白钠镁矾3.340 g溶于水配成100.00 mL溶液A;②取25.00 mL溶液A,加入足量的氯化钡溶液,得沉淀1.165 g;③另取25.00 mL溶液A,调节pH=10,用浓度为0.1000 mol·L-1的EDTA(Na2H2Y)标准溶液滴定Mg2+(离子方程式为Mg2+ + H2Y2-=MgY2-+ 2H+),滴定至终点,消耗标准溶液25.00 mL。
通过计算确定白钠镁矾的化学式。
【及时训练】碱式氯化铜有多种组成,可表示为Cu a(OH)b Cl c·xH2O。
为测定某碱式氯化铜的组成,进行下列实验:①称取样品1.1160 g,用少量稀HNO3溶解后配成100.00 mL溶液A;②取25. 00 mL溶液A,加入足量AgNO3溶液,得AgCl 0. 1722 g;③另取25. 00 mL溶液A,调节pH 4 ~ 5,用浓度为0.08000 mol·L-1的EDTA(Na2H2Y·2H2O)标准溶液滴定Cu2+ (离子方程式为Cu2++ H2Y2-=CuY2-+2H+),滴定至终点,消耗标准溶液30.00 mL。
第2单元: 定量分析方法1(课件内题目及答案)

货币市场收益率
• 银行贴现基准:
rBD
• 实际年收益率:
F - P0 360 F =面值 F t
EAY (1 HPY)
• 货币市场收益率:
365 / t
-1
rMM
18
360 HPY t
定量分析方法1 现金流贴现模型
L1-02831
第7题: 期限为120天的短期国库券的货币市场收益率为 3.25%。那么其持有期收益率和实际年收益率最接近于:
9
定量分析方法1 资金的时间价值
示例:Bob每年将7,000美元存入账户,一直持续了10年。 他每年的收益率为6%。请问,在10年结束时,该账户的 余额是多少? 解答:
t= 0 1
7,000
2
7,000
3
7,000
4
7,000
10
7,000
PMT = 7,000 N = 10 iP = 6
10
$92,265.56 FV = ?
定量分析方法1 资金的时间价值
期初年金
示例:Bob想从现在开始每年向自己的储蓄账户存入一笔相等金额的 存款。该年金的年收益为是6%。他希望在10年结束时,账户上的存款 有112,000美元。那么他每年必须存入多少存款? 解答:
t =0 [Begin模式]
PMT
1
PMT
2
PMT
3
PMT
4
PMT
10
FV N iP
• 货币加权收益率=内部收益率(IRR)
– 受到客户投资或撤资决定的影响。
投资业绩评估
• 时间加权收益率=几何平均数
– 不受客户投资或撤资决定的影响
第五章。定量分析概论

第五章。
定量分析概论一、选择题:(在题后所附答案中选择正确答案代号填入括号中)1、定量分析的任务是()a:测定物质的含量;b: 测定物质中的组成;c: 测定物质的组成及含量;d: 测定物质的有关组分的含量;2、下列论述中错误的是:()a:方法误差属于系统误差;b: 系统误差不包括操作误差;c: 系统误差呈正态分布d: 系统误差又称为可测定误差;3、滴定分析中出现下列情况,导致产生系统误差的是:()a:滴定时有溶液溅出;b:所有试剂含有干扰离子;c:试样未经充分混匀;d:砝码读错了。
4、下列措施中,能减少偶然误差的是()a:增加平行测定次数;b:进行空白实验;c:进行对照实验;d:进行仪器校准。
5、下列有关偶然误差的论述不正确的是()a:偶然误差具有单向性。
b:偶然误差具有随机性;c: 偶然误差的数值大小、正负出现的机率是相等的;d: 偶然误差是由一些不确定的偶然因素造成的。
6、下列有关偶然误差正态分布曲线特点的论述中不正确的是()a:曲线与横坐标间所夹的面积的总和,代表所有测定值出现的机率;b:横坐标x值等于总体平均值u时,曲线有极大值;c:曲线呈对称钟形,两头小中间大,说明小误差出现机率大,大误差出现机率小;d:曲线以u值的横坐标为中心呈镜面对称,说明正、负误差出现的几率相等。
7、下列论述中,正确的是()a:进行分析时,过失误差是不可避免的;b:精密度高,准确度一定高;c: 准确度高,一定需要准确度高;d: 准确度高,系统误差一定小。
8、定量分析要求测定结果的误差()a:愈小愈好;b:等于零;c:略大于允许误差;d: 在允许误差范围内。
9下列各项定义中不正确的是()a:绝对误差是测定值与真实值之差;b:相对误差是绝对误差在真实结果中所占百分率c:偏差是指测定结果与平均结果之差;d:平均偏差是单次测量偏差的平均值。
10、下列情况中,何者属于操作人员不应有的操作误差()a:分析天平用的砝码没有校准,b:滴定前用被滴定溶液淋洗锥形瓶,c:滴定前用操作溶液将滴定管淋洗几次;d:滴定管没有校准。
定量分析计算例题

定量分析计算例题例1呋塞米含量测定:取本品0.4988g,加乙醇30ml,微热使溶解,放冷,加甲酚红指示液4滴与麝香草酚兰指示液1滴,用氢氧化钠滴定液(0.1003mol/L)滴定至溶液显紫红色,消耗氢氧化钠滴定液(0.1003mol/L)14.86ml;并将滴定的结果用空白试验校正,消耗氢氧化钠滴定液(0.1003mol/L)0.05ml。
每1ml氢氧化钠滴定液(0.1mol/L)相当于33.07mg的呋塞米。
按干燥品计算,含C12H11ClN2O5S 不得少于99.0%。
【98.5% 】例2司可巴比妥原料药含量测定:取本品0.1043g,置250ml碘量瓶中,加水10ml,振摇使溶解,精密加漠滴定液(0.1 mol/L)25ml,再加盐酸5ml,立即密塞并振摇1分钟,在暗处静置15分钟后,微开瓶塞,加碘化钾试液10ml,立即密塞,摇匀后,用硫代硫酸钠滴定液(0.1012mol/L)滴定,至近终点时,加淀粉指示液,继续滴定至蓝色消失,并将滴定结果用空白试验校正。
每1ml漠滴定液(0.1 mol/L)相当于13.01mg的C12H^N2NaO。
按干燥品计算,含C12H^N2NaO不得少于98.5%。
已知样品消耗硫代硫酸钠滴定液(0.1012mol/L)17.20ml,空白试验消耗硫代硫酸钠滴定液(0.1012mol/L)25.02ml。
【98.7% 】例3奥沙西泮原料药含量测定:精密称定本品0.0157g,置200ml容量瓶中,加乙醇150ml,于温水浴中加热,振摇使溶解,放冷,用乙醇稀释至刻度,摇匀,精密量取5ml,置100ml容量瓶中,用乙醇稀释至刻度,摇匀,按分光光度法,在229nm处测定吸光度为0.480;另精密称取奥沙西泮对照品0.0149g,同法操作,测得229nm处吸光度为0.460;《中国药典》规定,本品按干燥品计算,含C15H]]ClN2O2应为98.0%〜102.0%。
该供试品含量是否合格?【99.0%】例4对乙酰氨基酚原料药含量测定:精密称取对乙酰氨基酚0.0411g,置250ml容量瓶中,加0.4% 氢氧化钠溶液50ml,加水至刻度,摇匀,精密量取5ml,置100ml容量瓶中,加0.4%氢氧化钠溶液10ml,加水至刻度,摇匀。
定量分析化学习题

第一章定量分析概论习题一1.将下列数据修约为两位有效数字=3.6643.667;3.651;3.650;3.550;3.649;pKa解:3.7;3.7;3.6;3.6;3.6;3.662.根据有效数字运算规则计算下列结果:(1)2.776+36.5789-0.2397+6.34(2)(3.675×0.0045)-(6.7×10-2)+(0.036×0.27)(3)50.00×(27.80-24.39)×0.11671.3245解:(1)45.46;(2)-0.040;(3)15.13. 测定镍合金的含量,6次平行测定的结果是34.25%、34.35%、34.22%、34.18%、34.29%、34.40%,计算(1)平均值;中位值;平均偏差;相对平均偏差;标准偏差;平均值的标准偏差。
(2)若已知镍的标准含量为34.33%,计算以上结果的绝对误差和相对误差。
解:(1)34.28%;34.27%;0.065%;0.19%;0.082%;0.034%(2)-0.05%;;-0.15%4. 分析某试样中某一主要成分的含量,重复测定6次,其结果为49.69%、50.90%、48.49%、51.75%、51.47%、48.80%,求平均值在90%、95%和99%置信度的置信区间。
解:置信度为90%的置信区间μ=(50.18±1.15)%置信度为95%的置信区间μ=(50.18±1.46)%置信度为99%的置信区间μ=(50.18±2.29)%14.用某法分析汽车尾气中SO含量(%),得到下列结果:4.88,4.92,4.90,24.87,4.86,4.84,4.71,4.86,4.89,4.99。
(1)用Q检验法判断有无异常值需舍弃?(2)用格鲁布斯法判断有无异常值需舍弃?解:(1)无(2)4.71、4.99应舍去第二章滴定分析习题二1.市售盐酸的密度为1.19g/mL,HCl含量为37%,欲用此盐酸配制500mL0.1mol/L的HCl溶液,应量取市售盐酸多少毫升?(4.15mL)2.已知海水的平均密度为1.02g/mL,若其中Mg2+的含量为0.115%,求每升海水中所含Mg2+的物质的量n(Mg2+)及其浓度c(Mg2+)。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
定量分析计算例题
例1 呋塞米含量测定:取本品0.4988g,加乙醇30ml,微热使溶解,放冷,加甲酚红指示液4滴与麝香草酚兰指示液1滴,用氢氧化钠滴定液(0.1003mol/L)滴定至溶液显紫红色,消耗氢氧化钠滴定液(0.1003mol/L)14.86ml;并将滴定的结果用空白试验校正,消耗氢氧化钠滴定液(0.1003mol/L)0.05ml。
每1ml氢氧化钠滴定液(0.1mol/L)相当于33.07mg的呋塞米。
按干燥品计算,含C12H11ClN2O5S不得少于99.0%。
【98.5%】
例2 司可巴比妥原料药含量测定:取本品0.1043g,置250ml碘量瓶中,加水10ml,振摇使溶解,精密加溴滴定液(0.1 mol/L)25ml,再加盐酸5ml,立即密塞并振摇1分钟,在暗处静置15分钟后,微开瓶塞,加碘化钾试液10ml,立即密塞,摇匀后,用硫代硫酸钠滴定液(0.1012mol/L)滴定,至近终点时,加淀粉指示液,继续滴定至蓝色消失,并将滴定结果用空白试验校正。
每1ml溴滴定液(0.1 mol/L)相当于13.01mg的C12H17N2NaO3。
按干燥品计算,含C12H17N2NaO3不得少于98.5%。
已知样品消耗硫代硫酸钠滴定液(0.1012mol/L)17.20ml,空白试验消耗硫代硫酸钠滴定液(0.1012mol/L)25.02ml。
【98.7%】
例3 奥沙西泮原料药含量测定:精密称定本品0.0157g,置200ml容量瓶中,加乙醇150ml,于温水浴中加热,振摇使溶解,放冷,用乙醇稀释至刻度,摇匀,精密量取5ml,置100ml容量瓶中,用乙醇稀释至刻度,摇匀,按分光光度法,在229nm处测定吸光度为0.480;另精密称取奥沙西泮对照品0.0149g,同法操作,测得229nm处吸光度为0.460;《中国药典》规定,本品按干燥品计算,含C15H11ClN2O2应为98.0%~102.0%。
该供试品含量是否合格?【99.0%】
例4 对乙酰氨基酚原料药含量测定:精密称取对乙酰氨基酚0.0411g,置250ml容量瓶中,加0.4%氢氧化钠溶液50ml,加水至刻度,摇匀,精密量取5ml,置100ml容量瓶中,加0.4%氢氧化钠溶液10ml,加水至刻度,摇匀。
依照分光光度法,在257nm波长处测得吸收度为0.582。
按C8H9NO2的百分吸收系数为719计算对乙酰氨基酚的百分含量。
【98.5%】
例5 甲苯磺丁脲片剂(标示量0.5g)的含量测定:取甲苯磺丁脲10片,精密称定为5.9480g,研细,精密称取片粉0.5996g,加中性乙醇25ml,微热,使其溶解,放冷,加酚酞指示剂3滴,用氢氧化钠滴定液(0.1008mol/L)滴定至粉红色,消耗量18.47ml。
每1ml氢氧化钠滴定液(0.1mol/L)相当于27.04mg的甲苯磺丁脲。
《中国药典》规定,本品含甲苯磺丁脲为标示量的95.0%~105.0%。
试计算本品的标示量百分含量。
【99.9%】
例6 盐酸普鲁卡因注射剂(规格1ml:50mg)含量测定:精密量取盐酸普鲁卡因注射液2ml,加水40ml,盐酸溶液(1→2)15ml,溴化钾2g,按照永停滴定法,用亚硝酸钠滴定液(0.1032mol/L)滴定,消耗亚硝酸钠滴定液(0.1032mol/L)3.50ml。
每1ml亚硝酸钠滴定液(0.1mol/L)相当于27.18mg 的C13H21N30•HCl。
【98.2%】
例7 甲硝唑片(标示量为50mg)含量测定:取本品10片,精密称定为0.5988g,研细,精密称取片粉0.05978g,置200ml容量瓶中,加盐酸溶液(9→1000)约180ml,振摇使甲硝唑溶解,加盐酸溶液(9→1000)稀释至刻度,摇匀,滤过。
精密量取续滤液5ml,置100ml量瓶中,加盐酸溶液(9→1000)至刻度,摇匀,按照紫外—可见分光光度法,在277nm波长处测定吸光度为0.4493,按C6H9N3O3的百分吸收系数为377计算,即得。
【95.5%】
例8 甲氧苄啶片(标示量为50mg)含量测定:取本品20片,精密称定为1.2003g,研细,精密称取0.05783g,置250ml容量瓶中,加稀醋酸约150ml,充分振摇使溶解,加稀醋酸稀释至刻度,摇匀,滤过,精密量取续滤液10ml,置100ml容量瓶中,加稀醋酸10ml,加水稀释至刻度,摇匀。
按照紫外—可见分光光度法,在271nm波长处测定吸光度为0.420。
另取甲氧苄啶对照品0.05134g,同法测定,在271nm波长处测定吸光度为0.416,计算,即得。
【107.6%】
例9 马来酸氯苯那敏注射液(标示量1ml:10mg)的含量测定:精密量取本品2ml,置100ml容量瓶中,加盐酸溶液稀释至刻度,摇匀。
精密量取稀释液5ml,置50ml容量瓶,用同一浓度盐酸溶液稀释至刻度,摇匀。
取该溶液置1cm厚的石英吸收池中,以相同盐酸溶液为空白,在264nm波长处测得吸收度为0.432,按百分吸收系数为217计算,即得。
《中国药典》规定,本品含马来酸氯苯那敏应为标示量的95.0%~110%。
【99.5%】
例10 注射用硫喷妥钠(C11H17N2NaO2S=264.33)的含量测定:精密称取内容物适量(约相当于硫喷妥钠0.25g),置500ml量瓶中,加水稀释至刻度,摇匀,量取此液适量,用0.4%氢氧化钠溶液定量稀释制成每1ml中约含5μg的溶液;另取硫喷妥(C11H18N2O2S=242.33)对照品,精密称定,加0.4%氢氧化钠溶液溶解并定量稀释制成每1ml中约含5μg的溶液。
在304nm的波长处分别测定吸收度,已知:称取本品内容物0.2658g,对照品浓度为5.05μg/ml,测得样品的吸收度为0.446,对照品的吸收度为0.477,本品规格0.5g,5支内容物重2.6481g。
计算本品相当于标示量的百分含量?【102.6%】。
