舒普深1.5g说明书
皮内注射操作流程、理论

皮内注射操作流程素质要求操作前准备评估患者1. 洗手,戴口罩2. 备齐用物且放置合理1. 核对医嘱、询问、了解患者的身体状况2. 评估患者有无药物过敏史及进食情况3. 评估患者病情、合作程度、注射部位的皮肤情况4. 解释、助(嘱)排尿,做好准备工作操作要点1. 核对药物方法正确,做到三查七对2. 检查瓶身、安瓿有无破损,药液有无变质3. 抽取或配置皮试溶液4.携用物至患者床旁,取舒适体位,至病房,核对,再次询问过敏史及进食情况5. 选定注射部位(前臂掌侧下1/3)6. 75%酒精消毒注射部位皮肤(2遍),消毒方法、范围正确7. 核对并抽取药液,排尽空气8. 绷紧皮肤,针头与皮肤成5°进针 9. 固定针栓(左手拇指)10. 注药0.1ml 形成皮丘,拔针,勿按压 11. 计时20min 后观察反应 12. 协助患者取舒适体位,将呼叫器放置于患者可及位置操作后1.告知患者注意事项2. 整理床单位,合理安置患者3. 清理用物,正确处理注射器及针头4. 洗手、脱口罩5.判断结果:皮试结果阴性或阳性的判断方法及记录,告知患者实验结果皮内注射操作理论部分一、目的:1.药物过敏试验。
2.预防接种。
3.局部麻醉起始步骤。
二、注意事项:1.贯彻无菌操作原则,保持用物和药液无菌,避免交叉感染。
2.为病人做药物过敏试验前,要备好急救药品。
3.做皮试忌用碘酊消毒,以免因脱碘不彻底影响局部反应的观察,且易与碘过敏反应相混淆。
4.若怀疑假阳性时,应做对照试验。
三、皮试结果判断阴性:皮丘局部无红肿,无自觉症状。
阳性:皮丘局部隆起,并出现红晕、硬块并有伪足出现,皮丘直径大于1cm,或出现头晕、胸闷及发痒等症状,严重时全身出现皮疹或过敏性休克反应。
四、皮试液的配制:1. 青霉素皮试配制:80万单位青霉素用4ml生理盐水稀释,20万单位/ml(1)取上液0.2ml,加生理盐水至1ml,2万单位/ml(2)取上液0.1ml,加生理盐水至1ml,2000单位/ml(3)取上液0.1ml,加生理盐水至1ml,200单位/ml(4)取0.1ml即为皮试液2. 舒普深皮试配制:1.5g舒普深用15ml生理盐水稀释,100mg/ml (1)取上液0.5ml,加生理盐水至1ml,50mg/ml (2)取上液0.1ml,加生理盐水至1ml,5mg/ml (3)取上液0.1ml,加生理盐水至1ml,0.5mg/ml (4)取0.05ml~0.1ml即为皮试液3. 凯福隆皮试配制:1.0g凯福隆用4ml生理盐水稀释,250mg/ml (1)取上液0.2ml,加生理盐水至1ml,50mg/ml (2)取上液0.1ml,加生理盐水至1ml,5mg/ml (3)取上液0.1ml,加生理盐水至1ml,0.5mg/ml (4)取0.1ml即为皮试液。
注射用头孢派酮舒巴坦钠说明书20110908(舒普深)1.5g,3.0g

【规格】 1.5g (以头孢哌酮计 1000mg 与以舒巴坦计 500 mg) 3.0g (以头孢哌酮计 2000mg 与以舒巴坦计 1000 mg)
【用法用量】
成人用药:
本品成人每日推荐剂量如下:
比例
头孢哌酮/舒巴坦(g)
2:1
1.5-3.0
头孢哌酮(g) 1.0-2.0
舒巴坦(g) 0.5-1.0
Version No: 20110908
第 5 页,共 11 页
类抗生素两者给药的间隔时间尽可能长一点。
乳酸钠林格注射液:由于本品与乳酸钠林格注射液混合后有配伍禁忌,因此应避免在最 初溶解时使用该溶液。在两步稀释法中,先用注射用水进行最初的溶解,再用乳酸钠林格注 射液作进一步稀释,从而得到能够相互配伍的混合药液(参见【用法用量】使用/操作说明 乳酸钠林格注射液部分)。
5. 对驾驶和操作机器能力的影响 头孢哌酮/舒巴坦临床应用经验表明,本品不会降低患者驾驶和操作机器的能力。 6. 配伍禁忌 氨基糖苷类抗生素:由于本品与氨基糖苷类抗生素之间有物理性配伍禁忌,因此两种药 液不能直接混合。如确需本品与氨基糖苷类抗生素合用时(参见【适应症】联合用药部分), 可采用序贯间歇静脉输注给药,但必须使用不同的静脉输液管,或在输注间歇期用一种适宜 的稀释液充分冲洗先前使用过的静脉输液管。另外,建议在全天用药过程中本品与氨基糖苷
【禁忌】 已知对青霉素类、舒巴坦、头孢哌酮及其它头孢菌素类抗生素过敏者禁用。
【注意事项】
1. 过敏反应
Version No: 20110908
第 4 页,共 11 页
有报道,接受β-内酰胺类或头孢菌素类抗生素治疗的患者可发生严重的、偶可致死的 过敏反应。这些过敏反应更易发生在对多种过敏原有过敏史的患者中。一旦发生过敏反应, 应立即停药并给予适当的治疗。
注射用头孢哌酮钠舒巴坦钠说明书--舒普深

注射用头孢哌酮钠舒巴坦钠说明书--舒普深(总8页)-本页仅作为预览文档封面,使用时请删除本页-头孢哌酮钠舒巴坦钠粉针剂说明书【药品名称】通用名:注射用头孢哌酮钠舒巴坦钠英文名:CefoperazoneSodiumandSulbactamSodiumforInjection汉语拼音:ZhusheyongToubaopaitongnaShubatanna商品名:舒普深英文商品名:SULPERAZON【成份】本品为复方制剂,其组分为头孢哌酮钠和舒巴坦钠。
头孢哌酮钠的化学名称为:(6R,7R)-3-[[(1-甲基-1H-四唑-5-基)硫]甲基]-7-[(R)-2-(4-乙基-2,3-二氧代-1-哌嗪碳酰氨基)-2-对羟基苯基-乙酰氨基]-8-氧代-5-硫杂-1-氮杂双环[辛-2-烯-2-甲酸钠。
化学结构式:分子式:C25H26N9NaO8S2分子量:Cas No:62893-20-3舒巴坦钠的化学名称为:(2S,5R)-3,3-二甲基-7氧代-4-硫杂-1-氮杂双环[庚烷-2-羧酸钠-4,4-二氧化物。
化学结构式:分子式:C8H10NNaO5S分子量:Cas No:69388-84-7【性状】本品为白色或类白色粉末。
【适应症】单独应用本品适用于治疗由敏感菌所引起的下列感染:上、下呼吸道感染;上、下泌尿道感染;腹膜炎、胆囊炎、胆管炎和其他腹腔内感染;败血症;脑膜炎;皮肤和软组织感染;骨骼和关节感染;盆腔炎、子宫内膜炎、淋病和其他生殖道感染。
联合用药:由于本品具有广谱抗菌活性,因此单用本品就能够治疗大多数感染,但有时也需要本品与其他抗生素联合应用。
当本品与氨基糖苷类抗生素合用时(参见配伍禁忌氨基糖苷类抗生素部分),在治疗过程中应监测患者的肾功能(参见用法与用量肾功能障碍患者的用药部分)。
【规格】(以头孢哌酮计1000mg,以舒巴坦计500mg)【用法与用量】成人用药:日剂量可增加到8克(1:1头孢哌酮/舒巴坦,即头孢哌酮与舒巴坦各4g)或12克(2:1头孢哌酮/舒巴坦,即头孢哌酮8克,舒巴坦4g)。
舒普深说明书
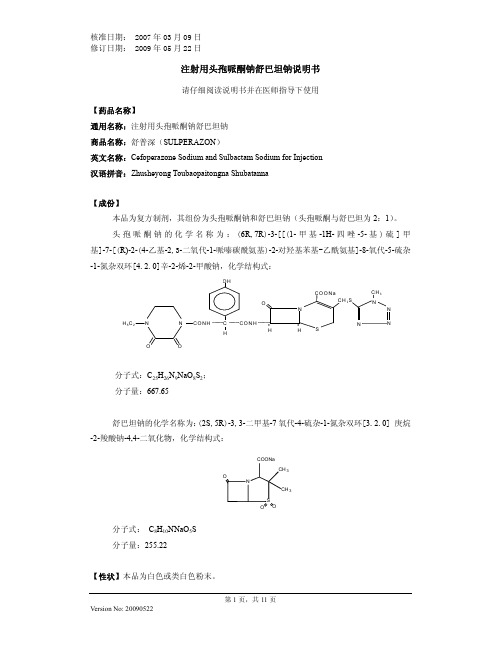
核准日期: 2007年03月09日 修订日期: 2009年05月22日注射用头孢哌酮钠舒巴坦钠说明书请仔细阅读说明书并在医师指导下使用【药品名称】通用名称:注射用头孢哌酮钠舒巴坦钠 商品名称:舒普深(SULPERAZON )英文名称:Cefoperazone Sodium and Sulbactam Sodium for Injection 汉语拼音:Zhusheyong Toubaopaitongna Shubatanna【成份】本品为复方制剂,其组份为头孢哌酮钠和舒巴坦钠(头孢哌酮与舒巴坦为2:1)。
头孢哌酮钠的化学名称为:(6R ,7R )-3-[[(1-甲基-1H-四唑-5-基)硫]甲基]-7-[(R)-2-(4-乙基-2,3-二氧代-1-哌嗪碳酰氨基)-2-对羟基苯基-乙酰氨基]-8-氧代-5-硫杂-1-氮杂双环[4.2.0]辛-2-烯-2-甲酸钠,化学结构式:分子式:C 25H 26N 9NaO 8S 2; 分子量:667.65舒巴坦钠的化学名称为:(2S ,5R )-3,3-二甲基-7氧代-4-硫杂-1-氮杂双环[3.2.0] 庚烷-2-羧酸钠-4,4-二氧化物,化学结构式:33分子式: C 8H 10NNaO 5S 分子量:255.22【性状】本品为白色或类白色粉末。
【适应症】单独应用本品适用于治疗由敏感菌所引起的下列感染:上、下呼吸道感染;上、下泌尿道感染;腹膜炎、胆囊炎、胆管炎和其他腹腔内感染;败血症;脑膜炎;皮肤和软组织感染;骨骼和关节感染;盆腔炎、子宫内膜炎、淋病和其他生殖道感染。
联合用药:由于本品具有广谱抗菌活性,因此单用本品就能够治疗大多数感染,但有时也需要本品与其他抗生素联合应用。
当本品与氨基糖苷类抗生素合用时(参见【注意事项】配伍禁忌氨基糖苷类抗生素部分),在治疗过程中应监测患者的肾功能(参见【用法用量】肾功能障碍患者的用药部分)。
【规格】1.5g (以头孢哌酮计1000mg与以舒巴坦计500 mg)【用法用量】成人用药:本品成人每日推荐剂量如下:比例头孢哌酮/舒巴坦(g)头孢哌酮(g)舒巴坦(g)2:1 1.5-3.0 1.0-2.0 0.5-1.0上述剂量分等量,每12小时给药一次。
舒普深产品知识

16.8
28.7
25.3
66.9
70.7
67.4
71
舒普深产品知识
CHINET 2016年细菌耐药监测数据
舒普深产品知识
目录
Part1 Part2 Part3
生产工艺 药物特征 说明书解读
成分
头孢哌酮 舒巴坦 舒普深是目前原研的唯一的第三代头孢菌素和-内酰胺酶抑制剂的复合制剂。
舒普深产品知识
舒普深产品有效期
法定有效期 2 年,产品有5%溢装量,可保证在整个有效期内产品的有 效活力在规定的范围内。
产品采用结晶型原料药,因此在稳定性和纯度等方面均优于冻干粉。 在较为宽松的储存条件下仍能保证有效期,国家标准是储存在20℃以下,
辉瑞标准是储存在25℃以下。
舒普深产品知识
舒普深产品知识
舒巴坦
头孢哌酮
10.4
26.8
20.0
20.4
5.7
9.8
19.1
39.0
5.9
5.6
27.0
36.7
在给药后不同时间测定,舒普深能够从血液迅速渗透到组织和体液中达到治
疗浓度
8. Okamura K, et al. Acta Urol Jpn. 1989;35:727-734.
13. Nakagawa K, et al. Surg Care. 1990;32(6):875-879.
目录
Part1 Part2 Part3
生产工艺 药物特征 说明书解读
特征一:抗菌谱广—覆盖院感常见菌
需氧菌
厌氧菌
革兰阳性菌
革兰阴性菌
革兰阳性菌
葡萄球菌 链球菌
大肠杆菌 克雷伯菌 枸橼酸菌 肠杆菌 沙门菌
舒普深注射液

皮肤反应:有报道,与所有青霉素类和。这些过敏反应易发生在有过敏史,特别是对青霉素过敏的 患者中。
用乳酸钠林格注射液 本品应使用灭菌注射用水进行溶解(参见配伍禁忌乳酸钠林格注射液部分)。采用两步 稀释法:先用灭菌注射用水溶解(如上表所示),再用乳酸钠林格注射液稀释至舒巴坦的浓 度为 5 毫克/毫升的溶液(用 2 毫升初配液稀释至 50 毫升乳酸钠林格注射液中或 4 毫升初配 液稀释至 100 毫升乳酸钠林格注射液中)。 用利多卡因
【规格】
1.0g(以头孢哌酮计 500 mg, 以舒巴坦计 500 mg) 1.5g(以头孢哌酮计 1000 mg, 以舒巴坦计 500 mg) 3.0g(以头孢哌酮计 2000 mg, 以舒巴坦计 1000 mg)
【用法用量】
成人用药:
本品成人每日推荐剂量如下:
比例
头孢哌酮/舒巴坦(克)
1:1
2.0-4.0
OH O
COONa C H 2S
N
CH3
N N
H 5C 2
N
N CONH
C
CONH
H
H
H
S
N
N
O
O
分子式:C25H26N9NaO8S2; 分子量:667.65
舒巴坦钠的化学名称为:(2S,5R)-3,3-二甲基-7 氧代-4-硫杂-1-氮杂双环[3.2.0] 庚烷 -2-羧酸钠-4,4-二氧化物,化学结构式:
发生严重过敏反应的患者须立即给予肾上腺素紧急处理,必要时应吸氧、静脉给予激 素,并采用包括气管内插管在内的畅通气道等治疗措施。
舒普深1.5g说明书

OH O
COONa CH2S
N
CH3
N N
H5C2 N
N CONH
C
CONH
H
H
H
S
N
N
O
O
分子式:C25H26N9NaO8S2; 分子量:667.65
舒巴坦钠的化学名称为:(2S,5R)-3,3-二甲基-7 氧代-4-硫杂-1-氮杂双环[3.2.0] 庚烷 -2-羧酸钠-4,4-二氧化物,化学结构式:
在血液透析患者中,舒巴坦的药物动力学特性有明显改变。头孢哌酮在血液透析患者中 的血清半衰期轻微缩短。因此在血样透析后,应给予一剂头孢哌酮/舒巴坦。
静脉给药: 采用间歇静脉滴注时,本品每瓶用适量的 5%葡萄糖溶液或 0.9%注射用氯化钠溶液或 灭菌注射用水溶解(参见使用/操作说明本品的溶解部分),然后再用上述相同溶液稀释至 20 毫升,静脉滴注时间应至少为 15-60 分钟。 尽管乳酸钠林格注射液可作为本品静脉注射液的溶媒,但不能用于本品最初的溶解过程 (参见配伍禁忌乳酸钠林格注射液部分和使用/操作说明乳酸钠林格注射液部分)。 采用静脉推注时,本品应按上述方法溶解,静脉推注时间至少应超过 3 分钟。 肌内注射: 尽管 2%盐酸利多卡因注射液可作为本品肌内注射液的溶媒,但不能用于本品最初的溶 解过程(参见配伍禁忌利多卡因部分和使用/操作说明利多卡因部分)。 使用/操作说明: 本品的溶解 本品每瓶内装 1.0 克,1.5 克和 3.0 克头孢哌酮/舒巴坦。
注射用头孢哌酮钠舒巴坦钠说明书20131225(舒普深)1 5g,3 0g

H5C2 N O
OH
O
N CONH C CONH H
H O
COONa C H 2S
N
CH3 N
N
H
S
N
N
分子式:C25H26N9NaO8S2; 分子量:667.65
舒巴坦钠的化学名称为:(2S,5R)-3,3-二甲基-7 氧代-4-硫杂-1-氮杂双环[3.2.0] 庚烷-2羧酸钠-4,4-二氧化物,化学结构式:
【成份】
本品为复方制剂,其组份为头孢哌酮钠和舒巴坦钠(头孢哌酮与舒巴坦为 2:1)。 头孢哌酮钠的化学名称为:(6R,7R)-3-[[(1-甲基-1H-四唑-5-基)硫]甲基]-7-[(R)-2-(4-乙 基-2,3-二氧代-1-哌嗪碳酰氨基)-2-对羟基苯基-乙酰氨基]-8-氧代-5-硫杂-1-氮杂双环[4.2.0]辛 -2-烯-2-甲酸钠,化学结构式:
头孢哌酮(g) 1.0~2.0
舒巴坦(g) 0.5~1.0
上述剂量分等量,每 12 小时给药一次。在治疗严重感染或难治性感染时,本品的每 日剂量可增加到 12g(2:1 头孢哌酮/舒巴坦,即头孢哌酮 8g,舒巴坦 4g)。舒巴坦每日推荐 最大剂量为 4g。
肝功能障碍患者的用药: 参见【注意事项】部分。 肾功能障碍患者的用药: 肾功能明显降低的患者(肌酐清除率<30ml/min)舒巴坦清除减少,应调整头孢哌酮/ 舒巴坦的用药方案。肌酐清除率为 15~30ml/min 的患者每日舒巴坦的最高剂量为 2g,分等 量,每 12 小时注射一次。肌酐清除率<15ml/min 的患者每日舒巴坦的最高剂量为 1g,分等 量,每 12 小时注射一次。遇严重感染,必要时可单独增加头孢哌酮的用量。 在血液透析患者中,舒巴坦的药物动力学特性有明显改变。头孢哌酮在血液透析患者中 的血清半衰期轻微缩短。因此应在血液透析结束后给药。 静脉给药: 采用间歇静脉滴注时,本品每瓶用适量的 5%葡萄糖溶液或 0.9%注射用氯化钠溶液或 灭菌注射用水溶解(参见【用法用量】使用/操作说明本品的溶解部分),然后再用上述相同 溶液稀释至 20ml,静脉滴注时间应至少为 15~60 分钟。 尽管乳酸钠林格注射液可作为本品静脉注射液的溶媒,但不能用于本品最初的溶解过程 (参见【注意事项】配伍禁忌乳酸钠林格注射液部分和【用法用量】使用/操作说明乳酸钠 林格注射液部分)。 采用静脉推注时,本品应按上述方法溶解,静脉推注时间至少应超过 3 分钟。 肌内注射: 尽管 2%盐酸利多卡因注射液可作为本品肌内注射液的溶媒,但不能用于本品最初的溶 解过程(参见配伍禁忌利多卡因部分和使用/操作说明利多卡因部分)。 使用/操作说明: 本品的溶解 本品每瓶内装 1.5g 或 3.0g 头孢哌酮/舒巴坦。
舒普深-反对意见处理

仅供内部使用
舒普深—出血
An open trial of cefoperazone plus sulbactam for the treatment of fever in cancer patients
前瞻性研究 673例发热(肿瘤)患者 1.5:1 40例,2:1 633例,q6h 6例(0.9%)发生凝血障碍,无出血
imipenem was as effective as the 4-g daily dose. Diarrhea was more frequent in patients receiving
cefoperazone, whereas nausea occurred more often with imipenem. No antibiotic-related hemorrhage
seizures were associated with high doses of imipenem. Seizures occurred in 3 of 29 patients (10.3%)
who were receiving 4 g/d of imipenem, in 3 of 136 patients (2.2%) who were receiving cefoperazone
4. 注意:用药5分钟内应视为过敏性休克的高危期。皮试前、 注药前以及在使用过程中都应严格观察,并随时做好抢救 准备。
8
仅供内部使用
皮试问题解答 如何避免头孢菌素皮试假阴性
1. 抗组胺药抑制I型变态反应,应在试验前24小时停药;
2. 阿司咪唑因其长效应用,应停药l周;
3. 肾上腺素能药、黄嘌呤类药对I型变态反应的皮试有抑制, 需停药12小时;
舒普深与稳可信存在配伍禁忌

舒普深与稳可信存在配伍禁忌发表时间:2012-06-18T10:38:50.670Z 来源:《医药前沿》2012年第2期供稿作者:杨芸杨美蓉[导读] 目前,临床上不断采用新药,但多数新药在说明书及《400种注射配伍变化检索表》中未查到相关配伍禁忌的说明。
杨芸杨美蓉(江苏省无锡市第五人民医院江苏无锡 214001)【中图分类号】R969.2 【文献标识码】A 【文章编号】2095-1752(2012)02-0180-01 目前,临床上不断采用新药,但多数新药在说明书及《400种注射配伍变化检索表》中未查到相关配伍禁忌的说明。
我们通过临床观察(肉眼观察)发现舒普森(头孢哌酮钠舒巴坦钠)与稳可信(盐酸万古霉素)存在配伍禁忌,现报道如下: 1 临床观察患者为肝功能衰竭行连续性血液透析滤过,有深静脉置管,感染严重,考虑复数菌感染,输入0.9%氯化钠100ml加舒普深1.5g(辉瑞制药有限公司),液路通畅,溶液无色澄清,0.9%氯化钠100ml加稳可信1.0g(苏州礼来公司)相互连输时,约1min发现输液管中及茂菲氏管中液体出现乳白色混浊,静置后出现颗粒状沉淀,立即更换输液器,液路通畅,严密观察患者无不良反应。
2 实验2.1 实验用物辉瑞制药有限公司生产的舒普深1.5g/支,江苏苏中药业集团股份有限公司的0.9%氯化钠注射液100ml, 苏州礼来公司的稳可信500mg/支。
2.2 实验方法将舒普深1.5 g用0.9%氯化钠注射液100ml溶解,将稳可信0.5加入0.9%氯化钠注射液100ml溶解,用5ml注射器各取上两种溶液1ml混合注入试管,约2min可见溶液变浑浊,8min可见细小的乳白色悬浮物,12min后可见大量的乳白色絮状沉淀,静止24h絮状物无变化[1]。
3 讨论舒普深(头孢哌酮钠舒巴坦钠)是一种复方制剂,头孢哌酮为第三代头孢菌素,通过抑制敏感细菌细胞壁的生物合成而达到杀菌作用,舒巴坦除对瑟菌科和不动杆菌外,对其他细菌无抗菌活性,但是舒巴坦对由B-内酰胺类抗生素耐药菌株产生的多数重要的B-内酰胺酶具有不可逆性的抑制作用,舒巴坦可防止耐药菌对青霉素类和头孢菌素类抗生素的破坏,并且舒巴坦钠与青霉素类和头孢菌素类抗生素具有明显的协同作用,本复方制剂对所有对头孢哌酮敏感的细菌均具有抗菌活性[2,是临床上常用的广谱抗菌药物,主要以静脉给药为主。
舒普深产品知识PPT课件

否 培养 –
培养 + 2
培养 –
是
培养 + 3
查找其他病原菌、
调整抗生素治疗,
可能的情况下进行
并发症;
寻找其他病原菌、并发症,
考虑
抗生素降阶梯治疗,
考虑其他诊断
考虑其他诊断
停用抗生素
对部分患者治疗7-8天后
2021
或其他感染部位
或其他感染部位
再进行评价
呼吸科肺炎
1.新出现的咳嗽、咳痰,或原有呼吸道疾病症状加重,并出现脓
2021
8
舒普深产品有效期
法定有效期 2 年,产品有5%溢装量,可保证在整个有效期内产品的有 效活力在规定的范围内。
产品采用结晶型原料药,因此在稳定性和纯度等方面均优于冻干粉。 在较为宽松的储存条件下仍能保证有效期,国家标准是储存在20℃以下,
辉瑞标准是储存在25℃以下。
2021
9
目录
Part1 Part2 Part3
换气次数为30次/小时,100%新风。 温度控制在20±1℃,湿度低于25%。 无菌室内定期进行福尔马林喷雾灭菌,并每天用平
碟法和棉签法对环境状况进行监测。 整个无菌环境定期进行严格的验证。
2021
6
舒普深产品的实际标准高于药典指标
性 状 :结晶性粉末;中国药典:粉末或结晶性粉末。 不溶性微粒(镜检): 10um 不超过700 个/瓶, 25 um
呼吸科肺炎诊疗流程
23
怀疑HAP、VAP或HCAP
获取下呼吸道(LRT)标本进行培养(定量或半定量)和显微镜检查
同时就可按照规范和当地微生物学资料开始经验性抗感染治疗
1
第2天和第3天:了解细菌培养结果并评价临床治疗反应: (体温、PCT、WBC、胸片、氧饱和度、脓痰、血液动力学改变和器官功能)
舒普深说明书

【成份】
本品为复方制剂,其组份为头孢哌酮钠和舒巴坦钠(头孢哌酮与舒巴坦为 2:1)。
头 孢 哌 酮 钠 的 化 学 名 称 为 : (6R,7R)-3-[[(1- 甲 基 -1H- 四 唑 -5- 基 ) 硫 ] 甲
基]-7-[(R)-2-(4-乙基-2,3-二氧代-1-哌嗪碳酰氨基)-2-对羟基苯基-乙酰氨基]-8-氧代-5-硫杂
血液系统:曾报道有患者出现中性粒细胞轻微减少(0.4%,5/1131)。与其他β-内酰 胺类抗生素一样,长期使用本品可发生可逆性中性粒细胞减少症(0.5%,9/1696)。在治疗 过程中,某些患者可出现直接库姆斯试验阳性反应(5.5%,15/269)。与文献中有关其他头 孢菌素的报道一样,本品可降低血红蛋白(0.9%,13/1416)和血细胞比积(0.9%,13/1409)。 曾发生过一过性嗜酸细胞增多(3.5%,40/1130)和血小板减少症(0.8%,11/1414)。有报 道,发生过低凝血酶原血症(3.8%,10/262)。
舒普深说明书

舒普深说明书【别名】舒巴坦-头孢哌酮、舒普深、瑞普欣【外文名】Sulbactam and Cefopcrazone, Cefperazone-Sulbactam【药理作用及用途】本品复合制剂,舒巴坦为广谱酶抑制剂同时具有较弱的抗菌活性,对金葡菌及阴性杆菌产生的β-内酰胺酶具有强的不可逆的抑制作用,但对某些阴性杆菌染色体介导的β-内酰胺酶无活性头孢哌酮是一第三代头孢菌素,对β-内酰胺酶的稳定性较差,二者联合,不但对阴性杆菌显示明显的协同抗菌活性,联合后的抗菌作用是单独头孢哌酮的4倍。
流感杆菌、产气杆菌、摩根杆菌、类杆菌、大肠杆菌、氟劳地枸橼酸杆菌、阴沟肠杆菌、不动杆菌、肺炎杆菌等均对本品有较好的敏感性。
主要用于由敏感菌引起的呼吸系统、泌尿生殖系统感染、腹膜炎、胆囊炎、胆道感染、腹腔内感染、败血症等的治疗。
【用法及用量】静脉滴注、肌内注射: 成人一次1-2g(头孢哌酮0.5~1g)每日2~4次。
小儿:每日40~80mg/kg(体重)分2~4次用药。
最大剂量:每日160mg/kg,分2~4次用药,舒巴坦的最大剂量每日不得超过80mg/kg。
【不良反应】本品应用中可出现头孢哌酮单用药的某些不良反应,但病人对本药有较好的耐受性。
皮肤过敏,腹泻,药物热。
可逆性中性粒细胞减少,血红蛋白及红细胞压积降低,一过性嗜酸性粒细胞增多,血小板减少和凝血酶原降低。
谷草转氨酶、谷内转氨酶、碱性磷酸酶或血胆红素一过性升高。
【注意事项】①对本品任何成份过敏者禁用。
β-内酰胺类药物过敏者慎用。
②严重胆囊炎患者、严重肾劝能不良者慎用。
③用药期间禁洒及禁服含酒精药物。
【规格】注射剂: lg中含舒巴坦 500mg、头孢哌酮 500mg。
头孢说明书

头孢说明书头孢氨噻醚酯说明书【别名】头孢泊肟酯,头孢氨噻醚酯【外文名】Cefpodoxime Proxetil ,Banan,Vantin【作用与用途】本品口服第三代头孢菌素.本品供口服,由肠道酯酶水解,释放出头孢泊肟(Cefpodoxime)而发挥抗菌活性、对链球菌、肺炎球菌、肠杆菌、克雷白菌、变形杆菌及流感杆菌等均有良好抗菌作用临床主要用于敏感菌所致的肺炎、急性支气管炎、咽喉炎、扁桃腺炎、肾盂肾炎、膀胱炎、淋病性尿道炎及皮肤软组织感染等。
【剂量与用法】剂量,成人100mg(效价)/次,2次/日,饭后服,12岁以下儿童每日2次,每次10mg/kg.【不良反应】主要为过敏反应,有皮疹、荨麻疹、瘙痒、嗳气及消化道反应等。
对青霉素过敏者慎用。
【规格】片剂:100mg/片,200mg/片。
混悬液:50mg/5ml, 100mg/5ml.氨噻肟吡戊头孢说明书【别名】头孢匹罗,氨噻肟吡戊头孢【外文名】Cefpirome ,Cefrom【作用与用途】本品半合成第四代头孢菌素,具广谱抗菌活性,对葡萄球菌、耐青霉素的肺炎球菌及肠球菌均有效对绿脓杆菌的效果与头孢他啶相似,对很耐抗生素的病原菌均有良好疗效。
临床主要用于严重的呼吸道、尿道感染及皮肤和软组织等感染。
【适应症】用于治疗严重下呼吸道感染、复杂性尿路感染等的疗效与第3代头孢曲松、头孢他定等相仿。
【用量用法】成人,1g~2g/次,1次/日,肌注,静注或静滴。
静脉注射:成人用量1~2g/次,1~2次/日。
【副作用】般为腹泻及皮疹等。
【规格】针剂:0.25g,0.5g, 1g,2.0g。
头孢地尼说明书【药理作用】本品口服第三代头孢菌素,抗菌谱广,对葡萄球菌和链球菌属的抗菌作用与头孢泊肟酯相仿,对肠杆菌科细菌的抗菌活性低于头孢克肟2-4倍肠球菌、铜绿假单胞菌和其他假单胞菌属、不动杆菌属等对本品耐药。
【临床应用】本品可用于治疗扁桃体炎、鼻窦炎、中耳炎、急性支气管炎、肺炎、腹腔、泌尿生殖道等感染。
舒普深产品知识

舒普深的无菌生产环境-舒普深在无菌区进行配料及混合,在万级洁净区,-局部百级进行粉针分装。->换气次数为30次/小时,100%新风。->温度控制在 0士1℃,湿度低于25%。-无菌室内定期进行福尔马林喷雾灭菌,并每天用平-碟法和棉签法对环境状况进行监测-整个无菌环境定期进行严格的验证。
舒普深产品的实际标准高于药典指标-性状:结晶性粉末;中国药典:粉末或结晶性粉末。->不溶性微粒(镜检):≥10um不超过700个/瓶,≥25Um25个/瓶;USP分别为3000个和300个;-中国药典不要求。-不溶性微粒(机检):≥10um:不超过500个/瓶,≥25Um:-50个/瓶;U P分别为3000个和300个;CP不要求。-D-内控标准要求头孢哌酮和舒巴坦每瓶装量均为475-525mg,-即标示量的95-110%;中国药典为 示量的90.0-115.0%。-有多项杂质指标551B,T-1551C,D,E,F,G 。
目录-◆Part1-生产工艺-◆Part2-药物特征-◆Part3-说明书解读
特征一:抗菌谱广一覆盖院感常见菌-需氧菌-厌氧菌-革兰阳性菌-革兰阴性菌-革兰阳性菌革兰阴性菌-葡萄球菌-大肠杆菌-不动杆菌-梭状芽胞杆菌-脆弱类 菌-链球菌-克雷伯菌-绿脓杆菌-真杆菌-其他类杆菌-枸橼酸菌-淋球菌-乳杆菌-梭杆菌-脑膜炎球菌-消化球菌-费氏球菌-沙门菌-百日咳杆菌-消化链球 -志贺菌-卡他莫拉菌-沙雷菌-摩根杆菌-奇异变形杆菌普罗菲登斯菌-普通变形杆菌小肠结肠炎耶尔森菌-流感嗜血杆菌嗜麦芽窄食单孢菌->与三代头孢比,增 了抗菌谱,尤其是不动和厌氧菌->舒巴坦能直接杀灭不动杆菌。
舒普深主要材料的供应商-活性原料头孢哌酮钠和舒巴坦钠:辉瑞日本名古屋工厂->药用西林瓶:由法国Saint Gobain Desjongeres公司 ->氯丁基橡胶塞:由新加坡West Pharmaceutical Services?公司供应等。-包装:由中国本地公司生产
注射用头孢哌酮钠舒巴坦钠说明书--舒普深之欧阳歌谷创作

头孢哌酮钠舒巴坦钠粉针剂说明书欧阳歌谷(2021.02.01)【药品名称】通用名:注射用头孢哌酮钠舒巴坦钠英文名:Cefoperazone Sodium and Sulbactam Sodium for Injection 汉语拼音:Zhusheyong Toubaopaitongna Shubatanna商品名:舒普深英文商品名:SULPERAZON【成份】本品为复方制剂,其组分为头孢哌酮钠和舒巴坦钠。
头孢哌酮钠的化学名称为:(6R,7R)-3-[[(1-甲基-1H-四唑-5-基)硫]甲基]-7-[(R)-2-(4-乙基-2,3-二氧代-1-哌嗪碳酰氨基)-2-对羟基苯基-乙酰氨基]-8-氧代-5-硫杂-1-氮杂双环[4.2.0]辛-2-烯-2-甲酸钠。
化学结构式:分子式:C25H26N9NaO8S2分子量:667.65Cas No:62893-20-3舒巴坦钠的化学名称为:(2S,5R)-3,3-二甲基-7氧代-4-硫杂-1-氮杂双环[3.2.0]庚烷-2-羧酸钠-4,4-二氧化物。
化学结构式:分子式:C8H10NNaO5S分子量:255.22Cas No:69388-84-7【性状】本品为白色或类白色粉末。
【适应症】单独应用本品适用于治疗由敏感菌所引起的下列感染:上、下呼吸道感染;上、下泌尿道感染;腹膜炎、胆囊炎、胆管炎和其他腹腔内感染;败血症;脑膜炎;皮肤和软组织感染;骨骼和关节感染;盆腔炎、子宫内膜炎、淋病和其他生殖道感染。
联合用药:由于本品具有广谱抗菌活性,因此单用本品就能够治疗大多数感染,但有时也需要本品与其他抗生素联合应用。
当本品与氨基糖苷类抗生素合用时(参见配伍禁忌氨基糖苷类抗生素部分),在治疗过程中应监测患者的肾功能(参见用法与用量肾功能障碍患者的用药部分)。
【规格】1.5g(以头孢哌酮计1000mg,以舒巴坦计500mg)【用法与用量】成人用药:本品成人每日推荐剂量如下:上述剂量分等量,每12小时给药一次。
注射用头孢哌酮钠舒巴坦钠与盐酸氨溴索注射液存在配伍禁忌 姜荣 姜华丽

注射用头孢哌酮钠舒巴坦钠与盐酸氨溴索注射液存在配伍禁忌姜荣姜华丽慢性支气管炎合并感染病人,临床上常用盐酸氨溴索(开顺) 进行祛痰治疗,同时应用药物头孢哌酮钠舒巴坦钠(舒普深)进行抗感染治疗。
注射用头孢哌酮钠舒巴坦钠为复方制剂,对流感嗜血杆菌、革兰阳性菌、铜绿假单胞菌具有良好的抗菌作用,盐酸氨溴索注射液为溴己新在体内的代谢物,具有粘痰排除、促进及溶解分泌物的特性,可促进呼吸道内粘稠分泌物的排除及减少粘液的滞留,主要适用于伴有痰液分泌不正常及排痰功能不良的急慢性呼吸道疾病,对于颅脑外科术后的患者,一般常用以上两种药物,在实际应用过程中,静滴输注头孢哌酮钠时,给予盐酸氨溴索静推时,发现输液管中有白色混浊物,重新更换输液管输入盐酸氨溴索时,无浑浊变色现象,为了证实上述两种药物是否存在配伍禁忌,我们对其进行了配伍试验,现报告如下。
1 病例资料病例1:慢性支气管炎合并感染病人,护士遵医嘱将0.9%氯化钠溶液100mL加入头孢哌酮钠舒巴坦钠2g静脉输注,随后静脉注射0.9%氯化钠溶液20mL加入开顺150mg,输液器头皮针内立即出现白色混浊,立即拔出针头,放置2h后依然呈白色混浊状。
病例2:慢性支气管炎合并感染病人,护士遵医嘱将0.9%氯化钠溶液100mL加入头孢曲松钠2g给病人静脉输注,随后静脉注射0. 9%氯化钠溶液20mL加入开顺150mg,输液器头皮针内立即出现白色混浊,立即拔出针头,放置2h后依然呈白色混浊状。
2 配伍试验(1)材料:注射用头孢哌酮钠每支1.5g;盐酸氨溴索每支15mg。
(2)方法:将注射用头孢哌酮钠加入0.9%氯化钠注射液100ml中,分别抽取头孢哌酮钠稀释液和盐酸氨溴索注射液3ml,使两者混合,随即出现白色混浊液,放置15-20min浑浊未变澄清。
3 讨论开顺为盐酸氨溴索的白色冻干状物或粉末,在药品说明书上的药物互相作用中注明:本品与抗生素协同治疗(阿莫西林、头孢呋辛、红霉素、多西环素) 可导致抗生素在肺组织中浓度升高,与其他药物合用所致临床相关不良反应影响未见报道。
舒普深产品知识[知识荟萃]
![舒普深产品知识[知识荟萃]](https://img.taocdn.com/s3/m/17dd45f57e21af45b207a83d.png)
舒巴坦
头孢哌酮
10.4
26.8
20.0
20.4
5.7
9.8
19.1
39.0
5.9
5.6
27.0
36.7
在给药后不同时间测定,舒普深能够从血液迅速渗透到组织和体液中达到治
疗浓度
8. Okamura K, et al. Acta Urol Jpn. 1989;35:727-734.
13. Nakagawa K, et al. Surg Care. 1990;32(6):875-879.
实验室检查:
铜绿假单胞 菌、 鲍曼不动杆菌 及产ESBL菌
无有
HCAP
有
经验性使用SUL
实验室检查: 铜绿假单胞菌、 鲍曼不动杆菌 及其它革兰氏阴 性菌
HAP
有感染MDR 的高危因素
轻度
6
多早发性
经验性使用其他抗生素
无
有
经验性使用SUL
5
VAP
中、重度
多迟发性
使用其他抗生素
转为SUL 4
使用其他抗生素 转为SUL 2
Kerry M. Empey, Pharmacotherapy 22(1):81-87, 2002
行业重点
“…在不同的研究中,亚安培南的使用被确定在当地是导致对碳氢霉烯耐药和beta内酰胺耐 药的铜绿假单胞菌主要相关因素”
Dr. Lepper et al, AAC, Sept. 2002, p. 2920–2925
225 个/瓶;USP分别为3000个和300个;中国药典不要 求。 不溶性微粒(机检): 10um: 不超过500 个/瓶, 25 um: 50 个/瓶; USP分别为3000个和300个;CP不要求。 内控标准要求头孢哌酮和舒巴坦每瓶装量均为475525mg,即标示量的95-110%;中国药典为标示量的90.0115.0%。 行业重点 有多项杂质指标国内不控制,而辉瑞却有严格的控制,如
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
OH O
COONa CH2S
N
CH3
N N
H5C2 N
N CONH
C
CONH
H
H
H
S
N
N
O
O
分子式:C25H26N9NaO8S2; 分子量:667.65
舒巴坦钠的化学名称为:(2S,5R)-3,3-二甲基-7 氧代-4-硫杂-1-氮杂双环[3.2.0] 庚烷 -2-羧酸钠-4,4-二氧化物,化学结构式:
血液系统:曾报道有患者出现中性粒细胞轻微减少(0.4%,5/1131)。与其他β-内酰 胺类抗生素一样,长期使用本品可发生可逆性中性粒细胞减少症(0.5%,9/1696)。在治疗 过程中,某些患者可出现直接库姆斯试验阳性反应(5.5%,15/269)。与文献中有关其他头 孢菌素的报道一样,本品可降低血红蛋白(0.9%,13/1416)和血细胞比积(0.9%,13/1409)。 曾发生过一过性嗜酸细胞增多(3.5%,40/1130)和血小板减少症(0.8%,11/1414)。有报 道,发生过低凝血酶原血症(3.8%,10/262)。
利多卡因: 由于本品与 2%盐酸利多卡因注射液混合后有配伍禁忌,因此应避免在最 初溶解时使用此溶液。在两步稀释法中,先用注射用水进行最初的溶解,再用 2%盐酸利多 卡因注射液作进一步稀释,从而得到能够相互配伍的混合药液(参见使用/操作说明利多卡
Version No:20070309
第 5 页,共 11 页
在血液透析患者中,舒巴坦的药物动力学特性有明显改变。头孢哌酮在血液透析患者中 的血清半衰期轻微缩短。因此在血样透析后,应给予一剂头孢哌酮/舒巴坦。
静脉给药: 采用间歇静脉滴注时,本品每瓶用适量的 5%葡萄糖溶液或 0.9%注射用氯化钠溶液或 灭菌注射用水溶解(参见使用/操作说明本品的溶解部分),然后再用上述相同溶液稀释至 20 毫升,静脉滴注时间应至少为 15-60 分钟。 尽管乳酸钠林格注射液可作为本品静脉注射液的溶媒,但不能用于本品最初的溶解过程 (参见配伍禁忌乳酸钠林格注射液部分和使用/操作说明乳酸钠林格注射液部分)。 采用静脉推注时,本品应按上述方法溶解,静脉推注时间至少应超过 3 分钟。 肌内注射: 尽管 2%盐酸利多卡因注射液可作为本品肌内注射液的溶媒,但不能用于本品最初的溶 解过程(参见配伍禁忌利多卡因部分和使用/操作说明利多卡因部分)。 使用/操作说明: 本品的溶解 本品每瓶内装 1.0 克,1.5 克和 3.0 克头孢哌酮/舒巴坦。
【规格】
1.0g(以头孢哌酮计 500 mg, 以舒巴坦计 500 mg) 1.5g(以头孢哌酮计 1000 mg, 以舒巴坦计 500 mg) 3.0g(以头孢哌酮计 2000 mg, 以舒巴坦计 1000 mg)
【用法用量】
成人用药:
本品成人每日推荐剂量如下:
比例
头孢哌酮/舒巴坦(克)
1:1
2.0-4.0
因部分)。
【孕妇及哺乳期妇女用药】
胃肠道反应:与其他抗生素一样,本品最常见的副作用为胃肠道反应。有报道,腹泻 /稀便最为常见(3.9%),其次为恶心和呕吐(0.6%)。
皮肤反应:有报道,与所有青霉素类和头孢菌素类抗生素一样,过敏反应表现为斑丘 疹(0.6%)和荨麻疹(0.08%)。这些过敏反应易发生在有过敏史,特别是对青霉素过敏的 患者中。
用乳酸钠林格注射液 本品应使用灭菌注射用水进行溶解(参见配伍禁忌乳酸钠林格注射液部分)。采用两步 稀释法:先用灭菌注射用水溶解(如上表所示),再用乳酸钠林格注射液稀释至舒巴坦的浓 度为 5 毫克/毫升的溶液(用 2 毫升初配液稀释至 50 毫升乳酸钠林格注射液中或 4 毫升初配 液稀释至 100 毫升乳酸钠林格注射液中)。 用利多卡因 本品应使用灭菌注射用水溶解(参见配伍禁忌利多卡因部分)。 为获得浓度≥250 毫克/毫升的头孢哌酮溶液,应采用两步稀释法:先用灭菌注射用水溶
发生严重过敏反应的患者须立即给予肾上腺素紧急处理,必要时应吸氧、静脉给予激 素,并采用包括气管内插管在内的畅通气道等治疗措施。
2. 肝功能障碍患者的用药 头孢哌酮主要经胆汁排泄。当患者有肝脏疾病和/或胆道梗阻时,头孢哌酮的血清半衰 期通常延长并且由尿中排出的药量会增加。即使患者有严重肝功能障碍时,头孢哌酮在胆汁 中仍能达到治疗浓度并且其半衰期仅延长 2-4 倍。 遇到严重胆道梗阻、严重肝脏疾病或同时合并肾功能障碍时,可能需要调整用药剂量。 同时合并有肝功能障碍和肾功能损害的患者,应监测头孢哌酮的血清浓度,根据需要调 整用药剂量。对这些患者如未密切监测本品的血清浓度,头孢哌酮的每日剂量不应超过 2 克。 3. 一般注意事项 与其他抗生素一样,少数患者使用头孢哌酮治疗后出现了维生素 K 缺乏,其机制很可 能与合成维生素的肠道菌群受到抑制有关,包括营养不良、吸收不良(如肺囊性纤维化患者) 和长期静脉输注高营养制剂在内的患者存在上述危险。应监测上述这些患者以及接受抗凝血 药治疗患者的凝血酶原时间,需要时应另外补充维生素 K。
总剂量 (克)
1.0 1.5 3.0
相当于头孢哌酮+舒巴坦的剂量 (克) 0.5+0.5 1.0+0.5 2.0+1.0
稀释液的体积 (毫升) 3.4 3.2 6.2
最高终浓度 (毫克/毫升)
125+125 250+125 250+125
本品在头孢哌酮和舒巴坦分别为 10-250 毫克/毫升和 5-125 毫克/毫升浓度范围内,可与 注射用水,5%葡萄糖注射液,生理盐水,5%葡萄糖和 0.225%氯化钠注射液,5%葡萄糖和 0.9%氯化钠注射液等配伍。
其他:头痛(0.04%)、发热(0.5%)、注射部位疼痛(0.08%)和寒战(0.04%)。 实验室检查异常:曾发现肝功能一过性升高,血清门冬氨酸转氨酶(SGOT)为 5.7% (94/1638),血清丙酮酸转氨酶(SGPT)为 6.2%(95/1529),碱性磷酸酶为 2.4%(37/1518), 胆红素为 1.2%(12/1040)。 局部反应:本品肌内注射耐受良好,偶有注射后注射部位出现一过性疼痛。与其他青 霉素类和头孢菌素类抗生素一样,当通过静脉插管注射本品时,某些患者可在注射部位发生 静脉炎(0.1%)。 有报道,本品上市后还发生了下列不良反应:一般不良反应:过敏反应(包括休克), 心血管系统:低血压,胃肠道:伪膜性肠炎,造血系统:淋巴细胞减少症,皮肤/附件:瘙 痒,Stevens-Johnson 综合征,泌尿系统:血尿,血管系统:血管炎。
核准日期: 2007 年 03 月 09 日
注射用头孢哌酮钠舒巴坦钠说明书
请仔细阅读说明书并在医师指导下使用 【药品名称】 通用名称:注射用头孢哌酮钠舒巴坦钠 商品名称:舒普深(SULPERAZON) 英文名称:Cefoperazone Sodium and Sulbactam Sodium for Injection 汉语拼音:Zhusheyong Toubaopaitongna Shubatanna
Version No:20070309
第 3 页,共 11 页
解(如上表所示),再用 2%利多卡因溶液稀释,使约 0.5%盐酸利多卡因溶液中头孢哌酮和 舒巴坦的浓度分别达到 250 毫克/毫升和 125 毫克/毫升。
【不良反应】
通常不良事件是从临床试验期间及产品上市后的报告中收集的。很多事件可能是由用 药以外的因素如潜伏的疾病引起的。由于多数情况下不可能确定特定的因果关系(甚至许多 不良事件并不是药物不良反应),因此即便在不能确定是否由本品引起的情况下,也在此报 告了所收集到的所有不良事件。本品通常耐受良好,大多数不良反应为轻度或中度,可以耐 受,不影响继续治疗。从约有 2500 位患者参加的比较性或非比较性临床试验数据库中观察 到下列不良反应:
COONa
O N
CH 3 CH 3
S OO
分子式: C8H10NNaO5S 分子量:255.22
【性状】本品为白色或类白色粉末。
【适应症】
Version No:20070309
第 1 页,共 11 页
单独应用本品适用于治疗由敏感菌所引起的下列感染: 上、下呼吸道感染; 上、下泌尿道感染; 腹膜炎、胆囊炎、胆管炎和其他腹腔内感染; 败血症; 脑膜炎; 皮肤和软组织感染; 骨骼和关节感染; 盆腔炎、子宫内膜炎、淋病和其他生殖道感染。 联合用药: 由于本品具有广谱抗菌活性,因此单用本品就能够治疗大多数感染,但有时也需要本品 与其他抗生素联合应用。当本品与氨基糖苷类抗生素合用时(参见配伍禁忌氨基糖苷类抗生 素部分),在治疗过程中应监测患者的肾功能(参见【用法用量】肾功能障碍患者的用药部 分)。
【禁忌】 已知对青霉素类、舒巴坦、头孢哌酮及其它头孢菌素类抗生素敏者禁用。【注意事项】
1. 过敏反应 有报道,接受β-内酰胺类或头孢菌素类抗生素治疗的患者可发生严重的及偶可发生的
Version No:20070309
第 4 页,共 11 页
致死性过敏反应。这些过敏反应更易发生在对多种过敏原有过敏史的患者中。一旦发生过敏 反应,应立即停药并给予适当的治疗。
Ref 2 p2 用法用量部分 paragraph 2, L4-5 p10, 药代动力学部分 paragraph cont, L 2 paragraph 2, L3
【成份】
本品为复方制剂,其组份为头孢哌酮钠和舒巴坦钠。
头 孢 哌 酮 钠 的 化 学 名 称 为 : (6R,7R)-3-[[(1- 甲 基 -1H- 四 唑 -5- 基 ) 硫 ] 甲 基]-7-[(R)-2-(4-乙基-2,3-二氧代-1-哌嗪碳酰氨基)-2-对羟基苯基-乙酰氨基]-8-氧代-5-硫杂 -1-氮杂双环[4.2.0]辛-2-烯-2-甲酸钠,化学结构式:
与其他抗生素一样,长期使用本品可引起不敏感细菌过度生长。因此在治疗过程中应 仔细观察患者的病情变化。与其他全身应用的抗生素一样,建议在疗程较长时应定期检查患 者是否存在各系统器官的功能障碍,其中包括肾脏、肝脏和血液系统。这一点对新生儿,尤 其是早产儿和其他婴儿特别重要。
