中国矿业大学《无机及分析化学》模拟试题(1)
《无机及分析化学BI》试题A卷(1)

是( )
A、AgCl 饱和溶液
B、1 mol·L-1NaCl
C、1 mol·L-1AgNO3
D、4 mol·L-1NaNO3
14. BaSO4 饱和溶液加水稀释后,下面说法正确的是( )
A. BaSO4 的溶解度增大
B. BaSO4 溶解度减小
C. BaSO4 的 Ks$p 增大
D. BaSO4 的离子积减小
36.在标准状态下,所有纯态单质的△fG
$ m
均为
0。(
)
37.比较两个化学反应的反应速率,反应物浓度较大的反应速率快。( ) 38.一定条件下的化学反应,随着反应的进行,速率常数和反应速率逐渐变小。( ) 39.正催化剂加快正反应速率,减小逆反应的速率。( ) 40.1.0 mol·L-1NaOH 和 1.0 mol·L-1NH3·H2O,它们的氢氧根离子浓度相同。( ) 41.某一元弱酸溶液被稀释后,解离度和氢离子浓度增加。( ) 42.在一定条件下,已知反应 H2A 2H++A2-,表明该反应是二元强酸。( ) 43.在有 AgCl 固体存在的溶液中,当加入等体积 1 mol·L-1 的 NaCl 溶液后,会使 AgCl 溶解度 显著减小。( ) 44.利用沉淀转化可使某些既难溶于水又不溶于酸的物质转化为可溶性物质。( ) 45.在分步沉淀中,当第一种被沉淀的离子浓度 c1≤1.0×10-5 mol·L-1,而第二种离子还没有生成 沉淀时,则这两种离子能被定性分离开。( ) 46.电极电势越高,电对中氧化态物质在水中氧化能力越强。( ) 47.在 Zn|ZnSO4||CuSO4|Cu 原电池中,向 ZnSO4 溶液中通入 NH3,电动势变小。( ) 48.氧化还原反应是参与反应的所有元素的原子都发生电子的转移或偏移。( ) 49.所有的配合物都必须包含内界和外界两部分。( ) 50.[Co(NO2)3(NH3)3]的命名为三硝基·三氨合钴(Ⅲ)。( ) 51.溶胶粒子带正电荷,所以胶核只吸附带正电荷的离子。( ) 52.同价反离子,水合离子半径越小,对胶体的凝结能力越强。( )
无机及分析化学(Ⅰ)习题解答

无机及分析化学(Ⅰ)习题解答目录第1章分散体系 (1)第2章化学热力学基础 (8)第3章化学反应速率和化学平衡 (15)第4章物质结构 (22)第5章分析化学概述 (27)第6章酸碱平衡 (31)第7章酸碱滴定法 (36)第8章沉淀溶解平衡 (44)第9章重量分析法和沉淀滴定法 (49)第10章配位化合物 (53)第11章配位滴定法 (62)第12章氧化还原反应 (67)第13章氧化还原滴定法 (78)第14章电势分析法 (83)第15章吸光光度分析法 (86)第16章试样分析中常用的分离方法简介 (90)第17章重要生命元素简述 (93)第18章原子核化学简介 (96)第1章 分散体系1-1.人体注射用的生理盐水中,含有NaCl 0.900%,密度为1.01g·mL -1,若配制此溶液3.00×103g ,需NaCl 多少克?该溶液物质的量浓度是多少?解:配制该溶液需NaCl 的质量为:m (NaCl)=0.900%×3.00×103g=27.0g该溶液的物质的量浓度为:-1-13-1-327.0g/58.5g mol (NaCl)==0.155mol L (3.0010g/1.01g m L )10c ⋅⋅⨯⋅⨯ 1-2.把30.0g 乙醇(C 2H 5OH)溶于50.0g 四氯化碳(CCl 4)中所得溶液的密度为1.28g∙mL -1,计算:(1)乙醇的质量分数;(2)乙醇的物质的量浓度;(3)乙醇的质量摩尔浓度;(4)乙醇的摩尔分数。
解:(1)w (C 2H 5OH) =25254(C H OH)30.0g (C H OH)(CCl )30.0g 50.0gm m m =++=0.38 (2)-12525-1-3(C H OH)30.0g/46g mol (C H OH)[(30.0+50.0)g /1.28g mL ]10n c V ⋅=⋅⨯==10.4mol·L -1 (3)b (C 2H 5OH) =-125-3430.0g(C H OH)46g mol (CCl )50.010kgn m ⋅=⨯=13.0mol·kg -1 (4)x (C 2H 5OH) =-125254-1-130.0g(C H OH)46g mol =30.0g 50.0g (C H OH)+(CCl )+46g mol 153.6g mol n n n ⋅⋅⋅ =0.650.660.650.33=+ 1-3.将5.0g NaOH 、NaCl 、CaCl 2分别置于水中,配成500mL 溶液,试求c (NaOH)、c (NaCl)、c (12CaCl 2)。
2010-2011-1无机及分析化学1(A)试卷

36、化学反应等温方程式(范特-荷甫等温方程式)的表达式为,某反应的标准平衡常数为1.0×10-3,该反应在标准态、298.15K时的自由能变化值 为,自发方向为。
37、H2(g)、C(石墨)、C(金刚石)、H2O(g)、H2O(l)、CO(g)、CO2(g)七种物质中,其标准摩尔生成焓 为零的物质有和,而标准摩尔燃烧焓 为零的物质有和。
12、对钾原子来说,其原子核外轨道能级顺序是:( )
A、E1s<E2s<E2p<E3s<E3p<E4s<E3d...B、E1s<E2s=E2p<E3s=E3p=E3d<E4s...
C、E1s=E2s<E2p=E3s<E3p<E3d=E4s...D、E1s>E2s=E2p>E3s=E3p=E3d>E4s...
7、中和pH相等的相同体积的HCl和HAc溶液,所需NaOH的量相等。( )
8、MgF2在MgCl2溶液中的溶解度比在水中的溶解度大。()
9、将反应2Fe3++Cu=2Fe2++Cu2+改写成Fe3++1/2Cu=Fe2++1/2Cu2+,两反应的KӨ和EӨ值均相同。( )
10、Fe2+与CN-生成的配合物磁力矩为0.00 B.M,根据配合物价键理论,推测Fe2+采取内轨型杂化。( )
A、4.75 B、4.751 C、9.25 D、9.251
28、某溶液中含有KCl、KBr和K2CrO4,浓度均为0.010molL-1。向溶液中逐滴加入
0.010molL-1的AgNO3溶液时,最先和最后沉淀的是:( )
大学《无机及分析化学》试题及答案

大学《无机及分析化学》试题及答案大学《无机及分析化学》试题及答案一、判断题 (每小题1分共10分 )1.σ键和π键在分子中均可单独存在。
()2.系统误差是不可测的。
()3.极性分子间仅存在取向力,非极性分子间只存在色散力。
()4.等价轨道处于全充满、全空、半充满状态时原子能量较低。
()5.施肥过多造成的“烧苗”现象,是由于植物细胞液的渗透压小于土壤溶液的渗透压引起的。
()6.醋酸溶液经稀释后其解离度增大,因而可使其H+ 浓度增大。
()7.BF3和NH3都具有平面三角形的空间结构。
()8.CO2与CH4的偶极矩均为零。
()9.共价键和氢键均有饱和性与方向性。
()10.在消除了系统误差之后,测定结果的精密度越高,准确度也越高。
()三、填空题 ( 共 25分 )1.命名[Cr(NH3)4Cl2]NO3为______________ ,中心离子为 ___________,配位原子为 ___________ ,配位数为___________,配体包括 ___________ 。
2.在含有AgCl(s)的饱和溶液中加入0.1 mol·L-1 的AgNO3 ,AgCl的溶解度将______________,这是由于______________________的结果。
3.NH3分子中N的杂化方式为 ___________杂化,空间构型为___________。
BCl3分子中B的杂化方式为 ______杂化,空间构型为___________。
4.原电池中,发生还原反应的电极为______极,发生氧化反应的电极为____极。
5.常用于标定HCl溶液的基准物质有 ___________ 、___________常用于标定NaOH溶液的基准物质有___________ 、 ___________ 。
6.24号元素的核外电子排布为________ 它位于元素周期表第________周期________族________区。
无机及分析化学分析化学概论考试卷模拟考试题.docx

《分析化学概论》考试时间:120分钟 考试总分:100分遵守考场纪律,维护知识尊严,杜绝违纪行为,确保考试结果公正。
1、定量分析工作要求测定结果的误差()。
( ) A.愈小愈好 B.等于零 C.没有要求 D.在允许误差范围内2、可减小分析测定的随机误差的方法是()。
( )A.提纯试剂B.进行空白实验C.进行回收实验D.增加平行测定的次数3、下列情况可产生系统误差的是()。
( ) A.试样未混匀 B.砝码未经校正 C.砝码读错 D.滴定管渗液滴4、下列各式中,有效数字位数正确的是()。
( )A.c (H+)=3.24×10-2(3位)B.pH=3.24(3位)C.0.420(4位)D.0.80g (3位)5、以未干燥的Na2CO3标定HCl ,则HCl 的浓度将()。
( )姓名:________________ 班级:________________ 学号:________________--------------------密----------------------------------封 ----------------------------------------------线-------------------------A.偏高B.偏低C.无影响D.不能确定6、以下试剂能作为基准物质的是()。
()A.100~110℃干燥的Na2CO3B.优级纯的KOHC.100~110℃干燥的K2Cr2O7 D.优级纯的Na2B4O7∙5H2O7、以风化的Na2B4O7∙nH2O标定HCl,则HCl的浓度将()。
()A.偏高B.偏低C.无影响D.不能确定8、下列不属于系统误差的是()。
()A.被称量的试样含有微量干扰物质B.蒸馏水含有微量杂质C.使用的容量瓶未经校正D.滴定管在使用前未排气泡9、下列有关置信区间的定义正确的是()。
()A.以真值为中心的某一区间包括测定结果的平均值的概率B.在一定置信度时,以测定值的平均值为中心的包括真值的范围C.真值落在某一可靠区间的概率D.在一定置信度时,以真值为中心的可靠范围10、下述有关平均值的置信区间的论述错误的是()()A.在一定的置信度和标准偏差时,测定次数越多,平均值的置信区间越小B.其他条件不变时,给定的置信度越高,平均值的置信区间越宽C.平均值的数值越大,置信区间越宽D.当置信度与测定次数一定时,一组测量值的精密度越高,平均值的置信区间越小11、滴定分析中,指示剂颜色突变时停止滴定,这一点称为()。
无机及分析化学模拟试卷及答案最后一套

无机及分析化学模拟试卷及答案最后一套一.、判断题(每小题1分共10分)1.系统误差是不可测的。
()2.σ键和π键在分子中均可单独存在。
()3.极性分子间仅存在取向力,非极性分子间只存在色散力。
()4.等价轨道处于全充满、全空、半充满状态时原子能量较低。
()5.渗透压相同的两种溶液用半透膜相距时,渗透压小的溶液将逼使渗透压大的溶液液面有所下降。
()6.醋酸溶液经吸收后其离解度减小,因而可使其h+浓度减小。
()7.bf3和nh3都具备平面三角形的空间结构。
()8.co2与ch4的偶极矩均为零。
()9.共价键和氢键均存有饱和状态性与方向性。
()10.在消解了系统误差之后,测量结果的精密度越高,准确度也越高。
()二、选择题(40分,每小题2分)1、物质的量浓度相同的以下叶唇柱溶液中,蒸气甩最低的就是()。
a.hac溶液b.cacl2溶液c.蔗糖溶液d.nacl溶液2、在500g水中含22.5g某非电解质的溶液,其凝固点为c0.465℃。
已知水的kf=1.86kkgmol-1,则溶质的摩尔质量为()。
a.172.4b.90c.180d.1353、10.下列各式中,有效数字位数正确的是()。
a.0.0978(4位)b.ph=3.24(3位)c.pka=1.80(2位)d.0.420(2位)-14、反应2no(g)+o2(g)=2no2(g),?rhm?=-144kjmol-1,?rsm?=-146jmol-1k。
反应达平衡时各物质的分压均为p?,则反应的温度为()。
a.780℃b.508℃c.713℃d.1053℃5、下列气相反应平衡不受压力影响的是()。
a.n2(g)+3h2(g)=2nh3(g)b.2no2(g)=n2o4(g)c.2co(g)+o2(g)=2co2(g)d.2no(g)=n2(g)+o2(g)6、下列几种条件变化中,一定能引起反应速率常数k值改变的是()。
a.反应温度发生改变b.反应容器体积发生改变c.反应压力发生改变d.反应物浓度发生改变7、对某一均为气相物质参加的吸热可逆化学反应,下列说法正确的是()。
无机及分析化学模拟试题
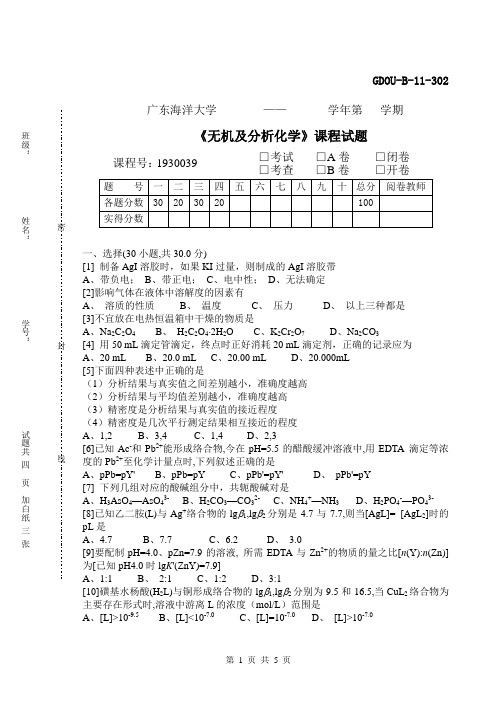
广东海洋大学 —— 学年第 学期 《无机及分析化学》课程试题 课程号: 1930039 □ 考试 □ A 卷 □ 闭卷 □ 考查 □ B 卷 □ 开卷一、选择(30小题,共30.0分) [1] 制备AgI 溶胶时,如果KI 过量,则制成的AgI 溶胶带 A 、带负电; B 、带正电; C 、电中性; D 、无法确定 [2]影响气体在液体中溶解度的因素有 A 、 溶质的性质 B 、 温度 C 、 压力 D 、 以上三种都是[3]不宜放在电热恒温箱中干燥的物质是 A 、Na 2C 2O 4 B 、 H 2C 2O 4⋅2H 2O C 、K 2Cr 2O 7 D 、Na 2CO 3 [4] 用50 mL 滴定管滴定,终点时正好消耗20 mL 滴定剂,正确的记录应为 A 、20 mL B 、20.0 mL C 、20.00 mL D 、20.000mL [5]下面四种表述中正确的是 (1)分析结果与真实值之间差别越小,准确度越高 (2)分析结果与平均值差别越小,准确度越高 (3)精密度是分析结果与真实值的接近程度 (4)精密度是几次平行测定结果相互接近的程度 A 、1,2 B 、3,4 C 、1,4 D 、2,3 [6]已知Ac -和Pb 2+能形成络合物,今在pH=5.5的醋酸缓冲溶液中,用EDTA 滴定等浓度的Pb 2+至化学计量点时,下列叙述正确的是 A 、pPb=pY' B 、pPb=pY C 、pPb'=pY' D 、 pPb'=pY [7] 下列几组对应的酸碱组分中,共轭酸碱对是 A 、H 3AsO 4—AsO 43- B 、H 2CO 3—CO 32- C 、NH 4+—NH 3 D 、H 2PO 4-—PO 43- [8]已知乙二胺(L)与Ag +络合物的lg β1,lg β2分别是4.7与7.7,则当[AgL]= [AgL 2]时的pL 是 A 、4.7 B 、7.7 C 、6.2 D 、 3.0 [9]要配制pH=4.0、pZn=7.9的溶液, 所需EDTA 与Zn 2+的物质的量之比[n (Y):n (Zn)]为[已知pH4.0时lg K '(ZnY)=7.9]A 、1:1B 、 2:1C 、1:2D 、3:1[10]磺基水杨酸(H 2L)与铜形成络合物的lg β1,lg β2分别为9.5和16.5,当CuL 2络合物为主要存在形式时,溶液中游离L 的浓度(mol/L )范围是A 、[L]>10-9.5B 、[L]<10-7.0C 、[L]=10-7.0D 、 [L]>10-7.0班级:姓名: 学号:试题共四页加白纸三张密封线GDOU-B-11-302[11]以下有关随机误差的论述正确的是A、正误差出现概率大于负误差B、负误差出现概率大于正误差C、正负误差出现的概率相等D、大小误差出现的概率相等[12]0.05 mol/L SnCl2溶液10 mL 与0.10 mol/L FeCl3溶液20 mL 相混合, 平衡时体系的电位是[已知此条件时ϕ' (Sn4+/Sn2+)= 0.14 V]ϕ' (Fe3+/Fe2+)= 0.68 V,A、0.14 VB、0.32 VC、0.50 VD、0.68 V[13]摩尔吸光系数(ε)的单位为A、mol/(L·cm)B、L/(mol·cm)C、mol/(g·cm)D、g/(mol·cm)[14]用分析天平称量试样时,在下列结果中不正确的表达是A、0.312gB、0.0963gC、0.2587gD、0.3010g[15]将浓度皆为0.1000mol/L的HAc和NaOH溶液等体积混合,该溶液的PH值为A、5.25B、7.00C、1.35D、8.72[16]浓度相同的下列物质水溶液的pH最高的是A、NaClB、NaHCO3C、NH4ClD、Na2CO3[17]AgNO3滴定NaCl时,若浓度均增加10倍,则突跃pAg增加A、1个单位B、2个单位C、10个单位D、不变化[18]用HCl标液测定硼砂(Na2B4O7·10H2O)试剂的纯度有时会出现含量超过100%的情况,其原因是A、试剂不纯B、试剂吸水C、试剂失水D、试剂不稳,吸收杂质[19]用铈量法测定铁时, 滴定至50% 时的电位是[已知ϕ' (Ce4+/Ce3+)= 1.44 V,ϕ' (Fe3+/Fe2+)= 0.68 V]A、0.68 VB、1.44 VC、1.06 VD、0.86 V[20]pH=1.00的HCl溶液和pH=13.00 的NaOH 溶液等体积混合,所得溶液的pH是-A、14B、12C、7D、6[21] 制备AgI溶胶时,如果AgNO3过量,则制成的AgI溶胶带A、带负电B、带正电C、电中性D、无法确定[22]Ba2+可沉淀为Ba(IO3)2或BaCrO4,然后借间接碘量法测定,今取一定量含Ba2+试液,采用BaCrO4形式沉淀测定,耗去0.05000 mol/L Na2S2O3标准溶液12.00 mL。
XX大学《无机及分析化学》期末考试复习题及参考答案(一)

称 取 褐 铁 矿 试 样 0.4017g , 溶 解 并 还 原 成 Fe2+, 用 0.02048mol⋅L−1 的 K2Cr2O7 溶 液 滴 定, 消 耗 26.45mL 。 计 算 褐 铁 矿 中 Fe2O3 的 百 含 量 。
10、(本小题 5 分)
= 0.005608g/mL ?
Fe(Ⅲ ) 配 位 物 的 常 数 如 下 :
( 1 ) Fe − 氟 配 合 物 K1 = 1.6×105 , K2 = 1.0×104 , K3 = 5.0×102 ;
( 2 ) Fe− 柠 檬 酸 配 合 物 K 不 稳 = 1.0×10−25 ;
A. 甲 基 橙;
B. 甲 基 红;
C. 酚 酞 ;
D. A.B.C 都 不 是
答( )
5、 对 于 酸 碱 指 示 剂, 全 面 而 正 确 的 说 法 是 : A. 指 示 剂 为 有 色 物 质;
B. 指 示 剂 为 弱 酸 或 弱 碱; C. 指 示 剂 为 弱 酸 或 弱 碱, 其 酸 式 或 碱 式 结 构 具 有 不 同 颜 色;
__________________________________________ 的 颜 色 , 终 点 时 的 颜 色 是 _____________________________ 的 颜 色。 5、(本小题 2 分)
EDTA 产 生 的 副 反 应 有 ____________________、___________________ 。 6、(本小题 2 分)
A. 进 行 对 照 试 验;
无机及分析化学考试题(附答案)

无机及分析化学期末考试试题答案附后石河子大学《无机及分析化学》考题试卷一一、选择题(1分×20=20分)1.土壤中NaCl 含量高时,植物难以生存,这与下列稀溶液性质有关的是( )。
A. 蒸气压下降B. 沸点升高C. 凝固点降低D. 渗透压2.0.10mol·L -1的下列溶液凝固点降低程度最大的是( )。
A. C 6H 12O 6(葡萄糖)B. KNO 3C. C 3H 5(OH)3(甘油)D. CuSO 43.下列反应的标准摩尔焓等于其产物的标准摩尔生成焓的反应是( )。
A. SO 2(g)+21O 2(g) SO 3(g) B. N 2(g)+O 2(g) 2NO(g) C. H 2(g)+21O 2(g) H 2O(g) D. CO(g)+21O 2(g) CO 2(g) 4.某反应的速率常数k 的单位为L·mol -1·s -1,则该化学反应的反应级数为( )。
A. 0B. 1C. 2D. 35.反应 A(g)+2B(g) E(S)+D(g) 达平衡时,下列表述正确的是( )。
A. K (正反应)+ K (逆反应)=1B. Δr G m (正反应)×Δr G m (逆反应)=1C. K (正反应)×K (逆反应)=1D. Δr G m (正反应)+Δr G m (逆反应)=16.下述四个量子数不合理的一组是( )。
A. 2,0,1,B. 3,1,0,-C. 4,2,1,D. 2,1,0,-7.下列分子都没有极性的一组是( )。
A. SO 2 NO 2 CO 2B. SO 3 BF 3 NH 3C. CH 4 BF 3 CO 2D. PCl 3 CCl 4 H 2O8.下列混合溶液中两种离子能够共存的是( )。
A. CO -23和Al 3+B. MnO -4和SO -23C. Fe 3+和Cu 2+D. Cr 2O -27和I -9.向pH=2的缓冲溶液中通入H2S(g)达饱和时(H2S浓度约为0.1mol·L-1),溶液中的c(S2-)(mol·L-1)为:{K a1 (H2S)=1.3×10-7,K a2 (H2S)=7.1×10-15}()。
无机及分析化学试卷(分析部分)[1]
![无机及分析化学试卷(分析部分)[1]](https://img.taocdn.com/s3/m/fa1593a8d1f34693daef3ef8.png)
无机及分析化学试卷(分析部分)试卷号:3一.单项选择题(按题中给出的字母A、B、C、D,您认为哪一个是正确的,请写在指定的位置内)1、对某试样平行测定,得到结果如下: 43.28%, 43.19% , 43.62% , 43.24 % 。
在置信度为90% 的情况下,四次测定的Q 检验值是0.76。
问这些结果的最佳平均值是:A. 43.24 ;B. 43.33;C. 43.19;D. 43.28答()2、滴定分析中,一般利用指示剂颜色的突变来判断化学计量点的到达,在指示剂变色时停止滴定。
这一点称为:A. 化学计量点;B. 滴定分析;C. 滴定;D. 滴定终点答()3、根据定义,酸是质子给予体,在NH3+H2O→NH4+ + OH-反应中酸是:A. NH3 ;B. H+ ;C. NH4+ ;D. H2O答()4、对于酸碱指示剂,全面而正确的说法是:A. 指示剂为有色物质;B. 指示剂为弱酸或弱碱;C. 指示剂为弱酸或弱碱,其酸式或碱式结构具有不同颜色;D. 指示剂在酸碱溶液中呈现不同颜色答()5、强碱滴定弱酸(K a =1.0⨯10-5)宜选用的指示剂为:A. 甲基橙;B. 酚酞;C. 甲基红;D. 络黑T答()6、溶液中含有等浓度的M ,N 离子。
欲用EDTA 选择滴定M 而N 不干扰,需要控制一定酸度,在此酸度下,下面错误关系式是:A. K MY>105K NY ;B. K'MY<105K'NY;C. K'MY>102K'MIn ;D. MIn 与In 应具有不同的颜色答()7、用EDTA 测定Ca2+时,Al3+将产生干扰。
为消除Al3+的干扰,加入的掩蔽剂是:A. NH4F ;B. KCN ;C. 三乙醇胺;D. 铜试剂答()8、在下列的叙述中,正确的是:A. Al3+与EDTA 反应很慢,故不能用EDTA 法测定其含量;B. Cr3+能使指示剂封闭或僵化,故不能用EDTA 法测定含量;C. 通过改变配位滴定的方式,可以测定Al3+和Cr3+的含量;D. Al3+只能用重量分析法测定其含量答()9、在氨性缓冲溶液中,用EDTA 标准溶液滴定Zn2+。
无机及分析化学试卷及答案1

一单选题1. 下列溶液中,pH最大的是(B )。
(2 分)A. 0.10mol·L-1 NH4NO3B. 0.10mol·L-1 Na3PO4C. 0.10 mol·L-1 NH4AcD. 0.10 mol·L-1 NaCl2. 一定温度下,反应N2(g) + 3H2(g) 2NH3(g)达平衡后,增大N2的分压,平衡移动的结果是(C)。
(2 分)A. 增大H2的分压B. 减小N2的分压C. 增大NH3的分压D. 减小平衡常数3. 某酸碱指示剂的p K HIn =5,其理论变色范围的pH为(C)。
(2 分)A. 2~8B. 3~7C. 4~6D. 5~74. 对可逆反应 2NO(g) N2(g)+O2(g)+ Q ,下列几种说法中正确的是(A)。
(2 分)A. Kθ与温度有关B. 增加NO的浓度,Kθ值增大C. 温度升高时,平衡右移D. 使用催化剂,Kθ值增大5. 在0.1 mol·L-1NaF 溶液中,下列关系正确的为(B)。
(2 分)A. [H+]≈[HF]B. [HF]≈[OH]C. [H]≈[OH]D. [OH]≈[HF]6. 下列论述中,正确的是(B)。
(2 分)A. 精密度高,准确度一定好B. 准确度好,一定要有高的精密度C. 精密度高,系统误差一定小D. 测量时,过失误差不可避免7. 下列物质可用直接法配制其标准溶液的有(D)。
(2 分)A. H2SO4B. KOHC. Na2S2O3D. 邻苯二甲酸氢钾8. 质子理论认为,下列物质中可以作为质子酸的是(B)。
(2 分)A. H 2S ,C 2O 42-,HCO 3B. H 2CO 3,NH 4+,H 2OC. Cl -,BF 3,OHD. H 2S ,CO 32-,H 2O二 判断题 (正确的填涂“A ”,错误的填涂“B ”。
)9. 误差是指测定值与真实值之间的差,误差的大小说明分析结果精密度的高低。
中国矿业大学《无机及分析化学》模拟试题

《无机及分析化学》模拟试题(1)【闭卷】本试题一共三道大题,满分100分。
考试时间120分钟。
注:1.答题前,请准确、清楚地填各项,涂改及模糊不清者、试卷作废。
2.试卷若有雷同以零分计。
一、选择题(每题2分,共50分)1. 含有Cl -和Br -的混合溶液,欲使Br -氧化为Br 2而不使Cl -氧化,应选择 ( ) (θ/Sn Sn 24++ϕ =0.15 V ,θ/Cl Cl 2-ϕ=1.3583 V ,θ/Br Br 2-ϕ=1.087 V ,θ/Cr O Cr 3272+-ϕ=1.33 V ,θ/Mn MnO 24+-ϕ=1.51 V , θ/Fe Fe 23++ϕ=0.771 V )A. SnCl 4B. K 2Cr 2O 7C. KMnO 4D. Fe 3+2. 已知下列反应的平衡常数PbSO 4(S)Pb 2++SO 42- K sp Θ(1) PbS (S)2++S 2- K sp Θ(2) 反应PbSO 4+S PbS+SO 4- 的K 为 ( ) A. K SPΘ(1) . K sp Θ(2) B. K sp Θ(1) /K sp Θ(2) C. K sp Θ(2) /K sp Θ(1) D. ( K sp Θ(1) /K sp Θ(2) )23. 0.04mol·L -1的H 2CO 3的水溶液, K 1Θ﹑K 2Θ分别为它的电离常数,该溶液的c (H +)浓度和c (CO 32-)的浓度分别为 ( ) A. 04.0θ1⨯K , K 1Θ B. 04.0θ1⨯K ,04.0θ2⨯K C. 04.0θ2θ1⨯⨯K K , K 2Θ D. 04.0θ1⨯K , K 2Θ4. 已知某一元弱酸的浓度为c ,用等体积的水稀释后,溶液的c (H +)浓度为 ( )A. 2c B. c K a 2θ C. c K a ⨯θ21 D. 2c K a ⨯θ 5. θ/Cr O Cr 3272+-ϕ的数值随pH 的升高而 ( )A. 增大B. 不变C. 减少D. 无法判断6. 用AgNO 3处理[Fe(H 2O)5Cl]Br 溶液,产生的沉淀主要是 ( )A. AgBrB. AgClC. AgBr 和AgClD. Fe(OH)37. 已知K f Θ[Ag(NH 3)2+]<K f Θ[Ag(CN)2-]下列情况中能溶解AgCl 最多的是 ( ) A. 1L 水 B. 1L3.0 mol·L -1NH 3·H 2OC. 1L3.0 mol·L -1KCND. 1L3.0 mol·L -1 HCl8. 10ml2.0×10-4 mol·L -1Na 2SO 4溶液中加入10ml2.0×10-4 mol·L -1的BaCl 2溶液 后,溶液中SO 42-离子的浓度为[K sp Θ(BaSO 4)=1.0×10-10] 青 ( ) A. >10-5 mol·L -1 B. <10-5 mol·L -1C. =10-5 mol·L -1D. =10-4 mol·L -19. Pb 2+离子的价电子层结构是 ( )A. 6s 26p 2B. 5s 25p 2C. 6s 2D.5s 25p 65d 106s 210. 在一个多电子原子中,具有下列各套量子数(n,l,m,m s )的电子,能量最大的电子具有的量子数是 ( )A. 3,2,+1,+1/2B. 2,1,+1,-1/2C. 3,1,0,-1/2D. 3,1,-1,+1/211. 密闭容器中,A ﹑B ﹑C 三种气体建立化学平衡,它们的反应是C, 在相同温度如果体积缩小2/3,则平衡常数K p 为原来的 ( )A. 3倍B. 9倍C. 2倍D. 不变12. 对于一个化学反应来说,下列哪一种是正确的? ( )A. △r G m 越负,反应速率越快B. △r H m 越负,反应速率越快C. 活化能越大, 反应速率越快D. 活化能越小, 反应速率越快13. 已知FeO (S) + C (S) = CO (q) + Fe (S) 反应的θm r H ∆为正, θm r S ∆为正,下列说法正确的是 ( )A. 低温下自发过程,高温下非自发过程B. 任何温度下均为非自发过程C. 高温下自发过程,底温下非自发过程D. 任何温度下均为自发过程14. K w Θ的值是6.4×10-15 (18 o C),1.00×10-14 (25 oC), 由此可推断出 ( ) A. 水的电离是吸热的 B. 水的pH25 o C 时大于15 oC 时 C. 18 o C 时, c (OH -)=1.0×10-7 D. 仅在25 oC 时水才为中性 15. 用配位(络合)滴定法测定石灰石中CaO 的含量,经四次平行测定,得x =27.50%,若真实含量为27.30%,则27.50%-27.30%=+0.20%,称为 ( )A. 绝对偏差B. 相对偏差C. 绝对误差D. 相对误差16. 用计算器算得 004471.122000.0036.11124.1236.2=⨯⨯ ,按有效数字运算(修约)规则,结果应为 ( )A. 12B. 12.0C. 12.00D. 12.00417. 测定CaCO 3的含量时,加入一定量过量的HCl 标准溶液与其完全反应,过量部分HCl 用NaOH 溶液滴定,此滴定方式属 ( )A. 直接滴定方式B. 返滴定方式C. 置换滴定方式D. 间接滴定方式18. 已知p K b Θ(NH 3)=4.75用0.10mol·L -1NaOH 溶液滴定0.10 mol·L -1HCl+0.05 mol·L -1NH 4Cl 混合溶液,合适的指示剂是 ( ) A. 甲基橙(p K a Θ=3.4) B. 溴甲酚兰(p K a Θ=4.1)C. 甲基红(p K a Θ=5.0)D. 酚酞(p K a Θ=9.1)19. 下列反应中滴定曲线对称的反应是 ( )A. Ce 4++Fe 2+=Ce 3++Fe 3+B. 2Fe 3++Sn 2+=2Fe 2++Sn 4+C. I 2+2S 2O 32-=2I -+S 4O 62-D. MnO 4-+5Fe 2++8H +=Mn 2++5Fe 3++4H 2O20. 在滴定分析测定中,将导致系统误差的是 ( )A. 试样未经充分混匀B. 滴定时有液滴溅出C. 砝码未经校正D. 沉淀穿过滤纸21. 欲配制0.2 mol·L -1HCl 溶液和0.2 mol·L -1H 2SO 4溶液,量取浓酸的合适的量器是 ( )A. 容量瓶B. 吸量管C. 量筒D. 酸式滴定管22.间接碘量法中加入淀粉指示剂的适宜时间是( )A. 滴定开始时B. 标准溶液滴定了近50%时C. 标准溶液滴定了近75%D. 滴定接近计量点时23. 标定HCl和NaOH溶液常用的基准物是()A. 硼砂和EDTAB. 草酸和K2Cr2O7C. CaCO3和草酸D. 硼砂和邻苯二甲酸氢钾24.用K2Cr2O7法测Fe2+,加入H3PO4的主要目的是( )A. 提高酸度,B. 同Fe3+形成稳定的无色化合物,减少黄色对终点的干扰ϕ的数值,增大突跃范围C. 减小++23/FeFeD. 防止Fe2+的水解25. 在EDTA配合滴定中,只考虑酸度影响,下列叙述正确的是( )A. 酸效应系数越大,配合物的稳定性越大B. 酸效应系数越小,配合物的稳定性越大C. pH越大,酸效应系数越大D. 酸效应系数越大,滴定突跃范围越大二、判断题(每题1分,共20分)1. 配合物中心离子的配位数就是该配合物的配位体的个数。
无机及分析化学试题.doc

无机及分析化学试题(1)系别:专业班级:姓名:学号:一、填空题(30分,每空2分)1、写出具有下列原子序数的原子的核外电子排布式:(1)11(2)172、0.2mol·L1HAc 溶液中H+的浓度等于________。
[Ka=1.8×10-5]3、CH分子中心原子发生杂化,空间构型4是。
4、滴定分析中,根据反应类型的不同,可分为_____________、___________、____________和___________等。
5、水分子之间存在着质子的传递作用,称为水的_____________作用,这种作用的平衡常数在25℃时等于______________。
6、沉淀物按物理性质的不同分为__________沉淀和__________沉淀。
7、朗伯—比耳定律:A=abc,其中符号c代表________,b代表_______,a 代表_______。
二、完成下列方程式(5分,每小题1分)1. MnO4- + Fe2++ H+—2. Cl2+ NaOH —3. S2O32- + H+—4. Hg2Cl2+ NH3—5. Pb2+ + Cr2O72- + H2O —三、选择题(20分,每正确选择2分)1、不用查表,指出下列反应焓变为正值的是┄┄┄()。
A.CaCO3(s)→CaO(s) + CO2(g)B. CaO(s) +H2O→Ca(OH)2(s)C.2Mg(s) + O2(g)→2MgO(s)D.O2(g)+ 2H2(g)→2H2O(l)2、下列哪一种物质既有离子键又有共价键┄┄┄┄┄()。
A. H2O B. NaOH C. HCl D.SiO23、在分光光度法中,宜选用的吸光度读数范围为┄()。
A.0~0.2B.0.1~0.3C.0.3~1.0D.0.2~0.8 4、下列关于价键理论对配合物的说法正确的是┄┄┄()。
A.任何中心离子与任何配体都可形成外轨型化合物;B.任何中心离子与任何配体都可形成内轨型化合物;C.中心离子用于形成配位键的原子轨道是经过杂化的等价轨道;D.以sp3d2和d2sp3杂化轨道成键的配合物具有不同的空间构型。
无机及分析化学考试题1

无机及分析化学试题及答案本科课程考试试卷2005-2006学年第一学期《无机及分析化学》课程考试试卷一、选择题(每题1.5分,共30分)1. 1. 下面几种溶液下面几种溶液下面几种溶液: : : ①① 0.1 mol·L -1 Al 2(SO 4)3 ;②;② 0.2mol·L -1CuSO 4;③0.3mol·L -1 NaCl NaCl;④;④;④ 0.3mol·0.3mol·L L -1 CO(NH 2)2(尿素);按溶液的凝固点由高到低排列,顺序正确的是(列,顺序正确的是( ))A A. ①②③④. ①②③④. ①②③④B B B. ①③②④. ①③②④. ①③②④C C C.. ④②①③ ④②①③ D. D. D. ④②③①④②③①④②③①2. 2. 对对Fe(OH)3正溶胶和As 2S 3负溶胶的凝聚能力大的是(负溶胶的凝聚能力大的是( )A . Na 3PO 4和AlCl 3B B..NaCl 和BaCl 2C C.. Na 3PO 4和MgCl 2D D..NaCl 和Na 2SO 43. 3. 溶胶发生电泳时,向某一方向定向移动的是(溶胶发生电泳时,向某一方向定向移动的是(溶胶发生电泳时,向某一方向定向移动的是( ))A A.胶核.胶核.胶核B B B.吸附层.吸附层.吸附层C C C.胶团.胶团.胶团D D D.胶粒.胶粒.胶粒4. 4. 在在298K 时,下列反应的r m H Q D 等于AgBr(s) f m H QD 的为(的为( ))A .Ag +(aq) + Br - (aq) = AgBr (s)B B..2Ag (s) + Br 2(l) = 2AgBr (s)C .Ag (s) + + ½½ Br 2(g) = AgBr(s)D = AgBr(s) D..Ag (s) + + ½½ Br 2(l) = AgBr (s) 5. 恒压条件下,某反应恒压条件下,某反应 A(s) + B(g) = 2C(g)为放热反应,则反应的(为放热反应,则反应的( )A .△U >0 W >0 B .△U <0 W <0 C .△U >0 W <0 D .△U <0 W >06. 当反应A 2 + B 2 = 2AB的速率方程为22(A )(B )v kc c =时,则此反应(时,则此反应( ) A. 一定是基元反应一定是基元反应 B. 一定是非基元反应一定是非基元反应 C. 不能肯定是否是基元反应不能肯定是否是基元反应 D. 反应为一级反应反应为一级反应7.7.下列四个量子数中,不能描述电子运动状态的是(下列四个量子数中,不能描述电子运动状态的是(下列四个量子数中,不能描述电子运动状态的是( ))A A..3, 1, 1, -1/2 B. 2, 1, 1, +1/2C. 3, 3, 0, -1/2D. 4, 3, -3, -1/2 C. 3, 3, 0, -1/2 D. 4, 3, -3, -1/28. 8. 氮原子的氮原子的2p 态电子分布为:态电子分布为:2p 2p x 12p y 12p z 1,决定这样排布的规则是(,决定这样排布的规则是( ))A. A. 鲍利不相容原理鲍利不相容原理鲍利不相容原理B. B. B.洪特规则洪特规则洪特规则C. C. C.能量最低原理能量最低原理能量最低原理D. D. D.屏蔽效应屏蔽效应屏蔽效应9.9.测得某反应正反应的活化能测得某反应正反应的活化能E a(+)=70 kJ.mol -1,逆反应的活化能E a(-)= 20kJ.mol -1,此反应的反应热为(,此反应的反应热为( ))A. 50kJ.mol -1B. -50kJ.mol -1C. 90kJ.mol -1D. -45kJ.mol-1 1010.下列说法正确的是(.下列说法正确的是(.下列说法正确的是( ))A. BCl 3分子中B —Cl 键是非极性的键是非极性的B. BCl 3分子中B —Cl 键的键矩为零键的键矩为零C. BCl 3分子是极性,而B —Cl 键是非极性的键是非极性的D. BCl 3分子是非极性,而B —Cl 键是极性的键是极性的11.11.符合朗伯符合朗伯符合朗伯--比尔定律的某一有色溶液,浓度为c 时透光度为0T ,当浓度为2c 时(时( ))A .012lg A T =B B..02lg A T =C C..0lg 2A T =D D..0lg 2T A = 12.12.用硼砂标定用硼砂标定HCl HCl,某同学在溶解硼砂时,用玻璃棒去搅拌锥形瓶中溶液后,,某同学在溶解硼砂时,用玻璃棒去搅拌锥形瓶中溶液后,不经处理拿出瓶外,标定结果会(不经处理拿出瓶外,标定结果会( ))A .偏高.偏高B B B.偏低.偏低.偏低C C C.无影响.无影响.无影响D D D.不一定.不一定.不一定13.13.要求滴定管的读数误差不超过±要求滴定管的读数误差不超过±要求滴定管的读数误差不超过±0.1%0.1%0.1%,则滴定剂的体积(终读数和初读数,则滴定剂的体积(终读数和初读数两次之差)至少应为(两次之差)至少应为( ))A .5.00 mLB B..10.00 mLC C..15.00 mLD D..20.00 mL14.14.在影响反应速度的因素中,在影响反应速度的因素中,即改变反应速度常数即改变反应速度常数,,又有效地改变活化能的因素是(素是( ))A .反应温度.反应温度B B B.反应物浓度.反应物浓度.反应物浓度C C C.体系的总压力.体系的总压力.体系的总压力D D D.加入催化剂.加入催化剂.加入催化剂15.15.已知已知12sp 24(Ag CrO ) 1.110K -=´,在1.1 mol mol··L -1Ag + 溶液中,若产生Ag 2CrO 4沉淀,2-4CrO 浓度应至少大于(浓度应至少大于()) A .1.11.1××10-11 mol mol··L -1 B B..6.56.5××10-5 mol mol··L -1C .0.10 mol 0.10 mol··L -1D D..1.11.1××10-10 mol mol··L -116.16.已知某原电池的电池反应为:已知某原电池的电池反应为:2+2+Zn(s)+Cu (aq)Zn (aq)+Cu(s)®,如果要提,如果要提高该原电池的电动势,可增加(高该原电池的电动势,可增加( ))A .Zn 2+ 的浓度的浓度B B B..Cu 2+的浓度的浓度 C C C..Zn(s)Zn(s)的尺寸的尺寸的尺寸 D D D..Cu(s) Cu(s) 的尺寸的尺寸的尺寸1717.分析测试的标准偏差愈大,表明下列哪一值愈低(.分析测试的标准偏差愈大,表明下列哪一值愈低( ))A .准确度.准确度B B B.精密度.精密度.精密度C C C.绝对误差.绝对误差.绝对误差D D D.平均值.平均值.平均值18. 19号元素K 的基态原子最外层电子的四个量子数为( ))A .4,0,0,+1/2B 4,0,0,+1/2 B..3,0,0,+1/2C 3,0,0,+1/2 C..4,1,1,+1/2D 4,1,1,+1/2 D..4,1,0,+1/219. 19. 若要使吸光度降低为原来的一半,最方便的做法是(若要使吸光度降低为原来的一半,最方便的做法是( ))A .将待测液稀释一倍.将待测液稀释一倍B B B.选用新的测定波长.选用新的测定波长.选用新的测定波长C .选用原厚度1/2的比色皿的比色皿D D D.更换显色剂.更换显色剂.更换显色剂20.20.在酸碱滴定中,选择指示剂可不必考虑的因素为(在酸碱滴定中,选择指示剂可不必考虑的因素为( ))A .pH 突跃范围突跃范围B B B.指示剂的变色范围.指示剂的变色范围.指示剂的变色范围C .指示剂的颜色变化.指示剂的颜色变化D D D.指示剂的分子结构.指示剂的分子结构.指示剂的分子结构二、 填空题(每空1分,共30分)1. 1. 等体积混合等体积混合0.008mol 0.008mol·· L -1 CaCl 2和 0.010mol 0.010mol··L -1 (NH 4)2C 2O 4溶液,制得CaC 2O 4溶胶,其溶胶胶团结构式为溶胶,其溶胶胶团结构式为 。
无机及分析化学考试题及参考答案

无机及分析化学考试题及参考答案一、选择题1. 下列哪个元素具有最高的电负性?a) 碳b) 氮c) 氧d) 硫2. 氯化钠是由正离子和负离子组成的化合物,其晶体结构属于下列哪种类型?a) 离子晶体b) 共价晶体c) 金属晶体d) 非晶体3. 下列哪种化合物在水中能够电离产生氢氧根离子(OH-)?a) 硝酸铵b) 硫酸铵c) 氯化钠d) 氢氧化铵4. 下列哪个元素具有最大的原子半径?a) 锂b) 钠c) 铷d) 钾5. 气体状态下的金属铝具有什么形式的结构?a) 单原子结构b) 双原子结构c) 多原子结构d) 多面体结构二、填空题1. 银的原子序数为47,电子结构为2,8,18,19,1。
请写出银的化学符号。
2. 铜的相对原子质量为63.55,其一个原子的质量为____________。
3. 锌离子的化学式为Zn2+,请写出其原子核中的质子数和中子数。
4. 硝酸是一种强酸,其化学式为____________。
5. 溴氯乙烷(C2H4BrCl)的结构式中,碳原子与溴原子之间的连线应_________。
1. 请解释下列术语的含义并举例说明:a) 酸性溶液b) 碱性溶液c) 中性溶液2. 简要描述下列实验的操作步骤以及结果:添加氯化银溶液于盐酸溶液中观察现象。
3. 请说明以下气体之间的关系:氧气(O2),一氧化氮(NO),二氧化氮(NO2),三氧化二氮(N2O3)。
四、计算题1. NaCl 在水中的溶解度为36g/100mL。
如果加入45g NaCl 到200mL 的水中,请计算是否形成饱和溶液。
2. 从化合物的摩尔质量(g/mol)计算化合物的质量百分比:C2H5OH (乙醇)3. 一段高炉内,熔化的铁经过冷却形成固态铁。
在这个过程中,铁发生了化学变化还是物理变化?请说明原因。
参考答案:1. c) 氧2. a) 离子晶体3. d) 氢氧化铵4. d) 钾5. b) 双原子结构二、填空题1. Ag2. 63.553. 质子数为30,中子数为354. HNO35. 直线三、简答题1.a) 酸性溶液:指溶液中氢离子(H+)浓度较高的溶液。
无机及分析化学试卷及答案1.讲课稿

无机及分析化学试卷1一、判断题:(每题1分,共10分。
正确 √;错误 ×)1. 具有sp 3等性杂化轨道类型的分子空间构型是平面三角型。
( )2. 一个化学反应不管是一步完成还是分几步完成,其热效应都相同。
( )3. 与纯溶剂相比,溶液的蒸气压一定降低。
( )4. 分析测定的精密度高,则准确度必然高。
( )5. 电子的波动性是电子运动时呈波浪式的前进。
( )6. 标定NaOH 溶液常用的基准物有邻苯二甲酸氢钾。
( )7. 酸碱滴定中选择指示剂的原则是指示剂的变色点与化学计量点完全符合。
( )8. 以铁铵矾为指示剂,用NH 4SCN 标准溶液滴定Ag +时,应在弱碱性条件下进行。
( )9. 在EDTA 配合滴定中酸效应系数愈小,配合物的稳定性愈大。
( )10. 有色溶液显现的颜色是透射光的颜色。
( )二、选择题:(每题1分,共20分)1. 稀溶液依数性中起决定性的性质是( )A. 溶液的蒸气压下降B. 溶液的沸点升高C. 溶液的凝固点降低D. 溶液具有渗透压2. 单位质量摩尔浓度的溶液是指1mol 溶质溶于( )A. 1 dm 3溶液B. 1000 g 溶液C. 1 dm 3溶剂D. 1000 g 溶剂3. 反应 A + B C ,焓变小于零,若温度升高10摄氏度,其结果是( )A. 对反应没有影响B. 使平衡常数增大一倍C. 不改变反应速率D. 使平衡常数减小4. 分几步完成的化学反应的总平衡常数是?( )A. 各步平衡常数之和B. 各步平衡常数之平均值C. 各步平衡常数之差D. 各步平衡常数之积5. 可以减少分析测试中随机误差的措施是( )A. 增加平行测定次数B. 进行方法校正C. 进行空白试验D. 进行仪器校正6. 当反应A 2 + B 2 → 2AB 的速率方程为 υ = k(A 2)(B 2)时,可以得出结论:此反应( )A. 一定是基元反应B. 一定是非基元反应C. 无法肯定是否为基元反应D. 对A 来说是基元反应7. 基态原子的第五层只有2个电子,则原子的第四电子层中的电子数( )A. 肯定为8个B. 肯定为18个C. 肯定为8~32个D. 肯定为8~18个8. 某元素原子基态的电子构型为[Ar] 3d84s2 ,它在元素周期表中的位置是()A. d区B. f区C. p区D. s区9. 对于原子的s轨道,下列说法中正确的是()A. 距原子核最近B. 球形对称C. 必有成对电子D. 具有方向性10. 已知某难溶盐AB2的溶解度为S(单位为mol·L-1),其溶度积为()A. S3B. S2C. 4S3D. S3/411. 过量AgCl溶解在下列各物质中,问哪种溶液中Ag+浓度最小()A. 100 cm3水B. 1000 cm3水C. 1000 cm3 0.5 mol·dm-3KNO3溶液D. 100 cm3 0.2 mol·dm-3KCl溶液12. 在0.10 dm3 0.10 mol·dm-3 HAc溶液中,加入0.10 mol NaCl晶体,溶液的pH将会()A. 升高B. 降低C. 不变D. 无法判断13. 两个半电池,电极相同,电解质溶液中的物质也相同,都可以进行电极反应,但溶液的浓度不同,它们组成电池的电动势()A. E= 0,E≠0B. E≠0,E≠0C. E≠0,E = 0D. E= 0,E = 014. 用Nernst方程式计算Br2/Br−电对的电极电势,下列叙述中正确的是()A. Br2的浓度增大,E增大B. Br−的浓度增大,E减小C. H+的浓度增大,E减小D. 温度升高对E无影响15. 下列分子中相邻共价键的夹角最小的是()A. BF3B. CCl4C. NH3D. H2O16. Al3+与EDTA形成()A. 非计量化合物B. 夹心化合物C. 鳌合物D. 聚合物17. 下列几种物质中最稳定的是()A. [Co(en)3]Cl3B. [Co(NH3)6] (NO3)3C. [Co(NH3)6]Cl2D. Co(NO3)318. 下列配离子在强酸中能稳定存在的是()A. [Fe(C2O4)]3-B. [AlF6]3-C. [Mn(NH3)6]2+D. [AgCl2]-19. 有色配位化合物的摩尔吸光系数与下列哪种因素有关?()A. 有色配位化合物的浓度B. 入射光的波长C. 配位化合物的稳定性D. 比色皿厚度20. 重量分析中的沉淀形式应当符合()A. 溶解度小B. 沉淀纯净含杂质少C. 相对分子量尽量大D. A、B和C三、填空题:(每空1分,共20分)1. 已知标准电极电势E(Cu2+/ Cu+)=0.153V, E(Cu+/ Cu)=0.521V,则E(Cu2/ Cu)= ,能发生歧化反应的物质是。
《无机及分析化学》前十一章模拟题(1)

《无机及分析化学》前十一章模拟题(1)姓名 专业 班级 得分一、单项选择:1.有一含N 2,CO 2和O 2的混合气体,其中N 2体积分数为20%、分压为20.26kPa ,混合气体的总压为 ( )A .101.3 kPaB .10.13 kPaC .30.39 kPaD .50.65 kPa2. 下列水溶液中凝固点最低的是 ( )A .0.1mol ·dm -3 C 12H 22O 11B .0.1 mol ·dm -3 HACC .0.1 mol ·dm -3 NaClD .0.1 mol ·dm -3 CaCl 23.下列说法正确的是 ( )A .溶胶可稳定存在一段时间,因此是热力学稳定体系B .从外观看,真溶液与溶胶无什么区别,因此溶胶是单相体系C .溶胶和高分子溶液同属于胶体分散系,因此两者具有完全相同的性质。
D .溶胶是高度分散的多相体系,是热力学不稳定体系4.在水解法制备的Fe(OH)3溶胶中,电位离子为 ( )A .Fe 3+B .Fe(OH)2+C .FeO +D .Fe(OH)2+5.已知2NO(g)+O 2(g)=2NO 2(g) kJ ·mol 4.114)298(−=∆K H m r θ-12.33)298,,(2=∆K g NO H m f θ kJ ·mol -1,则kJ ·mol /)298,,(k g NO H m f θ∆-1为A .90.4 B .147.6 C .-90.4 D .-147.6 ( )6.下列各反应中,哪个反应的和的数值最接近 ( )θm r H ∆ϑm r G ∆A .CCl 4(g)+2H 2O(g)=CO 2(g)+4HCl(g)B .CaO(s)+CO 2(g)=CaCO 3(s)C .Cu 2+(aq)+Zn(s)=Cu(S)+Zn 2+(aq)D .Na(s)+H +(aq)+H 2O(p)=Na +(aq)+H 2(g)+OH -(aq)7.在290K 时,将反应物A 放入密闭容器中发生下列反应:A(s)==B(g)+C(g)达到平衡时气体混合物的总压为2.68×104Pa,则K θ为 ( ) A .179.56 B .1.75×10-2 C .1.34 D .2.688. 25℃,对于电极反应O 2 + 4H + + 4e - = 2H 2O 来说,当p(O2)=100kPa 时,酸度与电极电势的关系是: ( )A.φ=φ°+0.059pHB.φ=φ°-0.059pHC. φ=φ°+0.0148pHD.φ=φ°-0.0148pH9.某反应的速率方程为r=kC ,则指前因子A 的单位为 ( )2A A .kJ ·mol -1 B .S -1 C .mol ·dm -3·S -1 D .dm 3·mol -1·S -110.向一反应体系中加入催化剂,正反应的活化能降低了ΔEa ,逆反应的活化能降低了ΔE a ˊ,则 ( )A .ΔEa=ΔE a ˊB .ΔEa >ΔE a ˊC .ΔEa <ΔE a ˊD .无法判断其大小11.在含有0.1mol ·dm -3 HCl 的0.1mol ·dm -3HAC 溶液中,哪一种表示是正确的( )A .C e(H +)=C e(Ac -)B .C e(Ac -) > C e(H +) C .C e(H +)>>C e(Ac -)D .以上都不正确12.下列溶液中不能组成缓冲溶液的是 ( )A .NH 3·H 2O 和NH 4ClB .H 2PO 和HPO−4−24C .NH 3·H 2O 和过量HCl D .HCl 和过量NH 3·H 2O13.Li 原子最外层上一个电子2S 1(顺时针自旋),其运动状态可描述为 ( )A .n=2, l=2, m L =1, m s =+1/2B .n=2, l=0, m L =0, m s =0C .n=2, l=0, m L =0, m s =+1/2D .n=2, l=1, m L =0, m s = -1/214.多电子原子中,n 、l 、m L 、m s 分别为下列数值,由其描述的电子能量最高的是( )A .(2,1,0,-21)B .(2,1,1,-21)C .(3,1,0,21)D .(3,2,0, 21) 16.已知BCl 3分子中硼以sp 2杂化轨道成键,则该分子的空间构型是 ( )A .三角锥形B .锯齿形C .正三角形D .直线形17.已知φθ(Fe 3+/Fe 2+)=0.77V , φθ(Sn 4+/Sn 2+)=0.15V , φθ(I 2/I -)=0.535V , φθ(Hg 2+/Hg )=0.851V , φθ(Br 2/B )=1.065V, φ−r θ(Fe 2+/Fe )=-0.402V ,问在Fe 2+,Sn 2+离子共存的溶液中,加入哪种物质,才能使Sn 2+变为Sn 4+,而Fe 2+不反应。
无机及分析化学考试题一(含答案)

《无机及分析化学》考题试卷一一、选择题(1分×20=20分)1.土壤中NaCl 含量高时,植物难以生存,这与下列稀溶液性质有关的是( )。
A. 蒸气压下降B. 沸点升高C. 凝固点降低D. 渗透压2.0.10mol·L -1的下列溶液凝固点降低程度最大的是( )。
A. C 6H 12O 6(葡萄糖)B. KNO 3C. C 3H 5(OH)3(甘油)D. CuSO 43.下列反应的标准摩尔焓等于其产物的标准摩尔生成焓的反应是( )。
A. SO 2(g)+21O 2(g) SO 3(g)B. N 2(g)+O 2(g) 2NO(g)C. H 2(g)+21O 2(g) H 2O(g)D. CO(g)+21O 2(g) CO 2(g)4.某反应的速率常数k 的单位为L·mol -1·s -1,则该化学反应的反应级数为( )。
A. 0B. 1C. 2D. 35.反应 A(g)+2B(g) E(S)+D(g) 达平衡时,下列表述正确的是( )。
A. K (正反应)+ K (逆反应)=1B. Δr G m (正反应)×Δr G m (逆反应)=1C. K (正反应)×K (逆反应)=1D. Δr G m (正反应)+Δr G m (逆反应)=16.下述四个量子数不合理的一组是( )。
A. 2,0,1,B. 3,1,0,-C. 4,2,1,D. 2,1,0,-7.下列分子都没有极性的一组是( )。
A. SO 2 NO 2 CO 2B. SO 3 BF 3 NH 3C. CH 4 BF 3 CO 2D. PCl 3 CCl 4 H 2O8.下列混合溶液中两种离子能够共存的是( )。
A. CO -23和Al 3+B. MnO -4和SO -23C. Fe 3+和Cu 2+D. Cr 2O -27和I -9.向pH=2的缓冲溶液中通入H 2S(g)达饱和时(H 2S 浓度约为0.1mol·L -1),溶液中的c (S 2-)(mol·L -1)为:{K a1 (H 2S)=1.3×10-7,K a2 (H 2S)=7.1×10-15}( )。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1《无机及分析化学》模拟试题(1)【闭卷】本试题一共三道大题,满分100分。
考试时间120分钟。
注:1.答题前,请准确、清楚地填各项,涂改及模糊不清者、试卷作废。
2.试卷若有雷同以零分计。
一、选择题(每题2分,共50分)1. 含有Cl -和Br -的混合溶液,欲使Br -氧化为Br 2而不使Cl -氧化,应选择 ( ) (θ/Sn Sn 24++ϕ =0.15 V ,θ/Cl Cl 2-ϕ=1.3583 V ,θ/BrBr 2-ϕ=1.087 V ,θ/Cr O Cr 3272+-ϕ=1.33 V , θ/MnMnO 24+-ϕ=1.51 V , θ/Fe Fe 23++ϕ=0.771 V )A. SnCl 4B. K 2Cr 2O 7C. KMnO 4D. Fe 3+2. 已知下列反应的平衡常数PbSO 4(S) 2++SO 42- K sp Θ(1)PbS (S) 2++S 2- K sp Θ(2)反应PbSO 4+S PbS+SO 4- 的K 为 ( )A. K SP Θ(1) . K sp Θ(2)B. K sp Θ(1) /K sp Θ(2)C. K sp Θ(2) /K sp Θ(1)D. ( K sp Θ(1) /K sp Θ(2) )23. 0.04mol·L -1的H 2CO 3的水溶液, K 1Θ﹑K 2Θ分别为它的电离常数,该溶液的c (H +)浓度和c (CO 32-)的浓度分别为 ( ) A. 04.0θ1⨯K , K 1ΘB. 04.0θ1⨯K , 04.0θ2⨯K2 C. 04.0θ2θ1⨯⨯K K , K 2Θ D. 04.0θ1⨯K , K 2Θ4. 已知某一元弱酸的浓度为c ,用等体积的水稀释后,溶液的c (H +)浓度为 ( )A. 2cB. c K a2θC. c K a ⨯θ21D. 2c K a ⨯θ5. θ/Cr O Cr 3272+-ϕ的数值随pH 的升高而( )A. 增大B. 不变C. 减少D. 无法判断6. 用AgNO 3处理[Fe(H 2O)5Cl]Br 溶液,产生的沉淀主要是 ( )A. AgBrB. AgClC. AgBr 和AgClD. Fe(OH)37. 已知K f Θ[Ag(NH 3)2+]<K f Θ[Ag(CN)2-]下列情况中能溶解AgCl 最多的是 ( )A. 1L 水B. 1L3.0 mol·L -1NH 3·H 2OC. 1L3.0 mol·L -1KCND. 1L3.0 mol·L -1 HCl8. 10ml2.0×10-4 mol·L -1Na 2SO 4溶液中加入10ml2.0×10-4 mol·L -1的BaCl 2溶液 后,溶液中SO 42-离子的浓度为[K sp Θ(BaSO 4)=1.0×10-10] 青 ( )A. >10-5 mol·L -1B. <10-5 mol·L -1C. =10-5 mol·L -1D. =10-4 mol·L -19. Pb 2+离子的价电子层结构是 ( )A. 6s 26p 2B. 5s 25p 23C. 6s 2D.5s 25p 65d 106s 210. 在一个多电子原子中,具有下列各套量子数(n,l,m,m s )的电子,能量 最大的电子具有的量子数是 ( )A. 3,2,+1,+1/2B. 2,1,+1,-1/2C. 3,1,0,-1/2D. 3,1,-1,+1/211. 密闭容器中,A ﹑B ﹑C 三种气体建立化学平衡,它们的反应是C, 在相同温度如果体积缩小2/3,则平衡常数K p 为原来的 ( )A. 3倍B. 9倍C. 2倍D. 不变12. 对于一个化学反应来说,下列哪一种是正确的? ( )A. △r G m 越负,反应速率越快B. △r H m 越负,反应速率越快C. 活化能越大, 反应速率越快D. 活化能越小, 反应速率越快13. 已知FeO (S) + C (S) = CO (q) + Fe (S) 反应的θm r H ∆为正, θm r S ∆为正,下列说法正确的是 ( )A. 低温下自发过程,高温下非自发过程B. 任何温度下均为非自发过程C. 高温下自发过程,底温下非自发过程D. 任何温度下均为自发过程14. K w Θ的值是6.4×10-15 (18 o C),1.00×10-14 (25 o C), 由此可推断出 ( )4A. 水的电离是吸热的B. 水的pH25 o C 时大于15 o C 时C. 18 o C 时, c (OH -)=1.0×10-7D. 仅在25 o C 时水才为中性15. 用配位(络合)滴定法测定石灰石中CaO 的含量,经四次平行测定,得 x =27.50%,若真实含量为27.30%,则27.50%-27.30%=+0.20%,称为 ( )A. 绝对偏差B. 相对偏差C. 绝对误差D. 相对误差16. 用计算器算得 004471.122000.0036.11124.1236.2=⨯⨯ ,按有效数字运算(修约)规则,结果应为 ( )A. 12B. 12.0C. 12.00D. 12.00417. 测定CaCO 3的含量时,加入一定量过量的HCl 标准溶液与其完全反应,过量部分HCl 用NaOH 溶液滴定,此滴定方式属 ( )A. 直接滴定方式B. 返滴定方式C. 置换滴定方式D. 间接滴定方式18. 已知p K b Θ(NH 3)=4.75用0.10mol·L -1NaOH 溶液滴定0.10 mol·L -1HCl+0.05 mol·L -1NH 4Cl 混合溶液,合适的指示剂是 ( )A. 甲基橙(p K a Θ=3.4)B. 溴甲酚兰(p K a Θ=4.1)C. 甲基红(p K a Θ=5.0)D. 酚酞(p K a Θ=9.1)19. 下列反应中滴定曲线对称的反应是 ( )A. Ce 4++Fe 2+=Ce 3++Fe 3+B. 2Fe 3++Sn 2+=2Fe 2++Sn 4+C. I 2+2S 2O 32-=2I -+S 4O 62-D. MnO 4-+5Fe 2++8H +=Mn 2++5Fe 3++4H 2O20. 在滴定分析测定中,将导致系统误差的是 ( )A. 试样未经充分混匀B. 滴定时有液滴溅出C. 砝码未经校正D. 沉淀穿过滤纸21. 欲配制0.2 mol·L-1HCl溶液和0.2 mol·L-1H2SO4溶液,量取浓酸的合适的量器是( )A. 容量瓶B. 吸量管C. 量筒D. 酸式滴定管22.间接碘量法中加入淀粉指示剂的适宜时间是( )A. 滴定开始时B. 标准溶液滴定了近50%时C. 标准溶液滴定了近75%D. 滴定接近计量点时23. 标定HCl和NaOH溶液常用的基准物是()A. 硼砂和EDTAB. 草酸和K2Cr2O7C. CaCO3和草酸D. 硼砂和邻苯二甲酸氢钾24.用K2Cr2O7法测Fe2+,加入H3PO4的主要目的是( )A. 提高酸度,B. 同Fe3+形成稳定的无色化合物,减少黄色对终点的干扰ϕ的数值,增大突跃范围C. 减小+3/Fe+2FeD. 防止Fe2+的水解25. 在EDTA配合滴定中,只考虑酸度影响,下列叙述正确的是( )A. 酸效应系数越大,配合物的稳定性越大B. 酸效应系数越小,配合物的稳定性越大C. pH越大,酸效应系数越大5D. 酸效应系数越大,滴定突跃范围越大二、判断题(每题1分,共20分)1. 配合物中心离子的配位数就是该配合物的配位体的个数。
2. 在HCl溶液中加入NaCl,由于产生同离子效应,溶液中的H+浓度会降低。
3. θϕ的值随溶液中Cu2+浓度的增加而升高。
/CuCu2+4. 酸碱完全中和后,溶液的pH等于7 。
5. 任何可逆反应在一定温度下,不论参加的物质的初始浓度如何不同,反应达平衡时,各物质的平衡浓度相同。
6. 根据电离平衡: H2S2H++S2-可知溶液中H+浓度是S2-离子浓度的两倍7. [Cu(NH3)4]2+的稳定常数比[Cu(en)2]2+的稳定常数小,因为[Cu(en)2]2+是螯合物。
8. 某一碱溶液中加入水稀释后,由于电离度增加[OH-]也增加。
9. 化学反应的Q p与反应的途径无关,但它却不是状态函数。
10. 即使在很浓的强酸水溶液中,仍然有OH-离子存在。
11.酸式滴定管一般用于盛酸性溶液和氧化性溶液,但不能盛放碱性溶液。
12.已记载的实验数据不可撕掉或涂改,有错误时,可划去并加以注明。
13.用100mL容量瓶准确量取100.00ml某标准溶液。
14.称取基准物质KBrO常用差减法进行。
315.多元弱碱在水中各型体的分布取决于溶液的pH。
16.氧化还原滴定中化学计量点时的电位为:67 21θ22θ11n n n n sp ++=ϕϕϕ17.Q 检验法进行数据处理时,若Q 计≤Q 0.90时,该可疑值应舍去。
18.指示剂的选择原则是:变色敏锐,用量少。
19.标定某溶液的浓度(单位:mol·L -1)得如下数据:0.01906、0.01910,其相对相差为0.2096%。
20.金属指示剂应具备的条件之一是1g K 'MY -1g K Min >2。
三、计算题(每题15分,共45分)1. 在298.15时,两电对++23Fe Fe 和Cu Cu 2+组成原电池,其中c (Fe 3+)=c (Fe 2+)=c (Cu 2+)=0.10 mol·L -1已知 θFe Fe 23++ϕ=0.771 V θCu Cu 2+ϕ=0.337 V 求:(1)写出原电池的电池符号,电极与电池反应(2)计算电池电动势(3)计算反应的平衡常数2. 要使0.05 mol 的AgCl (S) 溶解在500ml 氨水中,NH 3的浓度至少应为多大?已知: 7)Ag(NH θf 10123⨯=+K 10AgCl θsp 102-⨯=K3. 一含有H 2SO 4和H 3PO 4的混合液50.00ml 两份,分别用0.1000mol·L -1的 NaOH 滴定,第一份用甲基红作指示剂需26.15ml 滴至终点;第二份用酚酞作指 示剂需36.03ml 到达终点;求每升混合液中含每种酸多少克?()PO H (43θa2K = 6.2×10-8, )PO H (43θa3K =2.2×10-13)8模拟试题(1)参考答案一:1.B 2.B 3.D 4.B 5.C 6.A 7.C 8.C 9.C 10.A 11.D 12.D 13.C14.A 15.C 16.C 17.B 18.C 19.A 20C 21.C 22.D 23.D 24.C 25.B 二: 1.× 2.× 3.× 4.× 5.× 6.× 7.√ 8.× 9.√ 10.√ 11.√ 12.√ 13.× 14.× 15.× 16.× 17.× 18.× 19.× 20.√三:1. (1) Pt |(0.1)Fe (0.1),Fe ||(0.1)Cu |Cu 232+++ (1分)负极:Cu-2e=Cu 2+ 正极:Fe 3++e=Fe 2+ (2分)电池反应:Cu+2Fe 3+=Cu 2++2Fe 2+ (1分)(2).φ正=10592.0θFe Fe 23+++ϕlg 771.01.01.0= (1分)φ负=307.01.0lg 20592.0θCu Cu 2=++ϕ (1分)E = φ正 - φ负 = 0.771 - 0.307 = 0.464 (1分)(3).lg K θ=66.140592.0)337.0771.0(20592.0θ=-=nEK θ=4.57×1014 (3分)2.设:NH 3的平衡浓度为x mol ·L -1(1分)[Ag(NH 3)2]+=[Cl -]=0.1 mol·L -1 (1分) K j θ=K SP θ×K f θ=2×10-10×1×107=2×10-3=2r32r 3rr 23][NH 0.10.1][NH ][Cl ])[Ag(NH ⨯=-+ (6分)[NH 3]=510201.03=⨯- (1分)9 )L (mol 44.22.051NH 3-⋅=+=c (1分)3.596.100.501000200008.98)]15.2603.36(15.26[1000.0(g/L)SO H 42=⨯⨯--⨯= (5分) 10001)PO M(H V(NaOH)c(NaOH)(g/L)PO H 4343⨯⋅⋅= 936.100.501000100000.98)15.2603.36(1000.0=⨯⨯-⨯=(5分)。
