第三章 热力学第二定律(总复习题含答案)
2021年高中物理选修三第三章《热力学定律》知识点复习(答案解析)

一、选择题1.一定质量的理想气体经历一系列变化过程,如图所示,下列说法正确的是()→过程中,气体体积增大,从外界吸热A.a b→过程中,气体体积增大,从外界吸热B.b c→过程中,气体体积不变,向外界放热C.c a→过程中,气体内能增大,向外界放热D.c a2.某校开展探究性课外活动,一名同学用右图所示的装置研究气体压强、体积、温度三者之间的变化关系。
该同学选用导热良好的汽缸将其开口向下,内装理想气体,并将汽缸固定不动,但缸内活塞可自由滑动且不漏气,他把一温度计通过缸底小孔插入缸内,插口处密封良好,活塞下挂一个沙桶,沙桶装满沙子时活塞恰好静止。
他把沙桶底部钻一个小洞,让细沙慢慢漏出,外部环境温度恒定,由此可确定()A.外界对气体做功,内能增大B.外界对气体做功,温度计示数不变C.气体体积减小,温度计示数减小D.外界对气体做功,温度计示数增大3.为抗击新冠,防止病毒蔓延,每天都要用喷雾剂(装一定配比的84消毒液)对教室进行全面喷洒。
如图是某喷水壶示意图。
未喷水时阀门K闭合,压下压杆A可向瓶内储气室充气;多次充气后按下按柄B打开阀门K,水会自动经导管从喷嘴处喷出。
储气室内气体可视为理想气体,充气和喷水过程温度保持不变,则阀门()A.充气过程中,储气室内气体内能不变B.充气过程中,储气室内气体分子平均动能增大C.喷水过程中,储气室内气体吸热D.喷水过程中,储气室内气体压强不变4.下列说法正确的是A.物体吸收热量,其温度一定升高B.热量只能从高温物体向低温物体传递C.遵守热力学第一定律的过程一定能实现D.做功和热传递是改变物体内能的两种方式5.图为某种椅子与其升降部分的结构示意图,M、N两筒间密闭了一定质量的气体,M可沿N的内壁上下滑动,设筒内气体不与外界发生热交换,在M向下滑动的过程中A.外界对气体做功,气体内能增大B.外界对气体做功,气体内能减小C.气体对外界做功,气体内能增大D.气体对外界做功,气体内能减小6.下列说法正确的是A.自然界中涉及热现象的宏观过程都具有方向性B.气体压强越大,气体分子的平均动能就越大C.气体从外界吸收了热量,内能必定增加D.在绝热过程中,外界对气体做功,气体的内能减少7.如图所示,A、B为两相同的绝热气缸,用绝热活塞封闭了压强、体积、温度、质量均相同的同种气体,活塞和杠杆质量不计,活塞和杠杆接触,忽略一切摩擦.O为固定轴,且MO=NO,将A中气体温度升高(变化不大)到杠杆MN重新平衡,下列说法正确的是()A.B中气体温度不变B.B中气体温度降低C.A中气体克服外力做功,外界对B气体做功D.A中气体内能增加,B中气体内能减少8.有人设想在夏天用电冰箱来降低房间的温度.他的办法是:关好房间的门窗然后打开冰箱的所有门让冰箱运转,且不考虑房间内外热量的传递,则开机后,室内的温度将() A.逐渐有所升高B.保持不变C.开机时降低,停机时又升高D.开机时升高,停机时降低9.下列说法中正确的是()A.温度低的物体内能小B.外界对物体做功时,物体的内能一定增加C.温度低的物体分子运动的平均动能小D.做加速运动的物体,由于速度越来越大,因此物体分子的平均动能越来越大10.一定质量的理想气体从状态A变化到状态B,再变化到状态C,其变化过程的p V 图像如图所示()A.气体在A状态时的内能大于C状态时的内能B.气体在B状态时每个分子的动能都比A状态时大C.气体从状态A到B吸收的热量大于从状态B到C放出的热量D.气体从状态A到B吸收的热量等于从状态B到C放出的热量11.一定质量的理想气体从状态A开始,经A→B、B→C、C→A三个过程回到初始状态A,其状态变化过程的p-V图像如图所示。
第三章热力学第二定律 复习题

第三章 热力学第二定律一、选择题1、恒温恒压可逆相变过程中等于零的量是:A.U ∆;B.H ∆;C.G ∆;D.S ∆。
2、根据熵增大原理:A.隔离系统的熵永不减小;B.绝热系统的熵永不减小;C.系统和环境的熵的和永不减小; D 以上三者都对。
3、纯物质由液态蒸发为气态后其标准摩尔熵:A.增大;B.减小;C.不变;D.因物质种类不知所以不能确定。
4、理想气体的物质的量为n ,从始态A (P 1,V 1,T 1)变到末态B (P 2,V 2,T 2),其熵变的计算公式可用:( )A. ΔS = nRln(P 1/P 2) +⎰21T T p )T /dT C ( B. ΔS = nRln(P 1/P 2)-⎰21T T p )T /dT C ( C. ΔS = nRln(V 1/V 2)+ ⎰21T T p )T /dT C ( D. ΔS = nRln(V 1/V 2)-⎰21T T p )T /dT C ( 5、在标准压力P θ下,383.15K 的水变为同温下的蒸汽,吸热Q p 。
对于该相变过程,以下哪个关系式不能成立?( )A ΔG <0B ΔH=Q pC ΔS 隔离<0D ΔS 隔离>06、ΔG =0 的过程应满足的条件是(A) 等温等压且非体积功为零的可逆过程(B) 等温等压且非体积功为零的过程(C) 等温等容且非体积功为零的过程(D) 可逆绝热过程7、在一定温度下,发生变化的孤立体系,其总熵(A )不变 (B) 可能增大或减小 (C) 总是减小 (D)总是增大8、关于吉布斯函数G , 下面的说法中不正确的是(A) ΔG≤W'在做非体积功的各种热力学过程中都成立(B) 在等温等压且不做非体积功的条件下, 对于各种可能的变动, 系统在平衡态的吉氏函数最小(C) 在等温等压且不做非体积功时, 吉氏函数增加的过程不可能发生(D) 在等温等压下,一个系统的吉氏函数减少值大于非体积功的过程不可能发生9、关于热力学第二定律下列哪种说法是错误的(A) 热不能自动从低温流向高温(B) 不可能从单一热源吸热做功而无其它变化(C) 第二类永动机是造不成的(D) 热不可能全部转化为功10、关于克劳修斯-克拉佩龙方程下列说法错误的是(A) 该方程仅适用于液-气平衡(B) 该方程既适用于液-气平衡又适用于固-气平衡(C) 该方程假定气体的体积远大于液体或固体的体积(D) 该方程假定与固相或液相平衡的气体为理想气体11、关于熵的说法正确的是(A) 每单位温度的改变所交换的热为熵(B) 可逆过程熵变为零(C) 不可逆过程熵将增加(D) 熵与系统的微观状态数有关12、氢气进行不可逆循环(A)ΔU>0 (B) ΔS=0 (C) ΔS>0 (D) ΔS<013、下述过程,体系的ΔG何者为零?(A) 理想气体的等温膨胀(B) 孤立体系的任意过程(C) 在100℃,101325Pa下1mol水蒸发成水汽(D) 绝热可逆过程14、关于熵的性质, 下面的说法中不正确的是(A) 环境的熵变与过程有关(B) 某些自发过程中可以为系统创造出熵(C) 熵变等于过程的热温商(D) 系统的熵等于系统内各部分熵之和15、根据热力学第一定律,在一循环过程中()(A) 功与热可以完全相互转换(B) 功与热都不能完全相互转换(C) 功可以完全转变为热,热不能完全转变为功(D) 功不能完全转变为热,热可以完全转变为功16、在下列过程中, ΔG=ΔA的是(A) 液体等温蒸发(B) 气体绝热可逆膨胀(C) 理想气体在等温下混合(D) 等温等压下的化学反应17、在绝热恒容的系统中,H2和Cl2反应化合成HCl。
物理化学-课后答案-热力学第二定律

物理化学-课后答案-热力学第二定律-CAL-FENGHAI-(2020YEAR-YICAI)_JINGBIAN第三章 热力学第二定律【复习题】【1】指出下列公式的适用范围。
(1)min ln BB BS Rnx ∆=-∑;(2)12222111lnln ln ln P v p T V T S nR C nR C p T V T ∆=+=+; (3)dU TdS pdV =-; (4)G Vdp ∆=⎰(5),,S A G ∆∆∆作为判据时必须满足的条件。
【解】 (1)封闭体系平衡态,理想气体的等温混合,混合前后每种气体单独存在时的压力都相等,且等于混合后气体的总压力。
(2)非等温过程中熵的变化过程,对一定量的理想气体由状态A (P 1、V 1、T 1)改变到状态A (P 2、V 2、T 2)时,可由两种可逆过程的加和而求得。
(3)均相单组分(或组成一定的多组分)封闭体系,非体积功为0的任何过程;或组成可变的多相多组分封闭体系,非体积功为0的可逆过程。
(4)非体积功为0,组成不变的均相封闭体系的等温过程。
(5)S ∆:封闭体系的绝热过程,可判定过程的可逆与否; 隔离体系,可判定过程的自发与平衡。
A ∆:封闭体系非体积功为0的等温等容过程,可判断过程的平衡与否; G ∆:封闭体系非体积功为0的等温等压过程,可判断过程的平衡与否;【2】判断下列说法是否正确,并说明原因。
(1)不可逆过程一定是自发的,而自发过程一定是不可逆的; (2)凡熵增加过程都是自发过程; (3)不可逆过程的熵永不减少;(4)系统达平衡时,熵值最大,Gibbs 自由能最小;(5)当某系统的热力学能和体积恒定时,S ∆<0的过程不可能发生;(6)某系统从始态经过一个绝热不可逆过程到达终态,先在要在相同的始、终态之间设计一个绝热可逆过程;(7)在一个绝热系统中,发生了一个不可逆过程,系统从状态1变到了状态2,不论用什么方法,系统再也回不到原来状态了;(8)理想气体的等温膨胀过程,0U ∆=,系统所吸的热全部变成了功,这与Kelvin 的说法不符;(9)冷冻机可以从低温热源吸热放给高温热源,这与Clausius 的说法不符; (10)p C 恒大于V C 。
热力学第二定律复习题及解答

第三章 热力学第二定律一、思考题1. 自发过程一定是不可逆的,所以不可逆过程一定是自发的。
这说法对吗?答: 前半句是对的,后半句却错了。
因为不可逆过程不一定是自发的,如不可逆压缩过程。
2. 空调、冰箱不是可以把热从低温热源吸出、放给高温热源吗,这是否与第二定律矛盾呢?答: 不矛盾。
Claususe 说的是“不可能把热从低温物体传到高温物体,而不引起其他变化”。
而冷冻机系列,环境作了电功,却得到了热。
热变为功是个不可逆过程,所以环境发生了变化。
3. 能否说系统达平衡时熵值最大,Gibbs 自由能最小?答:不能一概而论,这样说要有前提,即:绝热系统或隔离系统达平衡时,熵值最大。
等温、等压、不作非膨胀功,系统达平衡时,Gibbs 自由能最小。
4. 某系统从始态出发,经一个绝热不可逆过程到达终态。
为了计算熵值,能否设计一个绝热可逆过程来计算?答:不可能。
若从同一始态出发,绝热可逆和绝热不可逆两个过程的终态绝不会相同。
反之,若有相同的终态,两个过程绝不会有相同的始态,所以只有设计除绝热以外的其他可逆过程,才能有相同的始、终态。
5. 对处于绝热瓶中的气体进行不可逆压缩,过程的熵变一定大于零,这种说法对吗? 答: 说法正确。
根据Claususe 不等式TQS d d ≥,绝热钢瓶发生不可逆压缩过程,则0d >S 。
6. 相变过程的熵变可以用公式H ST∆∆=来计算,这种说法对吗?答:说法不正确,只有在等温等压的可逆相变且非体积功等于零的条件,相变过程的熵变可以用公式THS ∆=∆来计算。
7. 是否,m p C 恒大于 ,m V C ?答:对气体和绝大部分物质是如此。
但有例外,4摄氏度时的水,它的,m p C 等于,m V C 。
8. 将压力为101.3 kPa ,温度为268.2 K 的过冷液体苯,凝固成同温、同压的固体苯。
已知苯的凝固点温度为278.7 K ,如何设计可逆过程?答:可以将苯等压可逆变温到苯的凝固点278.7 K :9. 下列过程中,Q ,W ,ΔU ,ΔH ,ΔS ,ΔG 和ΔA 的数值哪些为零?哪些的绝对值相等?(1)理想气体真空膨胀; (2)实际气体绝热可逆膨胀; (3)水在冰点结成冰;(4)理想气体等温可逆膨胀;(5)H 2(g )和O 2(g )在绝热钢瓶中生成水;(6)等温等压且不做非膨胀功的条件下,下列化学反应达到平衡:H 2(g )+ Cl 2(g )(g )答: (1)0Q WU H ==∆=∆=(2)0, R Q S U W =∆=∆= (3)e 0, , P G H Q A W ∆=∆=∆= (4)e 0, =, U H Q W G A ∆=∆=-∆=∆ (5)e = 0V U Q W ∆==(6)0=W,H U Q ∆=∆=,0=∆=∆G A10. 298 K 时,一个箱子的一边是1 mol N 2 (100 kPa),另一边是2 mol N 2 (200 kPa ),中间用隔板分开。
第三章热力学第二定律

第三章 热力学第二定律自测题㈠ 填空题1.在高温热源T 1和低温热源T 2之间的卡诺循环, 其热温熵之和()1212Q Q T T +=。
循环过程的热级效率()η=。
2.任一不可逆循环过程的热温熵之和,可以表示为()0Q T δ⎛⎫ ⎪⎝⎭⎰ 不可逆。
3.在绝热密闭的刚性容器中发生某一化学反应,此过程的()sys 0S ∆;()amb0S ∆。
4.系统经可逆循环后,S ∆( )0, 经不可逆循环后S ∆( )。
(填>,=,<)。
5.某一系统在与环境300K 大热源接触下经历一不可逆循环过程,系统从环境得到10kJ 的功,则系统与环境交换的热()Q =;()sys S ∆=;()amb S ∆=6.下列过程的△U 、△H 、△S 、△G 何者为零⑴ 理想气体自由膨胀( );⑵ H 2(g )和Cl 2(g )在绝热的刚性容器中反应生成HCl (g )的过程( );⑶ 在0 ℃、101.325 kPa 下水结成冰的相变过程( )。
⑷ 一定量真实气体绝热可逆膨胀过程( )。
⑸ 实际气体节流膨胀过程( )。
7.一定量理想气体与300K 大热源接触做等温膨胀,吸热Q =600kJ,对外所做功为可逆功的40%,则系统的熵变()S ∆=。
8. 1 mol O 2(p 1,V 1,T 1)和1 mol N 2(p 1,V 1,T 1)混合后,总压为2 p 1,总体积为V 1,温度为T 1,此过程的△S ( )0(填>,<或=,O 2和N 2均可看作理想气体)。
9.热力学第三定律用公式表示为:()()*m S =。
10. 根据 d G =-S d T+V d p 可知任一化学反应的(1)r m ΔT G p ⎛⎫∂= ⎪∂⎝⎭( ); (2)r m ΔP G T ∂⎛⎫= ⎪∂⎝⎭( );(3)r m ΔPV T ∂⎛⎫= ⎪∂⎝⎭( )。
11.某理想气体在500 K 、100 kPa 时,其m T S p ⎛⎫∂= ⎪∂⎝⎭ ( )(要求填入具体数值和单位)。
高中物理 选修三(2019)第三章 热力学定律 章末复习 综合练习 单元练习(含答案)
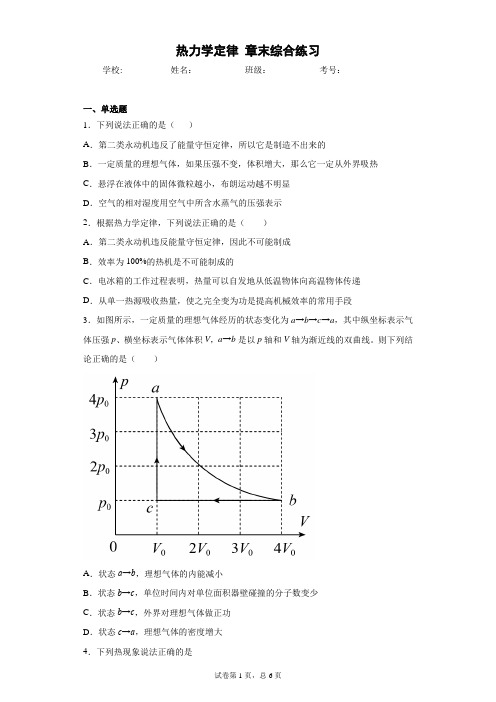
热力学定律章末综合练习学校:___________姓名:___________班级:___________考号:___________一、单选题1.下列说法正确的是()A.第二类永动机违反了能量守恒定律,所以它是制造不出来的B.一定质量的理想气体,如果压强不变,体积增大,那么它一定从外界吸热C.悬浮在液体中的固体微粒越小,布朗运动越不明显D.空气的相对湿度用空气中所含水蒸气的压强表示2.根据热力学定律,下列说法正确的是()A.第二类永动机违反能量守恒定律,因此不可能制成B.效率为100%的热机是不可能制成的C.电冰箱的工作过程表明,热量可以自发地从低温物体向高温物体传递D.从单一热源吸收热量,使之完全变为功是提高机械效率的常用手段3.如图所示,一定质量的理想气体经历的状态变化为a→b→c→a,其中纵坐标表示气体压强p、横坐标表示气体体积V,a→b是以p轴和V轴为渐近线的双曲线。
则下列结论正确的是()A.状态a→b,理想气体的内能减小B.状态b→c,单位时间内对单位面积器壁碰撞的分子数变少C.状态b→c,外界对理想气体做正功D.状态c→a,理想气体的密度增大4.下列热现象说法正确的是A .物体的温度越高,说明物体分子的平均动能越大B .波涛汹涌的海水上下翻腾,说明水分子热运动剧烈C .水凝结成冰,说明水分子的热运动已停止D .空调制冷时,将热量从低温室内传到高温室外,说明热传递是随意的,不具有方向性5.下列叙述正确的是( )A .外界对物体做功,物体的内能一定增加B .热量不能由低温物体传递到高温物体C .温度升高,物体内每个分子的热运动速率都增大D .自然界中进行的涉及热现象的宏观过程都具有方向性6.如图所示,固定的气缸内由活塞B 封闭着一定质量的理想气体,在外力F 作用下,将活塞B 缓慢地向右拉动.在拉动活塞的过程中,假设气缸壁的导热性能良好,环境的温度保持不变,则下列说法正确的是A .气体从外界吸热,内能增加B .气体向外界放热,内能减少C .气体对外界做功,气体压强变小D .外界对气体做功,气体压强变小7.如图所示,厚壁容器的一端通过胶塞插进一支灵敏温度计和一根气针,另一端有个用卡子卡住的可移动胶塞。
第三章 热力学第二定律

第三章 热力学第二定律【复习题】【1】指出下列公式的适用范围。
(1)min ln BB BS Rnx ∆=-∑;(2)12222111lnln ln ln P v p T V T S nR C nR C p T V T ∆=+=+; (3)dU TdS pdV =-; (4)G Vdp ∆=⎰(5),,S A G ∆∆∆作为判据时必须满足的条件。
【解】 (1)封闭体系平衡态,理想气体的等温混合,混合前后每种气体单独存在时的压力都相等,且等于混合后气体的总压力。
(2)非等温过程中熵的变化过程,对一定量的理想气体由状态A (P 1、V 1、T 1)改变到状态A (P 2、V 2、T 2)时,可由两种可逆过程的加和而求得。
(3)均相单组分(或组成一定的多组分)封闭体系,非体积功为0的任何过程;或组成可变的多相多组分封闭体系,非体积功为0的可逆过程。
(4)非体积功为0,组成不变的均相封闭体系的等温过程。
(5)S ∆:封闭体系的绝热过程,可判定过程的可逆与否; 隔离体系,可判定过程的自发与平衡。
A ∆:封闭体系非体积功为0的等温等容过程,可判断过程的平衡与否; G ∆:封闭体系非体积功为0的等温等压过程,可判断过程的平衡与否;【2】判断下列说法是否正确,并说明原因。
(1)不可逆过程一定是自发的,而自发过程一定是不可逆的; (2)凡熵增加过程都是自发过程; (3)不可逆过程的熵永不减少;(4)系统达平衡时,熵值最大,Gibbs 自由能最小;(5)当某系统的热力学能和体积恒定时,S ∆<0的过程不可能发生;(6)某系统从始态经过一个绝热不可逆过程到达终态,先在要在相同的始、终态之间设计一个绝热可逆过程;(7)在一个绝热系统中,发生了一个不可逆过程,系统从状态1变到了状态2,不论用什么方法,系统再也回不到原来状态了;(8)理想气体的等温膨胀过程,0U ∆=,系统所吸的热全部变成了功,这与Kelvin 的说法不符;(9)冷冻机可以从低温热源吸热放给高温热源,这与Clausius 的说法不符; (10)p C 恒大于V C 。
物理化学复习题目(含答案)67933

物理化学总复习第一章热力学第一定律∆=+只适用于:答案:D1.热力学第一定律U Q W(A)单纯状态变化(B)相变化(C)化学变化(D)封闭体系的任何变化∆约为:4157J 2.1mol单原子理想气体,在300K时绝热压缩到500K,则其焓变H3.关于热和功,下面说法中,不正确的是:答案:B(A)功和热只出现在体系状态变化的过程中,只存在于体系和环境的界面上(B)只有封闭体系发生的过程中,功和热才有明确的意义(C)功和热不是能量,而是能量传递的两种形式,可称为被交换的能量(D)在封闭体系中发生的过程,如果内能不变,则功和热对体系的影响必互相抵消4.涉及焓的下列说法中正确的是:答案:D(A)单质的焓值均为零(B)在等温过程中焓变为零(C)在绝热可逆过程中焓变为零(D)化学反应中体系的焓变不一定大于内能变化5.下列过程中,体系内能变化不为零的是:答案:D(A)不可逆循环过程(B)可逆循环过程(C)两种理想气体的混合过程(D)纯液体的真空蒸发过程6.对于理想气体,下列关系中那个是不正确的?答案:A(A )0)TU (V =∂∂ (B ) 0)V U (T =∂∂ (C ) 0)P U (T =∂∂ (D ) 0)P H (T =∂∂ 7. 实际气体的节流膨胀过程中,哪一组的描述是正确的?答案:A(A ) Q = 0 ;H ∆ =0;P ∆< 0 (B ) Q = 0 ;H ∆ = 0;P ∆> 0(C ) Q > 0 ;H ∆ =0;P ∆< 0 (D ) Q < 0 ;H ∆ = 0;P ∆< 08. 3mol 的单原子理想气体,从初态T 1=300 K 、p 1=100kPa 反抗恒定的外压50kPa 作不可逆膨胀至终态T 2=300 K 、p 2=50kPa ,对于这一过程的Q= 3741J 、W= -3741 J 、U ∆= 0 、H ∆= 0 。
9. 在一个绝热的刚壁容器中,发生一个化学反应,使物系的温度从T 1升高到T 2,压力从p 1升高到p 2,则:Q = 0 ;W = 0 :U ∆ = 0。
第三章 热力学第二定律复习题及解答

第三章 热力学第二定律一、思考题1. 自发过程一定是不可逆的,所以不可逆过程一定是自发的。
这说法对吗?答: 前半句是对的,后半句却错了。
因为不可逆过程不一定是自发的,如不可逆压缩过程。
2. 空调、冰箱不是可以把热从低温热源吸出、放给高温热源吗,这是否与第二定律矛盾呢?答: 不矛盾。
Claususe 说的是“不可能把热从低温物体传到高温物体,而不引起其他变化”。
而冷冻机系列,环境作了电功,却得到了热。
热变为功是个不可逆过程,所以环境发生了变化。
3. 能否说系统达平衡时熵值最大,Gibbs 自由能最小?答:不能一概而论,这样说要有前提,即:绝热系统或隔离系统达平衡时,熵值最大。
等温、等压、不作非膨胀功,系统达平衡时,Gibbs 自由能最小。
4. 某系统从始态出发,经一个绝热不可逆过程到达终态。
为了计算熵值,能否设计一个绝热可逆过程来计算?答:不可能。
若从同一始态出发,绝热可逆和绝热不可逆两个过程的终态绝不会相同。
反之,若有相同的终态,两个过程绝不会有相同的始态,所以只有设计除绝热以外的其他可逆过程,才能有相同的始、终态。
5. 对处于绝热瓶中的气体进行不可逆压缩,过程的熵变一定大于零,这种说法对吗? 答: 说法正确。
根据Claususe 不等式TQS d d ≥,绝热钢瓶发生不可逆压缩过程,则0d >S 。
6. 相变过程的熵变可以用公式H ST∆∆=来计算,这种说法对吗?答:说法不正确,只有在等温等压的可逆相变且非体积功等于零的条件,相变过程的熵变可以用公式THS ∆=∆来计算。
7. 是否,m p C 恒大于 ,m V C ?答:对气体和绝大部分物质是如此。
但有例外,4摄氏度时的水,它的,m p C 等于,m V C 。
8. 将压力为101.3 kPa ,温度为268.2 K 的过冷液体苯,凝固成同温、同压的固体苯。
已知苯的凝固点温度为278.7 K ,如何设计可逆过程?答:可以将苯等压可逆变温到苯的凝固点278.7 K :9. 下列过程中,Q ,W ,ΔU ,ΔH ,ΔS ,ΔG 和ΔA 的数值哪些为零?哪些的绝对值相等?(1)理想气体真空膨胀; (2)实际气体绝热可逆膨胀; (3)水在冰点结成冰; (4)理想气体等温可逆膨胀;(5)H 2(g )和O 2(g )在绝热钢瓶中生成水;(6)等温等压且不做非膨胀功的条件下,下列化学反应达到平衡:H 2(g )+ Cl 2(g )(g )答: (1)0Q WU H ==∆=∆=(2)0, R Q S U W=∆=∆=(3)e 0, , P G H Q A W ∆=∆=∆= (4)e 0, =, U H Q W G A ∆=∆=-∆=∆ (5)e = 0V U Q W ∆==(6)0=W,H U Q ∆=∆=,0=∆=∆G A10. 298 K 时,一个箱子的一边是1 mol N 2 (100 kPa),另一边是2 mol N 2 (200 kPa ),中间用隔板分开。
【复习题】热力学第二定律复习题

【关键字】复习题热力学第二定律一、选择题1.体系经历一个正的卡诺循环后,试判断下列哪一种说法是错误的?(a)体系本身没有任何变化(b)再沿反方向经历一个可逆的卡诺循环,最后体系和环境都没有任何变化(c)体系复原了,但环境并未复原(d)体系和环境都没有任何变化(答案) d (什么叫卡诺循环?以理想气体为工作物质,从高温(Th)热源吸收(Qh)的热量,一部分通过理想热机用来对外做功(Wr)另一部分(Qc)的热量放给低温(Tc)热源。
这种循环称为卡诺循环。
P102)2.一卡诺热机在两个不同温热源之间运转, 当工作物质为气体时, 热机效率为42%, 若改用液体工作物质, 则其效率应当(a)减少(b)增加(c)不变(d)无法判断(答案) c (卡诺定律的推论?P109-110)3.在pV图上,卡诺循环所包围的面积代表了(a) 循环过程的(b) 循环过程的自由能变化(c) 循环过程的熵变(d) 循环过程的焓变(答案)a4.当低温热源的温度趋近于0K时,卡诺热机的效率(a)趋近于1 (b)趋于无限大(c)趋于0 (d)大于其它可逆热机效率(答案) a (卡诺热机效率,卡诺定律?P108)( 所有工作于同温热源和同温冷源之间的热机,其效率都不能超过可逆机,即可逆机的效率最大。
)5.关于热力学第二定律下列哪种说法是错误的(a)热不能自动从低温流向高温(b)不可能从单一热源吸热做功而无其它变化(c)第二类永动机是造不成的(d)热不可能全部转化为功(答案) d (P107热力学第二定律的开尔文说法和克劳修斯说法)6.关于熵的说法正确的是(a)每单位温度的改变所交换的热为熵(b)可逆过程熵变为零(c)不可逆过程熵将增加(d)熵与系统的微观状态数有关(答案) d (熵函数的定义P110-111), ,7.熵变S是:(1) 不可逆过程热温商之和(2) 可逆过程热温商之和(3) 与过程无关的状态函数(4) 与过程有关的状态函数 以上正确的是(a ) 1,2 (b ) 2,3 (c ) 2 (d ) 4(答案) b (熵函数的定义和性质P110-111), 8.任意的可逆循环过程,体系的熵变(a)一定为零 (b)一定大于零 (c)一定为负 (d)是温度的函数 (答案) a9.封闭体系经过一循环过程后,则(a ) 体系的熵增加 (b ) U = 0(c ) Q = 0 (d ) 体系的T 、P 都不变(答案) d (什么叫过程函数,什么叫状态函数,状态函数的性质) 10.在始末态一定的热力学过程中(a )过程热为定值 (b )可逆热温商为定值 (c )热容为定值 (d )热力学能U 为定值 (答案) b11.对于不做非体积功的隔离体系,熵判据为(a )(d S )T,U ≥0 (b )(d S )p,U ≥0 (c )(d S )U,p ≥0 (d )(d S )U,V ≥0 (答案) d(熵熵判据P 113)>0 不可逆过程dS ad 或 dS iso (=dS sys +dS sur ) =0 可逆过程或平衡状态 <0 不可能发生的过程 .11. 在一定速度下发生变化的孤立体系,其总熵的变化是什么?(a) 不变 (b) 可能增大或减小 (c) 总是增大 (d) 总是减小(答案) c (熵增原理P 113-114),A B A B i()0QST→→δ∆-≥∑在绝热条件下,趋向于平衡的过程使体系的熵增加。
热力学第二定律复习题

热力学第二定律(r δ/0Q T =∑)→熵函数引出 0< (不可能发生的过程) 0= (可逆过程)0>(自发、不可逆过程)S ∆环)I R ηη≤ 不等式:)0A B iA BS →→∆≥函数G 和Helmholtz 函数A 的目的A U TS ≡-,G H TS ≡-d d d d d d d d T S p VT S V p S T p V S T V p -+---+ W ' =0,组成恒定封闭系统的 可逆和不可逆过程。
但积分时要用可逆途径的V ~p 或T ~S 间 的函数关系。
应用条件: V )S =-(∂p /∂S )V , (∂T /∂p )S =(∂V /∂S )pV )T =(∂p /∂T )V , (∂S /∂p )T =-(∂V /∂T )p应用:用易于测量的量表示不能直接测量的量,常用于热力学关系式的推导和证明<0 (自发过程) =0 (平衡(可逆)过程)判据△A T ,V ,W ’=0判据△G T ,p ,W ’=0<0 (自发过程) =0 (平衡(可逆)过程)基本计算公式/()/rS Q T dU W Tδδ∆==-⎰⎰, △S环=-Q体/T环△A=△U-△(TS) ,d A=-S d T-p d V△G=△H-△(TS) ,d G=-S d T-V d p不同变化过程△S、△A、△G 的计算简单pVT变化(常压下)凝聚相及实际气体恒温:△S =-Q r/T;△A T≈0 ,△G T≈V△p≈0(仅对凝聚相)△A=△U-△(TS),△G=△H-△(TS); △A≈△G恒压变温21,(/)Tp mTS nC T dT∆=⎰nC p,m ln(T2/T1)C p,m=常数恒容变温21,(/)TV mTS nC T dT∆=⎰nC V,m ln(T2/T1)C V,m=常数△A=△U-△(TS),△G=△H-△(TS); △A≈△G理想气体△A、△G的计算恒温:△A T=△G T=nRT ln(p2/p1)=- nRT ln(V2/V1)变温:△A=△U-△(TS),△G=△H-△(TS)计算△S△S=nC V,m ln(T2/T1)+nR ln(V2/V1)= nC p,m ln(T2/T1)-nR ln(p2/p1)= nC V,m ln(p2/p1)+ nC p,m ln(V2/V1)纯物质两相平衡时T~p关系g↔l或s两相平衡时T~p关系任意两相平衡T~p关系:m md/d/p T T V Hββαα=∆∆(Clapeyron方程)微分式:vap m2d lndHpT RT∆=(C-C方程)定积分式:ln(p2/p1)=-△vap H m/R(1/T2-1/T1)不定积分式:ln p=-△vap H m/RT+C恒压相变化不可逆:设计始、末态相同的可逆过程计S=△H/T;△G=0;△A≈0(凝聚态间相变)=-△n(g)RT (g↔l或s)化学变化标准摩尔生成Gibbs函数r m,BG∆定义r m B m,BBS Sν∆=∑,r m B f m,BBH Hν∆=∆∑,r m r m r mG H T S∆=∆-∆或r m B f m,BG Gν∆=∆∑G-H方程(∂△G/∂T)p=(△G-△H)/T或[∂(△G/T)/∂T]p=-△H/T2(∂△A/∂T)V=(△A-△U)/T或[∂(△A/T)/∂T]V=-△U/T2积分式:2r m0()//ln1/21/6G T T H T IR a T bT cT∆=∆+-∆-∆-∆应用:利用G-H方程的积分式,可通过已知T1时的△G(T1)或△A(T1)求T2时的△G(T2)或△A(T2)微分式热力学第三定律及其物理意义规定熵、标准摩尔熵定义任一物质标准摩尔熵的计算一、选择题1. 体系经历一个正的卡诺循环后,试判断下列哪一种说法是错误的? (a ) 体系本身没有任何变化(b ) 再沿反方向经历一个可逆的卡诺循环,最后体系和环境都没有任何变化 (c ) 体系复原了,但环境并未复原 (d ) 体系和环境都没有任何变化(答案) d (什么叫卡诺循环?以理想气体为工作物质,从高温(T h )热源吸收(Q h )的热量,一部分通过理想热机用来对外做功(Wr )另一部分(Qc)的热量放给低温(Tc)热源。
高中选修3-3热力学第二定律 热力学第二定律的微观解释练习题测试题复习题

【成才之路】2016高中物理第10章第4、5节热力学第二定律热力学第二定律的微观解释同步练习新人教版选修3-3基础夯实一、选择题(1~3题为单选题,4、5题为多选题)1.第二类永动机不可能制成,是因为( )A.违背了能量的守恒定律B.热量总是从高温物体传递到低温物体C.机械能不能全部转化为内能D.内能不能全部转化为机械能,同时不引起其他变化答案:D解析:第二类永动机的设想并不违背能量守恒定律,但却违背了涉及热量的能量转化过程是有方向性的规律。
故选项A错;在引起其他变化的情况下,热量可由低温物体非自发地传递到高温物体。
故B错。
机械能可以全部转化为内能。
2.我们绝不会看到:一个放在水平地面上的物体,靠降低温度,可以把内能自发地转化为动能,使这个物体运动起来。
其原因是( )A.这违反了能量守恒定律B.在任何条件下内能都不可能转化为机械能,只有机械能才会转化为内能C.机械能和内能的转化过程具有方向性,内能转化成机械能是有条件的D.以上说法均不正确答案:C解析:机械能和内能可以相互转化,但必须通过做功来实现。
由热力学第二定律可知,内能不可能全部转化成机械能,同时不引起其他变化。
3.下列叙述中正确的是( )A.对一定质量的气体加热,其内能可能减小B.在任何系统中,一切过程都朝着熵增加的方向进行C.物体的温度升高,分子热运动变得剧烈,每个分子动能都增大D.根据热力学第二定律可知,热量能够从高温物体传到低温物体,但不可能从低温物体传到高温物体答案:A解析:对一定质量的气体,内能的变化既与热传递有关又与做功有关,对气体加热,气体的内能可能减小,A正确。
系统总是自发地朝着熵增加的方向进行,B错误。
温度升高,分子的平均动能增大,但每个分子的动能不一定都增大,C错误。
热量在一定条件下可以从低温物体传到高温物体,D项错误。
4.从微观角度看( )A.热力学第二定律是一个统计规律B.一个孤立系统总是从熵大的状态向熵小的状态发展C.一个宏观状态所对应的微观状态越多,越是无序,熵值越大D.出现概率越大的宏观状态,熵值越大答案:ACD解析:由熵增加原理——一切自然过程总是沿着分子热运动的无序性增大的方向进行,可知B错误,A、C、D正确。
热力学第二定律(习题)

热力学第二定律(习题)一、选择题1.关于热力学第一定律和热力学第二定律,下列论述正确的是().A.热力学第一定律指出内能能够与其他形式的能相互转化,而热力学第二定律则指出内能不可能完全转化为其他形式的能,故这两条定律是相互矛盾的B.内能能够转化为其他形式的能,只是会产生其他阻碍,故两条定律并不矛盾C.两条定律差不多上有关能量的转化规律,它们不但不矛盾,而且没有本质区别D.事实上,能量守恒定律差不多包含了热力学第一定律和热力学第二定律2.以下哪个现象不违抗热力学第二定律().A.一杯热茶在打开盖后,茶会自动变得更热B.没有漏气、没有摩擦的理想热机,其效率可能是100%C.桶中浑浊的泥水在静置一段时刻后,泥沙下沉,上面的水变清,泥、水自动分离D.热量自发地从低温物体传到高温物体3.下列关于能量耗散的说法,正确的是().A.能量耗散使能的总量减少,违抗了能量守恒定律B.能量耗散是指耗散在环境中的内能再也不能被人类利用C.各种形式的能量向内能的转化,是能够自动全额发生的D.能量耗散导致能量品质的降低4.关于能源,以下说法中正确的是().A.煤、石油、天然气等燃料的化学能实际上是太阳能转化而成的B.能源的利用过程,实质上是能的转化和转移的过程C.到目前为止,人类所利用的所有能源实际上差不多上太阳能转化而成的D.核能和地热能来自地球本身5.当前世界上日益严峻的环境问题要紧源于().A.温室效应B.厄尔尼诺现象C.人类对环境的污染和破坏D.火山喷发和地震6.下列叙述中不正确的是().A.市区禁止摩托车通行是为了提高城区空气质量B.无氟冰箱的使用会使臭氧层受到不同程度的破坏C.大气中CO2含量的增多是引起温室效应的要紧缘故D.“白色污染”是当前环境爱护亟待解决的问题之一7.如图所示为电冰箱的工作原理图.压缩机工作时,强迫制冷剂在冰箱内外的管道中不断循环.那么,下列说法中正确的是().A.在冰箱内的管道中,制冷剂迅速膨胀并吸取热量B.在冰箱外的管道中,制冷剂迅速膨胀并放出热量C.在冰箱内的管道中,制冷剂被剧烈压缩并吸取热量D.在冰箱内的管道中,制冷剂被剧烈压缩并放出热量8.下面关于热力学第二定律微观意义的说法正确的是().A.从微观的角度看,热力学第二定律是一个统计规律B.一切自然过程总是沿着分子热运动无序性减小的方向进行C.有的自然过程沿着分子热运动无序性增人的方向进行,有的自然过程沿着分子热运动无序性减小的方向进行D.在任何自然过程中,一个孤立系统的总熵可不能减小9.第二类永动机不可能制成,这是因为().A.违抗了能量守恒定律B.热量总是从高温物体传递到低温物体C.机械能不能全部转变为内能D.内能不能全部转化为机械能,同时不引起其他变化10.装有浑浊黄河水的杯子置于与它温度相同的绝热容器中,过一段时问,泥沙沉淀,则杯中水温将().A.升高B.不变C.下降D.无法确定二、填空题11.热量会自动地从________传给________,但可不能自发地从_____ ___传给________,这说明:热传导的过程是有________的,那个过程能够向一个方向自发地进行,然而向相反的方向不能________地进行,要实现相反方向的过程,必须有________,因而产生________或引起________.12.依照热力学定律和分子动理论,可知理想气体在温度升高时,内能(填:不变、增大、减小);第二类永动机不可能制成的要紧缘故是违抗了13.只要确定了________,符合那个________的就叫做有序,有序和无序是相对的.无序意味着各处都一样,没有差别,而有序则相反.14.假如一个“宏观态”对应的“微观态”比较多,就说那个“宏观态”是比较________.三、解答题15.依照你对熵增加原理的说明,举出一些系统从有序变为无序的例子.16.有一座瀑布的高度是50 m,流量为12 m3/s,打算在瀑布底部利用水流能发电,设在瀑布顶处水流速率与从发电机处水轮机内流出速率相等,且水流能有65%被利用,求安装的发电机功率最多多大?(g取10 m/s2)17.水能是可再生能源,可连续地利用它来发电,为人类提供“清洁”的能源,若一水力发电站水库的平均流量为Q(m3/s),落差为h,发电效率为 ,则全年发电量(kW·h)是多少?(g取10m/s2)【答案与解析】一、选择题1.【答案】B【解析】热力学第一定律和热力学第二定律并不矛盾,机械能和内能的转化具有方向性,故B选项正确.2.【答案】C【解析】茶可不能自发地变得更热,选项A错误;不管什么样的热机,效率永久可不能达到100%,选项B错误;热量可不能自发地从低温物体传到高温物体,选项D错误。
物理化学答案第三章热力学第二定律

物理化学答案第三章热⼒学第⼆定律第三章热⼒学第⼆定律3.1 卡诺热机在的⾼温热源和的低温热源间⼯作。
求(1)热机效率;(2)当向环境作功时,系统从⾼温热源吸收的热及向低温热源放出的热。
解:卡诺热机的效率为根据定义3.5 ⾼温热源温度,低温热源。
今有120 kJ的热直接从⾼温热源传给低温热源,龟此过程的。
解:将热源看作⽆限⼤,因此,传热过程对热源来说是可逆过程3.6 不同的热机中作于的⾼温热源及的低温热源之间。
求下列三种情况下,当热机从⾼温热源吸热时,两热源的总熵变。
(1)可逆热机效率。
(2)不可逆热机效率。
(3)不可逆热机效率。
解:设热机向低温热源放热,根据热机效率的定义因此,上⾯三种过程的总熵变分别为。
3.7 已知⽔的⽐定压热容。
今有1 kg,10 °C的⽔经下列三种不同过程加热成100 °C的⽔,求过程的。
(1)系统与100 °C的热源接触。
(2)系统先与55 °C的热源接触⾄热平衡,再与100 °C的热源接触。
(3)系统先与40 °C,70 °C的热源接触⾄热平衡,再与100 °C的热源接触。
解:熵为状态函数,在三种情况下系统的熵变相同在过程中系统所得到的热为热源所放出的热,因此3.8 已知氮(N2, g)的摩尔定压热容与温度的函数关系为将始态为300 K,100 kPa下1 mol的N2(g)置于1000 K的热源中,求下列过程(1)经恒压过程;(2)经恒容过程达到平衡态时的。
解:在恒压的情况下在恒容情况下,将氮(N2, g)看作理想⽓体将代替上⾯各式中的,即可求得所需各量3.9 始态为,的某双原⼦理想⽓体1 mol,经下列不同途径变化到,的末态。
求各步骤及途径的。
(1)恒温可逆膨胀;(2)先恒容冷却⾄使压⼒降⾄100 kPa,再恒压加热⾄;(3)先绝热可逆膨胀到使压⼒降⾄100 kPa,再恒压加热⾄。
解:(1)对理想⽓体恒温可逆膨胀,D U = 0,因此(2)先计算恒容冷却⾄使压⼒降⾄100 kPa,系统的温度T:(3)同理,先绝热可逆膨胀到使压⼒降⾄100 kPa时系统的温度T:根据理想⽓体绝热过程状态⽅程,各热⼒学量计算如下2.12 2 mol双原⼦理想⽓体从始态300 K,50 dm3,先恒容加热⾄400 K,再恒压加热⾄体积增⼤到100 dm3,求整个过程的。
2021年高中物理选修三第三章《热力学定律》复习题(答案解析)(1)

一、选择题1.一定质量的理想气体经历一系列变化过程,如图所示,下列说法正确的是()→过程中,气体体积增大,从外界吸热A.a b→过程中,气体体积增大,从外界吸热B.b c→过程中,气体体积不变,向外界放热C.c a→过程中,气体内能增大,向外界放热D.c a2.“绿色、环保、低碳”是当今世界的关键词,“低碳”要求我们节约及高效利用能源。
关于能源与能量,下列说法正确的是()A.因为能量守恒,所以不要节约能源B.自然界中石油、煤炭等能源可供人类长久使用C.人类应多开发与利用风能、太阳能等新型能源D.人类不断地开发和利用新的能源,所以能量可以被创造3.一定质量的理想气体在某一过程中,气体对外界做功1.6×104J,从外界吸收热量3.8×104J,则该理想气体的()A.温度降低,密度减小B.温度降低,密度增大C.温度升高,密度减小D.温度升高,密度增大4.下列说法正确的是()A.物体放出热量,其内能一定减小B.物体对外做功,其内能一定减小C.物体吸收热量,同时对外做功,其内能可能增加D.物体放出热量,同时对外做功,其内能可能不变5.如图所示,一定质量理想气体的体积V与温度T关系图像,它由状态A经等温过程到状态B,再经等容过程到状态C。
则下列说法中正确的是()A.在A、B、C三个状态中B对应的压强最大B.在A、B、C三个状态中C对应的压强最大C.过程AB中外界对气体做功,内能增加D.过程BC中气体吸收热量,内能不变6.如图所示,一定质量的理想气体从状态A依次经过状态B、C和D后再回到状态A。
其中,A→B和C→D为等温过程,B→C为等压过程,D→A为等容过程。
关于该循环过程中,下列说法正确的是()A.A→B过程中,气体吸收热量B.B→C过程中,气体分子的平均动能减小C.C→D过程中,单位时间内碰撞单位面积器壁的分子数减少D.D→A过程中,气体分子的速率分布曲线不发生变化7.一定质量的理想气体从状态A开始,经状态B和状态C回到状态A,其状态变化的p—T图象如图所示,其中线AB与OT轴平行,线段BC与Op轴平行。
第三章热力学第二定律

第三章热力学第二定律第三章 热力学第二定律(一)主要公式及其适用条件1、热机效率1211211/)(/)(/T T T Q Q Q Q W -=+=-=η式中:Q 1及Q 2分别为工质在循环过程中从高温热源T 1所吸收的热量和向低温热源T 2所放出的热量,W 为在循环过程中热机对环境所作的功。
此式适用于在两个不同温度的热源之间所进行的一切可逆循环。
2、卡诺定理的重要结论⎩⎨⎧<=+不可逆循环可逆循环,0,0//2211T Q T Q不论是何种工作物质以及在循环过程中发生何种变化,在指定的高、低温热源之间,一切要逆循环的热温商之和必等于零,一切不可逆循环的热温商之和必小于零。
3、熵的定义式TQ dS /d r def = 式中:r d Q 为可逆热,T 为可逆传热r d Q 时系统的温度。
此式适用于一切可逆过程熵变的计算。
4、克劳修斯不等式⎰⎩⎨⎧≥∆21)/d (可逆过程不可逆过程T Q S上式表明,可逆过程热温商的总和等于熵变,而不可逆过程热温商的总和必小于过程的熵变。
5、熵判据∆S (隔) = ∆S (系统) + ∆S (环境)⎩⎨⎧=>系统处于平衡态可逆过程能自动进行不可逆,,0,,0 此式适用于隔离系统。
只有隔离系统的总熵变才可人微言轻过程自动进行与平衡的判据。
在隔离系统一切可能自动进行的过程必然是向着熵增大的方向进行,绝不可能发生∆S (隔)<0的过程,这又被称为熵增原理。
6、熵变计算的主要公式⎰⎰⎰-=+==∆212121r d d d d d T p V H T V p U T Q S对于封闭系统,一切可逆过程的熵变计算式,皆可由上式导出。
(1)∆S = nC V ,m ln(T 2/T 1) + nR ln(V 2/V 1)= nC p,m ln(T 2/T 1) + nR ln(p 2/p 1)= nC V ,m ln(p 2/p 1) + nC p,m ln(V 2/V 1)上式适用于封闭系统、理想气体、C V ,m =常数、只有pVT 变化的一切过程。
大学物理 热力学第二定律 习题(附答案)

nc
B → C 为等体降温降压过程, 有
he .c
om
① ②
解: ( 1 )由 题意及 相图有 :空气 可视为 刚性双 原子分 子理想 气体, 总自由 度数为
为 10 5 kW 的动力厂每秒能生产多少千克 0 � C 的水。 ) (已知冰的比热容 c = 2.08 kJ/kg ⋅ � C ,冰的熔解热 l = 333.6 kJ/kg 。 解:(1)在这两个恒温热源之间工作的热机效率的理论极限是可逆卡诺循环的效率:
η = 1−
273 − 40 T2 =1- = 78. 3% 273 + 800 T1
(2)一座输出功率为 105 kW 的动力工厂 每秒钟热机需做功 A = 10 5 × 10 3 = 10 8 ( J ) 每秒传给冷源的热量 Q 2 =
设每秒钟有 M kg 的冰熔化成 0 � C 的冰,则有
M = [ c(T0 − T2 ) + l ] = Q2
解:根据热力学第二定律(P306)的开尔文表述和不可逆过程定义知(1)错(4)对,根据热 机效率公式知(2)对,根据热力学第二定律的克劳修斯表述知(3)错。 故选 A
om
∆Q < 0, T
故选 D
4.关于热功转换和热量传递过程,有下面一些叙述: (1) 功可以完全变为热量,而热量不能完全变为功 (2) 一切热机的效率都只能够小于 1 (3) 热量不能从低温物体向高温物体传递 (4) 热量从高温物体向低温物体传递是不可逆的 以上这些叙述 [ ] (A) 只有(2)、(4)正确 (B) 只有(2)、(3) 、(4)正确 (C) 只有(1)、(3) 、(4)正确 (D) 全部正确
T A = 1 − 2 ,得 B 错,C 错。 Q T1
热力学第二定律复习题

(注意:变温过程的计算只能用公式, ) (凝聚态间相变) (4) 恒压可逆相变化:;; Trouton规则: (注: :常压下(正常)沸点;Trouton规则对极性高的液体或在150K以 下沸腾的液体不适用。液体中若分子间存在氢键或存在缔合现象,此规 则亦不适用) 不可逆相变化:设计始、末态相同的可逆过程计算和。 (5) 纯物质两相平衡时 Tp关系及相变焓的计算: 任意两相平衡Tp关系: (Clapeyron方程) 对于凝聚相,当近似认为、与温度、压力无关时,上式的积分式为 用此式可以根据已知p1下的相变温度(如熔点)T1求另一压力p2下的相变 温度(如熔点)T2。 若平衡系统为或、且设、气体可视为理想气体时,相变温度与气相平
2.2.10熵判据 将熵增原理应用于绝热过程或隔离系统(隔离系统中 发生的任何过程当然是绝热过程)得熵判据: 不可逆过程 或 可逆过程或平衡态 不可能发生的过程 在使用熵判据时必须分别进行环境熵变()和系统熵变的计算,再利 用总熵变,即隔离系统熵变作为变化方向的判据。在考虑了环境熵变的 前提下,熵判据可以用于任何系统的任何过程,无论是否恒温、是否恒 压、是否有化学反应或相变化都没有限制,这是使用熵判据的方便之 处。 而实际过程往往是恒温、恒温恒容或恒温恒压过程。因此,为了方 便起见,在热力学中又引进了另外两个辅助函数——Gibbs函数和 Helmaolz函数,从而得到封闭系统恒温恒容、条件下使用的Helmaolz判 据和恒温恒压、条件下使用的Gibbs判据。 2.2.11亥姆霍兹函数 定义 该函数为状态函数,且为广度量,对一定量的物质其绝对值不知 道,只能求其改变值。单位为J。 亥姆霍兹函数的主要性质有: 即,在恒温时可逆过程中系统所做的功等于亥姆霍兹函数的变化 值。在恒温不可逆变化过程中功的数值将大于亥姆霍兹函数的变化值。 可以这样认为,在恒温可逆过程中,系统亥姆霍兹函数的减少值全 部转变为功交换给环境;而在不可逆过程,系统的亥姆霍兹函数的减少 值只有一部分转化为功交换给环境。 如果不仅恒温而且恒容,且无体积功交换 说明在恒温恒容时,可逆过程亥姆霍兹函数的变化与非体积功相 等,而发生不可逆过程时非体积功的数值将大于亥姆霍兹函数的变化。
物理化学上册第五版天津大学出版社第三章热力学第二定律习题答案

物理化学上册第五版天津大学出版社第三章热力学第二定律习题答案3-1 卡诺热机在 T 1=600K 的高温热源和T 2=300K 的低温热源间工作,求:(1) 热机的效率;(2)当环境作功 –W=100kJ 时,系统从高温热源Q 1及向低温热源放出的 –Q 2。
解:(1)5.0600/)300600(/)(/1211=-=-=-=T T T Q W η (2)5.0/100/11==-Q kJ Q W ,得kJ Q 2001=kJ W Q Q 10021=-=+;kJ Q W Q 100)(21=-=--3-2卡诺热机在T 1=795K 的高温热源和T 2=300K 的低温热源间工作,求:(1)热机的效率;(2)当从高温热源吸热Q 1=250 kJ 时,系统对环境作的功 -W 及向低温热源放出的 –Q 2。
解:(1)6.0750/)300750(/)(/1211=-=-=-=T T T Q W η (2)kJ kJ Q W 1502506.01=⨯==-ηkJ W Q Q 15021=-=+;kJ Q W Q 100)(21=-=--3-3 卡诺热机在T 1=900K 的高温热源和T 2=300K 的低温热源间工作,求:(1)热机的效率;(2)当向低温热源放出的 –Q 2=100kJ 时,从高温热源吸热Q 1及对环境作的功 -W 。
解:(1)6667.0900/)300900(/)(/1211=-=-=-=T T T Q W η (2)6667.0/1=-Q W (a )W kJ Q -=-1001(b )联立求解得:Q 1=300 kJ ;-W=200kJ3-4 试证明:在高温热源和低温热源间工作的不可逆热机与卡诺热机联合操作时,若令卡诺热机得到的功W r 等于不可逆热机作出的功 – W ,假设不可逆热机的热机效率η大于卡诺热机的热机效率ηr ,其结果必然有热量从低温热源流向高温热源,而违反热力学第二定律的克劳修斯说法。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第三章热力学第二定律一、选择题1、如图,可表示理想气体卡诺循环的示意图是:()(A) 图⑴ (B)图⑵ (C)图⑶(D) 图⑷2、工作在393K和293K的两个大热源间的卡诺热机,其效率约为()(A) 83%(B) 25%(C)100%(D) 20%3、不可逆循环过程中,体系的熵变值()(A) 大于零(B) 小于零(C)等于零(D)不能确4、将1 mol 甲苯在101.325 kPa,110 ℃(正常沸点)下与110 ℃的热源接触,使它向真空容器中汽化,完全变成101.325 kPa 下的蒸气。
该过程的:()(A) Δvap S m= 0 (B) Δvap G m= 0 (C) Δvap H m= 0 (D) Δvap U m= 05、1mol理想气体从300K,1×106Pa绝热向真空膨胀至1×105Pa,则该过程()(A)ΔS>0、ΔG>ΔA (B)ΔS<0、ΔG<ΔA(C)ΔS=0、ΔG=ΔA (D)ΔA<0、ΔG=ΔA6、对理想气体自由膨胀的绝热过程,下列关系中正确的是( )(A)ΔT>0、ΔU>0、ΔS>0(B)ΔT<0、ΔU<0、ΔS<0(C)ΔT=0、ΔU=0、ΔS=0 (D)ΔT=0、ΔU=0、ΔS>07、理想气体在等温可逆膨胀过程中( )(A)内能增加(B)熵不变(C)熵增加(D)内能减少8、根据熵的统计意义可以判断下列过程中何者的熵值增大?()(A) 水蒸气冷却成水(B) 石灰石分解生成石灰(C) 乙烯聚合成聚乙烯(D) 理想气体绝热可逆膨胀9、热力学第三定律可以表示为:()(A) 在0 K时,任何晶体的熵等于零(B) 在0 K时,任何完整晶体的熵等于零(C) 在0 ℃时,任何晶体的熵等于零(D) 在0 ℃时,任何完整晶体的熵等于零10、下列说法中错误的是( )(A)孤立体系中发生的任意过程总是向熵增加的方向进行(B)体系在可逆过程中的热温商的加和值是体系的熵变(C)不可逆过程的热温商之和小于熵变(D)体系发生某一变化时的熵变等于该过程的热温商11、两个体积相同,温度相等的球形容器中,装有同一种气体,当连接两容器的活塞打开时,熵变为( )(A)ΔS=0(B)ΔS>0 (C)ΔS<0 (D)无法判断12、下列过程中系统的熵减少的是( )(A)在900O C时CaCO3(s)→CaO(S)+CO2(g) (B)在0O C、常压下水结成冰(C)理想气体的恒温膨胀(D)水在其正常沸点气化13、水蒸汽在373K,101.3kPa下冷凝成水,则该过程( )(A)ΔS=0 (B)ΔA=0 (C)ΔH=0 (D)ΔG=014、1mol单原子理想气体在TK时经一等温可逆膨胀过程,则对于体系( )(A)ΔS=0、ΔH=0 (B)ΔS>0、ΔH=0 (C)ΔS<0、ΔH>0 (D)ΔS>0、ΔH>015、300K时5mol的理想气体由10dm3等温可逆膨胀到100dm3,则此过程的( )(A)ΔS<0;ΔU=0 (B)ΔS<0;ΔU<0(C)ΔS>0;ΔU>0 (D)ΔS>0;ΔU=016、某过冷液体凝结成同温度的固体,则该过程中( )(A)ΔS(环)<0 (B)ΔS(系)> 0(C)[ΔS(系)+ΔS(环)]<0 (D)[ΔS(系)+ΔS(环)]>017、100℃,1.013×105Pa下的1molH2O(l)与100℃的大热源相接触,使其向真空器皿中蒸发成100℃,1.013×105Pa的H2O(g),判断该过程的方向可用( )(A)ΔG (B)ΔS(系) (C)ΔS(总) (D)ΔA18、下列四个关系式中,哪一个不是麦克斯韦关系式? (A) (∂T/∂V)s=(∂T/∂V)p (B)(∂T/∂V)s=(∂T/∂V)p (C) (∂T/∂V)T=(∂T/∂V)v (D) (∂T/∂V)T= -(∂T/∂V)p19、25℃时,1 mol 理想气体等温膨胀,压力从 10 个标准压力变到1个标准压力,体系吉布斯自由能变化多少? ( )(A) 0.04 kJ (B) -12.4 kJ (C) 1.24 kJ (D) -5.70 KJ20、从热力学基本关系式可导出 (∂U/∂S)v 等于:( )(A) (∂H/∂S)p (B) (∂F/∂V)T (C) (∂U/∂V)s (D) (∂G/∂T)p21、1mol 某液体在其正常沸点完全汽化,则该过程( )(A)ΔS=0 (B)ΔH=0 (C)ΔA=0 (D)ΔG=022、对于不做非体积功的封闭体系,下面关系式中不正确的是:( )(A) (∂H/∂S)p = T (B) (∂F/∂T)v = -S (C) (∂H/∂p)s = V (D) (∂U/∂V)s = p23、热力学基本方程 d G = -S d T + V d p ,可适应用下列哪个过程:( )(A) 298K 、标准压力下,水气化成蒸汽 (B) 理想气体向真空膨胀(C) 电解水制取氢气 (D) N 2 + 3H 2 =2NH 3未达到平衡24、一个由气相变为凝聚相的化学反应在恒温恒容下自发进行,问下列各组答案中,哪一个是正确( )(A) ΔS 体>0,ΔS 环<0 (B)ΔS 体<0,ΔS 环>0 (C)ΔS 体<0,ΔS 环=0 (D)ΔS 体>0,ΔS 环=025、下列四种表述:(1) 等温等压下的可逆相变过程中,体系的熵变ΔS =ΔH 相变/T 相变;(2) 体系经历一自发过程总有 dS > 0 ;(3) 自发过程的方向就是混乱度增加的方向 ;(4) 在绝热可逆过程中,体系的熵变为零 ;两者都不正确者为:(A) (1),(2) (B)(3),(4) (C)(2),(3) (D)(1),(4)二、判断题1、不可逆过程一定是自发的,而自发过程一定是不可逆的。
( )2、对于绝热体系,可以用0≥∆S 判断过程的方向和限度。
( )3、在-10℃,101.325 kPa 下过冷的H 2O ( l )凝结为冰是一个不可逆过程,故此过程的熵变大于零。
( ) 4、功可以全部变成热,但热一定不能全部转化为功。
( )5、系统达平衡时熵值最大,自由能最小。
( )6、在绝热系统中,发生一个从状态A→B 的不可逆过程,不论用什么方法,系统再也回不到原来状态了。
( ) 7、因为⎰=∆B A R T Q S /δ,所以只有可逆过程才有熵变;而T Q S B A IR /∑>∆δ,所以不可逆过程只有热温商,但是没有熵变。
( ) 8、因为T Q S B A IR /∑>∆δ,所以体系由初态A 经不同的不可逆过程到达终态B,其熵的改变值各不相同。
( ) 9、物质的标准熵△S m θ(298K)值就是该状态下熵的绝对值。
( )10、可逆热机的效率最高,在其它条件相同的情况下,由可逆热机牵引火车,其速度将最慢。
( )三、计算题1、300K 的2mol 理想气体由6.0×105Pa 绝热自由膨胀到1.0×105Pa ,求过程的ΔU、ΔH、ΔS、ΔA、ΔG,并判断该过程的性质。
2、1mol 理想气体B ,在298.15K 下,由1.00dm 3膨胀至10.00dm 3,求该过程的ΔU、ΔH、ΔS、ΔA、ΔG。
3、1mol 水由始态273K ,1×105PaH 2O(l)变到终态473K ,3×105PaH 2O(g),计算该过程的ΔS。
已知水的正常沸点时的汽化热为40610J·mol -1,水的比热为4.18J·K -1·g -1,水蒸汽的比热为1.422J·g -1·K -1,假定水蒸汽为理想气体。
4、1mol 液态苯在101,3kPa ,268K 能自动地凝固成101,3kPa ,268K 的固态苯,并放热9874J ,计算该过程的ΔS 和ΔG。
已知苯的正常熔点为278.5K ,苯的熔化热为9916J·mol -1,C p ,m (C 7H 16,l)=126.8J·K -1·mol -1,C p ,m (C 7H 16,s)=122.6J·K -1·mol -1。
5、苯的正常沸点为353.1K ,在此温度压力下,1molC 6H 6(l)完全蒸发为蒸气,已知C 6H 6(l)的汽化热为34.7kJ·mol -1,计算此过程的W 、Q 、ΔU、ΔH、ΔS、ΔA、ΔG。
6、计算下列过程的ΔH、ΔS、ΔG。
298K ,101.325kPa H 2O(l)→473K,405.3kPa H 2O(g)已知:S m ø(298K ,H 2O ,l)=188.7 J·K -1 水的比热为4.18 J·g -1·K -1 水蒸气的比热为1.422 J·g -1·K -1 水在正常沸点时的汽化热为40610 J·mol -1。
假设水蒸气为理想气体。
7、2mol 理想气体在269K 时,由4×105Pa ,11.2dm 3绝热向真空膨胀到2×105Pa ,22.4dm 3,计算ΔS,是否能利用熵判据判断该过程的性质?如何判断?8、对于气相反应CO 2+H 2=H 2O+CO ,已知Δr G m ø=42218.0-7.57TlnT+1.9×10-2T 2-2.8×10-6T 3-2.26T(J),求上述反应在1000K 时的Δr H m ø、Δr S m ø9、1mol ,C p ,m =25.12J·K -1·mol -1的理想气体B 由始态340K ,500kPa 分别经(1)可逆绝热;(2)向真空膨胀。
两过程都达到体积增大一倍的终态,计算(1)、(2)两过程的ΔS。
10、计算将10克He(设为理想气体)从500.1K ,202.6KPa 变为500.1K ,1013kPa 的ΔU,ΔH,ΔS,ΔG,ΔA。
第三章 热力学第二定律答案一、选择题二、判断题 1 2 3 4 5 6 7 8 9 10 × × × × × √ × × × √ 三、计算题 1、解:ΔU=0,H=0 ΔS=nRln(V 2/V 1)=nRln(p 1/p 2)=29.8J·K -1ΔA=ΔU -TΔS=-8940JΔG=ΔH -TΔS=-8940J ∵ΔS(总)=ΔS(体)+ΔS(环)=29.8J·K -1>0且环境不对体系做功∴该过程是自发过程2、解:U=A(T) ΔU=0 H=A(T) ΔH=0 ΔS=Rln(V 2/V 1)=19.14J·K -1 ΔA=-TΔS=-5708J·mol -1 ΔG=-TΔS=-5708J·mol -13、解:ΔS 1=23.48J·K -1 ΔS 2=108.87J·K -1 ΔS 3=6.08J·K -1ΔS 4=nRln(p 1/p 2)=-9.13J·K -1 ΔS=ΔS 1+ΔS 2+ΔS 3+ΔS 4=129.3J·K -14、解:ΔS 1=nC p ,m (l)ln(278.8/268)=4.87J·K -1 ΔS 2=-nΔvap H m ø/T=-35.61J·K -1ΔS 3=nC p ,m (s)ln(268/278.5)=-4.71J·K -1 ΔS(总)=ΔS 1+ΔS 2+ΔS 3=-35.45J·K -1ΔH(268K)=-9874J ΔG(268K)=ΔH(268K)-TΔS=-373J5、解:设C 6H 6(g)为理气 W=RT=2.94kJ·mol -1 Q=ΔH=34.7kJ·mol -1 ΔU=Q -W=31.8kJ·mol -1 ΔS=ΔH/T=98.3J·K -1·mol -1 ΔG=0ΔA=ΔG -pΔV=-2.94kJ·mol -16解:ΔS=nC p ,m (H 2O ,l)ln(373.2/298.2)+nΔvap H m ø/373.2+ nC p ,m (H 2O ,g)ln(473.2/373.2)=126.84J·K -1 S m ø (473K ,H 2O ,g)=ΔS+S m ø (298K ,H 2O ,l)=315.5J·K -1·mol -1ΔH=ΔH 1+ΔH 2+ΔH 3+ΔH 4=48.81Kj ΔG=ΔH -(T 2S 2-T 1S 1)=-44.21kJ7、解:ΔS=nRln(V 2/V 1)=11.53J·K -1 能用熵判据判断该过程的性质ΔS(环)=-Q/T=0 ΔS(总)=ΔS(环)+ΔS(体)=11.53J·K -1∵ΔS(总)>0 且环境不对体系做功 ∴该过程为自发过程8、解:1000K 时,Δr G m ø=3456.9J 又∵(∂ΔG/∂T)p =-ΔS=-7.57-7.57lnT+1.9×10-2×2T -3×2.84×10-6T 2-2.26 ∴ΔS m ø=7.57+7.57lnT-3.8×10-2T+8.52×10-6T 2+2.26将T=1000K 代入上式即得ΔS m ø=33.39J·K -1·mol -1 ΔH m ø=ΔG m ø+TΔS m ø=36855.06J·mol -19、解:(1)由T 2=T 1(V 1/V 2)γ-1得T 2=270KΔS=C p ,m ln(T 2/T 1)+Rln(V 2/V 1)=0(2)T 2=340K ΔS=Rln(V 2/V 1)=5.76J·K -110、解:He 分子量4,10克即为2.5mol2.5 mol He 500.1K 202.6kPa→ 2.5 mol He 500.1K 1013kPa因为是理想气体,所以ΔU=0 ΔH=0 ΔS=nRTln(p 1/p 2)=2.5×8.314ln(202.6×103/1013×103)=-33.45 J/K·mol 题号 1 23 4 5 6 7 8 9 10 答案 C BC BD D C B B D 题号 11 12 13 14 15 16 17 18 19 20 答案 A B DB D DC AD A 题号 21 22 23 24 25 答案 D D B B CΔG=ΔH-T ΔS=0-500.1×(33.45) =1.673×104 J/ mol ΔA=ΔU-T ΔS=0-500.1×(33.45)=1.673×104 J/ mol 28解:设炉温与大气温度均不改变,则可用ΔS=Q 1/T 1+Q 2/T 2计算。
