差热分析法(DTA)
实验一差热分析一、目的意义差热分析(dta,differentialthermal

实验一 差热分析一、目的意义差热分析(DTA ,differentialthermal analysis)是研究相平衡与相变的动态方法中的一种,利用差热曲线的数据,工艺上可以确定材料的烧成制度及玻璃的转变与受控结晶等工艺参数,还可以对矿物进行定性、定量分析。
本实验的目的:1.了解差热分析的基本原理及仪器装置;2.学习使用差热分析方祛鉴定未知矿物。
二、基本原理差热分析的基本原理是:在程序控制温度下;将试样与参比物质在相同条件下加热或冷却,测量试样与参比物之间的温差与温度的关系,从而给出材料结构变化的相关信息。
物质在加热过程中,由于脱水,分解或相变等物理化学变化,经常会产生吸热或放热效应。
差热分析就是通过精确测定物质加热(或冷却)过程中伴随物理化学变化的同时产生热效应的大小以及产生热效应时所对应的温度,来达到对物质进行定性和/或定量分析的目的。
差热分析是把试样与参比物质(参比物质在整个实验温度范围内不应该有任何热效应,其导热系数,比热等物理参数尽可能与试样相同,亦称惰性物质或标准物质或中性物质)置于差热电偶的热端所对应的两个样品座内,在同一温度场中加热。
当试样加热过程中产生吸热或放热效应时,试样的温度就会低于或高于参比物质的温度,差热电偶的冷端就会输出相应的差热电势。
如果试样加热过程这中无热效应产生,则差热电势为零。
通过检流计偏转与否来检测差热电势的正负,就可推知是吸热或放热效应。
在与参比物质对应的热电偶的冷端连接上温度指示装置,就可检测出物质发生物理化学变化时所对应的温度.不同的物质,产生热效应的温度范围不同,差热曲线的形状亦不相同(如图16-2所示)。
把试样的差热曲线与相同实验条件下的已知物质的差热曲线作比较,就可以定性地确定试洋的矿物组成。
差热曲线的峰(谷)面积的大小与热效应的大小相对应,根据热效应的大小,可对试样作定量估计。
三.仪器设备与装置差热分析所用的设备主要由加热炉,差热电偶,样品座及差热信号和温度的显示仪表等所组成。
差热分析法(DTA)简介 (Differential Thermal Analysis)

差热分析法(DTA)简介(Differential Thermal Analysis)1.DTA的基本原理差热分析是在程序控制温度下,测量物质与参比物之间的温度差与温度关系的一种技术。
差热分析曲线是描述样品与参比物之间的温差(ΔT)随温度或时间的变化关系。
在DAT试验中,样品温度的变化是由于相转变或反应的吸热或放热效应引起的。
如:相转变,熔化,结晶结构的转变,沸腾,升华,蒸发,脱氢反应,断裂或分解反应,氧化或还原反应,晶格结构的破坏和其它化学反应。
一般说来,相转变、脱氢还原和一些分解反应产生吸热效应;而结晶、氧化和一些分解反应产生放热效应。
差热分析的原理如图Ⅱ-3-1所示。
将试样和参比物分别放入坩埚,置于炉中以一定速率进行程序升温,以表示各自的温度,设试样和参比物(包括容器、温差电偶等)的热容量Cs、Cr不随温度而变。
则它们的升温曲线如图Ⅱ-3-2所示。
若以对t作图,所得DTA曲线如图Ⅱ-3-3所示,在0-a区间,ΔT大体上是一致的,形成DTA曲线的基线。
随着温度的增加,试样产生了热效应(例如相转变),则与参比物间的温差变大,在DTA曲线中表现为峰。
显然,温差越大,峰也越大,试样发生变化的次数多,峰的数目也多,所以各种吸热和放热峰的个数、形状和位置与相应的温度可用来定性地鉴定所研究的物质,而峰面积与热量的变化有关。
图Ⅱ-3-1差热分析的原理图 II-3-1 差热分析的原理图图II-3-2试样和参比物的升温曲线1.参比物;2.试样;3.炉体;4.热电偶(包括吸热转变)图Ⅱ-3-3 DTA吸热转变曲线TA曲线所包围的面积S可用下式表示式中m是反应物的质量,ΔH是反应热,g是仪器的几何形态常数,C是样品的热传导率ΔT是温差,t1是DTA曲线的积分限。
这是一种最简单的表达式,它是通过运用比例或近似常数g和C来说明样品反应热与峰面积的关系。
这里忽略了微分项和样品的温度梯度,并假设峰面积与样品的比热无关,所以它是一个近似关系式。
差热分析法(DTA)简介 (Differential Thermal Analysis)

差热分析法(DTA)简介(Differential Thermal Analysis)1.DTA的基本原理差热分析是在程序控制温度下,测量物质与参比物之间的温度差与温度关系的一种技术。
差热分析曲线是描述样品与参比物之间的温差(ΔT)随温度或时间的变化关系。
在DAT试验中,样品温度的变化是由于相转变或反应的吸热或放热效应引起的。
如:相转变,熔化,结晶结构的转变,沸腾,升华,蒸发,脱氢反应,断裂或分解反应,氧化或还原反应,晶格结构的破坏和其它化学反应。
一般说来,相转变、脱氢还原和一些分解反应产生吸热效应;而结晶、氧化和一些分解反应产生放热效应。
差热分析的原理如图Ⅱ-3-1所示。
将试样和参比物分别放入坩埚,置于炉中以一定速率进行程序升温,以表示各自的温度,设试样和参比物(包括容器、温差电偶等)的热容量Cs、Cr不随温度而变。
则它们的升温曲线如图Ⅱ-3-2所示。
若以对t作图,所得DTA曲线如图Ⅱ-3-3所示,在0-a区间,ΔT大体上是一致的,形成DTA曲线的基线。
随着温度的增加,试样产生了热效应(例如相转变),则与参比物间的温差变大,在DTA曲线中表现为峰。
显然,温差越大,峰也越大,试样发生变化的次数多,峰的数目也多,所以各种吸热和放热峰的个数、形状和位置与相应的温度可用来定性地鉴定所研究的物质,而峰面积与热量的变化有关。
图Ⅱ-3-1差热分析的原理图 II-3-1 差热分析的原理图图II-3-2试样和参比物的升温曲线1.参比物;2.试样;3.炉体;4.热电偶(包括吸热转变)图Ⅱ-3-3 DTA吸热转变曲线TA曲线所包围的面积S可用下式表示式中m是反应物的质量,ΔH是反应热,g是仪器的几何形态常数,C是样品的热传导率ΔT是温差,t1是DTA曲线的积分限。
这是一种最简单的表达式,它是通过运用比例或近似常数g和C来说明样品反应热与峰面积的关系。
这里忽略了微分项和样品的温度梯度,并假设峰面积与样品的比热无关,所以它是一个近似关系式。
热分析法—热重分析法(TG) 差热分析法(DTA) 差示扫描量热法( DSC) ppt课件

of the first Na-containing i-QC, i-Na13Au12Ga15,
which belongs to the Bergman type but has an
extremely low valence electron-to-atom (e/a)
value of 1.75
PPT课件
800
1000
1200
140 780
180 205
1030
450
PPT课件Tຫໍສະໝຸດ ℃10差热分析法(DTA)
参比物:在测量温度范围 内不发生任何热效应的物 质,如-Al2O3、MgO等。
程序控温下, 测量物与参比 物的温差与温 度的关系 ΔT=f(T) 正峰:放热 倒峰:吸热
PPT课件
11
差示扫描量热法
PPT课件
21
亮点
金属氧化物薄层通常制备方法:原子层沉积、脉冲激 光沉积、化学气相沉积、射频溅射、喷墨印刷等方法。
本文—— “combustion” process in which the
heat required for oxide lattice formation is provided by the large internal energies of the precursors
PPT课件
22
略:XRD 、电子迁移率等测试。。。。
PPT课件
23
贰
PPT课件
24
《应用化学》(德语:Angewandte Chemie) 每周出版一期 由德国化学会出版,由约翰威立公司发行。
PPT课件
25
主要内容
we report the discovery and characterizations
聚合物的差热分析(DTA)和差动热分析(DSC)

实验 聚合物的差热分析(DTA )和差动热分析(DSC)一、实验目的1.了解聚合物差热分析(DTA)和差动热分析(DSC)的基本原理和应用,及相互间的差别。
2.初步掌握解释聚合物DTA 和DSC 热谱图的方法。
3.了解CDR-4P 差热分析仪的构造原理、基本操作。
4.熟练掌握使用CDR-4P 差热分析仪分别测量聚合物差热分析(DTA)和差动热分析(DSC)。
二、实验原理热分析是测量在受控程序温度条件下,物质的物理性能随温度变化的函数关系的一组技术。
目前热分析已经发展成为系统的分析方法,它对于材料的研究是一种极为有用的工具,特别是在高聚合物的分析测定方面应用更为广泛。
它不仅能获得结构方面的信息,而且还能测定性能,热分析仪已成为从事材料测试的实验室必备的仪器。
差热分析是测定试样在受热(或冷却)过程中,由于物理变化或化学变化所产生的热效应来研究物质转化及化学反应的一种分析方法,(即在程序温度下,测量物质与参比物的温度差值△T 与温度的函数关系。
△T 向上为放热反应,向下为吸热反应)简称DTA (Differential Thermal Analysis )。
可用于测定物质在热反应时的特征温度及吸热或放出的热量,包括物质相变、分解、化合、凝固、脱水、蒸发等,尤其在聚合物(如聚烯烃、玻璃钢等)的热分析方面有重要意义。
差动热分析(DSC) 也叫做示差扫描热量法(Differential Scanning Calorimetry ),是在程序温度下,测量物质与参比物的功率差值△W 与温度的函数关系。
是和DTA 在应用上相近而在原理上稍有改进的一种热分析技术。
差动热分析仪CDR-4P 用于测定物质在热反应时的特征温度及吸热或放出的热量,包括物质相变、分解、化合、凝固、脱水、蒸发等物理或化学反应,广泛应用于无机、硅酸盐、陶瓷、矿物金属、航天耐温材料等领域。
是无机、有机、特别是高分子聚合物、玻璃钢等方面热分析的重要仪器。
差热分析法
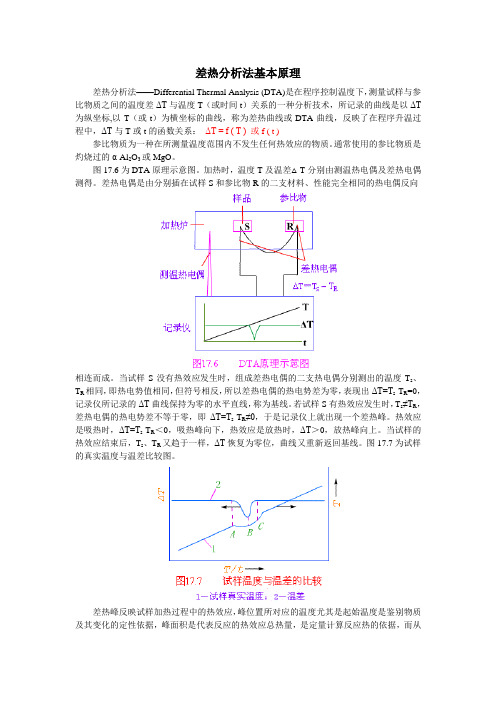
差热分析法基本原理差热分析法——Differential Thermal Analysis (DTA)是在程序控制温度下,测量试样与参比物质之间的温度差ΔT与温度T(或时间t)关系的一种分析技术,所记录的曲线是以ΔT 为纵坐标,以T(或t)为横坐标的曲线,称为差热曲线或DTA曲线,反映了在程序升温过程中,ΔT与T或t的函数关系:ΔT = f ( T ) 或f ( t )参比物质为一种在所测量温度范围内不发生任何热效应的物质。
通常使用的参比物质是灼烧过的α-Al2O3或MgO。
图17.6为DTA原理示意图。
加热时,温度T及温差△T分别由测温热电偶及差热电偶测得。
差热电偶是由分别插在试样S和参比物R的二支材料、性能完全相同的热电偶反向相连而成。
当试样S没有热效应发生时,组成差热电偶的二支热电偶分别测出的温度T s、T R相同,即热电势值相同,但符号相反,所以差热电偶的热电势差为零,表现出ΔT=T s-T R=0,记录仪所记录的ΔT曲线保持为零的水平直线,称为基线。
若试样S有热效应发生时,T s≠T R,差热电偶的热电势差不等于零,即ΔT=T s-T R≠0,于是记录仪上就出现一个差热峰。
热效应是吸热时,ΔT=T s-T R<0,吸热峰向下,热效应是放热时,ΔT>0,放热峰向上。
当试样的热效应结束后,T s、T R又趋于一样,ΔT恢复为零位,曲线又重新返回基线。
图17.7为试样的真实温度与温差比较图。
差热峰反映试样加热过程中的热效应,峰位置所对应的温度尤其是起始温度是鉴别物质及其变化的定性依据,峰面积是代表反应的热效应总热量,是定量计算反应热的依据,而从峰的形状(峰高、峰宽、对称性等)则可求得热反应的动力学参数。
表17.2列出了各种吸热和放热体系的类型,供判断差热峰产生机理时参考。
表17.2 差热分析中吸热和放热体系的主要类型现象(物理的原因)吸热放热现象(化学的原因)吸热放热结晶转变○○化学吸附○熔融○析出○气化○脱水○升华○分解○○吸附○氧化度降低○脱附○氧化(气体中)○吸收○还原(气体中)○氧化还原反应○○固相反应○○影响DTA的因素影响DTA的因素很多,下面讨论几种主要的因素:★升温速度的影响保持均匀的升温速度(ψ)是DTA的重要条件之一,即应:ψ = dT R / dt = 常数若升温速度不均匀(即ψ有波动),则DTA曲线的基线会漂移,影响多种参数测量。
热分析法—热重分析法(TG) 差热分析法(DTA) 差示扫描量热法( DSC)

热分析技术分类
测定的性质 质量
温度 热焓
挥发物 尺寸 电性质 光性质 磁性质
方法 热重分析法(TG)
微热重分析法(DTG) 差热分析法(DTA) 差示扫描量热法(DSC)
逸出气体分析法(EGA) 热膨胀法 热电法 热光法 热磁法
描述
程序控温下,测量物质的质量随温度的变 化 TG的基础上,利用计算机计算Δm-T的曲线 程序控温下,测量温度随程序温度的变化
TG,DTA,DSC曲线
相关文献 壹
JACS简介
Journal of the American Chemical Society 中文名:《美国化学会志》 化学杂志龙头 1879至今 134年历史
JACS简介
总引证次数和被引次数第一,远超第二 JACS每年有51期 JACS不收版面费,文章用彩色不加收费用 审稿周期10周。通讯是2个审稿人,全文是3个,全文审稿周期更长
IPS实质TFT
TFT:指薄膜晶体管,即每个液高速度、高亮度、高对比度, 最好的LCD彩色显示设备之一
文章内容: 金属氧化物半导体——耦合光透性、机械性能好、出色的电子性能。
TFT performance of many oxides exceeds that of amorphous silicon (a-Si:H), and their stability rivals or exceeds that of typical organic semiconductors
发展历史
1964年—— Watson等研制出可定量测量热量的差示扫描量热计,试样用量 为mg级。Mazieres研制的微量差热分析仪的试样量达到了10-100ug。 近十年来——热分析仪器与其他分析仪器的联用技术也发展很快,出现了 TG-MS、TG-GC、DTA-MS、TG-TGA等联用仪器,既节省试样用量又同时 获得更多的信息。
差热分析(DTA)
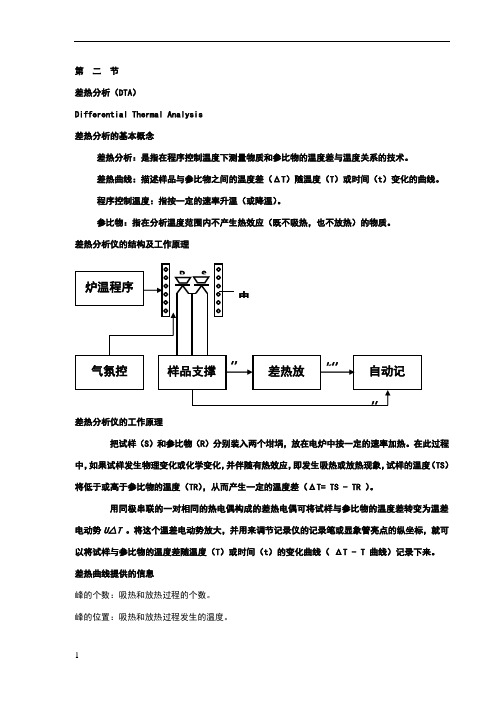
第二节差热分析(DTA)Differential Thermal Analysis差热分析的基本概念差热分析:是指在程序控制温度下测量物质和参比物的温度差与温度关系的技术。
差热曲线:描述样品与参比物之间的温度差(ΔT)随温度(T)或时间(t)变化的曲线。
程序控制温度:指按一定的速率升温(或降温)。
参比物:指在分析温度范围内不产生热效应(既不吸热,也不放热)的物质。
差热分析仪的结构及工作原理差热分析仪的工作原理把试样(S)和参比物(R)分别装入两个坩埚,放在电炉中按一定的速率加热。
在此过程中,如果试样发生物理变化或化学变化,并伴随有热效应,即发生吸热或放热现象,试样的温度(TS)将低于或高于参比物的温度(TR),从而产生一定的温度差(ΔT= TS - TR )。
用同极串联的一对相同的热电偶构成的差热电偶可将试样与参比物的温度差转变为温差电动势U△T 。
将这个温差电动势放大,并用来调节记录仪的记录笔或显象管亮点的纵坐标,就可以将试样与参比物的温度差随温度(T)或时间(t)的变化曲线(ΔT - T 曲线)记录下来。
差热曲线提供的信息峰的个数:吸热和放热过程的个数。
峰的位置:吸热和放热过程发生的温度。
峰的性质:向上,放热;向下,吸热。
峰的形状:热反应的速率。
峰的面积:吸收或释放的热量的多少。
基线的位置:样品与参比物的比热关系。
基线的长度:物质稳定存在的温度区间。
峰的面积与吸收或释放的热量的关系 峰的面积与吸收或释放的热量成正比。
式中, A 是吸热峰或放热峰的面积;ma 是试样中反应物的质量;ΔH 是单位反应物吸收或释放的热量,即单位反应物的焓变;g 是与仪器有关的系数; λs 是试样热导率。
利用Speil 公式,可以根据峰的面积求得反应过程中的焓变和反应物质的量。
ΔH= g λs A/ ma ma= A g λs / ΔH基线的位置与样品和参比物的比热关系 CR —参比物的比热 CS —试样的比热 V —升温速率 k —比例常数加热过程中会产生吸热或放热效应的各种物理化学过程Sa t t a g H m dt T T A λ∆=∆-∆=⎰21])([V kC C T SR a -=∆)(脱水作用—吸热• 自由水:存在于物质颗粒表面或微型裂隙中的水,110℃以下脱出。
差热分析法

差热分析法差热分析法(Differential Thermal Analysis,DTA)是一种常用的热分析技术,它通过比较样品与参比物的温度差异来研究样品的热性质。
DTA技术在化学、材料科学、地质学等多个领域具有广泛的应用。
DTA的工作原理基于样品和参比物在受热过程中吸收或释放热量的差异。
在实验中,样品和参比物被放置在两个相邻的炉区,受同等程度的升温条件控制。
当样品发生物理或化学变化时,其吸热或放热会导致样品与参比物温度的差异。
这些温度差异会通过一个差温探测器进行检测和记录。
DTA实验中,样品和参比物通常以粉末或粒状形式存在。
粉末样品可在合适的容器中进行测试,而固体样品则需先研磨成粉末以方便测试。
样品和参比物应具有相似的物理和化学性质,以确保实验的准确性和可靠性。
在DTA实验中,通常以升温速率为X轴,差温信号(样品与参比物温度差异)为Y轴来绘制曲线图。
曲线上出现的峰或谷表示样品发生了热事件,如相变、化学反应、放热或吸热过程等。
通过对峰的位置、峰的形状和峰的峰值进行分析,可以获得有关样品的热性质和热行为的信息。
DTA技术广泛应用于材料研究、催化剂研究、岩石和土壤分析、陶瓷研究等领域。
它可以用于研究材料的熔化过程、晶体相变、氧化、还原、析出和溶解等反应。
同时,DTA还可以用来测定热容、热导率、热膨胀系数等热性质参数。
通过结合其他热分析技术,如差热/差热衍生物分析(DTA/DSC)和差热差热衍生物重量分析(DTA/TGA),可以对样品进行更全面和深入的分析。
总之,差热分析法是一种用于研究样品热性质和热行为的重要工具。
它通过比较样品与参比物的温度差异,可以揭示样品发生的热事件和热特性,为材料研究和过程分析提供了有力的支持。
差热分析(DTA)

第 二 节差热分析(DTA )Differential Thermal Analysis 差热分析的基本概念差热分析:是指在程序控制温度下测量物质和参比物的温度差与温度关系的技术。
差热曲线:描述样品与参比物之间的温度差(ΔT )随温度(T )或时间(t )变化的曲线。
程序控制温度:指按一定的速率升温(或降温)。
参比物:指在分析温度范围内不产生热效应(既不吸热,也不放热)的物质。
差热分析仪的结构及工作原理差热分析仪的工作原理 把试样(S )和参比物(R )分别装入两个坩埚,放在电炉中按一定的速率加热。
在此过程中,如果试样发生物理变化或化学变化,并伴随有热效应,即发生吸热或放热现象,试样的温度(TS )将低于或高于参比物的温度(TR ),从而产生一定的温度差(ΔT= TS - TR )。
用同极串联的一对相同的热电偶构成的差热电偶可将试样与参比物的温度差转变为温差电动势U △T 。
将这个温差电动势放大,并用来调节记录仪的记录笔或显象管亮点的纵坐标,就可以将试样与参比物的温度差随温度(T )或时间(t )的变化曲线( ΔT - T 曲线)记录下来。
差热曲线提供的信息峰的个数:吸热和放热过程的个数。
峰的位置:吸热和放热过程发生的温度。
峰的性质:向上,放热;向下,吸热。
峰的形状:热反应的速率。
峰的面积:吸收或释放的热量的多少。
基线的位置:样品与参比物的比热关系。
基线的长度:物质稳定存在的温度区间。
峰的面积与吸收或释放的热量的关系 峰的面积与吸收或释放的热量成正比。
式中, A 是吸热峰或放热峰的面积;ma 是试样中反应物的质量;ΔH 是单位反应物吸收或释放的热量,即单位反应物的焓变;g 是与仪器有关的系数; λs 是试样热导率。
利用Speil 公式,可以根据峰的面积求得反应过程中的焓变和反应物质的量。
ΔH= g λs A/ ma ma= A g λs / ΔHSa t t a g H m dt T T A λ∆=∆-∆=⎰21])([C C SR -基线的位置与样品和参比物的比热关系 CR —参比物的比热 CS —试样的比热 V —升温速率 k —比例常数加热过程中会产生吸热或放热效应的各种物理化学过程脱水作用—吸热• 自由水:存在于物质颗粒表面或微型裂隙中的水,110℃以下脱出。
差热分析法(DTA)

6.3.1 基本原理
2012-3-8
5
6.3.2 差热曲线方程
为了对差热曲线进行理论上的分析, 为了对差热曲线进行理论上的分析 , 从 60年代起就开始进行分析探讨 , 但由于 年代起就开始进行分析探讨, 年代起就开始进行分析探讨 考虑的影响因素太多, 考虑的影响因素太多 , 以致于所建立的 理论模型十分复杂,难以使用。 理论模型十分复杂,难以使用。 1975年 , 神户博太郎对差热曲线提出了 年 一个理论解析的数学方程式, 一个理论解析的数学方程式 , 该方程能 够十分简便的阐述差热曲线所反映的热 力学过程和各种影响因素。 力学过程和各种影响因素。
2012-3-8 16
(二)
CS
在反应终点C, 反应终点 ,
d∆H = 0 dt
K ln (∆Tc − ∆Ta ) = − t CS
d∆T dt
= − K [∆T − ∆Ta ]
K ∆Tc = exp− CS
t + ∆Ta
(6 − 9)
反应终点C以后, 将按指数函数衰减直至 反应终点 以后,∆T将按指数函数衰减直至 以后 ∆T 基线) 2012-3-8 a(基线)
2012-3-8 20
6.3.3 差热分析仪
差热分析仪的组成
加热炉 温差检测器 温度程序控制仪 信号放大器 记录仪 气氛控制设备
2012-3-8 21
6.3.4 差热分析的影响因素
1. 仪器因素: 仪器因素: 炉子的形状结构与尺寸, 炉子的形状结构与尺寸,坩埚材料与 形状, 形状,热电偶位置与性能 2. 实验条件因素: 实验条件因素: 升温速率、 升温速率、气氛 3. 试样因素: 试样因素: 用量、 用量、粒度
2012-3-8 22
差热分析(Differencial Thermal Analysis, DTA)

差热分析的应用
提供的信息:
峰的位置 峰的形状 峰的个数
凝胶材料的烧结进程研究
DTA数据的记录方式
6)用时间或温度作为横坐标,从左到右为增加。 7)说明鉴定中间生成物和最后产物的方法。8)全部 原始记录的如实重复。 9)标明试样重量和试样稀释程度。 11)标明所用仪器的型号、商品名称及热电偶的几何 形状、材料和位置。
影响曲线形状的因素
• 影响差热分析的主要因素有三个方面:仪
DTA曲线及理论分析
DTA曲线
DTA曲线是指试样与参比物间的温差(ΔT) 曲线和温度(T)曲线的总称。
DTA曲线分析
① 零线:理想状态ΔT=0的线; ② 基线:实际条件下试样无热效应时的曲线部份; ③ 吸热峰:TS<TR ,ΔT<0时的曲线部份; ④ 放热峰:TS>TR , ΔT>0时的曲线部份; ⑤ 起始温度(Ti):热效应发生时曲线开始偏离基线的 温度; ⑥ 终止温度(Tf):曲线开始回到基线的温度;
稀释 剂的 加入 往往 会降 低差 热分 析的 灵敏
度!
差热曲线分析
差热曲线分析就是解释曲线上每个峰谷产生的原因,从 而分析被测物质是有那些物相组成的。峰谷产生的原因 有:
✓矿物质脱水 ✓相变 ✓物质的化合或分解 ✓氧化还原
差热分析的峰只表示试样的热效应,本身不反应更多 的物理化学本质。为此,单靠差热曲线很难做正确的解 释。现在普遍采用的联用技术。
✓ 如:在空气和氢气的气氛下
对镍催化剂进行差热分析, 所得到的结果截然不同(见 图)。在空气中镍催化剂被 氧化而产生放热峰。
稀释剂的影响
稀释剂是指在试样 中加入一种与试样不 发生任何反应的惰性 物质,常常是参比物 质。稀释剂的加入使 样品与参比物的热容 相近,能有助于改善 基线的稳定性,提高 检出灵敏度,但同时 也会降低峰的面积。
差热分析dta实验报告

差热分析dta实验报告引言差热分析(Differential Thermal Analysis, DTA)是一种常用的热分析技术,用于研究物质的热性质和相变行为。
本实验旨在通过DTA技术,对样品进行加热或冷却过程中的温度变化进行监测,并观察样品中可能存在的热性质和相变点。
实验方法实验仪器和试剂本次实验所使用的仪器为差热分析仪(DTA),试剂为待测试样品。
实验步骤1. 准备样品:将待测试样品准备成适当的形状和大小,确保样品的质量在仪器所能接受的范围之内。
2. 样品装填:将样品置于DTA仪器的样品台上,并确保样品与台面接触良好,以保证传热效果。
3. 设定实验条件:根据样品的性质和研究目的,设置合适的加热速率、升温范围和冷却速率。
4. 开始实验:启动DTA仪器,开始进行样品的加热或冷却处理。
5. 数据记录:在实验过程中,实时记录样品的温度变化情况。
6. 数据分析:利用DTA仪器的数据处理软件,对实验数据进行分析,获取样品的热性质和相变点。
实验结果与分析我们选择了一种未知样品进行差热分析实验,结果如下图所示:从实验结果图中可以看出,在样品加热过程中,出现了两个峰值,分别对应着两个不同的相变点。
根据峰值的温度和形状,可以初步判断样品可能存在的相变类型。
对于第一个峰值,其温度在600C左右,呈现出一个尖峰状,说明样品可能发生了固态相变。
根据不同物质的热性质,可以进一步判断该固态相变可能是晶体结构的变化或者晶格缺陷的形成等。
第二个峰值出现在800C左右,温度范围较宽,且峰值相对较平,表明该相变可能为液固相变或者化学反应等。
进一步的分析还需要结合实际的样品性质和反应条件,进行详细的比较和判断。
结论通过差热分析(DTA)实验,我们得到了待测试样品的热性质和相变点的初步信息。
根据实验结果分析,样品可能存在两个不同的相变类型,其中一个为固态相变,另一个为液固相变或者化学反应。
dta差示热分析法

DTA差示热分析法(Differential Thermal Analysis)是一种常用的物理分析方法,用于测定物质在加热过程中发生的热反应。
它通过比较样品与标准物质在相同加热条件下所产生的热量差来测定样品的热性质。
DTA差示热分析仪由加热装置、热量计、控温装置和计算机等组成。
在测定时,样品与标准物质分别放在不同的热量计内,并在加热装置的控制下加热。
根据样品与标准物质的热量差的变化,可以推断出样品在加热过程中发生的热反应。
DTA差示热分析法具有许多优点,例如测定精度高、结果可靠、操作简单等。
它常用于研究物质的热稳定性、热解、热氧化、热转化和热再结晶等方面。
在化工、冶金、材料、环境等领域都有广泛的应用。
DTA差示热分析法的原理是基于热力学第二定律,即在物质发生热反应时,会产生热量。
通过测定样品与标准物质的热量差的变化,可以推断出样品在加热过程中发生的热反应。
DTA差示热分析法的测定结果可以用温度-热量曲线表示。
在温度-热量曲线上,当样品发生热反应时,会出现热量差的陡峭变化,这就是所谓的热峰。
热峰的高度、宽度和位置可以反映样品的热性质。
DTA差示热分析法的操作过程也比较简单。
首先,将样品与标准物质分别放入不同的热量计内。
然后,设定加热温度和加热速率,并启动加热装置。
根据样品与标准物质的热量差的变化,计算机会自动记录温度-热量曲线。
DTA差示热分析法在研究物质的热性质方面有着广泛的应用。
例如,可以用它来测定物质的热稳定性,即物质在加热过程中是否会产生不稳定的热反应。
示差热分析(DTA)的定义

示差热分析(DTA)的定义•A technique in which the difference in temperature between the sample and a reference material is monitored against time or temperature while the temperature of the sample, in a specified atmosphere, is programmed.在一定的温度程序下,测量样品和参比物温度差与温度关系的技术。
ICTAC发行的“For Better Thermal Analysis and Calorimetry” 和JIS K 0129“热分析通则”对DTA 的定义如上所述。
DTA是检测试料与参比物质间温度差,伴随着温度变化的技术。
例如,试料发生融解或发生反应时,检测其与基准物质间的温度差。
【示差热分析(DTA)的解说】图1 示差热分析(DTA)的装置结构(参比物样品示差热电耦 加热炉样品温度T温度差 ΔT)DTA的装置结构如上图所示。
将试料和基准物质设置在加热炉内的对称位置上,根据温度程序控制加热炉,改变试料与基准物质的温度。
并如上图所示 通过热电耦检测试料与基准物质的温度差ΔT。
图2 示差热分析(DTA)的测量原理热炉参比物样品 样品融解开始放热反应 样品融解 吸热反应 温度的时间变化 温度差的时间变化) 检测的温度差(ΔT)随时间的变化。
T的信号被称为DTA 信号。
为参比物质,通常是指在测量温度范围的没有变化的物质(一般使用α-氧化铝)。
是指 从开始升温后到平稳状态以后样品与参比物的热容量的差。
通常把这个平稳状态的信号称做基线。
)可以检测出试料的转移温度和反应温度。
如(b)所示,吸热温度差取负方向,放热温度差取正方向。
(加上图所示是DTA 的测量原理。
(a)所示的是相对于时间的加热炉、基准物质、以及试料的温度。
差热分析法(DTA)简介(DifferentialThermalAnalysis)

差热分析法(DTA)简介(DifferentialThermalAnalysis)差热分析法(DTA)简介(Differential Thermal Analysis)1.DTA的基本原理差热分析是在程序控制温度下,测量物质与参⽐物之间的温度差与温度关系的⼀种技术。
差热分析曲线是描述样品与参⽐物之间的温差(ΔT)随温度或时间的变化关系。
在DAT试验中,样品温度的变化是由于相转变或反应的吸热或放热效应引起的。
如:相转变,熔化,结晶结构的转变,沸腾,升华,蒸发,脱氢反应,断裂或分解反应,氧化或还原反应,晶格结构的破坏和其它化学反应。
⼀般说来,相转变、脱氢还原和⼀些分解反应产⽣吸热效应;⽽结晶、氧化和⼀些分解反应产⽣放热效应。
差热分析的原理如图Ⅱ-3-1所⽰。
将试样和参⽐物分别放⼊坩埚,置于炉中以⼀定速率进⾏程序升温,以表⽰各⾃的温度,设试样和参⽐物(包括容器、温差电偶等)的热容量Cs、Cr不随温度⽽变。
则它们的升温曲线如图Ⅱ-3-2所⽰。
若以对t作图,所得DTA曲线如图Ⅱ-3-3所⽰,在0-a区间,ΔT⼤体上是⼀致的,形成DTA曲线的基线。
随着温度的增加,试样产⽣了热效应(例如相转变),则与参⽐物间的温差变⼤,在DTA曲线中表现为峰。
显然,温差越⼤,峰也越⼤,试样发⽣变化的次数多,峰的数⽬也多,所以各种吸热和放热峰的个数、形状和位置与相应的温度可⽤来定性地鉴定所研究的物质,⽽峰⾯积与热量的变化有关。
图Ⅱ-3-1差热分析的原理图 II-3-1 差热分析的原理图图II-3-2试样和参⽐物的升温曲线1.参⽐物;2.试样;3.炉体;4.热电偶(包括吸热转变)图Ⅱ-3-3 DTA吸热转变曲线TA曲线所包围的⾯积S可⽤下式表⽰式中m是反应物的质量,ΔH是反应热,g是仪器的⼏何形态常数,C是样品的热传导率ΔT是温差,t1是DTA曲线的积分限。
这是⼀种最简单的表达式,它是通过运⽤⽐例或近似常数g和C来说明样品反应热与峰⾯积的关系。
差热分析(DTA)

差热分析(DTA)
差热分析(DTA)是一种热分析技术,可以通过比较样品和参考样品之间的温度差异来揭示样品的热性能信息。
DTA通常被用于材料的热稳定性、相变温度、焓变化、重量变化等方面的研究。
DTA技术的基本原理是利用热电偶,将样品和参考样品置于同一热环境下,在恒定加热速率下,通过比较两个样品表面的温度差异来监测样品和参考样品之间的热流量差异。
当样品和参考样品中的物质发生热反应或相变时,会引起温度差异,从而在DTA曲线上观察到一个突变点或峰值,可以通过对曲线的分析来确定相变温度、焓变化等信息。
DTA技术在材料学、矿物学、化学、生物学等领域都有广泛的应用。
例如,可以通过DTA技术研究陶瓷的烧结温度、合金的相变温度、聚合物的热稳定性和分解温度、药物的热性质、生化反应中的热效应等等。
此外,DTA技术还可以与其他热分析技术如热重分析(TGA)和差热扫描量热分析(DSC)等相结合,进一步深入研究物质的热性能和物化性质。
在进行DTA分析时,需要注意以下几个方面:首先,样品和参考样品的配比应合适,以确保在热分析过程中二者之间的温度差异是合理的。
其次,选取合适的热分析条件如加热速率、加热温度范围等,以使观测到的热反应信号清晰明确。
最后,分析DTA曲线时,需要结合其他测试方法和材料性质了解样品的具体属性,避免出现误判。
总之,差热分析是一种重要的热分析技术,广泛应用于物质性质的研究和测试中。
在今后的研究中,DTA技术还将进一步发展和完善,支持更广泛、更具有实际意义的应用。
热重分析及差热分析

? 试样S与参比物 R分别装在两个坩埚内。在坩埚 下面各有一个片状热电偶,这两个热电偶相互反 接。对 S和R同时进行程序升温,当加热到某一温 度试样发生放热或吸热时,试样的温度 TS会高于 或低于参比物温度 TR产生温度差△ T,该温度差 就由上述两个反接的热电偶以差热电势形式输给 差热放大器,经放大后输入记录仪,得到差热曲 线,即DTA 曲线。
8)差热分析
DTA 8.电学特 16)热电学法 性
9.磁学特 17)热磁学法 性
热分析应用类型
1、成份分析 :无机物、有机物、药物和高聚物的鉴别和分 析以及它们的相图研究。
2、稳定性测定:物质的热稳定性、抗氧化性能的测定等。 3、化学反应的研究 :比如固 -气反应研究、催化性能测定、
反应动力学研究、反应热测定、相变和结晶过程研究。 4、材料质量测定 :如纯度测定、物质的玻璃化转变和居里
m = f ( T或t )
热重分析法 包括静态法和动态法两种类型
? 静态法又分等压质量变化测定和等温质量变化测定两种。 ? 等压质量变化测定又称自发气氛热重分析,是在程序控制
温度下,测量物质在恒定挥发物分压下平衡质量与温度关 系的一种方法。该方法利用试样分解的挥发产物所形成的 气体作为气氛,并控制在恒定的大气压下测量质量随温度 的变化,其特点就是可减少热分解过程中氧化过程的干扰 。等温质量变化测定 是指在恒温条件下测量物质质量与温 度关系的一种方法。该法每隔一定温度间隔将物质恒温至 恒重,记录恒温恒重关系曲线。
物质在温度变化过程中,常常伴随 宏观物理、化学 等 性质的变化,宏观上的这些性质变化通常又与物质的组成 和微观结构相关联。通过测量和分析物质在加热或冷却过 程中的物理、化学性质的变化,可以对物质进行 定性、定 量分析,从而实现对物质的结构鉴定,为新材料的研究和 开发提供热性能数据和精细结构信息。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
❖ 吸热峰、放热峰
❖ 峰宽:离开基线后又返回 基线之间的温度间隔(或时 间间隔)(B’D’)。
❖ 峰高:垂直于温度(或时间) 轴的峰顶到内切基线之距 离(CF)。
❖ 峰面积:峰与内切基线所 围之面积(BCDB)。
❖ 外推起始点(出峰点):峰 前沿最大斜率点切线与基
(6 10)
由于差热曲线从反应终 点c返回到基线的积分
表达式可表示为 :
Cs[Tc Ta ] K c [T Ta ]dt
(6 11)
c
H
K
[T
a
Ta ]dt K
c
[T
Ta ]dt
K a [T Ta ]dt KS
(6 12)
S:差热曲线和基线之间的面积
12.08.2020
精品课件
12.08.2020
精品课件
20
6.3.3 差热分析仪
差热分析仪的组成
加热炉
温差检测器
温度程序控制仪
信号放大器
记录仪
气氛控制设备
12.08.2020
精品课件
21
6.3.4 差热分析的影响因素
1. 仪器因素: 炉子的形状结构与尺寸,坩埚
材料与形状,热电偶位置与性能 2. 实验条件因素:
dT
在峰顶b点处,
0
dt
d dHt KTbTa
1d H T b T aK dt
(68)
➢ 峰高(ΔTb-ΔTa)与导热系数K成反比,K越 小,峰越高、尖,(峰面积几乎不变,因 反应焓变化量为定值)。因此可通过降低K 值来提高差热分析的灵敏度。
12.08.2020
精品课件
16
(二) 在反应终点C, dH 0
12.08.2020
精品课件
6
假
设:
❖试样S和参比物R放在同一加热的金属块W 中,使之处于同样的热力学条件之下。
➢1. 试样和参比物的温度分布均匀(无温 度梯度),且与各自的坩埚温度相同。
➢2. 试样、参比物的热容量CS、CR不随温 度变化。
➢3. 试样、参比物与金属块之间的热传导 和温差成正比,比例常数(传热系数)K 与温度无关。
12.08.2020
精品课件
1
✓ 差热曲线是由差热分析得到的记录曲线。纵坐标 是试样与参比物的温度差ΔT,向上表示放热反 应,向下表示吸热反应,横坐标为T(或t)。
12.08.2020
精品课件
2
DTA曲线术语
12.08.2020
典型的精品D课T件A曲线
3
12.08.2020
❖ 基线:ΔT 近似于0的 区段 (AB,DE段)。
12
TaC RK C S
(62)
✓ 1)程序升温速率Φ恒定才能获得稳定的 基线;
✓ 2)CR与CS越相近,ΔTa越小,因此试样 和参比物应选用化学上相似的物质;
✓ 3)升温过程中,若试样的比热有变化, ΔTa也发生变化,因此DTA曲线可以反映 出试样比热变化;
✓ 4)升温速率Φ值越小,ΔTa也越小。
Ta
CR CS K
精品课件
C Rd dRT tC Sd dRT tK T a (65)
C Sd dRT tK T W T R K T a (6 6 )
式3-式6,得:
C Sd d T td d H tK T T a (6 7 )
12.08.2020
精品课件
15
(一)
精品课件 线延长线的交点(G)。 4
6.3.1 基本原理
12.08.2020
精品课件
5
6.3.2 差热曲线方程
➢为了对差热曲线进行理论上的分析,从 60年代起就开始进行分析探讨,但由于 考虑的影响因素太多,以致于所建立的 理论模型十分复杂,难以使用。
➢1975年,神户博太郎对差热曲线提出了 一个理论解析的数学方程式,该方程能 够十分简便的阐述差热曲线所反映的热 力学过程和各种影响因素。
19
根据式(6-12)可得出下述结论:
❖1.差热曲线的峰面积S和反应热效应ΔH 成正比;
❖2.传热系数K值越小,对于相同的反应热 效应ΔH来讲,峰面积S值越大,灵敏度 越高。
(6-12)式中没有涉及程序升温速率φ, 即升温速率φ不管怎样,S值总是一定的。 由于ΔT和φ成正比,所以φ值越大峰形 越窄越高。
dt
CSd dTtKTTa
lnTcTaCKS t
TcexpC K StTa (69)
✓ Δ.202T0 a(基线)
精品课件
17
12.08.2020
精品课件
18
(三) 将(6-7)式积分整理后得到
c
H
Cs[Tc Ta ] K
[T
a
Ta ]dt
12.08.2020
精品课件
10
o-a之间是DTA基线形成过程
12.08.2020
精品课件
11
此过程中ΔT的变化可用下列方程描述:
Δ T C RK C S 1ex p c K st
(61 )
当t足够大时,可得基线的位置:
TaC RK C S
(62)
12.08.2020
精品课件
12.08.2020
精品课件
13
基线形成后继续升温,如果试样发生了吸热 变化,此时试样总的热流率为:
C Sd d S T tK T W T S d d H t
ΔH:试样全部熔化的总吸热量
(6 3 )
参比物总热流率 C RddRT tKTWTR (64)
dTW dTR
dt dt
12.08.2020
12.08.2020
精品课件
7
设Tw为金属块温度,即炉温
程序升温速率 : dT w
dt
当t=0时,TS=TR=Tw
12.08.2020
精品课件
8
12.08.2020
精品课件
9
❖ 差热分析时,炉温Tw以φ开始升温,由 于存在热阻,TS、TR均滞后于Tw,经过一 段时间以后,两者才以φ升温。
❖ 升温过程中,由于试样与参比物的热容 量不同(Cs≠CR)它们对Tw的温度滞后并 不同(热容大的滞后时间长),这样试 样和参比物之间产生温差△T。当它们的 热容量差被热传导自动补偿以后,试样 和参比物才按照程序升温速度φ升温。 此时△T成为定值△Ta,从而形成了差热 曲线的基线。
6.3 差热分析法(DTA)
( Differential Thermal Analysis)
❖定义:在程序控制温度下,测量物质和 参比物之间的温度差与温度关系的一种
技术。
❖当试样发生任何物理(如相转变、熔化、 结晶、升华等)或化学变化时,所释放 或吸收的热量使试样温度高于或低于参 比物的温度,从而相应地在DTA曲线上得 到放热或吸收峰。
