有机人名反应
有机化学人名反应大全

一、Arbuzov 反应亚磷酸三烷基酯作为亲核试剂与卤代烷作用,生成烷基膦酸二烷基酯和一个新的卤代烷:卤代烷反应时,其活性次序为:R′I >R′Br >R′Cl。
除了卤代烷外,烯丙型或炔丙型卤化物、a-卤代醚、a- 或 b-卤代酸酯、对甲苯磺酸酯等也可以进行反应。
当亚酸三烷基酯中三个烷基各不相同时,总是先脱除含碳原子数最少的基团。
本反应是由醇制备卤代烷的很好方法,因为亚磷酸三烷基酯可以由醇与三氯化磷反应制得:如果反应所用的卤代烷 R'X 的烷基和亚磷酸三烷基酯 (RO)3P 的烷基相同(即 R' = R),则Arbuzov 反应如下:这是制备烷基膦酸酯的常用方法。
除了亚磷酸三烷基酯外,亚膦酸酯 RP(OR')2和次亚膦酸酯 R2POR' 也能发生该类反应,例如:反应机理2 进行的分子内重排反应:一般认为是按 SN反应实例二、Arndt-Eister 反应酰氯与重氮甲烷反应,然后在氧化银催化下与水共热得到酸。
反应机理重氮甲烷与酰氯反应首先形成重氮酮(1),(1)在氧化银催化下与水共热,得到酰基卡宾(2),(2)发生重排得烯酮(3),(3)与水反应生成酸,若与醇或氨(胺)反应,则得酯或酰胺。
反应实例三、Baeyer----Villiger反应反应机理过酸先与羰基进行亲核加成,然后酮羰基上的一个烃基带着一对电子迁移到-O-O-基团中与羰基碳原子直接相连的氧原子上,同时发生O-O键异裂。
因此,这是一个重排反应具有光学活性的3---苯基丁酮和过酸反应,重排产物手性碳原子的枸型保持不变,说明反应属于分子内重排:不对称的酮氧化时,在重排步骤中,两个基团均可迁移,但是还是有一定的选择性,按迁移能力其顺序为:醛氧化的机理与此相似,但迁移的是氢负离子,得到羧酸。
反应实例酮类化合物用过酸如过氧乙酸、过氧苯甲酸、间氯过氧苯甲酸或三氟过氧乙酸等氧化,可在羰基旁边插入一个氧原子生成相应的酯,其中三氟过氧乙酸是最好的氧化剂。
(完整版)经典有机人名反应

有机化学人名反应1.拜耳维利格Baeyer----Villiger 反应(p317)反应机理(不要求)过酸先与羰基进行亲核加成,然后酮羰基上的一个烃基带着一对电子迁移到-O-O-基团中与羰基碳原子直接相连的氧原子上,同时发生O-O键异裂。
因此,这是一个重排反应具有光学活性的3---苯基丁酮和过酸反应,重排产物手性碳原子的枸型保持不变,说明反应属于分子内重排:不对称的酮氧化时,在重排步骤中,两个基团均可迁移,但是还是有一定的选择性,按迁移能力其顺序为:醛氧化的机理与此相似,但迁移的是氢负离子,得到羧酸。
反应实例2.康尼查罗Cannizzaro 反应(p321)凡α位碳原子上无活泼氢的醛类和浓NaOH或KOH水或醇溶液作用时,不发生醇醛缩合或树脂化作用而起歧化反应生成与醛相当的酸(成盐)及醇的混合物。
此反应的特征是醛自身同时发生氧化及还原作用,一分子被氧化成酸的盐,另一分子被还原成醇:脂肪醛中,只有甲醛和与羰基相连的是一个叔碳原子的醛类,才会发生此反应,其他醛类与强碱液,作用发生醇醛缩合或进一步变成树脂状物质。
具有α-活泼氢原子的醛和甲醛首先发生羟醛缩合反应,得到无α-活泼氢原子的β-羟基醛,然后再与甲醛进行交叉Cannizzaro反应,如乙醛和甲醛反应得到季戊四醇:反应机理醛首先和氢氧根负离子进行亲核加成得到负离子,然后碳上的氢带着一对电子以氢负离子的形式转移到另一分子的羰基不能碳原子上。
反应实例3.克莱森许密特Claisen—Schmidt 反应(交叉羟醛缩合)(p314)一个无氢原子的醛与一个带有氢原子的脂肪族醛或酮在稀氢氧化钠水溶液或醇溶液存在下发生缩合反应,并失水得到不饱和醛或酮:反应机理反应实例3.Claisen 重排烯丙基芳基醚在高温(200°C)下可以重排,生成烯丙基酚。
当烯丙基芳基醚的两个邻位未被取代基占满时,重排主要得到邻位产物,两个邻位均被取代基占据时,重排得到对位产物。
有机化学人名反应大全

一.Arbuzov 反响亚磷酸三烷基酯作为亲核试剂与卤代烷感化,生成烷基膦酸二烷基酯和一个新的卤代烷:卤代烷反响时,其活性次序为:R′I >R′Br >R′Cl.除了卤代烷外,烯丙型或炔丙型卤化物.a-卤代醚.a- 或 b-卤代酸酯.对甲苯磺酸酯等也可以进行反响.当亚酸三烷基酯中三个烷基各不雷同时,老是先脱除含碳原子数起码的基团.本反响是由醇制备卤代烷的很好办法,因为亚磷酸三烷基酯可以由醇与三氯化磷反响制得:假如反响所用的卤代烷 R'X 的烷基和亚磷酸三烷基酯 (RO)3P 的烷基雷同(即 R' = R),则Arbuzov 反响如下:这是制备烷基膦酸酯的经常运用办法.除了亚磷酸三烷基酯外,亚膦酸酯 RP(OR')2和次亚膦酸酯 R2POR' 也能产生该类反响,例如:反响机理一般以为是按 S N2 进行的分子内重排反响:反响实例二.Arndt-Eister 反响酰氯与重氮甲烷反响,然后在氧化银催化下与水共热得到酸.反响机理重氮甲烷与酰氯反响起首形成重氮酮(1),(1)在氧化银催化下与水共热,得到酰基卡宾(2),(2)产生重排得烯酮(3),(3)与水反响生成酸,若与醇或氨(胺)反响,则得酯或酰胺.反响实例三.Baeyer----Villiger反响反响机理过酸先与羰基进行亲核加成,然后酮羰基上的一个烃基带着一对电子迁徙到-O-O-基团中与羰基碳原子直接相连的氧原子上,同时产生O-O键异裂.是以,这是一个重排反响具有光学活性的3---苯基丁酮和过酸反响,重排产品手性碳原子的枸型保持不变,解释反响属于分子内重排:不合错误称的酮氧化时,在重排步调中,两个基团均可迁徙,但是照样有必定的选择性,按迁徙才能其次序为:醛氧化的机理与此类似,但迁徙的是氢负离子,得到羧酸.反响实例酮类化合物用过酸如过氧乙酸.过氧苯甲酸.间氯过氧苯甲酸或三氟过氧乙酸等氧化,可在羰基旁边拔出一个氧原子生成响应的酯,个中三氟过氧乙酸是最好的氧化剂.这类氧化剂的特色是反响速度快,反响温度一般在10~40℃之间,产率高.四.Beckmann重排肟在酸如硫酸.多聚磷酸以及能产生强酸的五氯化磷.三氯化磷.苯磺酰氯.亚硫酰氯等感化下产生重排,生成响应的代替酰胺,如环己酮肟在硫酸感化下重排生成己内酰胺:反响机理在酸感化下,肟起首产生质子化,然后脱去一分子水,同时与羟基处于反位的基团迁徙到缺电子的氮原子上,所形成的碳正离子与水反响得到酰胺.迁徙基团假如是手性碳原子,则在迁徙前后其构型不变,例如:反响实例五.Birch还原芬芳化合物用碱金属(钠.钾或锂)在液氨与醇(乙醇.异丙醇或仲丁醇)的混杂液中还原,苯环可被还原成非共轭的1,4-环己二烯化合物.反响机理起首是钠和液氨感化生成溶剂化点子,然后苯得到一个电子生成自由基负离子(Ⅰ),这是苯环的л电子系统中有7个电子,加到苯环上谁人电子处在苯环分子轨道的反键轨道上,自由基负离子仍是个环状共轭系统,(Ⅰ)暗示的是部分共振式.(Ⅰ)不稳固而被质子化,随即从乙醇中牟取一个质子生成环己二烯自由基(Ⅱ).(Ⅱ)在取得一个溶剂化电子改变成环己二烯负离子(Ⅲ),(Ⅲ)是一个强碱,敏捷再从乙醇中牟取一个电子生成1,4-环己二烯.环己二烯负离子(Ⅲ)在共轭链的中央碳原子上质子化比末尾碳原子上质子快,原因尚不清晰.反响实例代替的苯也能产生还原,并且经由过程得到单一的还原产品.例如六.Bouveault---Blanc还原脂肪族羧酸酯可用金属钠和醇还原得一级醇.α,β-不饱和羧酸酯还原得响应的饱和醇.芬芳酸酯也可进行本反响,但收率较低.本法在氢化锂铝还原酯的办法发明以前,广泛地被运用,非共轭的双键可不受影响.反响机理起首酯从金属钠获得一个电子还原为自由基负离子,然后从醇中牟取一个质子改变成自由基,再从钠得一个电子生成负离子,清除烷氧基成为醛,醛再经由雷同的步调还原成钠,再酸化得到响应的醇.反响实例醛酮也可以用本法还原,得到响应的醇:七.Bucherer反响萘酚及其衍生物在亚硫酸或亚硫酸氢盐存鄙人和氨进行高温反响,可得萘胺衍生物,反响是可逆的.反响时如用一级胺或二级胺与萘酚反响则制得二级或三级萘胺.如有萘胺制萘酚,可将其参加到热的亚硫酸氢钠中,再参加碱,经煮沸除去氨而得.反响机理本反响的机理为加成清除进程,反响的第一步(无论从哪个偏向开端)都是亚硫酸氢钠加成到环的双键上得到烯醇(Ⅱ)或烯胺(Ⅵ),它们再进行下一步互变异构为酮(Ⅲ)或亚胺(Ⅳ):反响实例八.苯基羟胺(N-羟基苯胺)和稀硫酸一路加热产生重排成对-氨基苯酚:在H2SO4-C2H5OH(或CH3OH)中重排生成对-乙氧基(或甲氧基)苯胺:其他芳基羟胺,它的环上的o-p位上未被代替者会起类似的重排.例如,对-氯苯基羟胺重排成2-氨基-5-氯苯酚:反响机理反响实例九.Berthsen,A.Y 吖啶合成法二芳基胺类与羧酸在无水ZnCl2存鄙人加热起缩合感化,生成吖啶类化合物.反响机理反响机理不详反响实例十.Cannizzaro 反响凡α位碳原子上无生动氢的醛类和浓NaOH或KOH水或醇溶液感化时,不产生醇醛缩合或树脂化感化而起歧化反响生成与醛相当的酸(成盐)及醇的混杂物.此反响的特点是醛自身同时产生氧化及还原感化,一分子被氧化成酸的盐,另一分子被还原成醇:脂肪醛中,只有甲醛和与羰基相连的是一个叔碳原子的醛类,才会产生此反响,其他醛类与强碱液,感化产生醇醛缩合或进一步变成树脂状物资.具有α-生动氢原子的醛和甲醛起首产生羟醛缩合反响,得到无α-生动氢原子的β-羟基醛,然后再与甲醛进行交叉Cannizzaro反响,如乙醛和甲醛反响得到季戊四醇:反响机理醛起首和氢氧根负离子进行亲核加成得到负离子,然后碳上的氢带着一对电子以氢负离子的情势转移到另一分子的羰基不克不及碳原子上.反响实例十一.Chichibabin 反响杂环碱类,与碱金属的氨基物一路加热时产生胺化反响,得到响应的氨基衍生物,如吡啶与氨基钠反响生成2-氨基啶,假如α位已被占领,则得γ-氨基吡啶,但产率很低.本法是杂环上引入氨基的轻便有用的办法,广泛实用于各类氮杂芳环,如苯并咪唑.异喹啉.丫啶和菲啶类化合物均能产生本反响.喹啉.吡嗪.嘧啶.噻唑类化合物较为艰苦.氨基化试剂除氨基钠.氨基钾外,还可以用代替的碱金属氨化物:反响机理反响机理还不是很清晰,可能是吡啶与氨基起首加成,(Ⅰ),(Ⅰ)转移一个负离子给质子赐与体(AH),产生一分子氢气和形成小量的2-氨基吡啶(Ⅱ),此小量的(Ⅱ)又可以作为质子的赐与体,最后的产品是2-氨基吡啶的钠盐,用水分化得到2-氨基吡啶:反响实例吡啶类化合物不轻易进行硝化,用硝基还原法制备氨基吡啶甚为艰苦.本反响是在杂环上引入氨基的轻便有用的办法,广泛实用于各类氮杂芳环,如苯并咪唑.异喹啉.吖啶和菲啶类化合物均能产生本反响.十二.Claisen酯缩合反响含有α-氢的酯在醇钠等碱性缩合剂感化下产生缩合感化,掉去一分子醇得到β-酮酸酯.如2分子乙酸乙酯在金属钠和少量乙醇感化下产生缩合得到乙酰乙酸乙酯.二元羧酸酯的分子内酯缩合见Dieckmann缩合反响.反响机理乙酸乙酯的α-氢酸性很弱(pK a-24.5),而乙醇钠又是一个相对较弱的碱(乙醇的pK a~15.9), 是以,乙酸乙酯与乙醇钠感化所形成的负离子在均衡系统是很少的.但因为最后产品乙酰乙酸乙酯是一个比较强的酸,能与乙醇钠感化形成稳固的负离子,从而使平衡朝产品偏向移动.所以,尽管反响系统中的乙酸乙酯负离子浓度很低,但一形成后,就不竭地反响,成果反响照样可以顺遂完成.经常运用的碱性缩合剂除乙醇钠外,还有叔丁醇钾.叔丁醇钠.氢化钾.氢化钠.三苯甲基钠.二异丙氨基锂(LDA)和Grignard试剂等.反响实例假如酯的α-碳上只有一个氢原子,因为酸性太弱,用乙醇钠难于形成负离子,须要用较强的碱才干把酯变成负离子.如异丁酸乙酯在三苯甲基钠感化下,可以进行缩合,而在乙醇钠感化下则不克不及产生反响:两种不合的酯也能产生酯缩合,理论上可得到四种不合的产品,称为混杂酯缩合,在制备上没有太大意义.假如个中一个酯分子中既无α-氢原子,并且烷氧羰基又比较生动时,则仅生成一种缩合产品.如苯甲酸酯.甲酸酯.草酸酯.碳酸酯等.与其它含α-氢原子的酯反响时,都只生成一种缩合产品.现实上这个反响不限于酯类自身的缩合,酯与含生动亚甲基的化合物都可以产生如许的缩合反响,这个反响可以用下列通式暗示:十三.Claisen—Schmidt反响一个无氢原子的醛与一个带有氢原子的脂肪族醛或酮在稀氢氧化钠水溶液或醇溶液存鄙人产生缩合反响,并掉水得到不饱和醛或酮:反响机理反响实例十四.Claisen 重排烯丙基芳基醚在高温(200°C)下可以重排,生成烯丙基酚.当烯丙基芳基醚的两个邻位未被代替基占满时,重排重要得到邻位产品,两个邻位均被代替基占领时,重排得到对位产品.对位.邻位均被占满时不产生此类重排反响.交叉反响试验证实:Claisen重排是分子内的重排.采取 g-碳14C 标识表记标帜的烯丙基醚进行重排,重排后 g-碳原子与苯环相连,碳碳双键产生位移.两个邻位都被代替的芳基烯丙基酚,重排后则仍是a-碳原子与苯环相连.反响机理Claisen 重排是个协同反响,中央经由一个环状过渡态,所以芳环上代替基的电子效应对重排无影响.从烯丙基芳基醚重排为邻烯丙基酚经由一次[3,3]s 迁徙和一次由酮式到烯醇式的互变异构;两个邻位都被代替基占领的烯丙基芳基酚重排时先经由一次[3,3]s 迁徙到邻位(Claisen 重排),因为邻位已被代替基占领,无法产生互变异构,接着又产生一次[3,3]s 迁徙()到对位,然后经互变异构得到对位烯丙基酚.代替的烯丙基芳基醚重排时,无论本来的烯丙基双键是Z-构型照样E-构型,重排后的新双键的构型都是E-型,这是因为重排反响所经由的六员环状过渡态具有稳固椅式构象的缘故.反响实例Claisen 重排具有广泛性,在醚类化合物中,假如消失烯丙氧基与碳碳相连的构造,就有可能产生Claisen 重排.十五.Clemmensen 还原醛类或酮类分子中的羰基被锌汞齐和浓盐酸还原为亚甲基:此法只实用于对酸稳固的化合物.对酸不稳固而对碱稳固的化合物可用还原.反响机理本反响的反响机理较庞杂,今朝尚不很清晰.反响实例十六.Combes 喹啉合成法Combes合成法是合成喹啉的另一种办法,是用芳胺与1,3-二羰基化合物反响,起首得到高产率的β-氨基烯酮,然后在浓硫酸感化下,羰基氧质子化后的羰基碳原子向氨基邻位的苯环碳原子进行亲电进攻,关环后,再脱水得到喹啉.反响机理在氨基的间位有强的邻.对位定位基团消失时,关环反响轻易产生;但当强邻.对位定位基团消失于氨基的对位时,则不轻易产生关环反响.反响实例十七.Cope清除反响叔胺的N-氧化物(氧化叔胺)热解时生成烯烃和N,N-二代替羟胺,产率很高.现实上只需将叔胺与氧化剂放在一路,不需分别出氧化叔胺即可持续进行反响,例如在湿润的二甲亚砜或四氢呋喃中这个反响可在室温进行.此反响前提平和.副反响少,反响进程中不产生重排,可用来制备很多烯烃.当氧化叔胺的一个烃基上二个β位有氢原子消失时,清除得到的烯烃是混杂物,但是 Hofmann 产品为主;如得到的烯烃有顺反异构时,一般以 E-型为主.例如:反响机理这个反响是E2顺式清除反响,反响进程中形成一个平面的五员环过度态,氧化叔胺的氧作为进攻的碱:要产生如许的环状构造,氨基和β-氢原子必须处于统一侧,并且在形成五员环过度态时,α,β-碳原子上的原子基团呈重叠型,如许的过度态须要较高的活化能,形成后也很不稳固,易于进行清除反响.反响实例十八.Cope重排1,5-二烯类化合物受热时产生类似于 O-烯丙基重排为 C-烯丙基的重排反响()反响称为Cope重排.这个反响30多年来引起人们的广泛留意.1,5-二烯在150—200℃单独加热短时光就轻易产生重排,并且产率异常好.Cope重排属于周环反响,它和其它周环反响的特色一样,具有高度的立体选择性.例如:内消旋-3,4-二甲基-1,5-己二烯重排后,得到的产品几乎全体是(Z, E)-2,6辛二烯:反响机理Cope重排是[3,3]s-迁徙反响,反响进程是经由一个环状过渡态进行的协同反响:在立体化学上,表示为经由椅式环状过渡态:反响实例十九.Curtius 反响酰基叠氮化物在惰性溶剂中加热分化生成异氰酸酯:异氰酸酯水解则得到胺:反响机理反响实例二十.Crigee,R 反响1,2-二元醇类的氧化产品因所用的氧化剂的种类而不合.用K2Cr2O7或KMnO4氧化时生成酸类.用特别氧化剂四乙醋酸铅在CH3COOH或苯等不生动有机溶剂中缓和氧化,生成二分子羰基化合物(醛或酮).氧化反响也可以在酸催化剂(三氯醋酸)存鄙人进行.本反响被广泛地运用于研讨醇类构造及制备醛.酮类,产率很高.反响机理反响进程中师长教师成环酯中央产品,进一步C--C键裂开成醛或酮.酸催化的场合,反响过程可以用下式暗示:反响实例二十一.Dakin反响酚醛或酚酮类用H2O2在NaOH存鄙人氧化时,可将分子中的-CHO基或CH3CO-基被-OH基所置换,生成相对应的酚类.本反响可运用以制备多远酚类.反响机理反响实例二十二.Elbs反响羰基的邻位有甲基或亚甲基的二芳基酮,加热时产生环化脱氢感化,生成蒽的衍生物:因为这个反响平日是在回流温度或高达400-450 °C的温度规模内进行,不必催化剂和溶剂,直到反响物没有水放出为止,在如许的高温前提下,一部分原料和产品产生碳化,部分原料酮被释放出的水所裂解,烃基产生清除或降解以及分子重排等副反响,致使产率不高.反响机理本反响的机理尚不清晰.反响实例二十三.Edvhweiler-Clarke 反响在过量甲酸存鄙人,一级胺或二级胺与甲醛反响,得到甲基化后的三级胺:甲醛在这里作为一个甲基化试剂.反响机理反响实例二十四.将一元酚类或类似化合物用过硫酸钾在碱性溶液中氧化羟基引入在原有羟基的对位或邻位,生成二元酚类.分子中的醛基或双键等都不影响.产率约20~48%.过硫酸钾的水溶液在加热时放出氧:芳伯胺类如用本试剂氧化时,变成硝基化合物.反响机理反响实例二十五.Favorskii重排a-卤代酮在氢氧化钠水溶液中加热重排生成含雷同碳原子数的羧酸;如为环状a-卤代酮,则导致环缩小.如用醇钠的醇溶液,则得羧酸酯:此法可用于合成张力较大的四员环.反响机理反响实例二十六.Friedel-Crafts烷基化反响芳烃与卤代烃.醇类或烯类化合物在Lewis催化剂(如AlCl3,FeCl3, H2SO4,H3PO4, BF3, HF等)存鄙人,产生芳环的烷基化反响.卤代烃反响的生动性次序为:RF > RCl > RBr > RI ; 当烃基超出3个碳原子时,反响进程中易产生重排.反响机理起首是卤代烃.醇或烯烃与催化剂如三氯化铝感化形成碳正离子:所形成的碳正离子可能产生重排,得到较稳固的碳正离子:碳正离子作为亲电试剂进攻芳环形成中央体s-络合物,然后掉去一个质子得到产生亲电代替产品:反响实例二十七.Friedel-Crafts酰基化反响芳烃与酰基化试剂如酰卤.酸酐.羧酸.烯酮等在Lewis酸(通经常运用无水三氯化铝)催化下产生酰基化反响,得到芬芳酮:这是制备芬芳酮类最重要的办法之一,在酰基化中不产生烃基的重排.反响机理反响实例二十八.Fries 重排酚酯在Lewis酸存鄙人加热,可产生酰基重排反响,生成邻羟基和对羟基芳酮的混杂物.重排可以在硝基苯.硝基甲烷等溶剂中进行,也可以不必溶剂直接加热进行.邻.对位产品的比例取决于酚酯的构造.反响前提和催化剂等.例如,用多聚磷酸催化时重要生成对位重排产品,而用四氯化钛催化时则重要生成邻位重排产品.反响温度对邻.对位产品比例的影响比较大,一般来讲,较低温度(如室温)下重排有利于形成对位异构产品(动力学掌握),较高温度下重排有利于形成邻位异构产品(热力学掌握).反响机理反响实例二十九.Fischer,O-Hepp,E重排N-亚硝基芳胺用盐酸或氢溴酸或其乙醇溶液处理时氨基氮上的亚硝基转移到芳核上去形成p-亚硝基芳胺(对位重排):平日产生对位重排,但在奈系化合物中如N-亚硝基-N-加基-2-奈胺则产生邻位重排成1-亚硝基化合物:反响机理在HCl存鄙人,N-亚硝基化合物起首解离成仲胺及NOCl然落后行亚硝基化:三十.Gabriel合成法邻苯二甲酰亚胺与氢氧化钾的乙醇溶液感化改变成邻苯二甲酰亚胺盐,此盐和卤代烷反响生成N-烷基邻苯二甲酰亚胺,然后在酸性或碱性前提下水解得到一级胺和邻苯二甲酸,这是制备纯净的一级胺的一种办法.有些情形下水解很艰苦,可以用肼解来代替:反响机理邻苯二甲酰亚胺盐和卤代烷的反响是亲核代替反响,代替反响产品的水解进程与酰胺的水解类似.反响实例三十一.Gattermann反响重氮盐用新制的铜粉代替亚铜盐(见)作催化剂,与浓盐酸或氢溴酸产生置换反响得到氯代或溴代芳烃:本法长处是操纵比较简略,反响可在较低温度下进行,缺陷是其产率一般较低.反响实例三十二.Gattermann-Koch 反响芬芳烃与等分子的一氧化碳及氯化氢气体在加压和催化剂(三氯化铝及氯化亚铜)存鄙人反响,生成芬芳醛:反响机理反响实例三十三.Gomberg-Bachmann 反响芬芳重氮盐在碱性前提下与其它芬芳族化合物偶联生成联苯或联苯衍生物:反响机理反响实例三十四.Hantzsch 合成法两分子b-羰基酸酯和一分子醛及一分子氨产生缩合反响,得到二氢吡啶衍生物,再用氧化剂氧化得到吡啶衍生物.这是一个很广泛的反响,用于合成吡啶同系物.反响机理反响进程可能是一分子b-羰基酸酯和醛反响,另一分子b-羰基酸酯和氨反响生成b-氨基烯酸酯,所生成的这两个化合物再产生Micheal加成反响,然后掉水关环生成二氢吡啶衍生物,它很溶液脱氢而芳构化,例如用亚硝酸或铁氰化钾氧化得到吡啶衍生物:反响实例三十五.Haworth 反响萘和丁二酸酐产生然后按尺度的办法还原.关环.还原.脱氢得到多环芬芳族化合物.反响实例三十六.Hell-Volhard-Zelinski 反响羧酸在催化量的三卤化磷或红磷感化下,能与卤素产生a-卤代反响生成a-卤代酸:本反响也可以用酰卤作催化剂.反响机理反响实例三十七.Hinsberg反响伯胺.仲胺分别与对甲苯磺酰氯感化生成响应的对甲苯磺酰胺沉淀,个中伯胺生成的沉淀能溶于碱(如氢氧化钠)溶液,仲胺生成的沉淀则不溶,叔胺与对甲苯磺酰氯不反响.此反响可用于伯仲叔胺的分别与判定.三十八.Hofmann烷基化卤代烷与氨或胺产生烷基化反响,生成脂肪族胺类:因为生成的伯胺亲核性平日比氨强,能持续与卤代烃反响,是以本反响不成防止地产生仲胺.叔胺和季铵盐,最后得到的往往是多种产品的混杂物.用大过量的氨可防止多代替反响的产生,从而可得到优越产率的伯胺.反响机理反响为典范的亲核代替反响(S N1或S N2)反响实例三十九.Hofmann清除反响季铵碱在加热前提下(100--200°C)产生热分化,当季铵碱的四个烃基都是甲基时,热分化得到甲醇和三甲胺:假如季铵碱的四个烃基不合,则热分化时老是得到含代替基起码的烯烃和叔胺:四十.Hofmann重排(降解)酰胺用溴(或氯)在碱性前提下处理改变成少一个碳原子的伯胺:反响机理反响实例四十一.Houben-Hoesch 反响酚或酚醚在氯化氢和氯化锌等Lewis酸的存鄙人,与腈感化,随落后行水解,得到酰基酚或酰基酚醚:反响机理反响机理较庞杂,今朝尚未完整解释反响实例四十二.Hunsdieecker 反响湿润的羧酸银盐在四氯化碳中与卤素一路加热放出二氧化碳,生成比原羧酸少一个碳原子的卤代烃:X = Br , Cl , I反响机理反响实例四十三.Kiliani氯化增碳法糖在少量氨的存鄙人与氢氰酸加成得到a-羟基腈,经水解得到响应的糖酸,此糖酸极易改变成内酯,将此内酯在含水的乙醚或水溶液顶用钠汞齐还原,得到比本来的糖多一个碳原子的醛糖.反响实例四十四.Knoevenagel 反响含生动亚甲基的化合物与醛或酮在弱碱性催化剂(氨.伯胺.仲胺.吡啶等有机碱)存鄙人缩合得到a,b-不饱和化合物.反响机理反响实例四十五.Koble 反响脂肪酸钠盐或钾盐的浓溶液电解时产生脱羧,同时两个烃基互相偶联生成烃类:假如运用两种不合脂肪酸的盐进行电解,则得到混杂物:反响机理反响实例四十六.Koble-Schmitt 反响酚钠和二氧化碳在加压下于125-150 ºC反响,生成邻羟基苯甲酸,同时有少量对羟基苯甲酸生成:反响产品与酚盐的种类及反响温度有关,一般来讲,运用钠盐及在较低的温度下反响重要得到邻位产品,而用钾盐及在较高温度下反响则重要得对位产品:邻位异构体在钾盐及较高温度下加热也能改变成对位异构体:反响机理反响机理今朝还不太清晰.反响实例四十七.Kolbe,H.Syntbexis of Nitroparsffini合成将含等摩尔的α-卤代羧酸与亚硝酸钠或钾的水溶液加热时,生成-硝基脂肪酸钠中央体,持续加热起分化感化,掉去CO2改变成硝基烷类及NaHCO3.本办法仅可实用于小量制备碳原子数在以下的硝基烷类(特别合适于制备硝基甲烷及硝基乙烷).而b-卤代羧酸与亚硝酸钾感化生成产品不克不及放出CO2,故不克不及产生此反响.反响实例四十八.Leuckart 反响醛或酮在高温下与甲酸铵反响得伯胺:除甲酸铵外,反响也可以用代替的甲酸铵或甲酰铵.反响机理反响中甲酸铵一方面供给氨,另一方面又作为还原剂.反响实例四十九.Lossen 反响或其酰基化物在单独加热或在碱.脱水剂(如五氧化二磷.乙酸酐.亚硫酰氯等)存鄙人加热产生重排生成异氰酸酯,再经水解.脱羧得伯胺:本重排反响后来有过反响机理本重排反响的反响机理与 ..机理相类似,也是形成异氰酸酯中央体:在重排步调中,R的迁徙和离去基团的离去是协同进行的.当R是手性碳原子时,重排后其构型保持不变:反响实例五十.Mannich 反响含有a-生动氢的醛.酮与甲醛及胺(伯胺.仲胺或氨)反响,成果一个a-生动氢被胺甲基代替,此反响又称为胺甲基化反响,所得产品称为Mannich碱.。
有机化学人名反应

取代反应:1,加特曼反应:加特曼(Gattermann L)发现:用催化量的金属铜代替氯化亚铜或溴化亚铜作催化剂,也可使重氮盐与盐酸或氢溴酸反应制得芳香氯化物或溴化物。
这样进行的反应叫做加特曼反应。
2,加特曼-科赫反应:苯、一氧化碳和氯化氢反应生成苯甲醛,此反应称为加特曼-科赫反应。
3,傅-克反应:芳香化合物芳环上的氢被烷基取代的反应称为傅-克烷基化反应;芳香化合物芳环上的氢被酰基取代的反应称为傅-克酰基化反应;统称傅-克反应。
4,布赫尔反应:萘酚在亚硫酸氢钠存在下与氨作用,转变成相应萘胺的反应称为布赫尔反应。
5,齐齐巴宾反应:吡啶与氨基钠反应,生成α-氨基吡啶,如果α位已被占据,则得γ-氨基吡啶,但产率很低。
这个反应称为齐齐巴宾(Chichibabin)反应。
6,刚穆伯—巴赫曼反应:芳香重氮盐中的芳基在碱性条件下与其它芳香族化合物偶联成联苯或联苯衍生物的反应称为刚穆伯(Gomberg)—巴赫曼(Bachmann)反应。
7,柯尔伯—施密特反应:干燥的酚钠或酚钾与二氧化碳在加温加压下生成羟基苯甲酸的反应称为柯尔伯—施密特(Kolbe-Schmitt)反应。
8,威廉森合成法:在无水条件下,醇钠和卤代烷作用生成醚的反应称为威廉森(Williamson A W)合成法。
9,席曼反应:芳香重氮盐和氟硼酸反应,生成溶解度较小的氟硼酸盐,后者加热分解产生氟苯,这称为席曼(Schiemann)反应。
10,桑德迈耳反应:1884年,桑德迈耳(Sandmeyer T)发现:在氯化亚铜或溴化亚铜的催化下,重氮盐在氢卤酸溶液中加热,重氮基可分别被氯或溴原子取代,生成芳香氯化物或溴化物。
这一反应称为桑德迈耳反应。
11,普塑尔反应:一些重氮盐在碱性条件下或稀酸的条件下可以发生分子内的偶联反应。
这个反应是普塑尔(Pschorr R)在寻找合成菲环的新方法中首先发现的,故称为普塑尔反应。
12,瑞穆尔—悌曼反应:酚与氯仿在碱性溶液中加热生成邻位及对位羟基醛的反应称为瑞穆尔—悌曼(Reimer —Tiemann)反应。
有机化学人名反应大全

一、Arbuzov 反应亚磷酸三烷基酯作为亲核试剂与卤代烷作用,生成烷基膦酸二烷基酯与一个新得卤代烷:卤代烷反应时,其活性次序为:R′I >R′Br 〉R′Cl.除了卤代烷外,烯丙型或炔丙型卤化物、a-卤代醚、a—或b-卤代酸酯、对甲苯磺酸酯等也可以进行反应。
当亚酸三烷基酯中三个烷基各不相同时,总就是先脱除含碳原子数最少得基团。
本反应就是由醇制备卤代烷得很好方法,因为亚磷酸三烷基酯可以由醇与三氯化磷反应制得:如果反应所用得卤代烷R’X得烷基与亚磷酸三烷基酯(RO)3P得烷基相同(即R'=R),则Arbuzov反应如下:这就是制备烷基膦酸酯得常用方法。
除了亚磷酸三烷基酯外,亚膦酸酯RP(OR')2与次亚膦酸酯R2POR'也能发生该类反应,例如:反应机理一般认为就是按SN2 进行得分子内重排反应:反应实例二、Arndt—Eister 反应酰氯与重氮甲烷反应,然后在氧化银催化下与水共热得到酸。
反应机理重氮甲烷与酰氯反应首先形成重氮酮(1),(1)在氧化银催化下与水共热,得到酰基卡宾(2),(2)发生重排得烯酮(3),(3)与水反应生成酸,若与醇或氨(胺)反应,则得酯或酰胺。
反应实例三、Baeyer——--Villiger反应反应机理过酸先与羰基进行亲核加成,然后酮羰基上得一个烃基带着一对电子迁移到—O-O-基团中与羰基碳原子直接相连得氧原子上,同时发生O-O键异裂.因此,这就是一个重排反应具有光学活性得3-—-苯基丁酮与过酸反应,重排产物手性碳原子得枸型保持不变,说明反应属于分子内重排:不对称得酮氧化时,在重排步骤中,两个基团均可迁移,但就是还就是有一定得选择性,按迁移能力其顺序为:醛氧化得机理与此相似,但迁移得就是氢负离子,得到羧酸。
反应实例酮类化合物用过酸如过氧乙酸、过氧苯甲酸、间氯过氧苯甲酸或三氟过氧乙酸等氧化,可在羰基旁边插入一个氧原子生成相应得酯,其中三氟过氧乙酸就是最好得氧化剂。
这类氧化剂得特点就是反应速率快,反应温度一般在10~40℃之间,产率高。
有机化学中国人名反应

有机化学中国人名反应中国人名反应是指以中国有机化学家的名字命名的有机化学反应。
这些反应通常是由这些化学家发现或发展,并且对有机化学领域的发展做出了重要贡献。
以下将介绍几个著名的中国人名反应。
1. 曾光明反应曾光明反应是由中国有机化学家曾光明教授于1981年首次报道的一种重要的合成方法。
该反应以金属有机化合物为催化剂,能够将酮类化合物与硅醚反应,形成相应的醇类化合物。
曾光明反应在有机合成中具有广泛的应用,可以高效地构建C-O键,是合成醇类化合物的重要工具。
2. 毛宗回反应毛宗回反应是由中国有机化学家毛宗回教授于1978年首次报道的一种重要的合成方法。
该反应以金属有机化合物为催化剂,能够将酮类化合物与有机硅化合物反应,生成相应的醇类化合物。
毛宗回反应在有机合成中广泛应用,具有高效、高选择性和环境友好等优点,被广泛用于合成复杂有机分子。
3. 李盛骏反应李盛骏反应是由中国有机化学家李盛骏教授于20世纪80年代中期首次报道的一种重要的合成方法。
该反应以金属有机化合物为催化剂,能够将炔烃与醛类化合物反应,形成相应的α,β-不饱和醛类化合物。
李盛骏反应在有机合成中具有重要的应用价值,可以高效地构建C-C键和C=O键,是合成复杂有机分子的重要工具。
4. 王立群反应王立群反应是由中国有机化学家王立群教授于1992年首次报道的一种重要的合成方法。
该反应以过渡金属催化剂为催化剂,能够将酮类化合物与炔烃反应,形成相应的烯醇类化合物。
王立群反应在有机合成中具有广泛的应用,可以高效地构建C-C键和C-O键,是合成天然产物和药物分子的重要工具。
5. 陈茵反应陈茵反应是由中国有机化学家陈茵教授于20世纪70年代末首次报道的一种重要的合成方法。
该反应以金属有机化合物为催化剂,能够将酮类化合物与酸类化合物反应,形成相应的酯类化合物。
陈茵反应在有机合成中具有重要的应用价值,可以高效地构建C-C键和C-O键,是合成酯类化合物的重要工具。
有机化学人名反应大全

一、Arbuzov 反应亚磷酸三烷基酯作为亲核试剂与卤代烷作用,生成烷基膦酸二烷基酯和一个新的卤代烷:卤代烷反应时,其活性次序为:R′I 〉R′Br〉R′Cl。
除了卤代烷外,烯丙型或炔丙型卤化物、a—卤代醚、a- 或b-卤代酸酯、对甲苯磺酸酯等也可以进行反应.当亚酸三烷基酯中三个烷基各不相同时,总是先脱除含碳原子数最少的基团。
本反应是由醇制备卤代烷的很好方法,因为亚磷酸三烷基酯可以由醇与三氯化磷反应制得:如果反应所用的卤代烷R’X的烷基和亚磷酸三烷基酯(RO)3P 的烷基相同(即R' = R),则Arbuzov 反应如下:这是制备烷基膦酸酯的常用方法。
除了亚磷酸三烷基酯外,亚膦酸酯RP(OR')2和次亚膦酸酯R2POR' 也能发生该类反应,例如:反应机理一般认为是按S N2 进行的分子内重排反应:反应实例二、Arndt-Eister反应酰氯与重氮甲烷反应,然后在氧化银催化下与水共热得到酸.反应机理重氮甲烷与酰氯反应首先形成重氮酮(1),(1)在氧化银催化下与水共热,得到酰基卡宾(2),(2)发生重排得烯酮(3),(3)与水反应生成酸,若与醇或氨(胺)反应,则得酯或酰胺。
反应实例三、Baeyer--—-Villiger反应反应机理过酸先与羰基进行亲核加成,然后酮羰基上的一个烃基带着一对电子迁移到-O-O-基团中与羰基碳原子直接相连的氧原子上,同时发生O—O键异裂.因此,这是一个重排反应具有光学活性的3-—-苯基丁酮和过酸反应,重排产物手性碳原子的枸型保持不变,说明反应属于分子内重排:不对称的酮氧化时,在重排步骤中,两个基团均可迁移,但是还是有一定的选择性,按迁移能力其顺序为:醛氧化的机理与此相似,但迁移的是氢负离子,得到羧酸.反应实例酮类化合物用过酸如过氧乙酸、过氧苯甲酸、间氯过氧苯甲酸或三氟过氧乙酸等氧化,可在羰基旁边插入一个氧原子生成相应的酯,其中三氟过氧乙酸是最好的氧化剂。
这类氧化剂的特点是反应速率快,反应温度一般在10~40℃之间,产率高。
有机人名反应
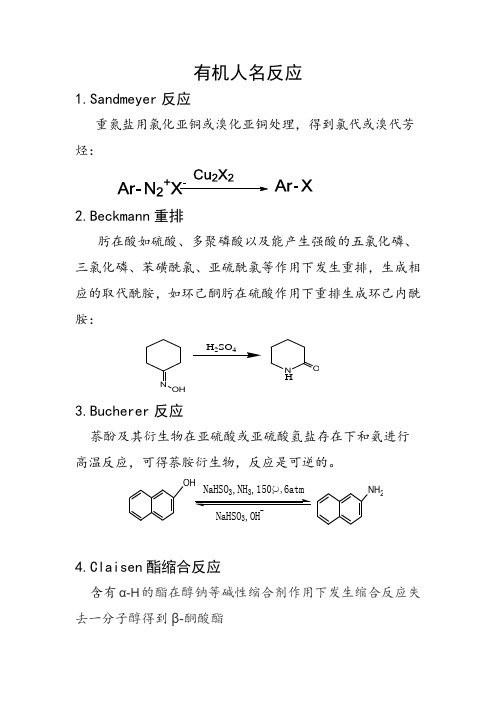
有机人名反应1.Sandmeyer 反应重氮盐用氯化亚铜或溴化亚铜处理,得到氯代或溴代芳烃:2.Beckmann 重排肟在酸如硫酸、多聚磷酸以及能产生强酸的五氯化磷、三氯化磷、苯磺酰氯、亚硫酰氯等作用下发生重排,生成相应的取代酰胺,如环己酮肟在硫酸作用下重排生成环己内酰胺:NOHH 2SO 4NHO3.Bucherer 反应萘酚及其衍生物在亚硫酸或亚硫酸氢盐存在下和氨进行高温反应,可得萘胺衍生物,反应是可逆的。
OHNH 2NaHSO 3,NH 3,150℃,6atm NaHSO 3,OH -4.Claisen 酯缩合反应含有 α-H 的酯在醇钠等碱性缩合剂作用下发生缩合反应失去一分子醇得到β-酮酸酯2CH 3CO 2C 2H 5C 2H 5ONaCH 3COCH 2CO 2C 2H 5五.Dakin 反应邻位或对位有羟基(或氨基)的芳醛或芳酮在碱溶液中用过氧化氢或其他过氧化物氧化,得到相应的多元酚。
CHOOHH2O2NaOH , 50℃ONaONa+HCO 2NaH +OHOH六.Curtius 反应酰基叠氮化物在惰性溶剂中加热分解生成异氰酸酯:R-C-Cl +NaN3OR-C-N3O R-N=C=O 加热七.Elbs 反应羰基的邻位有甲基或亚甲基的二芳基酮,加热时发生环化脱氢作用,生成蒽的衍生物。
OCH3300-400℃+ H 2O八.Gattermann 反应重氮盐用新制的铜粉代替亚铜盐(见Sandmeyer 反应)作催化剂,与浓盐酸或氢溴酸发生置换反应得到氯代或溴代芳烃,本法优点是操作比较简单,反应可在较低温度下进行,缺点是其产率一般较Sandmeyer 反应低。
Ar-N 2+X -+HX(浓)铜粉50℃Ar-XX=Cl,Br,CN,NO 2九.Hofmann 重排酰胺用溴(或氯)在碱性条件下处理转变为少一个碳原子的伯胺。
R-C-NH 2OBrNaOHR-N C OH 2ORNH 2十.Hantzsch 反应两分子b-羰基酸酯和一分子醛及一分子氨发生缩合反应,得到二氢吡啶衍生物,再用氧化剂氧化得到吡啶衍生物。
有机人名反应

有机人名反应有机人名反应1.Baeyer-Villiger氧化:酮过酸氧化成酯迁移规则:叔>仲>环己基>栄>伯〉屮基〉氢2.Corey-Kim氧化:醇在NCS/DMF作用后,碱处理氧化成醛酮3.Criegee邻二醇裂解:邻二醇山Pb (OAc) 4氧化成按基化合物4.Criegee臭氧化:烯绘臭氧化后水解成醛酮5.Dakin反应:对羟基苯屮醛由碱性H2O2氧化成对二酚6.Dess—Martin过碘酸酯氧化:仲醇山过碘酸酯氧化成酮7.Fleming氧化:硅烷经过酸化,过酸盐氧化,水解以后形成醇8.Hooker氧化:2—羟基一3烷基一1, 4一醍被KMnO4氧化导致侧链烷基失去一个亚屮基, 同时疑基和烷基位置互变9.Moffatt氧化(Pfitzner—Moffatt)氧化:用DCC和DMSO氧化醇,形成醛酮lO.Oppenauer氧化:烷氧基催化的仲醇氧化成醛酮11.Riley氧化:活泼亚屮基(拨基a位等)被SeO2氧化成酮12.Rubottom氧化:烯醇硅烷经过m—CPBA和K2CO3处理后a —羟基化13.Sarett氧化:CrO3?Py络合物氧化醇成醛酮14.Swern氧化:用(COC1)2,DMSO为试剂合Et3N淬灭的方法将醇氧化成拨基化合物15.Tamao—Kumada氧化:烷基氟硅烷被KF, H2O2, KHCO3氧化成醇16.Wacker氧化:Pd催化剂下,烯绘氧化成酮L.Barton —McCombie去氧反应:从相关的硫按基体中间用n—Bu3SnH, AIBN试剂经过自由基开裂发生醇的去氧作用2.Birch还原:苯环111 Na单质合液胺条件下形成环内二烯炷(带供电子基团的苯环:双键连接取代基;带吸电子基团的苯环,取代基在烯丙位。
)3.Brown硼氢化:烯怪和硼烷加成产生的有机硼烷经过碱性H2O2氧化得到醇4.Cannizzaro歧化:碱在芳香醛,中醛或者其他无a —氢的脂肪氢之间发生氧化还原反应给岀醇和酸5.Clemmensen还原:用锌汞齐和氯化氢将醛酮还原为亚中基化合物6.Corey—Bakshi—Shibata(CBS)还原:酮在手性恶I坐硼烷催化下的立体选择性还原7.Gribble眄I□朵还原:用NaBH4直接还原会导致N—烷基化,NaBH3CN在冰酷酸当中还原耐喙双键可以解决S.Gribble二芳基酮还原:用NaBH4在三氟乙酸中还原二芳基酮和二芳基甲醇为二芳基中烷,也可以应用于二杂芳环酮和醇的还原Q.Luche还原:烯酮在NaBH4-CeC13下发生1, 2—还原形成烯丙位取代烯醇10.McFadyen—Stevens还原:酰基苯磺酰J]井用碱处理成醛11.Meerwein—Ponndorf—Verley 还原:用Al (OPF) 3/Pr'OH 体系将酮还原为醇12.Midland还原:用B —3—a —浪烯一9 —BBN对酮进行不对称还原13.Noyori不对称氢化:拨基在Ru (ID BINAP络合物催化下发生不对称氢化还原14.Rosenmund还原:用BaSO4/毒化Pd催化剂将酰氯氢化成醛,如催化剂未被毒化,会氢化为醇15.Wolff-Kishner一黃鸣龙还原:用碱性月井将按基还原为亚屮基C成烯反应1.Boord反应:价卤代烷氧基与Zn作用生成烯怪2.Chugaev消除:黃原酸酯热消除成烯3.Cope消除:胺的氧化物热消除成烯炷4.Corey-Winter olefin烯烧合成:邻二醇经1,1-硫代拨基二咪醴和三甲氧基牒处理转化为相应的烯5.Doering-LaFlamme丙二烯合成:烯烧用澳仿以及烷氧化物处理以后生成同碳二澳环丙烷再反应生成丙二烯6.Horner-Wadsworth-Emmons反应:从醛合磷酸酯生成烯炷.副产物为水溶性磷酸盐,故以后处理较相应的Witting反应简单的多7.Julia-Lythgoe成烯反应:从飒合醛生成(E)-烯桂8.Peterson成烯反应:从a-硅基碳负离子合按基化合物生成烯绘.也成为含硅的Witting 反应9.Ramberg-Backlund烯桂合成:A-卤代砚用碱处理生成烯烧10.Witting反应:按基用麟叶立德变成烯绘U.Zaitsev消除:E2消除带来更多取代的烯坯D偶联反应1.Cadiot-Chodkiewicz偶联:从烘基卤和烘基酮合成双烘衍生物2.Castro—Stephens 偶联:芳基烘合成,同Cadiot-Chodkiewicz 偶联3.Eglinton反应:终端烘坯在化学计量(常常过量)Cu(Oac)2促进下发生的氧化偶联反应4.Eschenmoser偶联:从硫酰胺和烷基卤生成烯胺5.Glaser偶联:Cu催化终端烘桂的氧化自偶联6.Gomberg-Bachmann偶联:碱促进下芳基重氮盐和一个芳烧之间经自由基偶联生成二芳基化合物7.Heck反应:Pb催化的有机卤代物或者三氟磺酸酯和烯桂之间的偶联反应8.杂芳基Heck反应:发生在杂芳基受体上的Pd(Ph3P)4,Ph3P,CuI,Cs2CO3催化下的分子内或者分子间Heck反应9.Hiyama交义偶联反应:Pb催化有机硅和有机卤代物或者三氟磺酸酯等在诸如F—或者0H—之类的活化剂Pd(Ph3P)4,TBAF催化剂存在下发生的交义偶联反应10.Kumada交义偶联(Kharasch交义偶联):Ni和Pd催化下,格氏试剂和一个有机卤代物或者三氟磺酸酯之间的交叉偶联11.Liebeskind-Srogl偶联:硫酸酯和有机硼酸之间经过Pd催化发生交义偶联生成酮12.McMurry偶联:按基用低价Ti,如TiC13/LiAlH4产生的Ti(0)处理得到双键,反应是一个单电子过程13.Negishi交义偶联:Pd催化的有机Zn和有机卤代物,三氟磺酸酯等之间发生的交义偶联反应14.Sonogashira反应:Pd/Cu催化的有机卤和端基烘桂之间的交义偶联反应15.Stille偶联:Pd催化的有机Sn和有机卤,三氟磺酸酯之间的交义偶联反应16.Stille-Kelly偶联:双Sn试剂进行Pd催化下二芳基卤代物的分子交叉偶联17,Suzuki偶联:Pd催化下的有机硼烷和有机卤,三氟磺酸酯在碱存在下发生的交义偶联lS.Ullmann反应:芳基碘代物在Cu存在下的自偶联反应19.Wurtz反应:烷基卤经Na或Mg金属处理后形成碳碳单键20.Ymada偶联试剂:用二乙基氛基磷酸酯(EtO)2PO-CN活化竣酸E缩合反应:21.Aldol缩合:按基和一个烯醇负离子或一个烯醇的缩合22.Blaise反应:月青和a—卤代酯和Zn反应得到^一酮酯23.Benzoin缩合:芳香醛经CN —催化为安息香(二芳基乙醇酮)24.Buchner-Curtius-Schlotterbeck反应:拨基化合物和脂肪族重氮化物反应给出同系化的酮25.Claisen缩合:酯在碱催化下缩合为|3 —酮酯26.Corey-Fuchs反应:醛发生一碳同系化生成二澳烯桂,然后用BuLi处理生成终端烘炷27.Darzen缩水甘油酸酯缩合:碱催化下从a—卤代酯和按基化合物生成a,直一环氧酯(缩水甘油醛)28.Dieckmann缩合:分子内的Claisen缩合29.Evans aldol反应:用Evans手性鳌合剂,即酰基恶I坐酮进行不对称醇醛缩合30.Guareschi-Thorpe缩合(2—毗唳酮合成):氤基乙酸乙酯和乙酰乙酸在氨存在下生成2—毗唳酮31.Henry硝醇反应:醛和有硝基烷烧在碱作用下去质子化产生氮酸酯32.Kharasch加成反应:过渡金属催化的CXCI3对于烯桂的自山基加成33.Knoevenagel缩合:拨基化合物和活泼亚屮基化合物在胺的催化下缩合34.Mannnich缩合(按基胺甲基化):胺,甲醛,和一个带有酸性亚中基成分的化合物之间的三组分反应发生胺甲基化35.Michael加成:亲核碳原子对不饱和体系的共扼加成36.Mukaiyama醇醛缩合:Lewis酸催化下的醛和硅基烯醇聪之间的Aldol缩合37.Nozaki —Hiyama—KIshi反应:Cr—Ni双金属催化下的烯基卤对于醛的氧化还原加成38.Pechmann缩合(香豆素合成):Lewis酸促进的酸和|3—酮酯缩合成为香豆素39.Perkin反应:芳香醛和乙酊反应合成肉桂酸40.Prins反应:烯炷酸性条件下对于甲醛的加成反应41.Reformatsky反应:有机Zn试剂(从a—卤代酯来)对按基的亲核加成反应42.Reimer—Tiemann反应:从碱性介质当中从酚和氯仿合成邻屮酰基苯酚43.Schlosser对Witting反应的修正:不稳定的叶立徳和醛发生的Witting反应生成Z—烯桂,而改进的Schlosser反应可以得到E —烯疑44.Stetter反应(Michael—Stetter反应):从醛和a, [3 —不饱和酮可以得到1, 4—二拨基衍生物。
100种有机化学人名反应

120~200℃时热解,顺利产生烯烃,相应醇和氧硫
化碳。黄原酸酯在热解前制备不须离析除黄原酸酯外,其他的酯氨基甲酸酯,碳
酸酯和羧酸酯热解。特别是使用大分子量的羧酸酯(棕榈酸酯)的烯烃提供了有
利条件。因为这些酯本身沸点高,而热解温度较低(约
300℃),在液相中简单加热即可。
250℃
Cl OCH2CH=CH2
;
Cl 醚分子中,
如临位未被取代则不起重排反应,产生复杂的热分解作用。此反应是在苯环引入丙基的
简易方法,因为烯丙基可还原成丙基。
16. Claisen缩合反应(P352~354)
17. Claisen-Schmidt反应(P287)
N+
*
H CH3
CH3 △
H3C
*
CH3
CH2 +(CH3)2NOH
O
H5C6
C6H5
20. Criegee氧化法
乙二醇类在稀醋酸或苯溶液中,室温时用四乙酸铅进行很温和的氧化,两个相连的各带
有游离羟基的碳原子之间的碳链就断裂,得到定量的醛酮类。此法用于研究醇类结构及
此法用来合成呋喃类化合物,在吡啶或氨存在下,α
-氯化羰基化合物或α
,β-氯醚类与
1,3-二羰基化合物发生缩合反应,生成呋喃类化合物。
R C O H2C COOR'
O
COOR'
R
吡啶或氨
-H2O, -HCl
CH2
+
OC
Cl CH3
CH3
解,可得醛类化合物,
R’MgX中
15个有机人名反应

有机人名反班级:化学一班学号:41207046 姓名:袁雪薇1.Pschorr反应重氮盐在碱性条件下发生分子内偶联反应。
反应机理:一般认为,本反应是通过自由基进行的,在反应时,两个苯环必须在双键的同一侧,并且在同一个平面上。
2.Dkin反应邻位或对位有羟基(或氨基)的芳醛或芳酮在碱溶液中用过氧化氢或其他氧化物氧化,得到相应的多元酚。
化学方程式:反应机理:3.Baeyer-Viliger 氧化酮类化合物用过酸如或氧乙酸等氧化,可在羰基旁边插一个氧原子,生成相应的酯。
反应机理4.Vilsmeier 反应芳烃、活化烯烃化合物用二取代甲酰胺及三氯氧磷处理得到醛类。
是在芳环上引入甲酰基的常用方法。
化学方程式:反应机理:5. Hantzsch反应原料:羰基酸酯,醛,氨,氧化剂反应方程式:反应机理:R /ORO O R //+R /O ONH 3NR //CO 2R /RRR /O 2C主要应用:用于合成吡啶的同系物,在生物、医药等 6. Birch 反应原料:芳香化合物、碱金属(钠、钾或锂)、液氨、醇(乙醇、异丙醇或仲丁醇) 反应方程式:反应机理:主要应用:Birch 还原时连接芳香族和脂肪族化合物的桥梁,它使许多芳香族衍生物成为合成脂肪族化合物。
Birch 还原早期集中于烷基苯和芳香醚类化合物的合成,现在已扩展到芳香族酸、酯和酮等化合物,在天然有机产物合成中得到广泛应用。
例如手性环己烷衍生物的合成。
Na3Na +NH3Na +e+HHeEtOHHHeHH EtOHHH7. Fries重排原料:酚、酯、lewis酸也可以是硝基苯、硝基甲烷溶剂反应方程式:酚酯在lewis酸存在下加热发生酰基重排,生成邻羟基和对羟基芳酮的混合物。
邻对位比例取决于酚酯的结构、反应条件和催化剂等。
温度对产物比例影响较大,一般来说,较低温度下重排有利于形成对位异构产物,较高温度下有利于形成邻位异构产物。
反应机理:O CORAlCl3OHCOR+OHCO R3O CCH3OCH33165℃OHCH3H3CCO80~85%95%COCH3O COCH3AlCl3AlCl3+H3CCO+OH3CCOH+-AlCl3OHH3CCO主要应用:主要在药物合成中应用广泛,丙酸苯酯的Fries重排可以合成抗早产药利托君的中间体,还可以合成肾上腺素,是一种强心剂。
有机化学人名反应1-50

1. Arndt-Eistert 反应醛、酮与重氮甲烷反应,失去氮并重排成多一个CH2 基的相应羰基化合物,这个反应对于环酮的扩环反应很重要。
2. Baeyer-Villiger 氧化应用过氧酸使酮氧化成酯。
反应中在酮的羰基和相邻的碳原子之间引人一个氧原子。
如由樟脑生成内酯:有时反应能生成二或多过氧化物,但环状酮转变为内酯能得到单一的预期产物。
合适的酸为过硫酸(Caro’s 酸)、过氧苯甲酸、三氟过氧乙酸。
除环酮外,无环的脂肪、芳香酮也可发生此反应。
二酮生成酸酐类、α、β-不饱和酮得到烯醇酯类。
3. Bechamp 还原(可用于工业制备)在铁、亚铁盐和稀酸的作用下,芳香族硝基化合物能还原成相应的芳香胺。
当某些盐(FeCl2、FeCl3、FeSO4、CaCl2 等)存在时,所用酸无论是过量还是少量,甚至在中性溶液中都能够进行这种还原。
此方法适用于绝大部分各种不同结构的芳香族化合物,有时也用来还原脂肪族硝基化合物。
4. Beckmann 重排醛肟、酮肟用酸或路易斯酸处理后,最终产物得酰胺类。
单酮肟重排仅得一种酰胺,混酮肟重排得两种混合酰胺。
但一般质子化羟基的裂解和基团R 的转移是从相反的位置同时进行的。
无论酯酮肟和芳酮肟都会发生此反应。
环酮肟重排得内酰胺,这在工业生产上很重要,利用此反应可帮助决定异构酮肟的结构。
5. Beyer 喹啉类合成法芳香伯胺与一分子醛及一分子甲基酮在浓盐酸或ZnCl2 存在下,反应生成喹啉类化合物。
这是对Doebner-Miller 喹啉合成法的改进。
Doebner-Miller 合成法由芳胺和不饱和醛或酮反应得到喹啉衍生物。
6. Blanc 氯甲基化反应芳香族化合物苯、萘、蒽、菲、联苯及衍生物,在ZnCl2(或NH4Cl、AlCl3、SnCl4、H2SO4、H3PO4 )存在下,用甲醛和极浓盐酸处理,发生芳香化合物的氯甲基化反应。
对于取代烃类,取代基的性质对反应能力影响很亲电取代,烷基,烷氧基一般使反应速度增加,而卤素、羧基特别是硝基用乙醛得到氯乙基化。
100种有机化学人名反应(有机化学)

1. ArndtEistert反应醛、酮与重氮甲烷反应失去氮并重排成多一个CH2基的相应羰基化合物这个反应对于环酮的扩环反应很重要。
OCH2N2O-CH2NNN2重排O2. BaeyerVilliger氧化应用过氧酸使酮氧化成酯。
反应中在酮的羰基和相邻的碳原子之间引人一个氧原子。
如由樟脑生成内酯OCH3CH3CH3OOCH3CH3H2SO5有时反应能生成二或多过氧化物但环状酮转变为内酯能得到单一的预期产物。
合适的酸为过硫酸Caro’s 酸、过氧苯甲酸、三氟过氧乙酸。
除环酮外无环的脂肪、芳香酮也可发生此反应。
二酮生成酸酐类、α、β不饱和酮得到烯醇酯类。
3. Bechamp还原可用于工业制备在铁、亚铁盐和稀酸的作用下芳香族硝基化合物能还原成相应的芳香胺。
C6H5-NO2 2Fe 6HCl C6H5-NH2 2FeCl3 2H2O。
当某些盐FeCl2、FeCl3、FeSO4、CaCl2等存在时所用酸无论是过量还是少量甚至在中性溶液中都能够进行这种还原。
此方法适用于绝大部分各种不同结构的芳香族化合物有时也用来还原脂肪族硝基化合物。
4. Beckmann重排醛肟、酮肟用酸或路易斯酸处理后最终产物得酰胺类。
单酮肟重排仅得一种酰胺混酮肟重排得两种混合酰胺。
但一般质子化羟基的裂解和基团R的转移是从相反的位置同时进行的。
NOHRRRNHRONRROHRNHRO 无论酯酮肟和芳酮肟都会发生此反应。
环酮肟重排得内酰胺这在工业生产上很重要利用此反应可帮助决定异构酮肟的结构。
5. Beyer喹啉类合成法芳香伯胺与一分子醛及一分子甲基酮在浓盐酸或ZnCl2存在下反应生成喹啉类化合物。
NH2NHRRHNRRRCHORCOCH3HCl H2这是对Doebner-Miller喹啉合成法的改进。
Doebner-Miller合成法由芳胺和不饱和醛或酮反应得到喹啉衍生物。
NH2NHCH3HNCH3 H2CH3O2CH3CHO 6. Blanc氯甲基化反应芳香族化合物苯、萘、蒽、菲、联苯及衍生物在ZnCl2或NH4Cl、AlCl3、SnCl4、H2SO4、H3PO4 存在下用甲醛和极浓盐酸处理发生芳香化合物的氯甲基化反应。
有机化学人名反应

有机化学人名反应取代反应:1,加特曼反应:加特曼(GattermannL)发现:用催化量的金属铜代替氯化亚铜或溴化亚铜作催化剂,也可使重氮盐与盐酸或氢溴酸反应制得芳香氯化物或溴化物。
这样进行的反应叫做加特曼反应。
2,加特曼-科赫反应:苯、一氧化碳和氯化氢反应生成苯甲醛,此反应称为加特曼-科赫反应。
3,傅-克反应:芳香化合物芳环上的氢被烷基取代的反应称为傅-克烷基化反应;芳香化合物芳环上的氢被酰基取代的反应称为傅-克酰基化反应;统称傅-克反应。
4,布赫尔反应:萘酚在亚硫酸氢钠存在下与氨作用,转变成相应萘胺的反应称为布赫尔反应。
5,齐齐巴宾反应:吡啶与氨基钠反应,生成-氨基吡啶,如果位已被占据,则得-氨基吡啶,但产率很低。
这个反应称为齐齐巴宾(Chichibabin)反应。
6,刚穆伯—巴赫曼反应:芳香重氮盐中的芳基在碱性条件下与其它芳香族化合物偶联成联苯或联苯衍生物的反应称为刚穆伯(Gomberg)—巴赫曼(Bachmann)反应。
7,柯尔伯—施密特反应:干燥的酚钠或酚钾与二氧化碳在加温加压下生成羟基苯甲酸的反应称为柯尔伯—施密特(Kolbe-Schmitt)反应。
8,威廉森合成法:在无水条件下,醇钠和卤代烷作用生成醚的反应称为威廉森(WilliamonAW)合成法。
9,席曼反应:芳香重氮盐和氟硼酸反应,生成溶解度较小的氟硼酸盐,后者加热分解产生氟苯,这称为席曼(Schiemann)反应。
10,桑德迈耳反应:1884年,桑德迈耳(SandmeyerT)发现:在氯化亚铜或溴化亚铜的催化下,重氮盐在氢卤酸溶液中加热,重氮基可分别被氯或溴原子取代,生成芳香氯化物或溴化物。
这一反应称为桑德迈耳反应。
11,普塑尔反应:一些重氮盐在碱性条件下或稀酸的条件下可以发生分子内的偶联反应。
这个反应是普塑尔(PchorrR)在寻找合成菲环的新方法中首先发现的,故称为普塑尔反应。
12,瑞穆尔—悌曼反应:酚与氯仿在碱性溶液中加热生成邻位及对位羟基醛的反应称为瑞穆尔—悌曼(Reimer—Tiemann)反应。
有机人名反应

Oppenaue氧化欧芬脑尔氧化法:在异丙醇铝或叔丁醇铝存在下,仲醇和丙酮反应,仲醇氧化成酮,丙酮转化成还原成醇。
Pinacol重排频哪醇重排,相当于碳正离子重排。
Williamson合成法威廉姆逊合成法卤代烃和醇钠作用生成醚的方法。
Friedel-Crafts反应傅克反应(烷基化,酰基化)但苯环上连有吸电子基团如硝基等时,不能发生反应。
Haloform reaction卤仿反应:乙醛、甲基酮、乙醇和α-碳上连有甲基的仲醇与次卤酸盐反应生成卤仿和少一个碳的羧酸。
Aldol condensation羟醛缩合:两分子含有α-氢的醛在酸或碱催化下,相互结合形成β-羟基醛的反应。
Claisen-Schmidt反应克莱森-许密特反应:由芳香醛和含有α-氢的脂肪醛或酮进行交叉羟醛缩合生成α,β-不饱和醛或酮的反应。
Mannich反应曼尼希反应:含有α-活泼氢的酮与甲醛及胺反应,可以在酮的α位引入一个胺甲基。
Clemmensen还原法克莱门森还原法:醛、酮与锌汞齐和浓盐酸回流反应,羰基被还原成亚甲基黄鸣龙还原法:醛、酮在肼、氢氧化钠(或氢氧化钾)的水溶液中,与二缩乙二醇回流反应,被还原成亚甲基。
Meerwein-Ponndorf还原麦尔外因-彭杜尔夫还原:在异丙醇铝-异丙醇的作用下,醛、酮可悲还原成醇,异丙醇转化成丙酮。
Cannizzaro反应:康尼查罗反应:无α-氢的醛在浓碱作用下发生分子间反应,一分子醛被还原成醇,另一分子醛被氧化成酸。
Benzoin缩合反应:安息香缩合反应:芳醛在氰基负离子催化下,生成α-羟基酮的反应。
Wittig反应魏悌希反应:醛、酮与磷叶立德反应生成烯烃的反应。
Gattermann-Koch反应:盖特曼-柯赫反应:在催化剂无水氯化铝和氯化亚铜存在下,芳烃与氯化氢和一氧化碳混合气体作用,生成芳醛的反应。
Michael加成:麦克尔加成:α,β-不饱和醛或酮和亲核的碳负离子进行的1,4-共轭加成反应。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
Arndt-Eistert合成
【摘要】阿恩特-艾斯特尔特合成是用德国化学家弗里茨·阿恩特(Fritz Arndt,1885年-1969年)和贝恩德米·艾斯特尔特(Bernd Eistert,1902年-1978年)两人的名字命名的一个人名反应。
是一类羧酸的同系化反应,能将一个酸转变成它的高一级同系物或转变成同系列酸的衍生物,同时也是一种非常有用的增长羧酸碳链的合成方法,在化学中有很广的应用。
【关键词】酰氯;重氮甲烷;重氮酮;反应机理;碳链加长;应用
ABSTRACT The Arndt - Esther Stewart synthesis is the German chemist Fritz Arndt (Fritz Arndt, -1969, 1885) and Bain Suleyman • Esther Stewart (Bernd Eistert, 1902 -1978years) both named after a person's name reaction. Homologation reactions are a class of carboxylic acids, and capable of an acid into its high level homologues or converted into the acid derivative of the same series, is also a very useful synthetic method of the growth of a carboxylic acid carbon chain, Have wide application in the chemical.
KEY WORDS Chloride; Diazomethane; Diazoketone; Reaction Mechanism; Carbon chain length; Application
在多达上百种的人名反应中,德国化学家弗里茨·阿恩特和贝恩德米·艾斯特尔特的这个人名反应在化学界中着实是一个比较经典的化学反应,在这个反应中,能将酸类化合物变成酯、酰胺等等衍生类物质,在这反应中,他们在Wolff 重排反应的基础上发现了碳链的增长与利用,这才是一个化学界上的大突破,因为此反应可以用来增长C原子的数目,解决了一个化学界中的难题,故此反应的应用也在逐步扩大,在化学界中有着广泛的应用,我参考过一些研究论文,以此基础来研究的反应挺多的,如利用重氮甲烷为重氮化试剂,以非天然N—Fmoc —α—氨基酸为原料,运用Arndt-Eistert来研究合成8个对应的同系物手性非天然N—Fmoc—β—氨基酸。
基于上文所述,故本文主要介绍一些关于
Arndt-Eistert反应的合成机理、发现过程、反应过程、碳链加长、及一些简单的应用实例。
(3)在适当的试剂和催化剂(胶态银、铂、铜)存在条件下,重氮酮重排同时失去氮。
有水存在时得到酸,有醇存在时得到酯,当有氨或胺存在时则生成酰胺。
RCOCHN2+HOH Ag
RCH2CO2H+N2
RCOCHN2+R`OH Ag
RCH2CO2R`+N2
RCOCHN2+NH3Ag
RCH2CONH2+N2
RCOCHN2+R`NH2Ag
RCH2CONHR`+N2
2.发现历程
沃尔夫(Wolff)发现重氮酮能转变成酸的衍生物,此反应称为沃尔夫重排,例如沃尔夫发现ω—重氮苯乙酮(C6H5COCHN2)用乙酸铵和氧化银处理得到苯基乙酰胺C6H5CH2CONH2,产率很好,在当时无任何使用价值,因为重氮酮需通过一系列复杂的反应来制备,等到发现了制备重氮酮的办法后,沃尔夫重排反应应用于合成。
阿恩特和其共同合作者指出当酰氯慢慢加入过量的重氮甲烷溶液时,得到几乎定量产率的重氮酮,他们认为发生了下列反应。
RCOCl+CH2N2RCOCHN2+HCl ①
HCl+CH2N2CH3Cl+N2②
RCOCHN 2+HCl
RCOCH 2Cl+N 2 ③
最初的反应是形成重氮酮,同时放出氯化氢①,氯化氢和第二分子重氮甲烷作用形成氯甲烷②,若任有一些氯化氢在这种反应中没销毁,则和重氮酮作用得到ω—氯甲酮。
一般来说,重氮甲烷经常保持过量,则反应③被限制到很小程度。
因为过量的重氮甲烷几乎随着氯化氢的生成立即与它反应。
3.碳链加长
阿恩特和艾斯特研究了沃尔夫重排并指出反应非常通用,并指出联合由酰氯形成重氮酮和沃尔夫重排这两个反应构成了增长碳链的新方法(增加了一个亚甲基)
这个反应可能是重氮甲烷首先亲核进攻羰基的碳原子形成不稳定的中间产物(Ⅱ),自动除去HCl 得到重氮酮(Ⅲ)(一般情况下能分离出来)。
R
Cl
N
N
H
C H
N N
Ⅰ
Ⅱ
-HCl
C
R
O
N
-N
N
C
R
O
R
(Ⅲ)重氮酮
(Ⅳ)(Ⅴ)烯酮
重氮酮迅速放出氮,同时或随即发生R(带着它的一对电子)的重排反应得到烯酮(V )(烯酮在某些情况下能分离出来)。
烯酮和反应混合物中的水、醇、氨或胺反应得到相应的酸及其衍生物,反映的最终结果是在原来酸的羧基和α—碳原子之间加了一个—CH2—原子团。
HOOC-CH22
R O C
C
H
R
R'OH
RCH2CO2
R'
2
(V)
RCH22CONHR'
4.反应机理
5.应用
从反应机理可以看出这个合成方法是将一个酸经过三步反应转变为高一级的同系物,整个产率通常为50—80﹪,这个合成方法不包括强烈还原步骤,因此可以用来制备对还原剂敏感的化合物,例如硝基苯基乙酸能由硝基苯甲酰氯制
备产率很好。
COCL
NO 2
NO 2
COCHN
2NO 2
CH 2CO 2H
二元酸可通过它的酸性酯转变为高一级的同系物,而用其他方法难于完成这个合成。
例如戊二酸通过中间化合物酯酰氯转变为己二酸。
CH 2COCL
CH 2CH 2CO 2C 2H 5
2CH 2CO 2C 2H 5
CH 2COCHN 2CH 2CH 2CO 2CH 3CH 2CH 2CO 2C 2H 5
CH 2CH 2CO 2H 2CH 2CO 2H
这个合成方法在较低温度下进行,因此参加反应的物质分解的机会不像其它
合成中那样大,所以应用于合成复杂分子是很理想的,例如性激素的合成。
阿恩特—艾斯特合成亦能应用于杂环化合物。
例如:
S
CO 2H
S
CH 2CO 2H
2-(thiophen-2-yl)acetic acid thiophene-2-carboxylic acid
α-噻吩甲酸 α-噻吩乙酸
O
CO 2H
O
CH 2CO 2H
2-(benzofuran-3-yl)acetic acid
benzofuran-3-carboxylic acid
苯并呋喃-3-甲酸 苯并呋喃-3-乙酸 具有空间阻碍的酸的酰氯不能和重氮甲烷作用,例如同樟脑酸的酸性酯的酰氯,在这个化合物中酰氯基连于第三级碳原子上,另一个例子为2,4,6—三甲基苯甲酰率。
CH 3
COCl
H 3C
CH 3
2,4,6-trimethylbenzoyl chloride
C
CH 3
COCl C CH 3
C H
H 3C H 2C
CH 2CO 2CH 3
H 2C
methyl 2-(3-(chlorocarbonyl)-2,2,3-trimethylcycloheptyl)acetate 2,4,6-三甲基苯甲酰率
干扰因素
某些官能团如酚羟基,醛基,活泼亚甲基及α,β—不饱和羰基能和重氮甲烷作用,因此些官能团在合成中会发生干扰,所以在底物中不能有这些物质存在。
【参考文献】
1. 百度、互动百科
2. 维基百科全书
3. 研究生论文《运用Arndt-Eistert 来研究合成同系物手性非天然N —Fmoc —β—氨基酸》
4. 维普论文网
5. A. Wolff, Ann 394, 25 (1912).
6. F. Arndt, B. Eistert and W. Partale, Ber , 60 ,1364 (1927).
7. F. Arndt, B. Eistert and J. Amende, Ber, 61, 1949 (1928).
8. F. Arndt, J. Amende, Ber, 61 1122 (1928).
9. Yu , L.-C; Names Reaction In Organic Chemistry 284,322 (1984) (in Chinese). (俞凌翀 有机化学中的人名反应284,322 (1984)). 10. F. Arndt, B. Eistert, Ber, 68, 200 (1935). 11. 维基百科(沃尔夫重排反应)。
