难溶电解质的溶度积常数
高考难点:溶度积常数及其应用讲解

高考难点:溶度积常数及其应用一、沉淀溶解平衡中的常数(K sp)——溶度积1. 定义:在一定温度下,难溶电解质(S<0.01g)的饱和溶液中,存在沉淀溶解平衡,其平衡常数叫做溶度积常数(或溶度积)2. 表示方法:以M m A n(s) mM n+(aq) + nA m-(aq)为例(固体物质不列入平衡常数),K sp=[c(M n+)]m·[c(A m-)] n,如AgCl(s)Ag+(aq) + Cl-(aq),K sp=c(Ag+)·c(Cl-)。
3. 影响溶度积(K sp)的因素:K sp只与难容电解质的性质、温度有关,而与沉淀的量无关,并且溶液中的离子浓度的变化只能使平衡移动,并不改变溶度积。
4. 意义:①K sp反映了难溶电解质在水中的溶解能力,当化学式所表示的阴、阳离子个数比相同时,K sp数值越大的难溶电解质在水中的溶解能力相对越强;②可以用K sp来计算饱和溶液中某种离子的浓度。
二、判断沉淀生成与否的原则——溶度积规则通过比较溶度积与溶液中有关离子浓度幂的乘积——离子积(Q c)的相对大小,可以判断难溶电解质在给的条件下沉淀能否生成或溶解:1.Q c>K sp,溶液过饱和,既有沉淀析出,直到溶液饱和,达到新的平衡;2.Q c=K sp,溶液饱和,沉淀与溶解处于平衡状态;3.Q c<K sp,溶液未饱和无沉淀析出,若加入过量难溶电解质,难溶电解质溶解直至溶液饱和。
三、对溶度积的理解1. 溶度积和溶解度都可以用来表示物质的溶解能力,只与温度有关,而与难溶电解质的质量无关。
2. 用溶度积直接比较不同物质的溶解性时,物质的类型应相同。
对于化学式中阴、阳离子个数比不同的难溶电解质,不能通过直接比较K sp的大小来确定其溶解能力的大小(要分析溶解时所需最小浓度决定)。
3. 溶液中的各离子浓度的变化只能使沉淀溶解平衡移动,并不改变溶度积。
4. 当表达式中的浓度是表示平衡时的浓度时,要用[]符号表示,且此时的溶液为饱和溶液。
难溶电解质的溶解平衡的计算

解:(1)设AgCl的浓度为S1(mol/L),则:
AgCl(s)
Ag+(aq) + Cl-(aq)
ቤተ መጻሕፍቲ ባይዱ
平衡
S1
S1
K S sp
2 1
= 1.56 10-10
S1 1.25 105 mol / L 1.25 105 143 .5g / L
(1)溶度积与溶解度之间的关系
例1、已知Ksp,AgCl= 1.56 10-10, Ksp,Ag2CrO4= 9.0 10-12,试求AgCl和Ag2CrO4的溶解度(用g/L表示)
Ag+或Cl-浓度由小到大的顺序为④ < ① < ③ < ② < ⑤ ,故
AgCl的溶解度由 大到小的顺序为④ > ① > ③ > ② > ⑤。
答案:B
Ksp(Ag2CrO4 )=1.1×10-12 mol3•L-3 ] 提醒:难溶电解质溶解性的强弱可由其饱和溶液中 该难溶电解质的物质的量浓度的大小来衡量, 大者,溶解性强。也可计算出初中所学的溶解 度(单位:克),然后比较,大者,溶解性强。 两者不一致时,以前者为准。
Ag2CrO4(s)
2Ag + + CrO42-
解析:由于[Ag+] ·[Cl-]=KSP , Ag+或Cl-的浓度 越大,越能抑制AgCl的溶解, AgCl的溶解度就越小。
①[Cl-]=0.01mol·L-1
②[Cl-]=0.04mol·L-1
③[Cl-]=0.03mol·L-1
④[Cl-] =0mol·L-1
⑤[Ag+] =0.05mol·L-1
通式:AnBm(s)
nAm+(aq) + mBn-(aq)
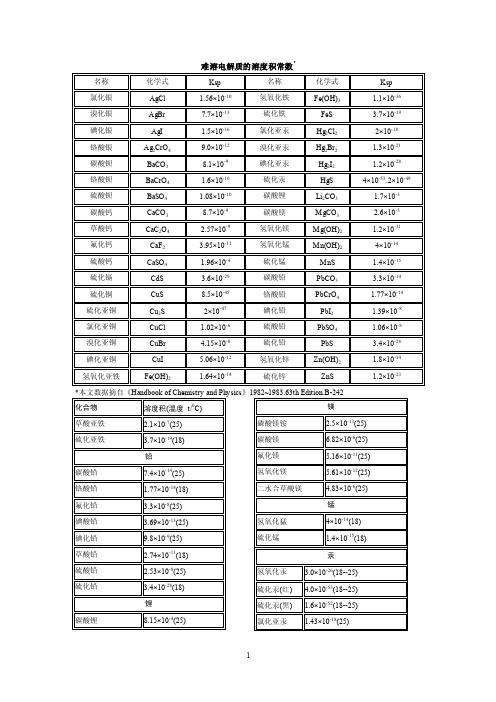
难溶电解质的溶度积常数
亚砷酸(H3AsO3) 25 正硼酸(H3BO3) 20 碳酸(H2CO3) 25
25
5.1×10-10 9.29 5.4×10-10 9.27 1 4.5×10-7 6.35 2 4.7×10-11 10.33
焦磷酸(H4P2O7) 20 25 25 25
1 1.2×10 0.91 2 7.9×10 2.10 3 2.0×10 6.70 4 4.8×10 9.32
氢氧化汞 硫化汞(红) 硫化汞(黑) 氯化亚汞
3.0×10-26(18--25) 4.0×10-53(18--25) 1.6×10-52(18--25) 1.43×10-18(25)
1
碘化亚汞 溴化亚汞
硫化镍(a) (ß) (r)
5.2×10-29(25) 6.4×10-23(25)
镍 3.2×10-19(18--25) 1.0×10-24(18--25) 2.0×10-26(18--25)
难 溶电 解质的 溶度 积常数 *
名称
化学式
Ksp
名称
化学式
Ksp
氯化银 溴化银
AgCl AgBr
1.56×10-10 7.7×10-13
氢氧化铁 硫化铁
Fe(OH)3 FeS
1.1×10-36 3.7×10-19
碘化银 铬酸银 碳酸钡 铬酸钡 硫酸钡 碳酸钙 草酸钙 氟化钙 硫酸钙 硫化镉 硫化铜 硫化亚铜 氯化亚铜 溴化亚铜
50g(NH4)2SO4 溶于 100ml 热水,冷却后过滤
溶解 69.5gFeSO4·7H2O 于适量水中,加入 5ml18mol·L-1 H2SO,用水稀释至 1L,置入小铁钉数枚
溶解 12.2g 锑粉于 50ml 浓 HNO3 微热,使锑粉全部作用成白色粉末, 用倾析法洗涤数次,然后加入 50ml6mol·L-1NaOH 溶解,稀释至 1L
难溶电解质的溶度积与溶解度之间的关系

难溶电解质的溶度积与溶解度之间的关系在化学溶解度常数的研究中,我们经常会遇到难溶电解质。
它们是指在水中溶解度非常小的电解质物质,比如银氯化物、铅碘化物等。
在研究这些物质时,我们需要了解它们的溶度积与溶解度之间的关系,这有助于我们更深入地理解溶解度常数的概念。
1. 溶度积的定义溶度积是指在一定温度下,难溶电解质在水中达到溶解平衡时,其离子浓度的乘积。
以银氯化物(AgCl)为例,其离子方程式为AgCl ⇄Ag⁺ + Cl⁻,在溶解平衡时,Ag⁺和Cl⁻的浓度分别为x,那么AgCl的溶度积Ksp就等于x²。
对于难溶电解质来说,Ksp的值通常非常小,代表其溶解度极低。
2. 溶解度与溶度积的关系难溶电解质的溶解度通常定义为单位体积溶液中难溶物质的质量。
溶解度是溶液饱和时,溶液中包含的物质的量,可以用溶度积来表达。
具体而言,当难溶电解质达到溶解平衡时,其溶解度与溶度积之间的关系为溶解度=√(Ksp)。
这表明,溶解度与溶度积之间存在平方根的关系。
3. 溶度积与溶解度的意义溶度积和溶解度的关系对我们有着重要的意义。
通过溶度积,我们可以了解难溶电解质在溶解平衡时离子的浓度,从而推导出其溶解度。
溶度积和溶解度的关系也是我们研究难溶电解质在水溶液中的行为和性质时的重要依据。
它还可以帮助我们预测在不同条件下溶液中难溶电解质的溶解度变化。
总结回顾通过上述分析,我们不难发现,难溶电解质的溶度积与溶解度之间存在着明显的关系。
溶度积是在溶解平衡下离子浓度的乘积,而溶解度则是溶液饱和时单位体积溶液中难溶物质的质量,其与溶度积之间存在平方根的关系。
这种关系帮助我们更深入地了解难溶电解质的溶解特性,以及在不同条件下其溶解度的变化规律。
个人观点对于难溶电解质的溶度积与溶解度之间的关系,我个人认为应该结合实际,在化学实验中进行验证和观察,以更加深入地了解其内在规律。
我们也可以进一步探讨难溶电解质的相关性质和应用,从而拓展对这一主题的理解和认识。
第8章 难溶电解质的沉淀溶解平衡1-溶度积常数

国
O
O
C
M
国
大
学
中
O
O
C
M
国
大
学
中
O
O
C
O
O
C
M
国
大
学
中
<0.1g /100g H2O
中
C
O
M
O
大
学
国
中
C
O
M
O
大
学
国
中
C
O
M
O
大
学
国
中
C
O
M
O
大
学
国
中
中
中
中
中
中
中
国
国
国
国
国
国
大
大
大
大
大
大
学
M
O
O
C
学
学
学
学
学
M
M
M
M
M
O
O
O
O
O
O
O
O
O
O
C
C
C
C
C
水是最常见的溶剂,任何物质在水中都有一定的溶解度,
国
中
难溶电解质
AB型:
C
M
O
O
C
M
O
O
C
M
O
O
C
M
O
O
C
O
M
O
M
O
O
C
θ 较大者,其 S 较大;
对组成类型相同的难溶电解质,sp
大
难溶电解质的溶度积

难溶电解质的溶度积溶度积严格地说,在水中绝对不溶的物质是不存在的。
通常将溶解度小于0.01 g/L的物质称为难溶电解质。
例如,在一定温度下,将过量AgCl固体投入水中,Ag+和Cl-离子在水分子的作用下会不断离开固体表面而进入溶液,形成水合离子,这是AgCl的溶解过程。
同时,已溶解的Ag+和 Cl-离子又会因固体表面的异号电荷离子的吸引而回到固体表面,这就是AgCl的沉淀过程。
当沉淀与溶解两过程达到平衡时,此时的状态称为沉淀溶解平衡。
溶解AgCl(s) ==== Ag+ + Cl-(未溶解固体) 沉淀 (已溶解的水合离子)根据平衡原理,其平衡常数可表示为但因c(AgCl)为常数,a(Ag+) = c(Ag+), a(Cl-) = c(Cl-)故上式可写成∴ a(Ag+) ´ a(Cl-) = c(Ag+) ´ c(Cl-) = K Ө = Ksp Ө即为多相离子平衡的平衡常数,称为溶度积常数(可简称溶度积)。
对于一般的难溶电解质AmBn的沉淀溶解平衡AmBn(s) ==== mAn+ + nBm-Ksp=c^m(An+)×c^n(Bm-)上式的意义是:在一定温度下,难溶电解质饱和溶液中各离子浓度幂的乘积为一常数。
严格地说,应该用溶解平衡时各离子活度幂的乘积来表示。
但由于难溶电解质的溶解度很小,溶液的浓度很稀。
一般计算中,可用浓度代替活度。
Ksp的大小反映了难溶电解质溶解能力的大小。
Ksp越小,则该难溶电解质的溶解度越小。
Ksp的物理意义;(1)Ksp的大小只与此时温度有关,而与难溶电解质的质量无关;(2)表达式中的浓度是沉淀溶解达平衡时离子的浓度,此时的溶液是饱和或准饱和溶液;(3)由Ksp的大小可以比较同种类型难溶电解质的溶解度的大小;不同类型的难溶电解质不能用Ksp比较溶解度的大小。
编辑本段溶解度和溶度积的相互换算Ksp与S均可判断溶解度大小,二者有无关系?根据溶度积常数关系式,可以进行溶度积和溶解度之间的计算。
第六章难溶电解质的沉淀-溶解平衡

四、同离子效应和盐效应
[ SO4 ] [Ca 2 ] K SP (CaSO4 ) K 2 [CO3 ] [Ca 2 ] K SP (CaCO3 )
当KSP(CaCO3)<<KSP(CaSO4)时,K很大,反 应正向进行;即由一种难溶物转化为另一种更难溶 的物质。
墨西哥“水晶洞”:世界上最大的自然水晶洞
H 2 S 2H 2O S 2H3O
K K a1 K a 2
[ S 2 ] [ H 3O ]2 [H 2S ]
(二)发生氧化还原反应使沉淀溶解 难溶硫化物的溶解 3CuS(s)+8HNO3(aq)=3Cu(NO3)2(aq)+
3S(s)+2NO(g)+4H2O(l)
CaCO3 + H3O+ Ca2+ + H2CO3 +H2O
例:25℃时,欲使0.010molZnS溶于1.0L盐酸中, 求所需盐酸的最低浓度? 解:ZnS(s) + 2H+(aq) c0 0.01 x ceq 0 x-0.02 Zn2+(aq) + H2S(aq) 0 0 0.01 0.01
K SP ( ZnS) [Zn 2 ] [ H 2 S ] [ S 2 ] K 2 [ H ]2 [ S ] K a1 ( H 2 S ) K a 2 ( H 2 S )
离子积常数与溶度积常数

离子积常数与溶度积常数
难溶电解质溶液中,其离子浓度计量系数的指数方次的乘积为离子积用Q表示;难溶电解质尽管难溶,但还是有一部分阴阳离子进入溶液,同时进入溶液的阴阳离子又会在固体表面沉积下来。
当这两个过程的速率相等时,难溶电解质的溶解就达到平衡状态,固体的量不再减少,这样的平衡状态叫溶解平衡,其平衡常数叫溶度积常数。
两者的区别是:离子积是任意情况下的有关离子浓度方次的乘积,而溶度积是沉淀溶解平衡时有关离子浓度方次的乘积。
难溶电解质溶度积常数

第三章第四节难溶电解质的溶解平衡—难溶电解质的溶度积常数【学习目标】1.正确理解和掌握溶度积K sp的概念,熟知溶度积常数的应用2.能应用溶度积常数K sp进行相关的计算。
【学习重、难点】能应用溶度积常数K sp进行相关的计算。
【知识梳理】一、难溶电解质的溶度积常数(K sp)1.概念:一定温度下,难溶电解质在溶液中达到沉淀溶解平衡状态时,各离子浓度保持不变,该沉淀溶解平衡的平衡常数称之为溶度积常数,简称,用表示。
2.表达式:对于沉淀溶解平衡M m A n mM n+(aq)+nA m-(aq),参照电离平衡原理得平衡常数:K sp =3.影响因素:(1)K sp只与难溶电解质的性质和有关,而与沉淀的量和溶液中的离子浓度无关。
并且溶液中的离子浓度的变化能使平衡移动,并不改变K sp。
(2)对于大部分溶解平衡,升高温度,平衡向移动,K sp,Ca(OH)2除外。
4.意义:K sp反映了难溶电解质在水中的溶解能力,当化学式所表示的阴、阳离子个数比相同时,K sp越大的难溶电解质在水中的溶解能力相对越强,溶解度。
但对化学式所表示的组成中阴、阳离子个数比不相同的电解质,则不能直接由它们的溶度积来比较溶解能力的大小,必须通过具体计算确定。
下表是几种难溶电解质的溶度积以及溶解能力的比较:沉淀溶解平衡K sp(18~25℃)溶解能力比较AgCl(s)Cl-(aq)+Ag+(aq) 1.8×10-10mol2. L-2AgCl> AgBr > AgI AgBr(s)Br-(aq)+Ag+(aq) 5.0×10-13mol2.L-2AgI(s)I-(aq)+Ag+(aq)8.3×10-17mol2.L-2Mg(OH)2(s)Mg 2+(aq)+2OH-(aq)1.8×10-11mol3.L-3Mg(OH)2> Cu(OH)2Cu(OH)2(s)Cu 2+(aq)+2OH-(aq)2.2×10-20mol3.L-35.应用—溶度积规则:比较K sp与溶液中有关离子浓度幂的乘积(离子积Q c)判断难溶电解质在给定条件下沉淀能否生成或溶解。
5第四章难溶强电解

析出,直至溶液达饱和为止。
18
沉淀反应的利用和控制
l.沉淀的生成
2.沉淀的溶解
19
沉淀的生成
l.加入沉淀剂
增大离子浓度,使溶液中Qi大于Ksp
2.控制溶液的pH值 对于氢氧化物沉淀和弱酸盐沉淀可通过加碱, 提高pH,使沉淀生成。
20
பைடு நூலகம்
加入沉淀剂
将等体积的2.0×10-3mol· -1 AgNO3溶液和2.0×10 L
-4
mol· -1NaCl溶液混合,能否析出AgCl沉淀? L 解: 混合后,溶液中
c(Ag+)=2.0×10-3/2=1.0×10-3 mol· -1 L
c(Cl-)=2.0×10-4/2=1.0×10-4 mol· -1 L
Qc =c(Ag+)· c(Cl-)=1.0×10-7
已知KspӨ(AgCl)=1.8×10-10
Kspө称为难溶强电解质的标准溶度积,简称溶度积
MmAn(s)
θ sp
mMn++nAmn m
K (M m A n ) [M
] [A
m n
]
4
难溶强电解质的溶解度
对于难溶强电解质MA,
K
MA(s)
M+ + A
设MA的溶解度为S mol· -1,则 L
S/cθ=[M+]=[A-]
[M ][A ] K
a M a A K a MA(s) K
溶度积
一定温度下,对确定的难溶强电解质,Kθap为常数, 称为活度积常数,按照活度的定义,可变为:
θ ( M [M ]) ( A [A ]) K ap
难溶电解质的溶度积与溶解度的关系

难溶电解质的溶度积与溶解度的关系1. 难溶电解质的概念难溶电解质是指在水中溶解度非常小的电解质,即使在饱和溶液中也很难溶解。
通常来说,难溶电解质的溶解度小于0.1mol/L。
这类物质在水中的溶解度十分有限,常常需要一定的条件或者较长的时间才能达到饱和。
2. 溶度积的概念溶度积是指在一定温度下,固体电解质在溶液中达到饱和时,其浓度乘积的值。
对于一般的电解质,其溶度积等于它的溶解度(mol/L)的n次方,其中n是电解质溶解时生成的离子数。
3. 难溶电解质的溶度积对于难溶电解质来说,由于它们在水中的溶解度极低,因此其溶度积也会非常小。
对于银氯化物(AgCl),其溶度积表达式为[K+] * [Cl-] = 1.8*10^-10,可以看出其溶度积的值非常小,说明了它在水中的溶解度很低。
4. 溶度积与溶解度的关系溶度积表示了固体电解质在溶液中达到饱和时的离子浓度乘积,而溶解度则是指在一定温度下,单位体积溶液中能溶解固体电解质的量。
二者是密切相关的,溶解度积的大小决定了电解质在水中的溶解度大小。
5. 个人观点和理解从溶度积和溶解度的关系来看,溶度积可以被看作是电解质在水溶液中溶解程度的衡量标准。
对于难溶电解质来说,其溶度积很小,导致其溶解度也非常低。
在化学实验和生产中,我们常常会根据溶度积的大小来判断一个物质在水中的溶解程度,这对于溶液的制备和纯度的控制都有着重要的意义。
总结回顾难溶电解质的溶度积与溶解度的关系,是化学中重要的概念之一。
通过对这一概念的深入理解,我们能更好地把握电解质在水溶液中的溶解特性,进而为化学实验和产业生产提供参考依据。
以上就是我对于难溶电解质的溶度积与溶解度的关系的见解和探讨,希望对您有所帮助。
难溶电解质是指在水中溶解度非常小的电解质,即使在饱和溶液中也很难溶解。
通常来说,难溶电解质的溶解度小于0.1mol/L。
这类物质在水中的溶解度十分有限,常常需要一定的条件或者较长的时间才能达到饱和。
难溶电解质的溶解平衡(全)

练
习
1、下列说法中正确的是( C ) A.物质的溶解性为难溶,则该物质不溶于水 B.不溶于水的物质溶解度为0 C.绝对不溶解的物质是不存在的 D.某粒子被沉淀完全是指该粒子在溶液中的浓度为零
Ksp 只与温度有关
3.Ksp的意义 Ksp反映了难溶电解质在水中的溶解能力。 ①对于同类型物质,Ksp数值越大,难溶电解质在水中的溶解能越
强。如由Ksp数值可知(p61),溶解能力:AgCl>AgBr>AgI, Cu(OH)2<Mg(OH)2 ②不同类型的物质,Ksp差距不大时不能直接作为比较依据。如某温 度下:AgCl(s) Ag+(aq)+Cl-(aq),Ksp=1.8×10-10 Mg(OH)2(s) Mg2+(aq)+2OH-(aq),Ksp=5.6×10-12 虽然Mg(OH)2的Ksp较小,但不能认为Mg(OH)2比AgCl更难溶。
溶度积的应用练习
(1)已知溶度积求离子浓度:
例1. 已知室温下PbI2的溶度积为7.1×10-9,求 2+和I-的浓度;在c(I-)=0.1mol· -1 饱和溶液中Pb L 的溶液中, Pb2+的浓度最大可达到多少?
解: PbI2(s)
Pb2+(aq) + 2I- (aq)
Ksp =c (Pb2+) · 2(I-) c c (Pb2+) = Ksp/c2(I-) =7.1×10-9/0.12 =7.1×10-7mol· -1 L
×100g÷1000g = 1.9×10-4g
1、向含有AgCl(s)的饱和AgCl溶液中加水,下列叙述正确 的( B ) A.AgCl的溶解度增大 B.AgCl的溶解度、Ksp均不变 C.Ksp(AgCl)增大 D.AgCl的溶解度、Ksp均增大 2、在饱和的CaSO4 溶液中下列哪种物质不存在( D ) A.Ca2+ B.SO42- C.H+ D.H2SO4
五大平衡常数的比较和应用
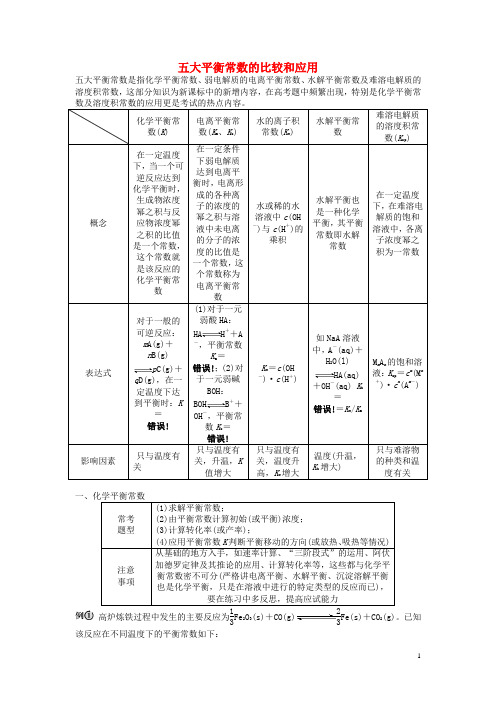
五大平衡常数的比较和应用五大平衡常数是指化学平衡常数、弱电解质的电离平衡常数、水解平衡常数及难溶电解质的溶度积常数,这部分知识为新课标中的新增内容,在高考题中频繁出现,特别是化学平衡常数及溶度积常数的应用更是考试的热点内容。
化学平衡常数(K ) 电离平衡常数(K a 、K b ) 水的离子积常数(K w ) 水解平衡常数 难溶电解质的溶度积常数(K sp )概念 在一定温度下,当一个可逆反应达到化学平衡时,生成物浓度幂之积与反应物浓度幂之积的比值是一个常数,这个常数就是该反应的化学平衡常数 在一定条件下弱电解质达到电离平衡时,电离形成的各种离子的浓度的幂之积与溶液中未电离的分子的浓度的比值是一个常数,这个常数称为电离平衡常数水或稀的水溶液中c (OH -)与c (H +)的乘积 水解平衡也是一种化学平衡,其平衡常数即水解常数 在一定温度下,在难溶电解质的饱和溶液中,各离子浓度幂之积为一常数 表达式 对于一般的可逆反应:m A(g)+n B(g) p C(g)+q D(g),在一定温度下达到平衡时:K =错误! (1)对于一元弱酸HA :HA H ++A -,平衡常数K a =错误!;(2)对于一元弱碱BOH :BOH B ++OH -,平衡常数K b =错误!K w =c (OH -)·c (H +) 如NaA 溶液中,A -(aq)+H 2O(l) HA(aq)+OH -(aq) K h =错误!=K w /K a M m A n 的饱和溶液:K sp =c m (M n+)·c n (A m -) 影响因素 只与温度有关 只与温度有关,升温,K 值增大 只与温度有关,温度升高,K w 增大 温度(升温,K h 增大) 只与难溶物的种类和温度有关一、化学平衡常数常考 题型 (1)求解平衡常数;(2)由平衡常数计算初始(或平衡)浓度;(3)计算转化率(或产率);(4)应用平衡常数K 判断平衡移动的方向(或放热、吸热等情况)注意 事项 从基础的地方入手,如速率计算、“三阶段式”的运用、阿伏加德罗定律及其推论的应用、计算转化率等,这些都与化学平衡常数密不可分(严格讲电离平衡、水解平衡、沉淀溶解平衡也是化学平衡,只是在溶液中进行的特定类型的反应而已),要在练习中多反思,提高应试能力高炉炼铁过程中发生的主要反应为13Fe 2O 3(s)+CO(g)23Fe(s)+CO 2(g)。
第七章_难溶电解质的沉淀-溶解平衡

则沉淀会溶解
8
离子积(或浓度商)J与溶度积Ksp°两者的
区别为∶ J表示难溶电解质达到沉淀-溶解平衡时或 未达到沉淀-溶解平衡时各离子浓度幂的乘
积。Ksp°表示难溶电解质达到沉淀-溶解平 衡时,溶液中各离子浓度幂的乘积。Ksp° 只是J的一个特例。在一定温度下,Ksp°是
一常数,而J不是常数。
9
第二节 沉淀-溶解平衡的移动
15
二、沉淀的溶解
当J <Ksp0 时沉淀发生溶解,使J 减小的
方法有
(1)生成弱电解质。 a、生成弱酸。例如难溶性弱酸盐:
FeS (s)+2H+
Fe2++H2S
K K 0 [F [2 ] H ]2 e [2 S H ][F [2 ] H ]2 e [2 S H ] [ [2 2 S S ] ]K a 0 s0 1 K F pa 0 2 ,e S6 .7 130
Ks0p(Ka0)2 5.51108 (KW 0 )2
可见Mg(OH)2易溶于HAc。
17
c、生成弱碱。例如:
Mg(OH)2 (s)+2NH4+
Mg2++2NH3H2O
K 0[M [2 N ]4 g []2H N 3]2 H [M [2 N ]4 g []2H N 3]2 H [ [O O- -] ]H H 2 2
解:(1)设AgCl的溶解度为S1(mol·L-1),则:
AgCl(s)
Ag+(aq) + Cl-(aq)
平
S1
S1
Ksp S12
S11.34105
(2)设Ag2CrO4的溶解度为S2(mol·L-1),则:
难溶电解质的沉淀与溶解

由于 CSO42-=0.001mol/l,CBa2+ =0.001mol/l 等量反应
但反应后 BaSO4 → Ba2+ + SO42- 沉淀溶解平衡仍存在 [Ba2+][SO42-] = Ksp (BaSO4) =1.1x10-10 [Ba2+]=(Ksp)1/2=10-5mol/l >10-6 故 不完全沉淀.
NH4Cl加入后,具有同离子效应,或者说NH3 与NH4+组 成缓冲溶液,则:
pOH pKb lg cNH 3 / cNH 4 lg 3105 lg1.8105 lg 0.16
cNH 4
CNH4+=0.096mol/dm3
WNH4Cl 0.096 0.1 53.5 0.513 g
[H+]在0.85 ~2.7x10-3moldm-3之间ZnS沉淀
例3. 将0.080dm3, 0.20 mol·dm-3的氨水和0.020 dm3,
0.10 mol·dm-3的MgCl2溶液混合后,(1)有无Mg(OH)2 沉淀生成?(2)要使体系中不产生Mg(OH)2沉淀,可在 溶液中加入固体NH4Cl,问加入NH4Cl多少克可达到 此目的? (Kөsp (Mg(OH)2)=1.8×10-11, Kөb (NH3)=1.8×10-5, M(NH4Cl)=53.5)
X= [Ba2+]=Ksp/ [SO42-]=1.1x10-10/0.001 =1.1x10-7mol/l Ba2+可沉淀完全
结论: 1. 沉淀的产生及完全程度主要与Ksp的大小有关。
( Ksp小的物质,易于产生沉淀;且易完全沉淀.) 2. 对于Ksp稍大的物质,可加入过量沉淀剂使其完全沉 淀;沉淀剂不宜过量50%(a.防止盐效应发生。b. 沉淀 剂与沉淀形成配合物等)
溶度积

溶度积自然界没有绝对不溶解的物质,许多通常认为不溶于水的物质也有微弱溶解于水的倾向,例如难溶盐氯化银在水中存在沉淀与溶解平衡。
在一定温度下,Ag+浓度和Cl-浓度的乘积为一定值。
如果对一般难溶盐强电解质在水中同样存在A mB n=mA++nB-在一定温度下,则K ap=[A+]m [B-]n式中Ksp为常数,它反映了物质的溶解能力,故称溶度积常数,简称溶度积。
其意义:在难溶强电解质饱和溶液中,组成该物质的各离子浓度的系数次方之积,在一定温度下为该物质固有的常数。
所谓难溶强电解质,可以是盐,亦可以是碱。
严格说,Kap应是难溶电解质在其饱和溶液中离子活度的系数次方之积,称为活度积。
因难溶电解质其溶度积很小,离子浓度近似地等于活度。
任何难溶电解质,不管它的溶解度多么小,在其饱和溶液中总有与其达成平衡的离子。
任何沉淀反应,无论它进行得多么完全,溶液中仍依然存在组成它的离子,而且其离子浓度系数次方之积必为常数。
只不过随难溶电解质的溶解能力的差异,Ksp 值有所不同。
溶度积可由该难溶电解质的溶解度求得。
例如,设氯化铅在水中的溶解度为s(mol·L-1),该盐在饱和溶液中完全电离(s)Pb2+(aq)+2Cl-(aq)PbClPb2+的浓度为s,Cl-的浓度为2s,故Ksp=〔Pb2+〕〔Cl-〕2=s(2s)2=4s3(mol3·L-3)溶度积的应用很广泛。
在定性分析中,利用金属硫化物、氢氧化物、碳酸盐等溶度积的差异分离金属离子。
若往氯化铅饱和溶液中加入氯化钾时,溶液中Cl-浓度增大,Pb2+和Cl-的浓度系数次方之积较氯化铅的溶度积大,这时将有部分离子发生Pb2++2Cl---→PbCl2的反应,将过剩的PbCl2沉淀出来,直至两种离子的浓度系数次方之积等于氯化铅的溶度积为止。
因此,为使溶解度小的物质完全沉淀,需要加入含有共同离子的电解质。
一些常见的难溶电解质的Ksp值见下表。
难溶电解质的溶度积常数25℃。
难溶电解质离子浓度的乘积就是该物质的标准溶度积常数。

难溶电解质离子浓度的乘积就是该物质的标准溶度积常数。
溶度积是一个有趣的物理概念,是指个别电解质在溶解中形成电解质离子浓度的乘积。
它提供了量子化学学科对离子双向反应的关键概念,用于解释物质溶解过程中发生的一些电解反应机制。
标准溶度积是一种特殊形式,即溶度积值(Ksp)。
它量化了两种离子浓度的乘积以及由混合电解质引起的共存双离子离子的溶解过程,衡量两种电解质的性质的综合相融。
它不仅是一种非常重要的电化学参量,而且还是配体结合与分子结构的简单方法。
标准溶度积是通过计算两种不同物质在溶解时的离子浓度乘积来获得的,也就是说标准溶度积就是这种物质离子浓度乘积的“浓度单位”,它表明在标准温度和压力下,一定体积中溶液中电解质离子浓度的乘积作为计量标准。
它可以精确地表示某种物质在一定条件下的溶解性,这对于了解物质溶解性、混合溶解物稳定性等方面具有重要作用。
总之,标准溶度积是用来量化某种物质离子浓度乘积的重要物理指标,对于其精确的测量非常有用。
只有真正了解到标准溶度积的作用才能更好地利用它,并开发出一些实用的应用。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
难溶电解质的溶度积常数(K sp )
(13年新课标Ⅰ)11.已知K sp(AgCl)=1.56×
10-10,K sp(AgBr)=7.7×10-13,K sp[Ag 2(CrO 4)]=9.0×10-12,某溶液中含有Cl - 、Br -和CrO 42-,浓度均为0.010mol/L ,向该溶液中逐滴加入0.010mol/L 的AgNO 3溶液时,三种阴离子产生沉淀的先后顺序为
A .Cl --、Br -、CrO 42-
B .CrO 42-、Br -、Cl -
C .Br -、Cl -、CrO 42-
D .Br -、CrO 42-、Cl -
(13年新课标Ⅱ)13.室温时,M(OH)2(s) M 2+(aq)+2OH -(aq)
K sp=a , c(M 2+)=b mol·L -1时,溶液的pH 等于
A .11()2b g a
B .11()2
a g
b C .14+11()2a g b D .14+ 11()2b g a 基于这两道高考题的迁移提升训练:
1.25 ℃时,向含有Cl -和I -的溶液中加入足量AgNO 3溶液,只生
成AgI 沉淀,下列关系式一定正确的是
A .25 ℃时,Ksp(AgI)> Ksp(AgCl)
B .原溶液中,>
C .原溶液中,c (Cl -)<c (I -)
D .原溶液中,c (Cl -)>c (I -)
2.已知:25 ℃时,K sp [Mg(OH)2]=5.6×10-12
K sp [Zn(OH)2]=1.0×10-17
K sp[Ca(OH)2]=4.0×10-6
离子浓度小于10-5mol/L时,认为该离子不存在。
则:
(1)25 ℃时,Ca(OH)2溶于水,形成的饱和溶液的物质的量浓度为。
(2)25 ℃时,欲使0.1 mol/L ZnCl2溶液中的Zn2+沉淀完全,需调节溶液的pH至少为。
(3)向含有Mg2+和Zn2+混合溶液中加入一定浓度的NaOH溶液,两种沉淀同时存在时,溶液中=。
3.已知:常温下,K sp(Ag2SO4)=1.4×10-5,物质的量浓度为0.28 mol·L-1的Na2SO4溶液与AgNO3溶液等体积混合后有沉淀析出,该AgNO3溶液的物质的量浓度不得低于______ mol·L-1。
4.已知:常温下,K sp(BaSO4)=1.1×10-10。
向BaSO4悬浊液中加入硫酸,当溶液的pH=2时,溶液中c(Ba2+)=。
5.下列对图像的叙述正确的是
A.据图①可判断可逆反应A2(g)+3B2(g) 2AB3(g)的△H>0 B.图②表示压强对可逆反应2A(g)+B(g) 3C(g)+D(s)的影响,乙的压强大
C.图③可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化
D.据图④,若除去0.1 mol·L-1 CuSO4溶液中的Fe3+,可向溶液中加入适量NaOH至pH约为7
6.根据下列实验现象得出的结论正确的是
7.已知Ag2SO4的K sp= c2(Ag+)×c(SO42-)=1.4×10-5,将适量Ag2SO4 固体溶于100 mL水中至刚好饱和,此时溶液中c(Ag+)=0.030
mol·L-1。
若t1时刻改变条件,下图中不正确的是。
