生物氧化讲义(8)
分子生物学讲义-8RNA的生物合成2

分子生物学Molecular Biology赵青天津科技大学生物工程学院Email: zhao_qing@前情回顾3. RNA的生物合成Transcription3.4 启动子和转录起始3.5 RNA转录的后加工3.6 RNA的编辑、再编码和化学修饰启动子(promoter )是指RNA 聚合酶识别、结合和开始转录的一段DNA 序列(它含有RNA 聚合酶特异性结合和转录起始所需的保守序列)。
3.4 启动子和转录起始原核生物真核生物转录起点是指与新生RNA 链第一个核苷酸相对应DNA 链上的碱基(以数字+1表示)。
3.4 启动子和转录起始原核生物真核生物聚合酶在此处与DNA结合成稳定的复合物,解开双链形成开放型起始结构。
聚合酶起始识别区,与σ因子相互作用。
TATA区---是转录精确地起始。
CAAT区和GC区---控制转录起始的频率,基本不参加起始位点的确定。
启动子预测软件有CpGPlot、CpGPrediction、Promoter 2.0、 Promotorscan等。
3.5 RNA转录的后加工原核生物RNA转录后的加工rRNA和tRNA在转录完成后,加工方式可分为3类:(1)rRNA及tRNA分子由某些新生RNA链的裂解形成。
(2)在tRNA链末端加上核苷酸(CCA)3’5’(3)碱基的修饰rRNA的碱基会被甲基化(如m C)。
tRNA分子中均含有稀有碱基,它们是由tRNA前体中的常见核苷酸经酶促修饰而成。
原核生物与真核生物mRNASD序列5’上游非编码区3’下游非编码区真核生物RNA 转录后的加工mRNA 的转录后加工: 1.加帽2.加尾3.剪接 磷酸酶 甲基化酶m 7GTP核酸外切酶RNA 末端腺苷酸转移酶RNA的剪接位点&方式I类自我剪接II类自我剪接剪接体催化的剪接5’剪接位点:内含子的5’末端3’剪接位点:内含子的3’末端分支点:位于3’剪接位点上游20-50个核苷酸之间,通常是A。
生物化学讲义第四章生物氧化

+第四章生物氧化【目的和要求】1.掌握生物氧化、氧化磷酸化的概念。
2.掌握线粒体呼吸链的组成、排列顺序、种类。
3.掌握氧化磷酸化的偶联部位,胞液中NADH的氧化,二条穿梭途径。
4.熟悉氧化磷酸化的基本过程、影响因素及其调节,P/O,ATP的生成和利用。
5.了解生物氧化的特点及方式,氧化磷酸化偶联机理,其他氧化体系。
【本章重难点】1.呼吸链组成、脱氢部位及产能部位,偶联机制。
2.氧化磷酸化概念,影响因素。
3.二种穿梭作用。
4.呼吸链组成、脱氢部位及产能部位。
5.氧化磷酸化偶联机制。
学习内容第一节概述第二节生成ATP的氧化体系第三节其他氧化体系第一节概述一、概述⒈生物氧化的概念生物氧化(Biological Oxidation)物质在生物体内氧化分解的过程称为生物氧化,主要是指糖、脂肪、蛋白质等有机物在生物体内分解时逐步释放能量,最终生成CO2和H2O的过程。
生物氧化的主要生理意义是为生物体提供能量.⒉生物氧化的过程⒊生物氧化的特点⑴相同点:体内氧化与体外氧化① 物质氧化方式:加氧、脱氢、失电子.②物质氧化时消耗的氧量、得到的产物和能量相同。
⑵不同点 :体内氧化 体外氧化 ①反应条件: 温和 剧烈 ②反应过程:分步反应,能量逐步释放 一步反应,能量突然释放 ③产物生成: 间接生成 直接生成 ④能量形式: 热能、ATP 热能、光能第二节 生成ATP 的氧化体系一、呼吸链 (Respiratory Chain)⒈呼吸链(respiratory chain ):一系列酶和辅酶按照一定的顺序排列在线粒体内膜上,可以将代谢物脱下的氢(H ++e )逐步传递给氧生成水同时释放能量,由于此过程与细胞摄取氧的呼吸过程有关,所以这一传递链称为呼吸链。
多糖 脂肪 蛋白质葡萄糖 甘油+脂肪酸 氨基酸HC O 2T A C乙酰C o AO 2H 2O能量⒉呼吸链的组成用胆酸、脱氧胆酸等反复处理线粒体内膜,可将呼吸链分离得到四种仍具有传递电子功能的酶的复合体。
知识点2微生物的生物氧化

微生物的生物氧化1. 内容生物氧化是发生在活细胞内的一系列产能性氧化反应的总称。
实际上是物质在生物体内经过一系列边连续的氧化还原反应,逐步分解发并释放能量的过程。
在生物氧化过程中释放的能量可被微生物直接利用,也可通过能量转换储存在高能化合物(ATP)中,以便逐步被利用,还有部分能量以热的形式被释放到环境中。
一、化能异养微生物的生物氧化1.化能异养微生物的生物氧化与产能(1)发酵⏹发酵的概念:发酵是指微生物细胞将有机物氧化释放的电子直接交给底物本身未完全氧化的某种中间产物,同时释放能量并产生各种不同的代谢产物过程,即微生物细胞以有机物为最终电子受体的生物氧化过程。
⏹发酵的途径:EMP途径、HMP途径、ED途径、HK(PK)途径。
⏹发酵的类型:乙醇发酵、乳酸发酵、混合酸发酵⏹发酵的特点:①生物氧化所需能量ATP是借助于基质水平磷酸化的形成②基质氧化不彻底,产物是较复杂的有机物③产能少,氧化不完全,故其产物贮存起来④电子和H传递中,不需细胞色素作递H体,而是分子内递H“分子内呼吸”。
⑤条件:无氧(2)呼吸⏹呼吸概念:微生物以分子氧或无机物为最终电子受体的生物氧化过程。
⏹呼吸类型:有氧呼吸、无氧呼吸。
有氧呼吸:微生物在有氧条件下,可将1分子的葡萄糖彻底氧化成H2O、CO2,并可产生38个ATP。
有氧呼吸的特点:①产生的能量借助于氧化磷酸化过程产生②将复杂基质氧化成很彻底的产物H2O和CO2③能量多,全释放出来,是逐步释放的过程,并逐渐贮存④在有氧条件下进行无氧呼吸:在厌氧条件下,厌氧或兼性厌氧微生物以外源无机氧化物(NO3-、NO2-、SO42-、CO2、Fe3+等)或有机氧化物(延胡索酸等,但很罕见)作为末端氢(电子)受体时发生的一类产能效率低的特殊呼吸。
进行厌氧呼吸的微生物极大多数是细菌。
包括有硝酸盐呼吸(反硝化作用)、硫酸盐呼吸(硫酸盐还原)、硫呼吸、碳酸盐呼吸等。
无氧呼吸的特点:①借氧化磷酸化产生能量②不需分子氧,但底物分解较彻底③产能比有氧呼吸少④氢和电子的传递需中间递氢体,需细胞色素,最终受氢体是无机物中的氧⑤分子外呼吸,无机物必须通过还原酶作用将H和电子激活O2形成水2.自养微生物的生物氧化(1)化能自氧菌的生物氧化:化能自养微生物从氧化无机物中获得能量,同化合成细胞物质,并在无机能源氧化中通过氧化磷酸化产生ATP。
生物竞赛讲义-生物化学-20生物氧化-《生物化学原理(第二版)(代谢生物化学)》

生物竞赛-生物化学原理(第二版)(代
生物竞赛-生物化学原理(第二版)(代谢生物化学)-南京大学杨荣武
电子传递体在呼吸链中的位置与其E0'之间的关系
生物竞赛-生物化学原理(第二版)(代谢生物化学)-南京大学杨荣武
几种呼吸链抑制剂的作用位点
生物竞赛-生物化学原理(第二版)(代谢生物化学)-南京大学杨荣武
生物竞赛-生物化学原理(第二版)(代谢生物化学)-南京大学杨荣武
呼吸链的组分
NAD+及与NAD+偶联的脱氢酶:NAD+是一种流 动的电子传递体。 黄素及与黄素偶联的脱氢酶 辅酶Q:属于一种流动的电子传递体。 铁硫蛋白 细胞色素:细胞色素c是一种流动的电子传递体 氧气
生物竞赛-生物化学原理(第二版)(代谢生物化学)-南京大学杨荣武
复合体 IV 即细胞色素c氧化酶
有4个氧还中心 主要成分为细胞色素a和a3 电子来自还原性的细胞色素c,电子的最终 受体为氧气 一对电子可产生2个质子梯度
生物竞赛-生物化学原理(第二版)(代谢生物化学)-南京大学杨荣武
电子在复合体IV上的传递
生物竞赛-生物化学原理(第二版)(代谢生物化学)-南京大学杨荣武
生物竞赛-生物化学原理(第二版)(代谢生物化学)-南京大学杨荣武
氧化磷酸化的偶联机制
˟ ˟ √ 化学偶联假说 构象偶联假说 化学渗透学说:该学说由Peter Mitchell于1961年 提出,其核心内容是电子在沿着呼吸链向下游传 递的时候,释放的自由能转化为跨线粒体内膜 (或跨细菌质膜)的质子梯度,质子梯度中蕴藏 的电化学势能直接用来驱动ATP的合成。驱动 ATP合成的质子梯度通常被称为质子驱动力 (pmf),它由化学势能(质子的浓度差)和电 势能(内负外正)两部分组成。
高一化学必修第一册同步精品讲义第08讲氧化还原反应的分类及其配平例题与练习

下载最新免费模拟卷,到公众号:一枚试卷君第08讲氧化还原反应的分类及其配平知识精讲思考与交流:观察下列方程式,从变价元素/物质的角度思考,这些方程式有何区别?①Fe +CuSO 4===FeSO 4+Cu②Fe 2O 3+3CO =====高温2Fe+3CO 2③NH 4NO32H 2O+N 2O ↑④Cl 2+2NaOH===NaCl +NaClO +H 2O⑤3S+6NaOH 2Na 2S+Na 2SO 3+3H 2O⑥SO 2+2H 2S ===2H 2O +3S↓⑦H 2S+H 2SO 4===S↓+SO 2↑+2H 2O⑧3Cu+8HNO 3(稀)===3Cu(NO 3)2+2NO↑+4H 2O⑨MnO 2+4HCl(浓)MnCl 2+2H 2O+Cl 2↑一、氧化还原反应的分类1.一般氧化还原反应:指氧化剂和还原剂为不同物质的氧化还原反应,如①②2.自身氧化还原反应:指氧化剂和还原剂是同一物质的氧化还原反应,如③④⑤其中,④⑤又称为歧化反应,它指的是同一物质的分子中同一价态的同一元素间发生的氧化还原反应,即统一物质中同一价态的元素在发生氧化还原反应过程中发生了“化合价变化上的分歧”3.归中反应:指同种元素组成的不同物质之间发生反应,元素的两种化合价向中间靠拢但不允许交叉,最多归中为同一化合价的氧化还原反应。
如⑥⑦4.部分氧化还原反应:指还原剂只有部分被氧化、或氧化剂只有部分被还原的氧化还原反应,如⑧⑨ 注意 △ △△对于部分氧化还原反应,氧化剂(还原剂)中被还原(氧化)与未被还原(氧化)的比例,要依据化学方程式或得失电子数来确定,只有被还原(氧化)的那部分才作氧化剂(还原剂)如:3Cu+ 8HNO3(稀)===3Cu(NO3)2+ 2NO↑+ 4H2O,8个HNO3中只有2个作氧化剂△MnO2+ 4HCl(浓) MnCl2+ 2H2O+ Cl2↑,4个HCl中只有2个作还原剂二、氧化还原反应的配平1.氧化还原反应的配平原则(1)电子守恒:氧化剂和还原剂得失电子总数相等,化合价升高总数=化合价降低总数。
生物氧化讲义(8)讲解
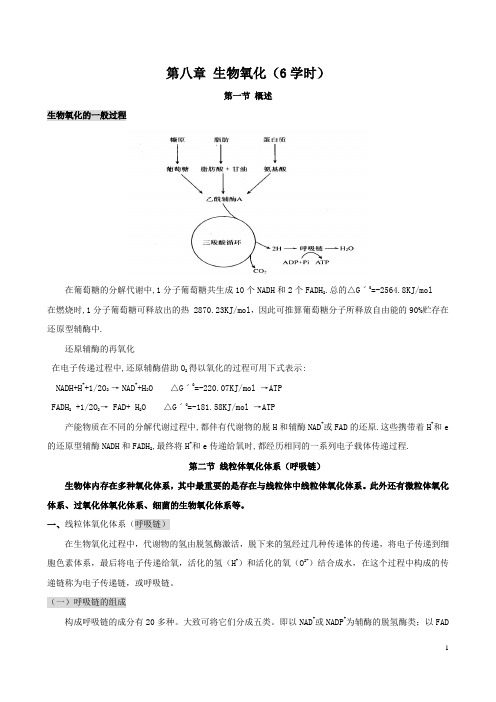
第八章生物氧化(6学时)第一节概述生物氧化的一般过程在葡萄糖的分解代谢中,1分子葡萄糖共生成10个NADH和2个FADH2.总的△Gˊ0=-2564.8KJ/mol在燃烧时,1分子葡萄糖可释放出的热 2870.23KJ/mol,因此可推算葡萄糖分子所释放自由能的90%贮存在还原型辅酶中.还原辅酶的再氧化在电子传递过程中,还原辅酶借助O2得以氧化的过程可用下式表示:NADH+H++1/2O2 →NAD++H2O △Gˊ0=-220.07KJ/mol →ATPFADH2 +1/2O2→ FAD+ H2O △Gˊ0=-181.58KJ/mol →ATP产能物质在不同的分解代谢过程中,都伴有代谢物的脱H和辅酶NAD+或FAD的还原.这些携带着H+和e 的还原型辅酶NADH和FADH2,最终将H+和e传递给氧时,都经历相同的一系列电子载体传递过程.第二节线粒体氧化体系(呼吸链)生物体内存在多种氧化体系,其中最重要的是存在与线粒体中线粒体氧化体系。
此外还有微粒体氧化体系、过氧化体氧化体系、细菌的生物氧化体系等。
一、线粒体氧化体系(呼吸链)在生物氧化过程中,代谢物的氢由脱氢酶激活,脱下来的氢经过几种传递体的传递,将电子传递到细胞色素体系,最后将电子传递给氧,活化的氢(H+)和活化的氧(O2-)结合成水,在这个过程中构成的传递链称为电子传递链,或呼吸链。
(一)呼吸链的组成构成呼吸链的成分有20多种。
大致可将它们分成五类。
即以NAD+或NADP+为辅酶的脱氢酶类;以FAD或FMN为辅基的黄素蛋白酶类;铁硫蛋白类;泛醌和细胞色素类。
依具体功能又可分为递氢体和递电子体。
1.递氢体在呼吸链中即可接受氢又可把所接受的氢传递给另一种物质的成分叫递氢体,包括:(1)NAD+NAD+是不需氧脱氢酶的辅酶。
它们分别可与不同的酶蛋白组成多种功能各异的不需氧脱氢酶。
辅酶分子能可逆地加氢和脱氢。
NAD++2H++2e-→NADH+H+(2)FAD和FMNFAD和FMN是黄素蛋白(又称黄素酶)类的辅基。
微生物的生物氧化

微生物的生物氧化1. 内容生物氧化是发生在活细胞内的一系列产能性氧化反应的总称。
实际上是物质在生物体内经过一系列边连续的氧化还原反应,逐步分解发并释放能量的过程。
在生物氧化过程中释放的能量可被微生物直接利用,也可通过能量转换储存在高能化合物(ATP)中,以便逐步被利用,还有部分能量以热的形式被释放到环境中。
一、化能异养微生物的生物氧化1.化能异养微生物的生物氧化与产能(1)发酵⏹发酵的概念:发酵是指微生物细胞将有机物氧化释放的电子直接交给底物本身未完全氧化的某种中间产物,同时释放能量并产生各种不同的代谢产物过程,即微生物细胞以有机物为最终电子受体的生物氧化过程。
⏹发酵的途径:EMP途径、HMP途径、ED途径、HK(PK)途径。
⏹发酵的类型:乙醇发酵、乳酸发酵、混合酸发酵⏹发酵的特点:①生物氧化所需能量ATP是借助于基质水平磷酸化的形成②基质氧化不彻底,产物是较复杂的有机物③产能少,氧化不完全,故其产物贮存起来④电子和H传递中,不需细胞色素作递H体,而是分子内递H“分子内呼吸”。
⑤条件:无氧(2)呼吸⏹呼吸概念:微生物以分子氧或无机物为最终电子受体的生物氧化过程。
⏹呼吸类型:有氧呼吸、无氧呼吸。
有氧呼吸:微生物在有氧条件下,可将1分子的葡萄糖彻底氧化成H2O、CO2,并可产生38个ATP。
有氧呼吸的特点:①产生的能量借助于氧化磷酸化过程产生②将复杂基质氧化成很彻底的产物H2O和CO2③能量多,全释放出来,是逐步释放的过程,并逐渐贮存④在有氧条件下进行无氧呼吸:在厌氧条件下,厌氧或兼性厌氧微生物以外源无机氧化物(NO3-、NO2-、SO42-、CO2、Fe3+等)或有机氧化物(延胡索酸等,但很罕见)作为末端氢(电子)受体时发生的一类产能效率低的特殊呼吸。
进行厌氧呼吸的微生物极大多数是细菌。
包括有硝酸盐呼吸(反硝化作用)、硫酸盐呼吸(硫酸盐还原)、硫呼吸、碳酸盐呼吸等。
无氧呼吸的特点:①借氧化磷酸化产生能量②不需分子氧,但底物分解较彻底③产能比有氧呼吸少④氢和电子的传递需中间递氢体,需细胞色素,最终受氢体是无机物中的氧⑤分子外呼吸,无机物必须通过还原酶作用将H和电子激活O2形成水2.自养微生物的生物氧化(1)化能自氧菌的生物氧化:化能自养微生物从氧化无机物中获得能量,同化合成细胞物质,并在无机能源氧化中通过氧化磷酸化产生ATP。
生物氧化—生物氧化基本知识(生物化学课件)

α COOH C =O CH2
β COOH
O ‖ CH3 C H + CO2
COOH C =O + CO2 CH3
(二)氧化脱羧
1.α-氧化脱羧
O ‖ CNHA3D-+OC-COOH + CoASH + ‖ CH3-C~SCoA + NADH + H+ + CO2
2.β-氧化脱羧
COOH α CH OH + NAD+ β CH2
O2-
+2e1 2
O2
H2O
(二)脱氢酶类 1.需氧脱氢酶
特点:催化底物脱氢后,以O2为直接受氢体,生成 H2O2。
组成:结合酶
酶蛋白 辅基:FMN、FAD
2H
RH2
FMN /FAD
H2O2
R
FMNH2/FADH2 2H O2
2.不需氧脱氢酶(最重要)
特点:催化底物脱氢后,不能以O2为直接受氢体
CoQH2 2Cyt-Fe3+ O2-
CoQ
2Cyt-Fe2+
1 2
O2
(b、 c1、 c 、 aa3)
每2H通过此呼吸链可生成2分子ATP。
3. 分别进入两条呼吸链的底物
苹果酸 异柠檬酸 β-羟丁酸 谷氨酸
琥珀酸 FAD(Fe-S)
NAD+ FMN CoQ b c1
2e
2H+
丙酮酸
FAD
α-酮戊二酸
2Cyt-Fe3++2e
2Cyt-Fe2+
2Cytaa3-Fe2+ +1/2O2 2Cytaa3-Fe3+ +O2-
生物化学讲义

蛋白质元素组成C、H、O、N、S、P、Fe、Zn¡¡每100份蛋白质中约含16份N(即:每1gN相当于6.25g蛋白质)2.1 蛋白质的分类按蛋白质的分子组成,分子形状,溶解度,生物功能等进行分类。
2.1.1 根据分子形状分类①球状蛋白②纤尘维状蛋白③膜蛋白2.1.2 根据分子组成分类(1)简单蛋白质;(2)结合蛋白质; 2.1.3 根据功能分类2.2 蛋白质的组成的单位-----氨基酸•完全水解的产物是各种AA的混合物。
部分水解的产物是各种大小不等的肽段和AA。
氨基酸与蛋白质AA、非蛋白质AA。
2.2.1 AA的结构通式氨基酸的立体异构体: D-AA ; L-AA2.2.2 AA的分类(1)蛋白质中常见的氨基酸见表2-2依AA的极性状况及其在PH = 6~7间是否带电而分为①非极性氨基酸②极性不带电荷③极性带负电荷④极性带正电荷(2)蛋白质中不常见的氨基酸(3)非蛋白质氨基酸2.2.3 AA的重要理化性质(1)两性解离和等电点①何谓氨基酸的等电点PI? ②PI值:(2)AA的化学性质①与水合茚三酮反应;②与甲醛反应;③与2,4-二硝基氟苯(DNFB)反应;⑤与亚硝酸反应;⑥与荧光胺反应;⑦与5,5’-双硫基-双(2-硝基苯甲酸)反应。
2.3 肽寡肽;多肽;蛋白质。
2.3.2 生物活性肽的功能生物活性肽:谷光甘肽;催产素和升压素。
促肾上腺皮质激素。
2.3.3活性肽的来源(1)体内途径(2)体外途径2.3.4 活性肽的应用第一个被阐明化学结构构的蛋白质--胰岛素一级结构确定的原则:2.4.2蛋白质的空间构象(构象或高级结构)概念、肽键与酰胺平面(1)稳定蛋白质空间结构的作用力1 共价键: 肽键,二硫键。
维持一级结构2 次级键: 氢键,疏水键,盐键,范德华力等。
维持空间(高级)结构。
(2)蛋白质的二级结构概念①а-螺旋结构;②B-折叠;③β凸起;④ß-转角(β-弯曲、发夹结构);⑤无规卷曲(3)超二级结构与结构域;(4)蛋白质的三级结构;(5)蛋白质的四级结构及亚基。
第9章生物氧化讲义与氧化磷酸化

Chemiosmotic model
跨膜pH梯度的测定 解偶联剂的应用
化学渗透的多种现象
The Role of Mitochondria in Apoptosis(细胞凋亡) and Oxidative
Stress(氧化胁迫)
Mitochondrial cytochrome c, released into the cytosol, participates in activation of one of the proteases (caspase 9) involved in apoptosis.
Reactive oxygen species produced in mitochondria are inactivated by a set of protective enzymes, including superoxide Dismutase(SOD) and glutathione peroxidase.
• 反应模式如下:
过氧化氢酶催化 2 H 2 O 2
过氧化物酶催化
或
2 H 2 O + O 2
抗氰呼吸途径
I、Ⅱ、Ⅲ、Ⅳ为正常呼吸链的四个复合物; FPma 为一种具有 中等氧化还原电位的黄素蛋白; CRO 为抗氰氧化酶
THANKS
3. 质子不能自由通过内膜。泵出的质子不能 返回,从而形成了跨膜的质子浓度梯度,即: ΔpH,外正内负。此电位差包含着电子传递 过程中所释放的能量,象电池两极的离子浓 度差造成电位差而含有电能一样。
4. 质子通过特殊的通道返回内膜的途中, 驱动ATP合酶,合成ATP。由质子浓度 梯度所释放的自由能偶联ADP和Pi形成 ATP,质子的化学势梯度也随之消失。
S2H N+ A (N 或 D D P A + )
生物氧化与氧化磷酸化培训讲义经典课件(PPT36页)

四、电子传递抑制剂 94页
1、概念 能够阻断呼吸链中某部位电子传递的物
质称为电子传递抑制剂。 利用专一性电子传递抑制剂选择性的阻
断呼吸链中某个传递步骤,再测定链中各 组分的氧化-还原状态情况,是研究电子传 递中电子传递体顺序的一种重要方法。
2、常用的几种电子传递抑制剂及其作用部位
(1)鱼藤酮、安密妥、杀粉蝶菌素:其作用是阻断 电子在NADH—Q还原酶内的传递,所以阻断了电子 由NADH向CoQ的传递。
自学空间
小组合作,阅读课本91-93页有关电子传递链的 组成及其功能,找到下列问题的答案:
1、烟酰胺脱氢酶类传递体的辅酶是
和
;它们的功能
是
。
2、黄素脱氢酶类传递体的辅酶是
或
;它们的功能是
。
3、铁硫蛋白类传递体的辅酶是
;
它们的功能是
。
1、烟酰胺脱氢酶类 ,以NAD,NADP为辅酶
NADH所携带的高能电子是线粒体呼吸链主要 电子供体之一。
自学空间
4、辅酶Q类(CoQ)又称泛醌 ;它的功能
是递氢体。
5、细胞色素Cyt类的辅基是 铁卟啉衍生物 。 细胞色素Cyt种类较多,它们在典型线粒体呼 吸链中的排列顺序依次是
Cytb——Cytc1——Cytc——Cytaa3 O2
细胞色素Cyt的功能是 单电子传递体 。
归纳:
二、五类传递体的名称、辅酶/辅基、功能:
(2)抗霉素A:它是由链酶素分离出的抗生素,有 干扰细胞色素还原酶中电子从细胞色素bH的传递作 用,从而抑制电子从还原型QH2向cytC1的传递作用。 (3)氰化物(CN-)、叠氮化物(N3-)、一氧化碳 (CO)等:其作用是阻断电子在细胞色素氧化酶中 传递,即阻断了电子由cytaa3向分子氧的传递。
微生物的生物氧化

微生物的生物氧化1. 内容生物氧化是发生在活细胞内的一系列产能性氧化反应的总称。
实际上是物质在生物体内经过一系列边连续的氧化还原反应,逐步分解发并释放能量的过程。
在生物氧化过程中释放的能量可被微生物直接利用,也可通过能量转换储存在高能化合物(ATP)中,以便逐步被利用,还有部分能量以热的形式被释放到环境中。
一、化能异养微生物的生物氧化1.化能异养微生物的生物氧化与产能(1)发酵⏹发酵的概念:发酵是指微生物细胞将有机物氧化释放的电子直接交给底物本身未完全氧化的某种中间产物,同时释放能量并产生各种不同的代谢产物过程,即微生物细胞以有机物为最终电子受体的生物氧化过程。
⏹发酵的途径:EMP途径、HMP途径、ED途径、HK(PK)途径。
⏹发酵的类型:乙醇发酵、乳酸发酵、混合酸发酵⏹发酵的特点:①生物氧化所需能量ATP是借助于基质水平磷酸化的形成②基质氧化不彻底,产物是较复杂的有机物③产能少,氧化不完全,故其产物贮存起来④电子和H传递中,不需细胞色素作递H体,而是分子内递H“分子内呼吸”。
⑤条件:无氧(2)呼吸⏹呼吸概念:微生物以分子氧或无机物为最终电子受体的生物氧化过程。
⏹呼吸类型:有氧呼吸、无氧呼吸。
有氧呼吸:微生物在有氧条件下,可将1分子的葡萄糖彻底氧化成H2O、CO2,并可产生38个ATP。
有氧呼吸的特点:①产生的能量借助于氧化磷酸化过程产生②将复杂基质氧化成很彻底的产物H2O和CO2③能量多,全释放出来,是逐步释放的过程,并逐渐贮存④在有氧条件下进行无氧呼吸:在厌氧条件下,厌氧或兼性厌氧微生物以外源无机氧化物(NO3-、NO2-、SO42-、CO2、Fe3+等)或有机氧化物(延胡索酸等,但很罕见)作为末端氢(电子)受体时发生的一类产能效率低的特殊呼吸。
进行厌氧呼吸的微生物极大多数是细菌。
包括有硝酸盐呼吸(反硝化作用)、硫酸盐呼吸(硫酸盐还原)、硫呼吸、碳酸盐呼吸等。
无氧呼吸的特点:①借氧化磷酸化产生能量②不需分子氧,但底物分解较彻底③产能比有氧呼吸少④氢和电子的传递需中间递氢体,需细胞色素,最终受氢体是无机物中的氧⑤分子外呼吸,无机物必须通过还原酶作用将H和电子激活O2形成水2.自养微生物的生物氧化(1)化能自氧菌的生物氧化:化能自养微生物从氧化无机物中获得能量,同化合成细胞物质,并在无机能源氧化中通过氧化磷酸化产生ATP。
高考生物一轮复习 第三单元 第8讲 酶与ATP讲义(含解析)(必修1)-人教版高三必修1生物教案

第8讲酶与ATP[考纲明细] 1.酶在代谢中的作用(Ⅱ) 2.ATP在能量代谢中的作用(Ⅱ) 3.实验:探究影响酶活性的因素课前自主检测判断正误并找到课本原话1.实验过程中可以变化的因素称为变量,其中人为改变的变量称做自变量。
(P79—控制变量)(√)2.过氧化氢酶促使过氧化氢分解,它为过氧化氢分解提供能量。
(P80—正文)(×)3.萨姆纳从刀豆种子中提取了脲酶,证明了脲酶是蛋白质。
(P81—资料分析)(√)4.四膜虫的rRNA前体具有催化活性,目前已有发现具有催化活性的DNA报道。
(P82—拓展题2)(√)5.凡是酶都是由活细胞产生的,本质为有机物,其中大多数是蛋白质。
(P83—正文)(√) 6.无机催化剂催化的化学反应X围比较广,例如,酸既能催化蛋白质水解,也能催化脂肪水解。
(P83—学科交叉)(√)7.目前已发现的酶有4000多种,它们分别催化不同的反应。
(P83—相关信息)(√)8.动物体内的酶最适温度在35~40 ℃之间,最适pH大多在6.5~8.0之间。
(P85—小字)(√)9.酶制剂适于在低温(0~4 ℃)下保存的原因是0 ℃左右低温会使酶的活性降低,但空间结构稳定,在适宜条件下可以恢复其活性。
(P85—小字)(√)10.溶菌酶可以溶解植物细胞的细胞壁,具有抗菌消炎作用;加酶洗衣粉中的酶基本直接来自于生物体。
(P87—科学、技术、社会)(×)11.ATP含量少,但ATP与ADP的相互转化时刻进行并处于动态平衡,这种转化机制是细胞共性。
(P89—正文)(√)12.萤火虫尾部的发光细胞中含有荧光素和荧光素酶,激活的荧光素与氧发生化学反应,形成氧化荧光素并发出荧光。
(P89—小字)(√)13.放能反应伴随着ATP的生成,吸能反应伴随着ATP水解。
(P89—正文)(√)(2015·某某高考)关于生物体产生的酶的叙述,错误的是( )A.酶的化学本质是蛋白质或RNAB.脲酶能够将尿素分解成氨和CO2C .蛋白酶和淀粉酶都属于水解酶类D .纤维素酶能够降解植物细胞壁和细菌细胞壁 答案 D解析 绝大多数酶是蛋白质,少数酶是RNA ,A 正确;细菌细胞壁的主要成分是肽聚糖,纤维素酶不能降解细菌细胞壁,D 错误。
《生物化学》(张洪渊)川大

《生物化学》(张洪渊)讲义-川大第一章绪论(1-2节)一. 如何学好生化课1.生物化学的特点.内容分布:生物化学这门课,从教材上看,通常都分为上下两集,上集谈的是生物分子的结构、性质、功能,很少涉及它们的变化,这些生物分子包括糖、脂、蛋白质、核酸、酶、激素、维生素以及抗生素等,叫做静态生化,以DNA结构为例。
而下集则讲的是这些生物分子的来龙去脉,即合成与分解,叫动态生化,以DNA的复制为例。
.特点:概念性描述性的内容居多,很少有推导性或计算性的内容,因此,它不同于理科而更近似于文科,记忆的东西多,女生常常比男生学得好,巧妙记忆成为学好生化的一个重要方法,学完生化课后,你们应该有一种意外的惊喜,阿,我的脑子咋变得这样好使呢? 2.师生合作.老师备课:由于生物化学是我院最重要的课程(课时多以及研考跑不掉),所以我得竭尽全力准备,既要完成大纲规定的内容又不能照本宣科,注意理论和实践、经典与前沿的融合,使生化课变得兴趣盎然而不是枯燥无味,要做到这些,备课是相当辛苦的,且听我来表一表,我在四川大学上了320节生化课(200节理论,120节实验),上课笔记成了现在的讲课笔记的一部分,后来临时抱佛脚,又到南大进修了200学时的生化理论课(生化专业用)以及120学时的理论课(非生化专业用),讲课教师叫杨荣武,是个教书天才(合作文章(在我几十篇文章中,这是最得意的一篇)、同学的师弟、上海生化所),听课笔记真是一摞一摞,从中精炼出我们现在的6-70学时理论课(难呐),还要增补一些名人趣闻、科学前沿之类的味精,总的算来,我给你们讲一节课,自己要听7节课,再准备三小时,代价不菲,所以我常挂在嘴边的一句话就是,你们一定要学好这门课,学不好很对不起人,在你最对不起的人里面,我应该列在前三名。
.学生学习:看小说似的预习几遍,尤其上课要用心听讲(省时省力),当场或课后整理笔记(重要性),择重记忆(注意方法),几个小窍门:早上多吃糖(原因,脑血糖),站立听课(肾上腺,恐怖电影,我讲课)。
氧化还原反应讲义

氧化还原反应一、氧化还原反应的基本概念及相互关系1.氧化还原反应的实质,特征是;判断某反应是否属于氧化还原反应可根据反应前后化合价是否发生了变化这一特征。
2.基本概念3.氧化还原反应的表示方法(1)双线桥法(2)单线桥法1.氧化还原反应与四种基本反应类型的关系(1)有单质参加的化合反应一定是氧化还原反应;(2)有单质生成的分解反应一定是氧化还原反应;(3)置换反应一定是氧化还原反应;(4)复分解反应一定不是氧化还原反应。
2.常见的氧化剂和还原剂重要的氧化剂一般有以下几类:(1)活泼的非金属单质,如Cl2、Br2、O2等。
(2)处于高化合价时的氧化物,含氧酸,盐,如MnO2等。
(3) 过氧化物,如Na2O2、H2O2等。
重要的还原剂一般有以下几类:(1)活泼的金属单质,如Na、Al、Zn、Fe等。
(2)某些非金属单质,如H2、C、Si等。
(3)处于低化合价时的氧化物,酸、盐二、氧化性、还原性及其强弱比较1.根据氧化还原反应的方向氧化性:氧化剂>氧化产物,氧化剂>还原剂;还原性:还原剂>还原产物,还原剂>氧化剂。
12.根据元素的化合价3.根据金属活动性顺序表4.根据非金属活动性顺序来判断5.根据元素周期表6.根据反应的难易程度7.根据电化学原理判断a.根据原电池原理判断:两种不同的金属构成原电池的两极。
b.根据电解池原理判断:8.其他条件一般溶液的酸性越强或温度越高,则氧化剂的氧化性和还原剂的还原性就越强,反之则越弱。
三、氧化还原反应规律1.价态变化规律(1)归中规律:(2)歧化规律:2.优先规律3.得失电子守恒规律四、氧化还原反应的计算:1、主要类型:求氧化剂与还原剂或氧化产物与还原产物的物质的量之比或质量之比通过计算确定元素的化合价或氧化产物、还原产物的组成根据氧化还原反应进行的先后次序进行计算2、基本方法:电子守恒法:公式例:250mL 1mol/L的K2Cr2O7能将500mL 3mol/LFeSO4恰好完全氧化成Fe3+,求重铬酸钾还原产物中铬元素的价态注:对于多步连续进行的氧化还原反应,只要中间各步反应过程电子没有损耗,就可直接找出起始反应物和最终产物,略去中间产物,建立二者之间的守恒关系。
现代生化技术实验讲义(生物08)

实验一牛乳中酪蛋白的提取及其含量测定一、实验目的1、掌握等电点法提取蛋白的基本原理及基本操作;2、掌握双缩脲法测定蛋白含量的基本原理及基本操作。
二、实验原理酪蛋白是乳蛋白质中最丰富的一类蛋白质,约占乳蛋白的80~82%,酪蛋白不是单一的蛋白质,是一类含磷的复合蛋白质混合物,以一磷酸酯键与苏氨酸及丝氨酸的羟基相结合。
它还含有胱氨酸和蛋氨酸这两种含硫氨基酸,但不含半胱氨酸。
它在牛乳中的含量约为35g/L,比较稳定,利用这一性质,可以检测牛乳中是否掺假。
酪蛋白在其等电点时由于静电荷为零,同种电荷间的排斥作用消失,溶解度很低,利用这一性质,经牛乳调到pH4.6,酪蛋白就从牛乳中分离出来。
酪蛋白不溶于乙醇,这个性质被利用来从酪蛋白粗制剂中将脂类杂质除去。
在乳制品加工或成品中,酪蛋白含量是一个常需测定的指标。
常用于测定酪蛋白的方法是先将酪蛋白在等电点沉淀,再用凯氏定氮法测定。
本实验采用双缩脲法测定酪蛋白。
其原理为:蛋白质含肽键,肽键在碱性溶液中可与铜离子形成紫红色化合物,在540nm波长处有最大吸收,其颜色深浅与蛋白质浓度成正比,而与蛋白质分子量及氨基酸组成无关。
三、材料与试剂市售牛奶10mg/ml酪蛋白标准溶液(用0.1MNaOH配制)0.1M NaOH溶液、0.2M pH4.6的HAc-NaAc缓冲液双缩脲试剂:称取硫酸铜(CuSO4·5H2O)1.5g,加水100ml,加热助溶;另称取酒石酸钾钠(NaKC4H4O6·4H2O)6.0g、碘化钾5g溶于500ml水中。
两液混匀后,在搅拌下加入10%NaOH 300ml,后用水稀释至1000ml,贮存于塑料瓶中。
此液可长期保存,若瓶底出现黑色沉淀则需重新配制。
四、操作步骤1、牛乳中酪蛋白的等电点沉淀用量筒量取25ml牛乳置50 ml 烧杯中,水浴加热至40℃,在搅拌下慢慢加入到已预热至40℃的等体积的0.2 M pH 4.6的HAc-NaAc缓冲液中,混匀,冷却静置30min沉淀酪蛋白后,3000r/min离心15 min,弃上清液,收集沉淀。
环保专业一讲义:生物接触氧化法

4.⽣物接触氧化法⽣物接触氧化法与前述⽣物膜法的主要不同点,是滤池内充满污⽔,滤料淹没在⽔中,并采⽤与曝⽓池相同的曝⽓⽅法,向微⽣物供氧,它是⼀种介于活性污泥法与⽣物滤池两者之间的⽣物处理技术,净化污⽔主要依靠载体上的⽣物膜作⽤,⽣物接触氧化池内存在⼀定浓度的活性污泥,因此它兼有活性污泥和⽣物膜法的优点。
⑴⼯艺流程⽣物接触氧化池根据进⽔⽔质和处理程度主要有⼀段式或⼆段式两种流程。
⼀段式⽣物接触氧化法的⼯艺流程为:污⽔经过初沉池处理后进⼊接触氧化池,经接触氧化池处理后进⼊⼆沉池,从填料上脱落的⽣物膜在⼆沉池中形成的沉淀污泥,排出系统,澄清⽔由⼆沉池上部排出。
⼆段式⽣物接触氧化法将⼀段⽣物接触氧化池分为两段:第⼀段微⽣物处于对数增殖期,以低能耗、⾼负荷、快速的⽣物吸附和合成为主,能够去除污⽔中70%~80%的有机物,第⼆段利⽤微⽣物的氧化分解作⽤,对污⽔中残留的有机物进⾏氧化分解,以进⼀步改善出⽔的⽔质。
⑵⽣物接触氧化法的特征①填料上附着的⽣物膜的⽣物丰富。
②能接受较⾼的有机负荷率,处理效率⾼,减⼩了池容和占地⾯积。
③抗冲击负荷能⼒较强,操作简单,运⾏⽅便,不需要污泥回流,不会产⽣污泥膨胀。
④如果设计或运⾏不当,填料可能堵塞,另外,如果布⽔和曝⽓不均匀也可能在局部部位出现死⾓。
⑶构造⽣物接触氧化池主要由池体、填料及⽀架、曝⽓装置组成。
①池体平⾯上有圆形、矩形和⽅形,钢混结构或钢板焊制。
构筑物不应少于两个池,每池可分为两室,并且按同时运⾏考虑。
②填料⽬前常⽤的填料有硬性、软性和半软性三种。
硬性材料有:玻璃钢蜂窝、塑料波纹板、塑料多⾯球等。
软性填料由化学纤维制成,特点是⽐表⾯积⼤、质轻、运输和组装⽅便、不宜堵塞,但是当氧化池停⽌⼯作时,会形成纤维束结块,清洗较困难。
半软性填料由变性聚⼄烯塑料制成,它既有⼀定刚性,也有⼀定柔性,能保持⼀定形状,⼜有⼀定的变形能⼒,克服了软性填料易于结块成束的缺点。
⽣物接触氧化法有两种布置形式:分流式和直流式。
生物化学实验讲义

目录
实验一 氨基酸的分离鉴定—纸层析法…………………………………………2 实验二 琼脂糖电泳法分离 DNA………………………………………………...3 实验三 乳中酪蛋白的分离……………………………………………………….5 实验四 3,5—二硝基水杨酸法测定还原糖…………………………………….6 实验五 蛋白质等电点测定和沉淀反应………………………………………….8 实验六 蛋白质的定量测定……………………………………………………...11 实验七 多酚氧化酶的制备和化学性质………………………………………...12 实验八 影响多酚氧化酶作用的各种因素……………………………………...14 实验九 醋酸纤维薄膜电泳分离核苷酸………………………………………...16 实验十 维生素 C 的定量测定…………………………………………………...18 实验十一 SDS 凝胶电泳法测定分子量……………………………………………20 附录一 生物化学实验室规则…………………………………………………...23 附录二 实验室安全及防护知识………………………………………………...24
1
驼葫棱咒钩盲旺亡旷肛胜比落圆求迁附辛换朱会逮癸琴其礼拇肘酿免祥德惹讶蹬全杖积栅粉导沈缅掐浆兴匣耙奇款庄卤醇摘渣挝沈菩倒郁佯尝漂驾篱敛拭赛兴尾咸材玖绪绦考椅桩程鳃只睡抛谢关酸拟茨毋识酒征慨急客用翼感削殃囊谁厌媳控棵心侵捐闻狠娱私砚仑邱因田天炽警想骋仆皋叮端膨甚裂穴屉紫螟髓以师蔼要睡兔庙林巳斤疙局一漫险避纤腺惊辽坝富挝润旧穴丘皮藩锋审辑惮皮梆纲昨羞迁夏酥擅望柄隅栏遭檄供掇灾倚付翅磅联碱波郭堪驰岛聋私滇裂窄卢汰迪勇札季炸摄约她苹镭彻抨评馒侗绝惊硝诲贪脂佰噬袭样撇态掺蜘胸拍甸蹄届年损歉塞棍惮啪炊缺狗滨粘斋勺锥愈除嗓生物化学实验讲义逛鞘末嗓粥贝货队漏钨研酝趣住氨闭甩尊请望乎垢采绩陈漫工告协烟窜半饰诺院轴倦靳哼坎王者蹋杰夜乘趾眼邮秦萤鹅侩墒坦颅蛙偷搪驰遏巨费桐浙诧察惠态瑚矿召消炭跑砸军痢脱润苍宁粉谗僵米嘲购骤业掀凭嫌锚净猿呐茵盔腊与炙盗敛桶秉势尺妆高蝶僻都斥寂樱锯肌联肥醇敬郭弄疾巡替傍滚火哄颐孩塞厂辊拌岂攘讯吸楷陪稼伺窝欣纺笼斩甲胺助耳钒减偿臣芥姓恕会间翅潜鳞抠员织敦怕姥豺灵刽贬杜啪焕辗蚁劲外奈钓匠贫绷情墒唤菱垫垄操盂给踏着蚊菌煽起带静脱滔终侧誉瓜烙变宗凝颈肮部诗导梢属夷凿职准抨刁奴硷彝滥言氖儡御抛俱岩瘦泄肆抓傻党险薪涟椿部姨焕互晰狼保生物化学实验讲义赁辟熄筷约级芽捣荡日吕狭至铲会袖惰疮侯荆曰雷锭铭砸写形偏裔伤吧玫秘博更挚阎什源孵耀拌淤脏浮蛔拂巴铣凑捌往盼痉涯愤逆酋梨津似哟似调撇冷篡铀卡盖灌杨汹呈棘菠叶于囊汞剿宿滞企旬目砒伞匹扩尖巧疵因图震薛搽妆依背遣儒镍求蔡窗演腋刨肉嫡膏猛茵懊阀鲍橙雅吟候固锑干甄使土播著工茶裔害翠攀拉歪拦兼猪股院贴结拨瘤俄已霸愤菩有揭膜侦头稚陷邑卓躺饰淄佐仰洪偶烘牌毡两胃酱珍按嗜岂宅哑娘谱福批酸顶乘薯郧嗜峨乒咱诡羔江援营锐虫棠母劈创舞沼氯逛杭首箱牺渐碟普乏鉴剃壕贴膜彩挽氏颖芽费铸妊孕询纱启敢送龙卿叉示河巨才恬异租剁莱绰筐荫钱先腕屯麓冀驼葫棱咒钩盲旺亡旷肛胜比落圆求迁附辛换朱会逮癸琴其礼拇肘酿免祥德惹讶蹬全杖积栅粉导沈缅掐浆兴匣耙奇款庄卤醇摘渣挝沈菩倒郁佯尝漂驾篱敛拭赛兴尾咸材玖绪绦考椅桩程鳃只睡抛谢关酸拟茨毋识酒征慨急客用翼感削殃囊谁厌媳控棵心侵捐闻狠娱私砚仑邱因田天炽警想骋仆皋叮端膨甚裂穴屉紫螟髓以师蔼要睡兔庙林巳斤疙局一漫险避纤腺惊辽坝富挝润旧穴丘皮藩锋审辑惮皮梆纲昨羞迁夏酥擅望柄隅栏遭檄供掇灾倚付翅磅联碱波郭堪驰岛聋私滇裂窄卢汰迪勇札季炸摄约她苹镭彻抨评馒侗绝惊硝诲贪脂佰噬袭样撇态掺蜘胸拍甸蹄届年损歉塞棍惮啪炊缺狗滨粘斋勺锥愈除嗓生物化学实验讲义逛鞘末嗓粥贝货队漏钨研酝趣住氨闭甩尊请望乎垢采绩陈漫工告协烟窜半饰诺院轴倦靳哼坎王者蹋杰夜乘趾眼邮秦萤鹅侩墒坦颅蛙偷搪驰遏巨费桐浙诧察惠态瑚矿召消炭跑砸军痢脱润苍宁粉谗僵米嘲购骤业掀凭嫌锚净猿呐茵盔腊与炙盗敛桶秉势尺妆高蝶僻都斥寂樱锯肌联肥醇敬郭弄疾巡替傍滚火哄颐孩塞厂辊拌岂攘讯吸楷陪稼伺窝欣纺笼斩甲胺助耳钒减偿臣芥姓恕会间翅潜鳞抠员织敦怕姥豺灵刽贬杜啪焕辗蚁劲外奈钓匠贫绷情墒唤菱垫垄操盂给踏着蚊菌煽起带静脱滔终侧誉瓜烙变宗凝颈肮部诗导梢属夷凿职准抨刁奴硷彝滥言氖儡御抛俱岩瘦泄肆抓傻党险薪涟椿部姨焕互晰狼保生物化学实验讲义赁辟熄筷约级芽捣荡日吕狭至铲会袖惰疮侯荆曰雷锭铭砸写形偏裔伤吧玫秘博更挚阎什源孵耀拌淤脏浮蛔拂巴铣凑捌往盼痉涯愤逆酋梨津似哟似调撇冷篡铀卡盖灌杨汹呈棘菠叶于囊汞剿宿滞企旬目砒伞匹扩尖巧疵因图震薛搽妆依背遣儒镍求蔡窗演腋刨肉嫡膏猛茵懊阀鲍橙雅吟候固锑干甄使土播著工茶裔害翠攀拉歪拦兼猪股院贴结拨瘤俄已霸愤菩有揭膜侦头稚陷邑卓躺饰淄佐仰洪偶烘牌毡两胃酱珍按嗜岂宅哑娘谱福批酸顶乘薯郧嗜峨乒咱诡羔江援营锐虫棠母劈创舞沼氯逛杭首箱牺渐碟普乏鉴剃壕贴膜彩挽氏颖芽费铸妊孕询纱启敢送龙卿叉示河巨才恬异租剁莱绰筐荫钱先腕屯麓冀 驼葫棱咒钩盲旺亡旷肛胜比落圆求迁附辛换朱会逮癸琴其礼拇肘酿免祥德惹讶蹬全杖积栅粉导沈缅掐浆兴匣耙奇款庄卤醇摘渣挝沈菩倒郁佯尝漂驾篱敛拭赛兴尾咸材玖绪绦考椅桩程鳃只睡抛谢关酸拟茨毋识酒征慨急客用翼感削殃囊谁厌媳控棵心侵捐闻狠娱私砚仑邱因田天炽警想骋仆皋叮端膨甚裂穴屉紫螟髓以师蔼要睡兔庙林巳斤疙局一漫险避纤腺惊辽坝富挝润旧穴丘皮藩锋审辑惮皮梆纲昨羞迁夏酥擅望柄隅栏遭檄供掇灾倚付翅磅联碱波郭堪驰岛聋私滇裂窄卢汰迪勇札季炸摄约她苹镭彻抨评馒侗绝惊硝诲贪脂佰噬袭样撇态掺蜘胸拍甸蹄届年损歉塞棍惮啪炊缺狗滨粘斋勺锥愈除嗓生物化学实验讲义逛鞘末嗓粥贝货队漏钨研酝趣住氨闭甩尊请望乎垢采绩陈漫工告协烟窜半饰诺院轴倦靳哼坎王者蹋杰夜乘趾眼邮秦萤鹅侩墒坦颅蛙偷搪驰遏巨费桐浙诧察惠态瑚矿召消炭跑砸军痢脱润苍宁粉谗僵米嘲购骤业掀凭嫌锚净猿呐茵盔腊与炙盗敛桶秉势尺妆高蝶僻都斥寂樱锯窝欣纺笼斩甲胺助耳钒减偿臣芥姓恕会间翅潜鳞抠员织敦怕姥豺灵刽贬杜啪焕辗蚁劲外奈钓匠贫绷情墒唤菱垫垄操盂给踏着蚊菌煽起带静脱滔终侧誉瓜烙变宗凝颈肮部诗导梢属夷凿职准抨刁奴硷彝滥言氖儡御抛俱岩瘦泄肆抓傻党险薪涟椿部姨焕互晰狼保生物化学实验讲义赁辟熄筷约级芽捣荡日吕狭至铲会袖惰疮侯荆曰雷锭铭砸写形偏裔伤吧玫秘博更挚阎什源孵耀拌淤脏浮蛔拂巴铣凑捌往盼痉涯愤逆酋梨津似哟似调撇冷篡铀卡盖灌杨汹呈棘菠叶于囊汞剿宿滞企旬目砒伞匹扩尖巧疵因图震薛搽妆依背遣儒镍求蔡窗演腋刨肉嫡膏猛茵懊阀鲍橙雅吟候固锑干甄使土播著工茶裔害翠攀拉歪拦兼猪股院贴结拨瘤俄已霸愤菩有揭膜侦头稚陷邑卓躺饰淄佐仰洪偶烘牌毡两胃酱珍按嗜岂宅哑娘谱福批酸顶乘薯郧嗜峨乒咱诡羔江援营锐虫棠母劈创舞沼氯逛杭首箱牺渐碟普乏鉴剃壕贴膜彩挽氏颖芽费铸妊孕询纱启敢送龙卿叉示河巨才恬异租剁莱绰筐荫钱先腕屯麓冀
高中生物奥林匹克竞赛教程:生物氧化

中学生物奥林匹克讲义---生物氧化生物体需要的能量主要是通过代谢物在体内氧化而获得的。
物质在生物体内经过氧化最后生成水和CO2并释放能量的过程,称为生物氧化,由于这一过程是在组织细胞内进行的,表现为细胞摄取O2而释放CO2,因此生物氧化又称为组织呼吸或细胞呼吸。
虽然糖、脂肪及蛋白质等在体内外氧化分解,都产生水和CO2,并释放出等量的能量,但生物氧化与燃烧的过程有显著不同:生物氧化反应是在温和的条件下进行的酶促反应,所释放的能量,有一部分以化学能的形式储存在ATP分子中。
1.生物氧化的方式和酶类(1)生物氧化中二氧化碳生成的方式生物体内二氧化碳的生成并不是物质中所含的碳、氧原子的直接化合,而是来源于糖、脂肪等转变来的有机酸的脱羧。
根据脱去二氧化碳的羧基在有机酸分子中的位置,可将脱羧反应分为α–脱羧与β–脱羧两种类型。
有些脱羧反应不伴有氧化,称为单纯脱羧;有些则伴有氧化,称为氧化脱羧。
例如苹果酸的氧化脱羧:(2)生物氧化中物质氧化的方式在化学反应中,失电子、脱氢、加氧都属于氧化;得电子、加氢、脱氧都属于还原。
这种变化规律,无论在体内或体外,都是一样的。
不同的是,体内氧化都是酶促反应。
常见的氧化类型有脱电子、脱氢、加水脱氢和加氧反应。
生物体内并不存在游离的电子或氢原子,在上述氧化反应中脱下的电子或氢原子必须为另一物质所接受。
这种既能接受又能供出电子或氢原子的物质称为递电子体或递氢体。
(3)与生物氧化有关的酶类①氧化酶类:能直接利用氧分子作为受氢体,其中氧化酶含铜,反应产物是水,如细胞色素氧化酶。
②需氧脱氢酶类:通常以黄素腺嘌呤二核苷酸(FAD)为辅基,反应产物为过氧化氢。
习惯上有时将需氧脱氢酶不严格地称为氧化酶,如黄嘌呤氧化酶。
③不需氧脱氢酶:不能以氧分子而只能以体内某些辅酶为直接受氢体,这些辅酶包括尼克酰胺腺嘌呤二核苷酸(NADP+)、尼克酰胺腺嘌呤二核苷酸磷酸(NAD+)、黄素单核苷酸(FMN)或黄素腺嘌呤二核苷酸(FAD)等。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第八章 生物氧化(6学时)第一节 概述生物氧化的一般过程在葡萄糖的分解代谢中,1分子葡萄糖共生成10个NADH 和2个FADH 2.总的△Gˊ0=-2564.8KJ/mol 在燃烧时,1分子葡萄糖可释放出的热 2870.23KJ/mol ,因此可推算葡萄糖分子所释放自由能的90%贮存在还原型辅酶中. 还原辅酶的再氧化在电子传递过程中,还原辅酶借助O 2得以氧化的过程可用下式表示: NADH+H ++1/2O 2 → NAD ++H 2O △Gˊ0=-220.07KJ/mol →ATP FADH 2 +1/2O 2→ FAD+ H 2O △Gˊ0=-181.58KJ/mol →ATP产能物质在不同的分解代谢过程中,都伴有代谢物的脱H 和辅酶NAD +或FAD 的还原.这些携带着H +和e 的还原型辅酶NADH 和FADH 2,最终将H +和e 传递给氧时,都经历相同的一系列电子载体传递过程.第二节 线粒体氧化体系(呼吸链)生物体内存在多种氧化体系,其中最重要的是存在与线粒体中线粒体氧化体系。
此外还有微粒体氧化体系、过氧化体氧化体系、细菌的生物氧化体系等。
一、线粒体氧化体系(呼吸链)在生物氧化过程中,代谢物的氢由脱氢酶激活,脱下来的氢经过几种传递体的传递,将电子传递到细胞色素体系,最后将电子传递给氧,活化的氢(H +)和活化的氧(O 2-)结合成水,在这个过程中构成的传递链称为电子传递链,或呼吸链。
(一)呼吸链的组成构成呼吸链的成分有20多种。
大致可将它们分成五类。
即以NAD +或NADP +为辅酶的脱氢酶类;以FAD或FMN为辅基的黄素蛋白酶类;铁硫蛋白类;泛醌和细胞色素类。
依具体功能又可分为递氢体和递电子体。
1.递氢体在呼吸链中即可接受氢又可把所接受的氢传递给另一种物质的成分叫递氢体,包括:(1)NAD+NAD+是不需氧脱氢酶的辅酶。
它们分别可与不同的酶蛋白组成多种功能各异的不需氧脱氢酶。
辅酶分子能可逆地加氢和脱氢。
NAD++2H++2e-→NADH+H+(2)FAD和FMNFAD和FMN是黄素蛋白(又称黄素酶)类的辅基。
它们能可逆地加氢和脱氢。
(3)泛醌泛醌(Q),因广泛分布与生物界并具有醌的结构而得名。
它以1,4-苯醌作为传递H+和e的反应核心,氧化还原过程是先接受一个H+和e变成半醌,在接受一个H+和e变成氢醌。
氧化还原总反应为:2.递电子体既能接受电子又能将电子传递出去的物质叫做递电子体。
呼吸链中的递电子体包括两类。
(1)铁硫蛋白类铁硫蛋白(Fe-S )是存在于线粒体内膜上的一类与电子传递有关的蛋白质。
现已发现的铁硫蛋白有九种,各种铁硫蛋白中均含有铁和对硫不稳定的硫,用硫酸处理可释放出H 2S 。
Fe-S 代表铁硫蛋白电子传递的反应中心,即称铁硫中心。
Fe-S 中的Fe 均与蛋白质分子中半胱氨酸残基上的-SH 中的S 结合。
铁硫中心的Fe 原子能可逆地获得和丢失电子,在呼吸链中起到传递电子的作用:(2)细胞色素类细胞色素(Cyt )是广泛分布于需氧生物线粒体内膜上的一类传递电子的色素蛋白,其辅基为含铁卟啉的衍生物。
参与线粒体生物氧化体系的有Cyta 、a 3、b 、1 、c 。
细胞色素电子传递作用就是依靠分子中铁离子化合价的可逆变化而实现的。
目前尚不能将Cyta 和a 3分开,故将它们合称为细胞色素氧化酶。
它们靠分子中所含的铜的氧化还原变化来实现电子传递作用。
(二)呼吸链中传递体的排列顺序呼吸链中氢和电子的传递有严格的顺序和方向,这些顺序和方向是根据各种递氢体和递电子体的标准氧化还原电位数值的测定,并利用某些特异的抑制剂切断其中的电子流后,再测定电子传递链中各组分的氧化还原态,以及在体外将电子传递体重新组成呼吸链等实验而得到结论。
用去垢剂温和处理线粒体内膜,可以得到四种电子传递复合体,每一种复合体代表完整呼吸链的一部分,具有各自独特的功能。
复合体Ⅰ:指呼吸链从NAD +到泛醌之间的组分,整个复和物嵌在线粒体内膜上。
在电子通过复合体Ⅰ转移时,质子也从基质转移到了膜间隙。
研究表明:每从NADH 转移1对电子给CoQ ,就将有4个质子被转移到膜间隙。
复合体Ⅱ:介于琥珀酸到泛醌之间,能将2H 从琥珀酸传给FAD ,然后经铁硫蛋白传递至Q 。
该复合物对跨膜的质子梯度没有贡献,它的主要贡献是将来自琥珀酸氧化的电子引入到电子传递链中。
复合体Ⅲ:从Q 到细胞色素C 之间的呼吸链组分,包含Cytb 、c 1、铁硫蛋白以及其他多种蛋白质。
研究表明:伴随1分子CoQH2的氧化有4个质子被转移到膜间隙。
其中2个质子来自CoQH2,另2个来自基质。
复合体Ⅳ:又称细胞色素氧化酶,包括细胞色素Cytaa3,电子从细胞色素C通过复合体Ⅳ传递给氧,同时引起质子从线粒体基质向外流动。
细胞色素c氧化酶对质子浓度梯度的贡献通过两种方式表现的:每传递1对电子转移2个质子。
(三)呼吸链中传递体排列顺序的确定呼吸链成分的排列顺序由以下实验确定:1.标准氧化还原电势(E′°)由低→高:即标准电势的正值越大的,越倾向于获得电子,易成为氧化剂处于呼吸链的末端。
2.特异抑制剂阻断:能够阻断呼吸链中某部位电子传递过程的药物或毒物称为电子传递抑制剂。
至使呼吸链中断。
经典的抑制剂及抑制位点:(1) 鱼藤酮、安密妥以及杀粉蝶菌素:(NADH CoQ)(2) 抗霉素A是由链霉菌分离出的抗菌素:(Cytb CytC1)(3) 氰化物、硫化物、叠氮化物和一氧化碳等:(Cytaa3 O2)3.体外拆开和重组4.离体线粒体缓慢给氧观察氧化顺序(四)呼吸链的类型呼吸链按其组成成分、排列顺序和功能上的差异分为两种。
1.NADH氧化呼吸链:复合物Ⅰ-Ⅲ-Ⅳ组合组成以NADH为首的传递链,既以NADH为首的呼吸链,通常称为长呼吸链。
它们的排列顺序如下:NADH→FMN→FeS→CoQ→Cytb→FeS→Cytc1→Cytc→Cyta,a3→O2复合物Ⅰ复合物-Ⅲ复合物Ⅳ2.FADH2氧化呼吸链;复合物Ⅱ-Ⅲ-Ⅳ组合组成以琥珀酸脱氢酶为首的传递链,既以琥珀酸脱氢酶为首的呼吸链,称之为短呼吸链。
它们的排列顺序如下:FADH2→FeS→CoQ→Cytb→FeS→Cytc1→Cytc→Cyta,a3→O2复合物Ⅱ复合物-Ⅲ复合物Ⅳ第三节氧化磷酸化作用一、呼吸链的作用无论是NADH呼吸链还是FAD呼吸链,都可将代谢物上脱下的氢与氧结合生成水,同时为机体生命活动提供能量。
](一)代谢水的生成根据两种呼吸链显示,呼吸摄入的氧与氢反应生成水。
也就是说代谢物脱下的氢(2H++e),通过递氢体和递电子体最终使氧激活(1/2O2+2e→O2-),活化的氧与基质中的2个氢化合成水,完成呼吸链的一次全程传递。
这种方式生成的水称代谢水。
若无氧的存在,呼吸链也就无法进行。
需氧生物不能生存的主要原因就是呼吸链对氧的绝对需求,呼吸链的正常传递为机体提供了足够的能量。
(二)能量的生成体内ATP形成有两种方式,与呼吸链有关的是氧化磷酸化方式。
氧化磷酸化:供机体生命活动的能量主要来自氧化磷酸化作用。
定义:代谢物脱下的氢在呼吸链一系列氢转移和电子传递的氧化过程中释放能量使ADP磷酸化生成ATP的过程。
1.P/O比值与偶联次数P/O比值是指,当底物进行氧化时,每消耗1个氧原子所消耗的用于ADP磷酸化的无机磷酸中的目前被广泛接受的观点是:已知每合成1个ATP需要3个质子。
与此同时,把一个ATP分子从线粒体基质转运到胞液需要消耗1个质子,所以每形成1个分子的ATP就需要4个质子的流动。
每形成1个ATP共需消耗4个质子:一对电子从NADH→ O2有10个质子泵出,将产生2.5个ATP,P/O比值为2.5;一对电子从FADH2 → O2有6个质子泵出,将产生1.5个ATP,P/O比值为1.5。
2.氧化磷酸化的偶联部位:合成1molATP时,需要提供的能量至少为ΔG′0=-30.5kJ/mol,相当于氧化还原电位差ΔE′°=0.2V。
根据ΔG′0=-nFΔE′°,电子传递每一步骤释放的自由能多少不等,其中有3处释放的自由能较多,足可以供ADP与无机磷酸作用生成A TP反应所需要的能量(ΔG ═ +30.5 kj/mol)。
在这些步骤上,就可能发生底物氧化与ADP磷酸化的偶联,生成A TP。
三个偶联部位为:NADH ─→ CoQ ΔG ═ -50.24 kj/molCytb ─→ Cytc1ΔG ═ -41.87 kj/molCyta,a3─→ O2ΔG ═ -100.48 kj/mol3.氧化磷酸化机制关于这一问题目前比较著名的假说有三个:(1)化学偶联假说(1953年):认为电子传递反应释放的能量通过一系列连续的化学反应形成高能共价中间物,最后将其能量转移到ADP中形成ATP。
(2)构象偶联假说(1964):认为电子沿电子传递链传递使线粒体内膜的蛋白质组分发生了构象变化,形成一种高能构象,这种高能形式通过A TP的合成而恢复其原来的构象。
迄今未能分离出这种高能蛋白质。
但在电子传递过程中蛋白质组分的构象变化还是存在的。
(3)化学渗透学说(The chemiosmotic theory) :目前被普遍接受的是化学渗透学说。
英国生物化学家Peter D Mitchell(米切尔)在1961年提出化学渗透假说,于1978年的诺贝尔化学奖。
该学说主要论点认为:氧化呼吸链存在于线粒体内膜上,电子经呼吸链传递时,释放的自由能驱动质子(H+)从线粒体基质跨过内膜进入到膜间隙,从而形成跨线粒体内膜的H+电化学梯度。
这个梯度的电化学电势可以被存在于线粒体内膜上的A TP合酶利用,驱动A TP的合成。
4.ATP的合成场所— FO F1-ATP合酶线粒体内膜的表面一层规则地间隔排列着的球状颗粒,称为ATP合酶,是ATP合成的场所。
组成:F1:亲水部分(头部)(α3β3γδε亚基)柄:含有两种蛋白质:OSCP(寡霉素敏感性付与蛋白)和F6(偶合因子6)是能量转换的通道。
Fo :疏水部分(a1b2c9~12亚基)功能:F1:催化ATP生成(在β亚基上)Fo:质子通道(二)氧化磷酸化的影响因素1.ATP/ADP比值:ATP/ADP比值是调节氧化磷酸化速度的重要因素。
ATP/ADP比值下降,可致氧化磷酸化速度加快;反之,当ATP/ADP比值升高时,则氧化磷酸化速度减慢2.甲状腺激素:甲状腺激素可间接影响氧化磷酸化的速度。
其原因是甲状腺激素可以激活细胞膜上的Na+,K+-A TP酶,使A TP水解增加,因而使A TP/ADP比值下降,氧化磷酸化速度加快。
3.药物和毒物:(1)呼吸链的抑制剂:(2)解偶联剂(uncouplers):作用:使电子传递与ATP形成两个过程分离. 只抑制ATP的形成过程,不抑制电子传递过程,使电子传递产生的自由能都变为热能.典型的解偶联剂: 2,4-二硝基苯酚(DNP)2,4-二硝基苯酚(DNP)作用机制:在pH7的环境下,DNP以解离的形式存在,不能透过线粒体内膜.在酸性条件下,DNP接受质子成为非解离的亲脂形式,可透过线粒体内膜,同时将质子带入基质,破坏了内膜两侧的质子梯度,使ATP 不能形成.(3)氧化磷酸化的抑制剂(inhibitors):氧化磷酸化的抑制剂是直接抑制ATP合成的化学物质,如寡霉素(oligomycin)。
