18.电子传递和氧化磷酸化
18电子传递和氧化磷酸化

琥珀酸-Q还原酶
琥珀酸是生物代谢过程(三羧酸循环)中产生的 中间产物,它在琥珀酸-Q还原酶(复合物II)催 化下,将两个高能电子传递给Q。再通过QH2-cyt, c还原酶、cyt.c和cyt.c氧化酶将电子传递到O2 。 琥珀酸-Q还原酶也是存在于线粒体内膜上的蛋白 复合物, 它比NADH-Q还原酶的结构简单,由4个 不同的多肽亚基组成。其活性部分含有辅基FAD 和铁硫蛋白。 琥珀酸-Q还原酶的作用是催化琥珀酸的脱氢氧化 和Q的还原。
细胞色素c(cyt.c)
它是电子传递链中一个 独立的蛋白质电子载体, 位于线粒体内膜外表, 属于膜周蛋白,易溶于 水。它与细胞色素c1含 有相同的辅基,但是蛋 白组成则有所不同。在 电子传递过程中,cyt. c通过 Fe3+ Fe2+ 的互变起 电子传递中间体作用。
细胞色素c氧化酶
-----半胱------半胱----- S S Fe Fe S S S S
-----半胱------半胱-----
NADH泛醌还原酶
简写为NADHQ还原酶, 即复合物I,它的作用是 催化NADH的氧化脱氢以及Q的还原。所以它既是一 种脱氢酶,也是一种还原酶。 NADHQ还原酶最 少含有16个多肽亚基。它的活性部分含有辅基FMN 和铁硫蛋白。 FMN的作用是接受脱氢酶脱下来的电子和质子,形 成还原型FMNH2。还原型FMNH2可以进一步将电子 转移给Q。
泛醌细胞色素c还原酶
简写为QH2-cyt. c还原酶, 即复合物III, 它是线粒体内膜上的一种跨膜蛋白复合物, 其作用是催化还原型QH2的氧化和细胞色素 c(cyt. c)的还原。
QH2-cyt. c 还原酶
QH2 + 2 cyt. c (Fe3+) ==== Q + 2 cyt. c (Fe2+) + 2H+
第五章电子传递和氧化磷酸化

述
第
三.生物氧化的特点
一 都是加氧、去氢、失去电子,都生成CO2和H2O 节,
(1)生物氧化是在细胞内进行的,,条件较温和
生 而体外反应条件剧烈
物 氧
(2)能量逐步释放出来,不会因骤然释放而损害 机体,同时能量得到有效的利用;而体外能量突 然爆发式释放出来
化 (3)生物氧化所释放出的能量中,大部分转换为 概 ATP分子中活跃的化学能,
应物产物的氧化还原电位计算。
生 氧还对:生物氧化包括一系列的氧化还原反应, 参与氧化还原反应的每一种物质都有氧化态和还
物 原态,称为氧还对。 氧 生化标准氧化还原电位:是指在pH7,25℃,氧 化 化态与还原态物质浓度(近似活度)为1mol/L
等标准条件下,与标准氢电极组成原电池测定得
概 到的氧化还原电位,符号为E0′。在生物体中,发 述 生氧化还原反应的每一氧还对,其电子转移势能
CO2和H2O,并释放出大量生命所需要的能量。
代 谢 的 三 个 阶 段
第
二.生物氧化的方式
1.脱氢氧化反应
一 (1)脱氢 节 在生物氧化中,脱氢反应占有重要地位。它是许
生 多有机物质生物氧化的重要步骤。催化脱氢反应 的是各种类型的脱氢酶。
物
COOH
COOH
氧 化
CH2 CH2 COOH
CH
+
CH
节 ATP的生成方式
生 (1)底物水平磷酸化:前一章EMP和TCA循环。
物 (2)光合磷酸化:光驱动电子在光合链中传递
氧
释放出能量,使ADP磷酸化生成ATP
化 (3)氧化磷酸化 :该章重点内容
概
述
第
五.高能化合物
生物氧化——电子传递和氧化磷酸化作用

氧还-回路机制示意图
质子转移的两种假设机制
(2)质子泵机制
这个机制的内容是,电子传递导致复合 体构象的变化,氨基酸残基在膜内侧结合H+, 构象变化后在膜外侧释放H+,从而把H+从膜 内侧运到膜外。
三种类型的Fe-S cluster
半胱氨酸的巯基硫
Fe
Fe2-S2
Fe4-S4
每传递2个电子,可 驱动4个H+从膜内侧 运到膜外侧。
NADH-Q还原酶 催化的电子传递
电子传递链各个成员
2.辅酶Q
辅 酶 Q ( Coenzyme Q ) 又 称 泛 醌 (ubiquinone),有时简称为Q或UQ,是一种脂溶 性物质,它可以接受1个电子还原成半醌中间体,再 接受1个电子还原成对苯二酚形式。由于其脂溶性强, 可以在线粒体内膜中扩散。它有一个长长的碳氢侧 链,哺乳动物中最常见的是具有10个异戊二烯单位 的侧链,简写为Q10,在非哺乳动物中这个侧链可能 只有6~8个异戊二烯单位。
琥珀酸-Q还原酶 催化的电子传递
电子传递链各个成员
4.细胞色素还原酶
细胞色素还原酶又称复合体Ⅲ、辅酶Q- 细胞色素c还原酶。它的作用是将还原型辅酶 Q的电子传递给细胞色素c。细胞色素还原酶 中含有细胞色素b,也含有2Fe-2S聚簇。
细胞色素(cytochrome)
细胞色素是一类含有血红素辅基的电子传递蛋 白质的总称。还原型细胞色素具有明显的可见光吸 收,可以看到α、β和γ三个吸收峰,其中α峰的波长 随细胞色素种类的不同而各有特异的变化,可用来 区分不同的细胞色素。氧化型细胞色素在可见光区 看不到吸收峰。细胞色素中的血红素有三种,分别 称为细胞色素a、b和c,同一种细胞色素血红素因结 合的蛋白质不同,其α吸收峰的波长会发生小的变化, 如 细 胞 色 素 还 原 酶 中 含 有 的 细 胞 色 素 b 就 分 为 bH (b562)和bL(b566)两种。
第三节 电子传递与氧化磷酸化
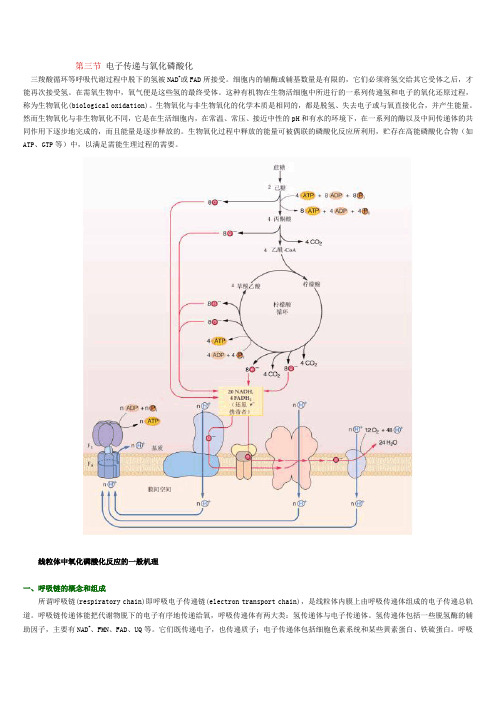
第三节电子传递与氧化磷酸化三羧酸循环等呼吸代谢过程中脱下的氢被NAD+或FAD所接受。
细胞内的辅酶或辅基数量是有限的,它们必须将氢交给其它受体之后,才能再次接受氢。
在需氧生物中,氧气便是这些氢的最终受体。
这种有机物在生物活细胞中所进行的一系列传递氢和电子的氧化还原过程,称为生物氧化(biological oxidation)。
生物氧化与非生物氧化的化学本质是相同的,都是脱氢、失去电子或与氧直接化合,并产生能量。
然而生物氧化与非生物氧化不同,它是在生活细胞内,在常温、常压、接近中性的pH和有水的环境下,在一系列的酶以及中间传递体的共同作用下逐步地完成的,而且能量是逐步释放的。
生物氧化过程中释放的能量可被偶联的磷酸化反应所利用,贮存在高能磷酸化合物(如ATP、GTP等)中,以满足需能生理过程的需要。
线粒体中氧化磷酸化反应的一般机理一、呼吸链的概念和组成所谓呼吸链(respiratory chain)即呼吸电子传递链(electron transport chain),是线粒体内膜上由呼吸传递体组成的电子传递总轨道。
呼吸链传递体能把代谢物脱下的电子有序地传递给氧,呼吸传递体有两大类:氢传递体与电子传递体。
氢传递体包括一些脱氢酶的辅助因子,主要有NAD+、FMN、FAD、UQ等。
它们既传递电子,也传递质子;电子传递体包括细胞色素系统和某些黄素蛋白、铁硫蛋白。
呼吸链传递体传递电子的顺序是:代谢物→NAD+→FAD→UQ→细胞色素系统→O2。
呼吸链中五种酶复合体(enzyme complex)的组成结构和功能简要介绍如下(图5-11,5-12)。
图 5-11 植物线粒体内膜上的复合体及其电子传递Ⅰ、Ⅱ、Ⅲ、Ⅳ、Ⅴ分别代表复合体Ⅰ、Ⅱ、Ⅲ、Ⅳ、Ⅴ; UQ库代表存在于线粒体中的泛醌库1.复合体Ⅰ 又称NADH∶泛醌氧化还原酶(NADH∶ubiquinone oxidoreductase)。
分子量700X103~900X103,含有25种不同的蛋白质,包括以黄素单核苷酸(flav in mononucleotide,FMN)为辅基的黄素蛋白和多种铁硫蛋白,如水溶性的铁硫蛋白(iron sulfur protein,IP)、铁硫黄素蛋白(iron sulfur flavoprotein,FP)、泛醌(ubiquinone,UQ)、磷脂(phospholipid)。
电子传递与氧化磷酸化

电子传递与氧化磷酸化在疾病中的作用研究
心血管疾病
研究表明,电子传递与氧化磷酸化在心血管 疾病中发挥重要作用。例如,某些遗传性疾 病如Leber遗传性视神经病和肌萎缩侧索硬 化症(ALS)与电子传递链的缺陷有关。
神经系统疾病
许多神经系统疾病如帕金森病、阿尔茨海默 病和亨廷顿氏病等也与电子传递与氧化磷酸 化的异常有关。这些疾病通常伴随着线粒体 功能障碍和氧化应激的增加。
02
在这个过程中,电子从还原剂(如NADH或FADH2)传递 到氧分子,同时伴随ATP的合成。
03
氧化磷酸化主要发生在线粒体内膜上,是细胞呼吸链的主要 组成部分。
氧化磷酸化的过程
电子从NADH或FADH2开始, 经过一系列传递体(如复合体 Ⅰ、Ⅲ、Ⅳ)传递到氧分子。
在这个过程中,质子被泵出线 粒体基质,形成质子梯度。
土壤修复
利用电子传递与氧化磷酸化原理,促进土壤中有机污染 物的降解和转化,实现土壤的生态修复。
THANKS FOR WATCHING
感谢您的观看
药物靶点
电子传递与氧化磷酸化过程中涉及的酶和蛋白质可以 作为药物设计的潜在靶点,用于开发新的药物。
药物筛选
利用电子传递与氧化磷酸化的机制,建立药物筛选模 型,快速筛选出具有潜在疗效的药物分子。
在环境保护领域的应用前景
废水处理
通过模拟电子传递与氧化磷酸化过程,开发高效、环保 的废水处理技术,降低废水中有害物质的含量。
03
氧化磷酸化过程中释放的能量可以用于合成高能化合物,如ATP、 GTP等,这些化合物在细胞内发挥着重要的生物学功能。
04
氧化磷酸化还参与细胞内氧化还原状态的调节,对于维持细胞内环境 的稳定具有重要意义。
第二章 生物氧化(电子传递与氧化磷酸化)

(电子传递与氧化磷酸化)
第一节 氧化还原电势 第二节 生物氧化概述 第三节 电子传递链(呼吸链) 第四节 氧化磷酸化 第五节 线粒体穿梭系统
1-还原电势
第一节、氧化还原电势
一、氧化还原电势: 1、概念: • 氧化还原反应:凡在反应过程中有电子从一种物质 (还原剂)转移到另一种物质(氧化剂)的化学反应。 往往是可逆的 • 还原剂:在氧化还原反应中提供电子的物质。 • 氧化剂:夺得电子的物质 • (氧化)还原电势:还原剂失去电子(氧化剂得到电 子)的倾向。 • 氧化-还原电子对:氧化剂和还原剂相偶联构成的, 任何氧化还原电子对都有特定的标准电势
1-还原电势-生物体内还原电势
生物体内一些反应的标准氧化还原电势(P117)
还原剂 铁氧还蛋白(还原态) 氧化剂 铁氧还蛋白(氧化态) E’0伏 -0.43
H2
NADH(+H+) NADPH(+H+) Cytb(Fe2+) 泛醌(还原态) Cytc(Fe2+) H2O
2H+
NAD+ NADP+ Cytb(Fe3+) 泛醌(氧化态) Cytc(Fe3+) 1/2O2+2H+
第三节
电子传递链(呼吸链)
一、线粒体的通透性
•外膜:自由透过小分子和离子 •内膜: •不能自由透过小分子和离子,包括 NADH、ATP、ADP、Pi和 H+。 •有电子传递体、ATP合酶(FoF1) •膜间隙:含有许多可溶性酶、底物和一 些辅助因子。 基质:有丙酮酸脱氢酶、TCA的酶、脂肪 酸氧化的酶、氨基酸氧化的酶、DNA、核 糖体、ATP、ADP、Pi、Mg2+、可溶的中 间产物、其他酶
正极反应: Cu↔Cu2++2e
电子传递与氧化磷酸化

(7)细胞色素C氧化酶(复合物Ⅳ)
由 cyt.a和a3 组成。复合物中除了含有铁卟啉 外,还含有2个铜原子(CuA,CuB)。cyta与CuA相 配合,cyta3与CuB相配合,当电子传递时,在细胞 色素的Fe3+ Fe2+间循环,同时在Cu2+ Cu+间循环, 将电子直接传递给O2,也叫末端氧化酶。
△G0’= -nF△E0’ = -nF (E0’受体 - E0’ 供体)
其中:n 是转移的电子数,F 是法拉第常数。
呼吸链中电子流动方向与ATP的生成
NADH
FADH2
2e-
三.电子传递抑制剂(P184)
凡能够阻断呼吸链中某一部位电子流的物质,称为 呼吸链电子传递抑制剂.
返回
各种抑制剂的作用位点
铁硫聚簇借Fe2+和 Fe3+的互变传递电子,每次传递
一个电子.(Fe3+ +e- Fe2+ )
Cys S
S
S Cys
+e-
Fe3+
Fe3+
Cys S
S
S Cys
Cys S
S
S Cys
Fe3+
Fe2+
Cys S
S
S Cys
(4)辅酶Q(泛醌,CoQ,是许多酶的辅酶)
辅酶Q(泛醌, CoQ, Q)是电子传递链中的唯一的一种非蛋 白质组分,功能基团是苯醌,在电子传递过程中可在醌型 (氧化型)与氢醌型(还原型)之间相互转变。NADH和 FADH2上的H和电子都必须经过辅酶Q最终传递到氧分子,因 此,它是电子传递链的中心和电子集中点。
NADH + H+ + FMN
电子传递和氧化磷酸化

解耦联剂存在和不存在条件下线粒体的呼吸 (a)过量的Pi和底物存在下,当加入ADP后,氧快速消耗, (b)加入解耦联剂2,4-二硝基苯酚后,底物的氧化过程没有发生ADP磷酸化
在没有ADP的条件下,称为解耦联剂的化合物可以刺激 底物的氧化,直至所有的可利用的氧被还原为止,但底物的 氧化过程没有发生ADP磷酸化。简言之,这些化合物的氧化 没有与磷酸化过程耦联。
12.3 贮存在质子浓度梯度中的能量具有电能和化学 能的成分
通过呼吸复合物转移到膜间隙的质子经过ATP合成酶返回基 质时,形成一个质子环流。质子浓度梯度的能量称为质子动力 势,类似于电化学中的电动势。
在一分子氧被一个还原剂 XH2 还原的电化学反应池中:
XH2+1/2O2 X+H2O
电子从阴极流出,阴极处的 XH2 被氧化:
12.1 真核生物中,氧化磷酸化发生在线粒体中 12.2 化学渗透假说解释了电子传递是如何与ADP的
磷酸化耦联的 12.3 贮存在质子浓度梯度中的能量具有电能和化学
能的成分 12.4 电子传递和氧化磷酸化取决于蛋白质复合物 12.5 穿梭机制使得胞液中的NADH可被有氧氧化
需氧生物能够利用氧将葡萄糖(以及其他有机物分 子)完全氧化,产生二氧化碳(CO2)和水(H2O)。葡萄糖 完全氧化的总反应可用下式表示:
1. 一个完整的线粒体内膜对于耦联是绝对需要的。膜对带电 的溶剂应当是不通透的,否则质子浓度梯度将消失,特殊的 转运体使得离子代谢物跨过膜。
2. 通过电子传递链的电子传递产生一个质子浓度梯度,线粒 体内膜外侧(膜间隙)的H+浓度很高。
3. 一个结合于膜上的酶-ATP合成酶在跨膜的质子转移电子由阴极流到阳极,阳极处的分子氧被还原:
1/2O2+2H++2e- H2O
电子传递和氧化磷酸化

一个典型的哺乳动物线粒体的直径是0.2m到0.8m,长度 为0.5m到1.5m,大小类似于大肠杆菌细胞。
线粒体外膜 线粒体外膜
膜间隙
线粒体基质
嵴
20.2 化学渗透学说解释了电子传递是如何 与ADP磷酸化耦联的
一个质子浓度梯度作为能量库用于驱动 ATP的形成的概念被称之化学渗透理论, 是由Peter Mitchell于1961年提出来的,获 得了1978年诺贝尔化学奖。
2 复合物I将来自NADH的电子传递给泛醌
复合物I NADH-泛醌氧化还原酶(也称之NADH脱氢酶) 催化NADH的两个电子转移给泛醌。
鱼藤酮(一种植物毒素)和安密妥加入到线粒体悬浮液将 阻断复合物 I 中的电子传递。
复合物I中电子转移和质子流
3 复合物II将电子由琥珀酸转移到泛醌
XH2
X+2H++2e-
电子由阴极流到阳极,阳极处的分子氧被还原:
1/2O2+2H++2e- H2O
由于两个反应池存在电势差,电子能够通过外部的导线流动。
电子流的方向和氧化剂还原的程度是由XH2和O2之间的自由能 的差确定的,而这一差别又取决于它们各自的还原电位。
化学电池
线粒体中
(a)在化学电池中,电子通过连接两个原电池的导线从XH2流向氧化剂O2。 (b)在线粒体中,质子被跨膜转运到膜间隙,造成跨膜的质子浓度梯度,
1. 一个完整的线粒体内膜对于耦联是绝对需要的。膜对带电 的溶剂应当是不通透的,否则质子浓度梯度将消失,特殊的 转运体使得离子代谢物跨过膜。
2. 通过电子传递链的电子传递产生一个质子浓度梯度,线粒 体内膜外侧(膜间隙)的H+浓度很高。
3. 一个结合于膜上的酶-ATP合成酶在跨膜的质子转移驱动反 应中催化ADP磷酸化。
电子传递与氧化磷酸化

催化ADP 和PI的转 变为ATP.
除以上之外还有:UQ和 Cytc UQ:电子传递链中非蛋白质成员 实现在复合体Ⅰ,Ⅱ,Ⅲ之间的传递。 Cytc: 线粒体内膜外侧的外周蛋白,是电子 传递链中唯一的可移动色素蛋白,通过辅 基中的铁离子价的可逆变化,在复合体Ⅲ 和Ⅳ之间传递电子。
在氰化物的存在下,某些植物呼吸不受抑 制,所以把这种呼吸称为抗氰呼吸。 抗氰呼吸电子传递途径与正常的NADH电子 传递途径交替进行,所以抗氰呼吸途径由 称为交替呼吸途径,简称交替途径。
①.利于授粉 ②.能量溢流 ③.增强抗逆性
植物线粒体膜间隙油附属2个外脱氢酶,分 别是外在的NADH 和NADPH脱氢酶,都对 鱼藤酮不敏感。 功能:催化细胞质中的NADH或NADPH的 氧化,把氧化脱下的电子直接传递给UQ库。
↓
O2
氧化
偶联
↓ 供生命活动,生化反应需要
ATP
磷酸化
½ O 2 → H+ + e
ATP
营养物分解
氧化磷酸化
肌肉收缩,物质转运 信息传递,腺体分泌
ADP
氧化磷酸化作用: 在生物氧化中,电子经过线粒体电子传递链传递到 氧,伴随ATP合酶催化,使ADP和磷酸合成ATP的过程。
线粒体内膜与氧化磷酸化
线粒体是生物氧化和能量转换的主要场所。是组 织细胞的“发电厂”。
在呼吸链一系列反应的最末端,有能活化 分子氧并生成ATP的末端氧化酶。 如:线粒体膜上:细胞色素c氧化酶和交替 氧化酶。 细胞质基质和微粒体中,还存在不产生ATP 的末端氧化酶体系。如:酚氧化酶. 抗坏血 酸氧化酶.乙醇酸氧化酶等。
重要的酚氧化酶:单酚氧化酶(酪氨酸酶 ) 和多酚氧化酶(儿茶酚氧化酶) 酚氧化酶是含铜的酶。
简述氧化磷酸化和电子传递的偶联机制

简述氧化磷酸化和电子传递的偶联机制
氧化磷酸化和电子传递是生物体中重要的代谢过程,它们之间存在着偶联机制。
氧化磷酸化是一种重要的代谢过程,它可以将低能量的磷酸化物转化为高能量的磷酸化物,从而提供细胞活动所需的能量。
氧化磷酸化的偶联机制是通过一系列的反应来实现的,首先,一种叫做ATP酶的酶将ATP分解为ADP和磷酸,然后,一种叫做磷酸酶的酶将磷酸与另一种叫做磷酸酰转移酶的酶结合,最后,一种叫做磷酸酰转移酶的酶将磷酸酰转移到另一种叫做磷酸酰转移酶的酶上,从而实现氧化磷酸化反应。
电子传递是一种重要的代谢过程,它可以将低能量的电子转移到高能量的电子,从而提供细胞活动所需的能量。
电子传递的偶联机制是通过一系列的反应来实现的,首先,一种叫做NADH的酶将NADH分解为NAD+和电子,然后,一种叫做电子转移酶的酶将电子转移到另一种叫做电子转移酶的酶上,最后,一种叫做电子转移酶的酶将电子转移到另一种叫做NADH的酶上,从而实现电子传递反应。
总之,氧化磷酸化和电子传递是生物体中重要的代谢过程,它们
之间存在着偶联机制,即通过一系列的反应来实现氧化磷酸化和电子传递反应。
这些反应可以提供细胞活动所需的能量,从而保证细胞的正常运作。
2014 生物氧化—电子传递和氧化磷酸化

非标准状态下,根据实际参加反应物和产物浓度, 用能斯特方程式计算,求出反应的电动势。
第三节 电子传递链
1. 电子传递过程: 指还原型的辅酶(NADH、 FADH2)通过电子传递再氧化的过程。
电子传递链:由一系列具有氧化还原作用的载体组成,
电子、质子通过呼吸链中4个复合体概况
(四)电子传递抑制剂:
能够阻断呼吸链中某部位电子传递的物质。
电子传递的抑制剂: 1. 鱼藤酮 、安密妥 、杀粉蝶菌素
NADH || CoQ
2. 抗霉素A
Cytb || CytC1
3. 氰化物、硫化氢、叠氮化物、CO
铂酸-Q还原酶(复合体II)、细胞色素还原酶(复合体
III)、细胞色素C和细胞色素氧化酶(复合体IV ) 。
• 主链上形成三个复合物,包埋在线粒体内膜,每
一复合体包括几个电子或氢传递体,三个复合物之间 由两个小电子载体(CoQ和CytC)相连。
•有三个ATP形成位点.
氧化呼吸链各组分的顺序排列是由以下实验确定的
并且按其对电子亲和力递增的顺序排列, 即电子从 NADH(-0.32V)系列电子传递体 氧(+0.82V)的方向传递。
2. 电子传递链(呼吸链)的组成特点
• 呼吸链中的传递体大多和水不溶性蛋白相结合,多
数嵌合在线粒体内膜中。传递体包括氢传递体(电 子、质子)和电子传递体两大类。
• 组成包括:NAD-Q还原酶(复合体I )、CoQ、琥
第二节 氧化还原电势 (E°)
还原电位可以 通过电化学装 置定量地测定。 其原理可以通 过一对电子从 锌原子转移到 一个铜离子 (Cu2+)的简 单的氧化-还 原反应来说明。
电子传递与氧化磷酸化

线粒体内膜的功能有3个方面:
1.氧化脱羧生成CO2的同时,NAD+、FAD还原为
NADH和FADH2,这发生在线粒体基质或面向基 质的内膜蛋白质上; 2.电子从NADH和FADH2传至线粒体内膜上,并同 时形成跨膜质子泵; 3.将储存在电化学质子梯度的能量由内膜上的 ATP合成酶合成ATP。
二、线粒体的跨膜转运系统
(一) 细胞溶质还原当量的跨膜转运
在胞液中代谢产生的NADH上的电子可
通过一定的穿梭系统转运进入线粒体内
膜的电子传递系统中
穿梭系统:
苹果酸-天冬氨酸穿梭 磷酸甘油穿梭
1.苹果酸穿梭
线粒体膜 胞液 NAD+ 苹果酸 基质 苹果酸 NAD
+
苹果酸脱氢酶
苹果酸脱氢酶
NADH + H+
草酰乙酸
α-酮戊二酸
NADHCoQ氧化还原酶 *简写为NADHQ还原酶,即复合物I,是一种黄
素蛋白。它的作用是催化NADH的氧化脱氢以 及Q的还原。所以它既是一种脱氢酶,也是一 种还原酶。
*NADHQ还原酶含有46个
多肽链。它的活性部分 含有辅基FMN和5-7个铁 硫簇。
辅基FMN
NADH + H+ + FMN FMNH2+ NAD+
呼吸毒物-阻断电子传递
某些物质能抑制呼吸链传递氧和电子,使氧化作用
受阻,自由能释放减少,不能合成分子ATP。 呼吸毒物:阿米妥、鱼藤酮、抗霉素A、CO、CN-等。
抑制部位
ATP ATP ATP FMN 代谢物→NADH→ Fe-S →CoQ→Cytb→Cytc1→c→aa3→O2 ↑ ↑ ↑ ↑
阿的平 阿米妥(麻醉药) 抗霉素A 鱼藤酮(杀虫药) CO CNN 3-
电子传递链与氧化磷酸化

铁-硫蛋白的Fe-S中心
仅指无机S
自学 2Fe-2S型
4Fe-4S型
参与单电子转移: Fe-S簇中只有1个 Fe被氧化或还原
蓝细菌Anabaena 7120的铁氧还蛋白 为2Fe-2S型
7
19-2
自学
泛醌 (Q/CoQ)
- 完全还原需要2H,经由 半醌基中间物形式以两步 反应完成 - 质体醌(叶绿体)和甲基萘 醌(细菌)也具有类似的在 膜结合e–传递链中携带e– 的功能 - 为脂溶性小分子,能在 线粒体内膜的脂双层中 自由扩散,从而在内膜 上其他移动性较低的e– 载体间传递还原当量 既能携带e–也能携带H+,
E’o = 0.045V
E’o = -0.32V (E’o = 0.031V) E’o = 0.816V ⊿E’o = 1.14V ∆G’o≈-220 kJ/mol 16 (cf. p335)
总矢量反应式(NADH型)
NADH + 11HN+ + ½O2 NAD+ + 10HP+ + H2O
1916
- 只添加ADP和Pi时, 呼吸(O2耗)和ATP 合成都很小
- 添加e–供体如琥珀酸 则立即显著增加
- 加入氰化物后又随即 被抑制
干扰ATP合酶使其合成受阻 H+不能返回基质 H+梯度加 大导致H+泵停转 e–流停止
30
G21.3 1
解偶联剂 (uncoupler)
使e–传递和ATP 合成相互分离
Dinitrophenol
2,4-二硝基苯酚 (DNP)
- 疏水性小分子(弱酸)
- 具有可解离H+ - 不影响e–传递和H+泵
【清华】18电子传递和氧化磷酸化习题与答案

18电子传递和氧化磷酸化习题与答案习题1.计算以下各氧化还原反应的标准还原电位和标准自由能变化:(a)乙醛+NADH +H+→乙醇+NAD+(其中NAD+/ NADH=-0.32V, 乙醛/乙醇=-0.20)(b)CoQH2 +2细胞色素C(Fe3+) →CoQ +2细胞色素C(Fe2+)+ 2H+(其中CoQ/CoQH2=0.45,细胞色素C(Fe3+)/细胞色素C(Fe2+)=0.08)2.超声处理产生的线粒体内膜碎片,内面朝外重新闭合形成称为亚线粒体颗粒的球状膜泡。
这些颗粒能够在NADH或CoQH2这样的电子源存在时,合成ATP。
画图显示在这些颗粒中从NADH开始的电子传递、质子转运和磷酸化过程。
假定氧化磷酸化的底物过量存在,当悬浮亚线粒体颗粒的悬浮液pH上升时,ATP合成是增加还是减少?3.含有过量ADP和Pi的线粒体悬浮液的耗O2曲线如下图所示(纵坐标为氧浓度,横坐标为时间):画出(a)当t为1时加入安密妥;(b)当t为1时加入安密妥;当t达到2时加入琥珀酸;(c)当t为1时加入CN-;当t达到2时加入琥珀酸;(d)当t为1时加入寡霉素;当t达到2时加入2,4-二硝基苯酚的各个耗O2曲线。
4.任何氧化还原电对的标准还原电势都是由半电池反应确定的。
NAD+/NADH和丙酮酸/乳酸的标准还原电位分别为-0.32V和-0.19V。
(a)哪一个共轭电对有较大失去电子的倾向?(b)哪一种为较强的氧化剂?(c)求在25℃、pH7时,下列反应的标准自由能变化ΔG°′以及反应的平衡常数。
丙酮酸+NADH +H+→乳酸+NAD+5.在正常的线粒体内,电子转移速度与ATP需求紧密联系在一起的:A TP的利用率低,电子转移速度也低;ATP的利用率高,电子转移就加快。
在正常情况下,当NADH作为电子供体时,每消耗一个氧原子产生的A TP数大约为3(P/O=3)。
(a)讨论解耦联剂的浓度相对来说较低和较高时对电子转移和P/O比有什么样影响?(b)摄入解耦联剂会大量出汗和体温升高。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
两条电子传递链 两条电子传递链
三、电子传递与ATP合成
• 细胞内ATP 的合成是在ADP水平上进行的 ADP + Pi → ATP • 异养生物体内高能磷酸键的形成方式有两种: – 底物水平磷酸化 – 氧化(电子传递水平)磷酸化
(一)生物体内ATP的生成方式
1. 底物水平磷酸化(substrate level phosphorylation) : • 物质分解代谢过程中,底物分子因脱氢、脱水等作 用,能量在分子内部重排形成高能磷酸酯键,并转移 给ADP形成ATP。
3-磷酸甘油酸激酶 3-磷酸甘油酸+ATP 1,3-二磷酸甘油酸+ADP 磷酸烯醇式丙酮酸+ADP 琥珀酰CoA+GDP 丙酮酸激酶 丙酮酸+ATP
琥珀酰CoA合成酶 琥珀酸+CoA+GTP GTP+ADP→ATP+GDP
2. 氧化磷酸化 (oxidative phosphorylation) :
3+
Fe-S 2Fe
2+
CoQ-Cytc还原酶
CoQ:CytC还原酶
二聚体功能单位 单体
细胞色素蛋白 细胞色素蛋白
• 结构:这是一类以铁卟啉为辅基的蛋白。 • 功能:在生物氧化反应中,通过Fe3+ Fe2+转变而传 递电子。(血红蛋白与肌红蛋白的血红素不发生价态 变化) • 细胞色素根据其铁卟啉辅基的结构以及吸收光谱的不 同分类: a, a3, b, c, c1….. • 只有Cyt c是可溶的,其余都是膜结合蛋白
Ⓢ 表示无机硫
借铁的价态变进行电子传递 Fe3+ Fe2+
泛醌( CoQ ) 泛醌( CoQ )
泛醌(辅酶Q, CoQ, Q)是存在于线粒体内膜膜双脂层 中的脂溶性有机化合物,因广泛存在得名,由多个异戊二 烯连接形成较长的疏水侧链,能在膜脂中自由泳动。
O CH3O CH3O O CH3 (CH2CH C CH2)nH CH 3
生物化学
第9章 生物氧化
——电子传递和氧化磷酸化
一、生物氧化的概念(biological oxidation) 生物氧化:糖类、脂类和蛋白质等物质在生物体内氧化分 解生产CO2和H2O,并释放出能量的过程。也称细胞氧化、 细胞呼吸。 生物体内的生物氧化的特点:
在 37℃,近中性的水环境中,由一系列酶催化进行,其
途径迂回曲折,但有条不紊;
反应逐步释放出能量,相当一部分能量以高能磷酸酯键的 形式(如ATP)储存起来,再供给机体所需。
特点:反应温和,多步反应,逐步放能
生物氧化的一般过程
糖原 甘油三酯 蛋白质
葡萄糖
脂酸+甘油
氨基酸
乙酰CoA
TCA
CO2 2H
ADP+Pi 呼吸链
ATP H2O
生物氧化发生的场所
线粒体离体实验测得的一些底物的P/O比值
2. 自由能变化与ATP的生成部位:
• 合成1molATP时,需要提供的能量至少为ΔG0’=-30.5 kJ/mol,相当于氧化还原电位差ΔE0’=0.2 V。
-0.06
复合体I
电位变化 ( Eº′) 自由能变化
复合体III
能否生成ATP
复合体IV
区段
Gº′=-nF Eº′ ( Gº′是否大于30.5KJ)
功能:
复合体Ⅰ
(1)将电子从NADH传递给泛醌 (ubiquinone)
NADH+H+ NAD+ FMN FMNH2 还原型Fe-S 氧化型Fe-S Q QH2
NADH脱氢酶
(2)4个质子由基质转到内膜外,因此,复合物 Ⅰ是由电子转移能所驱动的质子泵。
2.复合体Ⅱ(琥珀酸-CoQ还原酶):
琥珀酸脱氢酶 + 3 (Fe-S)
• 代谢物脱下的氢原子经电子传递链传递给氧过程中释 放的能量促使ADP磷酸化生成ATP。
释放能量
形成ATP
占体内ATP合成总量的95%
(二)氧化磷酸化的偶联部位
根据P/O比值和自由能变化推测氧化磷酸化的偶联部位! 1. P/O比值: • 通过测定在氧化磷酸化过程中,氧的消耗与无机磷酸消 耗之间的比例关系,可以反映底物脱氢氧化与ATP生成 之间的比例关系。 • 每消耗1mol O2所生成的ATP的mol数称为P/O比值。
线粒体基质:含有丙酮酸脱
氢酶复合物和柠檬酸循环途 径、脂肪酸 - 氧化途径、氨 基酸氧化途径等物质、能量 氧化途径。
二、生产ATP的氧化体系——呼吸链
代谢脱下的氢和电子通过多种酶和辅酶所催化的氧化还原 反应逐步传递,最终与分子氧为电子传递链或呼吸 链。 递氢体:呼吸链中参与传递H的酶和辅酶 递电子体:呼吸链中参与传递电子的酶和辅酶 在真核生物细胞内,呼吸链的酶和辅酶位于线粒体内膜 上;原核生物中,位于细胞膜上。
n=6-10
n=10:哺乳动物 n=6-8:非哺乳动物
氧化还原反应时可在醌型与氢醌型之间相互转变,是 电子传递链中唯一的非蛋白电子载体。
(氧化型,Q)
(还原型, QH2 )
CoQ 在 电 子 传 递 链中处于中心 地位
CoQ 不仅接受 NADH 脱氢酶和琥
珀酸脱氢酶的H,还接受脂酰CoA 脱氢酶等其他脱氢酶脱下的H,在 电子传递链中处于中心地位。
化学渗透假说的基本要点 化学渗透假说的基本要点
• 该学说认为氧化呼吸链存在于线粒体内膜上,当进行电 子传递时,H+通过质子泵的作用被排到线粒体内膜外侧 (膜间腔),从而在内膜两侧形成跨膜的pH梯度和跨膜 电位梯度(二者共同构成电化学梯度,即质子动力势, Proton-motive force )。 • 当质子顺浓度梯度回流时,这种形式的“势能”( H+梯度 渗透能)可以被位于线粒体内膜上的ATP合酶利用,用 于合成ATP。
实验证据
完整的线粒体内膜是氧化磷酸化必须的 线粒体内膜对H+等离子具不通透性 电子传递时H+由内向外泵出 在ATP形成时, H+由外向内流动 解偶联剂解除H+不通透性,则ATP合成解除
化学渗透假说详细示意图
胞液侧 +
H+ H+ Cyt c H+
+ + + + + Q
1.复合体Ⅰ(NADH-泛醌还原酶)
NADH脱氢酶 + 4 (Fe-S) NADH→ FMN; Fe-SN-1; Fe-SN-2; Fe-SN-3; Fe-SN-4 →CoQ
NAD+(NADP+)和NADH(NADPH)相互转变 H H
氧化还原反应时变化发生在五价氮和三价氮之间。
FMN结构中含核黄素,发挥功能的部位是异咯嗪 环,氧化还原反应时不稳定中间产物是FMN• 。
现在普遍认为呼吸链递氢和递电子所产生的能量并不完全
用于ATP的生成: 1 FADH2只生成1.5 ATP 1 NADH•H+只产生2.5 ATP。
(三)氧化磷酸化的偶联机制
化学渗透假说(chemiosmotic hypothesis) : 目前公认的氧化磷酸化的偶联机制是 1961年由Peter Mitchell提出的化学渗 透学说。
4 4
CuB+ CuB2+
细胞色素氧化酶(复合物 IV)
Heme a3 and CuB form a binuclear Fe-Cu center
The binuclear center of CuA. Cu+1Cu+1——Cu+1.5Cu+1.5
(二)呼吸链组分的排列顺序
• 通过四个方面的实验可确定呼吸链各组分的排列顺序: ① 标准氧化还原电位 ② 拆开和重组 ③ 特异抑制剂阻断 ④ 还原状态呼吸链缓慢给氧 (根据电子传递体氧化还原态时的吸收光谱变化进行检 测)
铁硫蛋白 铁硫蛋白 • 铁硫蛋白(Fe-S)共有9种同 工蛋白;分子中含有由半 胱氨酸残基硫原子及无机 硫原子与铁离子形成铁硫 中心(铁硫簇),一次可 传递一个电子至CoQ。
铁硫中心的结构 铁硫中心的结构
S
无机硫
S
半胱氨酸硫
铁硫蛋白中辅基铁硫簇 (Fe-S)含有等量铁原子 和硫原子,其中铁原子可进行Fe2+ Fe3++e 反应传 递电子。
4.复合体Ⅳ(细胞色素c氧化酶):
Cyt a + Cyt a3 + Cu 呼吸链的最后一 步 , 把 cyt c 的 电 子转移给O2还原生 成H2O
还原型Cyt c → CuA→a→a3→CuB → O2
复合物中除了含有铁卟啉外,还含有2个铜原子(CuA, CuB)。Cyt a与CuA相配合,cyt a3与CuB相配合,当 电子传递时,细胞色素的 Fe3+ 和 Fe2+ 间循环,同时 Cu2+ 和 Cu+间循环,将电子从cyt c直接传递给O2。
1948年,Eugene Kennedy和Albert Lehninger发现, 线粒体(内膜)是真核生物氧化磷酸化的场所,开始 了生物能传导的新世代。
Albert Lehninger
线粒体结构特点
外膜:小分子和离子可自由
透过
内膜:大多数小分子及离子 不能自由透过(包括H+)
内膜上含有呼吸链和 ATP 合 酶。
呼吸链中各种氧化还原对的标准氧化还原电位
氧化还原对
Eº' (V) -0.32 -0.30 -0.06 0.04(或0.10) 0.07 0.22 0.25 0.29 0.55 0.82
e EO’(大)
NAD+/NADH+H+ FMN/ FMNH2 FAD/ FADH2 Cyt b Fe3+/Fe2+ Q10/Q10H2 Cyt c1 Fe3+/ Fe2+ Cyt c Fe3+/Fe2+ Cyt a Fe3+ / Fe2+ Cyt a3 Fe3+ / Fe2+ 1/2 O2/ H2O
