烯烃的氧化与还原
烯烃臭氧化还原水解反应机理

烯烃臭氧化还原水解反应机理烯烃臭氧化还原水解反应机理一、引言烯烃是一类具有双键结构的碳氢化合物,其在工业上具有广泛的应用。
然而,由于烯烃易于发生自由基反应而导致环境污染和危害人体健康。
因此,对于研究烯烃的降解机理具有重要的意义。
本文将介绍烯烃臭氧化还原水解反应机理。
二、臭氧化反应1. 臭氧分子与双键结构发生加成反应臭氧分子(O3)与双键结构发生加成反应,生成一个环氧化合物。
例如,乙烯(C2H4)与臭氧分子发生加成反应后生成环氧乙烷(C2H4O)。
2. 环氧化合物发生裂解反应环氧化合物在存在水分子或酸催化剂的条件下可以发生裂解反应,生成醇和醛等物质。
例如,环氧乙烷在存在水分子或酸催化剂的条件下可以裂解为乙醇和乙醛。
三、还原反应1. 环氧化合物发生还原反应环氧化合物可以被还原为相应的醇。
例如,环氧乙烷可以被还原为乙醇。
2. 还原反应的影响因素还原反应的影响因素包括还原剂种类、反应温度、反应时间等。
常用的还原剂包括亚硫酸钠、亚硫酸氢钠、二氧化硫等。
四、水解反应1. 环氧化合物发生水解反应环氧化合物可以在存在水分子或碱催化剂的条件下发生水解反应,生成相应的醇和羟基化合物。
例如,环氧乙烷在存在水分子或碱催化剂的条件下可以水解为乙醇和乙二醇。
2. 水解反应的影响因素水解反应的影响因素包括催化剂种类、反应温度、反应时间等。
常用的碱催化剂包括氢氧化钠、氢氧化钾等。
五、结论烯烃臭氧化还原水解反应机理是一个复杂而重要的过程,对于研究烯烃降解机理具有重要的意义。
臭氧化反应、还原反应和水解反应是烯烃降解过程中的重要环节,其影响因素包括催化剂种类、反应温度、反应时间等。
通过对烯烃降解机理的深入研究,可以为环境保护和人类健康提供有力的支持。
乙烯的氧化反应方程式

乙烯的氧化反应方程式
乙烯(C2H4)是一种常见的烯烃,也被称为乙烯烃。
乙烯可以通过氧化反应转化为乙烯醛(乙醛),氧化反应的化学方程式如下所示:C2H4 + O2 → C2H4O
在这个方程式中,乙烯(C2H4)与氧气(O2)发生氧化反应,产生乙烯醛(C2H4O)。
乙烯氧化反应是一种重要的化学反应,也是工业生产中的一个重要步骤。
乙烯醛是一种有机化合物,常用于合成其他有机化合物,如乙醇和丙烯醛等。
乙烯氧化反应通常在高温和高压下进行,以促进反应的进行。
乙烯氧化反应是一个氧化还原反应。
在反应中,乙烯失去氢原子,氧气得到氢原子,形成乙烯醛。
氧气在反应中起到氧化剂的作用,促进乙烯的氧化反应。
乙烯氧化反应具有重要的应用价值。
乙烯醛是一种重要的有机合成中间体,可以用于合成各种有机化合物,如聚乙烯醛和聚醋酸乙烯酯等。
乙烯氧化反应也可以用于生产乙醛和其他有机化合物,广泛应用于化工、制药和农药等领域。
总的来说,乙烯的氧化反应是一种重要的化学反应,可以产生有机合成中间体乙烯醛,具有广泛的应用价值。
在工业生产中,乙烯氧
化反应是一个重要的步骤,可以用于合成各种有机化合物,推动化工产业的发展。
烯烃的反应机理

烯烃的反应机理烯烃是一类具有碳碳双键的有机化合物,其具有较高的反应活性和广泛的应用价值。
烯烃的反应机理是指烯烃分子在不同条件下发生反应时所经历的分子结构变化过程。
本文将以烯烃的反应机理为标题,介绍烯烃在不同反应中的机理及其应用。
1. 烯烃的加成反应机理烯烃的加成反应是指烯烃分子中的碳碳双键与其他分子中的原子或基团发生共价键形成新的化学键。
这种反应通常需要催化剂的存在,催化剂能够加速反应速率。
加成反应通常分为电子亲和性和立体选择性两个方面。
电子亲和性是指反应中电子密度较大的部分与反应物中具有电子亲和性的原子或基团发生作用,立体选择性是指反应发生后立体构型发生改变。
2. 烯烃的氧化反应机理烯烃的氧化反应是指烯烃分子与氧气或氧化剂发生反应,生成含有氧原子的产物。
这种反应可以分为完全氧化和部分氧化两种类型。
完全氧化是指烯烃分子的碳碳双键和氧气中的氧原子全部发生反应,生成二氧化碳和水等产物。
部分氧化是指烯烃分子中的部分碳碳双键与氧气或氧化剂反应,生成醇、酮等含氧化合物。
3. 烯烃的聚合反应机理烯烃的聚合反应是指烯烃分子中的多个碳碳双键发生共价键形成长链烃分子的过程。
这种反应需要催化剂的存在,催化剂能够引发烯烃分子中的碳碳双键发生开环反应,并与其他烯烃分子发生共价键形成长链烃分子。
聚合反应是一种重要的反应类型,广泛应用于塑料、橡胶、纤维等材料的合成。
4. 烯烃的裂解反应机理烯烃的裂解反应是指烯烃分子中的碳碳双键断裂,生成较小分子的过程。
这种反应通常需要高温和催化剂的存在,高温能够提供足够的能量使碳碳双键断裂,催化剂能够降低反应的活化能,加速反应速率。
裂解反应主要用于烯烃的炼制和烯烃衍生物的合成。
5. 烯烃的重排反应机理烯烃的重排反应是指烯烃分子中的碳碳双键位置发生变化的过程。
这种反应通常发生在高温和催化剂的存在下,高温能够提供足够的能量使烯烃分子中的碳碳双键断裂和形成,催化剂能够降低反应的活化能,加速反应速率。
烯烃的氧化反应

精选可编辑ppt
OH
26
6. 脱氢反应
• 钌络合物催化剂RuCl2(PPh3)3和叔胺氧化物可以 使伯醇或仲醇脱氢分别生成醛或酮。
精选可编辑ppt
27
N-甲基吗琳-N-氧化物是钌的再次氧化剂(reoxidation)。
精选可编辑ppt
28
• 氯化钯也能够把仲醇氧化成酮,O2是再次氧化剂。
可能的脱氢机理
H DO C H
H2C Pd (A)
H DO CH
Pd CH2
(B)
OD CH Pd CH3 (C)
O CH +Pd0+H+ CH3
DO CH CH2
CH2DCHO
➢ 以重水为溶剂时,产物中没有检出氘代物,否认了由 A还原消除生成乙烯醇再转化成乙醛的路线。
精选可编辑ppt
9
2. 其它烯烃的氧化反应
O CC + R C O O H
精选可编辑ppt
15
➢ 过渡金属络合物催化下,烷基过氧化氢ROOH 选择性氧化烯烃
催化剂:Mo、V、W、Ti等高氧化态的过渡金属络合物
精选可编辑ppt
16
• 环氧化反应的速度随烯烃取代基的增多而增大
利用VO(acac)2和ButOOH进行环氧化反应时, α-位有双键 的烯烃反应速度明显加快。
这是化学计量反应,早在1894年F.C.Phillips就作了报道,并将 此反应应用到Pd的分析上。
精选可编辑ppt
2
2). Pd(0)重新氧化成Pd(Ⅱ)
❖ Smidt发现,在反应中加入CuCl2可以将Pd(0)重新氧化生成 Pd(Ⅱ),从而使一个化学计量反应变为催化反应。
P d ( 0 )+ 2 C u C l2+ 2 C l- P d C l4 2 -+ 2 C u C l
有机合成中的氧化与还原

特点: 顺式加成 生成顺式连二醇。 顺式加成, 特点:1.顺式加成,生成顺式连二醇。 2.协同反应 协同反应
协同反应
协同反应是指起反应的分子- 协同反应是指起反应的分子-单分子或双分子 发生化学键的变化, -发生化学键的变化,反应过程中只有键变化 的过渡态,一步发生成键和断键,没有自由基 的过渡态,一步发生成键和断键, 或离子等活性中间体产生。 或离子等活性中间体产生。简单说协同反应是 一步反应,可在光和热的作用下发生。 一步反应,可在光和热的作用下发生。协同反 应往往有一个环状过渡态, 应往往有一个环状过渡态,如双烯合成反应经 过一个六元环过渡态,不存在中间步骤。 过一个六元环过渡态,不存在中间步骤。 注意:协同反应不是周环反应!! 注意:协同反应不是周环反应!! 简单说协同反应就是在反应过程中, 简单说协同反应就是在反应过程中,没有中间 一步完成的反应。 体,一步完成的反应。
RCH2OH RCOOH RCH(OH)R’ RCOR’
CH3COCH3+CO2+H20
3,CrO3/稀硫酸和 , 稀硫酸和CrO3/吡啶 氧化醇成醛或酮 吡啶----氧化醇成醛或酮 稀硫酸和 吡啶 上述两种试剂分别称为Tones试剂和 试剂和Sarrret 上述两种试剂分别称为 试剂和 试剂,将重铬酸钾的氧化活性降低, 试剂,将重铬酸钾的氧化活性降低,仅将醇氧 化成醛和酮
1.Tollens试剂,Fehling试剂,Benedit试剂的氧化 试剂, 试剂, 试剂 试剂 试剂的氧化
①应用范围 Tollens试剂([Ag(NH3)2]+): 试剂( 试剂 ( 醛(-CHO)
Fehling试剂(CuSO4,NaOH,酒石酸钾钠): 脂肪醛(RCHO) 试剂( 试剂 ,酒石酸钾钠): 脂肪醛( ) Benedit试剂( CuSO4,NaOH,柠檬酸钠): 除甲醛外的脂肪醛(RCHO) 试剂( 试剂 ,柠檬酸钠): 除甲醛外的脂肪醛( ) ②作用 RCHO RCHO
02-6.3 烯烃的氧化与还原

环状锇酸酯中间体
顺-1,2-二甲基-1,2-环戊二醇
1,4-bis(9-O-dihydroquinidinyl)phthalazine
氢化奎尼定1,4-(2,3-二氮杂萘)二醚
先环氧化,再 水解开环。
烯烃的氧化:羟氨化反应
烯烃的氧化:臭氧化反应
电子云密度 高,位阻小 的 C=C 键, 有利于臭氧 化反应的发 生。
烯烃的还原与氧化
主讲人 唐 翔 鹰 华中科技大学化学与化工学院
主讲内容
• 烯烃的还原反应 • 烯烃的氧化反应
烯烃的还原反应类型
烯烃加氢转变成烷烃的过程,称为烯烃的还原反应。还原反应类型:
催化加氢 二亚胺还原 硼氢化还原
烯烃的还原:催化加氢
含烯键的化合物在催化剂存在下可以与氢气发生加成反应,反应多数情况下以 顺式加成为主:
烯烃的还原:硼氢化还原
还原反应: 反应机理:
反应实例:
-蒎烯
烯烃的氧化反应
环氧化反应 双羟化反应 羟氨化反应 臭氧化反应
烯烃的氧化:环氧化反应
过氧酸 的氧化
环庚烯
间氯过氧苯甲酸
1,2-环氧环庚烷 间氯苯甲酸
工业上环氧乙烷制备
Sharpless 不对ቤተ መጻሕፍቲ ባይዱ环氧化反应
烯烃的氧化:双羟化反应
1,2-二甲基环戊烯
均相催化: 催化剂可以溶于有机溶剂的催化反应,通常是一些d8副族金属的配合物。 一般在常温常压下进行。
烯烃的还原:二亚胺还原
二亚胺是一类选择性很好的还原剂,能有效地还原烯键、炔键等非极性 的不饱和键,收率较高。而极性不饱和键如C=N,C≡N,NO2,S=O等则不受 影响。例如:
二亚胺的产生: 环状过渡态 反应过程
烯烃氧化反应燃烧通式

烯烃氧化反应燃烧通式
烯烃氧化反应是指烯烃与氧气发生反应产生的化学反应。
烯烃
是一类碳氢化合物,其分子中含有碳-碳双键。
烯烃氧化反应的通式
可以用一般化学方程式表示为,CnH2n + (3n+1/2)O2 → nCO2 +
nH2O。
在这个方程中,CnH2n代表烯烃分子,(3n+1/2)O2代表氧气
分子,nCO2代表生成的二氧化碳分子,nH2O代表生成的水分子。
烯烃氧化反应是一种燃烧反应,其过程中烯烃分子和氧气分子
发生燃烧,生成二氧化碳和水。
燃烧是一种氧化反应,通过释放能
量将有机物质氧化为二氧化碳和水。
燃烧反应通常伴随着放热现象,因为燃烧反应释放了化学键的能量。
需要注意的是,烯烃氧化反应的实际反应过程可能会受到反应
条件、催化剂等因素的影响,因此在实际应用中可能会有一定的变化。
但是上述通式可以作为烯烃氧化反应的一个基本表示,帮助我
们理解烯烃氧化反应的基本原理和特点。
总的来说,烯烃氧化反应的通式可以用简单的化学方程式表示,但在实际应用中可能会有一些变化,需要根据具体的反应条件和催
化剂来进行具体分析。
希望这个回答能够全面地解答你的问题。
烯烃的合成与反应

烯烃的合成与反应烯烃是一类具有双键结构的碳氢化合物,具有很高的化学反应性和广泛的应用领域。
烯烃的合成与反应包括了多种化学反应过程,本文将对烯烃的合成方法以及常见的反应类型进行介绍。
一、烯烃的合成方法1. 通过氢化反应得到烯烃:氢化反应是指将芳环化合物或者炔烃通过加氢反应转化为烯烃的方法。
通常使用催化剂,如Pd/C或Pd-BaSO4等来促进反应。
例如苯经过氢化反应可以得到环己烯。
2. 利用脱水反应合成烯烃:脱水反应是指通过脱去水分子生成双键结构的反应过程。
常见的脱水反应有酸催化脱水和醇脱水等。
例如,乙醇经过酸催化脱水可以得到乙烯。
3. 烯烃的氧化反应合成:烯烃可以通过氧化反应合成较复杂的有机化合物。
常用的氧化剂有酸性过氧化物、过硫酸盐等。
例如,乙烯经过环氧化反应可以得到环氧乙烷。
二、烯烃的反应类型1. 加成反应:加成反应是指在烯烃的双键上加入其他原子或者官能团的反应。
常见的加成反应有卤素加成、质子加成和酸催化加成等。
例如,乙烯与氢氯酸反应可以得到氯乙烷。
2. 消除反应:消除反应是指烯烃中的双键发生断裂并与其他原子或官能团结合,生成新化合物的反应。
常见的消除反应有氢氧化消除和醇酸消除等。
例如,环己烯经过氢氧化消除可以得到环己酮。
3. 聚合反应:聚合反应是指将烯烃分子中的双键进行开裂,并与其他烯烃形成共价键。
聚合反应是烯烃广泛应用于聚合物工业的重要反应之一。
例如,乙烯经过聚合反应可以得到聚乙烯。
4. 氧化反应:氧化反应是指烯烃分子中的双键与氧气发生反应,生成含有氧原子的化合物。
常见的氧化反应有醇的氧化和酮的氧化等。
例如,乙烯经过醇的氧化反应可以得到乙醛。
5. 还原反应:还原反应是指将烯烃分子中的双键还原为单键的反应。
常见的还原剂有氢气、氢化铝锂等。
例如,乙烯经过氢化反应可以得到乙烷。
总结:烯烃具有丰富的化学反应性和广泛的应用领域,其合成方法包括了通过氢化反应、脱水反应以及氧化反应等多种方式。
在烯烃的反应类型中,包括了加成反应、消除反应、聚合反应、氧化反应以及还原反应等。
烯烃被高锰酸钾氧化的规律

烯烃被高锰酸钾氧化的规律
烯烃是一种具有高反应活性的有机化合物,其分子中含有至少一个双键。
高锰酸钾是一种强氧化剂,可将烯烃氧化成相应的酮或羧酸。
下
面将介绍烯烃被高锰酸钾氧化的规律。
一、反应机理
在高锰酸钾的作用下,烯烃中的双键发生氧化加成反应,生成底物中
含有的双键与高锰酸钾的氧原子结合,形成邻二醇或环氧化物。
随后,产生的邻二醇或环氧化物进一步氧化,生成酮或羧酸。
二、影响反应的因素
1.底物结构:烯烃双键位置、取代基及大小对反应有影响。
例如,烯烃中的双键位于末端的氧化能力弱于内部双键。
另外,底物分子中的取
代基对反应速率和产物结构也有影响。
2.高锰酸钾浓度:高锰酸钾浓度越高,反应速率越快。
3.反应温度:反应温度越高,反应速率越快,但同时也会导致反应产物的杂质生成增加。
三、产物类型
烯烃被高锰酸钾氧化后,产物的类型主要包括酮和羧酸。
产物的取决于底物结构以及反应条件。
当烯烃分子中含有相应的官能团时,也会生成相应的产物,如含有羟基的烯烃会生成含有羟基的酮或羧酸。
四、应用
烯烃被高锰酸钾氧化的反应可用于有机合成中的氧化反应。
烯烃作为一种常见的有机底物,在有机化学的合成中得到了广泛应用。
因此,烯烃被高锰酸钾氧化的反应也成为了一种常用的有机合成反应。
该反应可以将底物转化为酮或羧酸,为有机化学研究提供了重要的有机合成手段。
ch3co3h和烯烃反应机理

ch3co3h和烯烃反应机理烯烃是一类具有双键结构的碳氢化合物,它们具有较高的反应活性,容易与其他化合物发生反应。
而ch3co3h是一种强氧化剂,可以引发烯烃的氧化反应。
本文将介绍ch3co3h与烯烃反应的机理。
在ch3co3h与烯烃反应中,首先发生的是烯烃的亲电加成反应。
烯烃中的双键上的π电子云较为密集,具有较高的电子密度。
而ch3co3h具有正电荷的氧原子,是一种强亲电试剂。
当ch3co3h与烯烃接触时,氧原子的正电荷会与烯烃的π电子云发生作用,形成一个碳正离子和一个醇酸根阴离子。
这个过程是一个化学键的断裂和形成的过程,生成的产物是一个新的化合物。
接下来的反应步骤是醇酸根阴离子的亲核取代反应。
由于醇酸根阴离子具有负电荷,是一种强亲核试剂。
它会与碳正离子发生亲核取代反应,将自己的负电荷转移到碳上,同时断裂碳上的化学键。
这个过程中,醇酸根阴离子会取代掉碳上的一个基团,生成一个新的化合物。
在亲核取代反应中,醇酸根阴离子可以选择与碳上的各个基团发生反应,形成不同的产物。
这取决于烯烃的结构和ch3co3h的反应条件。
例如,当烯烃是一个顺式烯烃时,醇酸根阴离子会与烯烃的两个碳原子中的一个发生反应,生成一个新的化合物。
而当烯烃是一个反式烯烃时,醇酸根阴离子会与烯烃的两个碳原子都发生反应,生成两个新的化合物。
除了亲电加成和亲核取代反应,ch3co3h与烯烃还可以发生其他类型的反应。
例如,它们可以发生氧化反应,将烯烃中的碳原子上的氢原子氧化为羟基。
这个反应是一个氧化还原反应,需要有合适的条件和催化剂。
ch3co3h与烯烃反应的机理是一个复杂的过程,包括亲电加成、亲核取代和氧化等多种反应类型。
这些反应在有机合成中具有重要的应用价值,可以用来构建复杂的有机分子结构。
在实际应用中,研究人员可以根据不同的需要选择合适的反应条件和催化剂,来实现特定的反应目标。
烯烃被氧气氧化机理

烯烃被氧气氧化机理
烯烃是一类具有双键结构的碳氢化合物,具有很强的化学反应性。
当烯烃接触到氧气时,会发生氧化反应,产生一系列的化学变化。
烯烃被氧气氧化的机理是通过自由基反应进行的。
首先,烯烃会与氧气发生加成反应,生成一个氧化物自由基。
这个自由基具有不稳定性,会进一步与其他烯烃分子反应。
这个反应会在氧化物自由基中心形成一个新的碳氧化物自由基,同时另一个烯烃分子将被转化为亚醇自由基。
这个亚醇自由基会进一步与其他氧化物自由基反应,生成更多的碳氧化物自由基。
在这个过程中,会产生很多自由基,它们会不断地与其他分子发生反应,形成新的自由基。
这个连锁反应会一直持续下去,直到所有的烯烃都被氧化为止。
氧化反应是一种十分重要的化学反应,它不仅可以用于制备有机化合物,还可以用于清洁工业废气,并帮助改善环境污染问题。
了解烯烃被氧气氧化的机理,对于开发新的有机化合物具有重要的意义。
- 1 -。
有机中的氧化反应

有机中的氧化反应有机中的氧化反应是在化学反应中非常重要和常见的一种类型。
许多有机分子在与氧气接触时,会发生氧化反应,从而产生新的化合物。
本文将介绍几种常见的有机氧化反应及其应用,以及如何进行实验控制。
1. 醇的氧化反应醇在接触到氧气时,可以发生氧化反应形成醛和酮。
这种反应被称为醇的氧化反应。
其中,一级醇可以被氧化成为醛,二级醇可以被氧化成为酮,而三级醇则不易发生氧化反应。
这种反应在有机合成中有着广泛的应用。
以二级醇为例,环己醇可以被氧化成为环己酮。
而环己酮又可以被进一步还原成为环己醇,从而实现化学反应平衡的控制。
2. 烯烃的氧化反应烯烃是另一种常见的有机分子,与氧气接触时可以发生氧化反应。
这种反应被称为烯烃的氧化反应。
其中,烯烃分子中的双键可以被氧气中的气体或金属氧化剂氧化,从而形成双键末端的羟基或羰基。
这种反应通常由过氧化氢或过氧化叔丁酮等强氧化剂催化。
这种反应在有机合成、高分子材料和生物化学等多个领域都有广泛的应用。
3. 阳离子的氧化反应阳离子是另一种重要的有机中间体,可以通过氧化反应来产生更复杂的化合物。
这种反应被称为阳离子的氧化反应。
其中,不饱和的烷基、芳基和烯基等结构会发生氧化反应,从而形成带有离子性的阳离子。
阳离子在许多有机合成中都有着重要的应用。
例如,碳正离子的中间体在芳香化反应中被广泛应用。
而芳基的氧化反应则可以生成类似苯甲醛和苯甲酸的化合物。
针对这些有机氧化反应,进行实验控制非常重要。
在实验中,需要精确控制反应条件,以获得最佳的反应结果和产物收率。
同时,需要注意一些步骤,如选择适当的催化剂、加入适量的助剂、控制反应温度等等。
总之,有机氧化反应是化学反应中一种非常重要的类型,有着广泛的应用。
了解这些反应的机制和实验控制是有机化学研究领域中不可或缺的一部分。
《脂肪烃的性质及应用》烯烃氧化与还原

《脂肪烃的性质及应用》烯烃氧化与还原《脂肪烃的性质及应用——烯烃氧化与还原》在化学的世界里,脂肪烃是一类重要的有机化合物,而烯烃作为脂肪烃中的一个重要分支,其氧化与还原反应具有独特的性质和广泛的应用。
烯烃是含有碳碳双键的烃类化合物,由于双键的存在,使得烯烃具有较高的反应活性。
首先,咱们来聊聊烯烃的氧化反应。
常见的烯烃氧化反应之一是高锰酸钾氧化。
在酸性条件下,高锰酸钾可以将烯烃氧化,根据烯烃结构的不同,会产生不同的氧化产物。
如果双键两端的碳原子上都连有氢原子,那么氧化后双键会断裂,生成羧酸;要是双键一端的碳原子上有氢原子,另一端没有,氧化后则生成酮。
这一反应在化学分析中常用于确定烯烃的结构。
另一种重要的氧化反应是臭氧氧化。
烯烃与臭氧反应,会先形成臭氧化物,然后在还原剂的作用下分解,得到醛、酮等产物。
这个反应在有机合成中可以用来制备一些特定的醛和酮。
烯烃的氧化反应在工业生产中也有着重要的应用。
比如说,在制备环氧乙烷的过程中,乙烯在银催化剂的作用下被氧气氧化,生成环氧乙烷。
环氧乙烷是一种重要的有机化工原料,广泛用于生产乙二醇、表面活性剂等产品。
说完了氧化,咱们再来说说烯烃的还原反应。
烯烃的还原最常见的方法就是催化加氢。
在催化剂的作用下,烯烃与氢气发生加成反应,双键被打开,生成相应的烷烃。
这是一个在工业上广泛应用的反应,例如通过催化加氢将植物油中的不饱和脂肪酸转化为饱和脂肪酸,从而提高油脂的稳定性和保存期限。
还有一种还原方法是使用金属氢化物,比如氢化铝锂(LiAlH₄)和硼氢化钠(NaBH₄)。
这些试剂能够选择性地还原烯烃中的双键,而对其他官能团的影响较小。
烯烃的氧化与还原反应不仅仅在化学合成和工业生产中发挥着重要作用,在我们的日常生活中也有着各种各样的应用。
比如在化妆品行业,通过对某些烯烃化合物的氧化或还原处理,可以得到具有特定功能和性质的成分,用于护肤、美容等产品。
在医药领域,利用烯烃的反应来合成药物分子或者对药物进行修饰,以改善其药效和安全性。
精细有机合成—氧化反应

(2) OsO4氧化 将烯烃加至Os04的醚溶液中,立即生成环状饿酸酯沉淀,再用亚 硫酸钠水溶液水解.得顺式二醇: 反应被三级胺,特别是被吡啶所加速,因而吡啶经常加入反应介质中。
(3) 合成一羟基化合物 将烯烃双键实现区域选择和立体选择一羟基化,可以通过硼氢化,然后将
所生成的烃基硼烷与碱性过氧化氢进行氧化,可以高产率得到一羟基化产物。硼 烷首先与烯烃进行硼氢化反应加到双键位阻小的一侧,在随后的氧化反应过程中, 保持构型不变。例如:
在苯基环己烷类液晶的重要中间体4—正烷基环己基苯甲酸酯的合成中, 便利用了卤仿反应。
3.Boeyr-Villiger氧化 拜耶尔—维立格(Baeyr-villiger)氧化。酮虽然对许多氧化剂是稳定的,但它
可以在酸催化下被过氧酸顺利氧化成酯或类酯。这个反应首先发生了过氧酸与酮 羰基的加成,然后再进行烃基的迁移,生成酯。
不饱和酮经常发生Baeyr-Villiger反应,优先于双键的氧化反应,因而 形成不饱和内酯。优先迁移的基团是氢。 Baeyr-Villiger氧化反应在合成 中有重要应用,它为由酮制备酯 提供了一种较方便的方法。
4、SeO2氧化 SeO2是一种选择性氧化剂,可直接广泛地用于氧化酮和醛至α-二羰基化
1975年Corey将CrO3溶于盐酸中,然后加入吡啶,得到的固体物 C5H5NHCrO3C1,简称为PCC(Pyridinium Chloro Chromate),这种 氧化剂的优点在于不氧化分子中的烯键.产率也较高
②活性二氧化锰氧化 活性MnO2对烯键和炔键无作用,因而广泛用于类胡萝卜素和维生素A中
氧化,发生碳碳键的断裂。
Pb(OAc)4不溶于水,因此它进行的氧化反应应在有机介质中(如冰乙酸) 中进行。 HIO4溶于水,可在水溶液中进行氧化反应。这两种氧化剂都可使氧 化停止在醛的阶段,产率较高。例如:
烯醇 氧化还原电位

烯醇氧化还原电位
烯醇指的是含有烯烃基的醇化合物。
烯醇在氧化还原反应中,可以发生氧化和还原反应。
烯醇的氧化反应通常会使烯烃部分发生氧化,生成羰基化合物。
烯醇的氧化还原电位一般较高,通常在正凯库仑(V)以上,
因此容易发生氧化反应。
其中,烯醇的氧化还原电位与它的分子结构息息相关,主要取决于烯烃基的位置和共轭体系的性质。
烯醇的还原反应通常会将烯烃部分还原为饱和烃。
烯醇的还原反应通常需要较低的氧化还原电位,一般在正凯库仑(V)以下。
还原剂常用的有金属氢化物、催化剂等。
总的来说,烯醇的氧化还原电位较高,容易发生氧化反应,而需要较低氧化还原电位才能发生还原反应。
烯烃的氧化
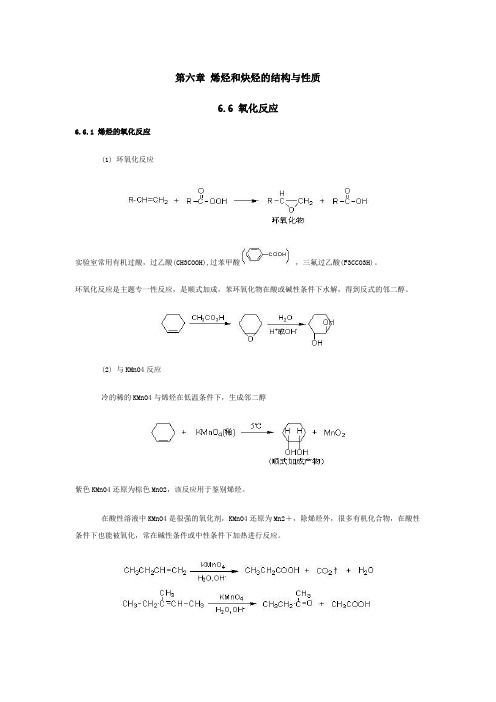
第六章烯烃和炔烃的结构与性质
6.6 氧化反应
6.6.1 烯烃的氧化反应
(1) 环氧化反应
实验室常用有机过酸,过乙酸(CH3COOH),过苯甲酸,三氟过乙酸(F3CCO3H)。
环氧化反应是主题专一性反应,是顺式加成,苯环氧化物在酸或碱性条件下水解,得到反式的邻二醇。
(2) 与KMnO4反应
冷的稀的KMnO4与烯烃在低温条件下,生成邻二醇
紫色KMnO4还原为棕色MnO2,该反应用于鉴别烯烃。
在酸性溶液中KMnO4是很强的氧化剂,KMnO4还原为Mn2+,除烯烃外,很多有机化合物,在酸性条件下也能被氧化,常在碱性条件或中性条件下加热进行反应。
从上面氧化产物可以看出=CH2被氧化为CO2,R-CH=被氧化为-COOH,而被氧化为
,因此利用反应产物推测原烯烃的结构。
(3) 与OsO4反应
反应的产率高,几乎定量进行,但OsO4价格昂贵,易升华且毒性很高,可用改进方法:用H2O2和催化量的OsO4,烯烃先与OsO4反应,OsO4被还原为OsO3。
H2O2可把OsO3氧化为OsO4,如此反复进行,直到反应完成。
环内有反式双键,经顺式加成后,得到反式邻二醇。
(4) 臭氧化反应
先生成不太稳定的臭氧化物,水解可以生成醛酮和H2O2,为了防止H2O2氧化醛,常加还原剂Zn,Zn和H2O2反应生成Zn(OH)2,也可以使用二甲硫醚(CH3SCH3)。
臭氧化反应的选择性很强,从反应的鉴定,可以推断出原来烯烃的结构。
6.6.2 炔烃的氧化反应
(1) 臭氧化反应
(2) 与KMnO4反应
两种氧化反应的最终产物都是羧酸。
根据产物的结构推知原炔烃结构。
烯烃高锰酸钾褪色方程式

烯烃高锰酸钾褪色方程式烯烃高锰酸钾褪色是一种常见的化学实验现象,它可以通过以下方程式来描述:C2H4 + 2KMnO4 + 2H2O → 2MnO2 + 2KOH + 2H2O + CO2在这个方程式中,C2H4代表烯烃(乙烯),KMnO4代表高锰酸钾,MnO2代表二氧化锰,KOH代表氢氧化钾,H2O代表水,CO2代表二氧化碳。
这个方程式描述了烯烃与高锰酸钾反应后产生的产物。
在实验中,烯烃与高锰酸钾反应会发生褪色现象。
高锰酸钾是一种紫红色的化合物,但当它与烯烃反应后,溶液的颜色就会逐渐变淡,直到完全褪色为止。
这是因为烯烃与高锰酸钾反应生成的产物中含有二氧化锰,它是一种棕黑色的固体,使溶液变为棕色。
随着反应的进行,溶液中的二氧化锰越来越多,颜色也逐渐加深,直到溶液完全褪色为止。
这个实验现象可以通过化学反应的原理来解释。
在反应中,烯烃与高锰酸钾发生氧化还原反应。
高锰酸钾是一种强氧化剂,它能氧化烯烃中的双键,生成相应的醇和醛。
同时,高锰酸钾自身也被还原为二氧化锰。
二氧化锰是一种黑色的固体,它沉淀在溶液中,使溶液变为棕色。
当溶液中的二氧化锰达到一定浓度时,溶液就会完全褪色。
这个实验现象可以进一步扩展,以探讨化学反应的速率和反应机理。
在实验中,可以改变烯烃和高锰酸钾的浓度、温度和反应时间,观察褪色速度的变化。
通过这些实验条件的改变,可以研究反应速率与反应物浓度、温度和反应时间的关系,从而推测出反应的速率方程和反应机理。
烯烃高锰酸钾褪色实验也可以应用于分析化学中。
通过测量褪色速度,可以确定烯烃和高锰酸钾的浓度,或者测定其他物质的浓度。
这个实验方法可以用于分析酒精浓度、水中有机污染物的浓度等。
烯烃高锰酸钾褪色实验是一种常见的化学实验现象,通过化学反应的原理可以解释该现象。
这个实验现象可以进一步扩展,以研究反应的速率和反应机理,也可以应用于分析化学中。
通过深入研究和理解这一实验现象,可以更好地理解化学反应的基本原理和应用。
