EDTA与螯合剂
edta二钠的作用与功效

edta二钠的作用与功效EDTA二钠是一种广泛应用于工业和化学实验室的一种化学试剂,其作用和功效主要分为以下几个方面:1. 螯合剂:EDTA二钠是一种强螯合剂,可与金属离子形成稳定的络合物。
其稳定络合能力在很大程度上取决于金属离子的价态和电荷密度。
EDTA二钠可以与多种金属离子形成络合物,如钙、铁、镁、锌、铜、铅等。
由于金属离子在生物化学中起到重要的催化和凝集作用,EDTA二钠被广泛应用于工业和医学领域。
例如,EDTA二钠可用于溶解石灰石中的钙离子,用于软化水质、净化饮用水和制备实验室纯水。
2. 螯合剂:EDTA二钠可通过螯合过程中与重金属离子的络合,防止其过早沉淀和析出,从而减少对环境的污染和对健康的危害。
EDTA二钠可用于清洗废水和净化污染的土壤。
它可以与汞、铅、镉、铬等重金属形成稳定的络合物,并防止它们从土壤中渗透到地下水中。
此外,EDTA二钠还可以用于工业废水的处理,并减少金属离子的浓度。
3. 配位试剂:EDTA二钠具有较高的配位能力,可以与多种金属离子形成具有稳定结构的络合物。
这些络合物可用作分析试剂、标准物质和参比物质。
例如,EDTA二钠可以用于测定水中钙、镁、铁、锌等金属离子的含量。
通常它们会形成明亮的色彩,便于准确测量。
EDTA二钠还可以用作标准物质,用于比较和检验其他化学物质的含量。
4. 食品添加剂:EDTA二钠也可以作为食品添加剂,起到增加食品的口感和延长保质期的作用。
它可以与铁离子结合,使之失去活性,从而阻止氧化反应的发生。
这有助于防止食品腐败和变质。
它还可以防止食品中的色素失去鲜艳的颜色,从而保持食物的美观和诱人的外观。
总结起来,EDTA二钠作为一种强螯合剂具有广泛的应用。
它不仅可以用于工业和化学实验室中的分析和配位试剂,还可以用于清洗废水和净化污染土壤。
此外,EDTA二钠还可以作为食品添加剂,延长食品的保质期并改善其口感。
它在环境保护、食品工业和化学研究等领域中发挥着重要作用。
常用螯合剂

常用螯合剂螯合剂是一类能与金属离子形成稳定络合物的化合物。
螯合剂可以通过给予金属离子一个或多个配体上的电子对来形成配位键。
常用的螯合剂有以下几种。
1. 乙二胺四乙酸(EDTA)乙二胺四乙酸(EDTA)是一种多功能螯合剂,广泛用于化学分析和工业生产中。
它能与多种金属离子形成稳定的络合物,并能有效螯合和去除金属离子,起到去污和稳定作用。
EDTA还可用作破坏细胞壁、抑制酶活性等方面的实验试剂。
2. 氰化物(CN-)氰化物(CN-)是一种强碱性的螯合剂,它能与金属离子形成氰化物络合物。
氰化物络合物通常具有较高的稳定性和溶解度,在金属提取和电镀等领域有广泛应用。
然而,氰化物具有强毒性和致命性,需在使用时小心操作,避免接触和吸入。
3. 亚硝酸盐(NO2-)亚硝酸盐(NO2-)也是一种常用的螯合剂,它能与金属离子形成亚硝酸盐络合物。
亚硝酸盐络合物通常具有较高的稳定性和溶解度,广泛用于水处理、金属腐蚀抑制和环境污染治理等领域。
亚硝酸盐还可用作爆炸物和药物的原料。
4. 有机酸有机酸是一类含有羧基的有机化合物,它们可以与金属离子形成稳定的络合物。
常用的有机酸螯合剂包括乙酸、苯甲酸、柠檬酸等。
有机酸络合物在食品、化妆品和医药等领域有广泛应用,可以起到抗氧化、保存、稳定等作用。
5. 胺类化合物胺类化合物是一类含有氮原子的有机化合物,它们可以与金属离子形成稳定的络合物。
常用的胺类螯合剂包括乙二胺、三乙矿、二乙矿等。
胺类螯合剂在化学分析、金属提取和催化反应等领域有广泛应用,可以提高反应的选择性和效率。
螯合剂在化学、生物和环境科学等领域发挥着重要作用。
通过与金属离子形成稳定络合物,螯合剂可以改变金属的性质和行为,扩展其应用范围。
不同的螯合剂适用于不同的金属离子和应用领域,选择合适的螯合剂可以提高实验和生产的效果。
然而,在使用螯合剂时,需要注意其毒性和环境影响,并遵循安全操作规程,以确保实验和生产的安全性和可持续性。
EDTA与螯合剂

3.与金属离子形成配合物的稳定性 必须小于EDTA与金属离子形成螯合 物的稳定性。
常用的指示剂有铬黑T,钙指示 剂,二甲酚橙,PAN等。现以铬黑T 为例,说明金属指示剂的变色原理。 铬黑T为弱酸性偶氮染料,能随溶液 pH值变化而显示不同的颜色。如用 符号NaH2ln表示铬黑T。在溶液中 有下列平衡:
二、氨羧螯合剂及氨羧 螯合滴定
(一)氨羧螯合剂的结构和特点 氨羧螯合剂中最重要同时应用最
广的是乙二氨四乙酸(EDTA)及其 二钠盐 (EDTA-2Na),统称为 EDTA。结构如下:
EDTA在水中溶解度小,故配制 标准溶液时,常用它的二钠盐。 EDTA的分子或离子中含有2个氨基 氮和4个羧基氧可与金属离子配合, 生成具有5个五元环的稳定性很高的 螯合物。如下图:
4.由于EDTA与金属离子螯合可形成5个五 元环,故生成的螯合物十分稳定。常见 金属离子的EDTA螯合物的lgKs 见表5-2。 表5-2 EDTA与部分金属离子螯合物的稳 定常数对数值
溶液中螯合物的稳定性除决定于螯 合物稳定常数的大小外,还与溶液 的pH值有关。不同的金属离子与 EDTA生成的螯合物的稳定性不同, 滴定时所需溶液的pH值也不同。因 此,在两种以上金属离子的混合溶 液中,常可以通过调节溶液的pH值, 用EDTA进行选择滴定。
Ca2++H2Y2- ⇌ CaY2- +2H+ Mg2+ + H2Y2- ⇌MgY2- +2H+
滴定终点时:
MgIn-+ H2Y2- ⇌MgY2- +HIn- +H+
紫红
蓝
螯合物:由中心原子与多齿配体形
螯合剂EDTA简介

螯合剂EDTA简介螯合剂EDTA简介概述:螯合剂是一种通过分子结构中的官能团与金属离子形成稳定络合物的化合物。
这些络合物能够改变金属离子的性质和化学活性,广泛应用于医药、环境、冶金、食品工业等领域。
在这些应用中,螯合剂EDTA(乙二胺四乙酸)是最为常见和重要的一种螯合剂。
本文将对EDTA的性质、应用和制备方法进行详细介绍。
性质:EDTA是一种白色结晶粉末,具有无味无臭的特点。
其化学式为C10H16N2O8,分子量为292.24。
EDTA具有强螯合能力,可以与许多过渡金属离子形成稳定的络合物。
它是一种弱碱性化合物,在水中能够溶解得很好。
其络合物的形成常数很大,使得EDTA成为理想的螯合剂。
应用:1. 医药应用:EDTA可以与铁、铜、钙等金属离子形成络合物,被广泛应用于药物配方中。
它可以被用来治疗重金属中毒,如铅中毒和铜中毒。
EDTA能够与这些有害物质形成络合物,提高其溶解度,从而加速其排出体外。
此外,EDTA也可以用于治疗缺铁性贫血和血液病。
2. 环境应用:EDTA在环境领域被广泛应用于土壤修复和废水处理。
由于它对金属离子有良好的螯合能力,EDTA可以与土壤中的重金属形成稳定的络合物,减少其毒性和迁移性,从而改善土壤质量。
在废水处理中,EDTA可以被用来去除废水中的重金属离子,减少对环境的污染。
3. 食品工业:EDTA被广泛用于食品工业中作为抗氧化剂和金属螯合剂。
食品中往往含有一定量的金属离子,这些金属离子容易与食品中的其他成分产生反应,导致食品品质的下降。
EDTA可以与这些金属离子形成络合物,防止其与其他成分发生反应,并延长食品的保质期。
制备方法:制备EDTA一般采用合成法。
首先将乙二胺与乙醇作用形成二乙胺,然后再与氯乙酸反应得到乙二胺四乙酸的初步产物。
最后,通过水解、精制和结晶等步骤得到高纯度的EDTA结晶粉末。
结论:螯合剂EDTA是一种重要而多功能的化学物质,广泛应用于医药、环境和食品工业等领域。
EDTA的特性与用途

EDTA的特性与用途EDTA(乙二胺四乙酸)是一种常用的螯合剂,可以与金属离子形成稳定的络合物。
EDTA具有多种特性和广泛的应用,下面将详细介绍。
1.螯合能力强:EDTA可以与许多金属形成稳定的1:1或1:2络合物,并能有效抑制金属离子的活性。
2.稳定性高:由于EDTA与金属离子之间形成了化学键,络合物具有较高的热稳定性和化学稳定性。
3.溶解性良好:EDTA在水中溶解度高,能够与溶液均匀混合。
4.酸碱性弱:EDTA在水溶液中能够稳定在大部分pH范围内。
5.较低的毒性:EDTA对人体和环境相对较安全,没有明显毒副作用。
1.金属离子的螯合剂:由于EDTA与金属离子形成稳定络合物,因此广泛用于金属离子的螯合和去除。
特别是在工业废水处理中,EDTA被用来去除废水中的重金属离子,减少对环境的污染。
此外,EDTA还可用于金属蠟浸出、电镀、催化剂制备等方面。
2.医药工业:EDTA广泛应用于药物的制备和稳定性改进。
例如,EDTA可以与一些药物形成配合物,增强药物的稳定性、水溶性和生物利用度等。
同时,EDTA也被用作药物注射液的稳定剂,延长药物的保质期。
3.食品工业:EDTA可用作食品的螯合剂,防止金属离子的存在对食品的氧化、变质产生不良影响。
此外,EDTA还能够在食品加工过程中稳定乳化液、色素和维生素等。
4.化妆品工业:EDTA可作为化妆品的抗氧化剂和稳定剂,延长化妆品的使用寿命。
此外,EDTA还能够调节乳化剂和表面活性剂的配方,增加产品的稳定性和可扩展性。
5.化学分析:EDTA常用作分析化学试剂,用于金属离子的定量分析。
例如,EDTA滴定法可用于测定钙、镁、铜、锌等金属离子的含量。
6.医学检验:EDTA血液采样管广泛用于临床医学的血液检验。
EDTA在采集血液时能够与细胞外的金属离子结合,阻止血液凝固,并保持血液样品稳定。
7.其他领域:EDTA还可应用于纺织工业、造纸工业、园林绿化等方面,用于脱除金属离子的存在,减少对产品的损害。
螯合剂之EDTA及其钠盐

EDTA 普遍应用于生物学各个领域,常用在电泳缓冲体系中,金属依赖性的蛋白水解酶或者核酸酶反应,细胞消化或者样品解聚过程等等。
EDTA 溶液已被用于一项帮助阐明抗原修复在乙醇固定涂片的免疫染色中作用的研究。
EDTA 溶液也被用于研究中以评估生物素标记的荧光素(b-FITC)的摄取和释放。
EDTA 常以二钠或者三钾盐的形式用作抗凝剂,作用机制在于它能够螯合血液中的钙离子从而阻止凝血发生。
Absin 供应的EDTA 是一种重要络合剂/螯合剂,常用做核酸酶、蛋白酶的抑制剂;也可用于消除重金属离子对酶的抑制作用。
1. 乙二胺四乙酸(EDTA) abs44059861生化研究中用作钙螯合剂,消除微量重金属导致的酶催化反应中的抑制作用。
常用络合剂试剂,也用作洗涤剂、血液抗凝剂等。
2. EDTA, 0.5 M, pH 8.0 abs9133本品是用DEPC(diethyl pyrocarbonate ,焦碳酸二乙酯)处理过的EDTA 溶液, 是一种螯合剂,用来消除重金属离子对酶的抑制作用,常用于分子生物学应用。
3. EDTA 二钠盐二水合物 abs44059863科研试剂,用于重金属定量分析剂,用作氨羧络合剂,还用于制药工业、彩色显影等。
4. EDTA 二钠盐 abs42222235是一种重要络合剂,用于络合金属离子和分离金属。
常用于分子生物学及电泳实验5. 10%EDTA 脱钙液 abs9223EDTA 是一种相对较好的螯合脱钙剂,对组织结构影响最小,可以较好的保存组织的某些酶类,经EDTA脱钙后的组织可以进行免疫组化和原位杂交染色。
但是该法脱钙速度太慢,一般脱需要数周至数月。
不适合常规标本脱钙使用。
对含钙组织最好固定之后,再进行脱钙或二者同时进行。
然后进行下游的实验,如脱水、透明、浸蜡、包埋、切片。
EDTA与螯合剂 ppt课件
ppt课件
10
溶液中螯合物的稳定性除决定于螯 合物稳定常数的大小外,还与溶液 的pH值有关。不同的金属离子与 EDTA生成的螯合物的稳定性不同, 滴定时所需溶液的pH值也不同。因 此,在两种以上金属离子的混合溶 液中,常可以通过调节溶液的pH值, 用EDTA进行选择滴定。
ppt课件
11
例如,在Mg2+离子和Zn2+离子的混合
测定水的总硬度时加NH3-NH4Cl缓 冲溶液调节pH ≈ 10,以铬黑T为指 示剂,用EDTA标准溶液滴定。溶液 中有关配合物的稳定性有如下顺序:
CaY2- > MgY2- >MgIn - > CaIn-
ppt课件
20
反应式如下:
加指示剂时:
Mg2+ + HIn2- ⇌ MgIn - + H+
蓝 紫红
ppt课件
18
可加入某种掩蔽剂(此试剂能与干 扰离子结合成更稳定的配合物,而 对被测离子无影响),把干扰离子 掩蔽起来,再滴定被测离子。例如 EDTA滴定Ca2+ Mg2+时,少量Fe3+, Al3+有干扰,可加入三乙醇胺消除 干扰。
ppt课件
19
(三)EDTA螯合滴定
示例-水的总硬度测定
水的总硬度是指水中Ca2 + , Mg2+ 的总硬度(以为mmol ·L-1单位)
12
(二)EDTA螯合滴定的基本原理
EDTA螯合滴定就是基于EDTA与
金属离子螯合反应的一种重要的滴定分 析方法,常用于测定溶液中金属离子的 含量。
EDTA螯合滴定的原理和基本过程:
滴定时使用的指示剂叫做金属指示剂。 它们是一类能与金属离子形成有色配合 物的水溶性有机染料。
螯合剂EDTA简介

螯合剂EDTA简介螯合剂EDTA简介螯合剂是指能够与金属离子形成稳定的络合物的化合物。
它们在许多领域中起着重要作用,包括医学、环境保护和工业化学等。
其中,以螯合剂EDTA(乙二胺四乙酸)最为著名和广泛使用。
EDTA是一种多羧酸化合物,其化学结构如下:乙二胺四乙酸(EDTA)由乙二胺和乙醇(甲醇)以甲基化反应的方式生成。
它的结构中有四个羧酸基团,分别位于乙胺上的四个空间方向,这使得EDTA能够有效地与金属离子形成络合物。
EDTA具有许多优异的性质,使其成为广泛使用的螯合剂。
首先,EDTA具有良好的水溶性,因此可以在溶液中方便地使用。
其次,EDTA在溶液中能够稳定金属离子的存在,形成络合物,从而阻止金属离子与其他物质发生反应。
此外,EDTA还具有选择性,即它能够选择性地与某些金属离子形成络合物,而对其他金属离子不产生影响。
这种选择性使得EDTA在许多分析方法中得到了广泛应用。
EDTA的络合反应是以配位键形式进行的,其中羧酸基团中的氧原子与金属离子之间形成了共价键。
由于EDTA与金属离子的配位能力较强,形成的络合物具有较高的稳定性。
这种稳定性使得EDTA能够有效地去除水中的金属离子,从而在环境保护和水处理中具有重要的应用价值。
EDTA在医学领域中被广泛用作抗凝剂。
它能够与钙离子配位,阻止凝血过程的发生。
因此,EDTA被用于血液采集和某些外科手术中,以减少出血问题的发生。
此外,EDTA还被用作某些疾病的治疗药物,如重金属中毒和铅中毒的治疗等。
在工业化学中,EDTA被广泛应用于金属表面处理,如镀铝、镀锌和电镀等。
在这些过程中,金属离子在溶液中稳定存在,并与EDTA形成络合物,从而进行有序的金属离子沉积和形成均匀的金属涂层。
此外,EDTA还被用作某些化学反应的催化剂,从而提高反应的效率和选择性。
尽管EDTA在许多领域中有着广泛的应用,但也存在一些潜在的问题。
首先,EDTA是一种难降解的有机物,因此在环境中的寿命较长。
edta的作用

edta的作用
EDTA,也称为乙二胺四乙酸(Ethylenediaminetetraacetic Acid),是一种广泛应用于化学、医学和工业领域的螯合剂。
它具有与金属离子形成络合物的能力,因此被广泛用作金属离子的螯合剂和螯合试剂。
EDTA的主要作用之一是在化学反应中控制和稳定金属离子的
存在。
在分析化学中,EDTA可用来配位和螯合金属离子并形
成稳定的络合物,从而使其在溶液中保持稳定且不沉淀。
这对于精确测定金属离子的浓度至关重要,尤其是在环境监测、食品分析和药物研究中。
此外,EDTA还可用于水处理和洗涤剂中,以去除水中的金属
离子,如钙、镁、铁等,从而防止水垢的形成。
这在家庭清洁产品、洗衣剂和洗碗剂中得到广泛应用,以保持管道和表面的清洁和光滑。
在医学领域,EDTA常用于治疗铅和其他重金属中毒。
由于EDTA可以与重金属形成稳定的络合物,并通过尿液排出体外,因此被用作螯合剂来促使重金属离子的排除。
该过程被称为螯合疗法,可以减少重金属对身体的毒性和损害。
综上所述,EDTA作为一种重要的螯合剂,具有控制金属离子
反应和稳定金属络合物的能力,在化学、医学和工业领域发挥着重要的作用。
edta标准溶液的作用

edta标准溶液的作用EDTA(乙二胺四乙酸)标准溶液是一种常用的配位化学试剂,用于许多实验室分析和化学反应中。
其主要作用是与金属离子形成稳定的络合物,从而实现对金属离子的螯合作用。
1. 金属离子螯合:EDTA标准溶液的主要作用是与金属离子形成络合物,将金属离子与其他物质分离,并提供准确的分析结果。
EDTA可以与多种金属离子结合,包括钙、镁、锌、铁、铜等。
这种络合作用可以用于分离和分析金属离子的浓度,例如使用EDTA标准溶液进行滴定分析。
2. 金属离子螯合指示剂:EDTA标准溶液还可用作金属离子螯合指示剂。
在滴定分析中,EDTA标准溶液可以与金属离子形成络合物,并改变溶液的颜色,作为指示剂用于确定滴定终点。
通过观察颜色变化,可以确定金属离子的浓度或者质量。
3. 金属离子分离:EDTA标准溶液可以用于分离金属离子,尤其是在环境和生物样本分析中。
由于EDTA的螯合作用强烈,可以将金属离子与其他化合物或杂质分离开。
这使得金属离子的分析更加准确可靠,并能排除其他干扰物质。
4. 缓冲溶液:EDTA标准溶液也可用作缓冲剂。
在一些化学反应中,pH的变化会对反应的速率和结果产生影响。
通过添加EDTA标准溶液,可以调节溶液的pH,使其保持在所需的范围内,从而更好地控制和调整化学反应。
综上所述,EDTA标准溶液是一种多功能的配位试剂,在实验室分析和化学反应中具有广泛应用。
它可以与金属离子形成络合物,用作螯合剂、指示剂和分离剂,还可以用作缓冲剂。
EDTA标准溶液的应用广泛且重要,为许多化学实验和分析提供了准确性和精确性。
edta的应用原理

EDTA的应用原理1. 介绍EDTA(乙二胺四乙酸)是一种常用的螯合剂,具有广泛的应用领域,特别是在化学分析、水处理和医药领域。
本文将详细介绍EDTA的应用原理。
2. EDTA的化学结构EDTA的化学结构如下:HOOC-CH2CH2-N(CH2COOH)2|CH2COOHEDTA具有两个羧基和四个乙二胺基,可以与金属离子形成稳定的配合物。
3. 螯合反应EDTA的应用原理主要与其螯合反应有关。
螯合反应是指EDTA与金属离子之间的结合反应。
EDTA的四个乙二胺基中的氮原子可以与金属离子形成配合物。
该配合物稳定性很高,可以防止金属离子发生反应。
4. EDTA的应用EDTA在化学分析、水处理和医药领域有着广泛的应用。
4.1 化学分析由于EDTA与金属离子形成稳定的配合物,可以用于分析金属离子的含量。
常见的应用是通过EDTA滴定法测定水中重金属离子的浓度。
通过添加EDTA溶液到待测样品中,观察到EDTA与金属离子形成螯合物后的颜色改变,从而计算出金属离子的浓度。
4.2 水处理由于EDTA可以与金属离子形成稳定的配合物,并具有解离金属离子的能力,因此在水处理中常用EDTA进行螯合去除水中的重金属离子。
EDTA可以与钙、镁、铁等离子形成络合物,使这些离子失去活性,降低水的硬度和金属离子的含量。
4.3 医药领域在医药领域,EDTA常用于螯合治疗中毒。
例如,EDTA可以与重金属毒素如铅、汞等离子形成稳定的配合物,从而帮助排出体内的有害物质。
EDTA也被用于治疗铁过载症和钙化疾病等疾病。
5. 安全注意事项在使用EDTA时,需要注意以下安全事项:•避免接触皮肤和眼睛,切勿吞咽;•使用时需佩戴防护手套、护目镜等个人防护装备;•储存时存放在干燥、通风的地方。
6. 结论EDTA作为一种螯合剂,在化学分析、水处理和医药领域有着广泛应用。
通过与金属离子形成稳定的配合物,EDTA能够解决许多相关领域的问题。
使用EDTA 时需要注意安全事项,确保安全使用。
非金属离子螯合剂

非金属离子螯合剂非金属离子螯合剂是一种化学物质,能够与金属离子形成稳定的络合物。
这些螯合剂广泛应用于医学、生物学、环境科学、工业等领域。
非金属离子螯合剂的主要作用是通过形成金属络合物来改变金属离子的性质,如稳定性、溶解性、反应性等。
下面将介绍几种常见的非金属离子螯合剂及其应用。
1. EDTA(乙二胺四乙酸):EDTA是一种经典的非金属离子螯合剂,能够与金属离子形成稳定的络合物。
在生物学和医学领域,EDTA常用于螯合金属离子,如Ca2+、Mg2+、Fe2+等,用于溶解血凝块、治疗金属中毒等。
此外,EDTA还被广泛应用于工业中的金属离子螯合剂、水处理剂等。
2. DTPA(二烷基亚胺三乙酸):DTPA是一种常用的非金属离子螯合剂,其结构中包含三个羧基和四个氮原子,能够与金属离子形成稳定的络合物。
DTPA在医学中常用于螯合镧系元素、放射性金属等,用于肿瘤治疗、医学影像等领域。
3. CDTA(巯基二乙酸):CDTA是一种含有巯基的非金属离子螯合剂,其结构具有较强的螯合能力。
CDTA常用于分离、富集、检测金属离子,如铜、镍、镉等,具有较高的选择性和灵敏度。
4. 苯醌二磺酸(AQDS):AQDS是一种具有强氧化性的非金属离子螯合剂,其分子结构中含有两个磺酸基团。
AQDS常用于环境领域中金属离子的螯合和去除,如处理重金属废水、降解有机废物等,具有较好的环境友好性。
5. 亚砜(DMSO):DMSO是一种含有硫原子的非金属离子螯合剂,具有良好的溶解性和渗透性。
DMSO广泛应用于生物领域中金属离子的螯合、溶解、储存,如细胞培养、蛋白质结构研究等,对细胞膜的渗透性也有一定的影响。
以上是几种常见的非金属离子螯合剂及其应用,这些螯合剂在不同领域具有重要的作用,为金属离子的研究和应用提供了有效的工具和手段。
随着科学技术的不断发展,非金属离子螯合剂的研究和应用将会越来越广泛,为人类社会的发展和进步做出更大的贡献。
螯合剂种类

螯合剂种类
螯合剂是一种能够与金属离子形成配合物的化合物,具有良好的稳定性和选择性,因此在很多工业、化学和生物领域得到广泛应用。
以下是一些常见的螯合剂种类及其应用:
1. 乙二胺四乙酸(EDTA):EDTA 是一种广泛用作配合剂的螯合剂,具有很强的与金属离子结合的能力。
EDTA 可以与多种金属离子形成配合物,例如生成稳定的钙盐和镁盐络合物,还可以用作食品、水处理和化学分析等方面。
2. 氨基酸:氨基酸可以通过它们的官能团与金属离子发生配位作用,形成稳定的络合物。
作为金属离子的螯合剂,氨基酸在化学、生物和医学领域得到广泛应用,例如在金属离子的分离和纯化、接近金属离子的化学催化、以及药物的设计和开发方面。
3. 磷酸盐:磷酸盐是另一种常见的螯合剂,可用于金属的稳定化和提纯,也可用于润滑油和高温润滑剂等领域。
例如,一些磷酸盐可以降低金属材料在高温下的磨损和氧化,从而增强它们的抗腐蚀性能和使用寿命。
4. 氢氧化物:一些氢氧化物也可以用作螯合剂,例如一些多聚氧化物和碱式碳酸盐,它们可以与金属离子发生化学反应,形成稳定的络合物。
这些化合物常用于医药和化学工业中,例如用于纺织品染色、水处理和药物的制造等领域。
需要注意的是,螯合剂种类繁多,每种化合物的螯合特性、稳定性和应用范围都有所不同,具体使用需要根据实际需要选择合适的螯合剂。
edta螯合顺序

edta螯合顺序EDTA螯合顺序是指在给定条件下,不同金属离子和EDTA的配位反应顺序。
EDTA是一种常用的螯合剂,可以与金属离子形成稳定的络合物,广泛应用于化学、生命科学和环境科学等领域。
了解EDTA螯合顺序对于合理选择螯合剂、控制化学反应和解析复杂的化学体系具有重要意义。
EDTA螯合顺序的研究起源于20世纪初,最初主要在铁、铜、镉和钴等金属离子的螯合反应中进行研究。
后来,研究人员逐渐发现,在不同的条件下,EDTA与不同的金属离子形成络合物的顺序也有所不同。
首先,EDTA螯合顺序与金属离子的电荷密度有关。
在相同pH条件下,金属离子的离子半径越大,电荷密度越低,螯合反应的速率越慢,因此螯合顺序也不同。
例如,在pH为7的条件下,EDTA与钙离子的络合常数最大,其次为镁、锰、铜、锌等一系列金属离子。
其次,EDTA螯合顺序还与酸碱度、络合物的稳定性和有机溶剂等因素有关。
在较低的pH下,EDTA的羧基部分更容易负载电子,成为更好的1,10-二恶二胺-4,7-二乙酸(H2EDTA)配体,从而加快了一些金属离子的螯合反应速度。
在有机溶剂中,EDTA更容易与溶剂中的金属离子形成络合物,从而限制了与水相中其他金属离子的反应。
最后,EDTA螯合顺序还受到其他离子和分子的影响。
例如,存在大量阴离子或配体的情况下,EDTA很容易与一些金属离子形成复杂的络合物,从而影响了其他金属离子螯合反应的速度和顺序。
总之,了解EDTA螯合顺序对于控制化学反应、调节金属离子的活性、加工原材料等具有重要意义。
需要强调的是,EDTA螯合顺序是一个复杂的研究领域,涉及到许多物理化学和生物化学方面的知识和实验技术。
只有深入理解和掌握了这些知识,才能更好地应用和发挥EDTA的螯合作用。
螯合剂的主要成分

螯合剂的主要成分
嘿,你问螯合剂的主要成分啊?那咱就来唠唠。
螯合剂这玩意儿啊,里面的成分还挺复杂嘞。
不过主要的成分呢,有这么几种。
一种是氨基羧酸类的东西。
这就像一群小帮手,能把金属离子紧紧地抓住。
比如说乙二胺四乙酸,也就是常说的 EDTA。
这玩意儿可厉害啦,能和很多金属离子结合,让它们别乱跑。
就像个小警察,把那些调皮的金属离子给管住。
还有一种是有机膦酸类的成分。
这就像一群小魔法师,能把金属离子变得乖乖的。
比如说羟基乙叉二膦酸,简称HEDP。
它能和金属离子形成稳定的化合物,防止金属离子捣乱。
就像给金属离子施了个魔法,让它们听话。
另外呢,还有聚羧酸类的成分。
这就像一群小保姆,能照顾好金属离子。
比如说聚丙烯酸,它能把金属离子包裹起来,不让它们惹麻烦。
就像给金属离子穿上了一件小棉袄,让它们暖和又听话。
除了这些主要成分呢,螯合剂里可能还会有一些其他的东西。
比如说一些辅助剂,能让螯合剂的效果更好。
或者一
些调节剂,能控制螯合剂的性能。
这些东西就像小助手,帮助主要成分发挥作用。
总之啊,螯合剂的主要成分就是氨基羧酸类、有机膦酸类和聚羧酸类的东西。
它们就像一群小伙伴,一起合作,把金属离子管得服服帖帖。
嘿嘿。
螯合剂种类

螯合剂种类螯合剂是一种化学物质,可以与金属离子形成稳定的络合物,从而改善金属离子的稳定性、降低金属离子的毒性或增加金属的可溶性。
螯合剂可以广泛应用于医学、农业和工业等领域。
以下是常用的螯合剂种类:1. EDTA(乙二胺四乙酸)EDTA是一种常用的螯合剂,能够络合和稳定多种金属离子,如钙、镁、锰、铁、铜和锌等元素。
EDTA还可以用于垃圾处理和水处理等领域。
2. DTPA(二异丙基三胺五乙酸)DTPA是一种能够络合稀土元素和铁离子的螯合剂,广泛应用于农业和医学领域。
它还可以用于石油开采、污水处理和金属清洗等工业领域。
3. EGTA(四乙二胺四乙酸)EGTA是一种专门用于螯合钙离子的螯合剂,可以被用来研究细胞内的钙离子通路。
EGTA也被应用于医学领域,如心脏手术中的心脏停跳。
4. CDTA(半胱氨酸)CDTA是一种钙螯合剂,能够在中性条件下络合和稳定钙离子。
它可以用于处理含有钙的污水,增强防腐剂的稳定性,以及帮助染料的溶解等领域。
5. NTA(乙二胺四乙酸)NTA是一种可以络合和稳定铁、锰、铜、镍和钴等金属离子的螯合剂。
NTA在医学领域已经被用于治疗重金属中毒。
6. 1,10-菲啰啉1,10-菲啰啉可以络合和稳定铁、钴、镍、铜和锌等金属离子,广泛应用于电池制造、染料制造和金属清洗等工业领域。
7. HEEDTA(羟乙基乙二胺三乙酸)HEEDTA是一种具有高螯合能力的螯合剂,可以络合稀土金属、铁和锰等金属离子。
HEEDTA在化妆品制造中被用作防腐剂。
8. EDDHA(乙二胺二(羟基苯甲酸))EDDHA是一种钙螯合剂,能够提高土壤中铁的可溶性,增加植物根系对铁的吸收率。
EDDHA广泛应用于农业领域,用于防治铁缺乏症和改善植物生长。
9. IDA(亚硝基二乙酸)IDA是一种用于治疗缺铁性贫血的药物,它能够将铁离子转移进入人体细胞,从而增加血红蛋白的合成。
10. DFO(除铁胺)DFO是一种用于治疗铁过载症的药物,能够络合和稳定体内的自由铁离子,改善铁过量引起的神经系统损害。
非生物螯合剂EDTA与生物螯合剂EDDS联合施用提高植物提取土壤重金属效应的研究

足 限制 了它在 植物 修复 技 术 中的实 际 应用 J 。高 生 物量作 物 对 重 金 属 累 积 含 量 一 般 不 高 , 但 由于 其 生物 量大 , 具有 较高 的重 金 属 累 积量 , 因而 利 用 高 生物 量作 物修 复土壤 已引起广 泛 的关 注 。 E D T A是 螯合诱 导 植物 修复 土壤 中最 常用 , 也 是研 究 最多 的一 种 螯 合 剂 , 能 大 幅 度 增 加植 物 对 重 金属 的 吸 收 和 富 集 , 提 高 植 物 修 复 效 率 J 。 但E D T A在环 境 中很难 降解 , 残 留时 间较 长 , 容 易 导 致处 理场 所 的重 金 属 向周 围 和地 下水 迁 移 , 造 成 二 次污 染 。生 物螯 合 剂 E D D S与 过渡 金 属具 有
d u c t i o n e ic f i e n c y , d i c 0 t y l e d o n 0 u s 0 i 1 s e e d r a p e( B r a s s i c a j u n i c a ) , mo n o c o t s m a i z e( Z e a ma y s L )p o t
E DT A a n d b i o l o g i c l a c h e l a t i n g a g e n t EDD S a p p l i c a t i o n o f p h y t o r e me d i a t i o n o f s o i l h e a v y me t a l s, b a —
金属螯合剂

金属螯合剂
金属螯合剂是一种能够与金属离子结合的化合物,它通常是无机物,也可以是有机物。
它们广泛应用于工业和实验室中,可用来洗涤金属表面,除去金属表面的污渍和残留物,从而改善金属表面的粗糙度,光滑度和耐腐蚀性。
针对金属表面污染的清洁除锈,金属螯合剂通常采用阴离子和阳离子的混合物,以溶解金属零件的多种污染物。
常用的金属螯合剂有:醋酸、氢氧化钠、EDTA、脲、尿素、磷酸等,其中,醋酸是最常用的螯合剂,用于去除铁和钢表面的氧化物。
EDTA具有抗氧化功能,抑制金属表面氧化,能去除金属基础表面的衍生物,如腐蚀微生物、细菌等,以及污染物如芳烃、烃类等。
而脲是一种强制性金属螯合剂,它能有效地去除金属表面的污染物,如游离酸、铁离子等,维持金属表面的稳定性和耐腐蚀性。
尿素具有良好的螯合性,能有效地清除金属表面的铁锈和油脂污染,同时也能够改善金属表面的磨损性能。
此外,磷酸也是常用的金属螯合剂,它可以清洗海水系统中残留的金属离子,以及清除金属表面的氧化物等污染物,并提高金属表面的光洁度。
此外,金属螯合剂还可以用于金属的表面处理和改善,有助于提高表面硬度、耐蚀性和绝缘强度,从而延长金属零件的使用寿命。
金属螯合剂的技术性、安全性、环保性和有效性都非常重要,而且它们的使用范围也很广泛,涵盖金属腐蚀和表面处理等各个领域。
随着金属螯合剂被越来越多的工业应用,它们将会在工业和日常生活
中发挥着重要的作用。
螯合剂种类

螯合剂种类什么是螯合剂?螯合剂是一类能够与金属离子形成稳定配合物的化合物。
它们通过形成共价键或离子键与金属离子结合,从而阻止金属离子发生化学反应或沉淀。
螯合剂可以被广泛应用于许多领域,包括医药、环境保护、工业加工等。
不同种类的螯合剂具有不同的特性,因此在实际应用中需要根据具体情况选择合适的螯合剂。
有机螯合剂有机螯合剂是一类主要由有机化合物构成的螯合剂。
由于有机螯合剂具有良好的溶解性和可选择性,它们在药物设计和水处理领域得到了广泛应用。
α-胎盘素α-胎盘素是一种最常用的有机螯合剂之一。
它具有与许多金属离子结合的能力,包括铁、铝、钙等。
α-胎盘素可以在医药领域用于治疗铁缺乏性贫血,同时也被用作工业废水处理剂。
β-环糊精β-环糊精是另一种常用的有机螯合剂。
它是一种大环多糖,可以与一些金属离子如氢氧化铁结合形成稳定的配合物。
β-环糊精在环境污染治理中起到了重要的作用,可以用来去除废水中的重金属离子。
EDTAEDTA,即乙二胺四乙酸,是一种广泛使用的有机螯合剂。
它可以与多种金属离子形成稳定的配合物,并用于许多不同的应用领域,如医药、食品工业、水处理等。
EDTA在医药领域被广泛用于螯合金离子,从而增强药物的稳定性和生物利用度。
无机螯合剂无机螯合剂主要由无机化合物构成,它们具有较高的化学稳定性和选择性,因此在某些特定的应用中表现出较好的性能。
氨四乙酸氨四乙酸是一种常见的无机螯合剂,也称为乙二胺四乙酸。
它可以与多种金属离子形成稳定的四个配位键,并且具有较好的溶解性。
氨四乙酸广泛应用于工业生产过程中,可以用于除垢、阻垢剂以及金属离子的稳定剂。
硫酸钠硫酸钠是一种无机螯合剂,常用于纸浆和纸张工业中的漂白过程。
它可以与一些金属离子形成络合物,从而降低金属离子对纸张的影响。
硫酸钠在漂白工艺中具有较好的稳定性和选择性。
酒石酸酒石酸是一种天然无机螯合剂,广泛存在于葡萄酒和葡萄酒渣中。
酒石酸可以与一些金属离子结合形成络合物,从而影响葡萄酒的质量和稳定性。
清洗剂中螯合剂的成分

清洗剂中螯合剂的成分
清洗剂中的螯合剂通常是指能够与金属离子形成稳定的络合物
的化合物。
常见的螯合剂成分包括EDTA(乙二胺四乙酸)、柠檬酸、醋酸、草酸等。
这些化合物能够与金属离子发生配位作用,形成不
溶于水的络合物,从而起到去除水垢、减少金属离子对清洁表面的
影响的作用。
从化学角度来看,螯合剂的成分是一种具有多个配位基团的有
机分子,这些配位基团能够与金属离子形成稳定的配合物。
这些配
位基团通常是羧基、羟基、胺基等官能团,它们能够与金属离子形
成配位键,从而阻止金属离子与表面产生化学反应,起到保护表面
的作用。
另外,从清洁效果的角度来看,螯合剂能够有效去除水垢和金
属盐沉积,使清洗剂更加有效地清洁表面。
螯合剂的作用还可以延
长清洁剂的有效使用寿命,提高清洁剂的性能稳定性。
总的来说,螯合剂在清洁剂中起着非常重要的作用,它能够有
效去除水垢和金属盐沉积,保护清洁表面,延长清洁剂的使用寿命,
提高清洁剂的性能稳定性。
因此,清洗剂中螯合剂的成分是非常关键的。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
精选课件
17
对于含有两种或两种以上金属离子 的混合溶液,可以通过调节溶液的
pH值,选择性地滴定其中某一离子。例 如,在Mg2+离子和Zn2+离子的混合溶液
中,可首先调节溶液pH ≈ 6.8,用铬黑
T作指示剂,用EDTA滴定Zn2+离子,
此时Mg2+离子不干扰。然后再调节溶液
pH ≈ 10,用EDTA滴定Mg2+离子。
精选课件
3
二、氨羧螯合剂及氨羧 螯合滴定
(一)氨羧螯合剂的结构和特点
氨羧螯合剂中最重要同时应用最 广的是乙二氨四乙酸(EDTA)及其 二钠盐 (EDTA-2Na),统称为 EDTA。结构如下:
精选课件
4
精选课件Biblioteka 5EDTA在水中溶解度小,故配制 标准溶液时,常用它的二钠盐。 EDTA的分子或离子中含有2个氨基 氮和4个羧基氧可与金属离子配合, 生成具有5个五元环的稳定性很高的 螯合物。如下图:
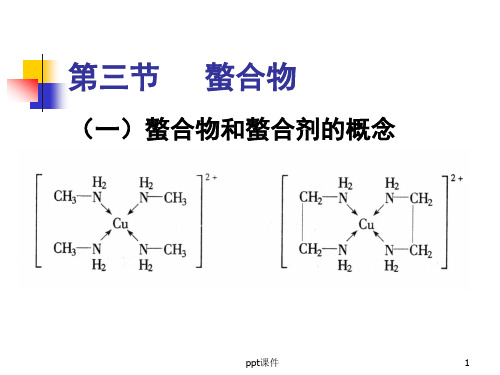
第三节 螯合物
(一)螯合物和螯合剂的概念
精选课件
1
螯合物:由中心原子与多齿配体形
成的环状配合物
螯合剂:能与中心原子形成螯和物 螯合效应:这种由于螯和物的生成 而使配合物的稳定性大大增加的作 用配合物中形成的鏊合环数目越多 其稳定性越强。
精选课件
2
形成的螯合环以五元环和六元环 最稳定。常见的螯合剂大多是有机 化合物,特别是具有氨基N和羧基O 的一类氨羧螯合剂使用得更广。
精选课件
15
精选课件
16
铬黑T能与许多金属离子如Ca2+ Mg2+ Zn2+Cd2+ 等形成红色的配合物。 在pH为7~11时,铬黑T显兰色,与 形成配合物的红色有明显区别,则 终点时颜色变化明显。因此,用铬 黑T作指示剂时最适宜的pH值为
9~10.5,一般用NH3-NH4Cl缓冲溶液 控制溶液pH值在10左右进行滴定。
精选课件
18
可加入某种掩蔽剂(此试剂能与干 扰离子结合成更稳定的配合物,而 对被测离子无影响),把干扰离子 掩蔽起来,再滴定被测离子。例如 EDTA滴定Ca2+ Mg2+时,少量Fe3+, Al3+有干扰,可加入三乙醇胺消除 干扰。
精选课件
19
(三)EDTA螯合滴定
示例-水的总硬度测定
水的总硬度是指水中Ca2 + , Mg2+ 的总硬度(以为mmol ·L-1单位)
精选课件
9
4.由于EDTA与金属离子螯合可形成5个五 元环,故生成的螯合物十分稳定。常见 金属离子的EDTA螯合物的lgKs 见表5-2。 表5-2 EDTA与部分金属离子螯合物的稳 定常数对数值
精选课件
10
溶液中螯合物的稳定性除决定于螯 合物稳定常数的大小外,还与溶液 的pH值有关。不同的金属离子与 EDTA生成的螯合物的稳定性不同, 滴定时所需溶液的pH值也不同。因 此,在两种以上金属离子的混合溶 液中,常可以通过调节溶液的pH值, 用EDTA进行选择滴定。
滴定终点前:
Ca2++H2Y2- ⇌ CaY2- +2H+ Mg2+ + H2Y2- ⇌MgY2- +2H+
滴定终点时:
MgIn-+ H2Y2- ⇌MgY2- +HIn- +H+
紫红
蓝
精选课件
21
水的总硬度按下式计算:
总硬度= 式中:
CEDTVAEDTA V水样 1000
CEDTA: EDTA 标准溶液的浓度( mol ·L-1 ) VEDTA : 消耗EDTA标准溶液的体积(L) V: 滴定时水样的体积(L)
精选课件
12
(二)EDTA螯合滴定的基本原理
EDTA螯合滴定就是基于EDTA与
金属离子螯合反应的一种重要的滴定分 析方法,常用于测定溶液中金属离子的 含量。
EDTA螯合滴定的原理和基本过程:
滴定时使用的指示剂叫做金属指示剂。 它们是一类能与金属离子形成有色配合 物的水溶性有机染料。
精选课件
13
作为金属指示剂必须具备以下条件: 1.与金属离子形成的配合物的颜色 与其本身(即未配合时)的颜色有 明显不同;
测定水的总硬度时加NH3-NH4Cl缓 冲溶液调节pH ≈ 10,以铬黑T为指 示剂,用EDTA标准溶液滴定。溶液 中有关配合物的稳定性有如下顺序:
CaY2- > MgY2- >MgIn - > CaIn-
精选课件
20
反应式如下:
加指示剂时:
Mg2+ + HIn2- ⇌ MgIn - + H+
蓝 紫红
精选课件
6
CaY2-的结构
精选课件
7
EDTA与金属离子的配合有以下特点: 1.螯合能力强 除碱金属以外,能与 几乎所有的金属离子形成稳定的螯 合物。
2.与金属离子形成的螯合物大多带 有电荷,因此易溶于水。
精选课件
8
3.简单的螯合比 不论几价的金属离子, 它们与EDTA总是1:1螯合。例如:
M2++H2Y2--MY2 - +2H + M3++H2Y2--MY - +2H + M4++H2Y2--MY +2H +
精选课件
11
例如,在Mg2+离子和Zn2+离子的混合
溶液中,调节溶液的pH ≈ 6.8, 这时
EDTA仍可与 Zn2+离子完全螯合,而与 Mg2+离子则完全不螯合,即Mg2+离子 的存在不会干扰EDTA 对Zn2+离子的螯 合滴定。
由于滴定时不断有离子的生成,为了 保持合适的pH值,使反应进行完全,滴 定前必须加入合适的缓冲溶液控制溶液 的pH值。
2.与金属离子形成的有色配合物具 有足够的稳定性;
3.与金属离子形成配合物的稳定性 必须小于EDTA与金属离子形成螯合 物的稳定性。
精选课件
14
常用的指示剂有铬黑T,钙指示 剂,二甲酚橙,PAN等。现以铬黑T 为例,说明金属指示剂的变色原理。 铬黑T为弱酸性偶氮染料,能随溶液 pH值变化而显示不同的颜色。如用 符号NaH2ln表示铬黑T。在溶液中 有下列平衡:
精选课件
22
此课件下载可自行编辑修改,此课件供参考! 部分内容来源于网络,如有侵权请与我联系删除!感谢你的观看!
