分子结构答案
DNA分子的结构习题 含答案

DNA分子的构造、复制限时训练1.以下列图是DNA构造模式图,据图所作的以下推测不正确的选项是〔〕A.限制性内切酶能将a处切断B.DNA连接酶能将a处连接C.解旋酶能切断b处D.连接b处的酶为RNA聚合酶2甲生物核酸的碱基组成为:嘌呤占46%、嘧啶占54%,乙生物遗传物质的碱基比例为:嘌呤占34%、嘧啶占66%,那么甲、乙生物可能是〔〕A.蓝藻、变形虫B.T2噬菌体、豌豆C.硝化细菌、绵羊D.肺炎双球菌、烟草花叶病毒3.分析一个DNA分子时,发现含有30%的腺嘌呤脱氧核苷酸,因此可知该分子中一条链上鸟嘌呤含量最大值可占此链碱基总数的〔〕A.20% B.30%C.40% D.70%4.一个DNA分子的一条链上,腺嘌呤比鸟嘌呤多40%,两者之和占DNA分子碱基总数的24%,那么这个DNA分子的另一条链上,胸腺嘧啶占该链碱基数目的( ) A.44% B.24% C.14% D.28%5.用15N标记细菌的DNA分子,再将它们放入含14N的培养基中连续繁殖四代,a、b、c为三种DNA分子:a只含15N,b同时含14N和15N,c只含14N,如以下列图,这三种DNA分子的比例正确的选项是( )6.DNA分子经过诱变,某位点上的一个正常碱基(设为P)变成了尿嘧啶。
该DNA连续复制两次,得到的4个子代DNA分子相应位点上的碱基对分别为U-A、A-T、G-C、C-G。
推测“P〞可能是( )A.胸腺嘧啶B.腺嘌呤C.胸腺嘧啶或腺嘌呤D.胞嘧啶7.假设将含有一对同源染色体的精原细胞的DNA分子用15N标记,并供给含14N的原料。
该细胞进展减数分裂产生的四个精子中,含15N标记的DNA的精子所占的比例是〔〕A.100% B.25%C.50% D.08.以下列图为真核生物染色体上DNA分子复制过程示意图,有关表达错误的选项是〔〕A.图中DNA分子复制是从多个起点同时开场的B.图中DNA分子复制是边解旋边双向复制的C.真核生物DNA分子复制过程需要解旋酶D.真核生物的这种复制方式提高了复制速率9.用15N标记含有100个碱基对的DNA分子,其中有胞嘧啶60个,该DNA分子在14N的培养基中连续复制四次。
分子结构练习及参考答案

专题9 分子结构一、选择题:1.以下物质种,含有非极性共价键的离子化合物是〔〕A、Na2O2B、NaOHC、H2O2D、MgCl22.以下物质中,含有极性共价键的是〔〕〔1〕N2(2)H2O (3)CCl4(4)Na2O2(5)NaOH (6)Na2OA、〔1〕〔2〕〔3〕 B.〔4〕〔5〕〔6〕C、〔2〕〔3〕〔5〕D(2)(4)(6)3.A原子的L电子层比B原子的L电子层少3个电子,B原子核外的电子总数比A原子电子总数多5个,那么A、B可能形成( )A、离子化合物B2A3B、离子化合物B3A2 C.共价化合物B3A2D、共价化合物BA24、根据“相似相溶〞的规律,以下溶剂可以用来从溴水中萃取溴的是〔〕(1)酒精〔2〕CCl4〔3〕液氨〔4〕苯〔5〕直馏汽油A、〔1〕〔2〕〔4〕〔5〕B、〔2〕〔4〕〔5〕C、〔1〕〔3〕〔5〕D、〔1〕〔3〕〔4〕5.以下各组物质中,化学键类型相同,分子的极性也相同的是〔〕A SO2和CH4B、CO2和CCl4C、SO2和CO2D、NH3和CCl46.含有极性键的非极性分子是〔〕(1)SO2(键角119ο)〔2〕CS2(直线型)〔3〕CCl4(4)NH3(5)CH2Cl2(6)BF3(平面正三角形)A、〔2〕〔3〕〔4〕B、〔1〕〔4〕〔6〕C、〔2〕〔3〕〔6〕D、〔2〕〔3〕〔5〕7.关于化学键的表达,正确的选项是〔〕A.离子化合物可能含共价键B.共价化合物可能含离子键C.离子化合物中只含离子键D.共价化合物中不含离子键8.以下分子中所含原子都满足最外层8电子结构的是〔〕A、光气〔COCl2〕 B.六氟化硫C、二氟化氙D、三氟化硼9.以下分子的结构中,原子的最外层电子不能满足8电子稳定结构的是〔〕A、CO2B、PCl3C、CCl4D、NO210.以下各分子中所有原子都满足最外层8电子结构的是〔〕A、BeCl2B、PCl3 C、PCl5 D、N211.以下性质中,可以证实某化合物内一定存在离子键的是〔〕A、可溶于水B、具有较高的熔点C、水溶液可以导电D、熔融状态能导电12、最近科学家研制的一种新分子,它具有空心的类似于足球的结构,分子式为C60,以下说法正确的选项是〔〕A、C60是一种新型的化合物B、C60和石墨都是碳的同素异形体C、C60中含有离子键D、C60的相对分子质量是720二、填空题:13、写出以下物质的电子式:〔1〕Cl2____________(2)N2_____________(3)HCl_______________(4)NH3_______________ 〔5〕H2O___________(6)H2O2___________(7)CO2____________(8)CH4________________ (9)PCl3____________(10)NaCl____________(11)MgCl2__________〔12〕Na2S____________ (13)NaOH___________(14)Na2O2__________(15)NH4Cl__________(16)甲基_____________ 17〕羟基__________〔18〕醛基___________〔19〕乙烯_________〔20〕乙炔______________ 〔21〕甲酸_______________14、用电子式表示以下物质的形成过程:(1)H2_____________________________________(2)HCl_______________________________ (3)H2S____________________________________(4)NH3______________________________ (5)KCl____________________________________(6)CaCl2_____________________________ (7)K2S___________________________________(8)BaCl2_____________________________________________ 15、化合物A是一种不稳定的物质,它的分子组成可用O x F y表示,10Ml氧气和10Ml氟气〔同温同压〕下,试答复:(1)A的化学式______________,理由______________________________(2)A分子中,x个氧原子呈-O-O-键状排列,每一根短线代表_________,A的电子式为____________,A分子的结构式为______________________.答案:1、A2、C3、B4、B5、B6、C7、AD8、A 9、D 10、BD 11、D 12、BD15、O3F2;1mol A分解产生了3mol O 原子,2mol F原子;在同温同压,体积比等于物质的量的比. F-O-O-O-F .。
分子结构练习20题

分子结构练习20题1、下列分子中,两个相邻共价键的夹角最小的是:A、BF3B、HS2C、NH3OD、H2正确答案:B2、下列分子和离子中,中心原子成键轨道不是sp2杂化的是:-A、NO3B、HCHOC、BF3D、NH3正确答案:D3、下列化合物中,极性最大的是:A、CS2B、HS2C、SO3D、SnCl4正确答案:B4、下列分子中,偶极矩不等于零的是:A、BeCl2B、BF3C、NF3D、CO2正确答案:C5、下列液态物质中只需克服色散力就能使之沸腾的是:A、HO2B、COC、HFD、Xe正确答案:D6、下列各组离子中,离子的极化力最强的是:A、K+、Li+B、Ca2+、Mg2+C、Fe3+、Ti4+D、Sc3+、Y3+正确答案:C7、下列物质熔点变化顺序中,不正确的是:A、NaF>NaCl>NaBr>NaIB、NaCl<MgCl 2<AlCl 3<SiCl 4C、LiF>NaCl>KBr>CsID、Al 2O 3>MgO>CaO>BaO正确答案:B8、下列原子轨道的n 相同,且各有一个自旋方式相反的不成对电子,则沿X 轴方向可形成π键的是:A、P X -P XB、P X -PyC、Py-P ZD、Pz-Pz正确答案:D9、下列分子或离子中,具有反磁性的是:A、O 2B、O 2-C、O 2+D、O 22-正确答案:D10、按分子轨道理论,下列稳定性排列正确的是:A、O 2>O 2+>O 22-B、O 2+>O 2>O 22-C、O 22->O 2>O 2+D、O 2+>O 22->O 2正确答案:B11、下列分子或离子中,中心原子的价层电子对几何构型为四面体,而分子(离子)的空间构型为V 字形的是:A、NH 4+B、SO 2C、ICl 2-D、OF 2正确答案:D12、几何形状是平面三角形的分子或离子是:A、SO 3B、SO 32-C、CH 3-D、PH 3正确答案:A13、下列分子中偶极矩大于零的是:A、BF 3B、PF 3C、SiF 4D、PF 5正确答案:B14、根据VSEPR 理论,BrF 3分子的几何构型为:A、平面三角形B、三角锥形C、三角双锥形D、T 字形正确答案:D15、下列分子中,离域π键类型为П33的是:A、O 3B、SO 3C、NO 2D、HNO 3正确答案:C16、下列晶格能大小顺序中正确的是:A、CaO>KCl>MgO>NaClB、NaCl>KCl>RbCl>SrOC、MgO>RbCl>SrO>BaOD、MgO>NaCl>KCl>RbCl正确答案:D17、在下列各种含氢化合物中,有氢键的是:A、CHF 3B、C 2H 6C、C 6H 6D、HCOOHE、CH 4正确答案:D18、在石墨晶体中,层与层之间的结合力是:A、金属键B、共价键C、范德华力D、大π键正确答案:C19、下列关于O 22-和O 2-的性质的说法中,不正确的是:A、两种离子都比O 2分子稳定性小B、O 22-的键长比O 2-键长短C、O 22-是反磁性的,而O 2-是顺磁性的D、O 22-的键能比O 2-的键能小正确答案:B20、若中心原子采用sp 3d 杂化轨道成键的分子,其空间构型可能是:A、三角双锥形B、变形四面体C、直线形D、以上三种均有可能正确答案:D。
普通化学习题答案-第八章 化学键和分子结构

5
General Chemistry
Chapter 3 Homework
2. 将下列化合物按熔点从高到低的顺序排列:
NaF SiF4 NaBr SiBr4 NaCl SiCl4 NaI SiI4 NaF >NaCl> NaBr> NaI> SiI4> SiBr4> SiCl4 >
◆同主族元素,自上而下,具有相同电荷的离子半径依次增大
如:r (Li+)<r (Na+)<r(K+)<r (Rb+)<r (Cs+);
r(F-)<r(Cl-)<r(Br-)<r(I-)
◆同一周期中,电子构型相同时,随着离子电荷数增加,正离
子半径减小,负离子半径增大
如:r (Na+) >r(Mg2+) >r (Al3+); r(F-)<r(O2-)<r(N3-)
SiF4 3. 指出下列各对分子之间存在的分子间作用力的类型(取向 力、诱导力、色散力、氢键):
(1) 苯和CCl4
(2) 甲醇和H2O
(3) CO2和H2O
(4) HBr和HI
(1) 色散力(非极性分子间) (2) 色散力、取向力、诱导力、氢键(极性分子间) (3) 色散力、诱导力、(极性和非极性分子间) (4) 色散力、取向力、诱导力、(极性分子间)
3.C2H4分子中包含有 5 个σ键, 1 个π键,两个C原子采用
了 sp杂2 化形式,π键在
C原子与
C原子间形成。
4.AgCl、AgBr、AgI在水中的溶解度依次 减小 ,颜色依
无机化学(上册):第9章 化学键与分子结构 习题答案
第9章化学键与分子结构习题1. 根据AgX晶格能理论值与实验值差别判断Ag-X共价键成分递增顺序。
AgF AgCl AgBr AgI实验值(kJ·mol-1)951 902 887 886理论值(kJ·mol-1)925 833 808 7742.从Cr原子的价层结构3d54s1来看,Cr失去1个4s电子后成为3d5半充满构型。
这种结构似应是稳定的,因而似应有CrX (X =F、Cl、Br、I)化合物存在,但实际上却未能制备出这类化合物。
理论计算CrCl晶格能为758 kJ·mol-1,已知金属Cr的升华能(397 kJ·mol-1)、Cl-Cl键的键能(242.6 kJ·mol-1)、Cr的第一电离能(653 kJ·mol-1)、Cl的第一电子亲合能(348.6 kJ·mol-1)。
设计CrCl的玻恩-哈伯热化学循环,计算CrCl(s)的标准摩尔生成焓(∆f H m o)。
另已知反应2CrCl(s)=CrCl2(s)+Cr(s)的标准摩尔自由能变为-486 kJ·mol-1。
比较说明CrCl稳定性,解释上述事实。
3.4. 温度为298 K时,已知(1)H2=2H(g), Δr1H m o= 436 kJ.mol-1,(2)O2=2O(g), Δr2H m o= 498 kJ.mol-1,(3)H2O(g)=2H(g)+ 2O(g), Δr3H m o= 930 kJ.mol-1 求:反应H2 (g)+½ O2 (g)= H2O (g) 的Δr H m o。
5. 写出下列分子的Lewis结构式:CF4、OF2、HCN、CO、NSF6. 写出下列离子的Lewis结构式:CF3+、C22-、PH2-、BH4-7. 乙炔的标准生成焓为226.6 kJ.mol-1,H-H、C-H键键能D H-H、D C-H分别为436 kJ.mol-1、415 kJ.mol-1,石墨的升华能∆sub H(C(s)) 为717 kJ.mol-1,求C≡C的键能D C≡C。
分子结构答案

分子结构——答案1.下列分子中只含键的为()。
A、HCN;B、H2O;C、CO;D、N2;E、C2H4解答或答案:B。
2.下列化合物中分子极性最大的是()A、CCl4;B、C2H5OH;C、I2;D、H2O;E、H2S解答或答案:D3.下列化合物=0的是()A、H2O;B、NH3;C、BF3;D、CH3Cl;E、HCl解答或答案:C4.在下列分子或离子中,没有孤对电子的是()。
A、H2O;B、NH3;C、H2S;D、NH4+;E、OH-5.乙醇和水之间的作用力为()。
A、色散力;B、取向力和诱导力;C、色散力和诱导力;D、取向力、诱导力和色散力;E、除D所述之外还有氢键解答或答案:E6.惰性气体在低温下能够被液化的原因在于()。
A、单原子分子有一定的体积;B、单原子分子有一定的质量;C、单原子分子间有相互作用;D、单原子分子在低温下形成氢键;E、原子是由带正电荷的核和带负电荷的电子组成的解答或答案:C7.下列说法中正确的是()。
A、p轨道之间以“肩并肩”重叠可形成键;B、p轨道之间以“头碰头”重叠可形成键;C、s轨道和p轨道“头碰头”重叠可形成键;D、s轨道和p轨道“头碰头”重叠可形成键;E、共价键是两个原子轨道“头碰头”重叠形成解答或答案:C8.甲烷(CH4)分子中,碳原子所采用的杂化方式为()。
A、sp;B、sp2;C、sp3;D、dsp2;E、spd2解答或答案:C9.下列各分子之间仅存在着色散力的是()。
A、甲醇和水;B、溴化氢和氯化氢;C、氮气和水;D、乙醇和水;E、苯和四氯化碳解答或答案:B10.下列分子中极性最小的是()。
A、NaF;B、HF;C、HCl;D、HBr;E、HI解答或答案:E11.下列分子中存在氢键的是()。
A、HF;B、CH4;C、HI;D、CCl4;E、CO2解答或答案:A12.下列化合物中,能形成分子内氢键的是()。
A、C O O HO H;B、CH3F;C、COOHHO;D、H2O;E、PH3解答或答案:A13.NH3分子中N原子采取不等性sp3杂化,分子在空间的构型为()。
基础化学李保山第二版10-分子结构习题答案

10 分子结构习题解答(p322-325)思考题1. Na和Cl、F之间,K和Cl、F之间能形成离子化合物。
2. 答案:Be2+ 2电子构型;Ca2+8电子构型;Fe3+9~17电子构型;Cu+ 18电子构型;Sn2+18+2电子构型;Pb4+18电子构型;O2-8电子构型。
3.答案:S2->K+>Na+>Mg2+4. Sn4+ >Fe2+ >Sn2+ >Sr2+>Ba2+5. S2->O2->F->Cu+ >Na+6. (1)半径比规则可以用来判断离子晶体的晶格类型。
晶格能可以用来衡量离子键的强弱。
(2)离子极化的结果使原来的离子键向共价键方向过渡。
(3)18电子构型的正离子极化率较强;18电子构型的负离子变形性较强。
7. 答案:原子轨道的角度分布方向是一定的,共价键的形成遵循最大重叠原则,所以只能在建轴方向上才能形成稳定的共价键,因而共价键具有方向性;每个原子的未成对电子数时一定的,有几个未成对电子就可以形成几个共用电子对,所以共价键具有饱和性。
8. (1)由两个相同或不相同的原子轨道沿轨道对称轴方向相互重叠而形成的共价键(头碰头),叫做σ键。
当两个原子的轨道从垂直于成键原子的核间连线的方向接近,发生电子云重叠而成键(肩并肩),这样形成的共价键称为π键。
(2)单键:在价键理论中,两个原子之间如只有一对共用电子,形成的化学键称为单键。
单电子键:在分子轨道理论中,只有一个电子填入分子轨道形成的化学键称为单电子共价键。
(3)同类型的杂化轨道可分为等性杂化和不等性杂化两种。
如果原子轨道杂化后形成的杂化轨道是等同的,这种杂化叫做等性杂化。
如果原子轨道杂化后形成的杂化轨道中有一条或几条被孤对电子所占据,使得杂化轨道之间的夹角改变,这种由于孤对电子的存在而造成杂化轨道不完全等同的杂化,叫做不等性杂化。
9. (1)BF3键角大,因为BF3中B的价电子结构为2s22p1,形成分子时,进行sp2杂化,三个sp2杂化轨道分别与三个F原子的p轨道成键,故BF3分子为平面三角形,键角为120度。
高中化学竞赛专题考试—分子结构(含答案)

高中化学竞赛专题考试——分子结构1(路易斯结构式、共振式、VSPER 理论)1.008Zr Nb Mo T cRu Rh Pd Ag Cd In S n S b T e I Hf T a W Re OsIr Pt Au Hg T l Pb Bi Po At Ac-Lr HLi BeB C N O F Na MgAl S i P Cl S K Ca S c T i V Cr Mn Fe Co Ni Cu Zn G a G e As S e BrRb Cs Fr S r Ba RaY La Lu -6.9419.01222.9924.3139.1040.0885.4787.62132.9137.3[223][226]44.9647.8850.9452.0054.9455.8558.9363.5558.6965.3910.8126.9869.7212.0128.0972.61114.8204.4118.7207.2112.4200.6107.9197.0106.4195.1102.9192.2101.1190.298.91186.295.94183.992.91180.991.22178.588.9114.0116.0019.0030.9774.92121.8209.032.0778.96127.6[210][210][210]126.979.9035.454.00320.1839.9583.80131.3[222]He Ne Ar Kr Xe Rn 相对原子质量Rf Db Sg Bh Hs Mt一. 选择题(每题只有一个正确选项,每题2分,共50分)1. 根据鲍林近似能级图,在多电子原子中,基态时,下列电子均处于一定的能级,其中占据能级最高轨道的电子是: ( )A 2,1,1,+1/2B 3,1,1,+1/2C 3,2,1,+1/2D 4,0,0,1/2 2. 下列离子的电子构型可以用[Ar]3d 6表示的是( )A Mn 2+B Fe 3+C Co 3+D Ni 2+3.下列离子半径变小的顺序正确的是( )A F ->Na +>Mg 2+Al 3+B Na +>Mg 2+>Al 3+>F -C Al 3+>Mg 2+>Na +>F -D F ->Al 3+>Mg 2+>Na +4. 下列元素的原子中,第一电离能最大的是 ( )A BeB BC CD N5. 下列物质中,含极性键的非极性分子是()A H2OB HClC SO3D NO26. 下列分子中,没有配位键的是()A COB (BeCl2)2C CH3OBF3D N2H47. NO3—合理的共振式总数为()A 1B 2C 3D 48.下列分子中,键级等于零的是()A.O2 B. F2 C. N2 D. Ne29.原子轨道沿两核连线以“肩并肩”方式进行重叠的是()A. б键B. 氢键C. π键D. 离子键10. 下列物种中,键长最短的是( )A O2B O2+C O2—D O22—11. 下列化合物中,极性最大的是()A CS2B H2OC SO3D SnCl412. 下列物种中,既是路易斯酸,也是路易斯碱的是()ACCl4 B SOCl2 C NH2— D Hg2+13. 估计下列分子中,键角最小的是()()A NH3B PH3C AsH3D SbH314.估计下列分子或离子中,键角最小的是()A NH3B NO3—C NF3D NCl315. 几何形状是平面三角形的离子是()A SO-23 B SnCl-3C CH-3D NO-316. 下列分子或离子为平面四方构型的是()A ICl4—B ClO4—C BrF4+D SF417. 下列分子或离子中,属于三角锥构型的是()A BCl3B H3O+C BrF3D CH+318. 下列化合物中,可能含有卤桥键的是()A SnCl4B BeCl2C CCl4D NCl319. IF5是共价化合物,但液态IF5是电的良导体,原因是IF5二聚后电离,得到各带一个单位正负电荷的阴阳离子,则在该液体中存在的阳离子的几何构型是()A 三角双锥B 四方锥C 平面四方D 变形四面体20 下列哪一个分子的空间构型为折线型()A N3—B I3—C SO32—D CO32—21.下列分子中,偶极矩不为零的是()A BeCl2B BF3C NF3D CH422. 下列分子或离子中,键角最大的是()A XeF2B NCl3C CO-23 D PCl+423 通过测定AB2型分子的偶极距,能够判断:()A分子的空间构型 B 两元素的电负性之差C A—B键的极性D A—B键的键长24. 下列分子中含有两个不同键长的是()A CO2B SO3C SF4D XeF425. 下列分子中,最不容易聚合的是()A N2O5B BeCl2C AlCl3D NO2二、填空题(共50分)26.(10分)指出下列分子中有几个σ键和π键数目。
无机化学答案 第2章分子对称性与分子结构-习题答案

aA2 =1/24 [1×1×4+8×1×1+3×1×0+6×(-1)×0+ 6×(-1)×2]=0
aE =1/24 [1×2×4+8×(-1)×1+3×2×0+6×0×0+6×0×2]=0
aT1 =1/24 [1×3×4+8×0×1+3×(-1)×0+6×1×0+6×(-1)×2]=0
4
aT2 =1/4 [1×3×4+8×0×1+3×(-1)×0+6×(-1)×0+6×1×2]=1 得Γ=A1 ⊕ T2
T2
3
0
-1 -1
1
(x , y , z)
(xy , xz , yz)
以CH4的 4 条杂化轨道为基(分别记为r1、r2、r 3、r 4),依据Td点群的对称元素对其进行
操作,得可约表示Γ:
Td
E
8C3
3C2
6S4
6σd
Γ
4
1
0
0
2
r 1、r2、r 3、r 4
用群分解公式将Γ约化:
aA1 =1/24(1×1×4+8×1×1+3×1×0+6×1×0+6×1×2)=1
2.5 [MA2B2]2-呈平面四边形构型时属D2h点群,含有对称元素:C2、2C2'、σh、i、2σv。[MA2B2]2 -呈四面体构型时属C2v点群,含有对称元素:C2、2σv。
2.6 C4h点群比D4h点群缺少 4 条垂直于主轴的C2'旋转轴。D4h点群的例子有配离子PtCl42-,C4h 点群例子有:
B
C
A
C
A
B
C2v
C
B
A
B
A
C
C2v
C
B
A
A
B
C
D2h
第二章分子结构之练习参考答案
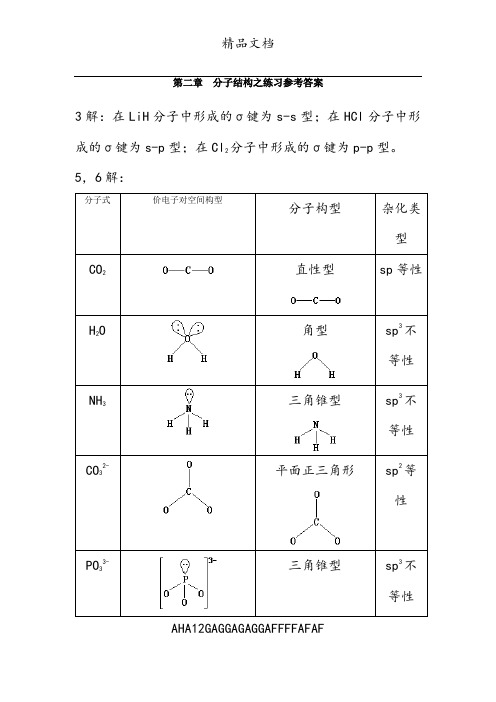
第二章分子结构之练习参考答案3解:在LiH分子中形成的σ键为s-s型;在HCl分子中形成的σ键为s-p型;在Cl2分子中形成的σ键为p-p型。
5,6解:分子式价电子对空间构型分子构型杂化类型CO2直性型sp等性H2O角型sp3不等性NH3三角锥型sp3不等性CO32-平面正三角形sp2等性PO33-三角锥型sp3不等性AHA12GAGGAGAGGAFFFFAFAFAHA12GAGGAGAGGAFFFFAFAFPO 3-四面体sp 3等性PO 43-正四面体sp 3等性9解: 分子式 价电子对总数 σ键数 π键数等电子体类型 孤对电子对数杂化类型 分子构型OF 2422126=+⨯- 2无AX 2(20e)2sp 3角型AHA12GAGGAGAGGAFFFFAFAFClF 3 532137=+⨯- 3 无 AX 3(28e)2 sp 3d 变形T型SOC l 24322126=+-⨯-3 2个d-p π反馈π键AX 3(26e) 1 sp 3三角锥型XeF 2522128=+⨯- 2 无 AX 2(22e)3 sp 3d直性型SF 6662166=+⨯- 6 无 AX 6(48e)sp 3d 2正八面体PCl 5552155=+⨯- 5 无 AX 5(40e)0 sp 3d三角双锥10解:丁三烯的路易斯结构式为:价电子总数:20;C1和C4为sp 2杂化,C2和C3为sp 杂化,C-C-C 键角为1800。
有一个由四个碳原子参与形成的π44大π键和由C2和C3原子参与形成的p-p π键。
这两个π键相互垂直。
11解:O 3-离子的价电子对总数=(6-2×2+1)÷2+2=3.5≈4,且其键角为1000,可推算其应采取sp3不等性杂化(因更接近109.50而非1200)。
由于孤对电子的排斥作用,使其键角小于109.50,离子空间构型为三角锥型。
12解:第二周期同核双原子分子中的Be2因键级等于零而不能稳定存在。
分子结构 习题答案

2、 结合Cl 2的形成,说明共价键形成的条件。
共价键为什么有饱和性共价键形成的条件:原子中必须有单电子,而且成单电子的自旋方向必须相反。
共价键有饱和性是因为:一个原子的一个成单电子只能与另一个成单电子配对,形成一个共价单键。
一个原子有几个成单电子便与几个自旋相反的成单电子配对成键。
电子配对后,便不再具有成单电子了,若再有单电子与之靠近,也不能成键了。
例如:每一个Cl 原子有一个带有单电子的p 轨道,相互以头碰头的形式重叠可以形成共价单键,且只能形成一个单键。
3、 画出下列化合物分子的结构式并指出何者是键,何者是键,何者是配位键。
H HHΖ?δδσσσPN I I IΖ?δδσσσN N N H H H H σσσσσ 膦PH 3, 三碘化氮NI 3 肼N 2H 4(N —H 单键)c C c H H HH σσσσσπ N NN O O o O H σσσσσππππ,乙烯, 四氧化二氮(有双键)。
4.PCl 3的空间构型是三角锥形,键角略小于10928,SiCl 4是四面体形,键角为10928,试用杂化轨道理论加以说明。
杂化轨道理论认为,在形成PCl 3分子时,磷原子的一个3s 轨道和三个 3p 轨道采取sp 3杂化。
在四个sp 3杂化轨道中,有一个杂化轨道被一对孤电子对所占据,剩下的三个杂化轨道为三个成单电子占据,占据一个sp 3杂化轨道的一对孤电子对,由于它不参加成键作用,电子云较密集于磷原子的周围,因此孤电子对对成键电子所占据的杂化轨道有排斥作用,为不等性杂化,所以键角略小于109°28′。
而在SiCl 4分子中,为等性杂化,没有不参加成键的孤电子对,四个杂化轨道都为四个成单电子占据,不存在孤电子对对成键电子对所占据杂化轨道的排斥作用,所以键角为109°28′。
5. 判断下列物种的几何构型,并指出中心原子采取何种杂化方式。
(1) AsF 4 (2) XeOF 3 (3) SF 5 (4) Cl 2CO(5) HO 2 (6) HNO 3 (7) I 3 (8) I 3分子式 杂化方式 电子对构型 分子构型AsF 4sp 3d三角双锥四角锥XeOF 3 sp 3d 三角双锥四角锥SF 5sp 3d三角双锥三角双锥Cl 2COsp 2平面正三角形C OClCl平面三角形HO 2 sp 3 角形O OHHNO 3 sp 2 平面正三角形N OOOH平面三角形I 3 sp 3 四面体 角形I 3- sp 3d三角双锥 直线形6、 试用价层电子对互斥理论写出下列各分子的分子构型,并用杂化轨道理论加以说明。
结构化学课后习题答案

结构化学课后习题答案结构化化学课后习题答案一、化学键与分子结构1. 选择题a) 正确答案:D解析:选择题中,选项D提到了共价键的形成是通过电子的共享,符合共价键的定义。
b) 正确答案:B解析:选择题中,选项B提到了离子键的形成是通过电子的转移,符合离子键的定义。
c) 正确答案:C解析:选择题中,选项C提到了金属键的形成是通过金属原子之间的电子云重叠,符合金属键的定义。
d) 正确答案:A解析:选择题中,选项A提到了氢键的形成是通过氢原子与高电负性原子之间的吸引力,符合氢键的定义。
2. 填空题a) 正确答案:共价键解析:填空题中,根据问题描述,两个非金属原子之间的键称为共价键。
b) 正确答案:离子键解析:填空题中,根据问题描述,一个金属原子将电子转移到一个非金属原子上形成的键称为离子键。
c) 正确答案:金属键解析:填空题中,根据问题描述,金属原子之间的电子云重叠形成的键称为金属键。
d) 正确答案:氢键解析:填空题中,根据问题描述,氢原子与高电负性原子之间的吸引力形成的键称为氢键。
二、有机化学1. 选择题a) 正确答案:C解析:选择题中,选项C提到了烷烃是由碳和氢组成的,符合烷烃的定义。
b) 正确答案:D解析:选择题中,选项D提到了烯烃是由含有一个或多个双键的碳原子组成的,符合烯烃的定义。
c) 正确答案:B解析:选择题中,选项B提到了炔烃是由含有一个或多个三键的碳原子组成的,符合炔烃的定义。
d) 正确答案:A解析:选择题中,选项A提到了芳香烃是由芳香环结构组成的,符合芳香烃的定义。
2. 填空题a) 正确答案:醇解析:填空题中,根据问题描述,含有羟基(-OH)的有机化合物称为醇。
b) 正确答案:醚解析:填空题中,根据问题描述,含有氧原子连接两个碳原子的有机化合物称为醚。
c) 正确答案:酮解析:填空题中,根据问题描述,含有羰基(C=O)的有机化合物称为酮。
d) 正确答案:酯解析:填空题中,根据问题描述,含有羧基(-COO)的有机化合物称为酯。
第二章 分子结构 习题答案

2、 结合Cl 2的形成,说明共价键形成的条件。
共价键为什么有饱和性?共价键形成的条件:原子中必须有单电子,而且成单电子的自旋方向必须相反。
共价键有饱和性是因为:一个原子的一个成单电子只能与另一个成单电子配对,形成一个共价单键。
一个原子有几个成单电子便与几个自旋相反的成单电子配对成键。
电子配对后,便不再具有成单电子了,若再有单电子与之靠近,也不能成键了。
例如:每一个Cl 原子有一个带有单电子的p 轨道,相互以头碰头的形式重叠可以形成共价单键,且只能形成一个单键。
3、 画出下列化合物分子的结构式并指出何者是σ键,何者是π键,何者是配位键。
H HHΖ?δδσσσPN I I IΖ?δδσσσN N N H H H H σσσσσ膦PH 3, 三碘化氮NI 3 肼N 2H 4(N —H 单键)c C c H H HH σσσσσπ N NN O O o O H σσσσσππππ,乙烯, 四氧化二氮(有双键)。
4.PCl 3的空间构型是三角锥形,键角略小于109︒28',SiCl 4是四面体形,键角为109︒28',试用杂化轨道理论加以说明。
杂化轨道理论认为,在形成PCl 3分子时,磷原子的一个3s 轨道和三个 3p 轨道采取sp 3杂化。
在四个sp 3杂化轨道中,有一个杂化轨道被一对孤电子对所占据,剩下的三个杂化轨道为三个成单电子占据,占据一个sp 3杂化轨道的一对孤电子对,由于它不参加成键作用,电子云较密集于磷原子的周围,因此孤电子对对成键电子所占据的杂化轨道有排斥作用,为不等性杂化,所以键角略小于109°28′。
而在SiCl 4分子中,为等性杂化,没有不参加成键的孤电子对,四个杂化轨道都为四个成单电子占据,不存在孤电子对对成键电子对所占据杂化轨道的排斥作用,所以键角为109°28′。
5. 判断下列物种的几何构型,并指出中心原子采取何种杂化方式。
(1) AsF 4- (2) XeOF 3+ (3) SF 5+ (4) Cl 2CO(5) HO 2- (6) HNO 3 (7) I 3+ (8) I 3-分子式 杂化方式 电子对构型 分子构型AsF 4-sp 3d三角双锥四角锥XeOF 3+ sp 3d 三角双锥四角锥SF 5+sp 3d三角双锥三角双锥Cl 2COsp 2平面正三角形C OClCl平面三角形HO 2- sp 3 角形O OHHNO 3 sp 2 平面正三角形N OOOH平面三角形I 3+ sp 3 四面体 角形I 3- sp 3d三角双锥 直线形6、 试用价层电子对互斥理论写出下列各分子的分子构型,并用杂化轨道理论加以说明。
分子结构习题及答案

分子结构习题及答案第四章分子结构习题1.是非判断题1-1化学键是相邻原子与原子(或离子与离子)之间的强烈相互作用。
1-2 50Sn2+是18+2电子构型,50Sn4+是18电子构型。
1-3 Al3+,Ba2+,Si(IV)的电子构型都属于8电子构型。
1-4具有未成对电子的两个原子相互接近时可以形成稳定的共价键。
1-5原子形成共价键的数目等于基态原子的未成对电子数。
1-6σ键的特点是原子轨道沿键轴方向重叠,重叠部分沿键轴呈圆柱形对称。
1-7一般来说,σ键的键能比π键键能小。
1-8 s电子与s电子配对形成的键一定是σ键,p电子与p电子配对形成的键一定为π键。
1-9两个σ键组成一个双键。
1-10键的强度与键长无关。
1-11所有非金属元素之间形成的化合物都不是离子化合物。
1-12μ=0的分子,其化学键一定是非极性键。
1-13共价键具有饱和性的原因在于每个原子提供一定数目的自旋方向相反的未成对电子。
1-14原子核外有几个未成对电子,就能形成几个共价键。
1-15共价键类型可以分为σ键和π键,π键的键能小于σ键的键能,因此π键的稳定性弱于σ键。
1-16烷烃分子中C-H键的键能为413 KJ·mol-1,因此提供413KJ·mol-1的能量能使甲烷和乙烷分子中C-H键断裂。
1-17沿键轴方向的s轨道和p轨道进行重叠可形成π键。
1-18原子轨道相互重叠应满足最大重叠原理,所以沿键轴以“头碰头”方式才能成键。
1-19原子轨道之所以要发生杂化是因为能增大成键能力。
1-20 sp3杂化是,s轨道的主量子数和p轨道的主量子数可以是不同的,也可以是相同的。
1-21 1个s轨道和3个p轨道,形成1个sp3杂化轨道。
1-22在sp,sp2,sp3杂化中,杂化轨道的成键能力随s轨道成分增多而增强。
1-23发生轨道杂化的原子轨道可以具有成对电子。
1-24原子轨道发生杂化,若轨道上有孤对电子存在,这类杂化是不等性的。
10 分子结构习题解答0

10 分子结构4510 分子结构习题解答(p309-311)1. 答案:DB BABBDDC2. 在下列各题的横线处填上正确的文字,符号或数值(1) 极性分子间的取向力由__偶极作用_产生,诱导力由__诱导偶极作用__产生。
色散力由瞬时偶极作用产生。
一般分子间力多以色散力为主。
(2)分子中的电子在分子轨道中的排布应遵循_能量最低原理_、Pauli不相容原理、Hund规则三规则。
对 2p轨道来说是__2___重简并的。
(3) HI分子间的作用力有_色散力、取向力和诱导力_,其中主要的作用力是色散力。
(4) 在HF分子中,分子轨道的类型有__3σ__、____1π____和____4σ____轨道。
通常_____1π___轨道与相应的原子轨道能量相等或相近。
(5) SO2的极化率比O3的____大____,C3H8比C2H6的极化率_____大___。
(6) A、B两元素同属第三周期,A单质在常温下为气体,B元素的原子序数比A 少3,A、B两元素形成的常见化合物分子式为__SiCl4___,其中心原子采用的杂化轨道是__sp3__,分子的空间构型为__正四面体_A、B原子间成键所用的轨道是_sp3-p__。
(7) 根据价层电子对互斥理论,确定下列分子或离子的几何形状:SO42-为__正四面体形__,PO43-为_正四面体形_,XeO4为_正四面体形_,XeO3为___三角锥形___。
(8) 按照杂化轨道理论,原子轨道发生等性杂化时,原子轨道的形状、_大小、伸展方向等_都发生改变。
形成的杂化轨道能量(或成键能力)相等。
(9) SCl2的空间构型为_角形_,中心原子采用__不等性sp3__杂化方式,有__2___对孤对电子,分子偶极矩__不等于_零。
(10) 对于下列分子的有关性质:A. NH3分子的空间构型;B. CH4分子中H-C-H的键角;C. O2分子的磁性;D. H2O分子的极性;可以用杂化轨道理论予以说明的有__A B D_,不能用杂化轨道理论说明的有_C_。
大学化学分子结构习题带答案

1.离子晶体中的化学键都是离子键。
()1.错2.CO 分子含有配位键。
()2.对3.所有分子的共价键都具有饱和性与方向性,而离子键没有饱和性与方向性。
()3.错4. 中心原子所形成的杂化轨道数等于参加杂化的原子轨道数。
()4.对5. 原子轨道发生杂化后可以增强成键能力。
()5.对6. 杂化轨道具有能量相等、空间伸展方向一定的特征。
()6.对7. 凡是中心原子采取sp3杂化轨道成键的分子,其空间构型都是正四面体。
()7.错8. 在任何情况下,每一个sp2杂化轨道所含的s、p成分均相同。
()8.错9. 由分子轨道理论可推知 O2-、O22-都比 O2稳定。
()9.错10. 按照分子轨道理论,N2+和 N2-的键级相等。
()10.对11. 色散力存在于一切分子之间。
()11.对12. 弱极性分子之间的分子间力均以色散力为主。
()12.对13. 氢键只存在于 NH3、H2O、HF 的分子之间,其它分子间不存在氢键。
()13.错14. 根据价层电子对互斥理论,分子或离子的空间构型取决于中心原子的价层电子对数。
()14.对15. 对 AB m型分子 ( 或离子 ) 来说,当中心原子 A 的价电子对数为 m 时,分子的空间构型与电子对在空间的构型一致。
()15.对16. AsF5是三角双锥形分子。
()16.错17. SO42-、ClO4-、PO43-的空间构型相同。
()17.对18. 下列化合物中既有离子键又有共价键和配位键的是()。
18.D(A) KF; (B) H2SO4; (C) CuCl2; (D) NH4NO3。
19. 关于离子键的本性,下列叙述中正确的是()。
19.D(A) 主要是由于原子轨道的重叠; (B) 由一个原子提供成对共用电子;(C) 两个离子之间瞬时偶极的相互作用; (D) 正、负离子之间的静电吸引为主的作用力。
20. 下列各组卤化物中,离子键成分大小顺序正确的是()。
20.A(A) CsF > RbCl > KBr > NaI;(B) CsF > RbBr > KCl > NaF;(C) RbBr > CsI > NaF > KCl;(D) KCl > NaF > CsI > RbBr。
大学化学分子结构、配合物习题及答案

一.分子结构6.(本题 2分) 4039下列各组离子中,离子的极化力最强的是 ( )(A) K+,Li+ (B) Ca2 +,Mg2 + (C) Fe3+,Ti4+ (D) Sc3+,Y3+6.(4039) (C)8.(本题 2分) 1075比较下列各组物质的熔点,正确的是- ( )(A) NaCl > NaF (B) CCl4> CBr4 (C) H2S > H2Te (D) FeCl3< FeCl28.(1075) (D)8.(本题 2分) 1075比较下列各组物质的熔点,正确的是- ( )(A) NaCl > NaF (B) CCl4> CBr4 (C) H2S > H2Te (D) FeCl3< FeCl28.(1075) (D)9.(本题 2分) 4018下列有关离子变形性的说法中,不正确的是 ( )(A) 外层 8 电子构型的离子的变形性小于其他电子构型的离子(B) 同一元素不同价态的负离子中,所带电荷越多变形性越小(C) 同种原子形成的阴离子比阳离子变形性大(D) 离子半径大,则变形性大(其他条件相同)9.(4018) (B)10.(本题 2分) 4019下列物质中,既有离子键又有共价键的是 ( )(A) KCl (B) CO (C) Na2SO4 (D) NH10.(4019) (C)11.(本题 2分) 4027试判断下列说法,正确的是 ( )(A) 离子键和共价键相比,作用范围更大(B) 所有高熔点物质都是离子型的(C) 离子型固体的饱和水溶液都是导电性极其良好的(D) 阴离子总是比阳离子大11.(4027) (A)12.(本题 1分) 4028下列物质中,既有离子键,又有共价键的是 ( )(A) AlCl3 (B) SiC (C) CaC2 (D) BN12.(4028) (C)15.(本题 2分) 4038试判断下列说法,正确的是 ( )(A) ⅠA,ⅡA,ⅢA族金属的 M3+阳离子的价电子都是 8 电子构型(B) ds区元素形成 M+和 M2 +阳离子的价电子是 18+2 电子构型(C) ⅣA族元素形成的 M2 +阳离子是 18 电子构型(D) d区过渡金属低价阳离子(+1,+2,+3)是 9~17 电子构型15.(4038) (D)填空:3.(本题 2分) 4020按从大到小的顺序排列以下各组物质 :(A) 按离子极化大小排列MnCl2,ZnCl2,NaCl,CaCl2 _____________________________________________________________________________________________;(B)按键的极性大小排列NaCl,HCl,Cl2,HI____________________________________________________________________________________________________。
无机化学练习题(含答案)第二章 分子结构

第二章分子结构2-1:区分下列概念:(1) 共价键和离子键;(2) 共价键和配位键;(3) 极性共价键和非极性共价键;(4) 金属导电和离子导电;(5) σ键和π键;(6) d2sp3杂化轨道和sp3d2杂化轨道;(7) 价键理论和分子轨道理论;(8) 成键分子轨道和反键分子轨道;(9) 定域键和离域键;(10) 导带、价带和禁带;答:(1)离子键:正离子和负离子之间的静电作用力;共价键:原子和原子之间轨道重叠的程度(共用电子对)。
(2)共价键和配位键:是共价键理论中的一对概念,后者又叫配位共价键。
前者的成键原子各自提供1个电子形成共用电子对;后者的共用电子对由成键原子的一方提供。
(3)极性共价键和非极性共价键:是共价键理论中的一对概念。
前者共用电子对偏向两个键原子中的一个;后者共用电子对同等程度地属于两个成键原子。
(4)金属导电和离子导电:前者是自由电子导电;后者通过正、负离子在溶液或熔体中运动导电。
(5)σ键和π键:是共价键理论中的一对概念。
前者重叠轨道的电子云密度绕键轴对称;后者重叠轨道的电子云密度绕键轴不完全对称。
(6)d2sp3杂化轨道:两条(n-1)d 轨道、一条ns 轨道和三条np 轨道杂化而得的轨杂化轨道: 一条ns 轨道、三条np 轨道和两条nd 轨道杂化而得的轨道。
(7)价键理论和分子轨道理论:它们是描述共价键的两种理论。
前者用原子轨道重叠的概念解释共价键的形成,将共价作用力的实质解释为核间较大的电子密度对两核的吸引力。
后者将分子看作一个整体,原则上不再承认分子中各原子原子轨道的个性,将共价键的形成归因于电子获得更大运动空间而导致的能量下降。
(8)成键分子轨道和反键分子轨道:这是分子轨道理论中的一对概念。
前者的能级低于成键原子原子轨道的能级;而后者恰相反。
成键轨道上的电子将核吸引在一起;反键轨道上的电子不但不能提供这种吸引力,而且使两核相互排斥。
(9)定域键和离域键:前者的成键电子属于两个成键原子,例如,H2O 分子中的两个O-H 键;后者的成键电子不属于某一两个特定的成键原子,例如金属中的自由电子都是成键电子,却不能将其分别归属于特定的金属离子。
北师大无机化学四版习题答案10分子结构

第10章 分子结构10.1 画出O 2、H 2O 2、CO 、CO 2、NCl 3、SF 4的路易斯结构式。
不要忘记标出孤对电子和分子的总电子数!解:O=OHO O HCOCOO12e 14e 10e 16eClN ClClFFF26e 34e评注:各种教科书对路易斯结构式的定义不尽相同。
涉及:( l )路易斯结构式是否一定要给出分子的立体结构?可以不涉及。
能表达更好。
(2 ) 路易斯结构式是否给出分子的全部电子?在有机化学中常不给出,但对初学者以给出为好。
(3) 路易斯结构式表达O2的结构时要不要给出三电子键?不必。
氧分子的三电子键属于分子轨道的理论表达,路易斯结构式一般不涉及分子轨道理论。
(4 ) 一氧化碳的路易斯结构式要不要给出配价键?最好给。
因此上面的CO 结构式最好写成:10.2 画出硫酸根各共振体的结构式。
SO OO OSOOOOSOOO OSOOO OSOOOOS OO O SOO OOSOO OOSOOO评注:SO 42-离子有32 个价电子,即16 对电子,因此,只要给出16 对电子,而且氧原子周围的电子数不超过8 的路易斯结构式都可以认为是硫酸根的共振结构式。
上列任一共振结构式并不能正确给出硫酸根的真实结构。
在有的教科书中用如下之一表达硫酸根的结构式:S O O OO2-2-也有的教科书将所有硫和氧原子之间的被都画成S 指向氧原子的箭头。
应当注意到的事实是,硫酸根中硫原子和氧原子之间的化学键明显具有双键的性质,用单键表达,是明显偏离事实的。
从形式电荷的角度,上面的两根双键的路易斯结构式的硫原子和两个氧原子都是零,另外两个氧原子因获得外加的电子而呈-1,是最合理的,而四根单键的结构式,形式电荷为S +2 ,O -1 ,也是可以成立的。
这是路易斯结构式不能克服的内在矛盾。
10.3 σ键可由s -s 、s -p 和p -p 原子轨道“头碰头”重叠构建而成,试讨论LiH (气态分子)、HCl 、Cl 2分子里的σ键分别属于哪一种?答:LiH 是s -s σ键:HCl 是s -p σ键;Cl 2是p -p σ键。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
(二)分子结构答案一.(5分)铋的化合物丰富多彩。
在液态SO 2中,AsF 5或其他五氟化物能氧化铋,其中能生成化合物A 。
经分析,A 为离子化合物,阳离子为多个铋原子组成的三角双锥型原子簇,阴离子为正八面体结构。
已知A 的阳离子中铋原子全部为8电子结构。
1.试确定A 的结构简式;2.写出生成A 的化学反应方程式。
答案:1.A :Bi 5(AsF 6)3(3分);2.10Bi +9AsF 5=2Bi 5(AsF 6)3+3AsF 3(2分)。
二.(7分)1.H 2O 的沸点(100℃)比HF 的沸点(20℃)高,为什么?2.气态氯原子与一个电子结合比气态氟原子与一个电子结合放出更多的能量,为什么? 3.Li 3V 2(PO 4)3是一种新型的锂离子正极材料。
其阴离子是由2种多面体组合而成的三维网状结构。
请具体指出其阴离子中各原子的连接形式。
答案:1.每个水分子平均最多可形成2个氢键,每个HF 分子平均最多生成1个氢键。
前者氢键数目多,总键能较大,故沸点较高。
(2分)2.氟原子半径小,外层孤对电子多,电子云密度大,电子间斥力大,使得氟原子结合一个电子形成气态F -时放出能量较少。
(2分)3.PO 4四面体、VO 6八面体通过共用顶点氧原子而组成三维骨架结构,每个VO 6八面体周围有6个PO 4四面体,而每个PO 4四面体周围有4个VO 6八面体。
(3分) 三.(7分)在液态SO 2中用叠氮酸铯与氰气反应定量生成铯的离子化合物。
其阴离子中含氮量为74.47%。
1.试画出该离子化合物中阴离子的结构式;2.说明每个原子的杂化类型和化学键型。
答案:1.(4分)2.环中的N 原子和C 原子分别采取sp 2杂化,端连的C 、N 原子分别采取sp 杂化。
键型有各原子之间的σ键和一个π键、一个π87(或者一个π65和二个π键)(3分)四.(12分)1999年美国化学家曾合成出一种能量极高、氧化性极强的白色固体盐X 。
盐X 的制备方法如下:氟化物A 与五氟化砷化合得到离子化合物B ,将B 盐放在干燥管中,装进特殊材料做成的细颈瓶中,于-196℃时通过金属真空管加入无水HF ,混合加热到室温,使B 盐溶解,细颈瓶一端与玻璃管相连,降温至-196℃后加入酸C ,反复升温(-78℃)、降温(-196℃),生成的HF 气体挥发出来,并带走大量的热,最终得到盐X 。
已知:①A 是共价分子,具有顺反异构体;②B 盐存在两种不同的氟原子。
③盐X 与盐B 具有相同的阴离子构型;④C 的阴离子为直线型,而X 的阳离子为V 型;⑤X 的含氟量为44%。
试根据上述信息,回答下列问题:1.画出A 分子和B 的阴阳离子的结构式。
2.分别写出制备B 、X 盐的化学方程式。
3.对于制备高能量的物质,一般采用低温,并能在低温下提供良好的溶解性的反应介质。
本实验中采用无水HF ,能吸收反应后放出的能量,并能对高度敏感性的物质起稳定作用。
请问:无水HF 为什么具备上述特点?4.化学家Chrite 随后成功地分离出了A 盐的阳离子。
请画出该阳离子的电子式,并预测其用途。
5.盐X 对水具有高度敏感性,能检出极其微量的水。
盐A 与水剧烈化合,并能发生强烈爆炸。
请写出该爆炸反应的化学方程式。
答案:1.(各1分)2.N2F2+AsF5=[N2F][AsF6] [N2F][AsF6]+HN3=[N5][AsF6]+HF(各1分)3.因为HF具有大偶极矩、低熔点(-80℃)和挥发性等特点(1.5分)4.[]+或(1分)具有极高的能量,用于“盐料炸弹”(1.5分)5.4N5[AsF6]+2H2O=4HF+4AsF5+10N2↑+O2↑(2分)五.(8分)2-吡啶酮(结构简式如右)是一种可以与自身互补的分子,在晶体或溶液中,它以氢键连接的二聚体形式存在。
若用乙炔基(-C≡C-)将两个2-吡啶酮连接有两种方式:(a)3、6位连接和(b)6,6位连接。
Wuest研究了(a)和(b)的聚集行为,在质子溶剂中(a)和(b)都以单体形式存在;在非质子溶剂中(a)以二聚体形式(c)存在,即使浓度很高时,(b)仍以单体形式存在。
在本体状态下,(a)形成分散的二聚体(c),(b)形成了平面的线性超分子聚合物(d),(d)有两种典型的空间构型。
1.指出2-吡啶分子中所成π键的情况;2.写出2-吡啶酮二聚体的结构简式;3.写出a、b的结构简式;4.画出二聚体(c)的结构简式;5.画出表示聚合物(d)的两种结构片段。
(1分)答案:1.π872.(1.5分)3.a:b:(各1分)4.(1.5分)5.(各1分)六.(15分)在铜的催化作用下氨和氟反应得到一种铵盐和一种三角锥体分子A(键角102°,偶极矩0.78×10-30C·m;对比:氨的键角107.3°,偶极矩4.74×10-30C·m);1.写出A的分子式和它的合成反应的化学方程式。
2.A分子质子化放出的热明显小于氨分子质子化放出的热。
为什么?3.A与汞共热,得到一种汞盐和一对互为异构体的B和C(相对分子质量66)。
写出化学方程式及B和C的立体结构。
4.B与四氟化锡反应首先得到平面构型的D和负二价单中心阴离子E构成的离子化合物;这种离子化合物受热放出C,同时得到D和负一价单中心阴离子F构成的离子化合物。
画出D、E、F的立体结构;写出得到它们的化学方程式。
5.A与F2、BF3反应得到一种四氟硼酸盐,它的阳离子水解能定量地生成A和HF,而同时得到的O2和H2O2的量却因反应条件不同而不同。
写出这个阳离子的化学式和它的合成反应的化学方程式,并用化学方程式和必要的推断对它的水解反应产物作出解释。
答案:1.NF3(1分)4NH3+3F2=NF3+3NH4F(1分)(共2分)2.N-F键的偶极方向与氮原子孤对电子的偶极方向相反,导致分子偶极矩很小,因此质子化能力远比氨质子化能力小。
画图说明也可(如:)(1分)3.2NF3+2Hg=N2F2+2HgF2(1分)(14+19)×2=66(每式1分)(共3分)4.D:E:F:(每式1分)2N2F2+SnF4=[N2F+]2[SnF6]2-(1分)[N2F+]2[SnF6]2-=[N2F]+[SnF5]-+N2F2(1分)(共5分)5.阳离子的化学式为NF4+。
(1分)NF3+F2+BF3=NF4+BF4-(1分)NF4+水解反应首先得到HOF(否则写不出配平的NF4+水解反应):NF4++H2O=NF3+HOF+H+定量生成NF3。
(1分)而反应2HOF=2HF+O2和反应HOF+H2O=HF+H2O2哪一反应为主与反应条件有关,但无论哪一反应为主却总是定量生成HF。
(1分)(共4分)七.(13分)1.为什么CsBrCl2热分解的反应是CrBrCl2=CsCl+BrCl,而不是CrBrCl=CsBr+Cl2?2.液体BrF5和AsF5都不是良导体,为什么两者混合后却成为导体?3.对下面测定的N、P的氢化物和氟化物的键角的各种相互差异作出解释。
NH3:107°PH3:102°NF3:93°PF3:104°4.比较化合物熔沸点高低并说明理由。
①CH3CH2OH和CH3OCH3②O3和SO2③HgCl2和HgI2④和答案:1.因为前一个反应生成CsCl的晶格能比CsBr的大,而且另一个产物BrCl是极性分子,它的键能除了轨道重叠而形成的共价键外,还附加一定成分的离子键。
(2分)2.BrF5和AsF5混合后发生如下反应:BrF5+AsF5→[BrF4]+[AsF6]-。
因反应所得产物为离子型化合物,故导电能力明显增加。
(2分)3.NH3107°、PH3102°两者键角不同的原因是NH3中N-H键的键长比PH3中P-H键的键长要短,所以在NH3中,成键电子对更靠近,排斥力更大,以致键角更大。
而NF393°、PF3 104°两者键角不同的原因是F上有孤对电子对,而P原子有空的3d轨道,可形成弱的反馈键,即F原子的孤对电子向P原子转移,以致键角变大。
或者可理解为形成了反馈键后,键级增大了,相当于有了双键的成分。
成键电子对之间的排斥力增大。
(3分)4.①CH3CH2OH>CH3OCH3:CH3CH3OH可形成分子间氢键,而CH3OCH3则不能,故CH3CH2OH熔沸点高。
②O3<SO2:O3为同种元素的原子形成的分子,极性较弱,而SO2分子的极性较强,其次O3分子的直径要小于SO2分子,因此O3分子间的色散力小于SO2分子间的色散力。
③HgCl2>HgI2:Hg2+半径大,变形性大,同时又有较强的极化能力。
阴离子半径Cl-I-,变形性Cl-I-。
因此,Hg2+和I-间有较强的附加极化作用,而Hg2+和I-间的极化作用较弱。
④<:两个混合物都可以形成氢键,但前者因取代基在邻位,有分子内氢键,熔沸点较低;后者只能形成分子间氢键,故溶沸点较高。
(各1.5分)八.(10分)由短周期两种元素组成的A气体通入到AsF5中,生成一种共价型离子化合物B、化合物C和一种氧化性气体D。
已知B的阴离子为正八面体构型,阳离子与O3是等电子体,在某非水溶剂中做电导实验,其电导性与NaCl相同。
化合物D呈四面体结构,可由AsF3与臭氧(等物质的量)反应制得,红外光谱显示,J中有一个AsF3没有的吸收。
1.试写出A、B、C、D的化学式;2.写出制备B和C的化学反应方程式;3.写出气体A与NH3反应的化学方程式。
答案:1.A:Cl2O(2分);B:[ClO2][AsF6](2分);J:OAsF3(1分);K:Cl2(1分)2.5Cl2O+3AsF5=2[ClO2][AsF6]+OAsF3+4Cl2AsF3+O3=OAsF3+O2(各1分)3.3Cl2O+10NH3=6NH4Cl+2N2+3H2O(2分)九.(6分)某短周期元素A,其最外层电子数是所在周期数的2倍,它的氢化物和氧化物能发生反应生成A的单质。
已知AF6是一种无色无味无毒的气体,具有很强的稳定性,可用作高压发电机的优良绝缘体。
AF6的分子结构如右图所示。
⑴A元素原子的电子排布式为。
⑵AF6分子的空间构型为型。
⑶如果F元素有两种稳定的同位素,则AF6有种同分异构体。
答案:(6分,每空2分)⑴1s22s22p63s23p4⑵正八面体⑶10十.(16分)某离子化合物X由一种有机阳离子和一种无机阴离子组成;元素分析得到H:5.33%、C:21.17%、N:6.17%、S:35.33%、Ge:32.00%;该阳离子和阴离子都具有正四面体型的空间对称性。
1.确定X的组成式(阴阳离子分开写);2.画出阴离子的空间构型;一定条件下X能与HgI2反应,通过自组装合成了微孔硫化物Y;Y的阴离子是通过X 的阴离子和HgS4变形四面体共用S形成的无限网状结构。
