蛋白质免疫印迹实验(Western Blot
免疫印迹实验注意事项

免疫印迹实验注意事项一、实验概述免疫印迹(Western blot)是一种重要的蛋白质检测技术,在生物医学研究中被广泛应用。
该实验通过将蛋白质样品经电泳分离,并将其转移到膜上,最终使用特异性抗体探测目标蛋白质。
然而,为了确保实验结果的准确性和可靠性,实验过程中需要注意以下事项。
二、实验仪器和试剂准备在进行免疫印迹实验之前,需要准备合适的仪器和试剂。
以下是一些注意事项:1. 仪器准备•确保电泳仪、转印仪和成像仪等仪器的功能正常,并进行必要的校准和测试。
•清洁仪器,避免污染和干扰实验结果。
2. 试剂准备•使用优质的试剂,并根据说明书正确配制试剂溶液。
•为避免批次差异,建议每次实验使用同一批试剂。
•试剂保存在适当的温度和条件下,以保证其稳定性。
3. 溶液准备•使用无菌、纯净的水和试剂配制实验所需的溶液。
•确保溶液的 pH 值正确,并进行必要的调整。
•溶液保存在适当的温度和条件下,避免污染和变质。
三、实验操作注意事项在进行免疫印迹实验时,需要注意以下操作事项:1. 样品处理•样品的制备和处理应严格按照实验要求进行,以确保样品的完整性和稳定性。
•样品处理过程中应尽量避免使用可能影响蛋白质结构和功能的试剂和条件。
2. 蛋白质的电泳分离•样品电泳前,必须对电泳胶进行适当的处理和准备,确保其质量和性能。
•样品电泳条件的选择要考虑样品性质和目标蛋白质的分子量等因素。
•电泳过程中,要严格控制电流和电压,避免产生异常结果。
3. 转膜过程•使用合适的滤纸和膜材料,并按照正确的方法和条件进行转膜操作。
•转膜时间和电压的选择要根据蛋白质的分子量和转膜效率进行调整。
4. 抗体探测和成像•使用具有较高亲和力和特异性的抗体进行探测,以提高结果的准确性和可靠性。
•抗体的浓度和反应时间应根据需要进行调整,避免产生过度或不足的信号。
•成像过程中,要确保暗室环境的光线充足、胶片或成像仪的参数设置正确。
5. 数据分析和结果解读•在进行数据分析和结果解读时,应使用合适的软件和方法,确保结果的准确性和可靠性。
蛋白质免疫印迹杂交实验 -

蛋白质免疫印迹杂交实验实验目的:1. 了解制备中抗原与抗体杂交显色的原理2. 初步掌握蛋白质印迹杂交实验的操作方法3. 观察和分析着色后的蛋白质的特点和含量实验原理:蛋白质印迹法(Western Blot)是一种蛋白质学中常用的检测方法,是将蛋白质从聚丙烯酰胺凝胶转移到固相载体上,再用探测反应和底物着色,从而检测在所分析的细胞或组织中目的基因表达的蛋白质情况。
大致过程:Western Blot法采用的是聚丙烯酰胺凝胶电泳,被检测物是蛋白质,“探针”是抗体,“显色”用标记的二抗。
经过PAGE(聚丙烯酰胺凝胶电泳)分离的蛋白质样品,转移到固相载体(例如硝酸纤维素薄膜)上,固相载体以非共价键形式吸附蛋白质,且能保持电泳分离的多肽类型及其生物学活性不变。
以固相载体上的蛋白质或多肽作为抗原,与对应的抗体起免疫反应,再与酶或同位素标记的第二抗体起反应,经过底物显色或放射自显影以检测电泳分离的特异性目的基因表达的蛋白成分。
实验材料:1.配置SDS-PAGE凝胶相关材料及各种缓冲溶液2.蛋白质样品:可以使用适当的裂解液,裂解细胞获得。
测定每个蛋白质样品浓度?实验步骤:蛋白质印迹法主要分三个阶段进行1、SDS聚丙烯酰胺凝胶电泳(SDS-PAGE)2、电转移,又称为转膜3、酶联免疫显色检测第一阶段:在这个阶段,经过变性处理的蛋白质样品经SDS处理后会带上阴性电荷,在聚丙烯酰胺凝胶中在电场的作用下从阴极向阳极泳动,且分子量越小,泳动速度就越快。
所以在此阶段,根据蛋白的泳动速度可以将样品中的蛋白质根据其分子量的大小进行分离,此阶段分离效果肉眼不可见。
如果想观察蛋白的电泳情况,可以在电泳完成后进行考马斯亮蓝染色进行观察。
第二阶段:即将在凝胶中已经分离的蛋白质条带通过电场的作用转移至硝酸纤维素膜上, 一般选用恒流300 mA,通电90 min即可将凝胶中的用恒流300 mA,通电90 min即可将凝胶中的蛋白条带转移到醋酸纤维素膜载体上。
蛋白质印迹分析(WesternBlotAnalysis)

蛋⽩质印迹分析(WesternBlotAnalysis)【实验⽬的】了解蛋⽩质印迹法的基本原理及其操作和应⽤。
【实验原理】蛋⽩质印迹法⼜称为免疫印迹法,这是⼀种可以检测固定在固相载体上蛋⽩质的免疫化学技术⽅法。
待测蛋⽩既可以是粗提物也可以经过⼀定的分离和纯化,另外这项技术的应⽤需要利⽤待测蛋⽩的单克隆或多克隆抗体进⾏识别。
如图所⽰,可溶性抗原,也就是待测蛋⽩⾸先要根据其性质,如分⼦量,分⼦⼤⼩,电荷以及其等电点等采⽤不同的电泳⽅法进⾏分离;通过电流将凝胶中的蛋⽩质转移到聚偏⼆氟⼄烯膜上;利⽤抗体(⼀抗)与抗原发⽣特异性结合的原理,以抗体作为探针钓取⽬的蛋⽩。
值得注意的是在加⼊⼀抗前应⾸先加⼊⾮特异性蛋⽩,如⽜⾎清⽩蛋⽩对膜进⾏“封阻”⽽防⽌抗体与膜的⾮特异性结合。
经电泳分离后的蛋⽩往往需再利⽤电泳⽅法将蛋⽩质转移到固相载体上,我们把这个过程称为电泳印迹。
常⽤的两种电转移⽅法分别为:1.半⼲法: 凝胶和固相载体被夹在⽤缓冲溶液浸湿的滤纸之间,通电时间为10分钟~30分钟。
2.湿法:凝胶和固相载体夹⼼浸放在转移缓冲溶液中,转移时间可从45分钟延长到过夜进⾏。
由于湿法的使⽤弹性更⼤并且没有明显浪费更多的时间和原料,因此我们在这⾥只描述湿法的基本操作过程。
对于⽬的蛋⽩的识别需要采⽤能够识别⼀抗的第⼆抗体。
该抗体往往是购买的成品,已经被结合或标记了特定的试剂,如辣根过氧化物酶。
这种标记是利⽤辣根过氧化物酶所催化的⼀个⽐⾊反应,该反应的产物有特定的颜⾊且固定在固相载体上,容易鉴别。
因此可通过对⼆抗的识别⽽识别⼀抗,进⽽判断出⽬标蛋⽩所在的位置。
其他的识别系统包括碱性磷酸酶系统和125I标记系统。
蛋白质免疫印迹(Western Blot )实验步骤和原理及注意事项

蛋白质免疫印迹(Western Blot )实验步骤和原理及注意事项1.收集蛋白样品(Protein sample preparation)可以使用适当的裂解液。
收集完蛋白样品后,为确保每个蛋白样品的上样量一致,需要测定每个蛋白样品的蛋白浓度。
根据所使用的裂解液的不同,需要采用适当的蛋白浓度测定方法。
因为不同的蛋白浓度测定方法对于一些去垢剂和还原剂等的兼容性差别很大。
BCA法。
2. 电泳(Electrophoresis)(1) SDS-PAGE凝胶配制(2) 样品处理在收集的蛋白样品中加入适量浓缩的SDS-PAGE蛋白上样缓冲液。
例如2X或5X的SDS-PAGE蛋白上样缓冲液。
使用5X的SDS-PAGE蛋白上样缓冲液可以减小上样体积,在相同体积的上样孔内可以上样更多的蛋白样品。
100℃或沸水浴加热3-5分钟,以充分变性蛋白(根据蛋白分子的大小,煮沸时间可适当变化,一般不低于5min。
煮沸只是变性蛋白,而不是分解,一般加了抑制酶不会分解。
煮沸对于SDS-PAGE凝胶电泳是必须的,只有煮沸,才能消除蛋白质的立体二级结构,伸展为一维线性结构,所以一般来讲二聚体都会解体,才能完全按照分子量跑电泳,加的蛋白Marker才有指示分子量的意义。
蛋白样品变性后与SDS充分结合,SDS使每个氨基酸带相同的电荷,使整个蛋白呈线性结构. 抗体因为要是线性表位结合的,100度煮10min 后13000,离心5分钟,取上清电泳,因为沉淀会导致拖尾.也可以取上清到另一管,4度可以放一周备再次电泳)。
(3)电泳i.清洗玻璃板:一只手扣紧玻璃板,另一只手蘸点洗衣粉轻轻擦洗。
两面都擦洗过后用自来水冲,再用蒸馏水冲洗干净后立在筐里晾干。
ii.灌胶与上样(1)玻璃板对齐后放入夹中卡紧。
然后垂直卡在架子上准备灌胶。
(操作时要使两玻璃对齐,以免漏胶。
)(2)配10%分离胶,加入TEMED后立即摇匀即可灌胶。
灌胶时,可用10 ml枪吸取5 ml胶沿玻璃放出,待胶面升到绿带中间线高度时即可。
Western blot实验步骤

1.9/ 4× 分 离 胶 缓 冲 液 3.61 (mL) 10% 过硫酸氨( L ) 112/
168
TEMED(L) 分离范围(kDa)
5.0/7.5 36-150
3.7/5.5 5 1.9/ 3.61 112/ 168 5.0/7.5
SDS-PAGE 蛋白电泳试剂
1. 丙烯酰胺和甲叉双丙烯酰胺单体溶液(Acr和Bis):
丙烯酰胺30g ,甲叉双丙烯酰胺0.8g,加水100ml ,滤 纸过滤后储存于棕色瓶中,4℃避光保存,pH不得超过 7.0。(光催化或碱催化其发生脱氨基反应)
• 2. 4x分离胶缓冲液 :Tris 18.17g, 10% SDS 4ml, HCl调pH至8.8, 定容到100ml。
• 7.染色液:称取考马斯亮蓝R-250 2.5g,加入
甲醇450ml,冰乙酸100ml、水650ml。
• 8.脱色液 :甲醇100ml,冰乙酸700ml,加水 830ml。 • 9.十二烷基硫酸钠(SDS)溶液:10%(w/v) 1g SDS,10ml去离子水配制,室温保存。
SDS-PAGE 电泳采用 Tris- 甘氨酸系统,即按分子克隆 中Sambrook等的方法(Sambrook, 1989)进行
• PVDF膜( 聚偏二氟乙烯,polyvinylidene fluoride)的预处理 : 在甲醇浸泡10秒湿润膜,转移缓冲液浸泡10-15 分钟,除去甲醇。PVDF是疏水性的,在转膜缓冲 液里很难浸透,甲醇处理后使更容易浸润,且甲 醇处理活化PVDF膜上面的正电基团,使它更容易 跟带负电的蛋白质结合; • PVDF膜是一种高强度、耐腐蚀的物质,PVDF膜 可以结合蛋白质,而且可以结合小片段的蛋白质, 最初是将它用于蛋白质的序列测定,虽然PDVF膜 结合蛋白的效率没有硝酸纤维素膜高,但由于它 的稳定、耐腐蚀使它成为蛋白测序理想的用品;
蛋白质免疫印迹Western Blot

Western Blot实验方法原理Western免疫印迹(Western Blot)是将蛋白质转移到膜上,然后利用抗体进行检测的方法。
对已知表达蛋白,可用相应抗体作为一抗进行检测,对新基因的表达产物,可通过融合部分的抗体检测。
与Southern或Northern杂交方法类似,但Western Blot 采用的是聚丙烯酰胺凝胶电泳,被检测物是蛋白质,“探针”是抗体,“显色”用标记的二抗。
经过PAGE分离的蛋白质样品,转移到固相载体(例如硝酸纤维素薄膜)上,固相载体以非共价键形式吸附蛋白质,且能保持电泳分离的多肽类型及其生物学活性不变。
以固相载体上的蛋白质或多肽作为抗原,与对应的抗体起免疫反应,再与酶或同位素标记的第二抗体起反应,经过底物显色或放射自显影以检测电泳分离的特异性目的基因表达的蛋白成分。
该技术也广泛应用于检测蛋白水平的表达。
实验步骤一、试剂准备1. SDS-PAGE试剂:见聚丙烯酰胺凝胶电泳实验。
2. 匀浆缓冲液:1.0 M Tris-HCl(pH 6.8) 1.0 ml;10%SDS 6.0 ml;β-巯基乙醇0.2 ml;ddH2O 2.8 ml。
3. 转膜缓冲液:甘氨酸2.9 g;Tris 5.8 g;SDS 0.37 g;甲醇200 ml;加ddH2O定容至1000 ml。
4. 0.01 M PBS(pH7.4):NaCl 8.0 g;KCl 0.2 g;Na2HPO4 1.44 g;KH2PO40.24 g;加ddH2O至1000 ml。
5. 膜染色液:考马斯亮兰0.2 g;甲醇80 ml;乙酸2 ml;ddH2O118 ml。
包被液(5%脱脂奶粉,现配):脱脂奶粉1.0 g 溶于20 ml的0.01 M PBS中。
6. 显色液:DAB 6.0 mg;0.01 M PBS 10.0 ml;硫酸镍胺0.1 ml;H202 1.0 μl。
二、蛋白样品制备1. 单层贴壁细胞总蛋白的提取(1)倒掉培养液,并将瓶倒扣在吸水纸上使吸水纸吸干培养液(或将瓶直立放置一会儿使残余培养液流到瓶底然后再用移液器将其吸走)。
WesternBlot蛋白免疫印迹法

3 Western blot3.1试剂配制1)30%聚丙烯酰胺储备液(Acr/Bis):丙烯酰胺(Acr), 29g;N,N-亚甲基双丙烯酰胺(Bis), 1g,去离子水溶解,37℃ 水浴助溶,定容至100mL。
0.45M m滤器过滤,棕色瓶4℃避光保存。
2)10%十二烷基硫酸钠(5口5):SDS,10g;H2O,80mL。
68℃加热溶解,浓HCl 调pH 至7.2,定容至100mL,室温保存。
3)10%过硫酸铵(AP):AP,1g;H2O,10mL。
避光,4℃保存。
(4℃2 周)4)分离胶缓冲液(1.5MTris-HCl pH8.8):Tris,18.17g;H2O 80mL。
用浓HCl 调pH 至8.8,定容至100mL,4℃保存。
5)浓缩胶缓冲液(1.0MTris-HCl pH6.8):Tris,12.11g;H2O 80mL。
用浓HCl 调pH 至 6.8,定容至100mL,4℃保存。
6)电泳缓冲液(10X):甘氨酸(Glycine),188g;Tris 30.2g;SDS,10g;H2O, 800mL。
调节pH 至8.3, 定容至1L,4℃保存(用时稀释为1义)。
7)5X SDS-PAGEloadingBuffer (5mL):1MTris-HCl(pH6.8),1.25mL;SDS,0.5g;澳酚蓝(BPB),25mg;甘油,2.5mL;加去离子水定容至5mL。
充分混匀,分装成500M L/份,室温保存。
使用前每份加入25M L p -巯基乙醇(2-ME),加入2-ME的loading buffer可在室温下保存一个月左右。
8)考马斯亮蓝染色固定液:40%双蒸水,10%醋酸,50%甲醇,室温保存9)考马斯亮蓝染色液:考马斯亮蓝R-250,250mg;甲醇,45ml;冰醋酸,10ml;H2O,定容至100ml。
室温保存。
10)考马斯亮蓝染色脱色液:醋酸,100ml;乙醇,50ml;dH2O 850ml,充分混合,室温保存11)膜转移缓冲液:甘氨酸,2.9g;Tris,5.8g;SDS,0.37g;力口H2O 600mL 充分溶解,加200mL 甲醇,混匀,定容至1匕,室温保存。
蛋白质免疫印迹实验
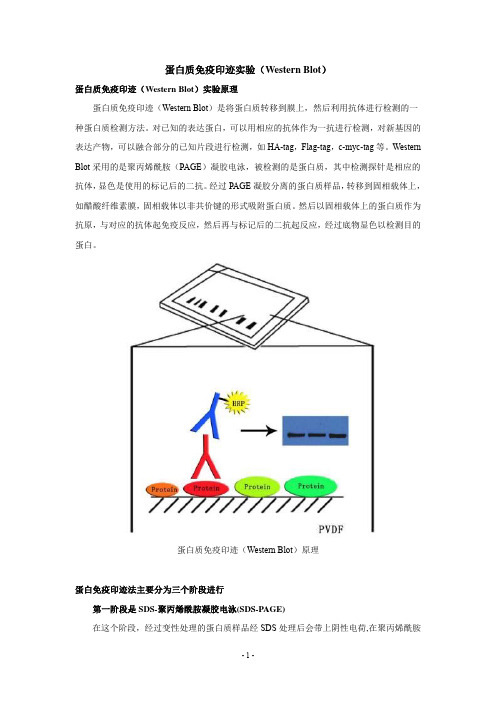
蛋白质免疫印迹实验(Western Blot)蛋白质免疫印迹(Western Blot)实验原理蛋白质免疫印迹(Western Blot)是将蛋白质转移到膜上,然后利用抗体进行检测的一种蛋白质检测方法。
对已知的表达蛋白,可以用相应的抗体作为一抗进行检测,对新基因的表达产物,可以融合部分的已知片段进行检测,如HA-tag,Flag-tag,c-myc-tag等。
Western Blot采用的是聚丙烯酰胺(PAGE)凝胶电泳,被检测的是蛋白质,其中检测探针是相应的抗体,显色是使用的标记后的二抗。
经过PAGE凝胶分离的蛋白质样品,转移到固相载体上,如醋酸纤维素膜,固相载体以非共价键的形式吸附蛋白质。
然后以固相载体上的蛋白质作为抗原,与对应的抗体起免疫反应,然后再与标记后的二抗起反应,经过底物显色以检测目的蛋白。
蛋白质免疫印迹(Western Blot)原理蛋白免疫印迹法主要分为三个阶段进行第一阶段是SDS-聚丙烯酰胺凝胶电泳(SDS-PAGE)在这个阶段,经过变性处理的蛋白质样品经SDS处理后会带上阴性电荷,在聚丙烯酰胺凝胶中在电场的作用下从阴极向阳极泳动,且分子量越小,泳动速度就越快。
所以在此阶段,根据蛋白的泳动速度可以将样品中的蛋白质根据其分子量的大小进行分离,此阶段分离效果肉眼不可见。
如果想观察蛋白的电泳情况,可以在电泳完成后进行考马斯亮蓝染色进行观察;第二阶段为电转移,又称为转膜。
即将在凝胶中已经分离的蛋白质条带通过电场的作用转移至硝酸纤维素膜上, 一般选用恒流300 mA,通电90 min即可将凝胶中的蛋白条带转移到醋酸纤维素膜载体上。
转移到载体上的蛋白条带也是肉眼不可见的,如果想观察转移的效果,可以在转移后对载体进行丽春红染液染色。
第三阶段为酶联免疫显色检测将印有蛋白质条带的硝酸纤维素膜(相当于包被了抗原的固相载体)依次与特异性抗体和酶标第二抗体作用后,加入能形成不溶性显色物的酶反应底物,使目的条带蛋白显色。
Western+blot+实验技术

凝胶成份
丙烯酰胺和N,N’-亚甲双丙烯酰胺 SDS 配胶的Tris缓冲液
TEMED
过硫酸铵(时间) Tris-甘氨酸电泳缓冲液
凝胶浓度与蛋白分离范围
凝胶浓度(%) 线性分离范围(KD)
ห้องสมุดไป่ตู้
15
10
12-43
16-68
7.5
5.0
36-94
57-212
转膜
硝酸纤 维素膜
转膜后检测
丽春红S染色 蛋白带出现后,于室温用去离子水漂洗硝酸纤维素滤 膜,换水几次。 印度墨汁染色 只用于放射性标记抗体或放射性标记A蛋白探针的 Western印迹过程。
封闭
脱脂奶粉(5%) BSA Western Blot 膜封闭液(生物试剂公司提供) 封闭:室温下1小时,低速摇晃
水溶液提取法 针对水、稀盐、稀酸或碱溶液中的蛋白质。稀盐和缓冲系统的水溶液
对蛋白质稳定性好、溶解度大、是提取蛋白质最常用的溶剂 。
细胞裂解液: 50 mmol/L Tris-HCl, 150 mmol/L Nacl ,5 mmol/L EDTA, 1%NP40 ,
0.05% PMSF , 2μg/mL Aprotinin, 0.5μg/mL Leupeptin , pH8.0
“微笑”或“倒微笑”
条带?
转膜及抗体检测
凝胶肿胀或卷曲?
可将凝胶在转膜之前放到转膜缓冲液 中浸泡5-10min
条带歪斜或漂移?
单个或多个白点? 转膜缓冲液过热?
电转仪长期使用导致海绵变薄,“三
明治”结构不紧凑导致。可在两块海 绵之间垫上少许普通的草纸
蛋白质免疫印迹(Western Blot,WB )

蛋白质免疫印迹(Western Blot,WB )标签:western-blot免疫印迹 蛋白质蛋白质免疫印迹可应用于:(1)从蛋白质混合物中检出目标蛋白质;(2)定量或定性确定细胞或组织中蛋白质的表达情况;(3)用于蛋白质-蛋白质、蛋白质-DNA、蛋白质-RNA相互作用后续分析。
实验材料蛋白质样品试剂、试剂盒裂解液 PBS SDS上样缓冲液 电泳缓冲液 转移缓冲液 丽春红染液 TBST TBS 洗脱抗体缓冲液 抗体仪器、耗材电泳仪移液器脱色摇床显影仪实验方法原理Western免疫印迹,是将蛋白质转移到膜上,然后利用抗体进行检测的方法。
对已知表达蛋白,可用相应抗体作为一抗进行检测,对新基因的表达产物,可通过融合部分的抗体检测。
与Southern或Northern杂交方法类似,但Western Blot采用的是聚丙烯酰胺凝胶电泳,被检测物是蛋白质,探针是抗体,显色用标记的二抗。
经过PAGE分离的蛋白质样品,转移到固相载体(例如硝酸纤维素薄膜)上,固相载体以非共价键形式吸附蛋白质,且能保持电泳分离的多肽类型及其生物学活性不变。
以固相载体上的蛋白质或多肽作为抗原,与对应的抗体起免疫反应,再与酶或同位素标记的第二抗体起反应,经过底物显色或放射自显影以检测电泳分离的特异性目的基因表达的蛋白成分。
该技术也广泛应用于检测蛋白水平的表达。
实验步骤一、试剂准备1. SDS-PAGE试剂:见聚丙烯酰胺凝胶电泳实验。
2. 匀浆缓冲液:1.0 M Tris-HCl(pH 6.8) 1.0 ml;10%SDS 6.0 ml;β-巯基乙醇 0.2 ml;ddH2O 2.8 ml。
3. 转膜缓冲液:甘氨酸 2.9 g;Tris 5.8 g;SDS 0.37 g;甲醇200 ml;加ddH2O定容至1000 ml。
4. 0.01 M PBS(pH7.4):NaCl 8.0 g;KCl 0.2 g;Na2HPO4 1.44 g;KH2PO40.24 g;加ddH2O至1000 ml。
蛋白质印迹分析(WesternBlotAnalysis)
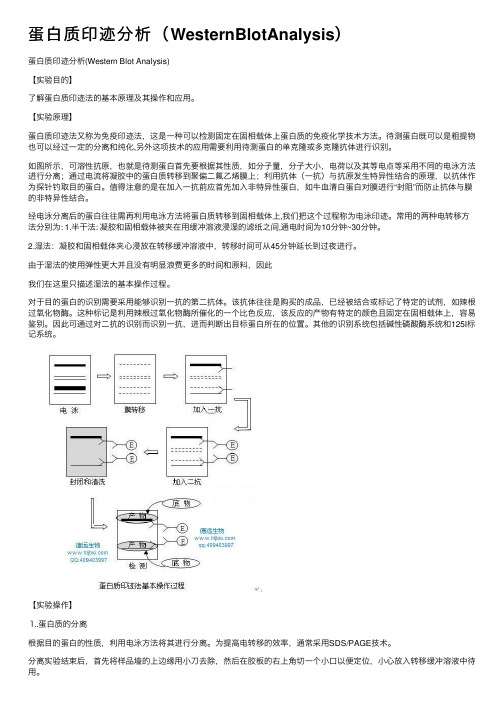
蛋⽩质印迹分析(WesternBlotAnalysis)蛋⽩质印迹分析(Western Blot Analysis)【实验⽬的】了解蛋⽩质印迹法的基本原理及其操作和应⽤。
【实验原理】蛋⽩质印迹法⼜称为免疫印迹法,这是⼀种可以检测固定在固相载体上蛋⽩质的免疫化学技术⽅法。
待测蛋⽩既可以是粗提物也可以经过⼀定的分离和纯化,另外这项技术的应⽤需要利⽤待测蛋⽩的单克隆或多克隆抗体进⾏识别。
如图所⽰,可溶性抗原,也就是待测蛋⽩⾸先要根据其性质,如分⼦量,分⼦⼤⼩,电荷以及其等电点等采⽤不同的电泳⽅法进⾏分离;通过电流将凝胶中的蛋⽩质转移到聚偏⼆氟⼄烯膜上;利⽤抗体(⼀抗)与抗原发⽣特异性结合的原理,以抗体作为探针钓取⽬的蛋⽩。
值得注意的是在加⼊⼀抗前应⾸先加⼊⾮特异性蛋⽩,如⽜⾎清⽩蛋⽩对膜进⾏“封阻”⽽防⽌抗体与膜的⾮特异性结合。
经电泳分离后的蛋⽩往往需再利⽤电泳⽅法将蛋⽩质转移到固相载体上,我们把这个过程称为电泳印迹。
常⽤的两种电转移⽅法分别为: 1.半⼲法: 凝胶和固相载体被夹在⽤缓冲溶液浸湿的滤纸之间,通电时间为10分钟~30分钟。
2.湿法:凝胶和固相载体夹⼼浸放在转移缓冲溶液中,转移时间可从45分钟延长到过夜进⾏。
由于湿法的使⽤弹性更⼤并且没有明显浪费更多的时间和原料,因此我们在这⾥只描述湿法的基本操作过程。
对于⽬的蛋⽩的识别需要采⽤能够识别⼀抗的第⼆抗体。
该抗体往往是购买的成品,已经被结合或标记了特定的试剂,如辣根过氧化物酶。
这种标记是利⽤辣根过氧化物酶所催化的⼀个⽐⾊反应,该反应的产物有特定的颜⾊且固定在固相载体上,容易鉴别。
因此可通过对⼆抗的识别⽽识别⼀抗,进⽽判断出⽬标蛋⽩所在的位置。
其他的识别系统包括碱性磷酸酶系统和125I标记系统。
【实验操作】⒈.蛋⽩质的分离根据⽬的蛋⽩的性质,利⽤电泳⽅法将其进⾏分离。
为提⾼电转移的效率,通常采⽤SDS/PAGE技术。
分离实验结束后,⾸先将样品墙的上边缘⽤⼩⼑去除,然后在胶板的右上⾓切⼀个⼩⼝以便定位,⼩⼼放⼊转移缓冲溶液中待⽤。
蛋白免疫印迹杂交实验方法

Western Blot(蛋白质免疫印迹技术)一、实验原理:与Southern或Northern杂交方法类似,但Western Blot采用的是聚丙烯酰胺凝胶电泳,被检测物是蛋白质,“探针”是抗体,“显色”用标记的二抗。
经过PAGE分离的蛋白质样品,转移到固相载体(例如硝酸纤维素薄膜)上,固相载体以非共价键形式吸附蛋白质,且能保持电泳分离的多肽类型及其生物学活性不变。
以固相载体上的蛋白质或多肽作为抗原,与对应的抗体起免疫反应,再与酶或同位素标记的第二抗体起反应,经过底物显色或放射自显影以检测电泳分离的特异性目的基因表达的蛋白成分。
该技术也广泛应用于检测蛋白水平的表达。
Western Blot(WB)是通过聚丙烯酰胺电泳根据分子量大小分离蛋白后,将蛋白转移至固相支持物—NC膜上,根据抗原和抗体之间的反应特性,通过特异性试剂(抗体)作为探针(一抗/二抗),对靶物质(抗原)进行检测。
蛋白质的Western印迹技术结合了凝胶电泳的高分辨率和固相免疫测定的特异敏感等多种特点,可检测到低至1~5ng(最低可到10-100pg)中等大小的靶蛋白。
Western Blot 流程图:样品聚丙烯酰胺凝胶电泳(SDS-PAGE)转膜封闭洗膜(3×5mins)孵育一抗(4度过夜或室温4-6小时)洗膜(3×10mins)孵育二抗(室温2小时)洗膜(3×10mins)显影SDS-PAGE分离蛋白的原理和操作:1. SDS-PAGE作用原理聚丙烯酰胺凝胶是网状结构,具有分子筛效应,它有两种形式,一种是非变性聚丙烯酰胺凝胶,蛋白质在电泳中保持完整的状态,蛋白在其中依三种因素分开:蛋白大小,形状和电荷。
另外一种是SDS-PAGE,SDS-PAGE仅根据蛋白分子量亚基的不同而分离蛋白。
这个技术首先是1967年由shapiro建立,他们发现在样品介质和丙烯酰胺凝胶中加入离子去污剂和强还原剂后,蛋白质亚基的电泳迁移率主要取决于亚基分子量的大小,电荷因素可以忽视。
蛋白免疫印迹技术(WesternBlot)介绍

• 上样
SDS-PAGE电泳
Staking gel Separating gel
转膜
• 膜的选择 最常用于Western Blot的转移膜主要是硝酸纤维素
(Nitrocellulose,NC)膜和聚偏二氟乙烯 (Polyvinylidene Fluoride, PVDF)膜,此外也有用尼龙膜、DEAE纤维素膜做蛋 白印迹。 • 孔径
蛋白免疫印迹技术介绍
主要内容
• Western Blot原理 • Western Blot特点及应用 • Western Blot一般流程 • Western Blot常见问原理
• 混合样品经SDS-聚丙烯酰胺凝胶电泳后分离,凝胶 中的蛋
一抗、二抗孵育
• 抗体选择 • 抗体稀释液 • 孵育条件 • 漂洗
显色
显色
• 化学发光检测
• 荧光法
显色
GE AI800凝胶成像系统
Western Blot 常见问题
• 样品制备 样本保存 蛋白酶抑制剂
• 抗体 正规厂家,有示例图 抗体保存 一抗二抗匹配 内参和对照
Western Blot 常见问题
法(Folin-酚试剂法)、 BCA法等。但各有优 缺点,大家可以根据具体情况选取。按相应 蛋白质定量试剂盒操作说明操作,测定样品 浓度
SDS-PAGE电泳
• SDS-PAGE 是在蛋白质样品中加入SDS和含有巯基乙醇的样品处理液, SDS是一种很强的阴离子表面活性剂,它可以断开分子内和分子间的 氢键,破坏蛋白质分子的二级和三级结构。
Western Blot 应用
• 从混合蛋白样品中检测目的蛋白 • 目的蛋白的组织定位 • 目的蛋白的表达量分析 • 目的蛋白与其他大分子间相互作用
蛋白质免疫印迹实验

蛋白质免疫印迹实验(Western Blot)蛋白质免疫印迹(Western Blot)实验原理蛋白质免疫印迹(Western Blot)是将蛋白质转移到膜上,然后利用抗体进行检测的一种蛋白质检测方法。
对已知的表达蛋白,可以用相应的抗体作为一抗进行检测,对新基因的表达产物,可以融合部分的已知片段进行检测,如HA-tag,Flag-tag,c-myc-tag等。
Western Blot采用的是聚丙烯酰胺(PAGE)凝胶电泳,被检测的是蛋白质,其中检测探针是相应的抗体,显色是使用的标记后的二抗。
经过PAGE凝胶分离的蛋白质样品,转移到固相载体上,如醋酸纤维素膜,固相载体以非共价键的形式吸附蛋白质。
然后以固相载体上的蛋白质作为抗原,与对应的抗体起免疫反应,然后再与标记后的二抗起反应,经过底物显色以检测目的蛋白。
蛋白质免疫印迹(Western Blot)原理蛋白免疫印迹法主要分为三个阶段进行第一阶段是SDS-聚丙烯酰胺凝胶电泳(SDS-PAGE)在这个阶段,经过变性处理的蛋白质样品经SDS处理后会带上阴性电荷,在聚丙烯酰胺凝胶中在电场的作用下从阴极向阳极泳动,且分子量越小,泳动速度就越快。
所以在此阶段,根据蛋白的泳动速度可以将样品中的蛋白质根据其分子量的大小进行分离,此阶段分离效果肉眼不可见。
如果想观察蛋白的电泳情况,可以在电泳完成后进行考马斯亮蓝染色进行观察;第二阶段为电转移,又称为转膜。
即将在凝胶中已经分离的蛋白质条带通过电场的作用转移至硝酸纤维素膜上, 一般选用恒流300 mA,通电90 min即可将凝胶中的蛋白条带转移到醋酸纤维素膜载体上。
转移到载体上的蛋白条带也是肉眼不可见的,如果想观察转移的效果,可以在转移后对载体进行丽春红染液染色。
第三阶段为酶联免疫显色检测将印有蛋白质条带的硝酸纤维素膜(相当于包被了抗原的固相载体)依次与特异性抗体和酶标第二抗体作用后,加入能形成不溶性显色物的酶反应底物,使目的条带蛋白显色。
蛋白质免疫印迹实验WesternBlot

摇动,待所检测的蛋白带显色达到最深程度后,将硝 酸纤维素薄膜转入 PBS 溶液中停止显色反应。取出 硝酸纤维素薄膜,自然晾干后拍照保存结果。
四 思考题
• 1. 为什么裁剪的滤纸必须与凝胶大小 完全一致?若不是这样结果会怎样?
• 2. 电转移时为什么都必须带手套小心 操作并除去气泡, 否则结果会怎样?
• 在进色后应时应注意哪些问题? • 请简述免疫印迹实验的原理,并将之与
免疫学相关概念联系起来。
2024/2/11
2024/2/11
一 实验原理
• 电泳将蛋白质从凝胶转移到固体支持物 上是通过电转移仪器完成的。它是将固 体支持物面对阳极、凝胶面对阴极,二 者结合在一起,然后将外面二侧用 Whatman 3MM滤纸结合,形成“三明治 ”结构,放入电转移仪器上,加入电泳 缓冲液,通上电源后,蛋白质即可从凝 胶上转移到固体支持物上。
2024/2/11
一 实验原理
其定量关系符合以下公式: • Ve=Vo+KV1 • Ve:某一溶质的洗脱体积 • Vo:层析柱的外水体积 • Vi:层析柱的内水体积 • K:某一溶质的分配系数
2024/2/11
二试剂和器材
1.试剂
电转移缓冲液 pH8.3 • 39mM甘氨酸 • 4.8mM Tris碱 • 0.037% SDS • 20% 甲醇 • 混合2.9克甘氨酸,5.8克Tris,0.37克SDS,加200ml甲2源自24/2/11三 操作步骤
Western blotting蛋白免疫印迹实验

7
生物实验培训
理论学习
课堂演示
一对一带教
个人实操
爱苏生物
1.4 WB 的特点
WB 是在蛋白质电泳分离和抗原、抗体检测基础上
发展起来的检测蛋白质的技术
SDS-PAGE 凝胶电泳:高分辨率
抗原抗体反应:特异性
转膜:灵敏度
8
生物实验培训
理论学习
课堂演示
一对一带教
课堂演示
一对一带教
个人实操
爱苏生物
1.2 蛋白免疫印迹的应用
检测样品中特异性蛋白质是否存在
例:李桂波.利用免疫印迹法钓取PC3M细胞中与人前列腺癌高转移 相关特异性短肽结合蛋白的研究[D].吉林:吉林大学,2007.
对特异性蛋白质进行半定量分析
例:
6
生物实验培训
4
生物实验培训
理论学习
课堂演示
一对一带教疫印迹的应用
基因在蛋白水平的表达研究
的免疫印迹分析[J].中国人兽共患病学报,2009,25(10):931-934.
例: 吴德平,王颖等.立氏立克次体蛋白抗原基因的表达和重组蛋白抗原
抗体活性检测
目 录
1.WB的概念
一 二 三 四
WB的基础 试剂与设备
2.WB的应用
3.WB的原理 4.WB的特点
实验步骤与结果分析 实验室常见问题解答
3
生物实验培训
理论学习
课堂演示
一对一带教
个人实操
爱苏生物
1.1 蛋白免疫印迹的概念
是将电泳分离后的总蛋白质从凝胶转移到固相支持物 NC 膜或 PVDF 膜上,然后用特异性抗体检测某特定抗原的 一种蛋白质检测技术。
Western_blotting

3. 显色反应
ECL超敏发光液
辣根过氧化物酶在过氧化氢存在的条件下催化鲁米诺,生成一种不稳定的中间 产物,当其衰变时即可发光。
二抗结合漂洗后,加入ECL超敏发光液,避光发光3-5分钟。
曝光
发出的光可使标准X-光片感光,产生较易识别的图像。
发光3-5分钟后,将膜夹如透明薄膜中,置于曝光夹(感光屏)中 曝光3min左右,然后进行显影液显影,定影液定影(和洗照片是 一样的)
方法一: 直接法
优点: 1.快速(一种抗体) 2.没有二抗交叉反应引起的 非特异性条带 缺点: 1.免疫反应性降低 2.无信号二级放大 3.抗体标记费时昂贵,使用不方便
抗原抗体反应
方法二: 间接法
优点: 1.免疫特异性不受标记影响 2.信号放大,灵敏度高(多个二抗
结合位点) 3.多种标记的二抗可供选择
免疫印迹的基本步骤
➢ 蛋白质样品的制备 ➢ 蛋白质的SDS-PAGE电泳 ➢ 蛋白质的膜转移 ➢ 封闭与抗原抗体反应 ➢ 显色(显影)反应
实验流程
样品收集制备 SDS-PAGE凝胶电泳分离蛋白
剥胶并电转移
封闭
一抗4℃孵育过夜 第二天,二抗37℃孵育1小时,显影曝光
条带灰度分析定量
蛋白质样品的制备
1. 电转移相关问题: 滤纸、胶、膜之间的大小。 滤纸、胶、膜之间千万不能有气泡,气泡会造成断路。 膜必须随时保持湿润(干膜法除外)。 系统降温
2. 抗体的性质 影响免疫印迹成败的一个主要因素是抗原分子中可被抗体识 别的表位的性质。只有那些能识别耐变性表位的抗体可与抗 原结合。
常见问题及解决办法
3 .样品中待检测蛋白质的含量 采用目前的技术,浓度低至0.1ng的蛋白亦可被检出 4. 背景问题 非特异性条带的来源一般有两种:一种是由于制剂中存在的非特异 抗体产生的背景条带,另一种则是由于特异性抗体与含有与待测抗原 类似表位的多肽发生的交叉反应 ① 弥散性高背景:可能原因是二抗产生,解决办法:缩短二抗孵育时 间;用高浓度的蛋白质来吸附二抗(二抗内加3%BSA);使用另外的 二抗;缩短一抗和二抗的孵育时间;延长每次清洗时间。
蛋白质印迹(Western blotting)实验操作步骤

蛋白质印迹/Western blotting实验操作步骤一、总蛋白的提取单层贴壁细胞总蛋白的提取:1)吸除培养液2)每皿细胞加4℃预冷的 PBS。
平放轻轻摇动 1min 洗涤细胞,然后弃去洗液。
重复上操作两次,共洗细胞三次以洗去培养液。
将PBS弃净后把培养瓶置于冰上。
(PBS会降低细胞裂解液的效价和总蛋白的浓度)3)加裂解液于冰上裂解 30 min,为使细胞充分裂解,培养瓶要经常来回摇动(可放置在4℃摇床裂解)。
4)裂解完后,用干净的刮棒将细胞刮于培养瓶的一侧(动作要快),然后用枪将细胞碎片和裂解液移至 1.5mL 离心管中。
(整个操作尽量在冰上进行)5)在EP管中将细胞震碎(10s/次,3次)6)于4℃下 12000rpm 离心 20-30 min。
(离心机提前预冷至4℃)7)将离心后的上清分装转移倒 1.5mL 的离心管中放于-20℃保存。
二、BCA法测蛋白浓度1)将BCA protein assay每孔 A液200μL,B液4μL混合,96孔板每孔加入22.5μLdd水,2.5μL蛋白提取液,200μLA+B混合液2)在烘箱中37℃,90r,孵育30min3)使用酶标仪测出吸光度后,使用公式y=0.9154x-0.118计算出蛋白浓度(浓度需要×10)4)将蛋白配成等浓度等体积(使用配置好的裂解液配),按照4:1加入5X loading buffer然后煮5min(100℃),放入-20℃保存三、SDS-PAGE电泳板子1.5mm,梳子1.5mm1)清洗玻璃板:一只手扣紧玻璃板,另一只手蘸点洗衣粉轻轻擦洗。
两面都擦洗过后用自来水冲洗2)验漏:玻璃板对齐后放入夹中卡紧,然后垂直卡在架子上,加满水验漏3)灌胶:验漏结束后用纸吸干水分,按方法配制下层胶(4mL+4mL+80μLAP),灌胶时,可用 1mL 枪吸取胶沿玻璃放出,待胶面升到绿带中间线高度时即可。
然后胶上加1 mL水,液封后的胶凝的更快。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
二试剂和器材
1.试剂
PBS: NaCl 8g,KCl 0.2g,Na2HPO4 1.44g,KH2PO4 0.24g 加双蒸水800ml,用HCl调pH到pH7.4,再加水到1000ml, 分装后,15磅20分钟灭菌。 4-氯萘酚显色液:用30mg 4-氯萘酚(简称4-CN)溶 于1ml无水乙醇中制成母液。将50μ14-CN对母液和 5μ130%的H2O2加入到5ml 0.05M/L Tris-Cl(pH7.6)中。 氨基黑染色液:0.1%氨基黑10-B、45%甲醇、10%冰 乙酸 氨基黑脱色液:90%甲醇、2%冰乙酸、8%水
三 操作步骤
2显色反应 首先进行分子量标记的氨基黑染色。切 下转有分子量标记的硝酸纤维素薄膜, 用含有0.3%吐温20的PBS缓冲液漂洗三 次后(每次15分钟),再将其浸入氨基 黑染液中,室温染色5分钟,然后置于 氨基黑脱色液中脱去背景,水中漂洗后 景干备用。
三 操作步骤
转有样品的硝酸纤维素薄膜用含有5%脱脂牛奶的PBS 缓冲液在室温下封闭2小时,同时1:100加入兔抗GST 第一抗体,平缓摇动,室温保温1小时。然后用PBS缓 冲液将硝酸纤维素薄膜漂洗4次,每次 30分钟。将辣 根过氧分物酶标记的羊抗兔免疫球蛋白第二抗 体用封 闭液稀释50倍后,加入吐温20至终浓度为0.05%,然 后与上述漂洗的硝酸纤维素薄膜进行反应,将膜浸于 其中,平放在平缓摇动的摇床平台上,室温温育 1小 时后,用PBS缓冲液将硝酸纤维素薄膜漂洗4次,每次 5 分 钟 , 再 加 入 4- 氯 萘 酚 显 色 液 , 加 入 5μ1 的 30%H2O2,将硝酸纤维素薄膜置于其中缓慢摇动,待 所检测的蛋白带显色达到最深程度后,将硝酸纤维素 薄膜转入 PBS 溶液中停止显色反应。取出硝酸纤维素 薄膜,自然晾干后拍照保存结果。
二试剂和器材
2.器材 电转移仪器 恒温摇床 硝酸纤维素薄膜 Whatman 3MM滤纸 电泳仪 裁纸刀 φ25cm培养皿
玻璃棒
三 操作步骤
1蛋白质电转移 戴上手套,取下SDS-PAGE凝胶,小心剥离凝胶。裁剪与凝胶同样大的 硝酸纤维素薄膜和六层Whatman 3MM滤纸,在硝酸纤维素薄膜左下角 剪去一角作为标记。将硝酸纤维素薄膜漂浮于去离子水的表面,使水从 膜的下部浸透以去除其间气泡,将Whatman 3MM滤纸在电转移缓冲液 中浸湿,用蒸馏水淋洗石墨电极,先将三层浸湿的滤纸放在阳极上,在 滤纸表面滚动玻璃棒以除去其间的气泡,再将浸湿的硝酸纤维素薄膜小 心平铺在滤纸上,用玻璃棒小心去除气泡。随后将12%SDS-PAGE凝胶 舒展平铺在硝酸纤维素薄膜上,用玻璃棒小心去除气泡,再将三层浸湿 的滤纸平铺在凝胶上,沁心去除气泡,最后加上石墨电极板,接通电源 进行电转移,电流的大小由凝胶的大小决定,为0.65mA/平方厘米。电 转移2小时后,停止通电,卸掉电转移装置,取下凝胶进行考马斯亮兰 染色,以检测电转移是否完全。小心取下硝酸纤维素薄膜,放在一张干 滤纸上,吸干30-60分钟后,开始进显色反应。
其定量关系符合以下公式: Ve=Vo+KV1 Ve:某一溶质的洗脱体积 Vo:层析柱的外水体积 Vi:层析柱的内水体积 K:某一溶质的分配系数
二试剂和器材
1.试剂
电转移缓冲液 pH8.3 39mM甘氨酸 4.8mM Tris碱 0.037% SDS 20% 甲醇 混合2.9克甘氨酸,5.8克Tris,0.37克SDS,加200ml甲醇, 定容到1000ml. 封闭缓冲液:5%(W/V)脱脂奶粉溶于PBS中
蛋白质免疫印迹实验
(Western Blotting)
一 实验原理
Western Blotting 是用来检测蛋白质的一种技术。 首先将含有待测蛋白的蛋白质混合物进行凝胶电泳分离, 然后将已经分离的蛋白质通过电泳技术从凝胶转移到固 体支持物上,这一固体支持物目前常为硝酸纤维素薄膜。 随后以待测蛋白质上抗原决定簇特异性的抗体(称为第 一抗体)为探针,与固体支持物上的蛋白质进行免疫反 应,最后用偶联有辣根过氧化物酶或碱性磷酸酯酶的抗 第一抗体的抗体(第二抗体)与第一抗体进行免疫反应, 只有与第一抗体特异性结合的待测蛋白才能与第二抗体 发生免疫反应。在有辣根过氧化物酶的底物用显色剂存 在时就会出现颜色反应,结合有第一抗体、第二抗体的 待测蛋白,通过颜色反应即能显现出来。
一 实验原理
电泳将蛋白质从凝胶转移到固体支持物 上是通过电转移仪器完成的。它是将固 体支持物面对阳极、凝胶面对阴极,二 者结合在一起,然后将外面二侧用 Whatman 3MM滤纸结合,形成“三明治” 结构,放入电转移仪器上,加入电泳缓 冲液,通上电源后,蛋白质即可从凝胶 上转移到固
1. 为什么裁剪的滤纸必须与凝胶大小 完全一致?若不是这样结果会怎样? 2. 电转移时为什么都必须带手套小心 操作并除去气泡, 否则结果会怎样? 在进色后应时应注意哪些问题? 请简述免疫印迹实验的原理,并将之与 免疫学相关概念联系起来。
