GC-YL-20890酸枣仁原料检验操作规程
YL-20480诃子原料检验操作规程

题目:补骨脂原药材检验操作规程
编号:TS-GC-YL-20490-02
制定人:
制定日期2020 年 月 日
版本:2
页数:1/3
审核人:
审核日期2020 年 月 日
颁发部门:质 量 部
批准人:
批准日期2020年 月 日来自生效日期2020 年 月 日目的:规范补骨脂原药材检验操作
范围:补骨脂原药材检验
计算公式:
(W1-W0)×V0
浸出物% =×100%
W样×(1-水分)×V1
式中:
W0------- 蒸发皿的重量(g)。
W1-------- 浸出物与蒸发皿的重量(g)。
W样------- 样品的重量(g)。
V0-------加溶媒体积(ml)。
V1-------取续滤液的体积(ml)。
【检查】
水分不得过13.0%(通则0832第二法)。
仪器:电热鼓风干燥箱、分析天平、等。
方法:取供试品2-5g,平铺于干燥至恒重的扁形称量瓶中,厚度不超过5mm,疏松供试品不超过10mm,精密称定,打开瓶盖在100-105℃干燥5小时,将瓶盖盖好,移置干燥器中,冷却30分钟,精密称定重量,再在上述温度干燥1小时,冷却,称重至连续两次称重的差异不超过5mg为止。根据减失的重量,计算供试品中的含水量(%)。
仪器:粉碎机、药筛、分析天平、坩埚、箱式电阻炉等。
方法:取供试品2~3g,过二号筛混合均匀后,置炽灼至恒重的坩埚中称定重量,缓缓炽热,注意避免燃烧,至完全炭化时,逐渐升高温度至500~600℃,使完全灰化至恒重。根据残渣重量,计算供试品中总灰分的含量(%)。
计算公式:
W1-W0
总灰分% =×100%
仪器:直尺。
酸枣仁质量标准及检验操作规程
XXXXXX有限公司原料质量标准及检验操作规程1 品名:1.1 中文名:酸枣仁1.2 汉语拼音:Suanzaoren2 代码:3 取样文件编号:4 检验方法文件编号:5 依据:《中国药典》(2020年版一部)。
6 质量标准:7 检验操作规程:7.1 试药与试剂:甲醇、酸枣仁皂苷A对照品、酸枣仁皂苷B对照品、水饱和的正丁醇、1%香草醛硫酸溶液、石油醚(60~90℃)、酸枣仁对照药材、斯皮诺素对照品、氯化钠、乙腈、乙醇。
7.2 仪器与用具:电子天平、回流装置、索氏提取器、烘箱、马福炉、水浴锅、硅胶G薄层板、紫外光灯、高效液相色谱仪。
7.3 性状:取本品适量,自然光下目测色泽,嗅闻气味。
7.4 鉴别:7.4.1取本品横切面制片显微镜(10×10)观察组织结构特征。
7.4.2取本品粉末1g,加甲醇30ml,加热回流1小时,滤过,滤液蒸干,残渣加甲醇0.5ml使溶解,作为供试品溶液。
另取酸枣仁皂苷A对照品、酸枣仁皂苷B对照品,加甲醇制成每1ml各含1mg的混合溶液,作为对照品溶液。
照薄层色谱法(附录7)试验,吸取上述两种溶液各5μl,分别点于同一硅胶G薄层板上,以水饱和的正丁醇为展开剂,展开,取出,晾干,喷以1%香草醛硫酸溶液,立即检视。
供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的斑点。
取本品粉末1g,加石油醚(60~90℃)30ml,加热回流2小时,滤过,弃去石油醚液,药渣挥干,加甲醇30ml,加热回流1小时,滤过,滤液蒸干,残渣加甲醇2ml使溶解,作为供试品溶液。
另取酸枣仁对照药材1 g,同法制成对照药材溶液。
再取斯皮诺素对照品,加甲醇制成每1ml各含0.5mg的溶液,作为对照品溶液。
照薄层色谱法(附录7)试验,吸取上述三种溶液各2μl,分别点于同一硅胶G薄层板上,以水饱和的正丁醇为展开剂,展开,取出,晾干,喷以1%香草醛硫酸溶液,置紫外光灯(365nm)下检视。
供试品色谱中,在与对照药材和对照品色谱相应的位置上,显相同的蓝色荧光斑点。
酸枣仁工艺规程
目录2、生产工艺流程4、质量监控:见“SCGL532301 酸枣仁生产关键工序质量监控要点”。
5. 原辅料、半成品、成品质量标准。
5.1 酸枣仁原料质量标准:见“ZLJS100101 原药材质量标准”。
5.2 酸枣仁中间产品质量标准:见“ZLJS400101 饮片中间产品质量标准”。
5.3 酸枣仁成品质量标准:见“ZLJS500101 饮片成品质量标准”。
6、包材质量标准和文字说明6.1 包材质量标准:见“ZLJS300101~ZLJS300601包装材料质量标准”6.2 包装说明文字:品名:酸枣仁规格:产地:重量:产品批号:生产日期:贮藏:置阴凉干燥处,防蛀生产企业:7、生产区的工艺卫生要求7.1 生产区卫生要求:执行“CSGL001401一般生产区环境卫生管理规程”,7.2 生产区清洁工作要求:执行“CSSOP000301一般生产区厂房清洁规程”, 7.3 生产区人员卫生要求:执行“SCGL000101一般生产区个人卫生规程”,7.4 生产区工作服管理要求:执行“SCGL005701一般生产区工作服管理规程”9、技术经济指标核算9.2包装材料物料平衡使用量+残损量+剩余量塑料袋物料平衡= ×100%(99.0-101.0%) 本批领用量使用数+残损数+剩余数标签物料平衡= ×100%(99.0-101.0%) 本批领用数9.3 包装材料消耗定额(按投料100kg计算)10、技术安全及劳动保护10.1 员工转岗或新工上岗前均要进行安全操作培训,熟悉本岗位的操作要点、质控要点及注意事项。
10.2 严格按工艺规程和岗位标准操作程序操作,切忌擅改工艺和岗位操作方法,工作应严肃认真。
10.3 电机设备严禁用水直接冲洗,清洁时亦不可用湿布擦拭。
在确保一切准备工作就绪后方可开机,以防轧手等事故发生。
10.4 设备定期保养,严格按设备维护保养管理制度操作使用。
10.5 拣选、切药、干燥、筛分等产尘、产湿岗位应有除尘排湿装置。
国产酸枣仁和进口酸枣仁含量检测报告

国产酸枣仁和进口酸枣仁含量检测报告国产酸枣仁和进口酸枣仁含量检测报告背景酸枣仁作为一种常用的中药材,是许多人日常生活中的健康食品之一。
然而,市场上存在着国产酸枣仁和进口酸枣仁两种不同来源的产品。
鉴于消费者对于产品质量的关注,本次报告旨在对国产酸枣仁和进口酸枣仁进行含量检测,并分析两者之间的差异。
检测方法1.样品选择:从市场上随机选取一定数量的国产酸枣仁和进口酸枣仁样品。
2.检测指标:本次检测主要关注以下指标:酸枣仁的总黄酮含量、维生素C含量、蛋白质含量。
3.检测设备:使用高效液相色谱仪和紫外分光光度计进行检测。
4.检测方法:按照国家相关标准进行样品的预处理、萃取和测定。
检测结果以下是本次酸枣仁含量检测的结果:国产酸枣仁 - 总黄酮含量:XX mg/g - 维生素C含量:XXmg/100g - 蛋白质含量:XX g/100g进口酸枣仁 - 总黄酮含量:XX mg/g - 维生素C含量:XXmg/100g - 蛋白质含量:XX g/100g结果分析根据以上结果可以得出以下结论:1.总黄酮含量:国产酸枣仁和进口酸枣仁的总黄酮含量相近,在XX mg/g左右,无明显差异。
2.维生素C含量:进口酸枣仁的维生素C含量略高于国产酸枣仁,但差别不大。
国产酸枣仁的维生素C含量为XXmg/100g,进口酸枣仁的维生素C含量为XX mg/100g。
3.蛋白质含量:国产酸枣仁和进口酸枣仁的蛋白质含量也相似,国产酸枣仁的蛋白质含量为XX g/100g,进口酸枣仁的蛋白质含量为XX g/100g。
结论综上所述,国产酸枣仁和进口酸枣仁在总黄酮含量、维生素C含量和蛋白质含量上并无明显差异。
消费者可根据个人需求和购买成本选择适合自己的产品。
参考文献•国家标准:XXXX•XXXX技术手册注:以上结果仅为本次检测得出的结论,具体情况处理时需根据您所在地区和市场的相关法规和标准来做出决策。
怎样继续?请问您还有其他要求或需要补充的内容吗?。
酸枣仁中5种重金属及有害元素含量的测定
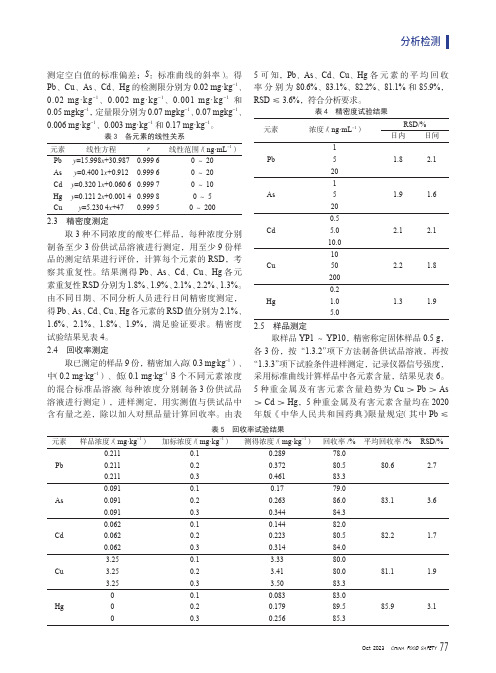
测定空白值的标准偏差;S:标准曲线的斜率)。
得Pb、Cu、As、Cd、Hg的检测限分别为0.02 mg·kg-1、0.02 mg·kg-1、0.002 mg·kg-1、0.001 mg·kg-1和0.05 mg·kg-1,定量限分别为0.07 mg·kg-1、0.07 mg·kg-1、0.006 mg·kg-1、0.003 mg·kg-1和0.17 mg·kg-1。
表3 各元素的线性关系元素线性方程r线性范围/(ng·mL-1)Pb y=15.998x+30.9870.999 60~20As y=0.400 1x+0.9120.999 60~20Cd y=0.320 1x+0.060 60.999 70~10Hg y=0.121 2x+0.001 40.999 80~5Cu y=5.230 4x+470.999 50~2002.3 精密度测定取3种不同浓度的酸枣仁样品,每种浓度分别制备至少3份供试品溶液进行测定,用至少9份样品的测定结果进行评价,计算每个元素的RSD,考察其重复性。
结果测得Pb、As、Cd、Cu、Hg各元素重复性RSD分别为1.8%、1.9%、2.1%、2.2%、1.3%。
由不同日期、不同分析人员进行日间精密度测定,得Pb、As、Cd、Cu、Hg各元素的RSD值分别为2.1%、1.6%、2.1%、1.8%、1.9%,满足验证要求。
精密度试验结果见表4。
2.4 回收率测定取已测定的样品9份,精密加入高(0.3 mg·kg-1)、中(0.2 mg·kg-1)、低(0.1 mg·kg-1)3个不同元素浓度的混合标准品溶液(每种浓度分别制备3份供试品溶液进行测定),进样测定,用实测值与供试品中含有量之差,除以加入对照品量计算回收率。
由表5可知,Pb、As、Cd、Cu、Hg各元素的平均回收率分别为80.6%、83.1%、82.2%、81.1%和85.9%,RSD≤3.6%,符合分析要求。
酸枣仁质量标准
1 目的:明确酸枣仁质量标准,确定质量、生产、采供质控依据。
2 范围:酸枣仁。
3 责任者:质量部、生产部、采供部。
4 内容 4.1基本信息4.1.1 物料代码:原药材Y120-1;饮片:Y120-2。
4.1.2 供应商:亳州市远光中药饮片厂甘肃渭源颜裕药业有限公司4.1.3 标准依据:《中国药典》2010年版第一增补本P124。
4.2 取样、检验方法或相关操作规程编号 4.2.1 取样管理规程SOP-QA-1005-00。
4.2.2 检验方法或相关操作规程编号4.2.2.1 酸枣仁检验操作规程SOP-QC-6120-00。
4.2.2.2 检验方法药材及成方制剂显微鉴别法SOP-QC-5007-00;薄层色谱法SOP-QC-5010-00; 杂质检查法 SOP-QC-5018-00;水分测定法 SOP-QC-5024-00; 灰分测定法 SOP-QC-5025-00;黄曲霉毒素测定法SOP-QC-5054-00; 高效液相色谱法SOP-QC-5011-00。
4.3 标准内容 4.3.1 药材:酸枣仁本品为鼠李科植物酸枣Z iziphus jujuba Mill.var.spinosa (Bunge)Hu ex文件编号 酸枣仁质量标准颁发部门QS-QC-0120-00GMP 办公室 版本号 生效日期1.0编制人/修订人审核人 批准人 日期审核日期批准日期 会签(分发)质量部、生产部、采供部总页数5页标准文件酸枣仁质量标准文件编号QS-QC-0120-00 版本号 1.0 第 2 页共 5 页H.F.Chou干燥成熟种子。
秋末冬初采收成熟果实,除去果肉和核壳,收集种子,晒干。
4.3.1.1 性状:本品呈扁圆形或扁椭圆形,长5~9mm,宽5~7mm,厚约3mm。
表面紫红色或紫褐色,平滑有光泽,有的有裂纹。
有的两面均呈圆隆状突起,有的一面较平坦,中间有1条隆起的总线纹;另一面稍突起。
一端凹陷,可见线形种脐;另端有细小突起的合点。
GC-YL-10100山柰检验操作规程
水分不得过15.0%(通则0832第四法)。
仪器:甲苯法仪器装置、分析天平、粉碎机、药筛等。
方法:取供试品适量(约相当于含水量1~4ml),精密称定,置A瓶中,加甲苯约200ml,必要时加入干燥、洁净的无釉小瓷片数片或玻璃珠数粒,连接仪器,自冷凝管顶端加入甲苯至充满B管的狭细部分。将A瓶置电热套中或用其他适宜方法缓缓加热,待甲苯开始沸腾时,调节温度,使每秒馏出2滴。待水分完全馏出,即测定管刻度部分的水量不再增加时,将冷凝管内部先用甲苯冲洗,再用饱蘸甲苯的长刷或其他适宜方法,将管壁上附着的甲苯推下,继续蒸馏5分钟,放冷至室温,拆卸装置,如有水黏附在B管的管壁上,可用蘸甲苯的铜丝推下,放置使水分与甲苯完全分离(可加亚甲蓝粉末少量,使水染成蓝色,以便分离观察)。检读水量,并计算成供试品的含水量(%)。
(2)薄层鉴别
仪器与试剂:分析天平、硅胶G薄层板、层析缸、明党参对照药材、正丁醇、冰醋酸等。
方法:取本品粉末0.25g,加甲醇5ml,超声处理10分钟,滤过,取滤液作为供试品溶液。另取对甲氧基肉桂酸乙酯对照品,加甲醇制成每1ml含5mg的溶液,作为对照品溶液。照薄层色谱法(通则0502)试验,吸取上述两种溶液各2μl,分别点于同一硅胶GF254薄层板上,以正己烷-乙酸乙酯(18:1)为展开剂,展开,取出,晾干,置紫外光灯(254nm)下检视。供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的斑点。
方法:取本品约5mm的短段适量,称定重量(准确至0.O1g),置烧瓶中,每100g供试品加水600ml,与玻璃珠数粒,振摇混合后,连接挥发油测定器与回流冷凝管。自冷凝管上端加水使充满挥发油测定器的刻度部分,并溢流入烧瓶时为止。置电热套中或用其他适宜方法缓缓加热至沸,并保持微沸约3小时,至测定器中油量不再增加,停止加热,放置片刻,开启测定器下端的活塞,将水缓缓放出,至油层上端到达刻度0线上面5mm处为止。放置1小时以上,再开启活塞使油层下降至其上端恰与刻度0线平齐,读取挥发油量,并计算供试品中挥发油的含量(%)
高效液相色谱法测定酸枣仁样品中的皂苷A和B的含量

高效液相色谱法测定酸枣仁样品中的皂苷A和B的含量摘要:采用索式提取法提取相同产地32种酸枣(Zizyphus jujube)仁中的皂苷A、B,并以高效液相色谱(HPLC)法测定其含量。
结果表明,不同品种酸枣仁皂苷A及B含量有一定差异,以8号酸枣仁皂苷A含量最高,14号酸枣仁皂苷A含量最低,26号酸枣仁皂苷B含量最高,14号酸枣仁皂苷B含量最低,26号和1002号的酸枣仁皂苷A的含量差异不大,但酸枣仁皂苷B的含量有较大差异。
以酸枣仁皂苷A和B能够较为全面评价酸枣仁的皂甙水平。
关键词:酸枣(Zizyphus jujube);酸枣仁皂苷;高效液相色谱鼠李科植物酸枣(Ziziphus jujube Mill var.spinosa(Bunge)Hu ex H.F.chou)在中国主要分布于陕西、山东、湖北、河南、安徽、辽宁、华北等地。
酸枣仁是其干燥成熟种子,其味酸性平,具有养肝宁心、安神敛汗功能,主治虚烦不眠、惊悸多梦、体虚多汗、津伤口渴等症,常作为安神药[1]。
据报道酸枣仁中含有多种功能性化合物[2-4],其中具有镇静催眠活性的化合物主要包括三萜皂苷和黄酮类化合物,其中酸枣仁皂苷A及B为其中主要有效成分[5,6],但由于产地不同,其含量差异极大。
本试验采用高效液相色谱法分析河北邢台产的32个品种酸枣仁样品中的酸枣仁皂苷A和B含量,为邢台酸枣仁的综合开发利用提供参考。
1 材料与方法1.1 材料与试剂酸枣仁样品由河北农业大学理学院提供;酸枣仁对照品购于上海顺勃生物工程有限公司。
色谱纯乙腈,购于Fisher公司;甲醇、石油醚、正丁醇、氨水均为分析纯,购于国药集团化学试剂有限公司。
1.2 仪器1200型高效液相色谱仪(Agilent,美国),配备二元梯度泵,紫外检测器,色谱工作站等;配用CO-3010型柱恒温控制箱(天津美瑞泰克科技有限公司生产);RE52CS型旋转蒸发仪(上海亚容生化仪器厂)。
1.3 方法1.3.1 样品溶液的制备酸枣仁样品粉碎后混和均匀,准确称取3.00 g样品,置于索氏提取器中,加入100 mL甲醇,100 ℃加热回流14 h后,挥干甲醇,残渣用30 mL水溶解,定量转移至60 mL分液漏斗中,加入石油醚萃取3次,每次15 mL,静置5 min,收集水层,加入水饱和正丁醇萃取4次,每次10 mL,静置15 min,收集正丁醇层,加入正丁醇饱和氨水溶液,萃取3次,每次10 mL,静置15 min,再收集正丁醇层,减压蒸发正丁醇,残渣用甲醇溶解,并定容至5 mL,摇匀,0.45 μm微孔滤膜过滤,备用。
酸枣仁检验标准操作规程
原药材检验标准操作规程目的:建立一个中药饮片原药材检验标准操作程序,确保检验结果准确可靠。
适用范围:中药原药材。
责任人:质量保证部主任、质量控制部主任、化验员。
标准来源:《中华人民共和国药典》2010年版一部、《安徽省中药饮片炮制规范》。
内容:1、性状取本品适量,放入白瓷盘中,用眼观察,可见以下性状特征:本品呈扁圆形或扁椭圆形,长5~9mm ,宽5~7mm,厚约3mm。
表面紫红色或紫褐色,平滑有光泽,有的有裂纹。
有的一面较平坦,中间有1条隆起的纵线纹;另一面稍突起。
一端凹陷,可见线形种脐;另端有细小突起的合点,种皮较脆,胚乳白色,子叶2,浅黄色,富油性。
气微,味淡。
2、鉴别主要使用仪器:电子分析天平、电子显微镜等。
2.1显微鉴别:2.1.1 试液配制2.1.1.1 水合氯醛试液:取水合氯醛50克,加水15毫升与甘油10毫升使溶解,即得。
2.1.1.2 甘油醋酸试液:取甘油、醋酸及水各等份混匀,即得。
2.1.1.3 稀甘油:取甘油33毫升,加水稀释至100毫升,再加樟脑一小块或液化苯酚1滴,即得。
2.1.2 供试品制备2.1.2.1 取本品10g,研细后取少量粉末,置载玻片上,滴加水合氯醛搅拌均匀,置酒精灯上加热透化;加稀甘油数滴,搅拌均匀,分装2~3片,加盖玻片,即得。
2.1.2.2 取研细的粉末少量置载玻片上,加甘油醋酸试液,搅拌均匀,加盖玻片,即得。
2.1.2.3取研细后取少量粉末,置载玻片上,滴加水搅拌均匀,同时滴加少许稀甘油,加盖玻片,即得。
2.1.3 置显微镜下观察可见本品粉末棕红色。
种皮栅状细胞棕红色,表面观多角形,直径约15μm,壁厚,木化,胞腔小。
内种皮细胞棕黄色,表面观长方形或类方形,壁连珠状增厚,木化。
子叶表皮细胞含细小草酸钙簇晶和方晶。
2.2薄层鉴别2.2.1取本品粉末1g,加甲醇30ml,加热回流1小时,滤过,滤液蒸干,残渣加甲醇0.5ml使溶解,作为供试品溶液。
另取酸枣仁皂苷A对照品、酸枣仁皂苷B对照品,分别加甲醇制成每1ml各含1mg的混合溶液,作为对照品溶液。
炒酸枣仁原料检验操作规程
GMP管理文件
一.目的:为规范炒酸枣仁的检验标准和生产要求,特制定此标准。
二.适用范围:适用于中药材炒酸枣仁的质量检验。
三.责任者:质量检验员
四.正文:
检品名称:炒酸枣仁
检验依据:《炒酸枣仁内控质量标准》
检验仪器:显微镜干燥箱马弗炉高效液相色谱仪
【性状】本品形如酸枣仁。
表面微鼓起,微具焦斑。
略有焦香气,味淡。
【鉴别】(1)本品粉末棕红色。
种皮栅状细胞棕红色,表面观多角形,直径约15um,壁厚,木化,胞腔小;侧面观呈长条形,外壁增厚,侧壁上、中部甚厚,下部渐薄;地面观类多角形或园多角形。
种皮内表皮细胞棕黄色,表面观长方形或类方形,垂周壁连珠状增厚,木化。
子叶表皮细胞含细小草酸钙簇晶和方晶。
(2)取本品粉末1g,加甲醇30ml,加热回流1小时,滤过,滤
液蒸干,残渣加甲醇0.5ml使溶解,作为供试品溶液。
另取酸枣仁皂苷A对照品、酸枣仁皂苷B对照品,加甲醇制成每1ml各含1mg 的混合溶液,作为对照品溶液。
照薄层色谱法试验,吸取上述两种溶液各5ul,分别点于同一硅胶G薄层板上,以水饱和的正丁醇为展开剂,展开,取出,晾干,喷以1%香草醛硫酸溶液,立即检视。
供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的斑点。
YL-11080常山原料检验操作规程

题目:常山原药材检验操作规程
编号:TS-GC-YL-11080-02
制定人:
制定日期2020年 月 日
版本:2
页数:1/3
审核人:
审核日期2020年 月 日
颁发部门:质 量 部
批准人:
批准日期2020年 月 日
生效日期2020年 月 日
目的:规范常山原药材检验操作
范围:常山原药材检验
分发部门: 质量部、 化验室、生产部
方法:测定法取药材或饮片细粉约10g(如二氧化硫残留量较髙,超过1000mg/kg,可适当减少取样量,但应不少于5g),精密称定,置两颈圆底烧瓶中,加水300〜400ml。打开回流冷凝管开关给水,将冷凝管的上端二氧化硫气体导出口处连接一橡胶导气管置于100ml锥形瓶底部。锥形瓶内加入3%过氧化氢溶液50ml作为吸收液(橡胶导气管的末端应在吸收液液面以下)。使用前,在吸收液中加人3滴甲基红乙醇溶液指示剂(2.5mg/ml),并用0.Olmol/L氢氧化钠滴定液滴定至黄色(即终点;如果超过终点,则应舍弃该吸收溶液)。开通氮气,使用流量计调节气体流量至约0.2L/min;打开分液漏斗的活塞,使盐酸溶液(6mol/L)10ml流入蒸馏瓶,立即加热两颈烧瓶内的溶液至沸,并保持微沸;烧瓶内的水沸腾1.5小时后,停止加热。吸收液放冷后,置于磁力搅拌器上不断搅拌,用氢氧化钠滴定(O.Olmol/L)滴定,至黄色持续时间20秒不褪,并将滴定的结果用空白实验校正。
粉末淡棕黄色。淀粉粒较多,单粒类圆形或长椭圆形,直径3~18μm,复粒少,由2~3分粒组成。草酸钙针晶成束,存在于长圆形细胞中,长10~50μm。导管多为梯状具缘纹孔导管,直径15~45μm。木纤维细长,直径10~43μm,壁稍厚。木薄壁细胞淡黄色,类多角形或类长多角形,壁略呈连珠状。
酸枣仁工艺规程

目录2、生产工艺流程4、质量监控:见“SCGL532301 酸枣仁生产关键工序质量监控要点”。
5. 原辅料、半成品、成品质量标准。
5.1 酸枣仁原料质量标准:见“ZLJS100101 原药材质量标准”。
5.2 酸枣仁中间产品质量标准:见“ZLJS400101 饮片中间产品质量标准”。
5.3 酸枣仁成品质量标准:见“ZLJS500101 饮片成品质量标准”。
6、包材质量标准和文字说明6.1 包材质量标准:见“ZLJS300101~ZLJS300601包装材料质量标准”6.2 包装说明文字:品名:酸枣仁规格:产地:重量:产品批号:生产日期:贮藏:置阴凉干燥处,防蛀生产企业:7、生产区的工艺卫生要求7.1 生产区卫生要求:执行“CSGL001401一般生产区环境卫生管理规程”,7.2 生产区清洁工作要求:执行“CSSOP000301一般生产区厂房清洁规程”, 7.3 生产区人员卫生要求:执行“SCGL000101一般生产区个人卫生规程”,7.4 生产区工作服管理要求:执行“SCGL005701一般生产区工作服管理规程”9、技术经济指标核算9.2包装材料物料平衡使用量+残损量+剩余量塑料袋物料平衡= ×100%(99.0-101.0%) 本批领用量使用数+残损数+剩余数标签物料平衡= ×100%(99.0-101.0%) 本批领用数9.3 包装材料消耗定额(按投料100kg计算)10、技术安全及劳动保护10.1 员工转岗或新工上岗前均要进行安全操作培训,熟悉本岗位的操作要点、质控要点及注意事项。
10.2 严格按工艺规程和岗位标准操作程序操作,切忌擅改工艺和岗位操作方法,工作应严肃认真。
10.3 电机设备严禁用水直接冲洗,清洁时亦不可用湿布擦拭。
在确保一切准备工作就绪后方可开机,以防轧手等事故发生。
10.4 设备定期保养,严格按设备维护保养管理制度操作使用。
10.5 拣选、切药、干燥、筛分等产尘、产湿岗位应有除尘排湿装置。
炒酸枣仁实验报告

一、实验目的1. 探究炒酸枣仁的炮制方法对药材有效成分的影响。
2. 评价炒酸枣仁的炮制工艺对药材品质的影响。
3. 为酸枣仁的临床应用提供科学依据。
二、实验材料1. 药材:酸枣仁(干燥,批号20190101,产地河南)。
2. 仪器:电热恒温干燥箱、电子天平、煎药机、煎药器、显微镜、分光光度计等。
3. 试剂:乙醇、盐酸、无水乙醇、氯仿等。
三、实验方法1. 炒酸枣仁工艺:将酸枣仁置于电热恒温干燥箱中,以150℃的温度烘烤30分钟,取出晾凉备用。
2. 指标测定:(1)水分测定:采用烘干法测定炒酸枣仁的水分含量。
(2)总黄酮含量测定:采用紫外-可见分光光度法测定炒酸枣仁中的总黄酮含量。
(3)总皂苷含量测定:采用高效液相色谱法测定炒酸枣仁中的总皂苷含量。
(4)酸枣仁中挥发油含量测定:采用气相色谱法测定炒酸枣仁中的挥发油含量。
3. 对比实验:将炒酸枣仁与生酸枣仁进行对比,观察炮制工艺对药材品质的影响。
四、实验结果1. 水分测定:炒酸枣仁的水分含量为8.5%,生酸枣仁的水分含量为12.0%。
2. 总黄酮含量测定:炒酸枣仁的总黄酮含量为1.23mg/g,生酸枣仁的总黄酮含量为1.10mg/g。
3. 总皂苷含量测定:炒酸枣仁的总皂苷含量为0.85mg/g,生酸枣仁的总皂苷含量为0.75mg/g。
4. 挥发油含量测定:炒酸枣仁的挥发油含量为0.50%,生酸枣仁的挥发油含量为0.45%。
5. 对比实验:炒酸枣仁与生酸枣仁在总黄酮、总皂苷和挥发油含量方面均有所提高,表明炒酸枣仁的炮制工艺对药材品质有显著改善作用。
五、实验讨论1. 炒酸枣仁炮制工艺对药材有效成分的影响:实验结果显示,炒酸枣仁炮制后,总黄酮、总皂苷和挥发油含量均有所提高。
这可能是由于炒制过程中,酸枣仁中的有效成分发生了化学反应,使得含量增加。
2. 炒酸枣仁炮制工艺对药材品质的影响:炒酸枣仁炮制后,水分含量降低,有利于药材的储存和运输。
同时,炒制过程中,酸枣仁中的有效成分得到提高,有利于提高临床疗效。
酸枣仁产地加工技术规程

酸枣仁产地加工技术规程1范围本文件规定了酸枣仁产地加工的术语和定义、酸枣采收、产地加工、规格等级、质量要求、包装及贮藏、生产记录。
本文件适用于酸枣仁产地加工。
2规范性引用文件下列文件中的内容通过文中的规范性引用而构成本文件必不可少的条款。
其中,注日期的引用文件,仅该日期对应的版本适用于本文件;不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB5749生活饮用水卫生标准SB/T11094中药材仓储管理规范《中华人民共和国药典》2020年版一部TCACM1021.70-2018中药材商品规格等级酸枣SB/T11182中药材包装技术规范3术语和定义下列术语和定义适用于本文件。
酸枣仁本品为鼠李科植物酸枣Ziziphus jujuba Mill.var.spinosa(Bunge)Hu ex H.F.Chou的干燥成熟种子。
4酸枣采收秋末(9月中下旬至10月中旬)冬初酸枣果皮颜色由青变红后,人工采摘新鲜、成熟的酸枣果实。
5产地加工5.1加工工艺鲜酸枣→果肉去除→果核干燥→破壳分筛→色选除杂→酸枣仁干燥→筛选分等。
5.2加工方法5.2.1果肉去除5.2.1.1干法去肉a)将鲜酸枣果实置于多层网带式干燥设备中烘干,要求烘房配有排湿装置,烘干温度50℃~60℃,干燥时间12~15h,烘至酸枣水分不高于15%。
b)经人工揉搓或对辊机器碾压酸枣果实,除去干燥果肉,过筛得到酸枣果核。
5.2.1.2湿法去肉a)将鲜酸枣果实放置在洁净的地面或晾晒台上摊薄晾晒,厚度不超4cm,每天翻动2~3次,晒至果实发软。
晾晒过程中注意检查,如有霉烂果实及时剔除。
如遇阴雨天,应及时放置在防雨通风处晾干,厚度不超过2cm,并加强翻动次数,防止雨水浇淋或雨水浸泡。
b)用饮用水(符合GB5749的要求)冲洗除去果核上残留的果肉,得到酸枣果核。
5.3果核干燥经干法去肉得到的酸枣果核直接进行破壳分筛,湿法去肉得到的酸枣果核需进行干燥处理。
YL-20180五味子原料检验操作规程

(1)显微鉴别
仪器与试剂:生物显微镜、酒精灯,水合氯醛、稀甘油等。
方法:取本品适量,用水合氯醛装片,置显微镜下观察:(1)本品横切面:外果皮为1列方形或长方形细胞,壁稍厚,外被角质层,散有油细胞;中果皮薄壁细胞10余列,含淀粉粒,散有小型外韧型维管束;内果皮为1列小方形薄壁细胞。种皮最外层为1列径向延长的石细胞,壁厚,纹孔和孔沟细密;其下为数列类圆形、三角形或多角形石细胞,纹孔较大;石细胞层下为数列薄壁细胞,种脊部位有维管束;油细胞层为1列长方形细胞,含棕黄色油滴;再下为3~5列小形细胞;种皮内表皮为1列小细胞,壁稍厚,胚乳细胞含脂肪油滴及糊粉粒。
分发部门: 质量部、 化验室、生产部
标 题
正 文
1
2
2.1
2.2
3
3.1
3.1.1
3.1.2
3.2
3.2.1
3.2.2
4
4.1
4.1.1
4.1.2
4.1.3
4.2
4.2.1
4.2.2
4.2.3
4.3
4.3.1
4.3.2
4.3.3
4.4
4.4.1
4.4.2
4.4.3
5
5.1
5.2
5.3
5.4
5.5
5.6
W样
式中:
W0----------- 坩埚重量(g)。
W1----------- 坩埚与灰分的重量(g)。
W样----------- 样品的重量(g)。
二氧化硫残留量:照二氧化硫残留量测定法(通则 2331)测定,不得过150mg/kg
仪器与试剂:两颈圆底烧瓶、电热套、竖式回流冷凝管、磁力搅拌器、分析天平、甲基红乙醇溶液指示剂、氢氧化钠滴定液滴、盐酸溶液(6mol/L)等。
YL-20060大枣原料检验操作规程
标 题
正 文
1
2
2.1
2.2
3
3.1
3.1.1
3.1.2
3.2
3.2.1
3.2.2
4
4.1
4.1.1
4.1.2
4.1.3
4.2
4.2.1
4.2.2
4.2.3
4.2.4
4.3
4.3.1
4.3.2
4.3.3
标准依据:《中国药典》2020年版一部及四部
【性状】
仪器:直Байду номын сангаас。
方法:取本品,置日光下观察,并用直尺测量:本品呈橢圆形或球形,长2~3.5cm,直径1.5~2.5cm。表面暗红色,略带光泽,有不规则皱纹。基部凹陷,有短果梗。外果皮薄,中果皮棕黄色或淡褐色,肉质,柔软,富糖性而油润。果核纺锤形,两端锐尖,质坚硬。气微香,味甜。
色谱条件与系统适用性试验以十八烷基硅烷键合硅胶为填充剂;以甲醇-乙腈-水(40:18:42)为流动相;采用柱后衍生法检测,①碘衍生法:衍生溶液为0.05%的碘溶液(取碘0.5g,加入甲醇100ml使溶解,用水稀释至1000ml制成),衍生化泵流速每分钟0.3ml,衍生化温度70℃;②光化学衍生法:光化学衍生器(254nm);以荧光检测器检测,激发波长=360nm(或365nm),发射波长λex=450nm。两个相邻色谱峰的分离度应大于1.5。
酸枣仁检测方法

酸枣仁检测方法酸枣仁总皂苷的含量测定操作规程B.1仪器和用具B.1.1紫外-可见分光光度仪B.1.2超声波清洗仪B.1.3分析天平:感量0.00001gB.2试剂和溶液B.2.1甲醇、香草醛、冰醋酸、高氯酸(均为分析纯)。
B.2.2酸枣仁皂苷A对照品。
B.3操作程序B.3.1标准品溶液制备精密称取于60℃减压2.67KPa以下干燥3小时的酸枣仁皂苷A对照品适量,加甲醇溶解,制成每1ml含1mg的溶液。
B.3.2供试品溶液制备精密称取酸枣仁提取物样品约1200mg于25mL容量瓶中,加入甲醇约20ml超声震荡30分钟,冷却至室温,用甲醇定容至刻度,摇匀用0.45μm微孔滤膜过滤,即得。
B.3.3试样的测定精密吸取对照品溶液及供试品溶液各200μL,分别置15ml具塞试管中,60℃水浴中挥干溶剂,精密加入新鲜配制的含5%香草醛冰醋酸溶液与高氯酸(2:8V/V)的混合液2ml,摇匀,密塞,置60℃水浴中加热15分钟,取出,立即放入冰水中冷却2分钟,精密加入冰醋酸定容至10ml,摇匀,以空白溶液作参比,于550nm波长处测定吸收度。
根据外标法依照以上操作数据计算含量。
酸枣仁皂苷A+B的含量测定操作规程C.1仪器和用具C.1.1高效液相色谱仪C.1.2超声波清洗仪C.1.3分析天平:感量0.0001gC.2试剂和溶液C.2.1水:双重蒸馏水。
C.2.2甲醇:分析纯;乙腈:色谱纯。
C.2.3酸枣仁皂苷A、B对照品:98%以上,使用前应在放有五氧化二磷的减压干燥器内干燥24小时。
C.3色谱条件及系统适用性C.3.1色谱柱:用十八烷基硅烷键合硅胶为填充剂。
C.3.2检测波长:204nm。
流速:1mL/min。
酸枣仁皂苷A峰的理论塔板数不得小于2000。
进样量20微升。
C.3.3流动相:乙腈:水=39:61V/V,用0.45μm滤膜过滤后使用。
C.4操作程序C.4.1对照品溶液的制备精密称取酸枣仁皂苷A、B对照品各约5mg于25mL容量瓶中,加入甲醇溶解定容至刻度。
酸枣仁水提物中药提取物

酸枣仁水提物中药提取物酸枣仁水提物【提取来源】本品为鼠李科植物酸枣Ziziphus jujubaMill. var. spinosa (Bunge) Hu ex H.F. Chou的种子水煎提取的水提物干粉。
【性状】本品为棕黄色至棕褐色粉末,有效成分可溶于甲醇、乙醇、热水。
【鉴别】取本品加甲醇制成5%溶液作供试液。
取酸枣仁标准对照药材1.0g加热水40ml,80℃超声提取30分钟,滤液蒸干,残渣加甲醇1ml溶解作对照液。
取上述二液各10μl,分别点于同一硅胶G板,一次点四板。
(1)以甲苯-乙酸乙酯-甲酸(6:10:1)展开,喷5%三氯化铝乙醇溶液,紫外灯365nm检视。
(2)以甲苯-丙酮-乙酸乙酯(5:2:1)展开,喷10%硫酸乙醇溶液,热风吹显。
(3)以甲苯-乙酸乙酯-水-甲酸(20:10:1:1)上层展开,紫外灯365nm检视,然后喷0.1%甲基红甲基橙溶液。
(4)以乙醇-正丁醇-水-丙酸(10:10:5:2)展开,喷0.5%茚三酮乙醇溶液,热风吹显。
以上四板,荧光斑点和可见光斑点对应率≥80%。
【检查】水分:不得过6.0%(附录Ⅸ H)灰分:不得过3.0%(附录Ⅸ K)重金属:不得过10ppm(附录Ⅸ E)砷盐:不得过2ppm(附录Ⅸ F)糊精:不得过2.0%(附录Ⅳ)【提取来源】本品5%热水溶液无沉淀,本品5%乙醇溶液有不溶性沉淀。
【浸出物】照水溶性浸出物测定法(附录X A)项下的热浸法测定,浸出率不少于94%。
【功能】镇静,催眠,抗惊,镇痛,降温,抗炎,抗焦虑,增强免疫,降血脂,降低血液黏度,增强记忆力。
用于心肌缺血、缺氧,烫伤,抑郁症。
【贮藏】阴凉,干燥,避光。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
4.5.2
4.5.3
4.5.4
4.5.5
4.5.6
4.5.7
4.6
4.6.1
4.6.2
4.6.3
5
5.1
5.1.1
5.1.2
5.1.3
5.1.4
5.1.5
5.2
5.2.1
5.2.2
5.2.3
5.2.4
5.2.5
标准依据:《中国药典》2020年版一部及四部
【性状】
仪器:直尺。
方法:取本品,置日光下观察,并用直尺测量:本品呈扁圆形或扁椭圆形,长5~9mm,宽5~7mm,厚约3mm。表面紫红色或紫褐色,平滑有光泽,有的有裂纹。有的两面均呈圆隆状突起;有的一面较平坦,中间有1条隆起的纵线纹;另一面稍突起。一端凹陷,可见线形种脐;另端有细小突起的合点。种皮较脆,胚乳白色,子叶2,浅黄色,富油性。气微,味淡。
B法取供试品粗粉1g,精密称定,置凯氏烧瓶中,加硝酸-高氯酸(4:1)混合溶液5~10ml,混匀,瓶口加一小漏斗,浸泡过夜。置电热板上加热消解,保持微沸,若变棕黑色,再加硝酸-高氯酸(4:1)混合溶液适量,持续加热至溶液澄明后升高温度,继续加热至冒浓烟,直至白烟散尽,消解液呈无色透明或略带黄色,放冷,转入50ml量瓶中,用2%硝酸溶液洗涤容器,洗液合并于量瓶中,并稀释至刻度,摇匀,即得。同法同时制备试剂空白溶液。
原料检验操作规程
题目:酸枣仁原药材检验操作规程
编号:TS-GC-YL-20890-02
制定人:
制定日期:2020年 月 日
版本:2
页数:1/4
审核人:
审核日期:2020年 月 日
颁发部门:质 量 部
批准人:
批准日期:2020年 月 日
生效日期:2020年 月 日
目的:规范酸枣仁原药材检验操作
范围:酸枣仁原药材检验操作
标准曲线的制备分别精密量取砷标准贮备液适量,用2%硝酸溶液稀释制成每1ml分别含砷0ng、5ng、10ng、20ng、30ng、40ng的溶液。分别精密量取10ml,置25ml量瓶中,加25%碘化钾溶液(临用前配制)1ml,摇匀,加10%抗坏血酸溶液(临用前配制)1ml,摇匀,用盐酸溶液(20→100)稀释至刻度,摇匀,密塞,置80℃水浴中加热3分钟,取出,放冷。取适量,吸入氢化物发生装置,测定吸收值,以峰面积(或吸光度)为纵坐标,浓度为横坐标,绘制标准曲线。
计算公式:
总灰分% = ×100%
式中:
W0----------- 坩埚重量(g)。
W1----------- 总灰分与坩埚的重量(g)。W
W样----------- 样品的重量(g)。
黄曲霉毒素照真菌毒素测定法(通则2351)测定。
本品每1000g含黄曲霉毒素B1不得过5μg,黄曲霉毒素G2、黄曲霉毒素G1、黄曲霉毒素B2和黄曲霉毒素B1的总量不得过10μg。
标准曲线的制备分别精密量取铅标准贮备液适量,用2%硝酸溶液制成每1ml分别含铅0ng、5ng、20ng、40ng、60ng、80ng的溶液。分别精密量取1ml,精密加含1%磷酸二氢铵和0.2%硝酸镁的溶液0.5ml,混匀,精密吸取20μ1注入石墨炉原子化器,测定吸光度,以吸光度为纵坐标,浓度为横坐标,绘制标准曲线。
分发部门: 质量部、 化验室、 生产部
标 题
正 文
1
2
2.1
2.1.1
3
3.1
3.1.1
3.1.2
3.2
3.2.1
3.2.2
3.3
3.3.1
3.3.2
4
4.1
4.1.1
4.1.2
4.1.3
4.2Байду номын сангаас
4.2.1
4.2.2
4.2.3
4.3
4.3.1
4.3.2
4.3.3
4.4
4.4.1
4.4.2
4.4.3
4.5
总灰分:不得过7.0%(通则2302)。
仪器:箱式电阻炉、分析天平、粉碎机、药筛、坩埚。
方法:取本品粉末3g,过二号筛混合均匀后,置炽灼至恒重的坩埚中,称定重量,(准确0.01g),缓缓炽热,注意避免燃烧,至完全炭化时,逐渐升高温度至500-600℃,使完全灰化至恒重。根据残渣重量,计算供试品中总灰分的含量(%)。
镉标准贮备液的制备精密量取镉单元素标准溶液适量,用2%硝酸溶液稀释,制成每1ml含镉(Cd)1μg的溶液,即得(0~5℃贮存)。
标准曲线的制备分别精密量取镉标准贮备液适量,用2%硝酸溶液稀释制成每1ml分别含镉Ong、0.8ng、2.0ng、4.0ng、6.0ng、8.0ng的溶液。分别精密吸取10μl,注入石墨炉原子化器,测定吸光度,以吸光度为纵坐标,浓度为横坐标,绘制标准曲线。
C法取供试品粗粉0.5g,精密称定,置瓷坩埚中,于电热板上先低温炭化至无烟,移入高温炉中,于500℃灰化5~6小时(若个别灰化不完全,加硝酸适量,于电热板上低温加热,反复多次直至灰化完全),取出冷却,加10%硝酸溶液5ml使溶解,转入25ml量瓶中,用水洗涤容器,洗液合并于量瓶中,并稀释至刻度,摇匀,即得。同法同时制备试剂空白溶液。
3.砷的测定(氢化物法)
测定条件采用适宜的氢化物发生装置,以含硼氢化钠和0.3%氢氧化钠溶液(临用前配制)作为还原剂,盐酸溶液(1→100)为载液,氮气为载气,检测波长为193.7nm。
砷标准贮备液的制备精密量取砷单元素标准溶液适量,用2%硝酸溶液稀释,制成每1ml含砷(As)1μg的溶液,即得(0~5℃贮存)。
仪器与试剂:光化学衍生器、离心机、荧光检测器检测等
本法系用高效液相色谱法(通则0512)测定药材、饮片及制剂中的黄曲霉毒素(以黄曲霉毒素B1、黄曲霉毒素B2、黄曲霉毒素G1和黄曲霉毒素G2总量计),除另有规定外,按下列方法测定。
色谱条件与系统适用性试验以十八烷基硅烷键合硅胶为填充剂;以甲醇-乙腈-水(40:18:42)为流动相;采用柱后衍生法检测,①碘衍生法:衍生溶液为0.05%的碘溶液(取碘0.5g,加入甲醇100ml使溶解,用水稀释至1000ml制成),衍生化泵流速每分钟0.3ml,衍生化温度70℃;②光化学衍生法:光化学衍生器(254nm);以荧光检测器检测,激发波长λex=360nm(或365nm),发射波长λex=450nm。两个相邻色谱峰的分离度应大于1.5。
方法:取供试品2-5g,平铺于干燥至恒重的扁形称量瓶中,厚度不超过5mm,疏松供试品不超过10mm,精密称定,打开瓶盖在100-105℃干燥5小时,将瓶盖盖好,移置干燥器中,冷却30分钟,精密称定重量,再在上述温度干燥1小时,冷却,称重至连续两次称重的差异不超过5mg为止。根据减失的重量,计算供试品中的含水量(%)。
供试品溶液的制备A法取供试品粗粉0.5g,精密称定,置聚四氯乙烯消解罐内,加硝酸3~5ml,混匀,浸泡过夜,盖好内盖,旋紧外套,置适宜的微波消解炉内,进行消解(按仪器规定的消解程序操作)。消解完余后,取消解内罐置电热板上缓缓加热至红棕色蒸气挥尽,并继续缓缓浓缩至2~3ml,放冷,用水转入25ml量瓶中,并稀释至刻度,摇匀,即得。同法同时制备试剂空白溶液。
供试品溶液的制备同铅测定项下供试品溶液的制备。
测定法精密吸取空白溶液与供试品溶液各10~20μ1,照标准曲线的制备项下方法测定吸光度(若供试品有干扰,可分别精密量取标准溶液、空白溶液和供试品溶液各1ml,精密加含1%磷酸二氢铵和0.2%硝酸镁的溶液0.5ml,混匀,依法测定),从标准曲线上读出供试品溶液中镉(Cd)的含量,计算,即得。
(2)薄层鉴别
仪器与试剂:分析天平、层析缸、三用紫外分析仪、硅胶G 薄层板酸枣仁皂苷A对照品等。
方法:取本品粉末1g,加甲醇30ml,加热回流1小时,滤过,滤液蒸干,残渣加甲醇0.5ml使溶解,作为供试品溶液。另取酸枣仁皂苷A对照品、酸枣仁皂苷B对照品,加甲醇制成每1ml各含1mg的混合溶液,作为对照品溶液。照薄层色谱法(通则0502)试验,吸取上述两种溶液各5μl,分别点于同一硅胶G薄层板上,以水饱和的正丁醇为展开剂,展开,取出,晾干,喷以1%香草醛硫酸溶液,立即检视。供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的斑点。
计算公式:
W样+W0-W1
样品含水量% = ×100%
式中:
W0 ----------------------------称量瓶的重量(g)。
W1---------------------------样品烘后与称量瓶的重量(g)。
W样 ---------------------------样品的重量(g)。
1.铅的测定(石墨炉法)
测定条件参考条件:波长283.3nm,干燥温度100~120℃,持续20秒;灰化温度400~750℃,持续20~25秒;原子化温度1700~~2100℃,持续4~5秒。
铅标准贮备液的制备精密量取铅单元素标准溶液适量,用2%硝酸溶液稀释,制成每1ml含铅(Pb)1μg的溶液,即得(0~5℃贮存)。
测定法分别精密吸取上述混合对照品溶液5μl、10μ1、15μl、20μl、25μl,注入液相色谱仪,测定峰面积,以峰面积为纵坐标,进样量为横坐标,绘制标准曲线。另精密吸取上述供试品溶液20~25μ1,注入液相色谱仪,测定峰面积,从标准曲线上读出供试品中相当于黄曲霉毒素B1、黄曲霉毒素B2、黄曲霉毒素G1、黄曲霉毒素G2的量,计算,即得。
【检查】
杂质(核壳等)不得过5%(通则2301)。
仪器:分析天平、药筛。
方法:取本品适量,挑拣杂质、药屑合并称重杂质量。
计算公式:
M1
杂质量=×100%
式中: M0
M0-------供试品重(g)
M1-------杂质重(g)
水分:不得过9.0%(通则0832第二法)。
仪器:电热鼓风干燥箱、分析天平、粉碎机、药筛等。
测定法精密量取空白溶液与供试品溶液各1ml,精密加含1%磷酸二氢铵和0.2%硝酸镁的溶液0.5ml,混匀,精密吸取10~20μl,照标准曲线的制备项下方法测定吸光度,从标准曲线上读出供试品溶液中铅(Pb)的含量,计算,即得。
