对叔丁基苯甲酸98-73-7
对叔丁基甲苯安全操作及保养规程

对叔丁基甲苯安全操作及保养规程一、前言叔丁基甲苯是一种广泛用于工业生产的有机化合物,具有强烈的挥发性和燃烧性,常用于溶解树脂、涂料、橡胶等合成材料。
但是,在使用叔丁基甲苯时,必须严格遵守安全操作规程,以保障自身安全和环境安全。
本文将详细介绍叔丁基甲苯的安全操作和保养规程。
二、基本概念1.叔丁基甲苯,化学式为C10H14,分子量为134.22,为无色液体。
2.叔丁基甲苯具有强烈的刺激性气味,可引起眼睛、喉咙、皮肤等部位的刺痛、灼热感和过敏反应。
3.叔丁基甲苯易于发生自燃和爆炸,在高温、火源条件下极易燃烧,产生有害气体和剧烈爆炸。
4.叔丁基甲苯易被皮肤吸收,进入血液循环系统后对内脏器官、神经系统、造血功能等造成严重影响。
三、安全操作规程1.严格遵守防火防爆措施。
在储存、搬运、使用叔丁基甲苯时,禁止使用明火、电器设备等易引发火源的物品,尽量避免与氧气、氢气等易于形成爆炸的物质接触。
2.穿戴防护装备。
操作人员应在使用前穿戴防护服、手套、防护眼镜、防毒面罩等必要的防护装备,避免直接接触叔丁基甲苯。
3.保持室内通风。
在操作过程中应尽量保持操作室内的空气流通,避免出现气味浓烈的情况。
4.避免误食误入。
叔丁基甲苯具有强烈的刺激性气味,应将其放置在离食品和易于误入口的物品远离的位置存放。
5.小心搬运。
在搬运叔丁基甲苯时,应尽量减少剧烈震荡和颠簸,避免产生火花或摩擦引发火源。
6.及时处理溢出、泄漏。
发现叔丁基甲苯泄漏时,应立即采取应急措施,将漏出的液体收集起来并进行处理,避免大面积泄漏对环境产生危害。
四、保养规程1.定期检查储存容器。
在储存叔丁基甲苯的容器上应注明其名称、生产日期、保质期等信息,并定期检查容器是否破损、泄漏、变质等情况。
2.保持存放环境干燥。
叔丁基甲苯应放置在阴凉、干燥的环境中,远离阳光直射和潮湿环境,避免受热变质。
3.定期更新物品。
过期、变质、瓶盖破损等情况的叔丁基甲苯应及时清理或更换。
4.定期维护仪器设备。
对叔丁基苯甲酸的合成

对叔丁基苯甲酸的合成
叔丁基苯甲酸是一种有机化合物,化学式为C11H14O2。
它是一种重要的有机中间体,广泛应用于医药、染料、香料等领域。
下面就对叔丁基苯甲酸的合成进行介绍。
一、叔丁基苯甲酸的合成方法
1. Friedel-Crafts反应法
Friedel-Crafts反应法是一种常用的制备叔丁基苯甲酸的方法。
具体步骤如下:
首先,将苯甲酸和叔丁基氯化铝加入反应瓶中,加热至反应温度,反应时间为数小时。
反应完毕后,将反应混合物酸化,得到叔丁基苯甲酸。
2. Grignard试剂法
Grignard试剂法也是一种制备叔丁基苯甲酸的方法。
具体步骤如下:
首先,将苯甲酸和溴丁烷在乙醚中反应,得到叔丁基苯甲酸丁酯。
然后,将叔丁基苯甲酸丁酯和镁粉在干乙醚中反应,得到Grignard试剂。
最后,将Grignard 试剂和二氧化碳反应,得到叔丁基苯甲酸。
二、叔丁基苯甲酸的应用
叔丁基苯甲酸是一种重要的有机中间体,广泛应用于医药、染料、香料等领域。
具体应用如下:
1. 医药领域:叔丁基苯甲酸可以用于制备一些药物原料,如对乙酰氨基酚、氨基酚等。
2. 染料领域:叔丁基苯甲酸可以用于制备染料中间体,如苯甲酸甲酯。
3. 香料领域:叔丁基苯甲酸可以用于制备香料中间体,如香叶醛。
三、叔丁基苯甲酸的安全性
叔丁基苯甲酸的毒性较低,但是对皮肤、眼睛等有刺激作用,应注意防护。
在使用过程中,应佩戴防护手套、护目镜等防护用品,避免接触皮肤和眼睛。
同时,应注意防火、防爆。
对叔丁基苯酚产品质量标准

对叔丁基苯酚产品质量标准叔丁基苯酚是一种重要的有机化合物,广泛应用于化工、医药、食品等领域。
其产品质量标准对于保障人们的生命健康及生产安全具有重要意义。
下面我就对叔丁基苯酚产品质量标准进行详细的制定和解释。
一、产品分类与定义叔丁基苯酚是一种白色结晶固体,化学名称为2-甲基-2-丙基苯酚,分子式为C10H14O,分子量为150.22。
按照不同用途,叔丁基苯酚可分为工业级叔丁基苯酚和医药级叔丁基苯酚两类产品。
工业级叔丁基苯酚主要用于防腐剂、合成酯等领域,医药级叔丁基苯酚主要用于医药制剂及医疗器械的消毒和杀菌。
二、产品质量指标(一)外观与色泽:工业级叔丁基苯酚应为白色结晶粉末,无明显杂质及色泽异物;医药级叔丁基苯酚应为白色结晶固体,无明显杂质及色泽异物。
(二)纯度:工业级叔丁基苯酚纯度不低于99%,医药级叔丁基苯酚纯度不低于99.5%。
(三)水分:工业级叔丁基苯酚水分不高于0.5%,医药级叔丁基苯酚水分不高于0.3%。
(四)杂质:任何杂质的含量均不得高于0.1%。
(五)重金属:铅、砷、汞等重金属的含量不得超过国家标准规定的限量。
三、产品检测方法(一)外观与色泽:肉眼观察。
(二)纯度:采用气相色谱法(GC)或高效液相色谱法(HPLC)进行检测,确保叔丁基苯酚的纯度符合标准要求。
(三)水分:采用称量法或干燥法进行检测,得出叔丁基苯酚的水分含量。
(四)杂质:采用化学分析法或质谱法进行检测。
(五)重金属:采用原子吸收光谱法(AAS)或电感耦合等离子体发射光谱法(ICP)进行检测,确保叔丁基苯酚中重金属含量符合标准要求。
四、产品包装与储存叔丁基苯酚产品应采用密封包装,防潮、防晒、防高温,并标有产品名称、规格、生产日期、批号等信息。
储存应放置于清洁、干燥、通风的仓库中,远离火种、热源及有毒有害气体,避免与酸碱、氧化剂等混存。
五、产品质量控制生产企业应遵循国家相关法律法规和标准,建立健全质量管理体系,严格控制原料采购、生产工艺和产品出厂检验,确保叔丁基苯酚产品的质量稳定可靠。
200种化学品理化特性表(83页)

200种化学品目录丙烯酸丁酯的理化及危险特性表 (1)丙烯酸的理化及危险特性表 (2)硝酸锌的理化及危险特性表 (3)过氧化二苯甲酰的理化及危险特性表 (4)过硫酸铵的理化及危险特性表 (5)丁酮的理化及危险特性表 (6)苯酚的主要理化和危险特性 (7)甲基叔丁基醚的主要理化及危险特性 (8)三聚氰酸的主要理化和危险特性 (9)季戊四醇的主要理化和危险特性 (10)硬脂醇的主要理化和危险特性 (11)多聚甲醛的主要理化和危险特性 (12)1,2-二甲苯的主要理化及危险特性 (13)1,3-二甲苯的主要理化及危险特性 (14)1,4-二甲苯的主要理化及危险特性 (15)环己烯的主要理化和危险特性 (16)二丁胺的主要理化和危险特性 (17)三乙胺的主要理化和危险特性 (18)甲基二氯硅烷的主要理化和危险特性 (19)异丁烯的主要理化和危险特性 (20)邻叔丁基苯酚的主要理化和危险特性 (21)对叔丁基苯酚的主要理化和危险特性 (22)环己烷的主要理化和危险特性 (23)二氯甲烷的主要理化和危险特性 (24)三氯甲烷的主要理化及危险特性 (25)硫脲的主要理化和危险特性 (26)六亚甲基四胺的主要理化和危险特性 (27)抗氧剂AT-10的主要理化和危险特性 (28)抗氧剂AT-76的主要理化和危险特性 (29)抗氧剂AT-3114的主要理化和危险特性 (30)催化剂JH-CMMS的主要理化和危险特性 (31)抗氧剂AT-168的主要理化和危险特性 (32)甲氧基钠的主要理化和危险特性 (33)氧气的理化及危险特性 (34)硝酸钾的理化及危险特性表 (35)硝酸钙的理化及危险特性表 (36)液氯的理化及危险特性 (37)盐酸的理化及危险特性 (38)丙酮理化及危险特性表 (39)次氯酸钠的理化及危险特性表 (40)二甲氧基甲烷的理化及危险特性表 (41)乙酸的理化及危险特性表 (42)香蕉水的理化及危险特性表 (43)甲醇的理化及危险特性表 (44)氰化亚铜的理化及危险特性 (45)硝酸的理化及危险特性 (46)硫酸的理化及危险特性 (47)铬酸的理化及危险特性 (48)铬酸酐的理化及危险特性 (49)氰化钠的理化及危险特性 (50)丁醇的理化及危险特性 (51)异丙醇的的理化及危险特性 (52)硝酸银的理化及危险特性表 (53)间戊二烯的理化及危险特性 (54)环戊二烯的理化及危险特性 (55)甲苯二异氰酸酯的理化及危险特性表 (56)200#溶剂油的理化及危险特性表 (57)聚氨酯漆固化剂理化及危险特性表 (58)聚氨酯漆稀释剂理化及危险特性表 (59)N,N--二甲基甲酰胺理化及危险特性 (60)丙烯腈理化及危险特性 (61)二氧化硫的特性 (62)异戊二烯的理化及危险特性 (63)醋酸丁酯的理化及危险特性 (64)醋酸乙酯的理化及危险特性 (65)甲苯的理化及危险特性 (66)环己酮的理化及危险特性 (67)三氯化铝(无水)的理化及危险特性 (68)氢氧化钠的理化及危险特性 (69)硝酸铅的理化及危险特性表 (70)电石理化及危险特性表 (71)乙炔理化及危险特性表 (72)氰化亚铜的理化及危险特性 (73)丙烯酸甲酯理化及危险特性................ 错误!未定义书签。
对叔丁基苯酚用途

对叔丁基苯酚用途1. 叔丁基苯酚简介叔丁基苯酚,化学式为C10H14O,是一种有机化合物。
它是苯酚的衍生物,具有叔丁基取代基。
叔丁基苯酚是一种无色结晶固体,在常温下稳定。
它具有一系列的物理和化学性质,使其在多个领域有广泛的应用。
2. 工业上的应用2.1 防腐剂叔丁基苯酚在工业上被广泛用作防腐剂。
由于其抗氧化和抗菌性能,它可以有效地延长产品的寿命。
叔丁基苯酚常被添加到润滑油、塑料和橡胶制品中,以防止其在制造、储存和使用过程中受到微生物的侵蚀和分解。
2.2 橡胶工业叔丁基苯酚在橡胶工业中也扮演着重要的角色。
它可以作为橡胶的抗老化剂和稳定剂使用,能够阻止橡胶在阳光、氧气和湿气的作用下发生老化和劣化。
叔丁基苯酚可以提高橡胶制品的耐候性和耐久性,延长其使用寿命。
2.3 化妆品叔丁基苯酚也被广泛应用于化妆品中。
它具有抗氧化和抗菌的特性,可以作为防腐剂和抗菌剂添加到化妆品中,保护产品不受细菌和其他微生物的污染。
叔丁基苯酚在护肤品、洗发水、沐浴露等产品中得到广泛应用。
3. 医药领域的应用3.1 消毒剂叔丁基苯酚在医药领域被用作消毒剂。
由于其抗菌性能,它可以有效地杀灭细菌、病毒和真菌,预防感染的发生。
叔丁基苯酚常被用于制备手部消毒剂、医疗器械消毒剂和伤口消毒剂等。
3.2 抗菌药物叔丁基苯酚还可以用于制备抗菌药物。
它的抗菌性能使其成为制备抗菌药物的重要原料。
叔丁基苯酚衍生物的合成和研究为抗菌药物的研发提供了重要的基础。
3.3 抗氧化剂叔丁基苯酚在医药领域还被用作抗氧化剂。
它具有抗氧化性能,可以保护细胞免受自由基的损害。
叔丁基苯酚可以用于制备抗氧化剂类药物,用于治疗一些与氧化应激相关的疾病。
4. 其他应用领域4.1 食品工业叔丁基苯酚在食品工业中也得到了应用。
它可以用作食品添加剂,增强食品的抗氧化性能,延长食品的保质期。
叔丁基苯酚被广泛添加到食用油、食品包装材料和肉制品等食品中。
4.2 环境保护叔丁基苯酚还可以用于环境保护。
GBT 22731-2008 日用香精禁限用物质清单

45 䓝-二烯-甲醇甲酸酯[2-(4-异丙基环己二烯)乙醇甲酸酯] 68683-20-5 46 3-丙叉基苯肽 47 庚炔羧酸甲酯 48 辛炔羧酸甲酯 49 橡苔提取物 50 树苔提取物 17369-59-4 111-12-6 111-80-8 90028-68-5 9005-50-4 90028-67-4 68648-41-9
附录B
日用香精中限用的香料及其在十一类加香产品中的最高限量
序号 中文名 1 2 3 4 5 6 7 8 9 α-戊基肉桂醇 α-戊基肉桂醛 大茴香醇 苄醇 苯甲酸苄酯 肉桂酸苄酯 水杨酸苄酯 对叔丁基二氢肉桂醛 对叔丁基-α-甲基氢化肉桂醛 CAS号 101-85-9 122-40-7 105-13-5 100-51-6 120-51-4 103-41-3 118-58-1 18127-01-0 80-54-6 105-54-1 104-55-2 539-40-5 141-27-5 106-22-9 1117-61-9 97-53-0 4602-84-0 106-24-1 6728-26-3 101-86-0 6259-76-3 107-75-5 1335-66-6 1423-46-7 68527-77-5 97-54-1 86803-90-9 93-51-6
141-05-9 119-84-6 6248-20-0 17874-34-9 40607-48-5 617-54-9 122-39-4 —
110-80-5 111-15-9 109-86-4 110-49-6 68916-52-9 623-15-4 5146-66-7 5585-39-7 18829-55-5 700-82-3 67746-30-9 183622-62-8 150-76-5 78-59-1 34131-99-2 85085-26-3 54814-64-1 8014-71-9 531-59-9 104-27-8
对叔丁基苯酚检测方法

对叔丁基苯酚Para-tertiary butyl phenol1 范围本标准规定了对叔丁基苯酚的技术要求、试验方法、检验规则和标志、包装、运输、贮存。
本标准适用于异丁烯、苯酚在催化剂作用下合成的对叔丁基苯酚。
分子式:C1O H14O。
结构式:相对分子质量:150.21(1995年国际相对原子质量)。
2 引用标准下列标准所包含的条文,通过在本标准中引用而构成为本标准的条文。
本标准出版时,所示版本均为有效。
所有标准都会被修订,使用本标准的各方应探讨使用下列标准最新版本的可能性。
GB/T 6678-1986 化工产品采样总则GB/T 6679-1986 固体化工产品采样通则GB/T 6682-1992 分析实验室用水规格和试验方法GB/T 9722-1988 化学试剂气相色谱法通则3 技术要求3.1 外观:白色至浅黄色薄片。
3.2 对叔丁基苯酚应符合表1的要求。
表1 对叔丁基苯酚的技术要求4 试验方法4.1 凝固点的测定4.1.1 测定装置凝固点的测定装置如图1所示,单位:mm。
a—空气保护管;b—凝固点测定管;c—标线;d—浴槽;e—搅拌;f—温度计;g—温度计;h—辅助温度计图1 凝固点的测定装置4.1.2 仪器a) 空气保护管:用玻璃制备,内外两壁均涂上防止模糊的硅油。
b) 凝固点测定管:材质为硬质玻璃管,管的内壁涂上防止模糊的硅油,但在接近试样的部分不涂硅油,插人空气保护管中,用软木塞固定。
c) 标线:试样液面的有限高度。
d) 浴槽:玻璃制容器,用作盛装传热液。
e) 搅拌:玻璃制遣,直径Ф= 3mm,下端为圈状,外径约18mm。
f) 温度计:水银玻璃温度计,温度范围70~110℃,最小分度值0.1℃。
g) 温度计:水银玻璃温度计,温度范围0~120℃,最小分度值0.5℃。
h) 辅助温度计:规格同g),其水银球放在试样的上面与温度计f)所示温度(凝固点温度)的中间位置。
4.1.3 浴液a) 加热浴液:水、甘油、磷酸三苯脂、植物油、硫酸等。
第三章精细化工篇(可编辑)

第三章精细化工篇第三章精细化工篇1、二硫化钼102、二甲基酮肟113、二甲基硅油114、二甲基丙烯酸乙二醇酯 125、二甲苯磺酸钠126、对叔丁基苯甲酸137、碘化钠 138、碘化钾 149、二丙二醇1510、一缩二丙二醇单甲醚1511、二丙二醇甲醚醋酸酯1612、正己烷1613、正辛醇1714、正己醇1715、己二胺1816、正丙醇1817、正己醇1918、正十三醇2019、正戊醇2020、硅油2021、富马酸二甲酯 2122、富马酸2123、二乙烯基砜2224、二乙二醇丁醚 2225、二氧化锡2326、二羟甲基丙酸 2327、甲基羟乙基纤维素2428、甲基丙烯酰氯 2429、甲基丙烯酸缩水甘油酯2430、甲醇钠2531、己二酸2632、己二酸二酰肼 2633、磺基水杨酸2634、磺胺嘧啶2735、环戊烯2736、环戊胺2837、环己醇2938、环己胺2939、甘露醇3040、甘氨酸又称:氨基乙酸、氨基醋酸、乙氨酸3041、联苯3142、壳聚糖3243、均苯四甲酸二酐3344、聚乙烯蜡3345、聚乙烯吡咯烷酮3446、聚维酮碘3547、聚己内酯3548、聚丙二醇3649、焦碳酸二乙酯 3650、间苯二芬3651、甲壳素3752、甲基乙烯酮3853、甲基纤维素3954、柠檬酸铁3955、吗啉4056、马来酸4057、氯化亚锡4158、硫化锌4259、硫代二甘酸4260、磷酸三乙酯4261、磷酸三丁酯4362、邻二氯苯4463、邻苯二甲酸二乙酯4564、邻苯二甲酸二甲酯4565、三氟甲磺酸4666、三氟醋酸4667、三醋酸甘油酯 4768、三苯基氯硅烷 4769、三苯基硅烷4870、乳糖4871、鞣花酸4872、茄尼醇4973、羟乙基纤维素 4974、硼氢化钠5075、三异丙基氯硅烷5176、三乙烯二胺5177、三乙基氯硅烷 5178、三乙基硅烷5279、三聚甲醛5280、三甲基溴硅烷 5381、三甲基氯硅烷 5382、三甲基碘硅烷 5483、三氯乙酸5484、三氯乙醇5585、三氟甲磺酸酐 5586、碳酸二苯酯5687、四氢吡咯5788、水杨酸苯酯5789、水合肼5890、水杨醛5891、叔丁基二甲基氯硅烷5992、叔丁基二苯基氯硅烷5993、叔丁醇钠5994、叔丁醇钾6095、叔丁醇6096、叔丁胺6197、吲哚6298、异戊醇6299、异佛尔酮二胺 63 100、异佛尔酮63101、异丁酸63102、异丁醛64103、异丙醇胺65104、乙酰氯66105、乙酰丙酮66106、乙二胺67107、乙酰苯胺67108、乙烯砜68109、乙炔黑68110、乙醛酸69111、乙基纤维素69 112、月桂酸70113、原乙酸三乙酯71 114、原乙酸三甲酯71 115、原甲酸三甲酯72 116、原甲酸三乙酯72 117、巴豆酸甲酯73 118、芥酸酰胺73119、原丁酸三乙酯74 120、原丁酸三甲酯74 121、原丙酸三乙酯75122、油酸酰胺75123、油醇 76124、吲哚乙酸76125、吲哚丁酸77126、胡椒基丁醚78 127、植酸 78128、正戊酸79129、正十二硫醇79 130、正丁酸80131、正丁醛81132、多乙烯多胺82 133、对硝基苯酚82 134、对甲基苯甲醛83 135、对碘甲苯83136、对苯醌二肟84 137、丁香酸85138、丁香醛85139、丁烯酮85140、丁二酸酐86141、碘苯 87142、氮酮 87143、丙烯酰胺88144、吡啶 89145、大茴香醛89146、大茴香醇90147、丙二酸91148、丙酸酐92149、草酰氯92150、丙烯酰氯93151、醋酸正丙酯93152、醋酸异丁酯94153、醋酸洗必泰94154、丙烯酸叔丁酯95 155、丙二腈95156、丙二醇96157、丙二醇甲醚醋酸酯96 158、苯酐 97159、苯扎溴铵97160、苯氧乙醇98161、苯乙酮98162、苯扎氯铵99163、苯甲醇99164、苯甲酰氯100165、苯妥英钠101166、胞嘧啶101167、氨基甲酸乙酯102 167、氨基甲酸甲酯102 168、阿斯巴甜103169、S-甲基异硫脲硫酸盐 103 170、N-甲基吗啉104171、N-乙基吗啉104172、N-溴代琥珀酰亚胺105173、N-氯代琥珀酰亚胺105174、N-羟甲基丙烯酰胺106175、N-甲基吡咯烷酮106176、N,N′-亚甲基双丙烯酰胺107 177、二苯甲烷二异氰酸酯 108178、5-硝基糠醛108179、2,4,6-三二甲氨基甲基苯酚109 180、DL-苹果酸109181、B(2)-巯基乙醇110182、B-环糊精111183、4-氨基吡啶111184、2,2-联吡啶112185、4,4-联吡啶112186、3-氨基吡啶113187、3-羟基吡啶113188、1,3-丁二醇114189、丙二醇114190、1,3-戊二醇115191、1,2-环己二胺115192、1,3-二氧戊环116193、1,4-丁烯二醇116194、1,4-二氧六环117195、1,6-已二醇117196、18-冠醚-6 118197、2,2-二甲基琥珀酸酐 119 198、二氯甲烷119199、醋酸丁酯119200、双酚A 120201、苯酐 120202、环氧氯丙烷120203、顺酐 121204、AES 121205、胡椒基丁醚122206、二辛酯122207、四氢呋喃122208、甲烷磺酰氯123209、环氧氯丙烷123210、N,N-二甲基乙醇胺124 211、甲基叔丁基醚124 212、四氢呋喃125213、二甲基亚砜125214、邻甲酚125215、间甲酚126216、对甲酚126217、间苯二酚127218、对苯二酚127219、叔丁胺127220、吗啉 128221、N-甲基吗啉128 222、三乙胺128223、二乙胺129224、乙二胺129225、一乙醇胺129226、二乙醇胺130227、三乙醇胺130228、二乙烯三胺131 229、三乙烯四胺131 230、三乙烯二胺131 231、多乙烯多胺132 232、N-氨乙基哌嗪132 233、PTMG 133234、IPDI 133235、1,6-己二醇133 236、哌嗪 134237、N-甲基哌嗪134 238、己二胺134239、环己胺135240、巯基乙酸135241、乙硫醇135242、环丁砜136243、正十二硫醇136 244、叔十二硫醇137 245、DAP单体 137246、N-甲基吡咯烷酮138 247、α-吡咯烷酮 138248、异丙醚139249、γ-丁内酯139250、吡啶 140251、六氢吡啶140252、3-甲基吡啶141253、3-氰基吡啶141254、2,4,6-三甲基吡啶141 255、丁二酸酐142256、乙二胺四乙酸142 257、EDTA二钠盐143258、EDTA四钠143259、β-羟乙基乙二胺144 260、N,N-二乙基羟胺144 261、甲基丙烯酸羟乙酯145 262、甲基丙烯酸羟丙酯145 263、甲基丙烯酸十四酯146 264、丙烯酸叔丁酯146 265、甲基丙烯酸月桂酯146 266、邻乙氧基苯甲酰氯147 267、三苯基磷147268、咪唑 147269、丙酸酐148270、甲基磺酰氯148271、乙二醛149272、戊二醛149273、聚乙烯基吡咯烷酮150 274、甲基丙烯酸环氧丙酯 151 275、DMF 151276、油酸酰胺152277、四氢吡咯152278、邻氨基苯甲酸153 279、山梨醇153280、甘露醇154281、BHT 155282、三氟乙酸155283、辛酸亚锡156284、MDI 156285、TDI 157286、叔辛胺157287、甲酰胺158288、苯骈三氮唑159289、邻氯苯甲醛159290、乙萘酚160291、甲萘酚160292、三正丁胺161293、正丁胺162294、乙酰氯162295、丁酰氯163296、戊酰氯164297、草酰氯164298、联苯 164299、庚酰氯165300、D-酒石酸165301、喹啉 166302、8-羟基喹啉166 303、间苯二甲酸167 304、DMT 168305、1,4-萘醌168306、丙二酸二乙酯169 307、丙二酸二甲酯169 308、多聚甲醛170309、正辛酸171310、癸酸 171311、癸二酸172312、二甲基硅油172 313、含氢硅油172314、D4 173315、三甲基氯硅烷173 316、白碳黑173317、2-氨基吡啶174 318、2-戊酮175319、邻苯二胺175320、间苯二胺176321、缩二脲176322、乙酰乙酸乙酯177 323、乙酰乙酸甲酯177 324、醋酸异丙烯酯178 325、原甲酸三甲酯178 326、氯甲酸甲酯179327、氯甲酸乙酯179328、二甲基酮肟180329、对硝基苯酚180330、邻硝基苯酚181331、1,4-二氧六环182 332、硫酸二乙酯182333、硫酸羟胺183334、异丙胺183335、二正丁胺184336、苯磺酰氯185337、碳酸二甲酯185338、碳酸二乙酯186339、硼氢化钠186340、硼氢化钾187341、邻苯二甲酸二甲酯187 342、邻苯二甲酸二乙酯188 343、邻苯二甲酸二丁酯189 344、异佛尔酮189345、MIBK 190346、二乙二醇二甲醚190347、愈创木酚191348、水杨酸191349、水杨酸钠192350、水杨酸甲酯193351、水杨酸苯酯193352、水杨酰胺194353、阿司匹林194354、氯化亚砜195355、十溴联苯醚195356、间苯三酚196357、L-半胱氨酸盐酸盐196 358、糠醛 197359、糠醇 197360、正庚醇198361、正戊醇199362、2,3-二溴-1,4-丁烯二醇199 363、胸腺嘧啶200364、丙烯酸甲酯200365、丙烯酸乙酯201366、丙烯酸羟丙酯201367、偶氮二异丁腈202368、NP-9 202369、油酸乙酯203370、乌洛托品203371、聚乙烯醇204372、蓖麻油204373、A-171硅烷偶联剂205 374、DOA 205375、TOTM 206376、环氧大豆油206377、乙酰丙酮207378、正戊酸207379、香柠檬油208380、硼酸三甲酯208381、醋酸乙酯208382、三丁基氯化锡209 383、硫脲 209384、二氧化硫脲210385、对甲基苯磺酸211 386、环己酮211387、山梨酸钾212388、偏苯三酸酐212389、磷酸三丁酯213390、邻甲苯胺213391、聚乙二醇214392、鞣酸 214393、单宁酸215394、没食子酸丙酯216 395、焦性没食子酸217396、苯肼 217397、丙炔醇217398、对氯苯甲醛218399、二丙酮醇219400、氯仿 219401、百里酚酞220402、丙烯酸丁酯220403、丙烯酸羟乙酯221 404、丙烯酸异辛酯222 405、甲基丙烯酸异辛酯222 406、新戊二醇222407、油酸甲酯223408、油酸丁酯223409、DIOP 224410、DINP 224411、DOS 225412、聚丙烯酸钠225413、薄荷脑226414、聚丙烯酰胺227415、OP,NP 228416、原甲酸三乙酯228 418、棕榈油229419、氢化植物油229420、天那水229421、13X分子筛229422、活性氧化铝230423、分子筛活化粉230424、甲基丙烯酸十八酯2301、二硫化钼英文:Molybdenum disulf分子式:MoS2?分子量:160.07类别:无机盐物化性质:黑灰色稍带银灰色光泽的粉末。
对叔丁基邻苯二酚-安全技术说明书MSDS

第一部分化学品及企业标识化学品中文名:对叔丁基邻苯二酚化学品英文名:4-tert-butylpyrocatecholCASNo.:98-29-3分子式:C10H14O2产品推荐及限制用途:工业及科研用途。
第二部分危险性概述紧急情况概述吞咽或皮肤接触有害。
造成严重皮肤灼伤和眼损伤。
可能导致皮肤过敏反应。
对水生生物毒性极大。
对水生生物有毒并具有长期持续影响。
GHS危险性类别急性经口毒性类别4急性经皮肤毒性类别4皮肤腐蚀/ 刺激类别1B皮肤致敏物类别1严重眼损伤/ 眼刺激类别1危害水生环境——急性危险类别1危害水生环境——长期危险类别2标签要素:象形图:警示词:警告危险性说明:H302+H312 吞咽或皮肤接触有害H314 造成严重皮肤灼伤和眼损伤H317 可能导致皮肤过敏反应H400 对水生生物毒性极大H411 对水生生物有毒并具有长期持续影响●预防措施:——P264 作业后彻底清洗。
——P270 使用本产品时不要进食、饮水或吸烟。
——P280 戴防护手套/穿防护服/戴防护眼罩/戴防护面具。
——P260 不要吸入粉尘/烟/气体/烟雾/蒸气/喷雾。
——P261 避免吸入粉尘/烟/气体/烟雾/蒸气/喷雾。
——P272 受沾染的工作服不得带出工作场地。
——P273 避免释放到环境中。
●事故响应:——P301+P312 如误吞咽:如感觉不适,呼叫解毒中心/医生——P330 漱口。
——P302+P352 如皮肤沾染:用水充分清洗。
——P312 如感觉不适,呼叫解毒中心/医生——P362+P364 脱掉沾染的衣服,清洗后方可重新使用——P301+P330+P331 如误吞咽:漱口。
不要诱导呕吐。
——P303+P361+P353 如皮肤沾染:立即脱掉所有沾染的衣服。
用水清洗皮肤/淋浴。
——P363 沾染的衣服清洗后方可重新使用。
——P304+P340 如误吸入:将人转移到空气新鲜处,保持呼吸舒适体位。
——P310 立即呼叫解毒中心/医生——P305+P351+P338 如进入眼睛:用水小心冲洗几分钟。
危险化学药品包括范围:

危险化学药品包括范围:1、闪点在45℃及45℃以下易燃液体(如:乙醚、汽油、二硫化碳、丙酮、苯、乙醇、丁醇等)。
2、易燃、容易自燃及遇水燃烧的固体(如:赤磷、黄磷、钾、钠、电石等)。
3、易燃及助燃气体(如:氢气、乙炔气、煤气、氧气等)。
4、易燃药品及能成为爆炸混合物或引起燃烧的氧化剂(如:氯酸钾、氯酸钠、硝酸钾、过氧化钠、硝酸等)。
5、腐蚀性药品(如:强酸、强碱、溴、甲醛、氢氧化钠等)。
6、剧毒药品及放射性药品。
剧毒品目录:(详细目录参见后面所附国家剧毒化学品目录(2012版))主要包括范围:氰化物砷化物氯化物磷化锌磷化铝氰酸硒黑硒粉巴豆醋酸铍氯饿酸铵醋酸苯汞苯甲氰醇四乙基铅马钱子碱汞及其化合物铊及其化合物亚硫酸糊剂灭散白蚊酸酚有机剧毒锡类硫酸二甲脂四羧基镍及其它羧基化合物醋酸铊及其它有机铊盐对硫磷及其它有机磷剧毒农药易制毒化学品名录:第一类1.1-苯基-2-丙酮2.3,4-亚甲基二氧苯基-2-丙酮3.胡椒醛4.黄樟素5.黄樟油6.异黄樟素7.N-乙酰邻氨基苯酸8.邻氨基苯甲酸9.麦角酸*10.麦角胺*11.麦角新碱*12.麻黄素、伪麻黄素、消旋麻黄素、去甲麻黄素、甲基麻黄素、麻黄浸膏、麻黄浸膏粉等麻黄素类物质*第二类1.苯乙酸2.醋酸酐3.三氯甲烷4.乙醚5.哌啶第三类1.甲苯2.丙酮3.甲基乙基酮4.高锰酸钾5.硫酸6.盐酸说明:一、第一类、第二类所列物质可能存在的盐类,也纳入管制。
二、带有*标记的品种为第一类中的药品类易制毒化学品,第一类中的药品类易制毒化学品包括原料药及其单方制剂。
剧毒化学品目录(2012版)一、剧毒化学品的判定界限1.剧毒化学品的定义剧毒化学品是指具有非常剧烈毒性危害的化学品,包括人工合成的化学品及其混合物(含农药)和天然毒素。
2.剧毒化学品毒性判定界限大鼠试验,经口LD50≤50mg/kg,经皮LD50≤200mg/kg,吸入LC50≤500ppm(气体)或2.0mg/L(蒸气)或0.5mg/L(尘、雾),经皮LD50的试验数据,可参考兔试验数据。
4-叔丁基苯酚(对叔丁基苯酚;对特丁基苯酚;4-羟基-1-叔丁基苯)的理化性质及危险特性表
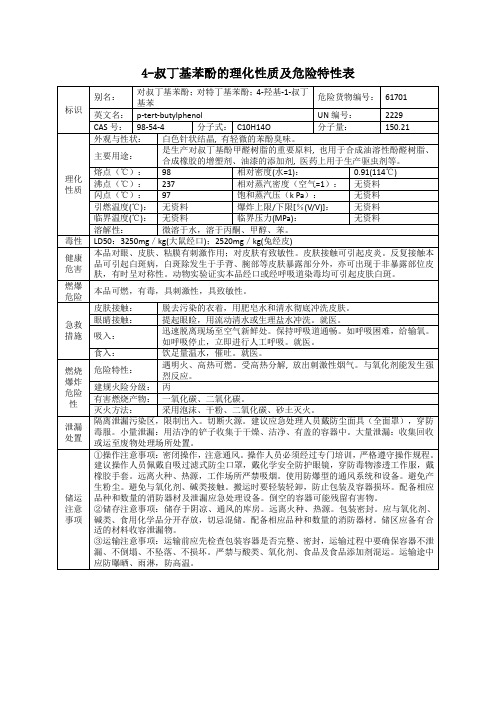
①操作注意事项:密闭操作,注意通风。操作人员必须经过专门培训,严格遵守操作规程。建议操作人员佩戴自吸过滤式防尘口罩,戴化学安全防护眼镜,穿防毒物渗透工作服,戴橡胶手套。远离火种、热源,工作场所严禁吸烟。使用防爆型的通风系统和设备。避免产生粉尘。避免与氧化剂、碱类接触。搬运时要轻装轻卸,防止包装及容器损坏。配备相应品种和数量的消防器材及泄漏应急处理设备。倒空的容器可能残留有害物。
爆炸上限/下限[%(V/V)]:
无资料
临界温度(℃):
无资料
临界压力(MPa):
无资料
溶解性:
微溶于水,溶于丙酮、甲醇、苯。
毒性
LD50:3250mg/kg(大鼠经口);2520mg/kg(兔经皮)
健康危害
本品对眼、皮肤、粘膜有刺激作用;对皮肤有致敏性。皮肤接触可引起皮炎。反复接触本品可引起白斑病,白斑除发生于手背、腕部等皮肤暴露部分外,亦可出现于非暴露部位皮肤,有时呈对称性。动物实验证实本品经口或经呼吸道染毒均可引起皮肤白斑。
主要用途:
是生产对叔丁基酚甲醛树脂的重要原料,也用于合成油溶性酚醛树脂、合成橡胶的增塑剂、油漆的添加剂,医药上用于生产驱虫剂等。
熔点(℃):
98
相对密度(水=1):
0.91(114℃)
沸点(℃):
237
相对蒸汽密度(空气=1):
无资料
闪点(℃):
97
饱和蒸汽压(k Pa):
无资料
引燃温度(℃):
无资料
危险特性:
遇明火、高热可燃。受高热分解,放出刺激性烟产物:
一氧化碳、二氧化碳。
灭火方法:
采用泡沫、干粉、二氧化碳、砂土灭火。
泄漏处置
隔离泄漏污染区,限制出入。切断火源。建议应急处理人员戴防尘面具(全面罩),穿防毒服。小量泄漏:用洁净的铲子收集于干燥、洁净、有盖的容器中。大量泄漏:收集回收或运至废物处理场所处置。
对叔丁基苯甲酸的制备工艺

二苯醚的制备工艺由氯苯与苯酚在苛性碱溶液中,以铜为催化剂缩合而得。
氢氧化钾、苯酚、氯苯按摩尔比配比1:1.4:1.06混合,加入铜粉,搅拌加热进行缩合反应。
反应结束后,用酸处理,分出二苯醚油层,经减压蒸馏得到二苯醚成品。
也可将氯苯和苯酚在氢氧化钠溶液中反应。
二苯醚的另一工业来源是作为氯苯水解制苯酚时的副产品。
用氢氧化钠进行氯苯水解的过程中,约有10%的氯苯转化成二苯醚,有些工艺这个比例可达20%。
通过萃取精制即得二苯醚产品。
对叔丁基苯甲酸的制备工艺一种对叔丁基苯甲酸的制备工艺,其特征在于:包括以下步骤:(1)、将甲苯、异丁烯和浓硫酸加入到反应釜中进行烷基化反应,得到粗品对叔丁基甲苯,烷基化反应的温度为20-24℃,时间为10-12小时,然后将粗品对叔丁基甲苯进行精馏得到对叔丁基甲苯;(2)、将制得的对叔丁基甲苯和复合催化剂加入到反应釜中通入氧气进行氧化反应,得到对叔丁基苯甲酸粗品,反应温度为110-180℃,时间为12-24小时,所述的复合催化剂由醋酸钴和溴化物组成,分别加入反应釜中;(3)、将对叔丁基苯甲酸粗品降温结晶、离心甩干,用对叔丁基甲苯进行清洗,然后将对叔丁基苯甲酸粗品加入甲苯中,升温溶解,再加入活性炭、硅藻土进行脱色,然后降温、结晶、离心,得对叔丁基苯甲酸精品;(4)、将对叔丁基苯甲酸精品经水洗后,用甲苯浇洗、离心、干燥,得对叔丁基苯甲酸成品。
一种合成对异丙基苯酚的新方法研究采用5%Pd/C作为转移氢催化剂,4-异丙基环己烯酮为氢给予剂,工业双戊烯为氢接受剂和溶剂进行反应,合成了对异丙基苯酚.考察了催化剂用量、反应时间和反应温度对反应的影响,确定了合成对异丙基苯酚的最佳反应条件:原料与5%Pd/C的配比为10∶0.7(质量比)、反应时间为30 min,在174℃回流温度下,对异丙基苯酚的产率可达87%.对催化剂的重复使用次数进行了考察,使用5次后催化剂活性是原来的89.7%. 更多还原在HZSM-5分子筛上,考察了温度,原料配比,催化剂的装填量,空速及不同硅铝比等对苯酚与异丙醇烷基化反应的影响。
ptaa分子式

ptaa分子式
PTAA(对叔丁基苯甲酸)是一种有机化合物,其分子式为C11H14O2。
它是白色至浅黄色结晶粉末,有刺激性气味。
不溶于水,可溶于乙醇、乙醚、苯等有机溶剂。
PTAA主要用于生产增塑剂、防老剂、香料、杀虫剂和彩色显影剂等。
其中,PTAA最重要的用途是生产增塑剂,如对叔丁基邻苯二酚(TBHQ)和叔丁基苯甲酸酯类。
这些增塑剂在塑料、橡胶、油漆、油墨等高分子材料中广泛应用,是重要的化工原料之一。
在生产过程中,PTAA通常采用甲苯或二甲苯为原料,通过液相氧化法或气相氧化法制备。
其中,液相氧化法是目前工业上最常用的方法,该方法是在催化剂的作用下,将甲苯或二甲苯在液相中与空气进行氧化反应,生成粗品PTAA。
经过精制提纯后,可以得到高纯度的PTAA。
除了作为化工原料外,PTAA还具有一定的生物活性。
研究表明,PTAA具有抗菌、抗炎、抗肿瘤等作用。
其中,对叔丁基苯甲酸酯类化合物在抗炎和抗肿瘤方面表现出较好的活性,可用于治疗类风湿性关节炎、银屑病、膀胱癌等疾病。
然而,这些生物活性的研究仍处于起步阶段,需要进一步的临床验证和应用。
总之,PTAA是一种重要的有机化合物,主要用于生产增塑剂、防老剂、香料、杀虫剂和彩色显影剂等。
在生产过程中,需要注意安全操作和环境保护。
同时,随着研究的深入,PTAA的生物活性也逐渐被发掘和应用,为医药和健康领域的发展提供了新的可能性。
高效液相色谱法测定食用油中多种抗氧化剂

高效液相色谱法测定食用油中多种抗氧化剂姚丽君(营口市食品药品检验检测中心,辽宁营口 115000)摘 要:目的:建立高效液相色谱法测定食用油中叔丁基对羟基茴香醚、叔丁基对苯二酚、二丁基羟基甲苯和没食子酸丙酯 4 种抗氧化剂的方法。
方法:采用乙腈直接提取法提取样品,C18固相萃取柱净化后,经X Bridge C18色谱柱分离,用二极管阵列检测器进行测定。
结果:叔丁基对羟基茴香醚、叔丁基对苯二酚、二丁基羟基甲苯和没食子酸丙酯4种抗氧化剂线性关系良好,当添加水平分别为5 mg·kg-1、50 mg·kg-1、100 mg·kg-1时,回收率为88.21%~96.72%,相对标准偏差低于10%,叔丁基对羟基茴香醚、叔丁基对苯二酚、二丁基羟基甲苯的最低检出限均为1 mg·kg-1,没食子酸丙酯的最低检出限为2 mg·kg-1。
结论:本方法检测结果准确性较高,可靠性较强,操作简单,适用性良好,可用于食用油中多种抗氧化剂的测定。
关键词:高效液相色谱法;食用油;抗氧化剂Determination of Various Antioxidants in Edible Oil by High Performance Liquid ChromatographyYAO Lijun(Yingkou Testing Center for Food and Drug Control, Yingkou 115000, China) Abstract: Objective: A HPLC method was developed for the determination of 4 antioxidants in edible oil, including tert-butyl-p-anisole, tert-butylhydroquinone, butylated hydroxytoluene and propyl gallate. Method: The samples were extracted by acetonitrile direct extraction method, purified by C18 solid phase extraction column, separated by X Bridge C18 column, and determined by diode array detector. Result: The linear relationship of tert-butyl-p-anisole, tert-butylhydroquinone, butylated hydroxytoluene and propyl gallate was good. When the addition levels were 5 mg·kg-1, 50 mg·kg-1, 100 mg·kg-1, the recovery rate was 88.21%~96.72%, and the relative standard deviation was less than 10%. The minimum detection limit of tert-butyl p-alkyl anisole, tert-butyl hydroquinone and butylated hydroxytoluene was 1 mg·kg-1, and the minimum detection limit of propyl gallate was 2 mg·kg-1. Conclusion: The method has high accuracy, strong reliability, simple operation and good applicability, and can be used for the determination of various antioxidants in edible oil.Keywords: high performance liquid chromatography; edible oil; antioxidants食用油是人们生活中必不可缺的食品之一,但油脂易受到光、氧气、微生物等的影响,经过水解、氧化等反应后,出现变质酸败,并分解成为油脂酸、甘油,油脂酸再次反应后生成氧化物,最终生成酮类、油脂酸等多种物质,不仅会使食用油味道发生变化,影响其营养成分,改变其感官性质,甚至引发人体癌变[1]。
危化品目录

一、危险化学品的定义和确定原则定义:具有毒害、腐蚀、爆炸、燃烧、助燃等性质,对人体、设施、环境具有危害的剧毒化学品和其他化学品。
确定原则:危险化学品的品种依据化学品分类和标签国家标准,从以下危险和危害特性类别中确定:1.物理危险爆炸物:不稳定爆炸物、、、、。
易燃气体:类别1、类别2、化学不稳定性气体类别A、化学不稳定性气体类别B。
气溶胶〔又称气雾剂〕:类别1。
氧化性气体:类别1。
加压气体:压缩气体、液化气体、冷冻液化气体、溶解气体。
易燃液体:类别1、类别2、类别3。
易燃固体:类别1、类别2。
自反应物质和混合物:A型、B型、C型、D型、E型。
自燃液体:类别1。
自燃固体:类别1。
自热物质和混合物:类别1、类别2。
遇水放出易燃气体的物质和混合物:类别1、类别2、类别3。
氧化性液体:类别1、类别2、类别3。
氧化性固体:类别1、类别2、类别3。
有机过氧化物:A型、B型、C型、D型、E型、F型。
金属腐蚀物:类别1。
2.健康危害急性毒性:类别1、类别2、类别3。
皮肤腐蚀/刺激:类别1A、类别1B、类别1C、类别2。
严重眼损伤/眼刺激:类别1、类别2A、类别2B。
呼吸道或皮肤致敏:呼吸道致敏物1A、呼吸道致敏物1B、皮肤致敏物1A、皮肤致敏物1B。
生殖细胞致突变性:类别1A、类别1B、类别2。
致癌性:类别1A、类别1B、类别2。
生殖毒性:类别1A、类别1B、类别2、附加类别。
特异性靶器官毒性-一次接触:类别1、类别2、类别3。
特异性靶器官毒性-反复接触:类别1、类别2。
吸入危害:类别1。
3.环境危害危害水生环境-急性危害:类别1、类别2;危害水生环境-长期危害:类别1、类别2、类别3。
危害臭氧层:类别1。
二、剧毒化学品的定义和判定界限定义:具有剧烈急性毒性危害的化学品,包括人工合成的化学品及其混合物和天然毒素,还包括具有急性毒性易造成公共安全危害的化学品。
剧烈急性毒性判定界限:急性毒性类别1,即满足以下条件之一:大鼠实验,经口LD50≤5mg/kg,经皮LD50≤50mg/kg,吸入〔4h〕LC50≤100ml/m3〔气体〕或〔蒸气〕或〔尘、雾〕。
对叔丁基苯甲酸团体标准

对叔丁基苯甲酸团体标准叔丁基苯甲酸团体标准一、范围本标准规定了叔丁基苯甲酸的要求、试验方法、检验规则和标志、包装、运输、贮存。
本标准适用于以叔丁醇和甲酸为原料经酯化反应而得的产品叔丁基苯甲酸。
二、规范性引用文件下列文件对于本文件的应用是必不可少的。
凡是注日期的引用文件,仅注日期的版本适用于本文件。
凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB/T 191 包装储运图示标志GB/T 6324.2 化学试剂 电导率测定通用方法GB/T 6682 分析实验室用水规格和试验方法三、要求叔丁基苯甲酸应符合下列要求:外观:白色或类白色结晶或结晶性粉末;纯度:≥98.0%;熔点:95.0~98.0℃;干燥失重:≤0.5%。
四、试验方法4.1 外观的测定:取适量样品,置于干燥洁净的白色瓷板上,用目视法测定其色泽。
4.2 纯度的测定:按照相关标准进行。
4.3 熔点的测定:按照相关标准进行。
4.4 干燥失重的测定:按照相关标准进行。
五、检验规则5.1 组批与抽样规则:按照相关标准进行。
5.2 出厂检验:每批产品应由生产厂质量检验部门进行出厂检验,保证符合本标准的要求。
出厂检验项目包括外观、纯度和熔点。
5.3 型式检验:在正常生产情况下,每年至少进行一次型式检验,其检验项目为本标准规定的全部项目。
有下列情况之一时,应进行型式检验:a)新产品试制定型鉴定时;b)正式生产后,如原料、工艺有较大改变,可能影响产品质量时;c)国家质量监督机构提出进行型式检验要求时。
5.4 判定规则:检验结果中若纯度和干燥失重有一项不符合要求,应从同批产品中重新抽取两倍量样品,对不符合要求的项目进行复验,复验结果仍不符合要求,则判定该批产品为不合格。
若熔点不符合要求,则该批产品不得复验,判定为不合格。
叔丁基结构式

叔丁基结构式叔丁基结构式(英文缩写为SAM),它是由两个碳原子、两个氢原子和一个基团所组成的,所以又称为甲基叔丁基醚或甲基叔丁基。
叔丁基的衍生物(例如2甲基-1-叔丁基),用于有机合成中间体及聚合引发剂等,也可作为粘合剂、增塑剂、润滑油添加剂、橡胶硫化促进剂等。
本品能随水蒸气挥发,使用时必须将其与水分离。
叔丁基与水接触能形成水合物,叔丁基水合物难溶于水。
叔丁基与氨、胺、醇、酮、醛等多种亲油性物质互相溶解。
叔丁基有吸湿性,暴露于空气中易氧化变色。
在工业上常用叔丁醇作为合成叔丁基化合物的原料。
在叔丁醇的叔丁基化反应中,通过3-甲基-丙酰胺盐酸盐与叔丁醇在硫酸存在下反应而得。
叔丁基不溶于水,溶于醚和四氯化碳,易溶于烃类和卤代烃。
1、叔丁醇的叔丁基化叔丁醇具有叔丁基结构式,在叔丁醇叔丁基化反应中,叔丁醇经碱性高锰酸钾溶液处理后再用亚硝酸钠还原成叔丁醇钠,然后再经还原成叔丁醇钾,最后催化脱氢制得叔丁基化合物。
叔丁醇可以先与甲醇或乙醇混合,用水和叔丁醇的混合溶剂萃取,分去水层后,减压蒸去叔丁醇。
将得到的叔丁基化合物在亚硝酸钠的存在下进行还原反应,即可制得叔丁基化合物。
叔丁基与金属(如镁、铝)反应,生成相应的烷基醇盐,故称为叔丁基试剂。
例如:可以用叔丁醇钠在亚硝酸钠的作用下还原三氯化铝,然后再将三氯化铝水合物溶于叔丁醇中,加热回流,冷却结晶析出叔丁基化合物。
2、从叔丁醇和叔丁醇钾的反应1、合成叔丁基锂,先要叔丁醇和叔丁醇钾共热,生成叔丁醇钾、叔丁醇,然后叔丁醇钾与硼氢化钠反应,硼氢化钠被转化成硼氢化钾,继续与叔丁醇钾反应,就会生成叔丁基锂。
2、叔丁醇钾是可以制备叔丁基锂的,要是从叔丁醇和叔丁醇钾的反应制备的话,实验室制取叔丁基锂,先要叔丁醇和叔丁醇钾共热,生成叔丁醇钾、叔丁醇,然后叔丁醇钾与硼氢化钠反应,硼氢化钠被转化成硼氢化钾,继续与叔丁醇钾反应,就会生成叔丁基锂。
这就是实验室制取叔丁基锂的方法,该方法是由美国诺贝尔奖获得者罗伯特·格罗斯( Robert Groves)于1938年发现的。
对硝基苯甲酸的制备
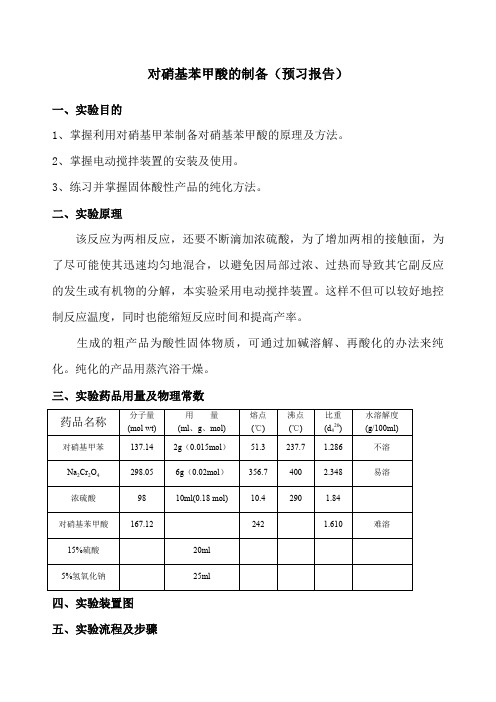
对硝基苯甲酸的制备(预习报告)一、实验目的1、掌握利用对硝基甲苯制备对硝基苯甲酸的原理及方法。
2、掌握电动搅拌装置的安装及使用。
3、练习并掌握固体酸性产品的纯化方法。
二、实验原理该反应为两相反应,还要不断滴加浓硫酸,为了增加两相的接触面,为了尽可能使其迅速均匀地混合,以避免因局部过浓、过热而导致其它副反应的发生或有机物的分解,本实验采用电动搅拌装置。
这样不但可以较好地控制反应温度,同时也能缩短反应时间和提高产率。
生成的粗产品为酸性固体物质,可通过加碱溶解、再酸化的办法来纯化。
纯化的产品用蒸汽浴干燥。
三、实验药品用量及物理常数四、实验装置图五、实验流程及步骤1.安装带搅拌、回流、滴液的装置如图2.在250ml的三颈瓶中依次加入6g对硝基甲苯,18g重铬酸钾粉末及40ml水。
3.在搅拌下自滴液漏斗滴入25ml浓硫酸。
(注意用冷水冷却,以免对硝基甲苯因温度过高挥发而凝结在冷凝管上)。
4.硫酸滴完后,加热回流0.5h,反应液呈黑色。
(此过程中,冷凝管可能会有白色的对硝基甲苯析出,可适当关小冷凝水,使其熔融滴下)。
5.待反应物冷却后,搅拌下加入80ml冰水,有沉淀析出,抽滤并用50ml 水分两次洗涤。
6.将洗涤后的对硝基苯甲酸的黑色固体放入盛有30ml 5%硫酸中,沸水浴上加热10min,冷却后抽滤。
(目的是为了除去未反应完的铬盐)7.将抽滤后的固体溶于50ml 5%NaOH溶液中,50℃温热后抽滤,在滤液中加入1g活性炭,渚沸趁热抽滤。
(此步操作很关键,温度过高对硝基甲苯融化被滤入滤液中,温度过低对硝基苯甲酸钠会析出,影响产物的纯度或产率)8.充分搅拌下将抽滤得到的滤液慢慢加入盛有60ml 15%硫酸溶液的烧杯中析出黄色沉淀,抽滤,少量冷水洗涤两次,干燥后称重。
(加入顺序不能颠倒,否则会造成产品不纯)。
9.混合溶剂重结晶粗对硝基苯甲酸。
六、实验注意事项1、安装仪器前,要先检查电动搅拌装置转动是否正常,搅拌棒要垂直安装,安装好仪器后,再检查转动是否正常。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
T;N
R-phrase(s)
R24;R62;R22;R42;R53
S-phrase(s)
S39;S45;S61;S28A
2.3 其它危害物
-无
3 成分/组成信息
3.1 物质
分子式 - C11H14O2 分子量 - 178.23
4 急救措施
4.1 必要的急救措施描述
一般的建议 请教医生。向到现场的医生出示此安全技术说明书。 如果吸入 如果吸入,请将患者移到新鲜空气处。如呼吸停止,进行人工呼吸。请教医生。 在皮肤接触的情况下 用肥皂和大量的水冲洗。立即将患者送往医院。请教医生。 在眼睛接触的情况下 用大量水彻底冲洗至少15分钟并请教医生。 如果误服 切勿给失去知觉者通过口喂任何东西。用水漱口。请教医生。
5.2 源于此物质或混合物的特别的危害
碳氧化物
5.3 救火人员的预防
如必要的话,戴自给式呼吸器去救火。
5.4 进一步的信息
无数据资料
6 泄露应急处理
6.1 人员的预防,防护设备ห้องสมุดไป่ตู้紧急处理程序
戴呼吸罩。避免粉尘生成。避免吸入蒸气、烟雾或气体。保证充分的通风。人员疏散到安全区域。避 免吸入粉尘。
6.2 环境预防措施
欧洲陆运危规 : 2811
国际海运危规 : 2811
国际空运危规 : 2811
14.2 联合国(UN)规定的名称
欧洲陆运危规:Toxicsolid,organic,n.o.s.(4-tert-Butylbenzoicacid) 国际海运危规:Toxicsolid,organic,n.o.s.(4-tert-Butylbenzoicacid) 国际空运危规:Toxicsolid,organic,n.o.s.(4-tert-Butylbenzoicacid)
化学品安全技术说明书
14.6 对使用者的特别预防
无数据资料
15 法规信息
15.1 专门对此物质或混合物的安全,健康和环境的规章 / 法规
法规信息 请注意废物处理也应该满足当地法规的要求。 若适用,该化学品满足《危险化学品安全管理条例》(2002年1月9号国务院通过)的要求。
https://
7.2 安全储存的条件,包括任何不兼容性
贮存在阴凉处。使容器保持密闭,储存在干燥通风处。
7.3 特定用途
无数据资料
8 接触控制/个体防护
8.1 暴露控制
适当的技术控制 根据工业卫生和安全使用规则来操作。休息以前和工作结束时洗手。 人身保护设备 眼/面保护 面罩與安全眼鏡请使用经官方标准如NIOSH(美国)或EN166(欧盟)检测与批准的设备防护眼部。 皮肤保护 戴手套取手套在使用前必须受检查。 请使用合适的方法脱除手套(不要接触手套外部表面),避免任何皮肤部位接触此产品. 使用后请将被污染过的手套根据相关法律法规和有效的实验室规章程序谨慎处理.请清洗并吹干双手 所选择的保护手套必须符合EU的886/EEC规定和从它衍生出来的EN376标准。 身体保护 防渗透的衣服,阻燃防静电防护服, 防护设备的类型必须根据特定工作场所中的危险物的浓度和含量来选择。 呼吸系统防护 如危险性评测显示需要使用空气净化的防毒面具,请使用全面罩式多功能防毒面具(US)或ABEK型 (EN14387)防毒面具筒作为工程控制的候补。如果防毒面具是保护的唯一方式,则使用全面罩式 送风防毒面具。呼吸器使用经过测试并通过政府标准如NIOSH(US)或CEN(EU)的呼吸器和零 件。
强氧化剂,强碱
10.6 危险的分解产物
无数据资料
11 毒理学资料
11.1 毒理学影响的信息
急性毒性 半数致死剂量 (LD50) 经口 - 大鼠 - 473 mg/kg 备注: 行为的:抽搐或对癫痫阈值的影响。 行为的:运动失调症 肺,胸,或者呼吸系统:呼吸困难 半数致死浓度(LC50) 吸入 - 大鼠 - 4 h - > 1,900 mg/m3 半数致死剂量 (LD50) 经皮 - 兔子 - > 900 mg/kg 亚 急性毒性 无数据资料 刺激性(总述) 无数据资料 皮肤腐蚀/刺激 无数据资料 严重眼损伤 / 眼刺激 眼睛 - 兔子 - 轻度的眼睛刺激 呼吸道或皮肤过敏 无数据资料 生殖细胞诱变 无数据资料 致癌性 此产品中没有大于或等于 0。1%含量的组分被 IARC鉴别为可能的或肯定的人类致癌物。 生殖毒性 无数据资料
如能确保安全,可采取措施防止进一步的泄漏或溢出。不要让产品进入下水道。
6.3 抑制和清除溢出物的方法和材料
收集和处置时不要产生粉尘。扫掉和铲掉。放入合适的封闭的容器中待处理。
7 安全操作与储存
7.1 安全操作的注意事项
避免接触皮肤和眼睛。避免形成粉尘和气溶胶。在有粉尘生成的地方,提供合适的排风设备。一般性的防 火保护措施。
14.3 运输危险类别
欧洲陆运危规 : 6.1
国际海运危规 : 6.1
国际空运危规 : 6.1
14.4 包裹组
欧洲陆运危规 : III
国际海运危规 : III
国际空运危规 : III
14.5 环境危害
欧洲陆运危规 :否
国际海运危规 海运污染物 :否
国际空运危规 : 无数据资料
https:// 4/5
Powered by TCPDF ()
5/5
化学品安全技术说明书
1 化学品及企业标识
1.1 产品标识符
化学品俗名或商品名: 对叔丁基苯甲酸 CAS No.: 98-73-7 别名: 4-叔丁基苯甲酸;
1.2 鉴别的其他方法
无数据资料
1.3 有关的确定了的物质或混合物的用途和建议不适合的用途
无数据资料
2 危险性概述
2.1 GHS分类
健康危害 急性毒性(经口):AcuteTox.4 急性毒性(经皮):AcuteTox.3 严重损伤/刺激眼睛:EyeIrrit.2 环境危害 急性水生毒性:AquaticAcute1
f) 起始沸点和沸程
无数据资料
g) 闪点
158 °C (316 °F) - closed cup
h) 蒸发速率
无数据资料
i) 可燃性(固体,气体) 无数据资料
j) 高的/低的燃烧性或爆炸性限度 无数据资料
k) 蒸气压
无数据资料
l) 相对蒸气密度
无数据资料
m) 相对密度
无数据资料
n) 溶解性 / 水溶性 无数据资料
12 生态学资料
12.1 毒性
对鱼类的毒性半数致死浓度(LC50)-鲫鱼(金鱼)-4mg/l-96h
12.2 持久存留性和降解性
无数据资料
12.3 生物积累的潜在可能性
无数据资料
12.4 土壤中的迁移
无数据资料
12.5 PBT 和 vPvB的结果评价
无数据资料
12.6 其它不利的影响
对鱼类的毒性 半数致死浓度(LC50) - 鲫鱼(金鱼) - 4 mg/l - 96 h
https:// 3/5
化学品安全技术说明书
特异性靶器官系统毒性(一次接触) 无数据资料 特异性靶器官系统毒性(反复接触) 无数据资料 潜在的健康影响
吸入 吸入有害。 可能引起呼吸道刺激。 吞咽 误吞对人体有害。 皮肤 如果被皮肤吸收会有毒性 可能引起皮肤刺激。 眼睛 引起眼睛刺激。 接触后的征兆和症状 可能发生对肝的伤害。, 可能发生对肾的伤害。, 据我们所知,此化学,物理和毒性性质尚未经完整的研 究。 附加说明 化学物质毒性作用登记: DG4708000
https:// 2/5
化学品安全技术说明书
9 理化特性
9.1 基本的理化特性的信息
a) 外观与性状
形状 : 薄片
颜色 : 白色
b) 气味
无数据资料
c) 气味临界值
无数据资料
d) pH值
无数据资料
e) 熔点/凝固点
162 - 165 °C (324 - 329 °F) - lit.
4.2 最重要的症状和影响,急性的和滞后的
可能发生对肝的伤害。,可能发生对肾的伤害。,据我们所知,此化学,物理和毒性性质尚未经完整的研 究。
https:// 1/5
化学品安全技术说明书
4.3 及时的医疗处理和所需的特殊处理的说明和指示
无数据资料
5 消防措施
5.1 灭火介质
火灾特征 无数据资料 灭火方法及灭火剂 用水雾,抗乙醇泡沫,干粉或二氧化碳灭火。
13 废弃处置
13.1 废物处理方法
产品 将剩余的和不可回收的溶液交给有许可证的公司处理。联系专业的拥有废弃物处理执照的机构来处理此 物质。与易燃溶剂相溶或者相混合,在备有燃烧后处理和洗刷作用的化学焚化炉中燃烧 污染了的包装物 按未用产品处置。 进一步的说明: 无数据资料
14 运输信息
14.1 UN编号
o) 辛醇/水分配系数的对数值 无数据资料
p) 自燃温度(°C / °F) 无数据资料
q) 分解温度
无数据资料
r) 粘度
无数据资料
10 稳定性和反应活性
10.1 反应性
无数据资料
10.2 化学稳定性
无数据资料
10.3 敏感性(危险反应的可能性)
无数据资料
10.4 避免接触的条件
无数据资料
10.5 不兼容的材料
2.2 GHS 标记要素,包括预防性的陈述
危害类型
GHS06:急毒性物质;
信号词
【危险】
危险申明
H302
如果吞食有害健康。
H311
皮肤接触将中毒。
H332
吸入有害健康。
警告申明
P280
戴防护手套/防护服/护眼/防护面具。
P312
如果你感到不适,呼叫解毒中心/医生。
RS
Hazard symbol(s)
