化学除磷的设计计算
化学除磷药剂投加量

化学除磷药剂化学除磷原理化学除磷是利用无机金属盐作为沉淀剂,与污水中的磷酸盐类物质反应形成难溶性含磷化合物与絮凝体,将污水中的溶解性磷酸盐分离出来。
化学除磷的药剂主要有铁盐、铝盐和石灰,由于石灰对生物处理的pH影响较大,加之容易引起管道堵塞问题;铝盐对人体和生物毒害比较大,给运行管理带来很多麻烦。
一般在以生物除磷为主,化学除磷为辅的污水处理厂中很多采用。
目前,国内常爱用铁盐作为沉淀剂,其与磷的化学反应式如下(1):Fe3++PO43- →Fe PO4↓(1)与沉淀反应相竞争的反应式金属离子与OH-的反应,反应式如下(2):Fe3++ 3OH- →Fe (OH)3↓(2)金属氢氧化物会形成大块的絮凝体,这对于沉淀产物的絮凝是有力的,同时还会吸附胶体状的物质、细微悬浮颗粒。
除磷药剂投加量的计算由式(1)可知去除1mol的磷酸盐,需要1mol的铁离子。
由于在实际工程中,反应并不是100%的有效进行的,加之OH-会参与竞争反应,与金属离子反应,生成相应的氢氧化物,如(2)式,所以实际中化学沉淀药剂一般需要超量投加,以保证达到所需的出水P浓度。
《给水排水设计手册》第五册和德国设计规范中都提到了同步沉淀化学除磷可按照1mol磷需要1.5mol的铁盐来考虑,为了计算方便,实际中将摩尔换算成质量单位,如1molFe=56gFe,1molP=31gP,也就是去除1kg的磷,当采用铁盐时需要投加:1.5×(56/31)=1.5×1.8=2.7Kg Fe/Kg P,计算举例:某城镇污水处理厂规模2万m3/d,已建成稳定运行,二沉池出水排放标准总磷≤1.0mg/L,运行数据表明二沉池出水实测总磷2.5mg/L,欲采用液体三氯化铁(FeCl3)作为同步化学除磷药剂,其有效成分为40%(400g/Kg FeCl3溶液),密度为1.42Kg/L,求所需要的除磷药剂。
解:化学除磷欲除去的磷含量2.5-1.0=1.5mg/L,所需要的Fe的投加量至少为2.7×1.5×20000×10-3=81Kg/d;折算成每天需要有效成分为40%的FeCl3溶液体积为V=81×(56+35.5×3)/(56×0.4×1.42)=420L=0.42m3/d六水合三氯化铁(FeCl3·6H2O)含量98%(1g FeCl3·6H2O含有0.203gFe)除去1mg/L P盐,需要多少ppm的FeCl3·6H2O?(2.7Kg Fe/Kg P)。
十分钟搞定!化学除磷剂的投加!

十分钟搞定!化学除磷剂的投加!全部的污水除磷方法都包含有两个必要的过程,首先将溶解性磷(磷酸盐)物质转化为不溶性悬浮(颗粒)性状态,然后通过固液分别将磷从污水中除去。
一、除磷剂的分类除磷剂是向污水中投加化学药剂,使水中磷酸根离子生成难溶性盐,形成絮凝体后与水分别,从而去除水中所含的磷。
从而将处理后水中的磷含量降至界限值以下,不需要转变原水处理流程,不需要增设大型水处理构筑物,简便易行,经济有用,可获得显著的社会和经济效益。
依据化学除磷法的原理介绍,除磷剂主要分为四类:1 、铝盐化学除磷药剂采纳铝盐作为药剂添加在化学除磷工艺中,常常使用的有三种,一种是硫酸铝,一种是氯化铝,还有一种是聚合氯化铝,在详细的反应过程中,包含两个主要的反应过程,首先是三价铝离子通过与磷酸根产生反应而消失沉淀,沉淀的化合物为AlPO4 。
其次是三价铝离子能够消失水解反应,在这一过程中会有正电荷以及单核羟基络合物以及多核羟基络合物的存在,在经过范德华力以及网捕等一系列的作用以后,就能达到比较抱负的沉淀效果,这样也就达到了化学除磷的要求。
在运用铝盐进行化学除磷的过程中,需要重点掌握 pH,这样才能达到抱负的除磷效果,否则会造成所排放的水体中铝盐超标。
2 、铁盐化学除磷药剂铁盐除磷药剂主要有硫酸亚铁、聚合氯化硫酸铁、氯化铁及聚合氯化铁等。
铁盐与铝盐除磷反应机理类似,之外还会发生剧烈水解并同时发生各种聚合反应吸附水中的磷。
Fe2+除磷效率与pH相关,但有关 Fe2+除磷最佳PH存在争议:有人认为PH=8时,Fe2+除磷效果最好,但讨论表明PH=7.5~8.5时不易生成沉淀,从而降低了除磷效率。
Fe2+除磷需要较高PH值,而环境污水厂处理中PH值往往低于 7.5。
另外,在水中 Fe3(PO4)2 没有FePO4稳定,这些都限制了二价铁盐在废水除磷中的应用,实际过程中可利用好氧池曝气的特点将Fe2+氧化成 Fe3+来提高化学除磷效率。
污水处理基本计算公式

基本组合作用弯矩表:
配筋及裂缝:
配筋计算方法:按单筋受弯构件计算板受拉钢筋。
裂缝计算根据《水池结构规程》附录A公式计算。
按基本组合弯矩计算配筋,按准永久组合弯矩计算裂缝,结果如下:
顶板配筋及裂缝表(弯矩:kN.m/m,面积:mm2/m,裂缝:mm)
(1)栅渣量与多种因素有关,在无当地运行资料时,可以采用以下资料。
格栅间隙16~25mm;0.10~0.05m3/103m3(栅渣/废水)。
格栅间隙30~50mm;0.03~0.01m3/103m3(栅渣/废水)。
(2)栅渣的含水率一般为80%,容重约为960kg/m3。
(3)在大型废水处理厂或泵站前的大型格栅(每日栅渣量大于0.2m3),一般应采用机械清渣。
3、其他参数
(1)过栅流速一般采用0.6~1.0m/s。
(2)格栅前渠道内水流速度一般采用0.4~0.9m/s。
(3)格栅倾角一般采用45°~75°,小角度较省力,但占地面积大。
(4)机械格栅的动力装置一般宜设在室内,或采取其他保护设备的措施。
(5)设置格栅装置的构筑物,必须考虑设有良好的通风设施。
式中:H——堰上水头(m);
Q——每座反应池出水量(m3/s),指污水最大流量( 0.579m/s);与回流污泥量、回流量之和(0.717×160% m3/s);
m——流量系数,一般采用0.4~0.5;
b——堰宽(m);与反应池宽度相等。
设计中取m=0.4,b=5.0m
设计中取为0.19m。
厌氧—缺氧—好氧池的最大出水流量为(0.66+0.66/1.368×160%)=1.43m3/s,出水管管径采用DN1500mm,送往二沉池,管道内的流速为0.81m/s。
化学除磷的设计计算

化学除磷的设计计算化学除磷主要是指通过化学反应去除废水或水体中的磷。
磷是一种常见的污染物,过量的磷会导致水体富营养化现象,引发藻类过度繁殖,破坏水生态系统的平衡。
因此,化学除磷是一种常见的废水处理方法。
1.确定磷的存在形式和浓度在开始设计之前,需要对废水或水体中磷的存在形式和浓度进行了解。
磷的存在形式可以是溶解态磷酸盐或悬浮态磷酸盐,浓度的高低将决定所需药剂的量。
2.选择合适的药剂常用的化学除磷药剂有氢氧化铁、聚合氯化铝(PAC)、硫酸铝等。
根据磷的形态和浓度,选择合适的药剂。
3.确定药剂添加量药剂添加量的确定需要根据废水或水体中磷的浓度、药剂的投加效果以及药剂的含磷量来计算。
以PAC为例,可以通过下面的公式计算药剂的添加量:药剂添加量=[P]×V×Y/(1000×C)其中,[P]为废水中的总磷浓度,V为废水体积,C为药剂中含磷量,Y为药剂的投加效果。
通常情况下,Y的取值为80-95%。
4.确定调节剂的添加量调节剂是为了控制药剂的沉淀速度和沉淀效果而添加的辅助剂。
调节剂的种类有很多,例如碳酸钠、盐酸等。
根据药剂的种类和使用经验,确定调节剂的添加量。
5.确定反应时间和反应条件反应时间和反应条件的确定是根据药剂的特性以及实际情况来决定的。
反应时间一般在10-30分钟之间,反应温度一般在20-50°C之间。
6.确定混合方式和反应器尺寸混合方式可以选择搅拌或通气等,根据实际情况选择适合的混合方式。
反应器尺寸的确定需要考虑废水流量以及反应时间,保证药剂与磷充分反应。
以上所述是化学除磷的设计计算的一般步骤,实际的设计计算需要根据具体的情况进行调整。
同时,为了保证化学除磷的效果,还需要在实施过程中进行监测和调整,以确保废水或水体中的磷达到合理的浓度标准。
化学除磷加药量及污泥量计算书
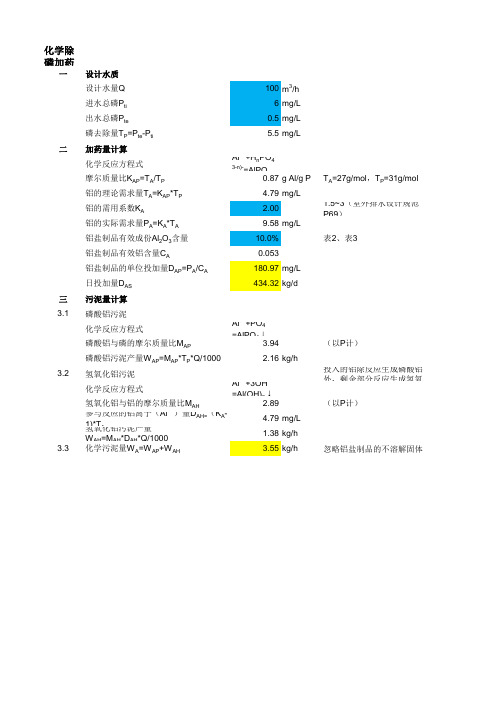
化学除磷加药量及污泥量计算
一设计水质
设计水量Q100m3/h
进水总磷P ti6mg/L
出水总磷P te0.5mg/L
磷去除量T P=P te-P ti 5.5mg/L
二加药量计算
化学反应方程式Al3++H n PO4(3-n)-=AlPO4↓+nH+
摩尔质量比K AP=T A/T P0.87g Al/g P T A=27g/mol,T P=31g/mol
铝的理论需求量T A=K AP*T P 4.79mg/L
铝的需用系数K A 2.00 1.5~3(室外排水设计规范P69)
铝的实际需求量P A=K A*T A9.58mg/L
铝盐制品有效成份Al2O3含量10.0%表2、表3
铝盐制品有效铝含量C A0.053
铝盐制品的单位投加量D AP=P A/C A180.97mg/L
日投加量D AS434.32kg/d
三污泥量计算
3.1磷酸铝污泥
化学反应方程式Al3++PO43-=AlPO4↓
磷酸铝与磷的摩尔质量比M AP 3.94(以P计)
磷酸铝污泥产量W AP=M AP*T P*Q/1000 2.16kg/h
3.2氢氧化铝污泥投入的铝除反应生成磷酸铝外,剩余部分反应生
化学反应方程式Al3++3OH-=Al(OH)3↓
氢氧化铝与铝的摩尔质量比M AH 2.89(以P计)
参与反应的铝离子(Al3+)量D AH=(K A-1)*T A 4.79mg/L
氢氧化铝污泥产量W AH=M AH*D AH*Q/1000 1.38kg/h
3.3化学污泥量W A=W AP+W AH 3.55kg/h忽略铝盐制品的不溶解固体
输入值计算值
设计规范P69)
铝外,剩余部分反应生成氢氧化铝。
化学除磷实验报告

化学除磷实验报告实验目的研究利用化学方法除去水体中的磷污染物,并评估该方法的效果。
实验原理磷是一种重要的营养元素,但过量的磷会导致水体中的富营养化现象,引发水华等环境问题。
除磷实验主要基于磷酸在酸性条件下与钙离子反应生成难溶性的磷酸钙沉淀的特性。
具体反应如下:H3PO4 + 3Ca2+ →Ca3(PO4)2↓+ 2H+实验中使用的除磷剂为氯化铝(AlCl3)。
实验步骤1. 准备1000ml脱离磷的污水;2. 将500ml污水分成两个容量瓶,每个瓶中加入250ml污水;3. 在一个容量瓶中加入100ml 10%的AlCl3溶液,并搅拌均匀;4. 在另一个容量瓶中加入相同体积的蒸馏水作为空白对照组;5. 放置一段时间后,观察和记录两个试管中溶液的颜色和浑浊度;6. 使用PH电极检测两个试管中溶液的酸度,并记录数据;7. 将两个试管中的溶液放置一段时间后,观察和记录沉淀的形成情况。
实验结果在加入AlCl3溶液的试管中,溶液从无色变为浑浊状态,而在空白对照组中无明显变化。
PH值在加入AlCl3溶液后明显下降,空白对照组中维持不变。
经过一段时间后,加入AlCl3溶液的试管中出现了白色的沉淀物,而空白对照组中没有沉淀物生成。
结论本实验使用化学方法成功除去了水体中的磷污染物。
加入AlCl3溶液后,溶液的颜色由无色变为浑浊,指示了磷酸钙的沉淀生成。
PH值的下降也证明了磷酸钙的生成反应。
实验结果显示,氯化铝作为除磷剂在酸性条件下具有良好的除磷效果。
实验改进1. 实验中使用的除磷剂可以尝试其他化学剂,比较不同剂型的除磷效果;2. 可以调整溶液的酸碱度,观察其对除磷效果的影响;3. 可以进行定量分析,测定溶液中磷酸盐离子的浓度变化。
环境意义磷污染是目前全球面临的严重环境问题之一。
本实验提供了一种利用化学方法除去水体中磷污染物的途径,为寻找可行的磷污染防治方法提供了新的思路和实验依据。
这有助于保护水体环境,预防水华等富营养化现象的发生。
化学除磷计算【范本模板】

前言在静止的或流动缓慢的水体中,如果磷的浓度过高,会造成水体的富营养化,其危害已众所周知,因而在污水处理中进行除磷是必要的。
我国《污水综合排放标准》(8978-1996)规定,城市污水处理厂磷酸盐(以P计)一级排放标准为0。
5mg/l。
磷的去除有化学除磷生物除磷两种工艺,生物除磷是一种相对经济的除磷方法,但由于该除磷工艺目前还不能保证稳定达到0.5mg/l出水标准的要求,所以要达到稳定的出水标准,常需要采取化学除磷措施来满足要求。
本文主要介绍化学除磷的基本机理、主要工艺形式和药剂投加量的计算方法。
2 污水中的磷负荷欧洲一些国家曾对生活污水中的总磷PT做过多次调查,主要结果见表1。
由人类食物产生的磷是不变的,但国内外目前普遍开始采用无磷洗涤剂,所以由洗涤剂产生的磷几年降低了许多。
城市污水原水中的磷浓度在我国主要取决于工业废水中的磷含量。
国外生活污水一般为10~25mg/l,我国一般为5~10mg/l.其大部分是无机化合磷,并是溶解状的,这一部分主要由来自洗涤剂的正磷酸盐和稠环磷酸盐组成。
总磷中的一小部分是有机化合磷,其以溶解和非溶解状态存在.稠环磷酸盐(如P3O105-)和有机化合磷(核酸)一般在污水管网中和污水处理中就已经转化为正磷酸盐(PO43—).3 化学除磷的基础化学除磷是通过化学沉析过程完成的,化学沉析是指通过向污水中投加无机金属盐药剂,其与污水中溶解性的盐类,如磷酸盐混合后,形成颗粒状、非溶解性的物质,这一过程涉及的是所谓的相转移过程,反应方程举例如式1。
实际上投加化学药剂后,污水中进行的不仅仅是沉析反应,同时还进行着化学絮凝反应,所以必须区分化学沉析和化学絮凝的差异(如图1所示)。
FeCl3+K3PO4→FePO4↓+3KCl式1污水沉析反应可以简单的理解为:水中溶解状的物质,大部分是离子状物质转换为非溶解、颗粒状形式的过程,絮凝则是细小的非溶解状的固体物互相粘结成较大形状的过程,所以絮凝不是相转移过程。
化学除磷理论及要求规范

6.7 化学除磷6.7.1 污水经二级处理后,其出水总磷不能达到要求时,可采用化学除磷工艺处理。
污水一级处理以及污泥处理过程中产生的液体有除磷要求时,也可采用化学除磷工艺。
6.7.2 化学除磷可采用生物反应池的前置投加、后置投加和同步投加,也可采用多点投加。
6.7.3 化学除磷设计中,药剂的种类、剂量和投加点宜根据试验资料确定。
6.7.4 化学除磷的药剂可采用铝盐、铁盐,也可采用石灰。
用铝盐或铁盐作混凝剂时,宜投加离子型聚合电解质作为助凝剂。
6.7.5 采用铝盐或铁盐作混凝剂时,其投加混凝剂与污水中总磷的摩尔比宜为1.5~3。
6.7.6 化学除磷时应考虑产生的污泥量。
6.7.7 化学除磷时,对接触腐蚀性物质的设备和管道应采取防腐蚀措施。
条文说明:6.7 化学除磷6.7.1 关于化学除磷应用范围的规定。
《城镇污水处理厂污染物排放标准》(GB18918)规定总磷的排放标准:当达到一级A标准时,在2005年12月31日前建设的污水厂为1mg/l,2006年1月1日起建设的污水厂为0.5mg/l。
一般城市污水经生物除磷后,较难达到后者的标准,故可辅以化学除磷,以满足出水水质的要求。
强化一级处理,可去除污水中绝大部分磷。
上海白龙港城市污水厂试验表明,当FeCl3投加量为40~80mg/l,或Al2(SO4)3•18H2O投加量为60~80mg/l 时,进出水磷酸盐磷浓度分别为2~9mg/l和0.2~1.1mg/l,去除率为60~95%。
污泥厌氧处理过程中的上清液、脱水机的过滤液和浓缩池上清液等,由于在厌氧条件下,有大量含磷物质释放到液体中,若回流入污水处理系统,将造成污水处理系统中磷的恶性循环,因此应先进行除磷,一般宜采用化学除磷。
6.7.2 关于药剂投加点的规定。
以生物反应池为界,在生物反应池前投加为前置投加,在生物反应池后投加为后置投加,投加在生物反应池内为同步投加,在生物反应池前后都投加为多点投加。
化学除磷加药量计算

生物除磷总去除率取70% Pti Pte 磷的去除率 铝盐的投加量(AL2/O3) 总投加量
需化学法去除进水磷含量 6 0.5 0.916666667 66.20754717 mg/l 1456.566038 Kg/d
1.8
3
3
4
5
计算铝盐制品的总投加量(式1-4): DAS = 0.87 × 2.2 × (3.5-0.5) 10000/0.159/1000 = 361(kg/d) 商品量
×
6
变化范围:328~394(kg/d) 计算磷酸铝污泥量(式3-2): WAP = 3.94 × (3.5-0.5) × 10000/1000 = 118.2(kg/d) 计算氢氧化铝污泥量(式3-5): WAH = 2.51×(2.2-1)×(3.5-0.5)×10000/1000 = 90.4(kg/d) 计算总化学污泥量(式3-6): WA = WAP + WAH = 209(kg/d) 干固体量 变化范围:194~224(kg/d) 计算碱度消耗(式4-1): ACA = 4.84 × (2.2-1) × (3.5-0.5) 17.4(mg/L) 按CaCO3 计
序号 1 2 确定设计参数:
过程及说明 采用铝盐 Qd = 10000 m /d,Pti = 3.5 mg/L,Pte = 0.5 确定药剂种类: 聚合氯化铝固体(一等品),Al2O3 含量30% 计算有效铝含量: Al2O3 摩尔质量102g,Al摩尔质量27g CA = 0.3×(2×27)/102 = 0.159 确定铝的需用系数: 磷的去除率:(3.5-0.5)/ 3.5 = 86% KA = 2.2(变化范围:2.0~2.4),KAP = 0.87 计算铝盐制品的单位投加量(式1-3): DAP = 2.2 × 0.87 × (3.5-0.5)/0.159 36(mg/L) 变化范围:33~39(mg/L) 商品确定设计参数: Qd = 10000 m /d,Pti = 3.5 mg/L,Pte = 0.5 mg/L 确定药剂种类: 六水氯化铁固体(一等品),FeCl3·6H2O含量98% 计算有效铁含量: FeCl3·6H2O 摩尔质量270g,Fe摩尔质量56g CF = 0.98×56/270 = 0.203 确定铁的需用系数: 磷的去除率:(3.5-0.5)/ 3.5 = 86% KF = 1.8(变化范围:1.6~2.0),KFP = 1.80 计算铁盐制品的单位投加量(式2-3): DFP = 1.8×1.8×(3.5-0.5)/0.203 = 48(mg/L) 变化范围:43~53(mg/L) 商品量 计算铁盐制品的总投加量(式2-4): DFS = 1.8×1.8×(3.5-0.5)×10000/0.203/1000 = 479(kg/d) 商品量 变化范围:426~532(kg/d) 计算磷酸铁污泥量(式3-8): WFP = 4.87×(3.5-0.5)×10000/1000 = 146.1(kg/d) 计算氢氧化铁污泥量(式3-11): WFH = 3.45×(1.8-1)×(3.5-0.5)×10000/1000 = 82.8(kg/d) 计算总化学污泥量(式3-12): WF = WFP + WFH = 229(kg/d) 干固体量 变化范围:208~250(kg/d) 计算碱度消耗(式4-2): ACF = 4.84×(1.8-1)×(3.5-0.5) = 11.6(mg/L) 按CaCO3 计
化学除磷设计怎么做?精华干货都在这了

化学除磷设计怎么做?精华干货都在这了1 化学除磷应用范围《城镇污水处理厂污染物排放标准》GB 18918规定的总磷的排放标准:当达到一级A标准时,在2005年12月31日前建设的污水厂为1mg/L,2006年1月1日起建设的污水厂为0.5mg/L。
一般城镇污水经生物除磷后,较难达到后者的标准,故可辅以化学除磷,以满足出水水质的要求。
强化一级处理,可去除污水中绝大部分磷。
上海白龙港污水厂试验表明,当FeCl ₃投加量为40mg/L~80mg/L,或Al₂(SO₄)₃·18H₂O投加量为60mg/L~80mg/L时,进出水磷酸盐磷浓度分别为2mg/L~9mg/L和0.2mg/L~1.1mg/L,去除率为60%~95%。
污泥厌氧处理过程中的上清液、脱水机的过滤液和浓缩池上清液等,由于在厌氧条件下,有大量含磷物质释放到液体中,若回流入污水处理系统,将造成污水处理系统中磷的恶性循环,因此应先进行除磷,一般宜采用化学除磷。
2 除磷剂的选择铝盐有硫酸铝、铝酸钠和聚合铝等,其中硫酸铝较常用。
铁盐有三氯化铁、氯化亚铁、硫酸铁和硫酸亚铁等,其中三氯化铁最常用。
采用铝盐或铁盐除磷时,主要生成难溶性的磷酸铝或磷酸铁,其投加量与污水中总磷量成正比。
可用于生物反应池的前置、后置和同步投加。
采用亚铁盐需先氧化成铁盐后才能取得最大除磷效果,因此其一般不作为后置投加的混凝剂,在前置投加时,一般投加在曝气沉砂池中,以使亚铁盐迅速氧化成铁盐。
采用石灰除磷时,生成Ca₅(PO₄)₃OH沉淀,其溶解度与pH值有关,因而所需石灰量取决于污水的碱度,而不是含磷量。
石灰作混凝剂不能用于同步除磷,只能用于前置或后置除磷。
石灰用于前置除磷后污水pH值较高,进生物处理系统前需调节pH值;石灰用于后置除磷时,处理后的出水必须调节pH值才能满足排放要求;石灰还可用于污泥厌氧释磷池或污泥处理过程中产生的富磷上清液的除磷。
用石灰除磷,污泥量较铝盐或铁盐大很多,因而很少采用。
化学除磷的设计计算

化学除磷的设计计算化学除磷是指利用化学反应原理和方法将水体中的磷污染物转化为无害形态或者将其去除的工程化技术。
化学除磷主要应用于处理农田排水、城市污水、工业废水等含磷废水。
本文将详细介绍化学除磷的设计计算方法。
1.磷的化学形态和存在方式磷在自然界中以无机磷和有机磷的形式存在,其中无机磷主要包括磷酸盐和重金属磷酸盐等。
磷酸盐通常以磷酸根(PO4^3-)的形式存在。
磷酸根的存在方式有溶解态、颗粒态和絮凝态。
其中溶解态磷酸根指的是以离子形式存在于水体中,颗粒态磷酸根指的是附着在颗粒表面,絮凝态磷酸根则是以胶体或气泡的形式存在于水体中。
2.化学除磷的原理化学除磷主要通过添加化学剂将水体中的磷酸根转化为难溶的磷酸钙或其他难溶物质,从而使磷酸根沉降、沉积或被过滤去除。
常用的化学剂包括氯化铝、硫酸铝、氧化铁、氧化铝等。
添加化学剂后,化学反应会产生沉淀,沉淀与颗粒状磷酸根结合形成大颗粒,从而在水体中迅速沉降。
(1)水体中磷酸根的浓度测定:需要进行水样采集,并通过磷酸盐的测定方法,如钼酸盐法、电磁法、原子吸收法等,测定水体中磷酸根的浓度。
(2)化学剂的选择:根据水体中磷酸根的浓度和水质情况,选择合适的化学剂。
(3)计算化学剂的投加量:需要根据化学反应的生成物平衡原理,计算出达到目标去除率所需的化学剂投加量。
(4)工艺参数的确定:包括搅拌时间、沉淀时间、混合速度等。
(5)设备设计及选型:包括混凝沉淀池、混合搅拌器和澄清池等设备的设计和选型。
(6)系统控制方案的设计:包括pH值的调节、化学剂的投加控制等。
通过上述的设计计算,可以指导实际的化学除磷工程建设和运行。
4.化学除磷的效果评价对于化学除磷的效果评价主要根据两个指标进行评估:去除率和处理效果。
去除率是指在单位时间内,化学除磷处理后水体中磷酸根浓度与处理前浓度之间的差异。
其计算公式为:磷酸根去除率(%)=(初始浓度-终止浓度)/初始浓度×100处理效果则通过监测水质指标,如总磷、水体浊度、COD、氨氮等指标的变化情况来评估。
化学除磷计算

化学除磷计算前言在静止的或流动缓慢的水体中,如果磷的浓度过高,会造成水体的富营养化,其危害已众所周知,因而在污水处理中进行除磷是必要的。
我国《污水综合排放标准》(8978—1996)规定,城市污水处理厂磷酸盐(以P计)一级排放标准为0.5mg/l。
磷的去除有化学除磷生物除磷两种工艺,生物除磷是一种相对经济的除磷方法,但由于该除磷工艺目前还不能保证稳定达到0.5mg/l出水标准的要求,所以要达到稳定的出水标准,常需要采取化学除磷措施来满足要求。
本文主要介绍化学除磷的基本机理、主要工艺形式和药剂投加量的计算方法。
2 污水中的磷负荷欧洲一些国家曾对生活污水中的总磷PT做过多次调查,主要结果见表1。
由人类食物产生的磷是不变的,但国内外目前普遍开始采用无磷洗涤剂,所以由洗涤剂产生的磷几年降低了许多。
城市污水原水中的磷浓度在我国主要取决于工业废水中的磷含量。
国外生活污水一般为10~25mg/l,我国一般为5~10mg/l。
其大部分是无机化合磷,并是溶解状的,这一部分主要由来自洗涤剂的正磷酸盐和稠环磷酸盐组成。
总磷中的一小部分是有机化合磷,其以溶解和非溶解状态存在。
稠环磷酸盐(如P3O105-)和有机化合磷(核酸 )一般在污水管网中和污水处理中就已经转化为正磷酸盐(PO43-)。
3 化学除磷的基础化学除磷是通过化学沉析过程完成的,化学沉析是指通过向污水中投加无机金属盐药剂,其与污水中溶解性的盐类,如磷酸盐混合后,形成颗粒状、非溶解性的物质,这一过程涉及的是所谓的相转移过程,反应方程举例如式1。
实际上投加化学药剂后,污水中进行的不仅仅是沉析反应,同时还进行着化学絮凝反应,所以必须区分化学沉析和化学絮凝的差异(如图1所示)。
FeCl3+K3PO4→FePO4↓+3KCl式1污水沉析反应可以简单的理解为:水中溶解状的物质,大部分是离子状物质转换为非溶解、颗粒状形式的过程,絮凝则是细小的非溶解状的固体物互相粘结成较大形状的过程,所以絮凝不是相转移过程。
除磷实验报告

一、实验目的1. 了解和掌握除磷的基本原理和方法。
2. 通过实验验证不同除磷剂的除磷效果。
3. 分析除磷过程中影响除磷效果的因素。
二、实验原理磷是水体富营养化的主要原因之一,过量的磷会导致水体中的藻类过度繁殖,进而引起水质恶化。
本实验通过向水体中加入除磷剂,使水体中的磷含量降低,从而达到净化水质的目的。
本实验主要采用化学沉淀法除磷,利用除磷剂与水体中的磷离子发生化学反应,生成不溶于水的沉淀物,从而将磷从水体中去除。
三、实验材料与仪器1. 实验材料:- 磷酸二氢钾(KH2PO4)- 氢氧化钠(NaOH)- 氯化铁(FeCl3)- 硫酸铝钾(KAl(SO4)2·12H2O)- 水样- 除磷剂(如活性炭、聚合硫酸铁等)2. 实验仪器:- 1000 mL 烧杯- 100 mL 容量瓶- 玻璃棒- 电子天平- pH计- 滴定管- 移液管- 水浴锅四、实验步骤1. 准备水样:取一定量的水样,测定其初始磷含量。
2. 配制除磷剂溶液:按照实验要求,配制一定浓度的除磷剂溶液。
3. 取100 mL水样于1000 mL烧杯中,加入适量的除磷剂溶液。
4. 用玻璃棒搅拌,使除磷剂与水样充分混合。
5. 将混合后的水样置于水浴锅中,加热至60-70℃,保持一段时间。
6. 加热完成后,用玻璃棒搅拌均匀。
7. 取一定量的混合液于100 mL容量瓶中,用去离子水稀释至刻度。
8. 使用pH计测定稀释后的水样的pH值。
9. 用滴定管滴加一定量的氢氧化钠溶液,直至水样pH值达到7.0。
10. 使用移液管取一定量的稀释后的水样,加入氯化铁溶液,滴加氢氧化钠溶液,直至出现淡红色沉淀。
11. 记录滴定过程中氢氧化钠溶液的用量。
12. 根据滴定结果,计算水样中磷的含量。
13. 重复实验,验证不同除磷剂的除磷效果。
五、实验结果与分析1. 实验结果:| 除磷剂 | 初始磷含量(mg/L) | 除磷后磷含量(mg/L) | 除磷率(%) || ------ | ------------------ | ------------------ | ---------- || 活性炭 | 0.8 | 0.2 | 75 || 聚合硫酸铁 | 0.8 | 0.1 | 87.5 || 氯化铁 | 0.8 | 0.05 | 93.75 |2. 分析:通过实验结果可以看出,不同除磷剂的除磷效果存在差异。
化学除磷理论及规范

6.7化学除磷污水经二级办理后,其出水总磷不可以达到要求时,可采纳化学除磷工艺办理。
污水一级办理以及污泥办理过程中产生的液体有除磷要求时,也可采纳化学除磷工艺。
化学除磷可采纳生物反响池的前置投加、后置投加和同步投加,也可采用多点投加。
化学除磷设计中,药剂的种类、剂量和投加点宜依据试验资料确立。
化学除磷的药剂可采纳铝盐、铁盐,也可采纳石灰。
用铝盐或铁盐作混凝剂时,宜投加离子型聚合电解质作为助凝剂。
采纳铝盐或铁盐作混凝剂时,其投加混凝剂与污水中总磷的摩尔比宜为1.5 ~ 3。
化学除磷时应试虑产生的污泥量。
化学除磷时,对接触腐化性物质的设备和管道应采纳防腐化举措。
条则说明:6.7化学除磷对于化学除磷应用范围的规定。
《城镇污水办理厂污染物排放标准》(GB18918) 规定总磷的排放标准:当达到一级 A 标准时,在 2005 年 12 月 31 日前建设的污水厂为 1mg/l ,2006 年 1 月 1 日起建设的污水厂为0.5mg/l 。
一般城市污水经生物除磷后,较难达到后者的标准,故可辅以化学除磷,以知足出水水质的要求。
加强一级办理,可去除污水中绝大多数磷。
上海白龙港城市污水厂试验表示,当 FeCl3 投加量为 40~ 80mg/l ,或 Al2(SO4)3•18H2O 投加量为 60~80mg/l 时,出入水磷酸盐磷浓度分别为2~ 9mg/l 和 0.2 ~ 1.1mg/l ,去除率为 60~ 95%。
污泥厌氧办理过程中的上清液、脱水机的过滤液和浓缩池上清液等,因为在厌氧条件下,有大批含磷物质开释到液体中,若回流入污水办理系统,将造成污水办理系统中磷的恶性循环,所以应先进行除磷,一般宜采纳化学除磷。
对于药剂投加点的规定。
以生物反响池为界,在生物反响池前投加为前置投加,在生物反响池后投加为后置投加,投加在生物反响池内为同步投加,在生物反响池前后都投加为多点投加。
前置投加点在原污水处,形成积淀物与初沉污泥一同清除。
污水除磷计算

3.94 0.67
Kg/d
氢氧化铝污泥投入的铝除反应生成磷酸铝外,剩余部分反应生成氢氧化铝沉淀
化学反应方程式:
AI3++3OH-=AI(OH)3↓
氢氧化铝与铝的摩尔质量比K=TAI(OH)3/TAI
2.89
参与反应的铝离子量DAH=(KA-1)*TA
2.22
mg/l
氢氧化铝污泥产量WAH=MAH*DAH*Q/1000
7% 7% 7%
AI2(SO4)3
7%
聚合氯化铝PAC
10%
聚合硫酸铁PFS 7%
镁含量 7%
铝27g/mol,磷31g/mol 部分反应生成氢氧化铝沉淀
铝27g/mol
解固体
投加系数
2.5
1.5~3(室外排水设计规范P69)
实际需铝量
3.70
mg/l
购买PAC固体中AI2O3有效含量
28%
%
有效铝含量
14.82%
%
所需投PAC的量
2.50
Kg/d
所需投PAC的量
0.90
t/年
污泥量计算
磷酸铝污泥化学方程式:
AI3++PO43--=AIPO4↓
磷酸铝与磷的摩尔质量比K=TAIPO4/TP 磷酸铝污泥产量W=M*TP*Q/1000
0.64
Kg/d
化学污泥量WA=WAP+WAH
1.31
Kg/d备注:忽略ຫໍສະໝຸດ 盐制品的不溶解固体I2O3)
1mol铝消耗1mol磷 铝27g/mol,磷31g/mol 1.5~3(室外排水设计规范P69)
查包装袋说明
药品铝和铁含量表
药品名称 含铁量 铝含量 钙含量
除磷PAC加药量计算
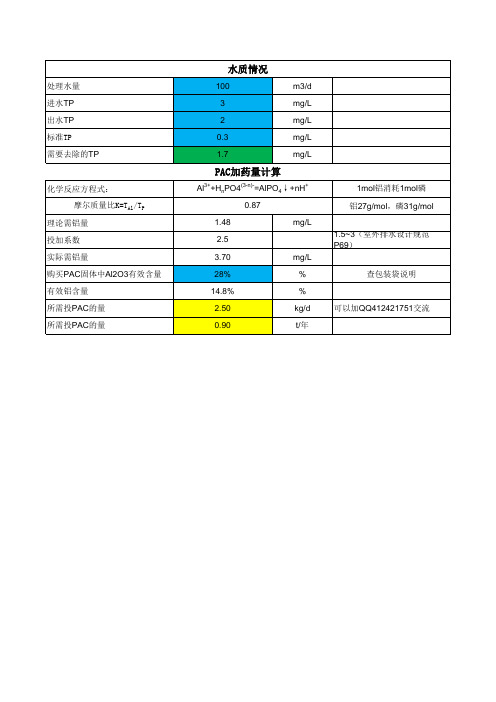
Al3++HnPO4(3-n)-=AlPO4↓+nH+
0.87
1.48
mg/L
2.5
3.70
mg/L
28%
%
14.8%
%
2.50
kg/d
0.90
t/年
1mol铝消耗1mol磷 铝27g/mol,磷31g/mol
1.5~3(室外排水设计规范 P69)
查包装袋说明
可以加QQ412421751交流
污泥量计算
处理水量 进水TP 出水TP 标准TP 需要去除的TP
化学反应方程式: 摩尔质量比K=TAl/TP
理论需铝量 投加系数 实际需铝量 购买PAC固体中Al2O3有效含量 有效铝含量 所需投PAC的量 所需投PAC的量
水质情况
100
m3/d
3
mg/L
2
mg/L
0.3
mg/L
1.7
mg/L
PAC加药量计算
Байду номын сангаас
磷酸铝污泥 化Al3学++反PO应4方3磷=A酸lP铝O4与↓磷 的摩尔质量
3.94 (以P计)
磷酸铝污泥 产量
0.67 kg/d
氢氧化铝污 泥投入的铝 化学反应方 程式 氢氧化铝与 铝的摩尔质
Al3++3OH=Al(OH)3↓
2.89 (以P计)
参与反应的 铝离子
2.22 mg/L
氢氧化铝污 泥产量
0.64 kg/d
化学污泥量 WA=WAP
1.31 kg/d 忽略铝盐制 品的不溶解
除磷PAC加药量计算

PAC加药量计算
Al3++HnPO4(3-n)-=AlPO4↓+nH+
0.87
2.Байду номын сангаас1
mg/L
2.5
6.53
mg/L
28%
%
14.8%
%
881.34
kg/d
317.28 44.06682028
t/年 mg/L
1mol铝消耗1mol磷 铝27g/mol,磷31g/mol
1.5~3(室外排水设计规范P69)
处理水量 进水TP 出水TP 标准TP 需要去除的TP
化学反应方程式: 摩尔质量比K=TAl/TP
理论需铝量 投加系数 实际需铝量 购买PAC固体中Al2O3有效含量 有效铝含量 所需投PAC的量 所需投PAC的量 核算PAC投加浓度
水质情况
20000
m3/d
10
mg/L
8
mg/L
5
mg/L
3
mg/L
污泥量计算
磷酸铝污泥 化Al3学++反PO应4方3磷=A酸lP铝O4与↓磷 的摩尔质量
3.94 (以P计)
磷酸铝污泥 产量
236.13 kg/d
氢氧化铝污 泥投入的铝 化学反应方 程式 氢氧化铝与 铝的摩尔质
Al3++3OH=Al(OH)3↓
2.89 (以P计)
参与反应的 铝离子
3.92 mg/L
氢氧化铝污 泥产量
226.45 kg/d
化学污泥量 WA=WAP
462.58 kg/d 忽略铝盐制 品的不溶解
碳源投加量及除磷药剂投加量计算公式

碳源计算公式1、碳源选择通常反硝化可利用的碳源分为快速碳源(如甲醇、乙酸、乙酸钠等)、慢速碳源(如淀粉、蛋白质、葡萄糖等)和细胞物质。
不同的外加碳源对系统的反硝化影响不同,即使外加碳投加量相同,反硝化效果也不同。
与慢速碳源和细胞物质相比,甲醇、乙醇、乙酸、乙酸钠等快速碳源的反硝化速率最快,因此应用较多。
表1 对比了四种快速碳源的性能。
2、碳源投加量计算1)氮平衡进水总氮和出水总氮均包括各种形态的氮。
进水总氮主要是氨氮和有机氮,出水总氮主要是硝态氮和有机氮。
进水总氮进入到生物反应池,一部分通过反硝化作用排入大气,一部分通过同化作用进入活性污泥中,剩余的出水总氮需满足相关水质排放要求。
2)碳源投加量计算同化作用进入污泥中的氮按BOD5 去除量的5%计,即0.05(Si-Se),其中Si、Se 分别为进水和出水的BOD5 浓度。
反硝化作用去除的氮与反硝化工艺缺氧池容大小和进水BOD5 浓度有关。
反硝化设计参数的概念,是将其定义为反硝化的硝态氮浓度与进水BOD5 浓度之比,表示为Kde(kgNO3--N/kgBOD5)。
由此可算出反硝化去除的硝态氮[NO3--N]=KdeSi。
从理论上讲,反硝化1kg 硝态氮消耗2.86kgBOD5,即:Kde=1/2.86(kg NO3--N/kgBOD5)=0.35(kg NO3--N/kgBOD5)污水处理厂需消耗外加碳源对应氮量的计算公式为:N=Ne 计-NsNe 计=Ni - KdeSi - 0.05(Si-Se)式中:N—需消耗外加碳源对应氮量,mg/L;Ne 计—根据设计的污水水质和设计的工艺参数计算出能达到的出水总氮,mg/L;Ns—二沉池出水总氮排放标准,mg/L;Kde—0.35,kgNO3--N/kgBOD5;Si—进水BOD5 浓度,mg/L;Se—出水BOD5 浓度,mg/L;Ne 计需通过建立氮平衡方程计算,生化反应系统的氮平衡见图1。
通过计算出的氮量,折算成需消耗的碳量。
水处理-除磷计算公式

1、除磷药剂投加量的计算 国内较常用的是铁盐或铝盐,它们与磷的化学反应如式(1)、(2)。 Al3++PO3-4→AlPO4↓(1) Fe3++PO3-4→FePO4↓(2) 与沉淀反应相竞争的反应是金属离子与 OH-的反应,反应式如式(3)、(4)。 Al3++3OH-→Al(OH)3↓(3) Fe3++3OH-→Fe(OH)3↓(4) 由式(1)和式(2)可知去除 1mol 的磷酸盐,需要 1mol 的铁离子或铝离子。 由于在实际工程中,反应并不是 100%有效进行的,加之 OH-会参与竞争,与金属离 子反应,生成相应的氢氧化物,如式(3) 和式(4),所以实际化学沉淀药剂一般需要超 量投加,以保证达到所需要的出水 P 浓度。 《给水排水设计手册》第 5 册和德国设计规范中都提到了同步沉淀化学除磷可按 1mol 磷需投加 1.5mol 的铝盐 (或铁盐)来考虑。 为了计算方便,实际计算中将摩尔换算成质量单位。如: 1molFe=56gFe,1 molAl=27gAl,1molP=31gP; 也就是说去除 1kg 磷,当采用铁盐时需要投加:1.5×(56/31)=2.7 kgFe/kgP; 当采用铝盐时需投加:1.5×(27/31)= 1.3kgAl/kgP。 2、需要辅助化学除磷去除的磷量计算 同 步 沉 淀 化 学 除 磷 系 统 中 ,想 要 计 算 出 除 磷 药 剂 的 投 加 量 ,关 键 是 先 求 得 需 要 辅 助 化 学除磷去除的磷量。对于已经运行的污水处理厂及设计中的污水处理厂其算法有所不 同。 1)已经运行的污水处理厂 PPrec=PEST-PER (5) 式中 PPrec—— 需 要 辅 助 化 学 除 磷 去 除 的 磷 量 , mg/L ; PEST —— 二 沉 池 出 水 总 磷 实 测 浓 度 , mg/L ; PER —— 污 水 处 理 厂 出 水 允 许 总 磷 浓 度 , mg/L 。 2)设计中的污水处理厂 根据磷的物料平衡可得: PPrec=PIAT-PER-PBM -PBioP (6) 式中 PIAT —— 生 化 系 统 进 水 中 总 磷 设 计 浓 度 , mg/L ; PBM ——通过生物合成去除的磷量,PBM= 0.01CBOD,IAT,mg/L; CBOD,IAT——生化系统进水中 BOD5 实测浓度, mg/L; PBioP—— 通 过 生 物 过 量 吸 附 去 除 的 磷 量 , mg/L 。 PBioP 值与多种因素有关,德国 ATV-A131 标准中推荐 PBioP 的取值可根据如下几 种情况进行估算:
除磷

污水处理中的化学除磷的工艺和方法磷的去除有化学除磷生物除磷两种工艺,生物除磷是一种相对经济的除磷方法,但由于该除磷工艺目前还不能保证稳定达到0.5mg/l出水标准的要求,所以要达到稳定的出水标准,常需要采取化学除磷措施来满足要求。
化学除磷是通过化学沉析过程完成的,化学沉析是指通过向污水中投加无机金属盐药剂,其与污水中溶解性的盐类,如磷酸盐混合后,形成颗粒状、非溶解性的物质,这一过程涉及的是所谓的相转移过程,反应方程举例如式1。
实际上投加化学药剂后,污水中进行的不仅仅是沉析反应,同时还进行着化学絮凝反应,所以必须区分化学沉析和化学絮凝的差异。
FeCl3+K3PO4→FePO4↓+3KCl 式1 污水沉析反应可以简单的理解为:水中溶解状的物质,大部分是离子状物质转换为非溶解、颗粒状形式的过程,絮凝则是细小的非溶解状的固体物互相粘结成较大形状的过程,所以絮凝不是相转移过程。
在污水净化工艺中,絮凝和沉析都是极为重要的,但絮凝是用于改善沉淀池的沉淀效果,而沉析则用于污水中溶解性磷的去除。
如果利用沉析工艺实现相的转换,则当向污水中投加了溶解性的金属盐药剂后,一方面溶解性的磷转换成为非溶解性的磷酸金属盐,也会同时产生非溶解性的氢氧化物(取决于PH值)。
另一方面,随着沉析物的增加及较小的非溶解性固体物聚积成较大的非溶解性固体物,使稳定的胶体脱稳,通过速度梯度或扩散过程使脱稳的胶体互相接触生成絮凝体。
最后通过固—液分离步骤,得到净化的污水和固一液浓缩物(化学污泥),达到化学除磷的目的。
根据化学沉析反应的基础,为了生成磷酸盐化合物,用于化学除磷的化学药剂主要是金属盐药剂和氢氧化钙(熟石灰)。
许多高价金属离子药剂投加到污水中后,都会与污水中的溶解性磷离子结合生成难溶解性的化合物。
出于经济原因,用于磷沉析的金属盐药剂主要是Fe3+、Al3+和Fe2+盐和石灰。
这些药剂是以溶液和悬浮液状态使用的。
二价铁盐仅当污水中含有氧,能被氧化成三价铁盐时才能使用。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
化学除磷的设计计算1前言在静止的或流动缓慢的水体中,如果磷的浓度过高,会造成水体的富营养化,其危害已众所周知,因而在污水处理中进行除磷是必要的。
我国《污水综合排放标准》(8978—1996)规定,城市污水处理厂磷酸盐(以P计)一级排放标准为0.5mg/l。
磷的去除有化学除磷生物除磷两种工艺,生物除磷是一种相对经济的除磷方法,但由于该除磷工艺目前还不能保证稳定达到0.5mg/l出水标准的要求,所以要达到稳定的出水标准,常需要采取化学除磷措施来满足要求。
本文主要介绍化学除磷的基本机理、主要工艺形式和药剂投加量的计算方法。
2污水中的磷负荷欧洲一些国家曾对生活污水中的总磷PT做过多次调查,主要结果见表1。
由人类食物产生的磷是不变的,但国内外目前普遍开始采用无磷洗涤剂,所以由洗涤剂产生的磷几年降低了许多。
城市污水原水中的磷浓度在我国主要取决于工业废水中的磷含量。
国外生活污水一般为10~25mg/l,我国一般为5~10mg/l。
其大部分是无机化合磷,并是溶解状的,这一部分主要由来自洗涤剂的正磷酸盐和稠环磷酸盐组成。
总磷中的一小部分是有机化合磷,其以溶解和非溶解状态存在。
稠环磷酸盐(如P3O105-)和有机化合磷(核酸)一般在污水管网中和污水处理中就已经转化为正磷酸盐(PO43-)。
3化学除磷的基础化学除磷是通过化学沉析过程完成的,化学沉析是指通过向污水中投加无机金属盐药剂,其与污水中溶解性的盐类,如磷酸盐混合后,形成颗粒状、非溶解性的物质,这一过程涉及的是所谓的相转移过程,反应方程举例如式1。
实际上投加化学药剂后,污水中进行的不仅仅是沉析反应,同时还进行着化学絮凝反应,所以必须区分化学沉析和化学絮凝的差异(如图1所示)。
FeCl3+K3PO4→FePO4↓+3KCl式1污水沉析反应可以简单的理解为:水中溶解状的物质,大部分是离子状物质转换为非溶解、颗粒状形式的过程,絮凝则是细小的非溶解状的固体物互相粘结成较大形状的过程,所以絮凝不是相转移过程。
在污水净化工艺中,絮凝和沉析都是极为重要的,但絮凝是用于改善沉淀池的沉淀效果,而沉析则用于污水中溶解性磷的去除。
如果利用沉析工艺实现相的转换,则当向污水中投加了溶解性的金属盐药剂后,一方面溶解性的磷转换成为非溶解性的磷酸金属盐,也会同时产生非溶解性的氢氧化物(取决于PH值)。
另一方面,随着沉析物的增加及较小的非溶解性固体物聚积成较大的非溶解性固体物,使稳定的胶体脱稳,通过速度梯度或扩散过程使脱稳的胶体互相接触生成絮凝体。
最后通过固—液分离步骤,得到净化的污水和固一液浓缩物(化学污泥),达到化学除磷的目的。
4化学除磷药剂的类型根据化学沉析反应的基础,为了生成磷酸盐化合物,用于化学除磷的化学药剂主要是金属盐药剂和氢氧化钙(熟石灰)。
许多高价金属离子药剂投加到污水中后,都会与污水中的溶解性磷离子结合生成难溶解性的化合物。
出于经济原因,用于磷沉析的金属盐药剂主要是Fe3+、Al3+和Fe2+盐和石灰。
这些药剂是以溶液和悬浮液状态使用的。
二价铁盐仅当污水中含有氧,能被氧化成三价铁盐时才能使用。
Fe2+在实际中为了能被氧化常投加到曝气沉砂池或采用同步沉析工艺投加到曝气池中,其效果同使用Fe3+一样,反应式如式2、3。
Al3++PO43-→AlPO4↓pH=6~7式2Fe3++PO43-→FePO4↓pH=5~5.5式3与沉析反应相竞争的反应是金属离子与OH的反应,所以对于各种不同的金属盐产品应注意的是金属的离子量,反应式如式4、5。
Al3++3OH-→Al(OH)3↓式4Fe3++3OH-→Fe(OH)3式5金属氢氧化物会形成大块的絮凝体,这对于沉析产物的絮凝是有利的,同时还会吸附胶体状的物质、细微悬浮颗粒。
需要注意的是有机物在以化学除磷为目的化学沉析反应中的沉析去除是次要的,但在分离时有机性胶体以及悬浮物的凝结在絮凝体中则是决定性的过程。
沉析效果是受PH值影响的,金属磷酸盐的溶解性同样也受PH的影响。
对于铁盐最佳PH值范围为5. 0~5.5,对于铝盐为6.0~7.0,因为在以上PH值范围内FePO4或AIPO4的溶解性最小。
另外使用金属盐药剂会给污水和污泥处理还会带来益处,比如会降低污泥的污泥指数,有利于沼气脱硫等。
由于金属盐药剂的投加会使污水处理厂出水中的Cl-或SO2-4离子含量增加。
如果沉析药剂溶液中另外含有酸的话,则需特别加以注意。
投加金属盐药剂后相应会降低污水的碱度,这也许会对净化产生不利影响。
当在同步沉析工艺中使用硫酸铁时,必须考虑对硝化反应的影响。
另外,如果污水处理厂污泥用于农业,使用金属盐药剂除磷时必须考虑铝或者铁负荷对农业的影响。
除了金属盐药剂外,氢氧化钙也用作沉析药剂。
在沉折过程中,对于不溶解性的磷酸钙的形成起主要作用的不是Ca2+,而是OH-离子,因为随着pH值的提高,磷酸钙的溶解性降低,采用Ca(OH)2除磷要求的pH值为8.5以上。
磷酸钙的形成是按反应式6进行的:5Ca2++3po43-+OH-→Ca5(PO4)3OH↓pH ≥8.5式6但在pH值为8.5到10.5的范围内除了会产生磷酸钙沉析外,还会产生碳酸钙,这也许会导致在池壁或渠、管壁上结垢,反应式如式7。
Ca2++CO32-→CaCO3式7与钙进行磷酸盐沉析的反应除了受到PH值的影响,另外还受到碳酸氢根浓度(碱度)的影响。
在一定的PH值惰况下,钙的投加量是与碱度成正比的。
对于软或中硬的污水,采用钙沉析时,为了达到所要求的PH值所需要的钙量是很少的,具有强缓冲能力的污水相反则要求较大的钙投加量。
污水除磷常用的药剂类型详见表2。
5化学沉析工艺化学沉析工艺是按沉析药剂的投加地点来区分的,实际中常采用的有:前沉析、同步沉析和后沉析或在生物处理之后加絮凝过滤。
(1)前沉析前沉析工艺的特点是沉析药剂投加在沉砂池中,或者初次沉淀池的进水渠(管)中,或者文丘里渠(利用涡流)中。
其一般需要设置产生涡流的装置或者供给能量以满足混合的需要。
相应产生的沉析产物(大块状的絮凝体)则在一次沉淀池中通过沉淀而被分离。
如果生物段采用的是生物滤池,则不允许使Fe2+药剂,以防止对填料产生危害(产生黄锈)。
前沉析工艺(如图2所示)特别适合于现有污水处理厂的改建(增加化学除磷措施),因为通过这一工艺步骤不仅可以去除磷,而且可以减少生物处理设施的负荷。
常用的沉析药剂主要是生灰和金属盐药剂。
经前沉析后剩余磷酸盐的含量为1.5-2.5mg/1,完全能满足后续生物处理对磷的需要。
(2)同步沉析同步沉析是使用最广泛的化学除磷工艺,在国外约占所有化学除磷工艺的50%。
其工艺是将沉析药剂投加在曝气池出水或二次沉淀池进水中,个别情况也有将药剂投加在曝气池进水或回流污泥渠(管)中。
图3是采用同步沉析的活性污泥法工艺简图。
当采用生物转盘工艺时,情况和活性污泥法类似,但对于生物滤池工艺能否将药剂投加在二次沉淀池进水中尚值得探讨。
(3)后沉析后沉析是将沉析、絮凝以及被絮凝物质的分离在一个与生物设施相分离的设施中进行,因而也就有二段法工艺的说法。
一般将沉析药剂投加到二次沉淀池后的一个混合池(M池)中,并在其后设置絮凝池(F池)和沉淀池(或气浮池)。
后沉析工艺简图如图4所示。
对于要求不严的受纳水体,在后沉析工艺中可采用石灰乳液药剂,但必须对出水PH值加以控制,比如采用沼气中的CO2进行中和。
采用气浮池可以比沉淀池更好地去除悬浮物和总磷,但因为需恒定供应空气而运转费用较高。
三种工艺的优缺点汇总于表3中。
6 化学沉析药剂量的计算由式2和式3去除一分子的磷酸盐,需要一分子的铁盐或者铝盐。
为了计算方便,实际计算采用克分子(mol)或者克原子量。
如:1mol H=1g molFe=56g 1molAl=27g 1mol P=31g在化学沉析除磷时,去除lmol(31g)P 至少需要lmol(56g)Fe ,或者至少需要1.8(56/31)倍的Fe ,或者O.9(27/31)倍的Al 。
也就是说去除lgP 至少需要1.8g 的Fe ,或者O.9g 的Al 。
由于在实际中,反应中并不是1OO%有效进行的,加之OH-会与金属离子竞争反应,生成相应的氢氧化,如式4和式5,所以实际化学沉析药剂投加一般需要超量投加,以保证达到所需要的出水P 浓度。
德国在计算时,提出了投加系数β的概念,即:β=(molFe,molAl)/molP 式8投加系数β是受多种因素影响的,如投加地点、混合条件等,实际投加时建议通过投加试验确定,图5是投加系数和磷减少量的关系。
在最佳条件下(适宜的投加、良好的混合和絮凝体的形成条件)β=1;在非最佳条件下,β=2到3或更高。
过量投加药剂不仅会使药剂费增加,而且因氢氧化物的大量形成也会使污泥量大大增加,这种污泥体积大、难脱水。
德国在实际计算中,为了有效地去除磷(出水保持<1mgP/1),β值为1.5,也就是说去除1kg磷,需要投加:1.5×(56/31)=2.7 kg Fe或者,1.5×(27/31)=1.3 kg Al若用石灰作为化学沉析药剂,则不能采用这种计算方法,因为其要求投加的pH值大于8.5,而且投加量受污水碱度(缓冲能力)的影响,所以其投加量必须针对各自的污水通过试验确定。
从严格意义上讲,投加系数β值的概念只适用于后沉析,对于前沉析和同步沉析在计算时还应考虑:·回流污泥中含有未反应的药剂;·在初次沉淀池中和生物过程去除的磷。
7计算举例例1:污水处理厂设计水量为10000m3/d,进水中的P浓度为14mg/1,出水P浓度要求达到1mg/l。
设计采用沉析药剂三氯化铝AlCl3,其有效成分为6%(60g/kgAlCl3),密度为1.3kg/l。
为同步沉析,试计算所需要的药剂量。
解:经过初次沉淀地沉淀处理后去除的磷为2mg/l,则生物处理设施进水的P浓度为11mg/l,经过生物同化作用去除的P为1mg/l。
则需经沉析去除的:P负荷=10000m3/d·(0.011-0.001)kg/m3=100kg/d设计采用投加系数β值为1.5,设计Al的投加量为:1.5×(27/31)×100=130kg Al/d折算需要药剂量为:130×1000(g/d)/60(g/kg)=2167kg/d AlCl3折算需要体积量为:2167(kg/d)/1.3(kg/l)=16671/dAlCl3例2:设计采用药剂硫酸亚铁FeSO4,有效成分为180gFe/kgFeSO4,在10℃时的饱和溶解度为400gF eSO4/l,其它设计参数同例1。
解:设计采用投加系数β值为1.5,设计Fe的投加量为:1.5×5631×100=270kg Fe/d折算需要药剂量为:270×1000(g/d)/180(g/kg)=1500kg/dFeSO4饱和溶液中的有效成分为:180(g/kg)·0.4(kg/l)=72gFe/l FeSO4折算需要体积量为:1500·1000(g/d)/72(g/l)=20833l/dFeSO48沉析对污水处理的影响(1)沉析对污水处理厂出水金属含量的影响在污水处理厂出水中金属和药剂的含量主要取决于对悬浮物的分离,当然药剂的投加、β值、pH值、污水碱度及投加技术也都对其有影响。
