糖绝对构型确定方法
糖的构型及其画法

一、单糖的结构表示单糖结构式的三种方法:Fischer 投影式、Haworth 投影式与优势构象式 1、葡萄糖(Fischer 投影式)D,L 表示相对构型结构式中,位号最大、离羰基最远的手性碳原子的羟基在右侧为D 型;羟基在左侧的为L 型。
CHO OH H H HO OH H OHHCH 2OH 5D-葡萄糖CHO OH H H HO OH H HHO2OH5L-葡萄糖2、Fischer 投影式不能表示单糖在水溶液中的真实存在形式,因此有了Haworth 投影式。
Haworth 投影式中,C4位羟基在面下为D 型,在面上则为L 型单糖成环后形成了一个新的手性碳原子,形成一对端基差向异构体,有α、β二种构型。
端基碳上的羟基与C4羟基在同侧称α型,异侧β型O OHHH OH HHOHCH 2OH O HOHHOH HOHCH 2OHβ-D-葡萄糖 α-D-葡萄糖3、虽然Haworth 式表示方法较Fischer 式有所改进,但它仍然就是一种简化了的方式,尚不能完全表达糖的真实存在状态。
经实验证明葡萄糖在溶液或固体状态时其优势构象就是椅式当C 4在面上,C 1在面下,称C1式(通常绝大多数单糖的优势构象就是C1式) 当C 4在面下,C 1在面上,称1C 式O123451C 式O12345C1式对于β-D型与α-L型葡萄糖,当优势构象为C1式时,C1-OH 在环的面上,处于横键上,1C式时,在竖键O O对于α-D型与β-L型葡萄糖,当优势构象为C1式时,C1-OH 在环的面下,处于竖键上,1C式时,在横键OO竖键与横键的具体写法:1、横键与环上的键隔键平行;2、横键与竖键在环的面上面下交替排列。
例:(E)-2,3,5,4′-四羟基二苯乙烯-2-O-β-D-葡萄糖苷HOHOOOHOOHOHOHOH单糖的绝对构型如何测定1、GC法将单糖与手性试剂反应,(相当于在糖中引入一个新的手性中心)然后通过GC比较与标准单糖D与L型单糖衍生物的比移值,比移植相同的即为构型相同,反之亦然。
单糖的立体化学汇总

2.4 苷类
苷,又称配糖体,是糖或糖的衍生物(如氨基 糖、糖醛酸等)与另一非糖物质(称为苷元或 配基,aglycone or genin)通过糖的端基碳 原子连接而成的化合物。
第二章 糖和苷
三. 糖的化学性质
3.1 氧化反应:
单糖分子中有醛(酮)基、伯醇基、仲醇基 和邻二醇基结构单元。一般来说,醛(酮) 基最易被氧化,伯醇次之。在控制反应条件 的情况下,不同的氧化剂可选择性的氧化某 些特定基团。如Ag+、Cu+和溴水可将醛基 氧化成羧基,硝酸可使醛糖氧化成糖二酸,
第二章 糖和苷
二. 糖和苷的分类
Байду номын сангаас
2.1 单糖
2.2 低聚糖
二糖:蔗糖 三糖:棉子糖 四糖:水苏糖 五糖:毛蕊糖 还原糖:槐糖、樱草糖等 根据有无游离的醛或酮基 非还原糖:蔗糖,大多 数的三、四、五糖等
根据单糖的个数
2.3 多聚糖
多聚糖,又称多糖,是由10个以上单糖基通过苷 键连接而成。
(1)均多糖(homosaccharide):由一种单糖组 成的多糖称为均多糖。如葡聚糖。 (2)杂多糖(heterosaccharide): 由二种以上 单糖组成的多糖称为杂多糖。如葡萄甘露聚糖 (glucomannan)。
通常要确定一种多糖的均一性,至少要有两种 以上的方法才能确定。
5.2 分子量的测定
单糖、低聚糖及其苷的分子量测定目前大多 用质谱法。如电喷雾质谱(electrospray ionization, ESIMS)及近年来发展起来的基 质辅助激光电离质谱或基质辅助激光解析电 离飞行时间质谱(MALDIMS或MALDITOF-MS)可测定多糖、蛋白质等高分子化 合物的分子量。
第三章 糖和苷类化合物2

R
H OH
O
β-D-糖
OH H
O
β-L-糖
H OH
R
O
α-L-糖
OH H
R
(二)、低聚糖
根据是否含有游离的醛基或酮基,分为: 非还原糖:单糖以端基羟基脱水缩合,无还原性。 如蔗糖,大多数的三、四、五糖 还原糖:单糖不以端基羟基脱水缩合,有还原性。 如芸香糖、麦芽糖、龙胆二糖等
HO
OH
O
O
还原
D-木糖醇 4.去氧糖 单糖分子一个或二个羟基为氢原子代替,该 类糖在强心苷中多见,并有特殊的性质。
糖的绝对构型:
六碳吡喃糖的C5(五碳呋喃糖的C4)上取 代基,向上为D型,向下为L型。
糖端基碳原子相对构型:
C1羟基与六碳糖C5(五碳糖的C4)取代基在 环同侧的为β 型。 C1羟基与六碳糖C5(五碳糖的C4)取代基在 环异侧的为α 型。
苦杏仁苷(镇咳)
(2)硫苷 糖半缩醛羟基和苷元上巯基(-SH)缩合 植物体内芥子酶常与硫苷共存,水解后的 苷元不含巯基,多为异硫氰酸酯类。
-
O3SO
N CH3 O
N CH2 CH CH2 C S
OSO3K glc
HO
S
O OH
黑芥子苷
OH
OH
萝卜苷
(3)氮苷 糖的端基碳原子与苷元上氮原子缩合。 生物化学中占重要位置:核酸重要组成 O
OH
D-呋喃甘露糖
D-呋喃阿洛糖
D-呋喃半乳糖
D-呋喃葡萄糖
结论2:六碳醛糖(含甲基五碳糖)的呋喃型 Haworth式中,C5-R为D, C5-S为L。
补充
糖的立体化学 3、F-H转化
2)五碳醛糖和六碳酮糖
第三章糖和苷类

苦杏仁苷 R=glc
野樱苷
R=H
9
天然药物化学
西安医学院
4、酯苷 是通过苷元羧基与糖缩合而成的苷。
OH O OH OH OH O R O CH2
CH2OH
山慈菇苷A 山慈菇苷B
R=H R=OH
5、吲哚苷 是由苷元吲哚醇中的羟基与糖缩合而成的苷。
O O glc N H H
+
OH N H
H N
[O] N H O
CHO HO H HO HO H OH H H CH2OH
L
CHO HO HO H HO H H OH H CH2OH
H HO H HO
CHO OH H OH H CH2OH
型
天然药物化学
西安医学院
4
②Haworth式:看不对称碳原子C5 取代基的
方向,向上为D,向下为L。
CH2OH O
O CH2OH OH
①碳原子数目少的糖>碳原子数目多的糖
②去氧糖>酮糖>醛糖
天然药物化学
西安医学院
17
[显色剂]
硝酸银试剂 还原糖显棕黑色
2、薄层色谱法 固定相 硅胶 移动相 极性大的溶剂系统 用 0.03mol/L硼酸溶液或无机盐水溶液代替 水制备薄层。 [显色剂]
硫酸的水或乙醇溶液
茴香醛-浓硫酸试剂
天然药物化学
西安医学院
1、醇苷 是通过苷元醇羟基与糖端基羟基脱水而成的苷。
OH O O OH HO OH
红景天苷
OH
天然药物化学
西安医学院
8
2、酚苷 是通过苷元酚羟基与糖端基羟基脱水缩合而 成的苷。
CH2OH
CH2OH
糖种类和构型的确定-2013 沈阳药科大学

4.02 (o), 3.74 (m) 4.02 (m)
73.8 66.7
39
32
D-Glc
24.1
L-Glc
样品
24.1
25.5
33
(三)芹糖构型的确定
由于芹糖是支链碳糖,在形成呋喃环的过程中,3位会 成为不对称的碳原子,因此会形成以下四种形式的异构体:
O OH
CH2OH
CHO H OH OH HOH2C CH2OH
OH
OH
HO
α-D-erythro-
β-D-erythroO OH
31
3. GC实验条件
进样器温度:270℃
进 样 量:1.0μL
分 流 比:10:1 载 气:氦气
柱 流 速:1.0ml/min
色 谱 柱:HP-5(30mm),内径0.32mm,膜厚0.25μm 柱 温:160℃(4℃/min) 200℃(keep5min,10℃/min) 240℃(keep10min) 检 测 器:FID 280℃(氮气体积流量: 30 ml/min) 氢气体积流量:40 ml/min 空气体积流量: 3400ml/min)
(2) 实验方法 1 mg标准糖与5 mg盐酸羟胺均匀混合,加入0.4 ml的吡啶, 90℃恒温水浴加热1小时,生成糖醇。反应物冷却至室温后,加 入0.6 ml乙酸酐,90℃水浴加热1小时,即生成糖腈乙酸酯衍生
物溶液,所得样品即可用GC分析。
27
2. GC实验条件
进样器温度:270℃
进 样 量:1.0μL
H-2
H-4 b
α -L-threo-
×
H-5
37
化合物结构:
Zhou and Qiu* et al. J. Nat. Prod. 2009, 72, 1563–1567
天然产物立体构型的确定方法

(2) 饱和环酮化合物的八区投影 • 环己酮各原子主要落在c平面“后区”,为判断旋
光分担方便起见采用投影法。
35
八区律规则:
• a). C-4的a和e,C-2和C-6的e键取代基均无 贡献。
• b). C-5的a和e,C-2的a键取代基均为正贡献。 • c). C-3的a和e,C-6的a键取代基均为负贡献。 • d). 旋光贡献具有加和性。 • e). 距离羰基越远,贡献越小。 • f). 基团越大,贡献越大。
作用:用来鉴定空间上接近的核,进而确定相对构型。
NOE
H H CH2OH
HO HO
O OR
OH
14
NOE最适合应用于刚性分子。在这种情况下,核组之间具 有确定的距离。根据NOE可以得到分子的立体化学信息。
���若样品为柔性分子,相对于核磁共振的时标,这样的分 子在溶液中存在着较快的构象互变,NOE测定的是个平均 的结果,因而无法得到具体的构象信息。
圆二色谱是吸收光谱,具有紫外吸收的手性化合物 可测定圆二色谱。 谱线特征:产生具有峰状或谷状Cotton 效应的图谱。 Cotton效应:平滑曲线在所测化合物的最大吸收波 长处出现的异常的峰状或谷状曲线。峰为正Cotton, 谷为负Cotton。
在化合物紫外最大吸收处,是ORD产生Cotton效 应谱线跨越基线的位置;是CD产生Cotton效应 谱线的位置。
左旋偏振光和右旋偏振光在通过手性介质时不但产生了旋光现象, 而且还产生了因吸收系数不同而导致的“圆二色性”(CD)
21
2.旋光性与旋光谱(ORD, Optical Rotatary Dispersion)
在一定温度下,用某一波长测定一光学性物质时,其旋光 性与样品浓度和洗手池的长度有下列关系。
一般糖苷中葡萄糖绝对构型的确定方法是

一般糖苷中葡萄糖绝对构型的确定方法是:先把糖苷在酸性条件下水解,用极性有机溶剂萃取其中的苷元,再将水溶液用1-三甲基硅烷基咪唑进行三甲基硅烷基化后,对烷基化产物进行GC分析,并与标准的D-和L-葡萄糖三甲基硅烷基化产物的保留时间进行比较,确定葡萄糖的绝对构型。
但我在审稿时,遇到如下问题,不知如何解决?对于下面这一类结构,葡萄糖通过醚键与一烷基相连,这一醚键在酸性条件下不易水解。
请问如何确定的葡萄糖绝对构型。
OR21答:我想R2上仍为半缩醛结构,在酸性条件下是可以分解的,不影响所述方法对构型的测定。
如果R1的结构不是很大,其它位的羟基硅醚化后,整体上应当具有好的挥发性,但会影响GC上的保留时间。
有时从糖的1-位H和2-位H的偶合常数J1,2,可推断六碳吡喃糖端基碳的立体结构属α-构型还是β-构型。
如葡萄糖或半乳糖,β-构型由于1-位H和2-位H间的二面角近于180°,其J1,2较大,为8 Hz左右,而α-构型二面角近于60°,J1,2为4 Hz左右。
由此可以区分苷键的α-和β-构型。
而甘露糖和鼠李糖的C2构型与葡萄糖的相反,2-位H在平伏键上,无论在α-或β-异构体中,与端基碳上质子间的二面角相近,约在60°左右,所以α-构型J1,2为1.6Hz 左右,β-构型为0.8 Hz左右,二者相差不大,难以区分羰基碳的构型。
六碳呋喃糖的J1,2在0~5 Hz,也缺乏测定端基碳构型的特征。
端基碳(C1或C2)的因形成半缩醛(酮),其共振峰的化学位移较大,在98~110ppm 之间。
在此区域内有几个信号表示可能有几种不同的单糖存在于糖链的重复单位之中。
端基碳上的半缩醛(酮)羟基在竖立键时该碳的化学位移较小于羟基在平伏键时的化学位移,以此可以区分该单糖为α-构型还是β-构型。
通过端基碳与氢的一键偶合常数1J H,C也可推断六碳吡喃糖端基碳的立体结构属α-构型还是β-构型,前者1J H,C为170~175Hz,后者1J H,C为160~165Hz。
糖种类和构型的确定-2013-沈阳药科大学

CH2OH HO
β -L-threo-
α -L-threo34
日本学者Tadashi等人研究以上四种形式的呋喃糖甲苷的氢 核磁共振性质,其中端基氢化学位移和偶合常数及端基碳化学 位移如下所示:
O OCH3
O
OCH3
CH2OH
OH
OH
HO
CH2OH
HO
α-D-erythro1
β-D-erythro2
C2-H
都约为60o (双面角)
无法通过J值来判定
19
b -D-甘露糖 C1-H
α-D-甘露糖
都约为60o (双面角)
C2-H
所以无法通过J值来判断构型
呋喃型糖偶合常数变化不大,不能用端基质子偶 合常数判断苷键构型
20
•偶合常数1JC1-H1:
21
(二) 糖的13C-NMR 1. 化学位移及偶合常数 • 端基碳: 95-105; CH-OH (C2、C3、C4) -- 70~85 CH2-OH (C6) 62 左右 CH3 < 20
22
2.苷化位移(Glycosylation shift, GS) 定义:糖与苷元成苷后, 苷元的-C, b-C和糖的 端基碳的化学位移值发生了变化, 这种变化称 苷化位移. 应用: 推测糖与苷元 ,糖与糖的连接位置 , 苷元 被苷化碳的绝对构型及碳氢信号归属.
24
四、糖的鉴定方法
单糖的鉴定方法
TLC
HPLC
GC
25
(用于确定糖的种类) (一)糖腈乙酸酯衍生化及GC分析
1. 标准糖糖腈乙酸酯衍生物的制备 (1) 反应原理 单糖和盐酸羟胺在吡啶中经加热后,反应生成糖肟,糖 肟与乙酸酐在加热条件下,继续反应生成具有挥发性的糖腈乙 酸酯衍生物。反应式如下:
单糖绝对构型的确定方法

单糖绝对构型的确定方法
嘿,朋友们!今天咱就来讲讲单糖绝对构型的确定方法。
这可是个挺有意思的事儿呢!
咱先来说说啥是单糖绝对构型。
就好比每个人都有自己独特的长相和特点一样,单糖也有它特别的“模样”。
那怎么确定这个“模样”呢?这就有门道啦!
有一种方法呢,就像认人似的,通过一些关键的“标志”来判断。
比如说,通过一些化学反应,看看单糖在反应中的表现,就像看一个人在特定情况下的行为一样,从而推断出它的构型。
这就好像你熟悉的朋友,他一抬手一投足,你就知道他要干啥,是不是很神奇?
还有啊,我们可以借助一些专门的仪器,就跟给单糖做个“全身检查”似的。
这些仪器可厉害了,能把单糖的各种细节都给暴露出来,然后我们就能清楚地知道它的绝对构型啦!你说这像不像孙悟空的火眼金睛,一下子就能看穿妖怪的真面目?
再想想啊,如果把单糖比作一个神秘的宝藏,那确定它的绝对构型就是找到打开宝藏大门的钥匙。
我们得仔细琢磨,用心探索,才能找到这把钥匙。
而且哦,确定单糖绝对构型可不是随随便便就能搞定的。
这需要我们有耐心,有细心,就跟侦探破案一样,不放过任何一个小线索。
要是马虎一点,说不定就搞错啦,那可不行!
有时候我就在想,这单糖的世界还真是奇妙无比。
我们就像是一群好奇的孩子,在这个奇妙的世界里努力寻找着答案。
难道不是吗?
总之呢,确定单糖绝对构型是个既有趣又有挑战性的事情。
我们得像探险家一样,勇敢地去探索,去发现。
相信只要我们用心,就一定能揭开单糖绝对构型的神秘面纱!。
糖构型

在实验室做过两次关于这个问题的seminar,总结一下1.天药课本上提到“一般来说”“对于常见的糖”这样的话,不包括多数L型的糖,(常见的鼠李糖是L型)2.如天药课本所言,多数糖的优势构象是C1式,当然这里的多数也指的是常见的糖。
3.绝对构型指的就是最远端手性碳的绝对构型,R对应于D,S对应于L。
相对构型就是成苷后端基碳相对于用来判断绝对构型的那个碳(以下简称为A碳)的构型问题,若定义苷键第二优先,则端基碳的绝对构型与A碳一致,则为β型,不一致,则为α型。
4.糖的相对构型(α或β),对于优势构象中二位羟基处于平伏键的吡喃糖来说,是可以用端基氢的偶合常数来定的,大偶合的为β型,小偶合的为α型;对于其他的糖,氢谱无法解决,如鼠李糖,甘露糖等,这时可以用碳谱来解决,具体数据随糖的种类变化而变化。
5.糖的绝对构型(D或L),需用衍生化液相,衍生化气相,手性色谱法,手性检测器,旋光比较,专一酶解法来确定。
对于苷元迫位碳的绝对构型已知的化合物来说,可以通过苷化位移来定糖的绝对构型,前提是该化合物需符合苷化位移规律。
6.提醒一点,β-D和β-L的糖是一对对映异构体,氢谱碳谱数据完全一致,只有旋光方向相反一般糖苷中葡萄糖绝对构型的确定方法是:先把糖苷在酸性条件下水解,用极性有机溶剂萃取其中的苷元,再将水溶液用1-三甲基硅烷基咪唑进行三甲基硅烷基化后,对烷基化产物进行GC分析,并与标准的D-和L-葡萄糖三甲基硅烷基化产物的保留时间进行比较,确定葡萄糖的绝对构型。
但我在审稿时,遇到如下问题,不知如何解决?对于下面这一类结构,葡萄糖通过醚键与一烷基相连,这一醚键在酸性条件下不易水解。
请问如何确定的葡萄糖绝对构型。
OR21答:我想R2上仍为半缩醛结构,在酸性条件下是可以分解的,不影响所述方法对构型的测定。
如果R1的结构不是很大,其它位的羟基硅醚化后,整体上应当具有好的挥发性,但会影响GC上的保留时间。
有时从糖的1-位H和2-位H的偶合常数J1,2,可推断六碳吡喃糖端基碳的立体结构属α-构型还是β-构型。
糖绝对构型确定方法
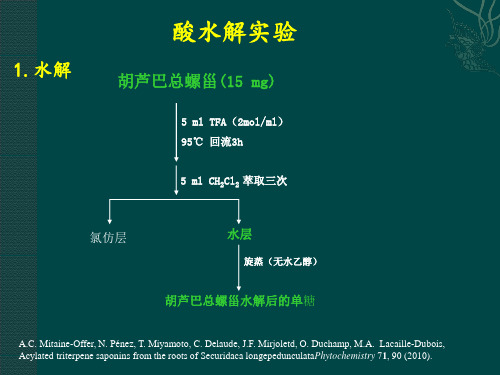
2.薄层检测(硅胶板):
展开剂:氯仿-甲醇-水(8:5:1) 显色剂:0.5%茴香醛-乙醇溶液
HLB D-Xyl L-Rha D-Glc D-Gal BⅡ
3.衍生化
15 mg 胡芦巴总螺甾水解后,除去TFA,加入 12 mg L-半胱氨酸甲酯 盐酸盐,用2ml无水吡啶溶解,密闭,60℃加热1h。再加入 2 ml 三甲基氯 硅烷和 4 ml 六甲基二硅烷,密闭,60℃加热30min。
850000 800000 750000 700000 650000 600000 550000 500000 450000 400000 350000 300000 250000 200000 150000 100000
50000 0
T im e - - >
4 .0 0
T IC : 1 0 0 9 2 7 -4 .D
D-Glc 标品 tR:17.933, 19.673
1 0 .0 0
1 5 .0 0
2 0 .0 0
2 5 .0 0
3 0 .0 0
3 5 .0 0
A bundance
2800000 2600000 2400000 2200000 2000000 1800000 1600000 1400000 1200000 1000000
D-Glc、D-Gal、L-Rha、D-Xyl(各2mg)加入 3 mg L-半胱氨酸甲酯 盐酸盐,用2ml无水吡啶溶解,密闭,60℃加热1h。再加入 0.5 ml 三甲基 氯硅烷和 1 ml 六甲基二硅烷,密闭,60℃加热30min。
S. Hara, H. Okabe, K. Mihashi, Chem. Pharm. Bull. 35, 501 (1987).
糖的构型及其画法

一、单糖的结构表示单糖结构式的三种方法:Fisc her 投影式、Haworth 投影式和优势构象式1、葡萄糖(Fischer 投影式)D ,L 表示相对构型结构式中,位号最大、离羰基最远的手性碳原子的羟基在右侧为D 型;羟基在左侧的为L 型.CHO OH H H HO OH H OHHCH 2OH 5D-葡萄糖CHO OH H H HO OH H HHO2OH5L-葡萄糖2、Fischer 投影式不能表示单糖在水溶液中的真实存在形式,因此有了Haworth 投影式.Hawo rth 投影式中,C4位羟基在面下为D 型,在面上则为L 型 单糖成环后形成了一个新的手性碳原子,形成一对端基差向异构体,有α、β二种构型。
端基碳上的羟基与C 4羟基在同侧称α型,异侧β型O OHHH OH HHOHCH 2OH O HOHHOH HOHCH 2OHβ-D—葡萄糖 α-D —葡萄糖3、虽然Hawo rt h式表示方法较F isc her 式有所改进,但它仍然是一种简化了的方式,尚不能完全表达糖的真实存在状态。
经实验证明葡萄糖在溶液或固体状态时其优势构象是椅式当C 4在面上,C 1在面下,称C1式(通常绝大多数单糖的优势构象是C1式) 当C4在面下,C 1在面上,称1C 式O123451C 式O12345C1式对于β-D型和α-L型葡萄糖,当优势构象为C1式时,C1—OH 在环的面上,处于横键上,1C式时,在竖键OO对于α-D 型和β-L 型葡萄糖,当优势构象为C1式时,C 1—O H 在环的面下,处于竖键上,1C 式时,在横键OO竖键和横键的具体写法:1、横键与环上的键隔键平行;2、横键与竖键在环的面上面下交替排列。
例:(E)-2,3,5,4′-四羟基二苯乙烯—2-O —β-D —葡萄糖苷HOHOOOHOOHOH OHOH单糖的绝对构型如何测定1、GC 法 将单糖与手性试剂反应,(相当于在糖中引入一个新的手性中心)然后通过G C比较与标准单糖D和L 型单糖衍生物的比移值,比移植相同的即为构型相同,反之亦然。
糖的绝对构型和相对构型

糖的绝对构型和相对构型
一、啥是糖的构型
嘿,同学们!咱们今天来聊聊糖的构型。
首先呢,啥是构型?简单说,就是糖分子中各个原子的空间排列方式。
就像咱们排座位一样,不同的排列方式就有不同的构型啦。
二、糖的绝对构型
那啥是糖的绝对构型呢?这可得好好讲讲。
其实啊,绝对构型就是根据分子中手性碳原子的连接方式来确定的。
比如说,在 Fischer 投影式中,羟基在右边的就是 D 型糖,羟基在左边的就是 L 型糖。
这就好比我们分左右两队,站右边的是一队,站左边的是另一队,是不是还挺好记的?
三、糖的相对构型
咱们再说说相对构型。
相对构型呢,是通过与已知构型的糖进行比较来确定的。
比如说,把一种未知构型的糖和已知的 D葡萄糖进行反应,如果反应结果相似,那可能就是和 D葡萄糖有相同的相对构型。
糖的绝对构型和相对构型是我们了解糖分子结构的重要概念,搞清楚它们,对于我们深入学习生物化学和有机化学可是很有帮助的哟!大家加油,好好掌握!。
理学糖和苷学习

本为一平面;吡喃型糖的六元氧环不在同一平 面上,有船式和椅式两种可能的构象
吡喃型糖在溶液或固体状态时其优势构象是 椅式构象(与分子内部的自由能有关)
第5页/共35页
第二节
糖和苷的分类
一、单糖
(一)、五碳醛糖——水中以氧环形式存在(五元、
环糊精——淀粉经淀粉酶水解生成的一种结 晶性低聚糖,环糊精具有良好的水溶性,环状 分子内侧具有疏水性,有包结脂溶性药物的性 能,可增加难溶性药物的溶解度,并对药物的 氧化分解具有一定的保护作用
第19页/共35页
三、多聚糖(多糖) 由10个以上的单糖基通过苷键连接而成的聚糖
植物界普遍存在,具显著生理活性,分子量几千~ 几十万,不亚于DNA水平,但研究透彻的多糖不太 多,作为能量和药用均有
第24页/共35页
根据苷键原子可分 (一)、氧苷(O-苷) 1、醇苷 通过苷元上的醇羟基与糖或糖的衍生物的半缩醛或
半缩酮羟基脱一分子水缩合而成的苷——皂苷、强心
苷、三萜皂苷、萜类苷
OO
O
O
O O β glc
OO OH
O
O
OH
* 红景天 苷
毛茛苷 第25页/共35页
獐牙菜苦苷
2、酚苷 通过苷元上的酚羟基与糖或糖的衍生物的半缩醛或半
第32页/共35页
glc
HO
O
OH O 牡荆 素
OH O
OH
HO
O
OH glc OH O
异牡 荆 素
glc
HO
O
OH
OH
glc OH O
三色堇 素
OH O OH
H
CH2OH
糖的绝对构型

五、糖的化学性质㈠氧化反应糖分子化学反应的活泼性:端基碳原子 > 伯碳 > 仲碳(即C1-OH、C6-OH、C2 C3 C4-OH)㈡糠醛形成反应(Molish反应)样品 + 浓H2SO4+ α-萘酚→紫色环多糖、低聚糖、单糖、苷类——Molish反应酸水解的规律:⑴苷原子不同,酸水解难易顺序:N > O > S > C(C-苷最难水解)⑵呋喃糖苷较吡喃糖苷易水解。
因五元呋喃环的颊性使各取代基处在重叠位置,形成水解中间体可使张力减小,故有利于水解。
⑶酮糖较醛糖易水解酮糖多为呋喃结构,而且酮糖端基碳原子上有-CH2OH大基团取代,水解反应可使张力减小。
⑷吡喃糖苷中:①吡喃环C5上取代基越大越难水解,水解速度为:五碳糖 > 甲基五碳糖 > 六碳糖 > 七碳糖> 糖醛酸②C5上有-COOH取代时,最难水解(因诱导使苷原子电子密度降低)⑸氨基取代的糖较-OH糖难水解,-OH糖又较去氧糖难水解。
2,6-二去氧糖 > 2-去氧糖 > 6-去氧糖> 羟基糖 > 2-氨基糖⑹在构象相同的糖中: a键(竖键)-OH多则易水解。
⑺芳香属苷较脂肪属苷易水解。
如:酚苷 > 萜苷、甾苷(因苷元部分有供电结构,而脂肪属苷元无供电结构)⑻苷元为小基团苷键横键比竖键易水解( e > a )(横键易质子化)苷元为大基团苷键竖键比横键易水解( a > e )(苷的不稳定性促使其易水解)一、糖的1H-NMR(1)1H-NMR判断糖苷键的相对构型在糖的1H-NMR中:端基质子——δ4.3-6.0 ppm左右其它质子——δ3.2-4.2 ppm可通过C1-H与C2-H的偶合常数,来判断苷键的构型(α、β)例如:D-葡萄糖用1H-NMR可判断一些糖的相对构型,但还有一些糖由于其结构上的原因,而无法利用1H-NMR来判断相对构型。
如:甘露糖、鼠李糖二、13C-NMR 在糖链结构测定中的应用端基碳——δ95~105 ppmD-葡萄糖苷 C 1——α-D 和β-L 型 97~101 ppmβ-D 和α-L 型 103~106 ppmCH-OH (C2、C3、C4) 68~85 ppmCH 2-OH (C6) 62 ppm 左右CH 3 < 20 ppm用门控去偶技术,可判断端基碳与端基质子的偶合常数。
糖的构型及其画法
一、单糖的结构表示单糖结构式的三种方法:Fischer 投影式、Haworth 投影式和优势构象式 1、葡萄糖(Fischer 投影式)D ,L 表示相对构型结构式中,位号最大、离羰基最远的手性碳原子的羟基在右侧为D 型;羟基在左侧的为L 型。
CHO OH H H HO OH H OHHCH 2OH 5D-葡萄糖CHO OH H H HO OH H HHOCH 2OH5L-葡萄糖2、Fischer 投影式不能表示单糖在水溶液中的真实存在形式,因此有了Haworth 投影式。
Haworth 投影式中,C4位羟基在面下为D 型,在面上则为L 型 单糖成环后形成了一个新的手性碳原子,形成一对端基差向异构体,有α、β二种构型。
端基碳上的羟基与C4羟基在同侧称α型,异侧β型O OHHH OHOH HHOHCH 2OH O HOHHOHOH HHOHCH 2OHβ-D-葡萄糖 α-D-葡萄糖3、虽然Haworth 式表示方法较Fischer 式有所改进,但它仍然是一种简化了的方式,尚不能完全表达糖的真实存在状态。
经实验证明葡萄糖在溶液或固体状态时其优势构象是椅式当C 4在面上,C 1在面下,称C1式(通常绝大多数单糖的优势构象是C1式) 当C 4在面下,C 1在面上,称1C 式O123451C 式O12345C1式对于β-D型和α-L型葡萄糖,当优势构象为C1式时,C1-OH 在环的面上,处于横键上,1C式时,在竖键O O对于α-D型和β-L型葡萄糖,当优势构象为C1式时,C1-OH 在环的面下,处于竖键上,1C式时,在横键OO竖键和横键的具体写法:1、横键与环上的键隔键平行;2、横键与竖键在环的面上面下交替排列。
例:(E)-2,3,5,4′-四羟基二苯乙烯-2-O-β-D-葡萄糖苷HOHOOOHOOHOHOHOH单糖的绝对构型如何测定1、GC法将单糖与手性试剂反应,(相当于在糖中引入一个新的手性中心)然后通过GC比较与标准单糖D和L型单糖衍生物的比移值,比移植相同的即为构型相同,反之亦然。
构型的判定1六碳醛糖构成的吡喃糖

第一节 单糖的立体化学
单糖的表示方法: 以D-葡萄糖(D-glucose)为例:
CHO
HO
H
H
OH
HO
H
H
OH
H
OH
CH2OH
H
OH
HO
HO
H
OH
H
CH2OH
Fischer投影式
CH2OH
H
O OH
OH H
OH
H
H OH
Haworth式
O
Haworth 简式
O
优势构 象式
第一节 单糖的立体化学
1. 单糖的Fischer、Haworth和构象式 天然界的单糖从三碳糖至八碳糖都有存在。 最简单的醛糖 甘油醛(glyceraldehyde) 最简单的酮糖 二羟基丙酮(1,3-dihydroxyacetone)
一 糖的定义
单糖(monosaccharide):糖的基本单位,又称碳水 化合物(Carbohydrates), 为多羟基的醛
(polyhydroxylaldehyde)或多羟基酮 (polyhydroxyketone). 为重要的一次代谢产物.
具有醛基的单糖称为醛糖(aldose),具有酮基 为酮糖(ketose)。
HHOOH2C
O
OH b-L
OH
HO
L型糖
规律1:D型糖采取C1式更稳定,L型葡萄糖采取1C式。
规律2:b-构型的端基OH总是处于平伏键。
必须记住的十种常见单糖:
OH
OH
OH
HO OH
4
HO HO
6
5O
2
1
3
OH
HO OH HO
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
850000 800000 750000 700000 650000 600000 550000 500000 450000 400000 350000 300000 250000 200000 150000 100000
50000 0
T im e - - >
4 .0 0
T IC : 1 0 0 9 2 7 -4 .D
800000 600000 400000 200000
0 T im e - - >
5 .0 0
T IC : 1 0 0 9 2 7 -3 .D
D-Xyl 标品 tR: 12.988, 14.765
1 0 .0 0
1 5 .0 0
2 0 .0 0
2 5 .0 0
3 0 .0 0
3 5 .0 0
Abundance
D-Glc 标品 tR:17.933, 19.673
1 0 .0 0
1 5 .0 0
2 0 .0 0
2 5 .0 0
3 0 .0 0
3 5 .0 0
A bundance
2800000 2600000 2400000 2200000 2000000 1800000 1600000 1400000 1200000 1000000
350000
300000
250000
200000
150000
100000
50000
T im e -->
0 5 .0 0
次生总螺甾
T IC : 1 0 0 9 2 7 - 6 .D
L-Rha tR :14.519 , 16.260 D-Glc tR:17.932 , 19.673
1 0 .0 0
1 5 .0 0
1.水解
酸水解实验
胡芦巴总螺甾(15 mg)
5 ml TFA(2mol/ml) 95℃ 回流3h 5 ml CH2Cl2 萃取三次
氯仿层
水层
旋蒸(无水乙醇)
胡芦巴总螺甾水解后的单糖
பைடு நூலகம்
A.C. Mitaine-Offer, N. Pénez, T. Miyamoto, C. Delaude, J.F. Mirjoletd, O. Duchamp, M.A. Lacaille-Dubois, Acylated triterpene saponins from the roots of Securidaca longepedunculataPhytochemistry 71, 90 (2010).
4.GC分析条件
安捷伦 6890 气相系统;HP-5毛细管柱 (30 m × 0.25 mm × 0.25 μm);柱 温:180 °C/250 °C,程序升温15 °C/min;载气:N2 (1 mL/min);进 样量:1.0 μL;分流比:1/50。
A bundance
450000
400000
L-Rha 标品 tR: 14.499, 16.266
6 .0 0
8 .0 0
1 0 .0 0
1 2 .0 0
1 4 .0 0
1 6 .0 0
1 8 .0 0
D-Glc、D-Gal、L-Rha、D-Xyl(各2mg)加入 3 mg L-半胱氨酸甲酯 盐酸盐,用2ml无水吡啶溶解,密闭,60℃加热1h。再加入 0.5 ml 三甲基 氯硅烷和 1 ml 六甲基二硅烷,密闭,60℃加热30min。
S. Hara, H. Okabe, K. Mihashi, Chem. Pharm. Bull. 35, 501 (1987).
2 0 .0 0
2 5 .0 0
3 0 .0 0
3 5 .0 0
D-Xyl tR:13.005 , 14.765
A bundance
3500000 3000000 2500000 2000000 1500000 1000000
500000 0 5 .0 0
T im e -->
T IC : 1 0 0 9 2 7 -2 .D
2.薄层检测(硅胶板):
展开剂:氯仿-甲醇-水(8:5:1) 显色剂:0.5%茴香醛-乙醇溶液
HLB D-Xyl L-Rha D-Glc D-Gal BⅡ
3.衍生化
15 mg 胡芦巴总螺甾水解后,除去TFA,加入 12 mg L-半胱氨酸甲酯 盐酸盐,用2ml无水吡啶溶解,密闭,60℃加热1h。再加入 2 ml 三甲基氯 硅烷和 4 ml 六甲基二硅烷,密闭,60℃加热30min。
