乙烯和苯的主要性质和用途课件-高中化学学业水平测试复习
合集下载
2023年人教版新教材安徽省高中化学学业水平考试复习第七单元 有机化合物 课件

2即C:HC3CHH3C2HO2HOH++2CNuaO→――△2→CCHH33CCHH2OO+NHa 2O++HC2u↑。
(2)将C上H3面CH两2O式H合在一并定得条:件下可被O2氧化为乙醛: 2CH3CH2OH+O2――C△u→2CH3CHO+2H2O。
考点梳理
二、乙酸的组成和主要性质 1.乙酸的分子组成与结构:
(1)将 A 通入溴水中,观察到的实验现象是
,A 分子中官能团是
。
(2)写出 CH3CH2OH 与 CH3COOH 反应生成 B 的化学方程式
。
(3)写出乙醇的一种用途 。
真题演练
5、(2016年·安徽)44.(5 分)乙烯、乙醇和乙酸是重要的有机物。回答下列
问题:
(1)将乙烯通入溴的四氯化碳溶液中,观察到的实验现象是
写出苯的燃烧、卤代、硝化、加氢反应方程式。
真题演练
1、(2020年·安徽)28.下列各组物质互为同分异构体的是( )
真题演练
2、(2019年·安徽)27.下列各组物质互为同分异构体的是( )
真题演练
3、(2018年·安徽)28.下列各组物质互为同分异构体的是( ) A.CH3CH=CH2和CH3C≡CH B.CH3CHBrCH2Br和CH2 BrCHBrCH3 C.CH3CH2CHO和 CH3OCH2CH3
考点梳理
2.有机化合物的同分异构现象 化合物具有相同的分子式,但具有不同结构的现象称为同分异构现象,
具有同分异构现象的化合物互称为同分异构体,
例如CH3CH2CH2CH3与
互为同分异构体。
考点梳理
二、甲烷、乙烯和苯的主要性质
1.甲烷:CH4与Cl2发生取 代反应需要光照条件,CH4 分子中的氢原子可被氯原 子逐一替代,依次生成四 种有机物:
(2)将C上H3面CH两2O式H合在一并定得条:件下可被O2氧化为乙醛: 2CH3CH2OH+O2――C△u→2CH3CHO+2H2O。
考点梳理
二、乙酸的组成和主要性质 1.乙酸的分子组成与结构:
(1)将 A 通入溴水中,观察到的实验现象是
,A 分子中官能团是
。
(2)写出 CH3CH2OH 与 CH3COOH 反应生成 B 的化学方程式
。
(3)写出乙醇的一种用途 。
真题演练
5、(2016年·安徽)44.(5 分)乙烯、乙醇和乙酸是重要的有机物。回答下列
问题:
(1)将乙烯通入溴的四氯化碳溶液中,观察到的实验现象是
写出苯的燃烧、卤代、硝化、加氢反应方程式。
真题演练
1、(2020年·安徽)28.下列各组物质互为同分异构体的是( )
真题演练
2、(2019年·安徽)27.下列各组物质互为同分异构体的是( )
真题演练
3、(2018年·安徽)28.下列各组物质互为同分异构体的是( ) A.CH3CH=CH2和CH3C≡CH B.CH3CHBrCH2Br和CH2 BrCHBrCH3 C.CH3CH2CHO和 CH3OCH2CH3
考点梳理
2.有机化合物的同分异构现象 化合物具有相同的分子式,但具有不同结构的现象称为同分异构现象,
具有同分异构现象的化合物互称为同分异构体,
例如CH3CH2CH2CH3与
互为同分异构体。
考点梳理
二、甲烷、乙烯和苯的主要性质
1.甲烷:CH4与Cl2发生取 代反应需要光照条件,CH4 分子中的氢原子可被氯原 子逐一替代,依次生成四 种有机物:
高中化学 第十五讲 烃甲烷、乙烯、苯课件

碳________键、___单_____键或叁键双等,有机化合物有链状分子 栏
和________状分子。
环
目 链
接
3.同分异构体:化合物____分__子__式相同,_____结__构_不(ji同égòu)
的现象称同分异构现象,其化合物________称同分异构体。
互
4.烃:仅含________、________两种元素(yuán sù)的
考点 整合
常温下一氯甲烷呈____气____态,二氯甲烷、三氯
甲烷(氯仿)、四氯甲烷(四氯化碳(sì lǜ huà难tàn))均是
________溶于水的油状液体。其中氯仿毒性较大,是麻
栏 目
醉剂。
链 接
第十五页,共35页。
考点 整合
【例2】 在光照(guāngzhào)条件下,下列物质中能 与甲烷反应的是( )
A.与乙烷互为同分异构体
栏 目
链
B.分子中存在碳碳三键
接
C.能使KMnO4溶液褪色
D.分子中存在碳氧双键
解析 乙烯(yǐ xī)易被氧化。
第二十八页,共35页。
考点 整合
考点(kǎo diǎn)4 苯(C6H6)
知识(zhī shi)回顾
1.分子结构特点:
(C6H6)平面正六边形结构,苯 栏
环上的碳碳键是介于碳碳__单__键__(d_ā_n和j碳iàn碳) __双__键____之间的特
苯与浓硝酸在加热和浓硫酸催化、脱水作用下生成硝基苯或(和)
多硝基苯。如:
栏 目 链 接
苯的硝化反应属于_取___代__(_q_ǔ反d应ài()填“取代”或“加成”)。
硝基苯有毒,与皮肤接触或它的蒸气被人体吸收,都能引起中毒。
人教版高中化学必修二课件第三章笫二节乙烯和苯

乙烯能使溴水褪色,说明乙烯与溴发生了反应 (双键断其一;加在两个不饱和碳上;产物单一) H H H H H +Br-Br H CC H H CC Br Br 1,2-二溴乙烷 CH2=CH2+Br2CH2BrCH2Br
加成反应:有机物分子中的不饱和的 碳原子与其它原子或原子团直接结合 生成新的化合物的反应。
现象 结论
现象
纯溴 催化剂 取代 不褪色
作用
点燃
苯不被酸性 KMnO4溶液 氧化 火焰明亮, 火焰明亮,•
含碳量高
练习
1.可用分液漏斗分离的一组混合物是 A.硝基苯和酒精B.溴苯和溴 CD C.苯和水D.硝基苯和水
•
2.将下列各种液体分别与溴水混合并振荡, 静置后混合液分成两层,下层几乎呈无色 的是 BE
第二节
来自石油和煤的两种基本化工原料
•
乙烯:来源于石油; 苯:来源于石油和煤。
现代工业的血液
•
石油化工发展水平
如何衡量
•
乙烯的用途
•
一、乙烯
(一)乙烯的物理性质
乙烯是一种无色、稍有气味、难溶于水的气体
☆工业上怎样获得乙烯?
石油裂解
•
探究:石蜡油的分解实验
①石蜡油:17个C以上的烷 烃混合物
•
二、苯
1.物理性质: 无色、特殊气味、有毒液体、不溶于 水易溶于有机溶剂,密度:苯小于水,易
挥发。
是重要的有机溶剂,萃取剂
•
苯的危害
室内环境中苯的来源主要是燃烧烟草的烟雾、溶剂、油漆、染色 剂、图文传真机、电脑终端机和打印机、粘合剂、墙纸、地毯、 合成纤维和清洁剂等。 短时间内吸入高浓度苯蒸汽可发生急性苯中毒,出现兴奋或酒醉 感,伴有黏膜刺激症状。轻则头晕、头痛、恶心、呕吐、步态不 稳;重则昏迷、抽搐及循环衰竭直至死亡;短期内吸入较高浓度 苯后可发生亚急性苯中毒,出现头昏、头痛、乏力、失眠、月经 紊乱等症状,并可发生再生障碍性贫血、急性白血病,表现为迅 速发展的贫血、出血、感染等。长期接触苯会对血液造成极大伤 害,引起慢性中毒。苯可以损害骨髓,使红血球、白细胞、血小 板数量减少,并使染色体畸变,从而导致白血病,甚至出现再生 障碍性贫血。苯可以导致大量出血,从而抑制免疫系统的功用, 使疾病有机可乘。有研究报告指出,苯在体内的潜伏期可长达1215年。 苯中毒对身体的危害归结为3种:致癌、致残、致畸胎。
加成反应:有机物分子中的不饱和的 碳原子与其它原子或原子团直接结合 生成新的化合物的反应。
现象 结论
现象
纯溴 催化剂 取代 不褪色
作用
点燃
苯不被酸性 KMnO4溶液 氧化 火焰明亮, 火焰明亮,•
含碳量高
练习
1.可用分液漏斗分离的一组混合物是 A.硝基苯和酒精B.溴苯和溴 CD C.苯和水D.硝基苯和水
•
2.将下列各种液体分别与溴水混合并振荡, 静置后混合液分成两层,下层几乎呈无色 的是 BE
第二节
来自石油和煤的两种基本化工原料
•
乙烯:来源于石油; 苯:来源于石油和煤。
现代工业的血液
•
石油化工发展水平
如何衡量
•
乙烯的用途
•
一、乙烯
(一)乙烯的物理性质
乙烯是一种无色、稍有气味、难溶于水的气体
☆工业上怎样获得乙烯?
石油裂解
•
探究:石蜡油的分解实验
①石蜡油:17个C以上的烷 烃混合物
•
二、苯
1.物理性质: 无色、特殊气味、有毒液体、不溶于 水易溶于有机溶剂,密度:苯小于水,易
挥发。
是重要的有机溶剂,萃取剂
•
苯的危害
室内环境中苯的来源主要是燃烧烟草的烟雾、溶剂、油漆、染色 剂、图文传真机、电脑终端机和打印机、粘合剂、墙纸、地毯、 合成纤维和清洁剂等。 短时间内吸入高浓度苯蒸汽可发生急性苯中毒,出现兴奋或酒醉 感,伴有黏膜刺激症状。轻则头晕、头痛、恶心、呕吐、步态不 稳;重则昏迷、抽搐及循环衰竭直至死亡;短期内吸入较高浓度 苯后可发生亚急性苯中毒,出现头昏、头痛、乏力、失眠、月经 紊乱等症状,并可发生再生障碍性贫血、急性白血病,表现为迅 速发展的贫血、出血、感染等。长期接触苯会对血液造成极大伤 害,引起慢性中毒。苯可以损害骨髓,使红血球、白细胞、血小 板数量减少,并使染色体畸变,从而导致白血病,甚至出现再生 障碍性贫血。苯可以导致大量出血,从而抑制免疫系统的功用, 使疾病有机可乘。有研究报告指出,苯在体内的潜伏期可长达1215年。 苯中毒对身体的危害归结为3种:致癌、致残、致畸胎。
高中化学课件必修二《第三章 第三节 乙烯和苯》(2)
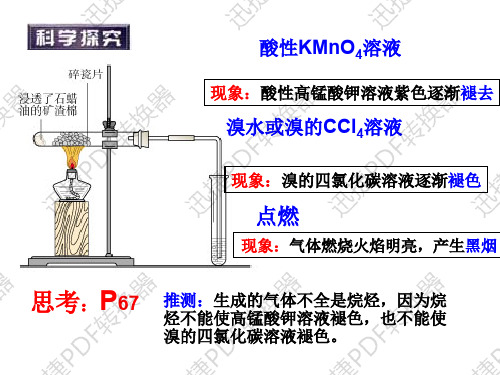
酸性KMnO4溶液
现象:酸性高锰酸钾溶液紫色逐渐褪去
溴水或溴的CCl4溶液
学科网
现象:溴的四氯化碳溶液逐渐褪色
点燃
现象:气体燃烧火焰明亮,产生黑烟
P 思考: 67 推测:生成的气体不全是烷烃,因为烷 烃不能使高锰酸钾溶液褪色,也不能使 溴的四氯化碳溶液褪色。
结论: 石蜡油分解的产物中有烯烃
什么叫烯烃?
H2C=CH2
5
含有碳碳双键的不饱和烃 C C
单烯烃 只有一个碳碳双键的烃(最简单的单烯烃是 乙烯 C2H4)
思考:多一个双键比同碳原子数的烷烃会少几个氢? 单烯烃通式为CnH2n(n≥2整数)
乙烯被称为“石化工业之母”,乙烯的
小 产量可以用来衡量一个国家的石油化工发展 资 水平。
料
最 简 单 的 烯 烃乙 烯源自:一、乙烯的物理性质
乙烯是 无 色 稍有 气味的气体; 在水中 难 (“易”或“难”)溶
学科网
于水;密度较空气略小 。
4
二、乙烯的结构 分子式:C2H4
H.. H.. 电子式: H:C::C:H
实验式(最简式):CH2
HH 结构式: H C C H
结构简式:
正:CH2=CH2
CH2CH2
空间构型:
现象:酸性高锰酸钾溶液紫色逐渐褪去
溴水或溴的CCl4溶液
学科网
现象:溴的四氯化碳溶液逐渐褪色
点燃
现象:气体燃烧火焰明亮,产生黑烟
P 思考: 67 推测:生成的气体不全是烷烃,因为烷 烃不能使高锰酸钾溶液褪色,也不能使 溴的四氯化碳溶液褪色。
结论: 石蜡油分解的产物中有烯烃
什么叫烯烃?
H2C=CH2
5
含有碳碳双键的不饱和烃 C C
单烯烃 只有一个碳碳双键的烃(最简单的单烯烃是 乙烯 C2H4)
思考:多一个双键比同碳原子数的烷烃会少几个氢? 单烯烃通式为CnH2n(n≥2整数)
乙烯被称为“石化工业之母”,乙烯的
小 产量可以用来衡量一个国家的石油化工发展 资 水平。
料
最 简 单 的 烯 烃乙 烯源自:一、乙烯的物理性质
乙烯是 无 色 稍有 气味的气体; 在水中 难 (“易”或“难”)溶
学科网
于水;密度较空气略小 。
4
二、乙烯的结构 分子式:C2H4
H.. H.. 电子式: H:C::C:H
实验式(最简式):CH2
HH 结构式: H C C H
结构简式:
正:CH2=CH2
CH2CH2
空间构型:
乙烯和苯ppt课件

CH2Cl-CH2OH 17
1、实验室制取氯乙烷, 是采取CH3-CH3与Cl2取代反应好, 还
是采用CH2=CH2与HCl加成反应好? 加成好,产物单一
2、CH4中混有C2H4, 欲除去C2H4得到CH4, 最好依次通过哪一
组试剂 ( C )
A. 澄清石灰水、浓硫酸 C. Br2水、浓硫酸
B. KMnO4酸性溶液、浓硫酸 D. 浓硫酸、KMnO4酸性溶液
精选ppt
42
苯分子的结构
分子式:C6H6 结构式:
结பைடு நூலகம்简式:
或
精选ppt
43
球棍模型
比例模型
结构特点:
1.具有平面正六边形结构,所有原子(十二原子)均在同
①SO2、C2H4使溴水褪色的化学方程式 。
②如何检验C2H4中混入SO2?如何除去?检验SO2除尽的 方法是什么?
Ⅰ
Ⅱ Ⅲ 精选ppt
Ⅳ
32
科学史话:苯的发现
十九世纪,欧洲许多国
家都使用煤气照明。煤气通
常是压缩在桶里贮运的,人
们发现这种桶里总有一种油
状液体,但长时间无人问津。
1825年英国科学家法拉第对
一、乙烯的分子组成和结构
1、分子式 C2H4 2、电子式
3、结构式
4、结构简式 CH2=CH2
5、键角
120°
CH2CH2
6、空间构型 平面四边形
精选ppt
8
乙烷和乙烯结构比较
分子式 键类别
C2H6 碳碳单键
C2H4 碳碳双键
键角 键能kJ/mol
原子空间相对位置
109 °28 ´
384
2个碳原子和6 个氢 不在同一平面内
乙烯和苯-课件

•
16、业余生活要有意义,不要越轨。2021/2/272021/2/27Februar y 27,顶峰,也仍要 自强不 息。2021/2/272021/2/272021/2/272021/2/27
谢谢观赏
You made my day!
我们,还在路上……
第 17 讲 乙烯和苯
1.了解乙烯和苯分子中碳原子间的成键特征。 2.了解乙烯、苯等有机化合物的主要性质,了解加成反应。 3.了解石油、煤和天然气的主要组成。 4.了解石油的分馏和煤的干馏。
乙烯的组成、结构、主要性质及加成反应 1.乙烯 (1)组成与结构。
结构式:
,六个原子__共__平面,键角为
焦炉 煤气
焦炉气
氢气、甲烷、乙烯、一 氧化碳
气体燃料、化工原料
粗氨水 粗苯
氨、铵盐 苯、甲苯、二甲苯
化肥、炸药、染料、医 药、农药、合成材料
苯、甲苯、二甲苯
煤焦油
酚类、萘
染料、医药、农药、合 成材料
沥青
筑路材料、制碳素电极
焦炭
碳
冶金、电石、燃料
(3)煤的气化。 煤的气化是将煤转化为可燃性气体的过程,主要反应为:
C(s)+H2O(g) CO(g)+H2(g)。 (4)煤的液化。 直接液化,使煤与氢气作用生成液体燃料;间接液化,使
煤先转化为 CO 和 H2,再催化合成甲醇等。
典例剖析
【例 3·单选Ⅰ】(2014 年广东学业水平·模拟)石油和煤都是 重要的化石能源,下列有关石油和煤的叙述正确的是( )。
A.都是混合物 B.都含有大量氧元素
(2)石油的炼制。
石油炼制 方法
分馏 常压
减压
催化裂化
在催化剂存在的
高考化学一轮复习 第九单元 有机化合物 9.1 甲烷、乙烯、苯课件

(1)烷烃一般只能发生取代反应,含有苯环的物质既能发生加成反
应也能发生取代反应;含有—COOH、—OH、—COOR等官能团的
物质均能发生取代反应。
(2)加成反应:反应物中一般含有碳碳双键、碳碳三键、苯环等。
(3)氧化反应:主要包括烯烃、醇被酸性高锰酸钾溶液氧化,葡萄
糖被新制氢氧化铜或银氨溶液氧化,醇的催化氧化等。注意大多数
(2)加成反应包括由烯烃反应生成烷烃、醇或氯代烃,由苯反应生
成环烷烃等。
12/11/2021
-15-
考点一
考点二
考点三
基础梳理
考点突破
例1聚苯乙烯塑料在生产、生活中有广泛应用,其单体苯乙烯可
由乙苯与二氧化碳在一定条件下发生如下反应制取:
+CO2
+CO+H2O
下列有关苯乙烯的说法正确的是( )
关闭
A.分子中含有5个碳碳双键
有机物能在氧气中燃烧,发生氧化反应。
12/11/2021
-13-
考点一
考点二
考点三
基础梳理
考点突破
4.依据反应条件判断
(1)当反应条件为稀酸并加热时,通常为酯或糖类的水解,属于取
代反应。
(2)当反应条件为光照且与卤素单质(氯气或溴蒸气)反应时,通常
为烷烃或苯环侧链烷基上的氢原子发生取代反应。
(3)当反应条件是在FeX3(X为卤素)的催化作用下与X2反应常为
考点二
考点三
基础梳理
考点突破
同分异构体的书写及判断
一、烷烃同分异构体的书写
1.原则
(1)“成直链、一线串”;(2)“从头摘、挂中间”;(3)“往边排、不到
端”,摘两碳,成乙基,二甲基,不重复,要写全。
应也能发生取代反应;含有—COOH、—OH、—COOR等官能团的
物质均能发生取代反应。
(2)加成反应:反应物中一般含有碳碳双键、碳碳三键、苯环等。
(3)氧化反应:主要包括烯烃、醇被酸性高锰酸钾溶液氧化,葡萄
糖被新制氢氧化铜或银氨溶液氧化,醇的催化氧化等。注意大多数
(2)加成反应包括由烯烃反应生成烷烃、醇或氯代烃,由苯反应生
成环烷烃等。
12/11/2021
-15-
考点一
考点二
考点三
基础梳理
考点突破
例1聚苯乙烯塑料在生产、生活中有广泛应用,其单体苯乙烯可
由乙苯与二氧化碳在一定条件下发生如下反应制取:
+CO2
+CO+H2O
下列有关苯乙烯的说法正确的是( )
关闭
A.分子中含有5个碳碳双键
有机物能在氧气中燃烧,发生氧化反应。
12/11/2021
-13-
考点一
考点二
考点三
基础梳理
考点突破
4.依据反应条件判断
(1)当反应条件为稀酸并加热时,通常为酯或糖类的水解,属于取
代反应。
(2)当反应条件为光照且与卤素单质(氯气或溴蒸气)反应时,通常
为烷烃或苯环侧链烷基上的氢原子发生取代反应。
(3)当反应条件是在FeX3(X为卤素)的催化作用下与X2反应常为
考点二
考点三
基础梳理
考点突破
同分异构体的书写及判断
一、烷烃同分异构体的书写
1.原则
(1)“成直链、一线串”;(2)“从头摘、挂中间”;(3)“往边排、不到
端”,摘两碳,成乙基,二甲基,不重复,要写全。
2018-2019年化学高中学业水平测试课件:第七章专题十四考点2乙烯和苯的主要性质和用途

第七章
有机化合物
专题十四 考点
烃——甲烷、乙烯、苯
乙烯和苯的主要性质和用途
一、乙烯的性质和用途 1.乙烯的物理性质:乙烯是无色气体;难溶于水; 密度较空气小。
2. 乙烯的结构: 分子式 C2H4, 结构式_____________, 结构简式 CH2===CH2,空间构型平面形。 3.乙烯的化学性质。 (1)乙烯的氧化反应。 点燃 ①可燃性:C2H4+2O2――→CO2+2H2O。 现象:火焰明亮,伴有黑烟。
3.苯的化学性质。 (1)可燃性。 点燃 化学方程式:2C6H6+15O2――→12CO2+6H2O。 现象:明亮火焰,有浓烟。
(2)取代反应。 与液溴的反应: FeBr3 +Br—Br――→ _______________________。 与硝酸的反应: 浓硫酸 +HO—NO2 ――→ __________________。 50~60℃ 加成反应: 催化剂 +3H2 ――→ _________________________。 △
(3)乙烯的加聚反应。 写出乙烯加聚反应化学方程式:
_____________________________________。 4.乙烯用途:制造聚乙烯,聚乙烯可用来制塑料。 乙烯是植物生长调节剂,水果催熟剂。
二、苯的性质和用途 1.苯的结构。 苯的分子式 C6H6, 结构简式 ________或 ________, 空间构型平面正六边形。 2.苯的物理性质。 苯在通常情况下, 是无色带有特殊气味的液体, 有毒, 不溶于水,密度比水小,熔、沸点低,易挥发。
B.有沉淀物生成 D.产物含有双键
解析: 乙烯通入溴的 CCl4 溶液中发生加成反应:
CH2===CH2+Br2―→ 2二溴乙烷。 答案:A
有机化合物
专题十四 考点
烃——甲烷、乙烯、苯
乙烯和苯的主要性质和用途
一、乙烯的性质和用途 1.乙烯的物理性质:乙烯是无色气体;难溶于水; 密度较空气小。
2. 乙烯的结构: 分子式 C2H4, 结构式_____________, 结构简式 CH2===CH2,空间构型平面形。 3.乙烯的化学性质。 (1)乙烯的氧化反应。 点燃 ①可燃性:C2H4+2O2――→CO2+2H2O。 现象:火焰明亮,伴有黑烟。
3.苯的化学性质。 (1)可燃性。 点燃 化学方程式:2C6H6+15O2――→12CO2+6H2O。 现象:明亮火焰,有浓烟。
(2)取代反应。 与液溴的反应: FeBr3 +Br—Br――→ _______________________。 与硝酸的反应: 浓硫酸 +HO—NO2 ――→ __________________。 50~60℃ 加成反应: 催化剂 +3H2 ――→ _________________________。 △
(3)乙烯的加聚反应。 写出乙烯加聚反应化学方程式:
_____________________________________。 4.乙烯用途:制造聚乙烯,聚乙烯可用来制塑料。 乙烯是植物生长调节剂,水果催熟剂。
二、苯的性质和用途 1.苯的结构。 苯的分子式 C6H6, 结构简式 ________或 ________, 空间构型平面正六边形。 2.苯的物理性质。 苯在通常情况下, 是无色带有特殊气味的液体, 有毒, 不溶于水,密度比水小,熔、沸点低,易挥发。
B.有沉淀物生成 D.产物含有双键
解析: 乙烯通入溴的 CCl4 溶液中发生加成反应:
CH2===CH2+Br2―→ 2二溴乙烷。 答案:A
高考化学一轮复习 专题 有机物 第1讲 甲烷、乙烯和苯课件

(1)组成和结构 分子式 电子式 CH4 ③ (2)物理性质 颜色 状态 ⑥ 气体
结构式 ④ 溶解性 ⑦
空间构型 ⑤ 密度
溶于水 比空气⑧
(3)化学性质 a.稳定性:与强酸、强碱和强氧化剂等一般不发生化学反应。 b.燃烧反应:⑨ c.取代反应:在光照条件下与 Cl2 反应:⑩ 次又生成了 。 。 ,依
答案 褪色原理不相同,前者是发生了加成反应,后者是被 酸性高锰酸钾溶液氧化。由于 CH4 与酸性 KMnO4 溶液不发生反应, 而 能使酸性 KMnO4 溶液褪色,因此可以用酸性 KMnO4 溶液鉴别 二者。 酸性 KMnO4 溶液会将 氧化成 CO2 而引入新杂质气体,因 此不能用酸性 KMnO4 溶液除去 CH4 中的 。
溶于水 比水小 低
Ⅰ.稳定性
不能与酸性 KMnO4 溶液反应,也不与溴水(或溴的四氯化碳溶 液)反应。 Ⅱ.取代反应 a.卤代反应:苯与液溴发生溴代反应的化学方程式为 ; b.硝化反应:化学方程式为 Ⅲ.加成反应 苯和 H2 发生加成反应的化学方程式为 Ⅳ.燃烧反应: 现象:火焰明亮并伴有浓烟。 四、煤、石油、天然气的综合利用 。 。 。
3.天然气的综合利用 (1)天然气是一种清洁的化石燃料,更是一种重要的化工原 料,它的主要成分是 。
(2)天然气与水蒸气反应制取 H2 的化学方程式为 。
1.煤的干馏,煤的气化,煤的液化,石油的裂化、裂解都属于 化学变化,石油的分馏属于物理变化。 2.裂化汽油中含有不饱和烃,能使溴水褪色,故不能用作卤 素单质的萃取剂。
1.重要的有机反应类型 (1)取代反应——甲烷的氯代反应、苯的溴代反应、苯的硝 化反应等。 (2)加成反应——乙烯与溴的反应、苯与氢气生成环己烷的 反应等。 (3)氧化反应——有机物的燃烧、乙烯使酸性高锰酸钾溶液 褪色等。 2.重要反应及其条件(回顾相应化学方程式的书写) (1)甲烷与氯气在光照条件下反应。 (2)乙烯与溴水或溴的四氯化碳溶液反应。
2020—2021年化学高中广东学业水平测试专题习题课件-第七章专题十四考点2乙烯和苯的主要性质和用途PPT28张

2020—2021年化学高中 广东学业水平测试专题 习题课件-第七章专题十 四考点2乙烯和苯的主要 性质和用途PPT28张
物质 结构特点
与Br2 反应
Br2试剂 反应条件
反应类型
甲烷
正四面体
纯溴 光照 取代
乙烯 所有原 子共面 溴水
无
加成
苯 平面正六边
形 纯溴
FeBr3 取代
氧化反 应
酸性 KMnO4(aq)
不能褪色
燃烧
火Hale Waihona Puke 呈淡蓝 色鉴别不能使溴水
和酸性
KMnO4溶 液褪色
溶液褪色
火焰明亮 ,带黑烟
能使溴水 和酸性 KMnO4 溶液褪色
不能褪色
火焰明亮, 带浓烟 将溴水加入 苯中振荡分 层,上层呈 橙红色,下 层为无色
物质 结构特点
与Br2 反应
Br2试剂 反应条件
反应类型
甲烷
正四面体
纯溴 光照 取代
乙烯 所有原 子共面 溴水
无
加成
苯 平面正六边
形 纯溴
FeBr3 取代
氧化反 应
酸性 KMnO4(aq)
不能褪色
燃烧
火Hale Waihona Puke 呈淡蓝 色鉴别不能使溴水
和酸性
KMnO4溶 液褪色
溶液褪色
火焰明亮 ,带黑烟
能使溴水 和酸性 KMnO4 溶液褪色
不能褪色
火焰明亮, 带浓烟 将溴水加入 苯中振荡分 层,上层呈 橙红色,下 层为无色
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
A.在常温常压下为液体 B.能使酸性KMnO4溶液褪色 C.可自身加成形成聚乙烯 D.能使溴的CCl4溶液褪色 解析:本题考查了乙烯的性质。乙烯通常情况下是 稍有气味的无色气体,它属于不饱和烃,分子中含有碳
碳双键,能够与溴水或溴的四氯化碳溶液发生加成反应 使溶液褪色,也能和酸性高锰酸钾溶液发生氧化反应使 溶液褪色,还能发生加聚反应制取塑料。
答案:A
苯是一种重要的有机化工原料,广泛用于合成
橡胶、塑料和医药等方面。下列关于苯的叙述不正确的
是( )
A.分子式为C6H6 C.能在空气中燃烧
B.属于不饱和烃 D.无色无毒的液体
解析:苯的分子式为C6H6,属于芳香烃,有毒,在 空气中燃烧会冒出大量浓烟。
答案:D
甲烷、乙烯与苯的结构和性质的比较
C.四氯化碳的电子式: D.臭氧的分子式:O3 解析:乙烯的最简式应该是CH2;乙醇的结构简式 应该是CH3CH2OH或C2H5OH;四氯化碳的电子式应该 是。 答案:D
非选择题 5.现有5种有机物:①乙烯 ,②乙醇,③乙醛,④ 乙酸,⑤乙酸乙酯。 (1)请分别写出其中含有下列官能团的有机物的结构 简式: —OH_____________,—CHO________________, —COOH______________。 (2)在上述5种有机物中(填写序号):
A.聚乙烯结构中存在碳碳双键 B.聚乙烯可由乙烯通过取代反应制得 C.聚乙烯与聚氯乙烯都是合成高分子材料 D.聚氯乙烯可由氯气与聚乙烯通过加聚反应制得 解析:本题考查了高分子化合物的知识。乙烯的加 聚产物中已经没有了碳碳双键。 答案:C
4.有关化学用语正确的是( ) A.乙烯的最简式:C2H4 B.乙醇的结构简式:C2H6O
(3)乙烯的加聚反应。 写出乙烯加聚反应化学方程式:______________。 4.乙烯用途:制造聚乙烯,聚乙烯可用来制____。 乙烯是植物生长调节剂,水果________。 二、苯的性质和用途 1.苯的结构。 苯的分子式______,结构简式________或 ______, 空间构型________。
物质 结构特点
甲烷 正四面体
乙烯
所有原 子共面
与Br2 反应
Br2试剂
反应条件 反应ห้องสมุดไป่ตู้型
纯溴
光照 取代
溴水
无 加成
苯 平面正 六边形
纯溴
FeBr3 取代
氧化 反应
酸性 KMnO4
(aq) 燃烧
鉴别
不能褪色 溶液褪色 不能褪色
火焰呈 淡蓝色
不能使溴 水和酸性 KMnO4 溶液褪色
火焰明亮, 火焰明亮,
单项选择题
1.(2019·广州学考模拟)通常用于衡量一个国家石油
化工发展水平的标志是( )
A.石油的产量
B.乙烯的产量
C.天然气的产量 D.汽油的产量
答案:B
2.下列物质含碳量最高的是( )
A.甲烷
B.乙烷
C.乙烯
D.苯
答案:D
3.高分子材料的合成与应用使我们的生活变得更加 丰富多彩。下列关于高分子材料的说法正确的是( )
带黑烟
带浓烟
将溴水加入 能使溴水和 苯中振荡分 酸性KMnO4 层,上层呈 溶液褪色 橙红色,下
层为无色
1.乙烯使溴水和酸性高锰酸钾溶液褪色的原理是 一样的。(×)
[分析] 乙烯与溴水发生加成反应,而使酸性高锰 酸钾溶液褪色发生的是氧化反应。
2.烯烃都能发生加成反应,烷烃也能。(×) [分析] 烯烃分子中均含有碳碳双键,可以发生加 成反应,而烷烃不可以。
2.苯的物理性质。 苯在通常情况下,是__________色带有________气 味的________体,有毒,________溶于水,密度比水 ________,熔、沸点________,易挥发。 3.苯的化学性质。 (1)可燃性。
点燃 化学方程式:2C6H6+15O2――→12CO2+6H2O。 现象:____________________________________。
3.苯分子中含有3个碳碳双键。(×) [分析] 苯分子中碳原子之间是介于单键和双键之间 的特殊的化学键,故不存在碳碳单键,也不存在碳碳双 键。 4.苯与溴水混合振荡后静置,溴水褪色说明苯分子 中含有碳碳双键。(×) [分析] 苯与溴水混合振荡后静置,溴水褪色,是苯 萃取出溴水中的溴单质而使溴水褪色,属于物理变化。
能发生银镜反应的是__________。 能发生消去反应的是__________。 能发生水解反应的是__________。 具有酸性且能发生酯化反应的是__________。 既能发生加成反应,又能发生聚合反应的是_____。
答案:(1)CH3CH2OH或C2H5OH CH3CHO CH3COOH (2)③ ② ⑤ ④ ①
现象:____________________________________。 ②乙烯可使酸性高锰酸钾溶液褪色。 乙烯易被强氧化剂如KMnO4_____,产物是CO2。 现象:溶液紫色褪去。利用此性质可以区别乙烯和 甲烷。 (2)乙烯的加成反应。 CH2===CH2+Br-Br―→__________________。 现象:使溴水褪色。 加成反应:有机物分子中____________________的 碳原子与__________________相结合的反应。
1.(2019年6月·广东学考·单选Ⅰ)将乙烯通入溴的
CCl4溶液中。下列说法准确的是( )
A.溶液褪色
B.有沉淀物生成
C.生成物属于烃 D.产物含有双键
解析:乙烯与溴发生了加成反应而生成无色物质。
答案:A
2.(2015年6月·广东学考·单选Ⅱ)检验乙烷中是否混 有少量乙烯的正确方法为( )
A.将气体点燃 B.将气体通入浓硫酸中 C.将气体通入水中 D.将气体通入溴的CCl4溶液中 解析:两者都能燃烧,A错;两者都不能与浓硫酸 反应,B错;两者都不溶解于水,C错;将气体通入溴的 CCl4溶液中,乙烯与溴发生加成反应使溶液褪色,而乙 烷不与溴的CCl4溶液反应,D正确。 答案:D
专题十四 烃——甲烷、乙烯、苯
考点2 乙烯和苯的主要性质和用途
一、乙烯的性质和用途 1.乙烯的物理性质:乙烯是________色气体; ________溶于水;密度较空气________。 2.乙烯的结构:分子式________,结构式 ________,结构简式________,空间构型________。 3.乙烯的化学性质。 (1)乙烯的氧化反应。 ①可燃性:C2H4+2O2―点―燃→CO2+2H2O。
(2)取代反应。 与液溴的反应:
+Br—Br―Fe―B→r3 _______________________。 与硝酸的反应:
浓硫酸 +HO—NO250―~―6→0℃_________________。 加成反应:
催化剂
+3H2
――→ △
_________________________。
乙烯可通过石油裂解获得。下列有关乙烯性质 的说法错误的是( )
碳双键,能够与溴水或溴的四氯化碳溶液发生加成反应 使溶液褪色,也能和酸性高锰酸钾溶液发生氧化反应使 溶液褪色,还能发生加聚反应制取塑料。
答案:A
苯是一种重要的有机化工原料,广泛用于合成
橡胶、塑料和医药等方面。下列关于苯的叙述不正确的
是( )
A.分子式为C6H6 C.能在空气中燃烧
B.属于不饱和烃 D.无色无毒的液体
解析:苯的分子式为C6H6,属于芳香烃,有毒,在 空气中燃烧会冒出大量浓烟。
答案:D
甲烷、乙烯与苯的结构和性质的比较
C.四氯化碳的电子式: D.臭氧的分子式:O3 解析:乙烯的最简式应该是CH2;乙醇的结构简式 应该是CH3CH2OH或C2H5OH;四氯化碳的电子式应该 是。 答案:D
非选择题 5.现有5种有机物:①乙烯 ,②乙醇,③乙醛,④ 乙酸,⑤乙酸乙酯。 (1)请分别写出其中含有下列官能团的有机物的结构 简式: —OH_____________,—CHO________________, —COOH______________。 (2)在上述5种有机物中(填写序号):
A.聚乙烯结构中存在碳碳双键 B.聚乙烯可由乙烯通过取代反应制得 C.聚乙烯与聚氯乙烯都是合成高分子材料 D.聚氯乙烯可由氯气与聚乙烯通过加聚反应制得 解析:本题考查了高分子化合物的知识。乙烯的加 聚产物中已经没有了碳碳双键。 答案:C
4.有关化学用语正确的是( ) A.乙烯的最简式:C2H4 B.乙醇的结构简式:C2H6O
(3)乙烯的加聚反应。 写出乙烯加聚反应化学方程式:______________。 4.乙烯用途:制造聚乙烯,聚乙烯可用来制____。 乙烯是植物生长调节剂,水果________。 二、苯的性质和用途 1.苯的结构。 苯的分子式______,结构简式________或 ______, 空间构型________。
物质 结构特点
甲烷 正四面体
乙烯
所有原 子共面
与Br2 反应
Br2试剂
反应条件 反应ห้องสมุดไป่ตู้型
纯溴
光照 取代
溴水
无 加成
苯 平面正 六边形
纯溴
FeBr3 取代
氧化 反应
酸性 KMnO4
(aq) 燃烧
鉴别
不能褪色 溶液褪色 不能褪色
火焰呈 淡蓝色
不能使溴 水和酸性 KMnO4 溶液褪色
火焰明亮, 火焰明亮,
单项选择题
1.(2019·广州学考模拟)通常用于衡量一个国家石油
化工发展水平的标志是( )
A.石油的产量
B.乙烯的产量
C.天然气的产量 D.汽油的产量
答案:B
2.下列物质含碳量最高的是( )
A.甲烷
B.乙烷
C.乙烯
D.苯
答案:D
3.高分子材料的合成与应用使我们的生活变得更加 丰富多彩。下列关于高分子材料的说法正确的是( )
带黑烟
带浓烟
将溴水加入 能使溴水和 苯中振荡分 酸性KMnO4 层,上层呈 溶液褪色 橙红色,下
层为无色
1.乙烯使溴水和酸性高锰酸钾溶液褪色的原理是 一样的。(×)
[分析] 乙烯与溴水发生加成反应,而使酸性高锰 酸钾溶液褪色发生的是氧化反应。
2.烯烃都能发生加成反应,烷烃也能。(×) [分析] 烯烃分子中均含有碳碳双键,可以发生加 成反应,而烷烃不可以。
2.苯的物理性质。 苯在通常情况下,是__________色带有________气 味的________体,有毒,________溶于水,密度比水 ________,熔、沸点________,易挥发。 3.苯的化学性质。 (1)可燃性。
点燃 化学方程式:2C6H6+15O2――→12CO2+6H2O。 现象:____________________________________。
3.苯分子中含有3个碳碳双键。(×) [分析] 苯分子中碳原子之间是介于单键和双键之间 的特殊的化学键,故不存在碳碳单键,也不存在碳碳双 键。 4.苯与溴水混合振荡后静置,溴水褪色说明苯分子 中含有碳碳双键。(×) [分析] 苯与溴水混合振荡后静置,溴水褪色,是苯 萃取出溴水中的溴单质而使溴水褪色,属于物理变化。
能发生银镜反应的是__________。 能发生消去反应的是__________。 能发生水解反应的是__________。 具有酸性且能发生酯化反应的是__________。 既能发生加成反应,又能发生聚合反应的是_____。
答案:(1)CH3CH2OH或C2H5OH CH3CHO CH3COOH (2)③ ② ⑤ ④ ①
现象:____________________________________。 ②乙烯可使酸性高锰酸钾溶液褪色。 乙烯易被强氧化剂如KMnO4_____,产物是CO2。 现象:溶液紫色褪去。利用此性质可以区别乙烯和 甲烷。 (2)乙烯的加成反应。 CH2===CH2+Br-Br―→__________________。 现象:使溴水褪色。 加成反应:有机物分子中____________________的 碳原子与__________________相结合的反应。
1.(2019年6月·广东学考·单选Ⅰ)将乙烯通入溴的
CCl4溶液中。下列说法准确的是( )
A.溶液褪色
B.有沉淀物生成
C.生成物属于烃 D.产物含有双键
解析:乙烯与溴发生了加成反应而生成无色物质。
答案:A
2.(2015年6月·广东学考·单选Ⅱ)检验乙烷中是否混 有少量乙烯的正确方法为( )
A.将气体点燃 B.将气体通入浓硫酸中 C.将气体通入水中 D.将气体通入溴的CCl4溶液中 解析:两者都能燃烧,A错;两者都不能与浓硫酸 反应,B错;两者都不溶解于水,C错;将气体通入溴的 CCl4溶液中,乙烯与溴发生加成反应使溶液褪色,而乙 烷不与溴的CCl4溶液反应,D正确。 答案:D
专题十四 烃——甲烷、乙烯、苯
考点2 乙烯和苯的主要性质和用途
一、乙烯的性质和用途 1.乙烯的物理性质:乙烯是________色气体; ________溶于水;密度较空气________。 2.乙烯的结构:分子式________,结构式 ________,结构简式________,空间构型________。 3.乙烯的化学性质。 (1)乙烯的氧化反应。 ①可燃性:C2H4+2O2―点―燃→CO2+2H2O。
(2)取代反应。 与液溴的反应:
+Br—Br―Fe―B→r3 _______________________。 与硝酸的反应:
浓硫酸 +HO—NO250―~―6→0℃_________________。 加成反应:
催化剂
+3H2
――→ △
_________________________。
乙烯可通过石油裂解获得。下列有关乙烯性质 的说法错误的是( )
