内毒素及其去除
除内毒素的方法

除内毒素的方法内毒素是一种对人体健康有害的毒素,它广泛存在于细菌、真菌和其他微生物中。
当内毒素进入人体后,它们会引发炎症反应、免疫系统紊乱及其他多种不良反应,严重影响健康。
因此,寻找有效的方法除去内毒素变得非常重要。
本文将介绍几种除内毒素的方法,包括物理方法、化学方法和生物方法。
物理方法物理方法是以物理性质对内毒素进行处理,使其失去毒性。
其中一种常见的物理方法是超滤。
超滤通过利用不同孔径的滤膜,将内毒素分离出来。
超滤膜可以选择性地阻止内毒素以及其他大分子物质通过,从而实现内毒素的去除。
此外,离心过滤也是一种物理方法,通过高速旋转使内毒素沉淀,从而将其除去。
化学方法化学方法主要是通过化学反应将内毒素转化为无害物质。
一个常见的化学方法是使用活性炭吸附内毒素。
活性炭具有高表面积和强吸附能力,可以将内毒素吸附在其表面,从而起到除毒作用。
此外,有些化学制剂,如聚乙烯吡咯烷酮(PEI)和多肽,也被用于结合内毒素,形成复合物,从而降低其毒性。
生物方法生物方法利用生物体内的酶或细胞来降解或清除内毒素。
其中一种常见的生物方法是使用内毒素结合蛋白(LBP)。
LBP是一种由宿主产生的蛋白质,它可以结合内毒素并将其清除。
另一种生物方法是利用乳酸菌。
乳酸菌是一类有益菌,研究表明它们可以分解内毒素并减少其毒性。
综合方法除了以上介绍的单一方法,综合方法也是一种有效的除内毒素策略。
综合方法将物理、化学和生物方法相结合,以提高除毒效果。
例如,可以同时使用超滤和活性炭吸附,以实现高效的内毒素去除。
此外,在除去内毒素的过程中,还应重视预防内毒素的生成。
一些措施包括保持食品的卫生、加强环境的消毒和防止霉菌滋生。
通过预防内毒素产生,可以降低内毒素对健康的危害,减少内毒素去除的工作量。
综上所述,除内毒素的方法多种多样,包括物理方法、化学方法和生物方法。
这些方法各有特点,并可以相互结合以提高除毒效果。
在除去内毒素的同时,也需要预防内毒素的生成,以进一步保护人体健康。
去内毒素质粒提取原理

去内毒素质粒提取原理内毒素质粒提取原理。
内毒素质粒提取是一种常用的生物实验技术,用于从细菌中提取内毒素质粒,以便进行后续的实验操作。
内毒素是一种存在于细菌细胞壁中的有毒物质,其存在会对实验结果产生干扰甚至影响实验结果的准确性,因此需要将其从细菌中去除。
下面将介绍内毒素质粒提取的原理及操作步骤。
1. 原理。
内毒素质粒提取的原理主要是利用离心技术和化学试剂的作用,将细菌细胞壁破裂并去除,从而得到内毒素质粒的提取物。
首先,通过离心将细菌培养液离心沉淀,得到含有细菌细胞的沉淀物。
然后使用化学试剂(如SDS、蛋白酶K等)对细菌细胞进行破裂和去除内毒素的处理,最终得到内毒素质粒的提取物。
2. 操作步骤。
(1)培养细菌,首先需要在含有适当营养物的培养基中培养目标细菌,使其达到适当的生长状态。
(2)离心沉淀,将培养好的细菌培养液进行离心,得到细菌细胞的沉淀物。
(3)破裂细胞,使用化学试剂(如SDS)对细菌细胞进行破裂,使内部的内毒素质粒暴露出来。
(4)去除内毒素,使用蛋白酶K等化学试剂去除内毒素,得到纯净的内毒素质粒提取物。
3. 注意事项。
在进行内毒素质粒提取实验时,需要注意以下几点:(1)操作环境要保持清洁,避免外源性内毒素的污染。
(2)化学试剂的使用要按照安全操作规范进行,避免对人身和实验物质造成伤害。
(3)离心操作要注意转速和离心时间的控制,以保证细菌细胞的充分沉淀。
(4)内毒素质粒提取物的保存要在低温条件下,避免其降解和污染。
4. 应用领域。
内毒素质粒提取技术主要应用于生物学实验中,如基因工程、蛋白表达等领域。
通过去除内毒素质粒,可以减少实验结果的干扰,提高实验的准确性和可重复性。
总之,内毒素质粒提取是一项重要的生物实验技术,其原理简单而有效,操作步骤清晰明了。
在实际应用中,需要严格按照操作规范进行,以确保实验结果的准确性和可靠性。
希望本文介绍的内容对您有所帮助,谢谢阅读!。
《内毒素及其去除》课件

利用某些微生物将内毒素作为营养物 质降解,从而降低其毒性,这些微生 物通常被称为“内毒素降解菌”。
05
CATALOGUE
内毒素去除技术的研究进展
新技术的研发与应用
生物膜过滤技术
利用生物膜的吸附作用去 除内毒素,具有高效、低 成本的优势。
免疫亲和技术
利用抗体与内毒素的特异 性结合,实现内毒素的特 异性去除。
纳米材料技术
利用纳米材料对内毒素的 吸附和捕获作用,实现内 毒素的去除。
现有技术的改进与优化
优化活性炭吸附技术
通过改进活性炭的孔径和表面性质,提高其对内毒素的吸附能力 。
强化超滤技术
通过提高超滤膜的孔径和膜材料的亲水性,提高超滤去除内毒素的 效果。
离子交换技术
通过优化离子交换剂的离子配比和粒径,提高其对内毒素的去除效 果。
02
内毒素的致死剂量因人而异,与机体的免疫状态、 健康状况等因素有关。
03
及时诊断和治疗内毒素中毒,可有效降低死亡率, 提高治愈率。
03
CATALOGUE
内毒素的检测与鉴定
内毒素检测的方法
01
02
03
04
鲎试验法
利用鲎变形细胞溶解物与内毒 素反应的原理,通过显色反应 或凝固反应来检测内毒素。
显色基质法
06
CATALOGUE
内毒素去除的实际应用
在医疗领域的应用
医疗设备消毒
通过去除内毒素,可以有效地降 低医疗设备上细菌的数量,从而
降低感染的风险。
药品生产
在药品生产过程中,去除内毒素可 以确保药品的安全性和有效性。
血液透析
在血液透析过程中,去除内毒素可 以降低患者体内的毒素水平,提高 治疗效果。
细菌内毒素的耐热性及去除方法

细菌内毒素的耐热性
我们知道细菌内毒素除了具有各种生物活性外,还具很强的耐热性,一般的高压灭菌不能使其灭活,需250℃30分钟以上的干热灭菌才能使其灭活,目前我国药典热原检查法和细菌内毒素检查法中关于玻璃用具的灭菌处理为180℃2小时或250℃30分钟以上,而日本药局方第十三改正为250℃1小时以上。
其它各国药典也大都如此,据国外文献报导,当对细菌内毒素的稀水溶液,在不同温度下保温处理后进行检测,发现其内毒素活性在200℃1小时时还能检测出来。
而只有当加热到250℃1小时才能完全灭活,国内细菌内毒素标准品的耐热情况虽然未能考察,但可以认为对细菌内毒素检查法中玻璃用具等的除菌最好采用250℃1小时以上的干烤处理。
细菌内毒素的除去方法
由于细菌内毒素具有很强的耐热性,因此对于它的去除采用一般的灭菌方法是无法达到的,尤其是制药行业注射剂中内毒素的除去,对于临床用药的安全性意义重大,因此对于药品中内毒素去除可以使用过滤及高压灭菌方法,而对于一般水溶液,则普通采用薄膜过滤后高压法,对于实验中所用器具可使用干热或射线给予灭活,其它也可使用酸、碱破坏的方法。
对于细菌内毒素检查法中所用实验用具的外源性内毒素除去方法,最好采用250℃2hr以上的干热灭菌方法。
内毒素消除干扰的方法

内毒素消除干扰的方法内毒素啊,这玩意儿就像个调皮的小恶魔,老在我们不注意的时候出来捣乱。
那怎么对付这个小恶魔,把它的干扰给消除掉呢?咱先来说说物理方法。
就好比家里有灰尘,我们可以用扫帚把它扫出去一样,对于内毒素,我们也可以通过一些物理手段来处理。
比如过滤,就像筛子筛东西似的,把那些大颗粒的内毒素给拦住,不让它们到处乱跑。
还有超滤,这就像是个更精细的筛子,能把更小的内毒素也给截留下来。
再说说化学方法。
这就像是给内毒素喂了一颗“毒药”,让它失去作恶的能力。
比如说酸碱处理,让内毒素在不合适的环境里没法嚣张。
还有一些特殊的化学试剂,能和内毒素发生反应,把它给“收拾”了。
然后呢,还有生物方法。
想象一下,内毒素就像是入侵的敌人,而我们的身体里有自己的“军队”,比如一些酶,它们就能专门对付内毒素,把它给降解掉,让它没法再兴风作浪。
还有啊,我们在日常生活中也得注意一些细节。
比如保持环境清洁,别让那些可能带有内毒素的东西随便进入我们的“领地”。
使用的器具要经常清洗消毒,这就像是给它们穿上一层“铠甲”,让内毒素没法轻易附着。
在处理内毒素的时候,可不能马虎大意啊!要是不认真对待,那不是给自己找麻烦吗?就像出门不看天气预报,结果被雨淋成了落汤鸡,多冤啊!我们得时刻保持警惕,用各种方法把内毒素的干扰降到最低。
想想看,如果内毒素肆意妄为,那我们的身体、我们的实验、我们的工作不都得乱套了吗?所以啊,一定要重视内毒素消除干扰的方法,把这个小恶魔牢牢地控制住。
别让它在我们的生活和工作中捣乱,让我们的一切都能顺顺利利的。
这可不是小事,这是关系到我们健康和工作质量的大事啊!大家可千万别不当回事儿,一定要认真对待,积极采取措施,让内毒素乖乖听话,别再给我们制造麻烦啦!。
内毒素灭活方法

内毒素灭活方法咱今儿就来聊聊内毒素灭活方法。
你可别小瞧这内毒素,它就像个捣乱的小恶魔,要是不把它处理好,那可会惹出不少麻烦呢!要说内毒素灭活,那方法还真不少。
就好比咱打扫房间,有各种各样的工具和办法。
首先呢,有一种方法叫高温法。
你想想看,把东西放在高温环境下烤一烤,是不是很多细菌病毒啥的就受不了啦?内毒素也不例外呀,高温能让它失去活性。
这就像夏天大太阳底下,那些小虫子都得找地方躲起来一样。
还有化学方法呢!用一些特定的化学试剂,就像给内毒素来个“魔法攻击”,让它乖乖就范。
这就好像给小恶魔施了个定身咒,让它动弹不得。
不过可得小心使用这些化学试剂哦,别一不小心用错了或者用多了,那可就糟糕啦!再来说说过滤法。
这就好比拿个筛子筛东西,把那些大颗粒的杂质都筛掉,留下纯净的部分。
内毒素也能通过这种方式被分离出去,让我们得到更干净、更安全的东西。
还有一种方法,就像是给内毒素来个“温柔一刀”,让它在不知不觉中被消灭。
这就是辐射法啦!用一些射线照一照,内毒素可能还没反应过来呢,就已经被搞定了。
你说这内毒素灭活方法是不是很神奇?每种方法都有它的特点和适用范围。
就像我们穿衣服,不同的场合要穿不同的衣服一样。
在实际应用中,我们得根据具体情况选择合适的方法。
要是选错了方法,那不就像大冬天穿个短袖出门,会被冻得够呛呀!咱可不能小看内毒素灭活这件事,它关系到很多方面呢!比如在医疗领域,要是药品或者医疗器械上有内毒素没处理好,那用在人身上会怎么样?想想都可怕!在食品行业也是一样,要是食品里有内毒素残留,那我们吃下去还能健康吗?所以啊,我们得重视内毒素灭活方法,把这个小恶魔彻底打败!让我们的生活更加安全、健康。
你说是不是这个理儿?咱可不能让内毒素这个小捣蛋鬼在我们身边捣乱呀!那可不行!大家都要记住这些方法,在需要的时候用起来,让内毒素无处可逃!。
生物制品中内毒素的危害及其去除方法的研究进展

生物制品中内毒素的危害及其去除方法的研究进展摘要:生物制品生产过程中中会有很多细菌在死亡或者分解后释放出各种毒素,这些毒素残留于生物制品中,会对机体内的单核进行作用,一旦细胞因子过量就会对有机体造成损害,也会引起有机体严重的病理反应,甚至危及生命。
我们要深入了解生物制品中毒素的危害,研究各种纯化分离方法来去除毒素,达到药品规定的毒素含量,方可投入市场让人们使用。
关键词:生物制品;毒素;危害;去除方法;研究一、引言生物制药过程难免因为人为因素和外界环境因素导致不可避免的细菌污染从而导致毒素产生,比如革兰氏阴性菌细胞在死亡或者分解后就会释放一种内毒素。
一般来说,适量的细胞因子可以激活有机体的免疫系统,对有机体是大有裨益的,但是过量的细胞因子就会引起有机体的严重病理反应,导致各种症状发生,危及有机体的生命和健康。
在对生物制品中的毒素进行分离以及认识的过程中,务必要对内毒素有效去除并且达到药品规定的内毒素含量标准,才能放心使用。
二、内毒素概述所谓内毒素是革兰氏阴性菌引发的脂多糖,有耐高温的属性,只有在250摄氏度的高温条件下灭菌才能成功,并破坏其生物活性,否则就难以彻底清除。
内毒素会因为细菌种类的不同而存在一些差异,比如临床症状会有很大不同。
但是主要会呈现出腹泻、发热、败血症情况。
当内毒素入侵有机体的不同组织和器官之后,所表现出的致病情况也有差异。
外毒素与内毒素是不同的,外毒素主要由革兰氏阳性菌引发的,部分也可以由革兰氏阴性菌引起,主要的成分是蛋白质,外毒素对化学物质和热源非常敏感,可以很容易丧失活性,这一点与内毒素有很大差别。
使用一定浓度的甲醛溶液处理后可以让外毒素完全失去活性,可以增强抗原性,诱使有机体产生抗毒素。
内毒素致病的反应有很多,常见的有发热反应,休克反应。
发热反应是微量的内毒素就可以引起的症状,体温上升源自内毒素中的脂多糖结合了蛋白质、白细胞分化抗原所引发的生理过程,当有机体受到了内毒素的感染,就会刺激免疫系统抵抗入侵的细菌并且伴随炎症反应,在细胞因子的作用之下,作用于宿主下丘脑的体温调节中枢受到干扰,就会促使有机体的体温升高。
去除内毒素的方法总结
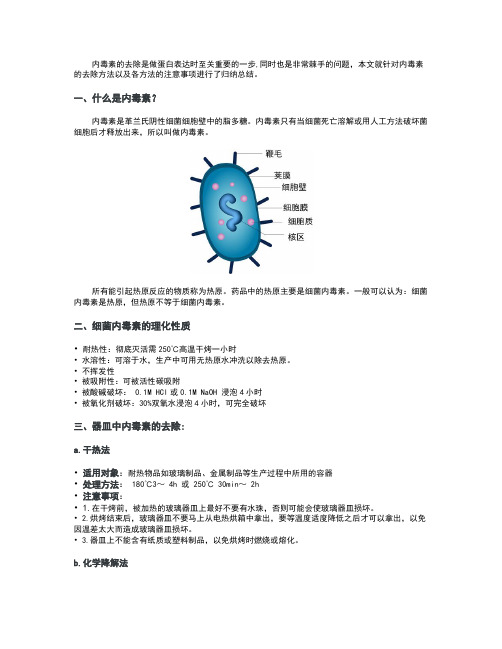
内毒素的去除是做蛋白表达时至关重要的一步,同时也是非常棘手的问题,本文就针对内毒素的去除方法以及各方法的注意事项进行了归纳总结。
一、什么是内毒素?内毒素是革兰氏阴性细菌细胞壁中的脂多糖。
内毒素只有当细菌死亡溶解或用人工方法破坏菌细胞后才释放出来,所以叫做内毒素。
所有能引起热原反应的物质称为热原。
药品中的热原主要是细菌内毒素。
一般可以认为:细菌内毒素是热原,但热原不等于细菌内毒素。
二、细菌内毒素的理化性质•耐热性:彻底灭活需250℃高温干烤一小时•水溶性:可溶于水,生产中可用无热原水冲洗以除去热原。
•不挥发性•被吸附性:可被活性碳吸附•被酸碱破坏: 0.1M HCl或0.1M NaOH 浸泡4小时•被氧化剂破坏:30%双氧水浸泡4小时,可完全破坏三、器皿中内毒素的去除:a.干热法•适用对象:耐热物品如玻璃制品、金属制品等生产过程中所用的容器•处理方法: 180℃3~ 4h 或 250℃ 30min~ 2h•注意事项:• 1.在干烤前,被加热的玻璃器皿上最好不要有水珠,否则可能会使玻璃器皿损坏。
• 2.烘烤结束后,玻璃器皿不要马上从电热烘箱中拿出,要等温度适度降低之后才可以拿出,以免因温差太大而造成玻璃器皿损坏。
• 3.器皿上不能含有纸质或塑料制品,以免烘烤时燃烧或熔化。
b.化学降解法•适用对象:主要用于去除玻璃、塑料和其它高分子材料器皿上的内毒素。
•处理方法:常用3~5%双氧水、重铬酸钾硫酸清洁液(重铬酸钾∶硫酸∶水常用配比1∶1∶10 或1∶2∶8 )、0.1M HCl或0.1 M NaOH浸泡去除。
一般处理4h以上。
•注意事项:佩戴防护用具,防止皮肤直接接触。
四、溶液中内毒素的去除但是,各种去内毒素的方法不是孤立的,可以相互结合使用。
比如,如果液相分离法得到的蛋白内毒素水平未达标,可以接着利用分子筛法进一步去除内毒素。
五、作为目前去内毒素常用的方法,液相分离法的注意事项值得我们重视1.液相分离方法应用于蛋白纯化中内毒素的去除a.目的蛋白上样后,用预冷的基础溶液+1% Triton X-114缓慢淋洗柱子,直至A280数值稳定不变;b.用预冷的去内毒素基础溶液淋洗柱子,直至A280数值达到基线,稳定不变;c.用各梯度去内毒素的洗脱液洗脱,收集各洗脱液于去内毒素的收集管中。
内毒素的检测和去除

内毒素的检测和去除1 内毒素及其来源1.1内毒素内毒素(endotoxin)是存在于革兰氏阴性菌细胞壁外膜表面的一种大分子物质,一般只有在细胞死亡或分解时自行释放到周围介质中,特殊条件下也可以从活细胞中直接泄漏出来。
内毒素又被称为热原,是一种脂多糖物质,具有耐热性,不易被去除。
若疫苗中存在一定浓度的内毒素,接种动物后,可引起动物发热,休克等,严重时甚至造成死亡。
1.2内毒素的来源因为革兰氏阴性菌无处不在,所以内毒素几乎存在于任何地方。
在疫苗生产中一定要重视和尽可能减少内毒素的污染。
生产用水中内毒素的含量是导致疫苗安全性的关键因素之一。
大量研究表明,疫苗生产过程中内毒素主要来源于培养液和配制用水,其在贮存过程中易受到革兰氏阴性菌的污染。
贮水罐,纯水系统的过滤器和连接管道,以及培养液容器等都可能受到革兰氏阴性菌的污染。
工作人员进出车间携带的物品,以及空气净化系统久不维护,都有可能造成生产车间内的空气尘埃浓度升高,导致内毒素污染。
生产用具、管道、泵、阀门、滤器等的清洗消毒不彻底也会造成内毒素污染。
生产原料的污染,如血液制品,细胞培养基。
人为操作不规范也会引起内毒素污染。
2内毒素的检测目前,内毒素的检测方法较多,但是各存在利弊,因此,选取检测方法要根据实际需求,不建议采取单一的检测方法。
2.1鲎试验法鲎试验法是通过酶的级联反应而实现,内毒素在二价阳离子的参与下激活C因子(FC),然后激活其它酶原,产生一系列凝集酶反应。
该方法是目前检测内毒素最特异和最灵敏的方法。
2.2重组C因子法重组C因子法是使用一个单一的蛋白(重组C因子)作为有效活性成分。
反应中内毒素激活重组C因子,活化的重组C因子将荧光底物裂解,产生荧光复合物,定量检测荧光复合物来量化内毒素。
这种方法可有效避免假阳性的产生。
该方法可用于药品生产,环境,器械生产中的内毒素检测。
2.3热原试验法该方法是比较广泛的检测热原的方法,利用微量内毒素可引起动物体温升高的特性来测试其含量。
去内毒素的方法及检查方法

去内毒素的方法及检查方法注:这部分内容为内毒素的检测方法及去除方法。
热原(pyrogen)是微生物产生的内毒素,是由磷脂、脂多糖和蛋白质组成的复合物,微量即可引起恒温动物体温异常升高。
其中脂多糖具有很强的热原活性。
由革兰氏阴性杆菌产生的热原致热能力最强,真菌、病毒也可以产生热原。
【相关链接】热原的危害一、热原的性质及除去热原的方法1.高温法热原的耐热性能良好,60℃加热1h不被分解破坏,100℃不降解,但180℃3~4h、200℃60min或250℃30~45min可使热原彻底破坏。
因此耐热物品如玻璃制品、金属制品、生产过程中所用的容器和其它用具以及注射时使用的注射器等,均可采用此法破坏热原。
但在通常使用的注射剂热压灭菌条件下不足以破坏热原。
2.吸附法热原在水溶液中可被活性炭、石棉、白陶土等吸附而除去。
由于活性炭性质稳定、吸附性强兼具助滤和脱色作用,故广泛用于注射剂生产,但应注意吸附药液所造成的主药的损失。
3.超滤法热原分子量为1×106左右,体积较小,约1~5nm,可以通过一般滤器和微孔滤膜,但采用超滤法如用 3.0~15nm超滤膜可将其除去。
4.蒸馏法热原能溶于水但不挥发,但可随水蒸气的雾滴进入注射用水中,因此制备注射用水时,原水中的热原可经蒸馏除去,但需多次蒸馏,,并加有隔沫装置,单次蒸馏往往效果不理想。
5.酸碱法热原能被强酸、强碱、强氧化剂破坏。
玻璃容器及用具如配液用玻璃器皿、输液瓶等可用重铬酸钾硫酸清洁液或稀氢氧化钠处理,破坏热原。
6.其它包括离子交换法、凝胶滤过法、反渗透法等。
二、热原的检查方法《中国药典》2005年版规定热原检查采用家兔法,细菌内毒素检查采用鲎试剂法。
1.热原检查法由于家兔对热原的反应与人基本相似,目前家兔法仍为各国药典规定的检查热原的法定方法。
《中国药典》2005年版规定的热原检查法系将一定剂量的供试品,静脉注入家兔体内,在规定时间内,观察家兔体温升高的情况,以判定供试品中所含热原的限度是否符合规定。
细菌内毒素的概念及去除内毒素在质粒抽提中的意义

细菌内毒素的概念及去除内毒素在质粒抽提中的意义引⼦内毒素在⼤家做质粒抽提时常接触的⼀个概念,其在免疫学更常以LPS的概念出现,但内毒素究竟是什么?为什么在质粒抽提的时候强调需要去内毒素?它对于我们这些并不从事免疫⽅⾯研究的科研⼈员⼜有什么需要了解的呢?遍寻⽹上,终发现核酸研究巨头——QIAGEN公司,已经就这些疑问做了⾮常好的总结,下⾯将相关⽹页的内容呈现给⼤家。
内毒素的概念内毒性也称为脂多糖或LPS,是⾰兰⽒阴性(如⼤肠杆菌,E.coli)胞膜上⼀种成分。
细菌外膜的外部脂质成分完全由内毒素分⼦组成。
⼀个E.coli包含约2百万个LPS分⼦,每个LPS分⼦⼜由疏⽔性的脂质A、复杂的多糖链以及带负电荷的磷酸基团组成。
因此每个内毒素既包含疏⽔区域也包含了亲⽔和带电区域,从⽽赋予其与其它分⼦相互作⽤的独特性质。
细菌在其活跃⽣长时表⾯的内毒素成分较少,⽽⼀旦其死亡则会释放⼤量内毒素。
在质粒提取的裂解过程中,内毒素会从细菌的外膜释放到裂解液中。
⼤肠杆菌胞膜的结构⽰意图内毒素(LPS)的结构⽰意图内毒素污染⼴泛存在于多种不同形式的质粒提取⽅法内毒素分⼦的化学结构、特性及其倾向于形成微团结构的特点,使其常与质粒DNA共存从⽽被共同纯化出来。
以CsCl超速离⼼纯化为例,内毒素分⼦度与质粒-EB复合体在CsCl中的密度⼏乎相当,因此纯化得到的DNA中内毒素污染依然存在。
同样的,在基于分⼦⼤⼩的层析树脂纯化法也难以区分内毒性分⼦形成的⼤体积微团与⼤分⼦DNA。
再者,阴离⼦交换树脂纯化法中,由于内毒素分⼦携带的负电荷也会与交换树脂相互作⽤,因此内毒素和DNA也会被⼀同纯化出来。
但是质粒中内毒素污染的程度与纯化的⽅法很有关系。
QIAGEN质粒提取试剂盒与2次CsCl梯度离⼼法均可得到低内毒素的⾼纯度DNA。
⽽硅胶柱法纯化的DNA内毒素污染要严重的多。
⽽使⽤EndoFree Plasmid Kits提取的DNA中内毒素的含量⼏乎可以忽略(<0.1 EU/µg)。
内毒素及其去除

构建生物经济体系
打造生物经济旗舰
疏水与分子筛
疏水层析法利用高盐增加蛋白疏水性与介质结合,而在 高盐体系中内毒素由于脂质 A部分有很强的疏水性发凝 集,无法与层析介质结合,因此能够有效去除内毒素
分子筛是利用凝胶的网状结构根据分子大小进行分离的 一种方法。一般抗体分子量为几万道尔顿,而内毒素分子 量为几十万至上百万道尔顿,常是多聚体,因此利用分子筛 可以有效去除内毒素,但其处理量小,处理时间较长。
适用于亲水性蛋白的内毒去除,会使一些有毒的 Triton X-114 残存在蛋白溶液中
构建生物经济体系
打造生物经济旗舰
阴离子交换层析
离子交换层析的速度快、载量高、浓缩效应好 ,在早期下游纯化中担当重要角色。一般而言, 内毒素比蛋白质在阴离子交换介质上的结合强 很多,分子量越小的内毒素结合得越强,多数要 在柱再生(1M氯化钠) 或在位清洗(1M氢氧化钠 )时才从介质上洗脱下来
内毒素去除方法存在选择性差,样品回收率低等问题。下面主要介 绍几种生产中常用的方法
一
相分离法Triton X-114
二
阴离子交换层析
三
疏水层析与分子筛
四
亲和层析
构建生物经济体系
打造生物经济旗舰
相分离法Triton X-114
此法用于较大重组蛋白质(rCK-bb、Rck-mb)中LPS的去除 ,经过三次相分离后,LPS从104 EU/ml降到了几个EU/ml, 去除率超过97%,蛋白的回收率大于90%。
内毒素在pH〉2时都是带负电。阴离子层析填料自身带 正电能够吸附内毒。可使用流穿模式,上样前样品PH控 制在目的蛋白PI以下,使其带正电。这样内毒素结合在 填料上,目的蛋白直接流穿
如二乙胺乙基(DEAE)阴 离子交换介质适于从碱性蛋 白质(即带正电的蛋白质, 如尿激酶)中去除内毒素,
去除热原细菌内毒素的方法

去除热原细菌内毒素的方法热原细菌(Thermophilic bacteria)是一类生活在高温环境下的细菌。
这些细菌能够产生大量的内毒素,对人体健康造成威胁。
因此,去除热原细菌内毒素成为保障食品安全和卫生的重要措施。
本文将介绍一些去除热原细菌内毒素的方法。
第一种方法是物理方法。
物理方法是利用物理性质对细菌进行杀灭或去除。
高温是热原细菌生长繁殖的必要条件,因此,可以利用高温杀菌的方法去除热原细菌。
传统的高温杀菌方法包括煮沸、高温蒸煮等。
通过将食品或饮水加热到高温,可以有效地杀灭细菌和去除内毒素。
此外,还可以利用压力蒸煮、蒸汽灭菌等高压杀菌方法,进一步提高杀菌效果。
第二种方法是化学方法。
化学方法是利用化学物质对细菌进行杀灭或去除。
常用的化学方法是利用消毒剂对食品和饮水进行处理。
消毒剂中的活性氯、过氧化氢等化学物质能够破坏细菌的细胞结构,达到杀菌的效果。
此外,抗菌剂也可以被用来防止热原细菌内毒素的生成。
抗菌剂能够抑制细菌的生长和繁殖,减少内毒素的产生。
然而,在使用化学方法的过程中需要注意剂量的选择和使用方法的正确。
第三种方法是生物方法。
生物方法是利用其他生物来去除热原细菌内毒素。
常用的生物方法包括利用益生菌、乳酸菌等有益菌来竞争热原细菌的营养和生存环境,减少细菌数量和内毒素的生成。
益生菌和乳酸菌能够产生乳酸等有益物质,调节肠道微生物平衡,减少毒素的吸收和损害。
此外,还可以利用其他微生物或酶来降解热原细菌内毒素。
这些微生物或酶能够分解内毒素的结构,降低毒性。
第四种方法是物理-化学联合方法。
物理-化学联合方法是将物理和化学方法结合起来使用,以提高去除热原细菌内毒素的效果。
例如,利用高温蒸煮结合消毒剂的使用,可以达到更好的杀菌和去除内毒素的效果。
此外,还可以利用紫外线辐射等物理性质对细菌进行杀灭,再结合化学方法去除内毒素。
总的来说,去除热原细菌内毒素的方法有物理方法、化学方法、生物方法和物理-化学联合方法等。
生物制剂中内毒素去除方法概述

(6)其他亲和吸附配基。 除以上所述配基之外还有很多 种配基如壳聚糖、季铵盐、胺类、多肽类等对 LPS 的去除也有 较好的效果。
三 展望 近年来,LPS 的去除研究已经取得了很大进展,生物技术 产品在制药工业中的比重越来越大,其 LPS 去除工艺的研发
以及工业化规模扩大仍是今后研究的热点。 参考文献: [1]焦炳华.分子内毒 素 学[M].上 海:上 海 科 学 技 术 文 献 出
(5)氨基酸。 自 20 世纪 80 年代起组胺(Him)、组氨酸(His) 就开始作为配基去除 LPS。由于 His 生物活性较高、价格和毒 副作用都较小而更受欢迎,其作用主要来自于连接载体与配 体 的 间 隔 臂(如 己 二 胺)和 组 氨 酸 上 的 咪 唑 环 ,但 受 pH 的 影 响较大。 除组氨酸外,赖氨酸、精氨酸等氨基酸也被认为能与 LPS 发生作用。
98
2015 年第 4 期
LPS 血症中的 LPS。 免疫亲和具有高度特异性,但是这种配基 制备困难,应用范围狭窄,同时还有价格昂贵、洗脱困难的问 题。
(2)多粘菌素 B(PMX-B)。 PMX-B 能 依 靠 其 环 形 肽 结 构 降解革兰氏阴性细菌的细胞壁,其阳离子与类脂 A 的磷酸基 团之间的静电作用力和疏水作用力使其能识别不同来源的 LPS 分子。 采用固定 PMX-B 的纤维素(或琼脂糖)载体 去 除 LPS,有良好的效果和稳定性。但是 PMX-B 的价格昂贵,且有 肾毒性和神经毒性,应谨慎应用。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1.高温烘烤 热原的耐热性能良好,60℃加热1h不被分解破坏,100℃不降解 ,但180℃3~4h、200℃60min或250℃30~45min可使热原彻底 破坏。此法适合玻璃器皿的去内毒
2.碱消毒(室温条件下)
主要用于玻璃、 塑料和 其它高分子材料器皿上 内毒素的去除
构建生物经济体系
打造生物经济旗舰
4.蒸馏法,超滤法,反渗透,此法一般在生产注射用水 时用到,蒸馏需要多级蒸馏并且加隔沫装置,反渗透成 本高。 5.吸附法,内毒素在水溶液中可被活性炭、石棉、白陶 土等吸附而除去。由于对蛋白有吸附故不适合用于生物 制品。 6.层析法,选用合适的层析填料和溶液体系,能够有 效去除产品中的内毒素,是目前单抗纯化生产中的主 流工艺。 7.相分离法、适用于蛋白制品,但各有缺点。
构建生物经济体系
打造生物经济旗舰
亲和层析
在低pH时,内毒素分子中磷酸酯基和羧基离子化减小。在分子内疏 水作用的驱使下内毒素分子趋于更为紧凑的结构,从而减少了相互 作用的位点,导致去除率的下降。随着溶液pH的增大,内毒素分子的 紧凑结构被分子内静电相互作用破坏,舒展的结构使内毒素分子与 固载于琼脂糖上的配基产生更为有效的作用,导致去除率的升高。 在高 pH 下内毒素去除率的下降可能是因为键合于基质上的疏水配 基的构像发生扭曲变形所致。
我国药典要求注射剂中细 菌内毒素<1EU/ml
细菌内毒素标准在制定时应定为计算值的1/3~1/2。
K 为人每公斤体重每小时最大可接受的内毒素剂量,单位 EU/(kg · h) M 为人每公斤体重每小时的最大供试品剂量,单位mg/(kg · h)
常用内毒素检测方法
凝胶法
内毒素与 鲎试剂的 凝胶反应
大于0.03EU/ml范围 0.006-300EU/mL
构建生物经济体系
打造生物经济旗舰
内毒素是什么
内毒素也称为脂多糖或 LPS,是革兰氏阴性菌 胞壁上一种成分(少数 阳性菌也能产生)。其 细胞壁外膜的外部脂质 成分完全由内毒素分子 组成 ,死亡时则会释 放大量内毒素。一个大 肠杆菌细胞约含有200 万个LPS分子
构建生物经济体系
打造生物经济旗舰
功能部分
需精密的专用仪器
构建生物经济体系
打造生物经济旗舰
自身特点 极少的养分G-即可存活, 内毒几乎无处不在 单体、聚集体种类繁多 性质不均一
相互作用 本身带负电,可以和带 正电的碱性蛋白结合
内毒素
通过二价阳离子(如 Ca2+) 的桥接作用和酸 性蛋白形成复合体 类脂A的疏水特性导致 其和疏水性蛋白结合
热稳定性高 180℃ 3 hours
适用于亲水性蛋白的内毒去除,会使一些有毒的 Triton X-114 残存在蛋白溶液中
构建生物经济体系
打造生物经济旗舰
阴离子交换层析
离子交换层析的速度快、载量高、浓缩效应好 ,在早期下游纯化中担当重要角色。一般而言, 内毒素比蛋白质在阴离子交换介质上的结合强 很多,分子量越小的内毒素结合得越强,多数要 在柱再生(1M氯化钠) 或在位清洗(1M氢氧化钠 )时才从介质上洗脱下来
构建生物经济体系
打造生物经济旗舰
疏水与分子筛
疏水层析法利用高盐增加蛋白疏水性与介质结合,而在 高盐体系中内毒素由于脂质 A部分有很强的疏水性发凝 集,无法与层析介质结合,因此能够有效去除内毒素
分子筛是利用凝胶的网状结构根据分子大小进行分离的 一种方法。一般抗体分子量为几万道尔顿,而内毒素分子 量为几十万至上百万道尔顿,常是多聚体,因此利用分子筛 可以有效去除内毒素,但其处理量小,处理时间较长。
内毒素去除方法存在选择性差,样品回收率低等问题。下面主要介 绍几种生产中常用的方法
一
相分离法Triton X-114
二
阴离子交换层析
三
疏水层析与分子筛
四
亲和层析
构建生物经济体系
打造生物经济旗舰
相分离法Triton X-114
此法用于较大重组蛋白质(rCK-bb、Rck-mb)中LPS的去除 ,经过三次相分离后,LPS从104 EU/ml降到了几个EU/ml, 去除率超过97%,蛋白的回收率大于90%。
结构复杂, 特异性部分
疏水性, 毒性部分
脂质 A 磷酸 基团
多糖 链
带负电
构建生物经济体系
打造生物经旗舰
不同的革兰氏阴性细菌,其 LPS的化学组成有一定的差别 ,但都含有内脂 A 部分
极 高 的 热 稳 定 性
带 负 电
亲 水 兼 疏 水
糖亲水 脂疏水
250℃ 30分钟
等电点 在2左右
构建生物经济体系
Thank You
构建生物经济体系
打造生物经济旗舰
亲和层析 以组氨酸 、 组胺、 多粘菌素 B、聚阳离子等为配基
亲和层析
将内毒素底物LAL或多粘菌素 B(PMB)偶联于CNBr-Sepharose 或NHS-Sepharose上,以此介质特 异性吸附内毒素,而让蛋白通过 。
Байду номын сангаас 构建生物经济体系
打造生物经济旗舰
亲和层析
亲和配基 PMB 与内毒素之间的作用主要是疏水与静电作用 ,而盐浓度即 离子强度的变化会反方向影响这两种作用 : 离子强度增大会增强亲和配基 PMB与内毒素之间的疏水作用,同时又会减 小两者之间的静电作用 ; 离子强度减小会减小亲和配基 PMB与内毒素之间的疏水作用,同时又会增 大两者之间的静电作用。疏水作用与静电作用的协同作用导致了上述结 果。
构建生物经济体系
打造生物经济旗舰
多种层析方法组合效果
生物技术药品的纯化, 主要是采用各种柱层 析技术,如疏水层析、 离子交换、亲和层析 、分子筛等,这些技术 纯化目标产品的同时 也可以有效去除内毒 素
虽然生物制品中内毒素的除去方法很多,但 还是很难将内毒素彻底去除,为了从根本上 解决内毒素的困扰,在生产前我们应该对生 产环境,生产器具,操作方法等进行严格控 制,将内毒素污染风险降到最低
浊度变化
浊度法
显色 基质法
0.006-15EU/ml
显色基团吸光度变化
部分药品由 于自身特殊 性无法通过 稀释法消除 干扰,因此 鲎试验还无 法完全取代 家兔热原试 验
缓慢翻转180°,目测 终点
简单,经济, 不需专用测定设 备 特异性不强 精密度、定量性差
简单、快速、灵敏 度高、检测范围宽
精度高、灵敏 度高 仪器和试剂贵, 操作比较复杂
内毒素在pH〉2时都是带负电。阴离子层析填料自身带 正电能够吸附内毒。可使用流穿模式,上样前样品PH控 制在目的蛋白PI以下,使其带正电。这样内毒素结合在 填料上,目的蛋白直接流穿
如二乙胺乙基(DEAE)阴 离子交换介质适于从碱性蛋 白质(即带正电的蛋白质, 如尿激酶)中去除内毒素,
成本低,吸附容量大, 但这种方法不适用于带 负电荷的蛋白
造生物经济旗舰
内毒素存在形式
单体
胶束
囊状
构建生物经济体系
打造生物经济旗舰
冷颤
医药制剂
本身不合格或放置 时间过长
发热,头痛 恶心,呕吐,脸色苍白
输液器
未消毒彻底
0.5—1 小时
血液循环障碍
注射器
操作污染
休克 死亡 2ng/kg体重即能引起发热
构建生物经济体系
打造生物经济旗舰
生物制品中内毒素标准
药品、生物制品的细菌内毒素限值(L,EU/mg)一般按以 下公式确定:
