红外光谱吸收峰
红外吸收光谱特征峰

红外吸收光谱特征峰1. 水平振动峰:大部分物质在红外光谱中显示出实数振动峰,这些峰通常位于1500-4000 cm^-1区间。
在这个区间内,主要的振动模式有:C-H拉伸振动,C=O伸缩振动,C-N伸缩振动和O-H伸缩振动等。
2. 弯曲振动峰:这些峰通常位于500-1500 cm^-1区间,代表物质中相对较低能量的振动模式。
其中,主要的弯曲振动包括:C-H弯曲振动、O-H弯曲振动和C-N弯曲振动等。
3. 拉曼峰:拉曼光谱是一种与红外光谱类似的光谱,主要用于研究物质的分子振动。
拉曼光谱中的峰通常位于200-4000 cm^-1区间,包括了与红外光谱重叠的水平和弯曲振动。
4. 振动-转动峰:当分子既有振动运动又有转动运动时,红外光谱中会出现振动-转动峰。
这些峰通常位于0-500 cm^-1区间,具有特定的振动和转动组合频率,可以用来确定分子的对称性。
5. 过渡金属峰:一些过渡金属化合物在红外光谱中显示出独特的吸收峰。
这些峰通常位于400-2000 cm^-1区间,对应于金属-配体之间的振动模式。
6. 质子峰:质子(H+)在红外光谱中呈现为一个孤立线峰。
质子峰的位置通常在1500-2500 cm^-1之间,变化范围较大,取决于质子的环境。
红外吸收光谱中的这些特征峰可以提供物质的结构、键合和功能基团等信息。
通过分析化合物在红外光谱中的峰值位置和形状,可以确定其化学组成和化学结构,实现化合物的鉴定和分析。
同时,红外光谱还可以用于跟踪反应过程、监测化学变化和定量分析等方面。
这些特征峰在各个研究领域,如有机化学、材料科学和生物化学等中都有广泛的应用。
红外吸收光谱特征峰,史上最全-红外中no吸收峰

表15.1 典型无机化合物的紧张基团频率(/cm-1)之相礼和热创作化合物基团X-H伸缩振动区叁键区双键伸缩振动区部分单键振动和指纹区烷烃-CH3asCH:2962±10(s)asCH:1450±10(m)sCH:2872±10(s)sCH:1375±5(s)-CH2-asCH:2926±10(s)CH:1465±20(m)sCH:2853±10(s)CH:2890±10(s)CH:~1340(w)烯烃CH:3040~3010(m)C=C:1695~1540(m)CH:1310~1295(m)CH:770~665(s)CH:3040~3010(m)C=C:1695~1540(w)CH:970~960(s)炔烃-C≡C-H CH:≈3300(m)C≡C:2270~2100(w)芳烃CH:3100~3000(变)泛频:2000~1667(w)C=C:1650~1430(m)2~4个峰CH:1250~1000(w) CH:910~665单取代:770~730(vs)≈700(s)邻双取代:770~735(vs) 间双取代:810~750(vs)725~680(m)900~860(m) ~对双取代:860~790(vs)醇类R-OH OH:3700~3200(变)OH:1410~1260(w)CO:1250~1000(s)OH:750~650(s)酚类Ar-OH OH:3705~3125(s)C=C:1650~1430(m)OH:1390~1315(m)CO:1335~1165(s)脂肪醚R-O-R'CO:1230~1010(s) 酮C=O:≈1715(vs)醛CH:≈2820,≈2720(w)双峰C=O:≈1725(vs)羧酸OH:3400~2500(m)C=O:1740~1690(m)OH:1450~1410(w)CO:1266~1205(m)酸酐C=O:1850~1880(s)C=O:1780~1740(s)CO:1170~1050(s)酯泛频C=O:≈3450(w)C=O:1770~1720(s)COC:1300~1000(s)胺-NH2NH2:3500~3300(m)双峰NH:1650~1590(s,m) CN(脂肪):1220~1020(m,w)CN(芳香):1340~1250(s)-NH NH:3500~3300(m)NH:1650~1550(vw)CN(脂肪):1220~1020(m,w)CN(芳香):1350~1280(s)酰胺asNH:≈3350(s)C=O:1680~1650(s)CN:1420~1400(m) sNH:≈3180(s)NH:1650~1250(s)NH2:750~600(m)NH:≈3270(s)C=O:1680~1630(s) CN+NH:1310~NH+CN:1750~1515(m)1200(m)C=O:1670~1630酰卤C=O:1810~1790(s)腈-C≡N C≡N:2260~2240(s)硝基化合物R-N02NO2:1565~1543(s)NO2:1385~1360(s)CN:920~800(m)Ar-NO2NO2:1550~1510(s)NO2:1365~1335(s)CN:860~840(s)不明:≈750(s)吡啶类CH:≈3030(w)C=C及C=N:1667~1430(m)CH:1175~1000(w)CH:910~665(s)嘧啶类CH:3060~3010(w)C=C及C=N:1580~1520(m)CH:1000~960(m)CH:825~775(m)* 表中vs,s,m,w,vw用于定性地暗示吸取强度很强,强,中,弱,很弱.中红外光谱区一样平常划分为官能团区和指纹区两个区域,而每个区域又可以分为多少个波段.官能团区官能团区(或称基团频率区)波数范围为4000~1300cm-1,又可以分为四个波段.★4000~2500cm-1为含氢基团x—H(x为O、N、C)的伸缩振动区,由于折合质量小,以是波数高,次要有以下五种基团吸取● 醇、酚中O —H :3700~3200cm-1,无缔合的O —H 在高 一侧,峰形尖锐,强度为s缔合的O —H 在低一侧, 峰形宽钝, 强度为s● 羧基中O —H : 3600~2500cm-1,无缔合的O —H 在高 一侧,峰形尖锐,强度为s缔合可延伸至2500 cm-1,峰非常宽钝,强度为s● N —H : 3500~3300 cm-1, 伯胺有两个H ,有对称和非对称两个峰,强度为s—m叔胺无H ,故无吸取峰●C —H : <3000 cm-1为饱和C :~2960 cm-1 (),~2870 cm-1()强度为m-s~2925 cm-1 (),~2850 cm-1()强度为m-s~2890 cm-1强度为w>3000 cm-1为不饱和C :(及苯环上C-H)3090~3030cm-1强度为m~3300 cm-1强度为m● 醛基中C —H :~2820及~2720两个峰强度为m-s ★2500~2000 cm-1 为叁键和累积双键伸缩振动吸取峰,次要包含-C≡C -、-C≡N 叁键的伸缩振动及、等累积双键的非对称伸缩振动,呈现中等强度的吸取.在此波段区中,还有S —H 、Si —H 、P —H 、B —H 的伸缩振动. ★2000~1500 cm-1 为双键的伸缩振动吸取区,这个波段也是比较紧张的区域,次要包含以下几种吸取峰带.●C=O伸缩振动,出如今1960~1650 cm-1,是红外光谱中很特征的且每每是最强的吸取峰,以此很容易判别酮类、醛类、酸类、酯类、酸酐及酰胺、酰卤等含有C=O的无机化合物.●C=N、C=C、N=O的伸缩振动,出如今1675~1500 cm-1.在这波段区中,单核芳烃的C=C骨架振动(呼吸)呈现2~4个峰(中等至弱的吸取)的特征吸取峰,通常分为两组,分别出如今1600 cm-1和1500 cm-1左右,在确定有否芳核的存在时具有紧张意义.●苯的衍生物在2000~1670 cm-1波段出现C—H面外弯曲振动的倍频或组合数.由于吸取强度太弱,运用价值不如指纹区中的面外变形振动吸取峰,如图15.9所示.如在分析中有必要,可加大样品浓度以进步其强度.图15.9 苯环取代类型在2000~1667cm-1和900~600cm-1的谱形★1500~1300 cm-1饱和C—H变形振动吸取峰,—CH3出如今1380及1450 cm-1两个峰,出如今1470 cm-1,出如今1340 cm-1.这些吸取带强度均为m至w .指纹区指纹区:波数范围为1300~600cm-1.指纹区可以分为两个波段:★1300~900cm-1这个波段区的光谱信息很丰富,较为次要的有如下几种:●几乎全部不含H的单键的伸缩振动,如C—O、C—N、C—S、C—F、C—P、Si—O、P—O等,其中C—O的伸缩振动在1300~1000cm-1,是该区吸取最强的峰,较易辨认.●部分含H基团的弯曲振动,如RCH=CH2,端烯基C—H弯曲振动为990、910cm-1的两个吸取峰;RCH=CHR反式结构的C—H吸取峰为970 cm-1(顺式为690 cm-1)等.●某些较重原子的双键伸缩振动,如C=S、S=O、P=O等.此外,某些分子的团体骨架振动也在此区发生吸取.★900~600cm-1这波段中较为有价值的两种特征吸取:●长碳链饱和烃,,n≥4时,呈现722cm-1有一中至强的吸取峰,n减小时,变大;●苯环上C—H面外变形振动吸取峰的变更,可以判别取代状况,此区域的吸取峰比泛频带2000~1670cm-1灵敏,因而更具运用价值,见所示.其吸取峰地位为:无取代的6个C—H,670~680cm-1,单吸取带;苯:单取代苯:5个C—H,690~700cm-1,740~750cm-1,两个吸取带;邻位双取代4个C—H,740~750cm-1,单吸取带;苯:间位双取代3个C—H,690~700cm-1,780~800cm-1,两个吸取带;苯:另一个C—H,~860cm-1,弱带,供参考;对位双取代2个C—H,800~850cm-1,单吸取带.苯:这些吸取带的强度为中等(偶然强)。
红外光谱1000左右的吸收峰

红外光谱1000左右的吸收峰
红外光谱中,吸收峰的位置通常与特定的化学键或者分子振动模式有关。
在1000 cm-1左右的区域,常见的吸收峰主要与以下几种化学键或分子振动有关:
C-O键的拉伸振动:在醇、醚或酯等含有C-O键的有机化合物中,C-O键的拉伸振动通常会在1050-1150 cm-1的区域产生吸收峰。
C-N键的拉伸振动:在胺或酰胺等含有C-N键的有机化合物中,C-N键的拉伸振动通常会在1080-1360 cm-1的区域产生吸收峰。
S=O键的拉伸振动:在磺酰或亚磺酰等含有S=O键的有机化合物中,S=O键的拉伸振动通常会在1000-1300 cm-1的区域产生吸收峰。
C-Cl键的拉伸振动:在含有C-Cl键的有机化合物中,C-Cl键的拉伸振动通常会在600-800 cm-1的区域产生吸收峰,但在某些情况下也可能出现在1000 cm-1左右。
以上只是一些常见的情况,实际上在1000 cm-1左右的吸收峰可能与其他类型的化学键或分子振动有关。
具体的判断需要结合化合物的结构和其他谱图信息。
ch4 h2o红外光谱吸收峰

ch4 h2o红外光谱吸收峰在红外光谱学中,CH4(甲烷)和H2O(水)的分子各自具有特定的红外光谱吸收峰,这些峰可以用于识别这些分子的存在并提供有关它们的结构和化学性质的信息。
甲烷 (CH4) 的红外光谱吸收峰:
1. C-H 伸缩振动:在约3000 cm⁻¹附近,有一个强烈的吸收峰,代表着C-H键的伸缩振动。
2. C-H 弯曲振动:在约1400 cm⁻¹附近,有一个较强的吸收峰,对应着C-H键的弯曲振动。
水 (H2O) 的红外光谱吸收峰:
1. O-H 伸缩振动:在约3400 cm⁻¹附近,水分子显示一个广泛的吸收峰,代表O-H键的伸缩振动。
这个峰很宽,因为水分子中的氢键作用使得振动频率分布在一个较宽的范围内。
2. H-O-H 弯曲振动:在约1600 cm⁻¹附近,水分子显示一个较弱的吸收峰,对应着H-O-H键角的弯曲振动。
这些吸收峰的位置和强度可以通过红外光谱仪来测定,并且提供了关于分子中键的类型和状态的信息。
这种技术在化学分析、光谱学和环境科学等领域中被广泛应用。
1/ 1。
红外的吸收峰

红外的吸收峰一、红外光谱简介红外光谱是一种无损分析技术,通过测量物质在红外辐射下的吸收、散射、透射等现象来研究物质的结构和性质。
红外光谱技术广泛应用于化学、生物、材料科学等领域,成为一种重要的分析手段。
二、红外吸收峰的概念红外吸收峰是红外光谱图中出现的特征吸收峰,与物质的分子结构和化学键有关。
不同的化学键对红外光的吸收具有特定的频率和强度,在红外光谱图中表现为吸收峰。
三、红外吸收峰的分类根据吸收发生的位置和特征,红外吸收峰可以分为以下几类:1. 强度峰强度峰是红外光谱图中最高的峰,代表了分子中最强的吸收带。
强度峰通常对应于物质中具有最大摩尔吸光系数的化学键。
2. 弱度峰弱度峰对应于较弱的吸收带,通常出现在强度峰的附近。
弱度峰可能是由于较小的摩尔吸光系数或者较低的浓度引起的。
3. 重叠峰重叠峰是指在红外光谱图中多个吸收峰重叠在一起,形成一个宽而平坦的峰。
重叠峰常常是由于分子中多个化学键同时吸收红外光而引起的。
4. 锐度峰锐度峰是红外光谱图中出现的尖锐而窄的峰,通常对应于分子中具有较高对称性的化学键。
锐度峰的出现可以提供关于分子结构的有用信息。
四、红外吸收峰的解读红外光谱图中的吸收峰可以提供物质的结构和组成信息。
通过对吸收峰的解读,可以得到以下信息:1. 化学键的存在和类型不同类型的化学键对红外光的吸收具有特定的频率和强度。
通过对吸收峰的位置和形状进行分析,可以确定物质中存在的化学键类型,如C-H键、O-H键、C=O键等。
2. 分子结构的确定红外光谱图中的吸收峰可以提供有关分子结构的信息。
例如,通过观察C=O键的吸收峰位置和形状,可以确定化合物中的酮、醛等官能团。
3. 分子间相互作用的研究红外光谱图中的吸收峰还可以用于研究分子间的相互作用。
例如,通过观察氢键的吸收峰,可以研究分子中氢键的形成和破裂过程。
五、红外吸收峰的应用红外光谱技术在许多领域都有广泛的应用,包括化学、生物、医药、环境等。
下面列举几个常见的应用领域:1. 药物研究红外光谱技术可以用于药物的结构鉴定和质量控制。
红外光谱标准吸收峰

红外光谱标准吸收峰1. 羰基吸收峰。
羰基是化合物中常见的功能团之一,其吸收峰通常出现在1650-1820 cm^-1的范围内。
酮和醛的羰基吸收峰位置略有不同,酮的羰基吸收峰通常出现在1715-1725 cm^-1,而醛的羰基吸收峰则出现在1680-1740 cm^-1。
通过观察羰基吸收峰的位置和形状,可以初步判断化合物中是否存在酮或醛基团。
2. 羟基吸收峰。
羟基的吸收峰通常出现在3200-3600 cm^-1的范围内,其位置和形状可以提供关于羟基取代位置和数量的信息。
醇和酚的羟基吸收峰位置略有不同,醇的羟基吸收峰通常出现在3200-3500 cm^-1,而酚的羟基吸收峰则出现在3600 cm^-1附近。
通过分析羟基吸收峰的位置和强度,可以初步判断化合物中是否存在醇或酚基团。
3. 烷基吸收峰。
烷基的吸收峰通常出现在2800-3000 cm^-1的范围内,其位置和形状可以提供关于烷基取代位置和数量的信息。
通过观察烷基吸收峰的位置和强度,可以初步判断化合物中是否存在烷基取代基团。
4. 硫醚吸收峰。
硫醚的吸收峰通常出现在650-950 cm^-1的范围内,其位置和形状可以提供关于硫醚取代位置和数量的信息。
通过观察硫醚吸收峰的位置和强度,可以初步判断化合物中是否存在硫醚基团。
5. 硫酸酯吸收峰。
硫酸酯的吸收峰通常出现在1200-1300 cm^-1的范围内,其位置和形状可以提供关于硫酸酯取代位置和数量的信息。
通过观察硫酸酯吸收峰的位置和强度,可以初步判断化合物中是否存在硫酸酯基团。
总结,红外光谱标准吸收峰的位置和形状可以提供关于功能团的信息,帮助分析人员快速了解化合物的结构和成分。
通过对红外光谱图谱中吸收峰的观察和分析,可以为化合物的鉴定和分析提供重要参考。
因此,掌握红外光谱标准吸收峰的特点和规律对于正确解读和分析红外光谱图谱具有重要意义。
fe—o红外吸收峰

fe—o红外吸收峰红外吸收峰是指分子在红外光谱中出现的吸收峰。
红外光谱是一种研究物质结构和分子振动的重要手段,通过测量物质在红外光波段的吸收特性,可以对物质的成分和结构进行分析和鉴定。
不同化合物的红外吸收峰具有独特的特征,可以用来识别不同化合物的存在。
下面将介绍几种常见的红外吸收峰及其相关参考内容。
1. O-H吸收峰:O-H吸收峰是指含有羟基(-OH)官能团的化合物在红外光谱中出现的吸收峰。
一般而言,O-H吸收峰出现在3200-3600cm-1区域,具有宽而强烈的吸收峰。
在红外光谱中,O-H吸收峰的位置和形状可以提供关于羟基取代程度和氢键形成的信息。
参考内容:- 《Spectroelectrochemistry of Heme Proteins: Study of O―H Oscillator Strengths and their Relationship to Protein Structure》,B.Brad R. Hinton等,Journal of the American Chemical Society,2009年本文研究了含有血红素的蛋白质的红外吸收光谱,探讨了O-H振动模式的强度与蛋白质结构之间的关系。
2. C=O吸收峰:C=O吸收峰是指含有酮基(C=O)或醛基(C=O)官能团的化合物在红外光谱中出现的吸收峰。
一般而言,酮基的C=O吸收峰出现在1650-1760 cm-1,而醛基的C=O吸收峰出现在1680-1750 cm-1。
C=O吸收峰的位置和强度可以提供关于官能团的信息,例如酮基和醛基的存在以及它们的取代程度。
参考内容:- 《Determination of Ether Linkage in Phospholipids by Infrared Absorption Spectroscopy》,Gerald J. Chang等,Journal of the American Chemical Society,1990年该文研究了磷脂类化合物中醚键的C=O吸收峰,通过红外吸收光谱的定量分析,测定了醚键的含量和取代程度。
1600左右的红外吸收峰

1600左右的红外吸收峰红外吸收峰是指在红外光谱中出现的特定波数范围内的吸收峰。
这些吸收峰可以提供有关物质结构和化学键的信息,因此在红外光谱分析中具有重要的意义。
本文将以1600左右的红外吸收峰为标题,探讨与之相关的物质和应用。
一、红外吸收峰的基本原理和特点红外光谱是一种将物质吸收或发射红外辐射的技术。
当物质受到红外辐射时,分子内的键振动和分子间的转动会发生改变,从而导致特定波数的红外辐射被吸收。
这种吸收现象在红外光谱图上表现为吸收峰。
红外吸收峰的位置和强度与物质的化学组成和结构密切相关。
不同化学键和官能团对应着不同的红外吸收峰位置,因此可以通过分析红外光谱来确定物质的组成和结构。
二、1600左右的红外吸收峰的应用领域和相关物质1. 蛋白质结构分析:在1600左右的波数范围内,常见的红外吸收峰包括酰胺I和酰胺II峰。
这些峰对应着蛋白质中的肽键振动,可以用于分析蛋白质的二级结构和构象变化。
2. 羧酸的检测:在1600左右的波数范围内,羧酸官能团的C=O 伸缩振动会产生吸收峰。
通过分析这些吸收峰的位置和强度,可以确定样品中羧酸的存在和含量。
3. 聚合物材料研究:1600左右的红外吸收峰可以用于分析聚合物材料的结构和性质。
例如,聚酰胺中的酰胺连接会产生特定的吸收峰,可以通过分析这些峰来确定聚酰胺的结构和组成。
4. 药物分析:许多药物分子中含有羧酸、酮、醇等官能团,这些官能团的振动会在1600左右的波数范围内产生吸收峰。
通过分析这些吸收峰的位置和强度,可以用于药物的质量控制和分析。
三、红外吸收峰的分析方法和仪器设备红外光谱分析通常使用红外光谱仪进行。
这种仪器能够测量样品吸收红外光谱的强度和波数,并绘制成红外光谱图。
分析师可以通过观察红外光谱图中吸收峰的位置和形状,来判断样品中的化学键和官能团。
在进行红外光谱分析时,需要将样品制备成透明、均匀的薄膜或片状,并将其放置在红外光谱仪的样品室中进行测量。
通过与已知物质进行比对,可以确定样品中的红外吸收峰的来源和含量。
红外吸收光谱峰位的影响因素

红外吸收光谱峰位的影响因素光谱峰位的影响因素分子内基团的红外吸收会受到邻近基团及整个分子其他部分的影响,也会因测定条件及样品的物理状态而改变。
所以同一基团的特征吸收会在一定范围内波动。
影响因素有: 1. 化学键的强度一般地说化学键越强,则力常数K 越大,红外吸收频率ν 越大。
如碳碳三键,双键和单键的伸缩振动吸收频率随键强度的减弱而减小。
伸缩振动频率 (cm -1) 2150 1715 1200 2. 诱导效应诱导效应可以改变吸收频率。
如羰基连有拉电子基团可增强碳氧双键,加大C=O 键的力常数K ,使C=O 吸收向高频方向移动。
C=O 伸缩振动频率(cm -1 ) 1715 1815 ~ 17853. 共轭效应共轭效应常使C =O 双键的极性增强,双键性降低,减弱键的强度使吸收向低频方向移动。
例如羰基与α、β不饱和双键共轭,从而削弱了碳氧双键,使羰基伸缩振动吸收频率向低波数位移。
C=O 伸缩振动频率(cm -1) 1715 1685 ~ 16704. 成键碳原子的杂化状态一般化学键的原子轨道s 成分越多,化学键力常数K 越大,吸收频率越高。
sp sp 2 sp 3C?H伸缩振动频率(cm-1)3300 3100 29005. 键张力的影响主要是环状化合物环的大小不同影响键的力常数,使环内或环上基团的振动频率发生变化。
具体变化在不同体系也有不同。
例如:环丙烷的C-H伸缩频率在3030 cm-1,而开链烷烃的C-H伸缩频率在3000 cm-1以下。
6.氢键的影响氢键的形成使电子云密度平均化,从而使伸缩振动频率降低。
形成氢键后基团的伸缩频率都会下降。
游离羧酸的C=O键频率出现在1760 cm-1 左右,在固体或液体中,由于羧酸形成二聚体,C=O键频率出现在1700 cm-1 。
分子内氢键不受浓度影响,分子间氢键受浓度影响较大。
例如:乙醇的自由羟基的伸缩振动频率是3640 cm-1,而其缔合物的振动频率是3350 cm-1。
红外吸收光谱特征峰特别整理版

红外吸收光谱特征峰特别整理版红外吸收光谱是一种常见的分析技术,可以通过观察物质在红外辐射下吸收的特定波长的光来确定它的结构和组成。
红外吸收光谱在许多领域都得到广泛应用,包括有机化学、药物研发、食品安全等。
在红外吸收光谱中,一些特定的吸收峰代表了特定的官能团或化学键,因此可以用于识别和鉴定物质。
下面是一些常见的红外吸收光谱特征峰的整理。
1. 羟基(OH)吸收峰:羟基的吸收峰通常出现在3200-3600 cm^-1的范围内。
在醇、酚和羧酸等化合物中,羟基的振动可产生广泛的吸收峰。
2. 胺基(NH)吸收峰:胺基的吸收峰通常出现在3100-3500 cm^-1之间。
在胺类化合物中,氨基的振动会引起这些吸收峰的出现。
3. 羧基(COOH)吸收峰:羧基的吸收峰通常出现在1700-1750 cm^-1之间。
在羧酸和酰胺等化合物中,这些吸收峰代表了羧基的存在。
4. 醛基(C=O)吸收峰:醛基的吸收峰通常出现在1700-1750 cm^-1之间。
在醛和酮等化合物中,醛基的振动会产生这些吸收峰。
5. 烯烃(C=C)吸收峰:烯烃的吸收峰通常出现在1600-1680 cm^-1之间。
在芳香烃和烯烃等化合物中,双键的振动会引起这些吸收峰的出现。
6. 芳香环(C-H)吸收峰:芳香环的吸收峰通常出现在3000-3100cm^-1之间。
在含芳香环的化合物中,芳香环上的氢原子的振动会产生这些吸收峰。
7. 硝基(NO2)吸收峰:硝基的吸收峰通常出现在1500-1600 cm^-1之间。
在含硝基的化合物中,硝基的振动会引起这些吸收峰的出现。
8. 卤素(C-X)吸收峰:卤素的吸收峰通常出现在500-800 cm^-1之间。
在含卤素的化合物中,卤素的振动会产生这些吸收峰。
上述仅是一些常见的红外吸收光谱特征峰,实际上还有很多其他化学键和官能团的吸收峰可供分析使用。
红外吸收光谱是一种非常有用的工具,可用于鉴定和定量分析不同物质。
通过观察红外光谱图中的吸收峰,我们可以获得有关被测物质结构和组成的重要信息,从而在科学研究和工业生产中得到广泛应用。
常见的红外光谱的吸收峰

常见的红外光谱的吸收峰红外光谱是一种常用的分析技术,可以用于研究物质的结构和成分。
在红外光谱中,不同的分子吸收不同波长的红外辐射,这些吸收峰通常对应着分子中特定的化学键或功能团。
下面是一些常见的红外光谱的吸收峰。
首先是羟基(-OH)的吸收峰,通常出现在3200-3600 cm^-1的高频区。
这是因为羟基中的氧原子与氢原子之间的振动引起了这一吸收峰。
另外,在亚甲基(C-H)、甲基(CH3)和亚甲基(CH2)的振动也会产生吸收峰,分别出现在3000-2800 cm^-1和1470-1375 cm^-1的区域。
接下来是羰基(C=O)的吸收峰,这是一个非常重要的功能团,可以出现在不同的波数区域。
酮和醛中的羰基通常在1700-1725 cm^-1的区域产生吸收峰,而酸和酯中的羰基则出现在1725-1750 cm^-1的区域。
此外,有机硫化合物中的硫-碳(S-C)键通常在550-600 cm^-1产生吸收峰,而硫-氢(S-H)键则在2500-2600 cm^-1产生吸收峰。
另外,氨基(-NH2)和芳香胺(-NH)通常在3500-3300 cm^-1的区域产生吸收峰。
此外,烷基和脂肪酸的C-H键通常产生多个吸收峰,出现在3000-2800 cm^-1的区域。
而含有芳香环的化合物通常在1600-1500 cm^-1的区域产生吸收峰。
这些是一些常见的红外光谱的吸收峰,当然不同的化合物可能产生不同的吸收峰,因此在解读红外光谱时需要结合化合物的其他特征和谱图进行分析。
红外光谱的分析是一项重要的化学技术,在有机化学、药物化学、材料科学等领域有着广泛的应用。
通过研究和理解红外光谱的吸收峰,我们可以更好地理解和解释分子的结构和性质。
红外光谱特征吸收峰讲解
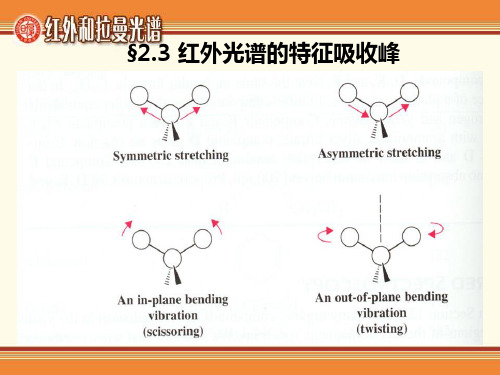
O R C Cl
伸缩(cm-1 ) 1715
1815~1785
3. 共轭效应
由于羰基与α 、β 不饱和双键共轭削弱了碳 氧双键,使羰基伸缩振动吸收频率减小
O R C R
O R C C C
R
O C C C
+
C=O伸缩(cm-1)
1715
1685~1670
4. 成键碳原子的杂化类型 化学键的原子轨道 s 成分越多,化学键 力常数 k 越大,吸收频率越大 C H C H C H sp sp2 3100 sp3 2900
C H
(C-H面外弯曲) 官能团 吸收频率(cm-1)
______________________________________________________
R
CH
CH2
1000和900
顺式 RCH CHR 反式
730~675
970~960 880 840~800
R2C CHR
R2C CH2
C
O
指纹区
1500~400 cm-1 吸收带多,整个分子振动转动引起的,反映整个 分子的特征。可用于鉴定两个化合物是否同一化合物
1500~400cm-1 (某些键的伸缩和C-H弯曲振动吸收)
官能团 吸收频率(cm-1) ______________________________________________ NO2 1565~1545和1385~1360 C O(醇,酚,羧酸,酯,酸酐) 1300~1000 胺 1350~1000 C N 伸缩 酰胺 1420~1400 CH3 1460和1380 (C-H面内弯曲) CH2 1465(C-H面内弯曲) 1340(C-H面内弯曲)
红外光谱吸收峰值

红外光谱吸收峰值
红外光谱是一种常用的分析技术,可以用于物质的结构鉴定、功能群的确定以及化合物的定量分析。
不同的化学键和功能团在红外光谱中会表现出特定的吸收峰,以下是一些常见的红外光谱吸收峰值的示例:
1.羰基吸收峰:C=O键通常在波数范围在1600-1800 cm^-1
处出现。
酮和醛通常在1710-1740 cm^-1处吸收,而羧酸和酰氯的羰基吸收位于1700-1800 cm^-1。
2.羧酸吸收峰:羧酸的羧基会在2500-3500 cm^-1附近出现
宽而强烈的吸收峰,称为羧酸的O-H伸缩振动。
3.羧酸盐吸收峰:羧酸盐的COO-官能团通常在1300-1600
cm^-1附近显示出C=O拉伸振动峰。
4.烷基(碳氢化合物)吸收峰:烷基的C-H键通常会在
2800-3200 cm^-1范围内显示吸收峰。
5.羟基吸收峰:羟基通常在3200-3600 cm^-1之间显示广泛
的吸收峰。
这些只是一些常见的红外光谱吸收峰值示例,不同化合物的红外光谱吸收峰的位置和强度会有所不同。
因此,在进行红外光谱分析时,需要参考已知的标准光谱或数据库来进行对比和鉴定。
总结 红外光谱频率与官能团特征吸收峰
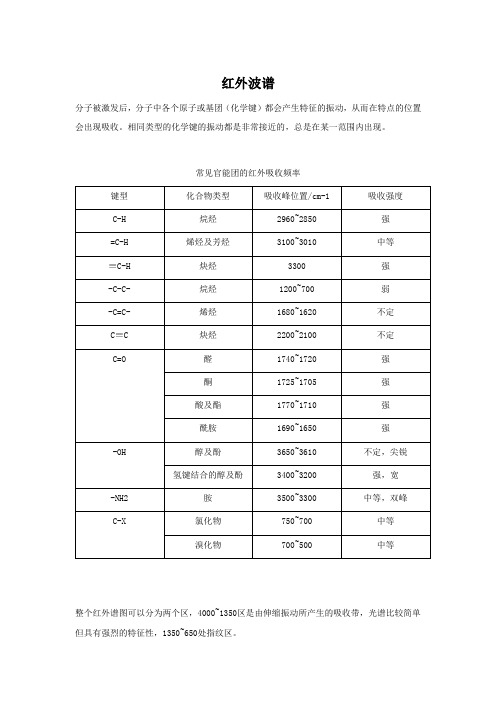
红外波谱分子被激发后,分子中各个原子或基团(化学键)都会产生特征的振动,从而在特点的位置会出现吸收。
相同类型的化学键的振动都是非常接近的,总是在某一范围内出现。
常见官能团的红外吸收频率整个红外谱图可以分为两个区,4000~1350区是由伸缩振动所产生的吸收带,光谱比较简单但具有强烈的特征性,1350~650处指纹区。
通常,4000~2500处高波数端,有与折合质量小的氢原子相结合的官能团O-H, N-H, C-H, S-H 键的伸缩振动吸收带,在2500-1900波数范围内常常出现力常数大的三件、累积双键如:- C≡C-,- C≡N, -C=C=C-, -C=C=O, -N=C=O等的伸缩振动吸收带。
在1900以下的波数端有-C=C-, -C=O, -C=N-, -C=O等的伸缩振动以及芳环的骨架振动。
1350~650指纹区处,有C-O, C-X的伸缩振动以及C-C的骨架振动,还有力常数较小的弯曲振动产生的吸收峰,因此光谱非常复杂。
该区域各峰的吸收位置受整体分子结构的影响较大,分子结构稍有不同,吸收也会有细微的差别,所以指纹区对于用已知物来鉴别未知物十分重要。
有机化学有机化合物红外吸收光谱σ伸缩振动,δ面内弯曲振动,γ面外弯曲振动一、烷烃饱和烷烃IR光谱主要由C-H键的骨架振动所引起,而其中以C-H键的伸缩振动最为有用。
在确定分子结构时,也常借助于C-H键的变形振动和C-C键骨架振动吸收。
烷烃有下列四种振动吸收。
1、σC-H在2975—2845 cm-1范围,包括甲基、亚甲基和次甲基的对称与不对称伸缩振动2、δC-H在1460 cm-1和1380 cm-1处有特征吸收,前者归因于甲基及亚甲基C-H 的σas,后者归因于甲基C-H的σs。
1380 cm-1峰对结构敏感,对于识别甲基很有用。
共存基团的电负性对1380 cm-1峰位置有影响,相邻基团电负性愈强,愈移向高波数区,例如,在CH3F中此峰移至1475 cm-1。
红外的吸收峰

红外吸收峰是红外光谱中的重要特征,其峰位等于分子或者基团的振动频率,强度大,是红外的主要吸收峰。
基频峰的峰位等于分子或者基团的振动频率,是红外光谱中最重要的吸收峰之一。
在红外光谱中,不同基团具有不同的振动频率,因此可以根据红外光谱的峰位置和强度来判断样品的基团组成和结构。
例如,烷烃的C-H伸缩振动在3000~2800 cm-1处出现较强的吸收峰,烯烃的C=C伸缩振动在1650~1600 cm-1处出现较强的吸收峰,芳香族化合物的苯环伸缩振动在1500~1450 cm-1处出现较强的吸收峰等。
需要注意的是,红外光谱的峰位置和强度受到多种因素的影响,如样品的状态、测试条件、仪器性能等,因此在进行红外光谱分析时需要注意这些因素的影响。
同时,由于不同基团可能存在多个振动频率,因此需要对红外光谱进行精细的分析和理解,以便得到准确的样品结构信息。
红外吸收光谱特征峰特别整理版

表15.1 典型有机化合物的重要基团频率(/cm-1)化合物基团X-H伸缩振动区叁键区双键伸缩振动区部分单键振动和指纹区烷烃-CH3asCH:2962±10(s) asCH:1450±10(m)sCH:2872±10(s)sCH:1375±5(s)-CH2-asCH:2926±10(s)CH:1465±20(m)sCH:2853±10(s)CH:2890±10(s)CH:~1340(w)烯烃CH:3040~3010(m) C=C:1695~1540(m) CH:1310~1295(m)CH:770~665(s)CH:3040~3010(m) C=C:1695~1540(w) CH:970~960(s)炔烃-C≡C-HCH:≈3300(m) C≡C:2270~2100(w)芳烃CH:3100~3000(变)泛频:2000~1667(w)C=C:1650~1430(m)2~4个峰CH:1250~1000(w) CH:910~665单取代:770~730(vs)≈700(s)邻双取代:770~735(vs) 间双取代:810~750(vs)725~680(m)900~860(m) ~对双取代:860~790(vs)醇类R-OHOH:3700~3200(变) OH:1410~1260(w)CO:1250~1000(s)OH:750~650(s) 酚类Ar-OHOH:3705~3125(s) C=C:1650~1430(m) OH:1390~1315(m)CO:1335~1165(s)脂肪醚R-O-R'CO:1230~1010(s)酮C=O:≈1715(vs)醛CH:≈2820,≈2720(w)双峰C=O:≈1725(vs)羧酸OH:3400~2500(m) C=O:1740~1690(m) OH:1450~1410(w)CO:1266~1205(m)酸酐C=O:1850~1880(s)C=O:1780~1740(s)CO:1170~1050(s)酯泛频C=O:≈3450(w) C=O:1770~1720(s) COC:1300~1000(s)胺-NH2NH2:3500~3300(m)双峰NH:1650~1590(s,m) CN(脂肪):1220~1020(m,w)CN(芳香):1340~1250(s)-NHNH:3500~3300(m) NH:1650~1550(vw) CN(脂肪):1220~1020(m,w)CN(芳香):1350~1280(s)酰胺asNH:≈3350(s) C=O:1680~1650(s) CN:1420~1400(m)sNH:≈3180(s) NH:1650~1250(s) NH2:750~600(m)NH:≈3270(s) C=O:1680~1630(s)NH+CN:1750~1515(m)CN+NH:1310~1200(m)C=O:1670~1630酰卤C=O:1810~1790(s)腈-C≡NC≡N:2260~2240(s)硝基化合物R-N02NO2:1565~1543(s) NO2:1385~1360(s)CN:920~800(m)Ar-NO2NO2:1550~1510(s) NO2:1365~1335(s)CN:860~840(s)不明:≈750(s)吡啶类CH:≈3030(w) C=C及C=N:1667~1430(m) CH:1175~1000(w) CH:910~665(s)嘧啶类CH:3060~3010(w) C=C及C=N:1580~1520(m) CH:1000~960(m) CH:825~775(m)*表中vs,s,m,w,vw用于定性地表示吸收强度很强,强,中,弱,很弱。
水在红外光谱中出现的吸收峰数目

水在红外光谱中出现的吸收峰数目
水在红外光谱中出现的吸收峰数目取决于其分子结构和所使用的红外光谱范围。
一般来说,水分子在红外光谱中会出现多个吸收峰,这些峰主要集中在中红外区域(2.5-25μm)。
在中红外区域,水分子的主要吸收峰包括:
1.羟基(OH)伸缩振动,大约在3400-3200cm-1范围内,这是水分子最强的吸收峰之一。
2.羟基(OH)弯曲振动,大约在1640-1610cm-1范围内,这也是水分子比较强的吸收峰之一。
3.碳氢(C-H)伸缩振动,大约在2970-2840cm-1范围内,这是脂肪族化合物的主要吸收峰之一。
4.碳氢(C-H)弯曲振动,大约在1450-1300cm-1范围内,这也是脂肪族化合物的主要吸收峰之一。
除了以上主要的吸收峰外,水分子还可能存在其他较弱的吸收峰。
因此,具体的水红外光谱吸收峰数目可能会因实验条件和使用的光谱范围而有所不同。
红外吸收光谱特征峰特别整理版

表15.1 典型有机化合物的重要基团频率(/cm-1)化合物基团X-H伸缩振动区叁键区双键伸缩振动区部分单键振动和指纹区烷烃-CH3asCH:2962±10(s) asCH:1450±10(m)sCH:2872±10(s)sCH:1375±5(s)-CH2-asCH:2926±10(s)CH:1465±20(m)sCH:2853±10(s)CH:2890±10(s)CH:~1340(w)烯烃CH:3040~3010(m) C=C:1695~1540(m) CH:1310~1295(m)CH:770~665(s)CH:3040~3010(m) C=C:1695~1540(w) CH:970~960(s)炔烃-C≡C-HCH:≈3300(m) C≡C:2270~2100(w)芳烃CH:3100~3000(变)泛频:2000~1667(w)C=C:1650~1430(m)2~4个峰CH:1250~1000(w) CH:910~665单取代:770~730(vs)≈700(s)邻双取代:770~735(vs) 间双取代:810~750(vs)725~680(m)900~860(m) ~对双取代:860~790(vs)醇类R-OHOH:3700~3200(变) OH:1410~1260(w)CO:1250~1000(s)OH:750~650(s) 酚类Ar-OHOH:3705~3125(s) C=C:1650~1430(m) OH:1390~1315(m)CO:1335~1165(s)脂肪醚R-O-R'CO:1230~1010(s)酮C=O:≈1715(vs)醛CH:≈2820,≈2720(w)双峰C=O:≈1725(vs)羧酸OH:3400~2500(m) C=O:1740~1690(m) OH:1450~1410(w)CO:1266~1205(m)酸酐C=O:1850~1880(s)C=O:1780~1740(s)CO:1170~1050(s)酯泛频C=O:≈3450(w) C=O:1770~1720(s) COC:1300~1000(s)胺-NH2NH2:3500~3300(m)双峰NH:1650~1590(s,m) CN(脂肪):1220~1020(m,w)CN(芳香):1340~1250(s)-NHNH:3500~3300(m) NH:1650~1550(vw) CN(脂肪):1220~1020(m,w)CN(芳香):1350~1280(s)酰胺asNH:≈3350(s) C=O:1680~1650(s) CN:1420~1400(m)sNH:≈3180(s) NH:1650~1250(s) NH2:750~600(m)NH:≈3270(s) C=O:1680~1630(s)NH+CN:1750~1515(m)CN+NH:1310~1200(m)C=O:1670~1630酰卤C=O:1810~1790(s)腈-C≡NC≡N:2260~2240(s)硝基化合物R-N02NO2:1565~1543(s) NO2:1385~1360(s)CN:920~800(m)Ar-NO2NO2:1550~1510(s) NO2:1365~1335(s)CN:860~840(s)不明:≈750(s)吡啶类CH:≈3030(w) C=C及C=N:1667~1430(m) CH:1175~1000(w) CH:910~665(s)嘧啶类CH:3060~3010(w) C=C及C=N:1580~1520(m) CH:1000~960(m) CH:825~775(m)*表中vs,s,m,w,vw用于定性地表示吸收强度很强,强,中,弱,很弱。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
红外光谱吸收峰
物质的红外光谱是其分子结构的反映,谱图中的吸收峰与分子中各基团的振动形式相对应。
多原子分子的红外光谱与其结构的关系,一般是通过实验手段得到。
这就是通过比较大量已知化合物的红外光谱,从中总结出各种基团的吸收规律。
实验表明,组成分子的各种基团,如O-H、N-H、C-H、C=C、C=OH和C C等,都有自己的特定的红外吸收区域,分子的其它部分对其吸收位置影响较小。
通常把这种能代表及存在、并有较高强度的吸收谱带称为基团频率,其所在的位置一般又称为特征吸收峰。
≡物质的红外光谱是其分子结构的反映,谱图中的吸收峰与分子中各基团的振动形式相对应。
多原子分子的红外光谱与其结构的关系,一般是通过实验手段得到。
这就是通过比较大量已知化合物的红外光谱,从中总结出各种基团的吸收规律。
实验表明,组成分子的各种基团,如O-H、N-H、C-H、C=C、C=OH和C
一、基团频率区和指纹区
(一)基团频率区
中红外光谱区可分成4000 cm-1 ~1300 cm-1和1800cm-1 (1300 cm-1 )~ 600 cm-1两个区域。
最有分析价值的基团频率在4000 cm-1 ~ 1300 cm-1 之
间,这一区域称为基团频率区、官能团区或特征区。
区内的峰是由伸缩振动产生的吸收带,比较稀疏,容易辨认,常用于鉴定官能团。
在1800 cm-1 (1300 cm-1 )~600 cm-1 区域内,除单键的伸缩振动外,还有因变形振动产生的谱带。
这种振动与整个分子的结构有关。
当分子结构稍有不同时,该区的吸收就有细微的差异,并显示出分子特征。
这种情况就像人的指纹一样,因此称为指纹区。
指纹区对于指认结构类似的化合物很有帮助,而且可以作为化合物存在某种基团的旁证。
基团频率区可分为三个区域:
(1)4000 ~2500 cm-1 X-H伸缩振动区,X可以是O、H、C或S等原子。
O-H基的伸缩振动出现在3650 ~3200 cm-1 范围内,它可以作为判断有无醇类、酚类和有机酸类的重要依据。
当醇和酚溶于非极性溶剂(如CCl4),浓度于0.01mol. dm-3时,在3650 ~3580 cm-1处出现游离O-H基的伸缩振动吸收,峰形尖锐,且没有其它吸收峰干扰,易于识别。
当试样浓度增加时,羟基化合物产生缔合现象,O-H基的伸缩振动吸收峰向低波数方向位移,在3400 ~3200 cm-1 出现一个宽而强的吸收峰。
胺和酰胺的N-H伸缩振动也出现在3500~3100 cm-1
CH(不是炔烃)基的吸收基出现在2890 cm-1 附近,但强度很弱。
不饱和的C-H伸缩振动出现在3000 cm-1以上,以此来判别化合物中是否含有不饱和的C-H键。
苯环的C-H键伸缩振动出现在3030 cm-1附近,它的特征是强度比饱和的C-H浆稍弱,但谱带比较尖锐。
≡因此,可能会对O-H伸缩振动有干扰C-H的伸缩振动可分为饱和和不饱和的两种。
饱和的C-H伸缩振动出现在3000 cm-1以下,约3000~2800 cm-1,取代基对它们影响很小。
如-CH3 基的伸缩吸收出现在2960 cm-1和2876 cm-1附近;- CH2基的吸收在2930 cm-1 和2850 cm-1附近;
不饱和的双键=C-H的吸收出现在3010~3040 cm-1范围内,末端= CH2的吸收出
现在3085 cm-1附近。
CH上的C-H伸缩振动出现在更高的区域(3300 cm-1 )附近。
≡叁键
(2)2500~1900 为叁键和累积双键区。
N基的吸收越弱,甚至观察不到。
≡N基越近,-C ≡N基吸收比较强而尖锐。
若分子中含有O原子,且O原子离-C ≡N基的缩振动在非共轭的情况下出现在2240~2260 cm-1附近。
当与不饱和键或芳香核共轭时,该峰位移到2220~2230 cm-1附近。
若分子中含有C、H、N原子,-C ≡C-R,因为分子是对称,则为非红外活性。
-C ≡C-R出现在2190~2260 cm-1附近。
如果是R-C ≡-C 'CH的伸缩振动出现在
2100~2140 cm-1附近,R≡C-R两种类型,R-C≡-C 'CH和R≡N等等叁键的伸缩振动,以及-C =C=C、-C=C=O等累积双键的不对称性伸缩振动。
对于炔烃类化合物,可以分成R-C≡C、-C≡主要包括-C
(3)1900~1200 cm-1为双键伸缩振动区
该区域重要包括三种伸缩振动:
①C=O伸缩振动出现在1900~1650 cm-1,是红外光谱中很特征的且往往是最强的吸收,以此很容易判断酮类、醛类、酸类、酯类以及酸酐等有机化合物。
酸酐的羰基吸收带由于振动耦合而呈现双峰。
②C=C伸缩振动。
烯烃的C=C伸缩振动出现在1680~1620cm-1,一般很弱。
单核芳烃的C=C伸缩振动出现在1600 cm-1和1500 cm-附近,有两个峰,这是芳环的骨架结构,用于确认有无芳核的存在。
③苯的衍生物的泛频谱带,出现在2000~1650 cm-1范围,是C-H面外和C=C面内变形振动的泛频吸收,虽然强度很弱,但它们的吸收面貌在表征芳核取代类型上是有用的。
(二)指纹区
C-H对称弯曲振动,对识别甲基十分有用,C-O的伸缩振动1300~1000 cm-1 ,是该区域最强的峰,也较易识别。
δ1375 cm-1的谱带为甲基的≈1. 1800(1300)~900 cm-1区域是C-O、C-N、C-F、C-P、C-S、P-O、Si-O等单键的伸缩振动和C=S、S=O、P=O等双键的伸缩振动吸收。
其中
2.900~650 cm-1区域的某些吸收峰可用来确认化合物的顺反构型。
例如,烯烃的=C-H面外变形振动出现的位置,很大程度上决定于双键的取代情况。
对于RCH=CH2结构,在990 cm-1和910 cm-1出现两个强峰;为RC=CRH结构是,其顺、反构型分别在690 cm-1和970 cm-1出现吸收峰,可以共同配合确定苯环的取代类型。
二、常见官能团的特征吸收频率
基团频率主要是由基团中原子的质量和原子间的化学键力常数决定。
然而,分子内部结构和外部环境的改变对它都有影响,因而同样的基团在不同的分子和不同的外界环境中,基团频率可能会有一个较大的范围。
因此了解影响基团频率的因素,对解析红外光谱和推断分子结构都十分有用。
影响基团频率位移的因素大致可分为内部因素和外部因素。
内部因素:
1. 电子效应
包括诱导效应、共轭效应和中介效应,它们都是由于化学键的电子分布不均匀引起的。
(1)诱导效应(I 效应)
由于取代基具有不同的电负性,通过静电诱导作用,引起分子中电子分布的变化。
从而改变了键力常数,使基团的特征频率发生了位移。
例如,一般电负性大的基团或原子吸电子能力强,与烷基酮羰基上的碳原子数相连时,由于诱导效应就会发生电子云由氧原子转向双键的中间,增加了C=O键的力常数,使C=O的振动频率升高,吸收峰向高波数移动。
随着取代原子电负性的增大或取代数目的增加,诱导效应越强,吸收峰向高波数移动的程度越显著。
(2)中介效应(M效应)
当含有孤对电子的原子(O、S、N等)与具有多重键的原子相连时,也可起类似的共轭作用,称为中介效应。
由于含有孤对电子的原子的共轭作用,使C=O上的电子云更移向氧原子,C=O双键的电子云密度平均化,造成C=O键的力常数下降,使吸收频率向低波数位移。
对同一基团,若诱导效应和中介效应同时存在,则振动频率最后位移的方向和程度,取决于这两种效应的结果。
当诱导效应大于中介效应时,振动频率向高波数移动,反之,振动频率向低波数移动。
2 . 氢键的影响
氢键的形成使电子云密度平均化,从而使伸缩振动频率降低。
游离羧酸的C=O键频率出现在1760 cm-1 左右,在固体或液体中,由于羧酸形成二聚体,C=O键频率出现在1700 cm-1 。
分子内氢键不受浓度影响,分子间氢键受浓度影响较大。
3. 振动耦合
当两个振动频率相同或相近的基团相邻具有一公共原子时,由于一个键的振动通过公共原子使另一个键的长度发生改变,产生一个“微扰”,从而形成了强烈的振动相互作用。
其结果是使振动频率发生感变化,一个向高频移动,另一个向低频移动,谱带分裂。
振动耦合常出现在一些二羰基化合物中,如,羧酸酐。
(4)Fermi共振
当一振动的倍频与另一振动的基频接近时,由于发生相互作用而产生很强的吸
收峰或发生裂分,这种现象称为Fermi共振。
外部因素
外部因素主要指测定时物质的状态以及溶剂效应等因素。
同一物质的不同状态,由于分子间相互作用力不同,所得到光谱往往不同。
分子在气态时,其相互作用力很弱,此时可以观察到伴随振动光谱的转动精细结构。
C-H为1742 cm-1 ,而在液态时为1718 cm-1 。
在溶液中测定光谱时,由于溶剂的种类、溶剂的浓度和测定时的温度不同,同一种物质所测得的光谱也不同。
通常在极性溶剂中,溶质分子的极性基团的伸缩振动频率随溶剂极性的增加而向低波数方向移动,并且强度增大。
因此,在红外光谱测定中,应尽量采用非极性的溶剂。
液态和固态分子间作用力较强,在有极性基团存在时,可能发生分子间的缔合或形成氢键,导致特征吸收带频率、强度和形状有较大的改变。
例如,丙酮在气态时的。
