法罗培南钠胶囊
50种抗生素DDD值最新版本
0.6
3
氨苄西林舒巴坦钠 3g/支
支
3
2
哌拉西林舒巴坦钠 1.25g/支
支
1.25
14
哌拉西林三唑(他唑)巴坦钠 4.5g/支
支
4.5
14
磺苄西林钠针 1g/支
支
1
15
氟氯西林钠针 0.25g/支
支
0.25
2
阿莫西林/氟氯西林 0.5
支
0.5
5
第一代头孢菌素类
头孢氨苄 0.25g*30s/盒
片
0.25
支
2
4
头孢哌酮舒巴坦钠(舒普深) 1g/支
支
1
4
头孢他啶针 0.5g/支
支
0.5
4
头孢他啶针(复达欣) 1g/支
支
1
4
头孢地嗪钠针 0.5/支
支
0.5
2
头孢米诺针 0.5/支
支
0.5
2
拉氧头孢针 0.25/支
支
0.25
4
其他β-内酰胺类
氨曲南针 0.5g/支
支
0.5
4
氨曲南针 1g/支
支Байду номын сангаас
1
4
头孢美唑钠针 0.5g/支
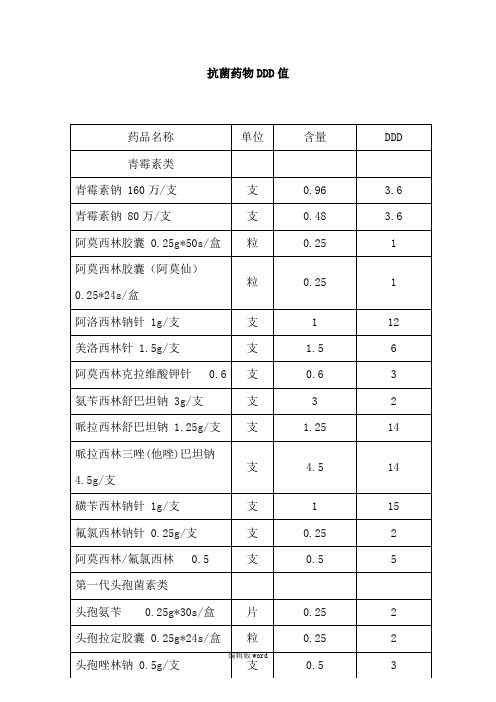
抗菌药物DDD值
药品名称
单位
含量
DDD
青霉素类
青霉素钠 160万/支
支
0.96
3.6
青霉素钠 80万/支
支
0.48
3.6
阿莫西林胶囊 0.25g*50s/盒
粒
0.25
1
阿莫西林胶囊(阿莫仙)0.25*24s/盒
粒
法罗培南钠的合成

法罗培南钠的合成
法罗培南钠是一种广谱抗生素,被广泛应用于治疗各种感染症状。
其合成的过程相对繁琐,但十分重要。
下面我们就从以下几个方面来介绍法罗培南钠的合成。
一、前体物的合成
法罗培南钠的合成需要使用到前体物,其中一种重要的前体物是3-氨基苯甲酸。
3-氨基苯甲酸的合成需要将苯甲酸与亚硝氢反应后,再经过氢化反应,得到3-氨基苯甲酸。
这个过程中涉及到有机合成化学,需要有较高的专业知识和技术能力。
二、法罗培南的合成
法罗培南的合成分为两步,第一步是通过酯化反应将3-氨基苯甲酸和4-硝基苯基酯合成为酯化物,第二步是通过水解反应得到法罗培南。
具体反应如下:
1. 酯化反应
将3-氨基苯甲酸和4-硝基苯基酯在硫酸存在下加热,发生酯化反应,得到N-(4-硝基苯基)-3-(苯甲酸基)-L-丙氨酰胺酯(FPA 酯)。
2. 水解反应
将FPA酯在碳酸氢钠的存在下加热,发生水解反应,得到法罗培南。
三、法罗培南钠的合成
将法罗培南与钠离子结合,就可以得到法罗培南钠。
法罗培南钠的合成需要使用到碳酸氢钠和氢氧化钠,这些化学试剂的浓度和添加方法等需要精确控制。
总的来说,法罗培南钠的合成需要有机合成化学、化学分析和控制等多方面的技术支持,需要有独特的实验室和设备条件。
虽然合成过程繁琐,但是法罗培南钠的应用范围广泛,特别是在医学领域有着重要的地位和作用。
新型青霉烯类抗生素法罗培南钠

新型青霉烯类抗生素法罗培南钠
周庆英;徐丽洒;孙勇
【期刊名称】《中国新药杂志》
【年(卷),期】2008(17)4
【摘要】法罗培南钠(faropenem sodium)是青霉烯类中惟一既可口服又可注射
的抗生素,它经由阻止细菌细胞壁合成而显现抗菌、杀菌作用,具有独特的药动学性质.其抗菌谱广泛,包括需氧G+菌、需氧G-菌及厌氧菌.在呼吸道、泌尿道、妇产科、口腔科以及眼科感染上已取得了良好的效果.现对法罗培南钠的作用机制、抗菌活性、毒理学、药动学及临床研究进展进行综述.
【总页数】4页(P345-347,352)
【作者】周庆英;徐丽洒;孙勇
【作者单位】青岛大学医学院药学系,青岛,266021;山东省临沂市药品检验所,临沂,276001;青岛大学医学院药学系,青岛,266021;青岛大学医学院药学系,青
岛,266021
【正文语种】中文
【中图分类】R978.1
【相关文献】
1.新型碳青霉烯类抗生素多尼培南的药效分析 [J], 顾觉奋;王婧
2.口服青霉烯类抗生素法罗培南钠的药理作用与临床评价 [J], 黄剑峰
3.新型碳青霉烯类抗生素厄他培南 [J], 来小丹;刘松青;林彩
4.新型青霉烯类抗生素——法罗培南 [J], 赵一飞;冯昱;叶俊杰
5.新型金属β内酰胺酶抑制剂ME1071体外增强碳青霉烯类抗生素对产金属β内酰胺酶铜绿假单胞菌的抗菌活性研究 [J], Ishii Y;Eto M;Mano Y;王鹏(摘译);王明贵(审校)
因版权原因,仅展示原文概要,查看原文内容请购买。
法罗培南钠片说明书

法罗培南钠片说明书【药品名称】通用名:法罗培南钠片英文名:Faropenem Sodium Tablets汉语拼音:Faluopeinanna Pian【性状】本品为白色薄膜衣片,去除薄膜衣呈白色至淡黄色。
【适应症】由葡萄球菌、链球菌、肺炎球菌、肠球菌、卡他莫拉克氏菌、大肠杆菌、柠檬酸杆菌、克雷白氏杆菌、肠杆菌、奇异变形杆菌、流感嗜血杆菌、消化链球菌、痤疮丙酸杆菌、拟杆菌等敏感菌所致的下列感染性疾病:1、泌尿系统感染:肾盂肾炎、膀胱炎、前列腺炎、睾丸炎;2、呼吸系统感染:咽喉炎、扁桃体炎、急慢性支气管炎、肺炎、肺脓肿(肺脓疡病);3、子宫附件炎、子宫内感染、前庭大腺炎;4、浅表性皮肤感染症、深层皮肤感染症,痤疮(伴有化脓性炎症);5、淋巴管炎、淋巴结炎、乳腺炎、肛周脓肿、外伤、烫伤和手术创伤等继发性感染;6、泪囊炎、麦粒肿、睑板腺炎、角膜炎(含角膜溃疡);7、外耳炎、中耳炎、鼻窦炎;8、牙周组织炎、牙周炎、颚炎。
【用法用量】应由医生根据感染类型、严重程度及病人的具体情况适当增减本药剂量。
推荐用法用量如下:对浅表性皮肤感染症、深层皮肤感染症、淋巴结炎、慢性脓皮病,乳腺炎、肛周脓肿、外伤、烫伤和手术创伤等(浅表性)二次感染,咽喉炎、急慢性支气管炎、扁桃体炎,子宫附件炎、子宫内感染、前庭大腺炎,眼睑炎、睑腺炎、泪囊炎、睑板腺炎、角膜炎、角膜溃疡,外耳炎、牙周组织炎、牙周炎、颚炎等,口服法罗培南钠片,成人患者通常一次150-200mg,一日3次。
对肺炎、肺脓肿,肾盂肾炎、膀胱炎(除单纯性膀胱炎外)、前列腺炎、睾丸炎、中耳炎、鼻窦炎等,口服法罗培南钠片,成人患者通常一次200-300mg,一日3次。
【不良反应】日本进行的临床试验中,总计2207例患者中被报告有127例(5.8%)发生不良反应。
其中主要不良反应为:腹泻,55件(2.5%);腹痛,19件(0.9%);稀便,15件(0.7%);发疹,13件(0.6%);恶心,12件(0.5%)等。
法罗培南钠片疗程大概是多少?

法罗培南钠片疗程大概是多少?
药物治疗不同的疾病,就需要有不同的治疗方案,而药物就需要按疗程服用才好,而不是随意用药,那么,法罗培南钠片疗程大概是多少?
法罗培南钠片正常健康成人空腹时单次口服本药150、300或600mg,约1~1.5小时后分别达到最高血浆浓度2.4、6.2或7.4μg/ml。
本药半减期约为1小时,且与用药剂量无关。
正常健康成人餐后单次口服本药300mg,发现达到最大血浆浓度时间较空腹用药时延迟约1小时,最大血浆浓度、半减期及血浆浓度一时间曲线下面积(AU C)几乎均未出现差异。
【注意事项】
大家在用药的时候,药物说明书里面有三种标识,一般要注意一下:
1.第一种就是禁用,就是绝对禁止使用。
2.第二种就是慎用,就是药物可以使用,但是要密切关注患者口服药以后的情况,一旦有不良反应发生,需要马上停止使用。
3.第三种就是忌用,就是说明药物在此类人群中有明确的不良反应,应该是由医生根据病情给出用药建议。
如果一定需要这种药物,就可以联合其他的能减轻不良反应的药物一起服用。
大家以后在服用药物的时候,多留意说明书,留意注意事项,避免不良反应的发生。
本文到此结束,谢谢大家!。
法罗培南钠片说明书_法罗培南钠片

法罗培南钠片说明书_法罗培南钠片法罗培南钠片(君迪)适用于敏感菌所引起的下述感染病症。
1.脓疱性痤疮、集簇性痤疮、疖、痈、传染性脓疱病、丹毒、蜂窝织炎、淋巴管炎、化脓性甲沟炎、皮下脓肿、汗腺炎、慢性脓皮病。
下面是店铺整理的法罗培南钠片说明书_法罗培南钠片,欢迎阅读。
目录法罗培南钠片商品介绍通用名:法罗培南钠片生产厂家: 鲁南贝特制药有限公司批准文号:国药准字H20133145药品规格:0.2g_12片药品价格:¥237元法罗培南钠片说明书【通用名称】法罗培南钠片【商品名称】法罗培南钠片(君迪)【英文名称】FaropenSodiumTablets【拼音全码】FaLuoPeiNanNaPian【主要成份】法罗培南钠。
【性状】法罗培南钠片为白色片。
【适应症/功能主治】法罗培南钠片适用于敏感菌所引起的下述感染病症。
1.脓疱性痤疮、集簇性痤疮、疖、痈、传染性脓疱病、丹毒、蜂窝织炎、淋巴管炎、化脓性甲沟炎、皮下脓肿、汗腺炎、慢性脓皮病。
2【规格型号】0.2g_12s【用法用量】1.咽喉炎、扁桃体炎和急性支气管炎、脓疱性痤疮、蜂窝织炎、淋巴管炎、乳腺炎、肛周脓肿、外耳炎、牙周组织炎等,成人口服法罗培南钠片每次150~200mg,每日3次。
2.肺炎、肺化脓、肾盂肾炎、膀胱炎(单纯性除外)、前列腺炎、附睾炎、中耳炎、鼻窦炎等,成人口服法罗培南钠片每次200~300mg,每日3次。
此外,根据年龄和症状进行适量增减。
【不良反应】不良反应发生率低,主要不良反应为腹泻、皮疹等,停药后即可恢复。
【禁忌】对法罗培南钠片过敏者禁用。
【注意事项】1.与健康成人相比,高龄者随年龄增加而肾功能降低,血药浓度半衰期延长,可能出现血药浓度持续较高。
2.高龄者可能出现伴随有泻痢、软便的全身状况恶化,应仔细观察,有该类症状出现时停用法罗培南钠片,进行适当处置。
3.高龄者可能出现因维生素K缺乏而引起的出血趋势。
4.孕妇及哺乳期妇女仅在治疗的益处高于其危险时服用法罗培南钠片。
法罗培南钠胶囊

法罗培南钠胶囊项目概况1、药品名称通用名:法罗培南钠胶囊化学名:(+)-(5R,6S)-6-[(1R)-1-羟基乙基]-7-氧代-3-[(2R)-四氢-2-呋喃基]-4-硫杂-1-氮杂双环[3.2.0]庚-2-烯-2-羧酸钠盐·水合物英文化学名: Sodium (+)-(5R,6S)-6-[(1R)-1-hydroxyethyl]-7-oxo-3-[(2R)-tetrahydro-2-furanyl]-4-thia-1-azabicyclo[3.2.0]hept-2-ene-2-carboxylate· hydrate 英文名:Faropenem Sodium Capsule汉语拼音名:Faluopeinan Na JiaonangCAS登录号:122547-49-3代号:ALP-201;SUN-5555;SY-5555;WY-49605商品名:待定化学结构式:分子式:C12H14NNaO5S· H2O分子量:352.342 命名依据与所属类别2.1命名依据根据“新药命名制定原则”,制剂的命名为原料药通用名加剂型,本品的原料药命名为“法罗培南钠”,故将其胶囊剂命名为法罗培南钠胶囊。
2.2 注册分类法罗培南钠由化学合成方法制得,为日本Suntory公司开发的抗菌药物,1997年在日本上市,已被《日本抗生物质医药品基准》(XIV版)收载,但尚未在我国国内上市销售,根据《药品注册管理办法》(暂行)的规定,本品属于化学药品注册分类第3(1)项。
立题目的与依据一、选题的目的与依据1928年,亚历山大·弗莱明发现了青霉素。
1938年,英国牛津大学病理学家弗洛里和德国生物化学家钱恩从期刊资料中找到了有关青霉素的文献。
1939年他们得到了英国和美国的有关组织和基金会的支持。
经过一年多的努力,弗洛里和钱恩终于提纯了青霉素的结晶。
1940年,青霉素时入临床试验阶段,经过对五位受试者的临床观察证明青霉素具的较好的效果。
法罗培南钠治疗呼吸道细菌性感染15例

法罗培南钠治疗呼吸道细菌性感染15例左鹏;熊盛道;熊维宁;徐永健;刘瑾;赵建平;马静;周敏【期刊名称】《医药导报》【年(卷),期】2007(26)12【摘要】目的观察法罗培南钠片治疗呼吸道细菌性感染的有效性和安全性.方法采用随机、双盲、双模拟平行对照试验设计,将入选的呼吸道感染患者30例随机分为治疗组和对照组各15例.治疗组给予法罗培南钠片0.2 g,potid,同时服用头孢克洛模拟胶囊0.25 g,tid;对照组给予头孢克洛胶囊0.25 g,po,tid,同时服用法罗培南钠模拟片0.2 g,tid,疗程均为5~10 d.观察两组临床疗效和安全性.结果治疗组和对照组总治愈率分别为50.0%与61.5%,有效率分别为100.0%和92.3%,细菌清除率均为91.7%.治疗组和对照组与药物相关的不良反应发生率均为0.以上结果两组间比较差异无显著性.结论法罗培南钠片治疗呼吸道细菌性感染疗效确切,安全性好.【总页数】3页(P1456-1458)【作者】左鹏;熊盛道;熊维宁;徐永健;刘瑾;赵建平;马静;周敏【作者单位】华中科技大学同济医学院附属同济医院呼吸内科,武汉,430030;华中科技大学同济医学院附属同济医院呼吸内科,武汉,430030;华中科技大学同济医学院附属同济医院呼吸内科,武汉,430030;华中科技大学同济医学院附属同济医院呼吸内科,武汉,430030;华中科技大学同济医学院附属同济医院呼吸内科,武汉,430030;华中科技大学同济医学院附属同济医院呼吸内科,武汉,430030;华中科技大学同济医学院附属同济医院呼吸内科,武汉,430030;华中科技大学同济医学院附属同济医院呼吸内科,武汉,430030【正文语种】中文【中图分类】R978.11;R969.4【相关文献】1.法罗培南钠片与头孢呋辛酯片治疗泌尿系统细菌性感染对照研究 [J], 邓蕙;张道友;黄文祥;刘成伟;周向东;张唯力;余英杰;朱卫民;张艮甫;章辉2.法罗培南钠片和头孢呋辛酯片治疗呼吸道细菌性感染成本-效果分析 [J], 孟雅杰;李应瑞;侯栩3.法罗培南钠片治疗细菌性感染的随机双盲对照临床研究 [J], 杨春;姚云清;刘成伟4.法罗培南钠片与头孢呋辛酯片治疗呼吸道细菌性感染135例 [J], 邓蕙;张道友;黄文祥;刘成伟;周向东;张唯力;余英杰;朱卫民;张艮甫;章辉5.法罗培南钠治疗急性细菌性呼吸道感染疗效观察 [J], 常越;徐纪;杨超;韩一平;李强因版权原因,仅展示原文概要,查看原文内容请购买。
法罗培南钠片医治细菌性感染的随机双盲对照临床研究

法罗培南钠片医治细菌性感染的随机双盲对照临床研究【摘要】目的评判国产法罗培南钠片医治细菌性感染的临床疗效与平安性。
方式采纳多中心、双盲、随机对如实验设计,以头孢克洛为对照药,两组均口服,每次2片,tid,疗程5~10d。
结果本研究共纳入60例,法罗培南组和头孢克洛组各30例,其中法罗培南组及头孢克洛组纳入ITT分析均为30例,PP分析别离为28和30例。
疗程终止时,呼吸系统PP人群中,法罗培南组与头孢克洛组医治后总痊愈率和有效率别离为71.43%与47.67%和92.86%与93.33%,泌尿道PP人群中,法罗培南组与头孢克洛组总痊愈率和有效率别离为85.71%与73.33%和100%与93.33%。
疗程终止时两组细菌清除率均别离为83.33%和79.17%,法罗培南组和头孢克洛组的不良反映发生率别离为10.71%和20%,要紧表现为恶心、呕吐、头晕、皮疹、腹泻等。
以上结果两组比较无统计学不同(P>0.05)。
结论国产法罗培南钠片医治呼吸道感染和泌尿道感染疗效确切,平安性较好。
【关键词】法罗培南钠片头孢克洛细菌性感染随机双盲对照A multicenter, randomized controlled clinical study onABSTRACT Objective To evaluate the clinical efficacy and safety of domestic faropenem in the treatment of bacterialinfections. Methods We designed a multicenter, double blind, randomized controlled clinical trial and used cefaclor as control. Both groups were given 2 tablets three times daily, orally for 5 to 10 days. Results A total of 60 patients were enrolled in the study. Two groups were both distributed 30 patients. There was 30 patients who enrolled in ITT (intention to treat analysis) and the group of faropenem was 28 and the group of cefaclor was 30 in PP(per protocol). The cure and effective rates were 71.43% vs 47.67% and 92.86% vs 93.33% in the per protocol patients with respiratory infections, the cure and effective rates were 85.71% vs 73.33% and 100% vs 93.33% in the per protocol patients with urinary infections; the bacterial eradication rate were 83.33% vs 79.17%; the adverse events rate were 10.71% vs 20%, the adverse events were nausea, vomit, dizziness, rash, diarrhea and so on. There were no significant differences between the two groups (P>0.05). Conclusions Domestic faropenem is effective and safe for the treatment of bacterial infections.KEY WORDS Faropenem sodium tablets; Cefaclor; Bacterial infection; Randomized controlled clinical study法罗培南是青霉烯母核的2位上接有一个四氢呋喃基团,化学结构较稳固,它对需氧和厌氧的革兰阳性菌、革兰阴性菌显示出广谱的抗菌活性,专门是对耐药的葡萄球菌、肠球菌等革兰阳性菌和拟杆菌等厌氧菌的活性都优于现有的口服抗菌药。
2023年关于法罗培南解析

(8)横纹肌溶解症(发生率不明):有时可能发生以肌肉疼痛、肌无力感、CK(CPK)上升、血中和尿中肌红蛋白上升等为特征的横纹肌溶 解症且还有可能伴之发生急性肾功能不全等严重肾功能损害。一旦出现这些症状即应中止用药并采取适当处置措施。
( 6 ) 肝 功 能 不 全 。 黄 疸 ( 0 . 1 % 不 到 ) : 因 有 时 可 能 发 生 A S T ( G O T ) 、 A LT ( G P T ) 、 A L P 等 升 高 及 出 现 黄 疸 , 故 应 通 过 定 期 检 查 等 予 以 充 分观察。一旦确认发生异常,即应中止用药并采取适当处置措施。
2、遗传毒性:Ames试验、培养细胞基因突变试验和染色体异常试验、小鼠微核试验结果均未发现法罗培南钠具有致突变性。
3、生殖毒性:大鼠在器官形成期经口给药320、800和2000mg/kg,在妊娠前和妊娠初期及围产期、哺乳期经口给药80、 360和1620mg/kg,结果除了见大鼠摄食量发生轻度变化外,总体状态和体重均未变化。试验显示法罗培南钠对母鼠生殖功 能、胎鼠和新生鼠没有影响,且未发现药物存在致畸性。家兔在器官形成期经由静脉给药50、100和200mg/kg,结果 100mg/kg以上给药组出现软便、腹泻和流产;200mg/kg给药组发生母兔死亡、胎兔死亡数量增加和胎兔轻度发育迟缓,但 试验未见法罗培南钠存在致畸性。
药物相互作用
1、亚胺培南-西司他丁钠动物试验(大鼠)报告:可导致本药血药浓度提高。
2、西司他丁钠抑制代谢酶所致呋塞米动物试验(狗)报告:本药肾毒性增加。
3、有报告称,丙戊酸钠和碳青霉烯类药物如麦罗培南、帕尼培南、亚安培南等并用可使丙戊酸血 药浓度降低,由此导致癫痫发作复发。
法罗培南钠治疗泌尿系统感染疗效评价

显效 19( 32.76) 12( 20.34)
进步 3( 5.17) 9( 15.25)
总有效率 55( 94.83) 50( 84.75)
2.2 细菌 学 疗 效 分 析 法 罗 培 南 钠 组 与 头 孢 克 洛 组 细 菌 清 除率比较差异无统计学意义( χ2 = 0.199 0, P > 0.05) 。见表 2。 法罗培南钠组 8 例无菌落发育, 头孢克洛组 11 例无菌落发 育, 故无细菌学效果评价。
3 讨论 泌尿系感染最常见的致病菌是革兰阴性杆菌, 其中以大
肠杆菌最为常见, 其次是变形杆菌、克雷伯杆菌、产碱杆菌和 铜 绿 假 单 孢 菌[1]。 大 肠 杆 菌 最 常 见 于 无 症 状 菌 尿 、非 复 杂 性 尿 路 感 染 和 首 次 发 生 的 尿 路 感 染 患 者[2]。法 罗 培 南 钠 作 用 机 制 是 阻断细菌细胞壁的合成与青霉素结合蛋白具有很强的结合 性, 从而发挥杀菌作用。本研究结果表明法罗培南钠和头孢 克洛抗生素治疗泌尿系感染都取得了满意的临床疗效和细 菌学疗效, 2 组之 间 在 药 效 及 安 全 性( 不 良 反 应) 方 面 差 异 均 无统计学意义, 说明法罗培南钠不失为治疗敏感菌泌尿系统 感染可选药物和对常用抗感染药物耐药的难治性泌尿系统 感染的首选药物之一。
( 2006-09-18 收稿 2007-03-13 修回) ( 本文编辑 孙东建)
作者单位: 300211 天津医科大学第二医院肾内科
1 对象与方法 1.1 研 究 对 象 本 研 究 117 例 患 者 为 我 院 2005 年 9 月— 2006 年 5 月就诊且 确 诊 为 泌 尿 系 感 染 的 患 者 , 将 其 随 机 、双 盲分为法罗培南钠组 58 例和头孢克洛组 59 例。法罗培南钠 组 男 20 例 , 女 38 例 ; 年 龄 17~65 岁 , 平 均( 41 ±13) 岁 ; 其 中 急 性 肾 盂 肾 炎 15 例 , 慢 性 肾 盂 肾 炎 急 性 发 作 18 例 , 急 性 膀 胱炎 15 例, 其他 10 例。头孢克洛组男 18 例, 女 41 例; 年龄 15~67 岁 , 平 均( 38 ±15) 岁 ; 其 中 急 性 肾 盂 肾 炎 18 例 , 慢 性 肾盂肾炎急性发作 20 例, 急性膀胱炎 13 例, 其他 8 例。2 组 患 者 在 年 龄( t = 1.121) 、性 别( χ2 = 0.211) 及 病 种( χ2 = 0.501) 分布方面差异无统计学意义( 均 P > 0.05) , 具有可比性。 1.2 治疗方法 法 罗 培 南 钠 组 : 法 罗 培 南 钠 片( 山 东 鲁 南 贝 特 制 药 有 限 公 司) 200 mg/次 , 3 次/d。 疗 程 5~10 d; 头 孢 克 洛 组: 头孢克洛胶囊( 海南海口市制药厂) 250 mg/次, 3 次/d。疗 程 5~10 d。 1.3 疗 效 判 定 治 疗 前 、治 疗 第 4 天 、治 疗 结 束 后 第 1 天 , 详 细 观 察 患 者 症 状 、体 征 。血 尿 常 规 、肝 、肾 功 能 、细 菌 学 检 查 于用药前及停药后各检查 1 次。根据上述结果综合评价以确 定临床疗效, 分为痊愈、显效 、进 步 、无 效 4 级 。 痊 愈 : 症 状 、 体征、化验及病原菌检查均恢复正常。显效: 上述 4 项中有一 项未恢复正常。进步: 上述 4 项中有二项或三项未恢复正常。 无效: 上述 4 项均未 恢 复 正 常 或 用 药 72 h 后 病 情 有 所 加 重 。 痊愈和显效合计为有效。 1.4 细菌学疗 效 判 断 标 准 清 除 : 治 疗 结 束 后 原 有 致 病 菌 消失。部分清除: 原有多种致病菌中有几种已被清除。未清 除: 治疗结束后原有的致病菌依然存在。替换: 在治疗结束后 第 1 天分离到一种新的致病菌, 但没有任何临床症状, 不需 要进行治疗。 1.5 统计学方 法 使 用 SPSS 10.0 软 件 进 行 统 计 学 分 析 , 计 数资料行 χ2 检验和确切概率法, 计量资料比较用 t 检验。
口服青霉烯类抗生素法罗培南钠的药理作用与临床评价_黄剑峰

口服青霉烯类抗生素法罗培南钠的药理作用与临床评价黄剑峰【摘要】 法罗培南钠是具有青霉烯基本骨架的青霉烯类口服抗生素,经由阻止细菌细胞壁合成而发挥抗菌、杀菌作用。
临床研究表明,法罗培南钠对各种青霉素结合蛋白(P B P )具有高亲和性,特别是对细菌增殖做必需的高分子P B P 呈现很高的亲和性,适用于成人和儿童由单一或多种对法罗培南钠敏感的细菌引起的感染。
现综述其药理作用、药动学及临床评述。
【关键词】 法罗培南钠;药理作用;青霉烯;抗生素 作者单位:550003贵州省骨科医院药剂科 法罗培南钠(F a r o p e n e m s o d i u m T a b l e t s ,化学名称:(5R ,6S )-6-[(1R )-1-羟基乙基]-7-氧代-3-[(2R )-四氢呋喃-2-基]-4-硫代-1-氮杂二环[3、2、0]庚-2-烯-2-羧酸单钠2.5水合物);化学结构式为:法罗培南钠是全球第一个口服青霉烯类抗生素,由江苏正大天晴药业股份有限公司生产,2006年上市以来,对临床各科感染,取得了很好的治疗效果。
现对法罗培南钠的药理作用、药动学与临床应用进行综述。
1 药理作用本品为具青霉烯基本骨架的青霉烯类口服抗生素,它经由阻止细菌细胞壁合成而发挥抗菌、杀菌作用。
对各种青霉素结合蛋白(P B P )具有高亲和性,特别是对细菌增殖所必需的高分子P B P 呈现高亲和性。
体外实验表明法罗培南钠对需氧性革兰氏阳性菌、需氧性革兰氏阴性菌及厌氧菌具广泛抗菌谱;尤其是对需氧性革兰氏阳性菌中的葡萄球菌、链球菌、肺炎球菌、肠球菌,需氧性革兰氏阴性菌中的柠檬酸杆菌、肠杆菌、百日咳噬血杆菌以厌氧菌中的消化链球菌、拟杆菌等显示较强杀菌效力。
并显示对各种细菌产生β-内酰胺酶稳定,对β-内酰胺霉产生菌具有较强抗菌活性。
2 药动学正常健康成人空腹时单次口服本药150、300、或600m g ,约1~1.5h 后分别达到最高血浆浓度2、4、6.2或7.4μg /m l 。
小儿法罗培南钠颗粒说明书

20170308:说明:依据原研单位最新版(第15版,2011年颁布)干糖浆说明书核定,包括了儿童的数据。
20171225:【药理毒理】依据药理毒理专业核定版确定核准日期:修改日期:小儿法罗培南钠颗粒说明书请仔细阅读说明书并在医师指导下使用【药品名称】通用名称:小儿法罗培南钠颗粒商品名称:菲若姆英文名称:Pediatric Faropenem Sodium Granules汉语拼音:Xiao’er Faluopeinanna Keli【成份】本品主要成份为法罗培南钠。
其化学名称:(5R,6S)-6-[(R)-1-羟乙基]-7-氧代-3-[(R)-2-四氢呋喃基]-4-硫杂-1-氮杂双环[3.2.0]庚-2-烯-2-羧酸钠盐二倍半水合物。
化学结构式:2.5H2OH分子式:C12H14NNaO5S·2.5H2O分子量:352.34【性状】本品为橙色颗粒。
【适应症】本品为颗粒剂,主要用于对法罗培南敏感的细菌所致的儿童下列感染性疾病的治疗。
1、儿童患者本品适用于对法罗培南敏感的葡萄球菌属、链球菌属、肺炎链球菌、肠球菌属、卡他莫拉克氏菌、大肠杆菌、枸橼酸杆菌、克雷伯氏杆菌、奇异变形杆菌、流感嗜血杆菌及百日咳菌引起的儿童下列感染性疾病的治疗:浅表皮肤及皮肤组织感染、深层皮肤及皮肤组织感染、淋巴管炎、淋巴结炎、慢性皮肤化脓性疾病、咽喉炎、扁桃体炎、急性支气管炎、肺炎、膀胱炎、肾盂肾炎、中耳炎、鼻窦炎、牙周组织炎、猩红热、百日咳。
【规格】0.05g(按C12H15NO5S计算)。
【用法用量】1、用法将本品适量用水溶解后口服。
本品需临用时配制,配制后不能长时间放置,用水溶解后应迅速用药,必要时可放在冰箱内保存,但也应尽快使用。
2、用量应由医生根据感染类型、严重程度及病人的具体情况适当增减本药剂量。
为防止出现耐药菌株,原则上应做细菌敏感性试验,并在保证疗效的前提下使用最短的疗程。
儿童推荐用量:通常,儿童每次5mg/kg,每日3次。
3“消炎抗菌”队伍中的新宠,你认识吗?

“消炎抗菌”队伍中的新宠,你认识吗?普天药械网--新品首发编者按:法罗培南钠是一种新的碳青霉烯类药物,属非典型β-内酰胺类抗生素,通过其共价键与参与细胞壁合成的青霉素结合蛋白(PBP)结合而抑制细菌细胞壁的合成,使细菌胞壁缺损,菌体膨胀裂解,从而达到抗菌作用。
法罗培南钠胶囊本期,普天药械网《新品发布会》为您带来由杭州恒通医药有限公司供应的法罗培南钠胶囊。
企业简介杭州恒通医药有限公司成立于2006年,是一家以营销新特药品为主业,涵盖产品研发和进出口业务的医药企业。
公司主要经营批发各类化学药制剂、生化药品、中成药以及国外进口药品的申报和代理。
公司的产品线包括抗生素、心脑血管、血液系统、消化系统、抗肿瘤、神经系统药和营养液等多个种类。
杭州恒通严格按照GSP要求,以国内先进水平为目标,建立了完善、规范的质量保证体系。
公司获得韩国大元制药株式会社授权,在中国进口并总经销其生产的注射用盐酸头孢替安(规格:0.5g,1.0g,商品名:海替舒)。
这是国内首家原瓶进口的头孢替安,深受各地医院和广大患者欢迎。
适应症由葡萄球菌、链球菌、肺炎球菌、肠球菌、卡他莫拉克氏菌、大肠杆菌、柠檬酸杆菌、克雷白氏杆菌、肠杆菌、奇异变形杆菌、流感嗜血杆菌、消化链球菌、痤疮丙酸杆菌、拟杆菌等中敏感菌所致的下列感染性疾病:1、泌尿系统感染:肾盂肾炎、膀胱炎、前列腺炎、睾丸炎;2、呼吸系统感染:咽喉炎、扁桃体炎、急慢性支气管炎、肺炎、肺脓肿(肺脓疡病);3、子宫附件炎、子宫内感染、前庭大腺炎;4、浅表性皮肤感染症、深层皮肤感染症,痤疮(伴有化脓性炎症);5、淋巴管炎、淋巴结炎、乳腺炎、肛周脓肿、外伤、烫伤和手术创伤等继发性感染;药理作用法罗培南钠是一种新的碳青霉烯类药物,属非典型β-内酰胺类抗生素,通过其共价键与参与细胞壁合成的青霉素结合蛋白(PBP)结合而抑制细菌细胞壁的合成,使细菌胞壁缺损,菌体膨胀裂解,从而达到抗菌作用。
除此之外,对细菌的致死效应还应包括触发细菌的自溶酶活性,缺乏自溶酶的突变株则表现出耐药性。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
法罗培南钠胶囊项目概况1、药品名称通用名:法罗培南钠胶囊化学名:(+)-(5R,6S)-6-[(1R)-1-羟基乙基]-7-氧代-3-[(2R)-四氢-2-呋喃基]-4-硫杂-1-氮杂双环[3.2.0]庚-2-烯-2-羧酸钠盐·水合物英文化学名: Sodium (+)-(5R,6S)-6-[(1R)-1-hydroxyethyl]-7-oxo-3-[(2R)-tetrahydro-2-furanyl]-4-thia-1-azabicyclo[3.2.0]hept-2-ene-2-carboxylate· hydrate 英文名:Faropenem Sodium Capsule汉语拼音名:Faluopeinan Na JiaonangCAS登录号:122547-49-3代号:ALP-201;SUN-5555;SY-5555;WY-49605商品名:待定化学结构式:分子式:C12H14NNaO5S· H2O分子量:352.342 命名依据与所属类别2.1命名依据根据“新药命名制定原则”,制剂的命名为原料药通用名加剂型,本品的原料药命名为“法罗培南钠”,故将其胶囊剂命名为法罗培南钠胶囊。
2.2 注册分类法罗培南钠由化学合成方法制得,为日本Suntory公司开发的抗菌药物,1997年在日本上市,已被《日本抗生物质医药品基准》(XIV版)收载,但尚未在我国国内上市销售,根据《药品注册管理办法》(暂行)的规定,本品属于化学药品注册分类第3(1)项。
立题目的与依据一、选题的目的与依据1928年,亚历山大·弗莱明发现了青霉素。
1938年,英国牛津大学病理学家弗洛里和德国生物化学家钱恩从期刊资料中找到了有关青霉素的文献。
1939年他们得到了英国和美国的有关组织和基金会的支持。
经过一年多的努力,弗洛里和钱恩终于提纯了青霉素的结晶。
1940年,青霉素时入临床试验阶段,经过对五位受试者的临床观察证明青霉素具的较好的效果。
1943年青霉素药物完成了商业化生产并且正式进入临床治疗。
此后青霉素以及许多半合成的青霉素不断应用于临床,二十世纪七十年代发现了头孢菌素,此后又不断发现了许多半合成的头孢菌素并在临床上广泛应用,这些抗生素在临床上的广泛应用挽救了无数人的生命,然而寻求广谱、高效、低毒的新型抗生素一直是人类追求的目标。
1975年哈佛大学著名化学家Woodward根据青霉素与头孢菌素融合,向青霉素骨架中引入双键,以增大β—内酰胺环的反应性,从而提高抗菌活性的设想,设计了青霉烯。
初期的化合物,如6-苯氧乙酰氨基青霉烯酸等因反应性高,极不稳定,与预期相反,未显示出良好的生物活性。
1976年发现链霉菌产生的1位硫变为碳的碳青霉烯类抗生素硫霉素,继而开发出抗菌作用优异的亚胺培南,其6位均为反式羟乙基。
借鉴碳青霉烯类抗生素的构效关系,用此基团取代原来的6-酰氨基,既保持青霉烯β—内酰胺环的反应性,有改善了其稳定性,从而确立了青霉烯类抗生素的基础。
经过长时间的研究,于1997年开始由第一个青霉烯法罗培南投放市场。
法罗培南为新型广谱抗菌药物,即可口服有可肌注。
对除绿脓杆菌外的需氧G+菌、G-菌均显示出广谱抗菌活性,尤其对金葡菌、耐青霉素的肺炎球菌、粪链球菌等G-菌与脆弱拟杆菌等厌氧菌的抗菌作用明显优于头孢替安(Cefotiam,CTM)、头孢特仑(cefteram,CFTM)、头孢克肟(Cefixime,CFIX)与头孢克洛(Cefaclor,CCL)等现有的头孢菌素。
对葡萄球菌属、链球菌属、流感杆菌、淋球菌等G+菌、G-菌的抗菌活性等同或优于CFTM、CFIX、CCL及阿莫西林(Amoxicillin,AMPC)等。
本品对β—内酰胺酶稳定,可不被其失活,耐药菌株少,对头孢菌素耐药的弗氏枸橼酸杆菌、阴沟肠杆菌等亦有良好作用。
本品对金葡球菌的青霉素结合蛋白(PBP-1,2,3)、大肠杆菌PBP-2显示出强亲和力,表明本品抗菌作用强。
法罗培南空腹单次口服150,300及600mg后的Cmax分别为2.36,6.24和7.37μg·mL-1,AUC为3.95,11.72和15.59μg·h·mL-1,t1/2约1h,12h尿中排泄5%,在粪便中未检出。
用法罗培南治疗各科感染1506例,有效率为80.3%,出现不良反应的占5.9%。
采用双盲法比较治疗复杂性尿路感染,法罗培南(900mg/d,分3次给药)的临床有效率和细菌清除率与头孢替安酯(600mg/d,分3次给药)相同,不良反应发生率为2.6%,头孢替安酯则为5.7%。
法罗培南对脱氢肽水解酶-I(DHP-I)稳定,给药时无需与脱氢肽水解酶-I抑制剂合用。
目前,我国在青霉烯的研究开发还刚刚起步,与国外相比还有较大的差距,法罗培南钠(Faropenem Farron)是由日本Suntory公司生物医学研究所合成,并与山之内制药公司共同开发的新口服青霉烯类抗生素,已被《日本抗生物质医药品基准(十四版)》(JPⅩⅣ)收载。
经过检索发现本品没有在我国申请专利保护,也没有行政保护,因此开发本品不但可以把国外的优秀药品引入我国,满足国内的临床需求,产生良好的经济效益和社会效益。
同时通过研制开发本产品,可以逐步积累开发本类新药的经验,为以后进行化学结构修饰和改造,从而为形成自己的创新产品打下基础。
二、国内外研究和生产使用情况法罗培南钠(Faropenem Farron)是由日本Suntory公司生物医学研究所合成,并与山之内制药公司共同开发的新口服青霉烯类抗生素,已被《日本抗生物质医药品基准(十四版)》(JPⅩⅣ)收载。
在美国许可证已转让给Wyeth-Ayerst公司。
本品于1990年10月在日本组织了研究会,开始基础临床研究,经历了Ⅰ、Ⅱ、Ⅲ期临床研究,于1997年首次在日本上市,用于感染性疾病的治疗。
目前本品国内尚无进口,亦无国内厂家、科研单位开发及生产本品的报道,但在国内的一些期刊上,有关于本品合成工艺研究的报道以及介绍本品的一些综述性文章。
三、国内外有关该品的专利及行政保护情况法罗培南钠为日本Suntory(三得利)公司开发的抗菌药物,1997年在日本上市。
经过检索中国专利库、世界专利库、美国专利库、欧洲专利库、日本专利库等专利数据库,检索的结果是:法罗培南钠化合物1985年由日本三得利公司在国外申请专利,美国专利号为:US4997829,该产品和西司他丁的复方制剂申请有外国专利,美国专利号为:US5354748,该产品的一种酯衍生物在国外申请有专利,美国专利号为:US5830889,以上专利没有在中国申请专利,法罗培南钠的一种局部用药制剂和法罗培南钠与二胺乙酸盐组成的口服制剂在中国申请了专利,中国专利号为:CN99800139,CN00802237。
该产品没有在中国申请行政保护。
因此开发法罗培南钠及其制剂只要不使用上述中国专利保护的制剂技术,将不存在构成专利侵权问题。
国内外相关的临床研究资料综述法罗培南钠(SY5555)为日本Suntory公司生物医学研究所合成,并与山之内制药公司共同开发的新的口服碳青霉烯类抗生素,属非典型 -内酰胺类药物。
本品对需氧及厌氧革兰氏阳性菌、阴性菌均显示出广谱抗菌作用,尤其对葡萄球菌、粪肠球菌等需氧革兰氏阳性菌及拟杆菌等厌氧菌的抗菌作用优于现有口服头孢菌素,对革兰氏阴性菌活性与口服头孢菌素相似,本品对各种 -内酰胺酶稳定,耐药菌株少,在临床上可用于敏感菌引起的各种感染。
各种临床前研究显示,本品安全性高,与碳青酶烯类相比,肾毒性及中枢神经毒性低。
第I期临床试验确认了本品的耐受性,对体内药代动力学及抗菌作用的综合分析认为本品具有临床价值。
本品在临床上用于敏感菌引起的各种感染。
一、药理作用法罗培南钠是一种新的碳青霉烯类药物,属非典型 -内酰胺类抗生素,通过其共价键与参与细胞壁合成的青霉素结合蛋白(PBP)结合而抑制细菌细胞壁的合成,使细菌胞壁缺损,菌体膨胀裂解,从而达到抗菌作用。
除此之外,对细菌的致死效应还应包括触发细菌的自溶酶活性,缺乏自溶酶的突变株则表现出耐药性。
人和哺乳动物无细胞壁,不受β-内酰胺类药物的影响,因而本类药具有对细菌的选择性杀菌作用,对宿主毒性小。
二、体外抗菌作用1.抑菌作用中盐哲士等报道SY5555对链球菌和肠球菌有较强的抗菌活性,对链球菌属的MIC90低于0.05 g/mL,对多种肠杆菌科的细菌的MIC90低于6.25 g/mL。
但对费氏柠檬菌和粘质沙雷氏菌的MIC90分别为25和100 g/mL。
以氨比西林、哌拉西林、头孢唑林、头孢美唑、头孢噻肟和头孢哌酮为对照药,SY5555对流感嗜血杆菌的抗菌活性在所有试验药中最强,对厌氧菌(包括脆弱拟杆菌、梭杆菌属、消化链球菌属和艰难梭菌)有较强的抗菌活性。
那须孝昭等报道,SY5555对需氧菌(除了铜绿假单胞菌之外)和厌氧菌有广谱抗菌作用,特别是对革兰氏阳性菌(包括粪肠球菌)和厌氧菌,SY5555的抗菌活性强于头孢泊肟、头孢替胺及头孢克罗(CCL)。
2.杀菌作用中盐哲士等报道,用肺炎链球菌、粪肠球菌、金黄色葡萄球菌(MSSA)、大肠埃希氏菌、肺炎克雷伯氏杆菌和流感嗜血杆菌各2株来检测SY5555的最小杀菌浓度(MBC)和最小抑菌浓度(MIC),并比较这两种浓度。
MBC都在与之相应MIC的4倍以内,显示SY5555有很强的杀菌作用。
那须孝昭等报道,SY5555的MBC(≤0.025 25 g/ml),在19株被验菌中有15株与其MIC相当,另外4株的MBC是MIC的2倍。
因此,本药1倍或2倍的MIC浓度对被验菌就有杀菌作用。
而头孢类药对多种细菌的MBC是MIC的2倍以上。
此外,试验表明法罗培南的耐药获得速度缓慢。
三、药代动力学日本42所医疗单位以法罗培南钠的药代动力学进行了研究,结果汇总如下:法罗培南钠单次口服150、300及600mg后的血峰浓度Cmax分别为2.36、6.24及7.37 g/ml,AUC 分别为3.95、11.72、15.59 g•h/ml,血药浓度与剂量相关。
血中T1/2在各种剂量下均约1h。
因受肾脱氢肽酶-I(DHP-I)分解,本品尿排泄率低,12h内尿排泄率为5%。
与空腹时给药相比,饭后口服血药浓度达峰时间(Tmax)延长,Cmax、AUC值降低,但幅度不大,T1/2及尿排泄率无差异,可以认为,饮食没有影响。
与丙磺舒联用时Tmax、T1/2延长,AUC也增大,表明本品排泄机制系经肾小管分泌。
对本品300mg与头孢替安酯(CTM-HE)200mg饭后给药的药代动力学进行的比较显示,Cmax、AUC本品稍高,Tmax、T1/2大致相同,尿排泄率以CTM-HE高。
